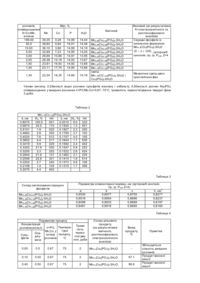
Середні фосфати мангану-кобальту тригідрати та спосіб їх одержання
Номер патенту: 70214
Опубліковано: 15.09.2004
Автори: Антрапцева Надія Михайлівна, Щегров Леонід Миколайович
Формула / Реферат
1. Середні фосфати мангану-кобальту тригідрати із загальною формулою ![]() , де
, де ![]() , як каталізатори селективного окислення вуглеводнів.
, як каталізатори селективного окислення вуглеводнів.
2. Спосіб одержання середніх фосфатів мангану-кобальту тригідратів із загальною формулою ![]() , де
, де ![]() , який полягає в тому, що у реакційну посудину, термостатовану при 30-90°С, паралельно при неперервному перемішуванні подають суміш 0,1-0,4 моль/л водних розчинів сульфатів (хлоридів, нітратів) мангану і кобальту, що беруть у співвідношенні мангану і кобальту (атомному)
, який полягає в тому, що у реакційну посудину, термостатовану при 30-90°С, паралельно при неперервному перемішуванні подають суміш 0,1-0,4 моль/л водних розчинів сульфатів (хлоридів, нітратів) мангану і кобальту, що беруть у співвідношенні мангану і кобальту (атомному) ![]() , і 0,3-0,6 моль/л водний розчин середнього фосфату натрію (калію) у співвідношенні
, і 0,3-0,6 моль/л водний розчин середнього фосфату натрію (калію) у співвідношенні ![]() , суспензію термостатують протягом 1-3 діб, осад, що утворюється, відокремлюють, промивають водою (Т:Р = 1:5), висушують при 50°С до постійної маси.
, суспензію термостатують протягом 1-3 діб, осад, що утворюється, відокремлюють, промивають водою (Т:Р = 1:5), висушують при 50°С до постійної маси.
Текст
Винахід відноситься до синтезу нових хімічних сполук, а саме, середніх фосфатів мангану-кобальту тригідратів , із загальною формулою Мn3- xСох(РO4)2×3Н2 O, де (0 < x £ 1 25 ) , що можуть бути використані як каталізатори селективного окислення вуглеводнів, та способу їх одержання. В літературі з числа фосфатів, що містять у кристалічній решітки ті ж самі атоми - манган і кобальт, і які можна розглядати як аналоги середніх фосфатів, що заявляються, відомі подвійні дигідрофосфати марганцю-кобальту складу Мn1- xСох(Н 2РO4)×2Н2O (0 < x < 1,0 ) [Авт. свид. СССР №1648898, С01В25/45, опубл. 15.05.91. Бюл. №18]. Вони за хімічною природою являють собою безперервний твердий розчин заміщення, що кристалізується в моноклінній сингонії (просторова група Р 21/n, Z=2). Основу кристалічної решітки Мn1-xСох(Н 2РO4)×2Н2O складають октаедри Мn-O6 і Со-О6, до координаційного оточення яких входять дві молекули кристалізаційної води та чотири фосфа тних тетраедри. Координаційний багатогранник формується з двох зв'язків типу М-O(ОН2) і чотирьох зв`язків типу М-О(O2РО2Н2). , Подвійні дигідрофосфати Мn1- xСох(H2РO 4)2×2Н2 O (0 < x < 1 0 ) одержують взаємодією за кімнатної температури механічної суміші гідроксокарбонатів марганцю та кобальту з концентрованою фосфорною кислотою, яку беруть у кількості 200% від стехіометрії. Використовують їх у тваринництві як мінеральну кормову добавку [Авт. свид. СССР №1648898, С01В25/45, опубл. 15.05.91. Бюл. №18]. Проте вперше синтезовані середні фосфати мангану-кобальту тригідрати із загальною формулою Мn3, Сoх(РO4) 2×3Н2O, де 0 < x £ 1 25 , відрізняються від відомих подвійних дигідрофосфатів Мn1-xСо х(H2РO 4)2×2Н2O x (0 < x < 1 0 ) такими важливими показниками, як кристалічна структура, ступінь протонізації, хімічна природа та , , хімічний склад. Мn3- xСoх(РO4) 2×3Н2O, де 0 < x £ 1 25 , кристалізуються в орторомбічній сингонії (просторова група Pcnb, Z=4) і утворюють обмежений твердий розчин заміщення на відміну від Мn1-xСо х(H2РO 4)2×2Н2O, що мають , широкі області гомогенності. Мn3-xСoх(РO4) 2×3Н2O, де 0 < x £ 1 25 - це середні (тризаміщені) солі фосфорної кислоти на відміну від дигідрофосфатів Мn1- xСох(H2РO4)2×2Н2 O, які є однозаміщеними солями. Відмінність у хімічному складі витікає з емпіричних формул цих фосфатів. Це обумовлює значні відмінності в їх фізико-хімічних і експлуатаційних властивостя х, зокрема, у каталітичних. Найбільш близьким до твердого розчину середніх фосфатів мангану-кобальту тригідратів із загальною , формулою Мn3-xСo х(РO 4)2×3Н2O, де 0 < x £ 1 25 , за технічною суттю і досягаємому результату є подвійні гідрофосфати марганцю-кобальту тригідрати складу Мn1-xСo хHРO4×3Н2O (0 < x £ 0,2 ) (прототип) [Патент Російської Федерації №2056350, С01В25/45, опубл. 20.03.96. Бюл.№8]. Мn1- xСoхНРO 4×3Н2O (0 < x £ 0,2 ) за хімічною природою є сполуками перемінного складу, які утворюють обмежений твердий розчин заміщення. Кристалізуються Мn1-xСохНРO4×3Н2 О в орторомбічній сингонії (просторова група Рbса, число формульних одиниць Z=8). Основу кристалічної решітки складають октаедри двох видів Мn-О 6 і Со-О6. Вони знаходяться в одній кристалографічній позиції, утворюючи єдину кристалічну структур у сполуки. Координаційне оточення октаедрів складають три фосфатни х те траедри та три молекули кристалізаційної води. Мn1- xСохНРO 4×3Н2О (0 < x £ 0,2 ) мають такий вміст інгредієнтів (у перерахунку на оксиди), мас. %: МnО - 27,6633,83; СоО - 6,82-0,77; Р2O5 - 34,45-34,60; Н2O - решта до 100%. Одержують Мn1-xСохНРO 4×3Н2О (0 < x £ 0,2 ) спільним осадженням іонів Мn2+ і Со2+ гідрофосфат-іоном НРO42- з розбавлених фосфорнокислих розчинів, що одержують взаємодією механічної суміші свіжеосаджених гідроксокарбонатів марганцю і кобальту, взятих у певному співвідношенні, з фосфорною кислотою (40-80%-ний водний розчин) за фіксованих значень концентрації водневих іонів (рН2,6-2,8). Значення рН реакційного середовища контролюють за допомогою рН-метра і підтримують постійним, регулюючи подачу Н 3РO4 (блок автоматичного титрування БАТ-15) і суміші гідроксокарбонатів. Осад, що утворюється, відокремлюють від маточного розчину, промивають водою, висушують до постійної маси. Використовують Мn1- xСохНРO 4×3Н2О (0 < x £ 0,2 ) як основу люмінесцентних матеріалів з регульованою інтенсивністю випромінювання в короткохвильовій області спектру, термочутливі фарби, емалі, хімічні реактиви, вихідні речовини для одержання дифосфатів [Патент Російської Федерації №2056350, С01В25/45, опубл. 20.03.96. Бюл. №8]. Використання їх як каталізаторів невідоме. Винаходом ставиться завдання створення ряду нових хімічних сполук - середніх фосфатів мангану-кобальту , тригідратів із загальною формулою Мn3- xСoх(РO 4)2×3Н2O 0 < x £ 1 25 , що можуть бути використані як каталізатори селективного окислення вуглеводнів, та розробці способу їх одержання. Поставлене винаходом завдання досягається спільним осадженням катіонів Мn2+ і Co2+ з суміші водних розчинів солей (сульфатів, нітратів, хлоридів), взятих у певному співвідношенні, розчином середнього фосфату натрію (або калію) за співвідношення Р/SМn,Со=0,5-0,7. Для одержання середніх фосфа тів мангану-кобальту тригідратів із загальною формулою Мn3-xСoх(РO4) 2×3Н2O (0 < x £ 1 25) у реакційну посудину, термостатовану за 30-90°С (переважно 75°С), паралельно при неперервному , перемішуванні подають суміш 0,1-0,4моль/л (переважно 0,25моль/л) водних розчинів сульфатів (хлоридів або нітратів) мангану і кобальту, що беруть у співвідношенні мангану до кобальту (атомне) К=Мn/Со=199,0-1,40, і 0,30,6моль/л (переважно 0,5моль/л) водний розчин осаджувача - середнього фосфату натрію (калію), які беруть у співвідношенні n=Р/SМn,Со=0,5-0,7 (переважно 0,67). Суспензію термостатують протягом 1-3 діб, осад, що утворюється, відфільтровують, промивають водою (Т:Р=1:5), висушують при 50°С до постійної маси. Вказаний спосіб дозволяє одержати середні фосфати мангану-кобальту тригідрати із загальною формулою , Мn3- xСoх(РO 4)2×3Н2 O. Визначені за результатами хімічного аналізу значення х змінюються у межах (0 < x £ 1 25) . , Вміст інгредієнтів у Мn 3-xСo х(РO4) 2×3Н2O (0 < x £ 1 25 ) такий, мас. %: манган 23,35-39,35; кобальт 17,63-0,28; фосфор 14,90-14,99; вода 13,66-14,44. Вихід готового продукту складає 94-98%. В табл.1 наведено характеристики синтезованих середніх фосфатів мангану-кобальту тригідратів із загальною формулою Мn3-xСo х(РO 4)2×3Н2O і залежність його складу від умов одержання (співвідношення К=Мn/Со в суміші вихідних розчинів). За даними табл.1, вмістом мангану і кобальту в складі Мn3- xСoх(РO 4)2×3Н2O можна керувати, змінюючи для цього під час синтезу склад суміші вихідних розчинів. , Факт утворення нової хімічної сполуки - середніх фосфатів складу Мn3- xСoх(РO4) 2×3Н2O (0 < x £ 1 25 ) підтверджений результатами фізико-хімічних досліджень і, зокрема, даними хімічного, рентгенофазового та ІЧ спектроскопічного аналізів (табл.1-3). В табл.2 наведено рентгенометричні характеристики одного з синтезованих середніх фосфа тів Mn1,75Co1,25(PO4)2×3H2 O, що містить максимально можливу кількість кобальту -17,63% (ДРОН - 3М, з'єднаний з обчислювальним комплексом на базі ЕОМ типу IBM PC/AT, Co Ka, Fe-фільтр, вн утрішній стандарт NaCl). В табл.3 представлено результати прецизійних рентгенографічних досліджень фосфатів складу Мn3(0 < x £ 1 25 ) із різним вмістом мангану і кобальту, на основі яких були визначені параметри , xСo х(РO4) 2×3Н 2O елементарних комірок (а, в, с) у кристалічних решітках синтезованих фосфатів. Встановлено, що вони змінюються лінійно залежно від вмісту в фосфата х мангану і кобальту. Це знаходиться в повній відповідності до закону Вегарда і є найбільш вагомим доказом індивідуальності та хімічної природи синтезованих нових середніх фосфа тів мангану, кобальту тригідратів із загальною формулою Мn3- xСoх(РO 4)2×3Н2O (0 < x £ 1 25 ) . Одержані дані (табл.1-3) дозволяють зробити висновок, що синтезовані сполуки є індивідуальними, тобто містять манган, кобальт, фосфор в одній кристалічній гратці і не містять сторонніх домішок. , Межі зміни значень х, що встановлені для Мn3-xСoх(РO 4)2×3Н2O - 0 < x £ 1 25 , розкривають його хімічну природу як твердого розчину заміщення з обмеженою областю гомогенності. Насиченим членом цього ряду сполук є фосфа т складу Mn1,75Co1,25(PO 4)2×3H2O. Середніх фосфатів мангану-кобальту тригідратів, значення х в яких перевищує 1,25, не утворюється. В умовах, коли співвідношення К=Мn/Со у складі вихідних розчинів менш ніж 1,40, утворюється механічна суміш дво х кристалічних фаз (табл.1). , Середні фосфати мангану-кобальту тригідрати із загальною формулою Мn3-xСoх(РO4) 2×3Н2O (0 < x £ 1 25 ) являють собою полікристали орторомбічної сингонії (просторова група Рсnb, число формульних одиниць Z=4). Катіони Мn2+ і Со2+ ізоморфно входять в октаедри Мn-О6 і Со-О6, координаційне оточення яких складають чотири атоми оксигену фосфатних те траедрів і два атоми оксигену молекул води. Октаедри у кристалічній гратці Мn3xСo х(РO4) 2×3Н 2O займають три кристалографічно нееквівалентні положення. Прояв ізоморфних заміщень мангану на кобальт відбувається в октаедрах двох типів і визначає область існування синтезованих середніх фосфатів Мn30 < x £ 1 25 . , xСo х(РO4) 2×3Н 2O як Встановлені дані однозначно свідчать, що синтезовані середні фосфати тригідрати Мn3-xСo х(РO4) 2×3Н2O, де 0 < x £ 1 25 , і прототип - подвійні гідрофосфати тригідрати – Мn1- xСoхНРO 4×3H2O (0 < x £ 0,2) мають різні , кристалічні структури. Відповідність винахідницькому рівню нових хімічних сполук - середніх фосфатів мангану-кобальту тригідратів із , загальною формулою Мn3-xСo х(РO 4)2×3Н2O, де 0 < x £ 1 25 , обумовлено: , 1. Різницею кристалічних структур середніх фосфатів, що заявляються - Мn3-xСoх(РO4)2×3Н2 O (0 < x £ 1 25 ) (0 < x £ 0,2) просторова група Pcnb, число формульних одиниць Z=4 і прототипу – Мn1-xСo хНРO4×3Н2O просторова група Рbса, число формульних одиниць Z=8). Це обумовлює цілий ряд їх відмінних особливостей, зокрема: • різне взаємне розташування атомів у кристалічній гратці сполук; • різні кристалографічні параметри і об'єм елементарних комірок, кути між атомними площинами; • відмінні типи, міцність і кількість хімічних зв'язків, що реалізуються в кристалічних структурах сполук; • різні хімічні властивості. 2. Різницею в ступені протонізації синтезованих середніх фосфатів (трьохзаміщені солі фосфорної кислоти) і прототипу (двозаміщені солі фосфорної кислоти). 3. Різницею хімічного (кількісного) складу фосфатів, що заявляються, і прототипу. 5. Різницею у фізико-хімічних властивостях, зокрема, у ступені дисперсності, питомої поверхні, концентрації кислотних центрів. 6. Різницею в призначенні. Середні фосфати тригідрати, що заявляються, можна використовувати як каталізатори. Прототип використовують як основу люмінесцентних матеріалів, термочутливі фарби, емалі, хімічні реактиви, вихідні речовини для одержання дифосфатів. Відповідність винахідницькому рівню способа одержання середніх фосфатів мангану-кобальту тригідратів Мn3, Сoх(РO4) 2×3Н2O (0 < x £ 1 25) обумовлено: x 1. Різницею технологічних операцій та обладнання для одержання середніх фосфатів, що заявляються, і прототипу. Процес одержання середніх фосфатів передбачає їх осадження в результаті гомогенної взаємодії двох розчинів, взятих у певному співвідношенні. Одержання прототипу відбувається підчас гетерогенної взаємодії механічної суміші твердих гідроксокарбонатів і розчину фосфорної кислоти. Одержання середніх фосфатів не потребує контролю рН. Синтез прототипу - процес частково автоматизований. Він передбачає контроль рН реакційної маси, що забезпечується за допомогою рН-метра, і підтримку його значення постійним подачею розчину Н 3РО4 за допомогою блоку автоматичного титрування (БАТ15). 2. Різницею вихідних реагентів. Водні розчини сульфатів (нітратів або хлоридів) і осаджувача - середнього , фосфа ту натрію (калію) - вихідні реагенти для одержання середніх фосфатів Мn3- xСoх(РO 4)2×3Н2O, де 0 < x £ 1 25 . Гідроксокарбонати, фосфорна кислота, пероксид водню - для одержання прототипу - подвійних гідрофосфатів марганцю-кобальту. 3. Різницею в режимах процесу, що забезпечують одержання середніх фосфатів Мn3- xСoх(РO4) 2×3Н2O, де 0 < x £ 1 25 . , В табл.4 наведено обґрунтування вибору параметрів способу одержання середніх фосфатів мангану-кобальту , тригідратів із загальною формулою Мn3- xСoх(РO4) 2×3Н2O, де 0 < x £ 1 25 . Із даних табл.1, 4, що характеризують взаємопов'язаний вплив основних параметрів синтезу Мn3, Сoх(РO4) 2×3Н2O, де 0 < x £ 1 25 , випливає, що цільовий продукт найкращої якості з високим виходом одержують за x такими умовами: концентрація розчинів сульфатів (хлоридів, нітратів) – 0,1-0,4моль/л, осаджувача - середнього фосфа ту натрію – 0,3-0,6моль/л, співвідношення мангану до кобальту (атомне) в складі суміші розчинів солей К=М n/Со=199,0-1,40; співвідношення розчинів солей і осаджувача (атомне) - n=P/SMn,Co=0,5-0,7; температура синтезу 30-90°С. Суспензію термостатують при 30-90°С протягом 1-3 діб, відокремлюють, відмивають водою (Т:3=1:5), висушують при 50°С до постійної маси. Невиконання хоча б однієї з вказаних умов не дає можливості одержати кристалічний цільовий продукт у вигляді індивідуальної сполуки. , Нижче наведено конкретні приклади одержання середніх фосфатів Мn3-xСo х(РO 4)2×3Н2O (0 < x £ 1 25) різного хімічного складу. Приклад 1 В термостатований за 75°С реакційний посуд поступово при постійному перемішуванні подають суміш 0,25моль/л водних розчинів сульфатів мангану (200мл) і кобальту (97,62мл) і 0,45моль/л розчин Na3PO4 (205,25мл). Тверду фаз у, яка осаджується, термостатують при 75°С протягом 3 діб, відфільтровують, промивають водою (Т:Р=1:5), сушать при 50°С до постійної маси. Одержують кристалічний продукт складу Мn2,0Со0,75(РO4) 2×3Н2О. Вміст в ньому, мас. %: Мn - 26,38; Со - 14,18; Р - 14,93; Н2O - 13,67. Вихід готового продукту (по фосфор у) - 96,7%. Приклад 2 В термостатований при 50°С реакційний посуд подають, аналогічно прикладу 1, суміш 0,3моль/л водних розчинів сульфатів (200мл мангану, 66,67мл кобальту) і 138,15мл 0,5моль/л розчину Nа3РО4. Тверду фазу термостатують при 50°С протягом 2 діб, відфільтровують, промивають водою (Т:Р=1:5), сушать при 50°С до постійної маси. Одержують кристалічний продукт складу Мn2,25Со0,75(РO 4)2×3Н2О. Вміст в ньому, мас. %: Мn - 29,69; Со - 10,66; Р- 14,91; H 2О - 13,95. Вихід готового продукту (по фосфор у) - 96,4%. Приклад 3 Синтез і термостатування твердої фази проводять при 80°С. В реакційний посуд подають, аналогічно прикладу 1, суміш водних розчинів сульфатів з концентрацією 0,2моль/л (мангану 200мл, кобальту 1,01мл) і 343,80мл 0,4моль/л розчин Na3PO4. Подальші операції виконують аналогічно прикладу 1. Одержують кристалічний продукт складу Мn2,98Со0,02(РO4) 2×3Н2О. Вміст в ньому, мас. %: Мn - 39,35; Со - 0,28; Р - 14,99; Н2O - 14,44. Ви хід готового продукту (по фосфор у) - 97,3%. Приклад 4 Синтез проводять аналогічно прикладу 1, використовуючи в складі суміші водних розчинів 200мл сульфату мангану і 153,98мл сульфату кобальту (К=Мn/Со=1,50). Одержують тверду фазу, яка складається з механічної суміші двох кристалічних фаз. Приклад 5 Те ж саме, що в прикладі 1, але розчину Nа3РO4 подають 422мл (значення n=P/SMn,Co перевищує 0,7). У складі продукту присутня домішкова фаза - подвійна натрієва сіль. Однією з можливих галузей практичного застосування синтезованих середніх фосфа тів Мn3- xСoх(РO 4)2×3Н2O, 0 < x £ 1 25 , є хімічна промисловість, де вони можуть бути використані як каталізатори селективного окислення , де вуглеводнів. Для перевірки працездатності нових середніх фосфатів із загальною формулою Мn3-xСo х(РO4) 2×3Н2O, де 0 < x £ 1 25 , за вказаним призначенням були проведені випробування їх каталітичних властивостей у реакціях , окислення н-бутанолу та окислювального приєднання метану до толуолу. Випробування проводили у кварцевому реакторі на установці з протокою газової суміші та хроматографічним аналізом продуктів за стандартними методиками. Схема дослідів передбачала одержання показників, що характеризують каталітичну активність середніх фосфа тів із різним вмістом мангану і кобальту, і порівняння їх з аналогічними характеристиками відомих каталізаторів, що використовуються для цієї мети. В табл.5 наведено результати випробувань, що свідчать про перспективність використання Мn30 < x £ 1 25 як каталізаторів у реакціях окислення н-бутанолу та окислювального приєднання , xСo х(РO4) 2×3Н 2O, де метану до толуолу. Таблиця 1 Склад вихідних Склад твердої фази розчинів, співвідношення К=Со/Мn, атомне 199,00 50,0 10,00 5,00 3,00 2,05 1,50 1,40 Мас. % Мn Со Р Н2О 39,35 38,82 36,10 32,89 26,69 26,38 23,91 23,11 0,28 0,84 3,86 7,23 10,66 14,18 16,93 17,70 14,99 15,01 14,95 14,95 14,91 14,93 14,92 14,90 14,44 14,36 14,19 14,05 13,95 13,67 13,68 13,66 1,30 22,34 18,35 14,80 14,16 Фазовий (за результатами ІЧ спектроскопічного та рентгенофазового аналізів) Середні фосфати із загальною формулою Мn3- xСО х(РO 4)2.3Н2O (0 < x £ 1 25) , орторомб , сингонія, пр. гр. Рcnb , Z=4 Хімічний Мn2,98Сo0,02(РО4)2×3Н2 О Мn2,94Сo0,06(РО4)2×3Н2 О Мn2,73Сo0,27(РО4)2×3Н2 О Мn2,49Сo0,51(РО4)2×3Н2 О Мn2,25Сo0,75(РО4)2×3Н2 О Мn2,00Сo1,00(РО4)2×3Н2 О Мn1,81Сo1,19(РО4)2×3Н2 О Мn1,75Со1,25(РО4)2×3Н2 О суміш Мn1,75СО 1,25(РО 4)2×3Н2О і Со3(РО4)2×8Н2О Ме ханічна суміш дво х кристалічних фаз Умови синтезу: 0.25моль/л водні розчини сульфатів мангану і кобальту; 0,50моль/л розчин Nа3РO4; співвідношення у вихідних розчинах n=Р/SМn,Со=0,67; 75°С; тривалість термостатування твердої фази 3 доби. Таблиця 2 d, нм 0.8070 0.6874 0.5101 0.4662 0.4024 0.3852 0.3419 0.3302 0.3200 0.2944 0.2548 0.2202 0.2106 0.2075 Мn1,75Сo1,25(РO4)2×3Н2 O І/Іo , % hkl d, нм 100.0 001 0.2010 34.5 110 0.1930 1.9 020 0.1827 2.8 200 0.1769 7.6 012 0.1707 4.4 211 0.1644 0.9 220 0.1592 21.9 030 0.1547 3.3 202 0.1522 21.9 131 0.1462 22.8 321 0.1414 2.7 240 0.1373 1.4 104 0.1315 4.4 402 І/Іo , % 6.0 1.3 2.3 2.7 4.0 1.1 2.4 0.8 2.6 3.1 1.9 0.6 1.1 hkl 332 051 250 152 105 530 442 253 424 235 514 126 306 Таблиця 3 Склад синтезованих середніх фосфа тів Мn2,49Сo0,51(РO4)2×3Н2 O Мn2,25Сo0,75(РO4)2×3Н2 O Мn2,00Сo1,00(РO4)2×3Н2 O Мn1,75Сo1,25(РO4)2×3Н2 O Параметри елементарної комірки, нм (орторомб сингонія, пр. гр. Рcnb Z=4) а b с V, нм 3 0,9530 0,9977 0,8705 0,8277 0,9516 0,9954 0,8696 0,8237 0,9498 0,9933 0,8688 0,8197 0,9481 0,9916 0,8680 0,8160 Таблиця 4 Параметри процесу Концентрація Трива розчинів,моль/л n=P/S Темпералість тура Mn,Co у термоОсаскладі процесу, Сульджустатувафатів розчинів °С ння, доби вача Склад цільового продукту (за результатами хімічного, рентгенофазового, спектроскопічного аналізів) Вихід продукту, % 0,05 0.5 0.67 75 2 Мn3- xСох(РO 4)2×3Н2 O 0,10 0.50 0.67 75 2 Мn3- xСох(РO 4)2×3Н2 O 97,1 0,40 0.50 0.67 75 2 Мn3- xСох(РO 4)2×3Н2 O 96,6 Примітка Збільшується кількість вихідних розчинів. Продукт високої якості Продукт високої якості 0,45 0.50 0.67 75 2 Мn3- xСох(РO 4)2×3Н2 O 0.25 0.60 0.45 75 2 Мn3- xСох(РO 4)2×8Н2 O 0,25 0.45 0.75 75 2 0,25 0.50 0.70 25 2 Мn3- xСох(РO 4)2×3Н2 O 0,25 0.50 0.50 95 2 Мn3- xСох(РO 4)2×3Н2 O 0,25 0.45 0.67 90 2 Мn3- xСох(РO 4)2×3Н2 O 97.0 0,25 0.45 0.67 30 2 Мn3- xСох(РO 4)2×3Н2 O 95.4 0,25 0.45 0.67 75 0,5 0,25 0.45 0.67 75 4 Мn3- xСох(РO 4)2×3Н2 O 0,3 0.30 0.50 75 3 Мn3- xСох(РO 4)2×3Н2 O 96.7 Збільшується тривалість кристалізації. Зменшується вихід продукту Утворюється домішка натрієвої солі. Збільшується тривалість процесу. Ускладнюється здійснення процесу. Продукт високої якості Продукт високої якості Погіршується якісний-склад продукту Збільшуються витрати на синтез Продукт високої якості. , * За способом прототипом середні фосфати тригідрати складу Мn3-xСо х(РO 4)2×3Н2O, де (0 < x £ 1 25) , не можуть бути одержані. Таблиця 5 Окислення н-бутанолу Приєднання метану до толуолу Селективність, Температура, Конверсія Селективність, % Температура, Конверсія, Каталізатор % °С % °С толуолу,% С4Н8 С4Н6 С6Н6 C8H10 350 41 11 8 700 67 12 14 Мn2,25Сo0,75(PO4)2×3Н2 O 350 34 14 16 700 64 10 15 Мn1,75Сo1,25(PO4)2×3Н2 O КНОБ-12/6 350 42 10 12 La-V-P-О 700 42 5 12
ДивитисяДодаткова інформація
Назва патенту англійськоюMedium phosphates of mangane-cobalt trihydrates and a method for obtaining the same
Автори англійськоюAntraptseva Nadiia Mykhailivna, Schehrov Leonid Mykolaiovych
Назва патенту російськоюСредние фосфаты мангана-кобальта тригидраты и способ их получения
Автори російськоюАнтрапцева Надежда Михайловна, Щегров Леонид Николаевич
МПК / Мітки
МПК: C01B 25/37, C01B 25/26, C01G 51/00, C01G 45/00, C01B 25/34
Мітки: мангану-кобальту, тригідрати, одержання, середні, спосіб, фосфати
Код посилання
<a href="https://ua.patents.su/5-70214-seredni-fosfati-manganu-kobaltu-trigidrati-ta-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Середні фосфати мангану-кобальту тригідрати та спосіб їх одержання</a>
Попередній патент: Твердий розчин циклотетрафосфатів магнію-цинку та спосіб його одержання
Наступний патент: Автоматичний насос-дозатор
Випадковий патент: Спосіб і пристрій для призначення користувачам використовувати arq-чергування в системі безпровідного стільникового зв'язку