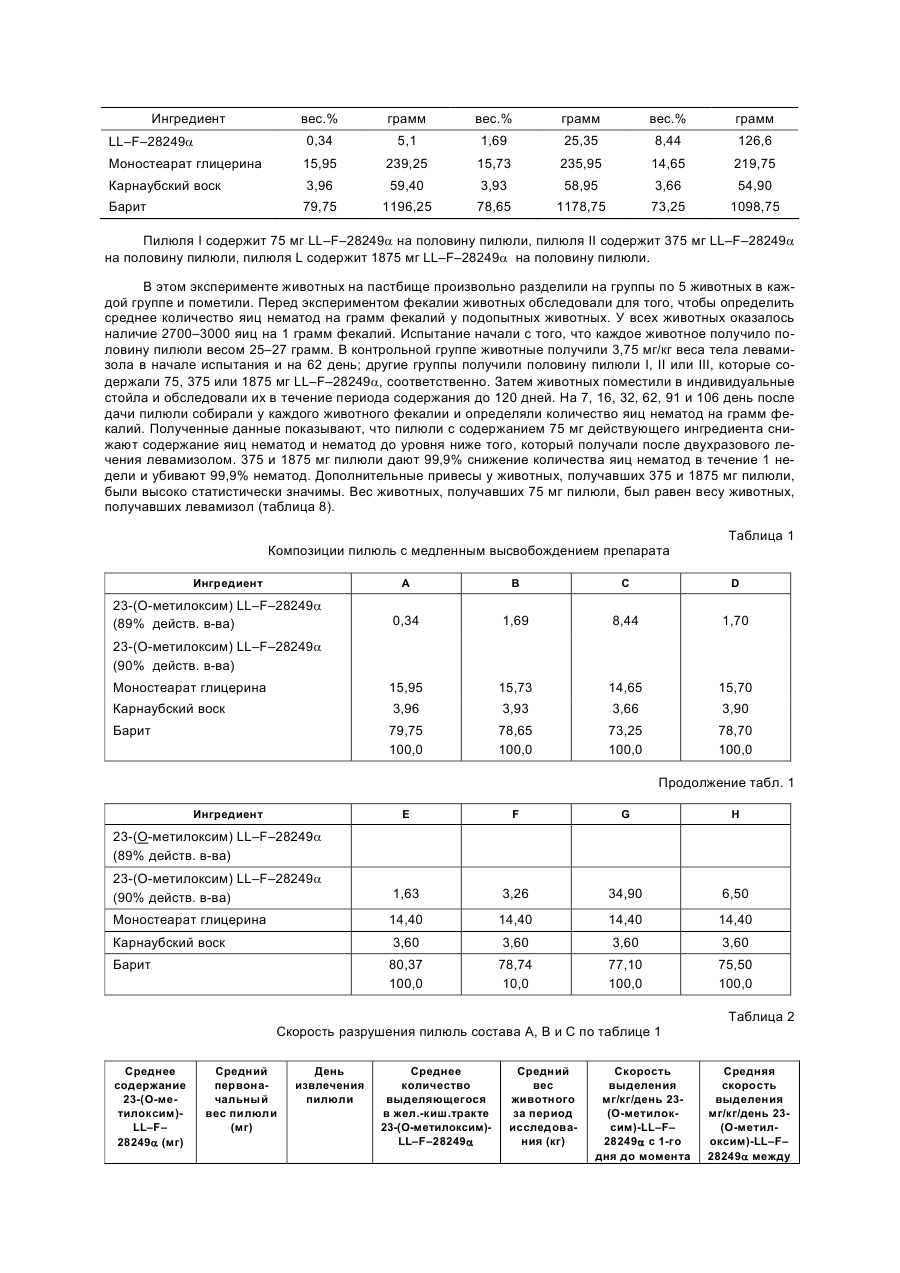
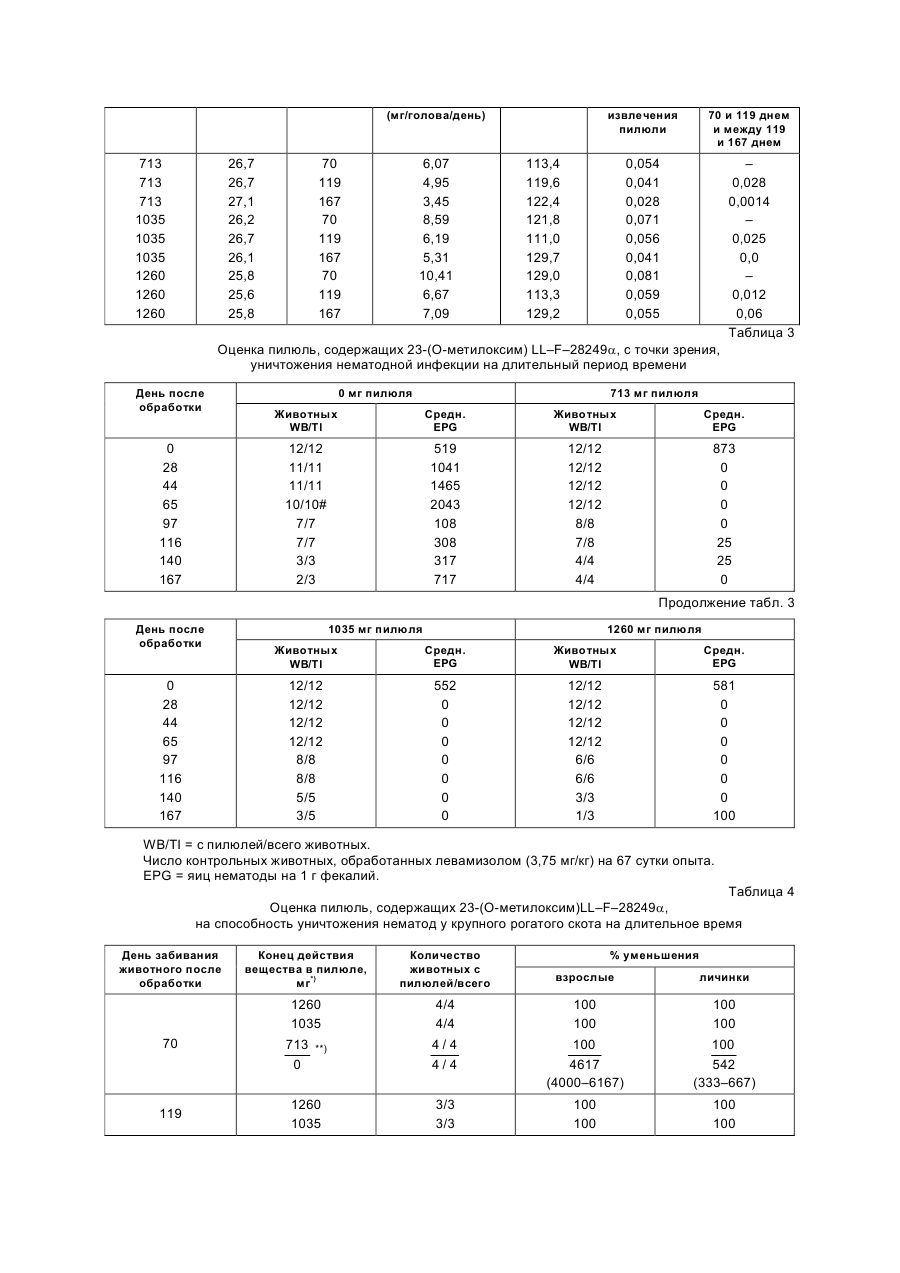
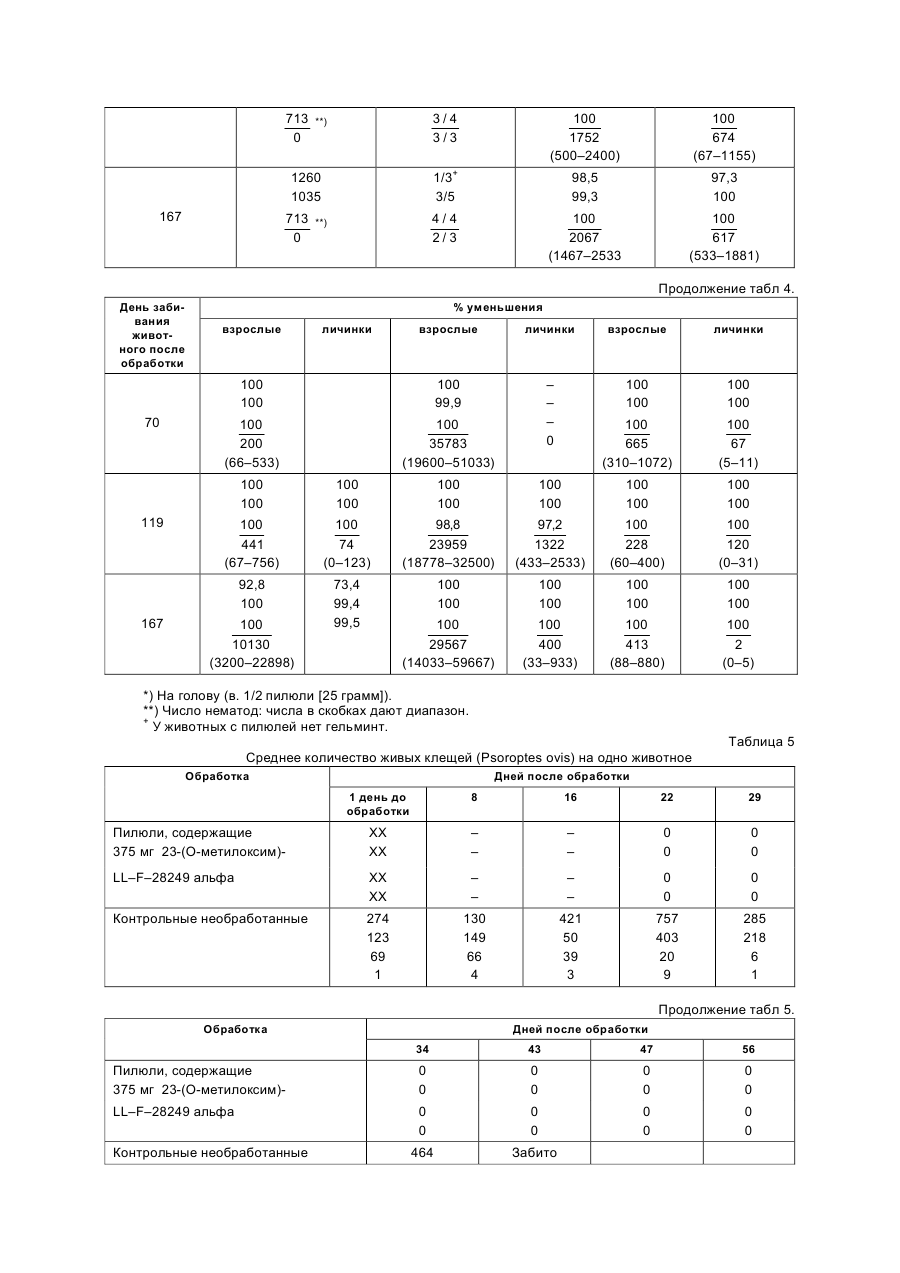
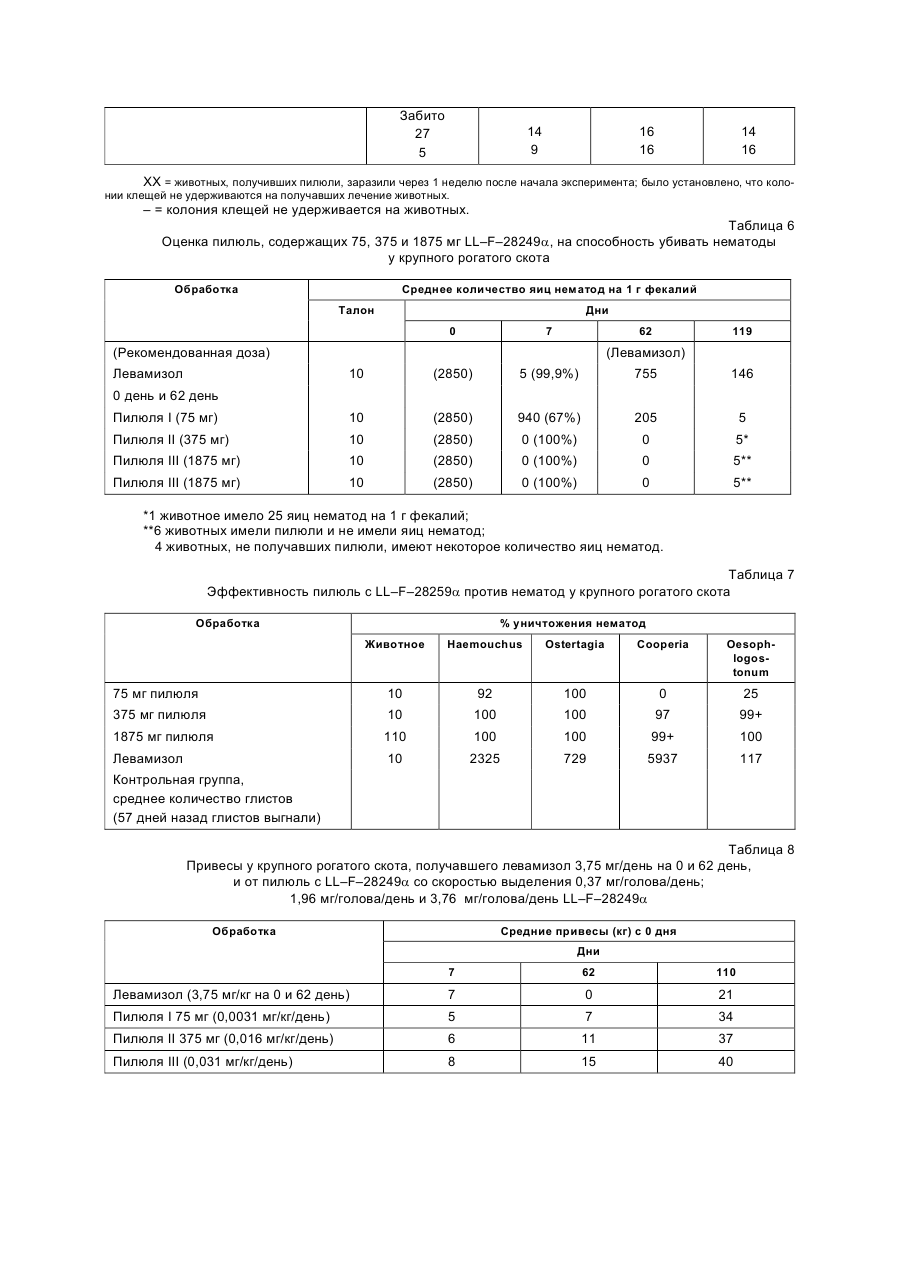
Болюс з пролонованим виділенням активного інгредієнта, спосіб захисту жуйних тварин від зараження гельмінтами, спосіб профілактики аб0 пригнічення, системного контролю зниження або запобігання зараженнь у жуй
Номер патенту: 37173
Опубліковано: 15.05.2001
Автори: Вуд Ірвін Бойден, Тутхілл Річард Бодман, Діц Джозеф Чарлз
Формула / Реферат
1. Болюс с пролонгированным выделением активного ингредиента для орального введения жвачным животным эффективный для защиты указанных жвачных животных на длительный период времени против заражения взрослыми особями и личинками гельминтов, эндопаразитов, эктопаразитов и акарид, отличающийся тем, что содержит 0,3-10 вес.% LL-F28249α, 23-(0-метилоксим) LL-F28249 α или их производное, 10-20 вес.% моностеарата глицерина, 3,0-10,0 вес,% карнаубского воска и 70,0-85 вес.% сульфата бария или измельченного барита.
2. Болюс по п.1, отличающийся тем, что он включает 1,0-8,5 вес.% указанных 23-(0-метилоксим) LL-F28249α или LL-F28249 α , 14-16 вес.% моностеарата глицерина, 3,0-5,0 вес.% карнаубского воска и 70-80 вес.% барита.
3. Болюс по п.1, отличающийся тем, что содержит 0,3-1,0 вес.% LL-F-28249 α или 23-(0-метилоксим) LL-F-28249 α , 14-16 вес.% моностеарата глицерина, 3,0-5,0 вес.% карнаубского воска и 78,01-82,7 вес.% сульфата бария или измельченного барита.
4. Способ защиты жвачных животных от заражения гельминтами, эндопаразитами, эктопаразитами и акаридами, отличающийся тем, что орально вводят указанным животным, подлежащим защите, в течение 120-180 дней болюс, непрерывно выделяющий в желудочно-кишечный тракт указанного жвачного животного 0,04 мг/голова/день-15,63 мг/голова/день LL-F-28249 α или 23-(0-метилоксим) LL-F-28249 α .
5. Способ по п.4, отличающийся тем, что указанный болюс выделяет в пищеварительный тракт указанных жвачных животных 0,2-10,4 мг/голова/день LL-F-28249 α или 23-(0-метилоксим) LL-F-28249 α .
6. Способ профилактики или подавления заражения нематодами и клещами } крупного рогатого скота, отличающийся тем, что орально вводят животным, подлежащим
защите на срок до 167 дней, болюс с долговременным выделением активного ингредиента, содержащий 75-1875 мг LL-F-28249 α или 23-(0-метилоксим) LL-F-28249 α , диспергированных в смеси, содержащей 14-16 вес.% моностеарата глицерина, 3-5 вес.% карнаубского воска и 70-80,5 вес.% сульфата бария или мелкого барита.
7. Способ по п.6, отличающийся тем, что указанный болюс выделяет в пищеварительный тракт указанных жвачных животных 0,001-0,075 мг/кг веса животного LL-F-28249 α или 23-(0-метилоксим) LL-F-28249 α .
8. Способ системного контроля эктопаразитных заражений жвачных животных, отличающийся тем, что орально вводят указанным животным болюс с долговременным выделением активного ингредиента, содержащий инсектицидно эффективное количество LL-F-28249 α, 23-(0-метилоксим) LL-F-28249 α или их производных, который непрерывно выделяет в рубец обрабатываемого животного системно-эффективное количество LL-F-28249, 23-(0-метилоксим) LL-F-28249 α или их производное.
9. Способ по п.8, отличающийся тем, что указанный болюс содержит 375-1875 мг LL-F-28249 α, или 23-(0-метилоксим) LL-F-28249 α, 14-16 вес.% моностеарата глицерина, 3-5 вес.% карнаубского воска и 70-80 вес.% барита.
10. Способ снижения или предотвращения заражения пастбищ для жвачных животных инфицирующими нематодами, эндопаразитами, эктопаразитами и акаридами, которые заражают указанных животных, отличающийся тем, что орально вводят указанным жвачным животным болюс с медленным выделением активного ингредиента, эффективный для защиты указанных жвачных животных на длительный период времени от заражения гельминтами, эндопаразитами, эктопаразитами и акаридами и содержащий 0,3-10 вес.% LL-F-28249 α, или 23-(0-метилоксим) LL-F-28249 α, 10-20 вес.% моностеарата глицерина, 3-10 вес.% карнаубского воска и 70-85 вес.% сульфата бария или мелкого барита, таким образом указанное лечение убивает эндо- и эктопаразитов и/или подавляет их репродуктивный цикл, таким образом, удаляя яйца указанных паразитов из фекалий жвачных животных.
11. Способ получения болюсов с пролонгированном высвобождением для орального употребления жвачными животными и обеспечивающий по своему действию защиту указанных жвачных животных в течение продолжительного времени от инфицирования взрослыми или личинковыми особями гельминтов, эндопаразитических насекомых, эктопаразитических насекомых и акарид, отличающийся тем, что смешивают
0,3-10% по массе LL-F-28249 α, 23-(0-метилоксим) LL-F-28249 α, или его производного; 10-20% по массе глицерин-моностеарата; 3,0-10,0% по массе карнаубского воска и 70-85% по массе сульфата бария или баритной мелочи с последующим литьевым формованием смеси, используя трехстадийный температурный профиль, включающий фазу подачи, выдерживаемую при температуре, которая ниже температуры размягчения смеси, переходную фазу при нагреве выше температуры размягчения и фазы литьевого формования, на которой смесь впрыскивают в форму при температуре ниже температуры размягчения и охлаждают форму для затвердевания болюсов.
12. Способ по п. 11, отличающийся тем, что смесь гранулируют перед литьевым формованием.
13. Способ по п.11, отличающийся тем, что смесь содержит 1,0-8,5% по массе LL-F-28249 α, или 23-( 0-метилоксим) LL-F-28249 α, 14-16% по массе глицерин-моностеарата; 3,0-5,0% по массе карнаубского воска и 70-80% по массе баритной мелочи.
14. Способ по п. 11, отличающийся тем, что смешивают 0,3-1,0% по массе LL-F-28249 α, или 23-(0-метилоксим) LL-F-28249 α, 14-16% по массе глицерин-моностеарата; 3,0-5,0% по массе карнаубского воска и 78,01 %-82,7% по массе сульфата бария или баритной мелочи с последующим литьевым формованием смеси с использованием трехстадийного температурного профиля, включающего фазу подачи, выдерживаемой при температуре ниже температуры размягчения смеси, фазу перехода при повышенной температуре выше температуры размягчения и фазы литьевого формования, на которой смесь впрыскивают в форму при температуре ниже температуры размягчения; и охлаждают форму для затвердевания болюсов.
Текст
Болюс с пролонгированным выделением активного ингредиента, способ профилактики, лечения или уничтожения немотад, акарид, эндо- и эктопаразитных заражений у жвачных животных. Способ получения болюсов. Настоящее изобретение относится к композициям пилюль, содержащим профилактически эффективное количество соединения LL–F–28249a, 23-(О-метилоксим)LL–F–28249a или их производных, к введению их жвачным животным для профилактики или уничтожения нематод, эндопаразитов, эктопаразитов или акарицидного заражения у указанных животных в течение длительного периода времени. Более точно, настоящее изобретение относится к новым пилюлям с долговременным выделением препарата, включающим 0,3–10,0 вес.% LL–F–28249a, 23-(О-метилоксим)LL–F–28249a или их производные, 10,0–20,0 вес.% глицерина моностеарата, 3,0–10,0 вес.% карнаубского воска и 70,0–85,0 вес.% сульфата бария. Оно также относится к способу защиты жвачных животных в течение длительного периода времени от заражения нематодами эндо- и эктопаразитами и акаридами и обеззараживания пастбищ для исключения заражения указанными паразитами, который заключается в оральном введении указанным жвачным животным пилюли, как описано выше, которая непрерывно выделяет в рубец животного в течение длительного периода времени терапевтически или профилактически эффективное количество LL–F– 28249a, 23-(О-метоксим)LL–F–28249a или их производного. К удивлению, было также обнаружено, что уничтожение или предупреждение нематодного заражения у жвачных животных можно достичь при чрезвычайно низких уровнях содержания LL–F–28249a или 23(О-метоксим) LL–F–28249a в пилюлях по настоящему изобретению, содержащих от 0,3 до менее 1,0 вес.% LL–F–28249a, 23-(О-метилоксим)LL–F–28249a или их производного; 14–16 вес.% моностеарата глицерина, 3–5 вес.% карнаубского воска и 78,01–82,7 вес.% барита. Кроме того, мы обнаружили, что пилюли по настоящему изобретению эффективны для профилактической борьбы с паразитами, поражающими поголовье, и что это профилактическое действие оказывается благодаря постоянному присутствию чрезвычайно малых количеств LL–F–28249a или 23-(О-метилоксим)LL–F–28249a. Мы также наблюдали, что такое профилактическое воздействие на жвачных животных не только защищает их от заражения нематодами, эндопаразитами, эктопаразитами и акаридами, но также способствует получению больших привесов по сравнению с животными, не получившими препарат, или с животными, которых обрабатывали другими антигельминтными, антибактерицидными или акарицидными средствами. Предпочтительные композиции для пилюль, эффективных для борьбы и/или профилактики инcектицидного, нематодного и акарицидного заражения жвачных животных, таких как крупный рогатый скот, овцы, козы, буйволы, бизоны, олени и т.п., включают 1,0–8,5 вес.% LL–F–28249a, 23-(О-метилоксим)LL–F– 28249a, 14,0–16,0 вес.% моностеарата глицерина, 3,0–5,0 вес.% карнаубского воска и 70,0–80,5% барита. Одним из предпочтительных вариантов осуществления настоящего изобретения является пилюля с долговременным выделением препарата для орального введения жвачным животным, которая является эффективной для защиты указанных животных в течение длительного периода времени (до 6 месяцев) против заражения взрослыми особями и личинками гельминтов, эндопаразитов, эктопаразитов и акарид, которая содержит 0,3–10 вес.% LL–F–28249a, 23-(О-метилоксим)LL–F–28249a или их производных, 10–20 вес.% моностеарата глицерина, 3,0–10 вес.% карнаубского воска и 70,0–85 вес.% сульфата бария или мелкого барита. Один особенно предпочтительный вид пилюль с долговременным выделением препарата содержит от 0,3 до менее 1,0 вес.% LL–F–28249a, 23-(О-метилоксим)LL–F–28249a, 14–16 вес.% моностеарата глицерина, 3,0–5,0 вес.% карнаубского воска и 78,01–82,7 вес.% сульфата бария или мелкого барита. Удивительно, но профилактическое введение пилюль по настоящему изобретению жвачным животным (чрезвычайно низкие дозы в день в некоторых случаях) не только способствует предотвращению и/или уничтожению нематод, эндо-, эктопаразитов и акарид, но также способствует значительному увеличению привесов по сравнению с необработанными животными или с теми животными, которых лечили другими антигельминтными, антибактериальными или акарицидными веществами. Получение композиций для пилюль с долговременным высвобождением препарата по настоящему изобретению осуществляют путем смешения в определенном весовом соотношении при температуре ниже температуры плавления воска или смеси 0,3–10% активного ингредиента, 3–10% карнаубского воска, 10– 20% моностеарата глицерина и 70–85% фармацевтически и фармакологически приемлемого носителя с высокой плотностью, выбранного из группы, включающей сульфат бария и барита. Эту смесь можно использовать непосредственно на стадии инжекционного формования, или смесь предварительно превращают в таблетки или хлопья с помощью экструдера или шуппен-аппарата и затем полученные таблетки или хлопья используют для инжекционного формования. После смешения смесь выгружают и либо подают в экструдер, либо непосредственно загружают в инжекционный формователь. Если для улучшения однородности желательно таблетирование, то смесь гранулируют, используя трехступенчатый температурный профиль, включающий зону загрузки, поддерживаемую при температуре ниже температуры плавления воска, горячую переходную зону, в которой поддерживают температуру выше температуры плавления воска и стеарата, и зону дозирования, температура в которой поддерживается ниже температуры плавления воска и стеарата, причем используют прямоточную матрицу, оборудованную прерывателем, причем узел, включающий матрицу, оборудованную прерывателем, поддерживают при той же температуре, что и зону дозирования. Полученный экструдированный материал охлаждают на воздухе и нарезают на таблетки требуемого размера. Улучшенной однородности можно также достичь путем превращения в хлопья смеси активного ингредиента, воска и сульфата бария или бариевого наполнителя, после чего осуществляют гранулирование на имеющемся в продаже оборудовании. Полученные таблетки и/или сухую смесь материалов направляют в систему инжекционного формования, которая имеет трехстадийный температурный профиль, аналогичный использовавшемуся при получении таблеток, а именно, зона питания с температурой ниже температуры размягчения смеси, переходная зона с температурой выше температуры размягчения и зона инжектирования, где смесь инжектируют в формы при температуре ниже температуры размягчения смеси. Форму охлаждают для того, чтобы пилюли затвердели. Полученные пилюли затем извлекают из форм и упаковывают. Хотя вышеописанный процесс можно осуществить, используя сульфат бария или другие наполнители и утяжелители, мелкий барит является предпочтительным. Использование мелкого барита в процессе имеет ряд преимуществ по сравнению с использованием сульфата бария со степенью очистки, соответствующей американскому стандарту, например, использование барита повышает твердость пилюли и снижает скорость разрушения пилюли. Таким образом, эта пилюля обеспечивает более контролируемую скорость разрушения и более долговременное высвобождение LL–F–28249a, 23-(О-метилоксим) LL–F– 28249a. Также в процессе изготовления смесей, содержащих воск, моностеарат глицерина и активный ингредиент, было обнаружено, что использование мелкого барита вместо сульфата бария по американскому стандарту, позволяет получить менее липкие и более легкие в обращении твердые смеси. Получение пилюль по настоящему изобретению путем инжекционного формования не требует низкотемпературного помола твердой смеси или использования дополнительных смазок, которые часто требуются в других способах, таких как прессование таблеток. Еще одно преимущество состоит в том, что не нужным становится рециркулирование частиц, оставшихся на 100 меш ситах. Прессование таблеток требует использования материала размером 100 меш для прессования, т.к. использование материала с размером частиц меньше 100 меш приводит к более быстрому высвобождению активных ингредиентов из пилюль . В предпочтительном способе получения пилюль с LL–F–28249a и 23-(О-метилоксим) LL–F–28249a по настоящему изобретению путь инжекционного формования время цикла сокращено до 40–50 секунд. Полная активность может ожидаться, если рабочие условия поддерживаются ниже 140оС. Крайне необходимым рабочие условия включают: а) увеличивающийся температурный профиль, т.е. полая часть при температуре окружающей среды и температура сопла 90оС; б) время впрыскивания 20 с; в) давление выпрыскивания 0,5 т на дюйм и г) время охлаждения 20 с. Эти условия приводят к температуре плавления 89– 90оС, что значительно ниже критической температуры для разложения. Временно (температурные исследования показывают, что благодаря этой превосходной стабильности возможен непрерывный рецикл вертикальных летников и летниковых каналов. Полученные литьем под давлением пилюли имеют более высокую плотность, являются более твердыми и, по-видимому, разрушаются с меньшей скоростью (определяемой по распаду метанола) чем залитые пилюли. Также реологические данные показывают,что лучшая "смачиваемость" барита может защитить активный ингредиент от термального разложения. Хотя литье под давлением является предпочтительным способом приготовления пилюль по настоящему изобретению, следует понимать, что указанные пилюли можно получить методами ручного литья. Следует также понимать, что размер пилюль можно менять значительно для обеспечения размеров пилюль, пригодных для всех видов и размеров жвачных животных. Используя метод ручного литья, моностеарат и карнаубский воск смешиваются, расплавляются и нагреваются до 105+5оС. В этот расплав добавляют активный ингредиент и перемешивают до однородной суспензии. При непрерывном перемешивании в эту суспензию вводят барит. Смешивание продолжается до получения однородной кремообразной смеси. Полученное в результате вещество вливают в форму, охлаждают до комнатной температуры и вынимают из формы. В этом случае, безусловно, размер и масса полученных пилюль определяется размерами используемых форм. Настоящее изобретение ниже иллюстрируется неограничивающими примерами. Пример 1. Приготовление инокулята. Типичную среду, используемую для выращивания различных стадий инокулята, получают по следующей формуле. Декстроза 1,0% Декстрин 2,0% Дрожжевой экстракт 0,5% NZ амин 0,5% Карбонат кальция 0,1% Вода до (г) 100% Эту среду стерилизуют 100 мл часть этой стерильной среды в колбе засевают соскобами мицелия препарата на агаре Streptomyces cyaneogrisens noncyanogenus NRRL 15773. Затем эту среду усиленно перемешивают во вращающемся вибраторе в течение 48–72 часов при 28оС, обеспечивая первичный инокулянт. Этот первичный инокулянт затем используют для инокуляции 1 л вышеуказанной стерильной среды, которая затем выращивается аэробно при 28оС в течение 48оС, обеспечивая вторичный инокулянт. Пример 2. Ферментация. Ферментационную среду следующей формулы получают из такого состава. Декстрин 1,0% Соевый пептон 1,0% Мелясса 2,0% Карбонат кальция 0,1% Вода (г) до 100% Эту среду стерилизуют и затем 30 л часть инокулируют 1 л вторичного инокулянта, полученного в примере 1. Ферментацию проводят при 30оС при расходе стерильного воздуха. 30 л/мин., обратном давлении 8 фунтов на кв.дюйм и перемешивании мешалкой при 500 оборотах в минуту в течение 91 часов, убирая в это время мешанку. Пример 3. Выделение LL–F–28249a. 26 л всей убранной мешанки, полученной в примере 2, смешивают с 1500 г диатомовой земли и фильтруют. Мицелиевый слой промывают 5 л воды и фильтрат и промыв удаляют. Полученную мицелиевую лепешку смешивают с 10 л метанола в течение 1 часа, затем фильтруют и промывают 5 л метанола. Экстракт и промывку метанола объединяют и выпаривают до водного остатка 1–2 л. Этот водный остаток смешивают с двойным объемом хлористого метилена и перемешивают 30 минут. Фазу хлористого метилена выделяют и затем концентрируют до сиропа, получая 27 г сырого вещества. Эти 27 г сырого вещества растворяют в смеси хлористого метилена и метанола, фильтруют через вату и безводный сульфат натрия и затем выпаривают, получая 7 г масла. 170 г часть силикагеля суспендируют в 12,5% этилацетата в хлористом метилене и вливают для образования колонки 2,5 х 58 см. Это масло растворяют в 12,5% этилацетата в хлористом метилене и вносят в колонку. Эту колонку элюируют этой же смесью растворителей. Вначале подвижную фазу перегоняют при 1,3 мл/мин. и собирают 15-минутные фракции. Через 10 фракций расход снижают до 0,5 мл/мин, так что фракции I–10 имеют 20 мл, равномерно уменьшаясь до 10 мл и фракции II–98 содержали около 7 мл. При фракции 99 расход увеличили для получения 25 мл фракций через 10 минут. Эти фракции проверили тонкослойной хроматографией (ТСХ) в смеси этилацетат: хлористый метилен (1:1). Фракции 55–62 объединили и выпарили, получив 150 мг твердого вещества, содержащего LL–F– 28249a и b. 150 мг этого твердого вещества, содержащего LL–F–28249a и b хроматографировали препаративной ЖХВД, используя колонку обратной фазы Whatman С 8,2 x 50 cм), элюированную 80% метанола в воде. Расход 10 мл/мин и собираются 2-минутные фракции. Фракции 58–69 объединяются, метанол испаряется, добавляют трет-бутанол и смесь лиофилизируют, получая 60 мг чистого LL–F–28249a. Это соединение может быть представлено следующей формулой: OH CH3 O CH3 O CH3 H3C O O CH3 CH3 OH O CH3 OH Пример 4. 5-0-трет-бутилдиметилсилил-LL–F–28249a. В 500 мл СН2Сl2 70 г LL–F–28249a перемешивают с 82,04 г имидазола при 20оС под азотом. Затем в течение 5 минут добавляют 43 г трет-бутилдиметилсилилхлорида в 400 мл СН2Cl2. Через час реакцию проверяют на завершение при помощи ЖХВД, используя 50% CH3CN/50% H2O в режиме искривленного градиента в течение 10 минут на колонке быстрого анализа Whatman partisil CCS/C8 при расходе 1 мл/мин. Добавляли еще 3 г трет-бутилдиметилсилихлорида и через 3 часа состав представляет 92,3% продукт, 0,3% LL–F– 28249a и 1,16% дисилилированного вещества. Смесь разбавили СH2Cl2 и влили в 2 л H2O. Слой CH2Cl2 выделили. Водную часть экстрагировали 2 л СH2Сl2 и объединенные органические слои обезводили (Na2SO4). CH2Cl2 выпарили в вакууме и получили 166 г целевого соединения, которое идентифицировали масс-спектрометрией и спектрометрией ЯМР. Пример 5. 5-0-трет-бутилдиметилсилил-23-оксо-LL–F–28249a. В 5 л сухого CH2Cl2 под азотом перемешивали 116 г 5-0-трет-бутилдиметилсилил-LL–F–28249a и при 22оС добавили 540 г NaOAc, а затем добавили 172,5 г пиридинхлорхромата (ПХХ). Через 1 час добави ли еще 15 г ПХХ, поскольку реакция по анализу ЖХВД не завершена. Через 2 часа добавили еще 10 г и реакционную смесь перемешивали всего 5 часов. Эту смесь вылили в 6 л смеси ледяной воды и выделили CH2Cl2. Водный слой экстрагировали CH2Cl2 и объединенные слои CH2Cl2 промывали водой и обезводили (Na2SO4). CH2Cl2 выпарили в вакууме и получили 197,8 г сырого продукта, который растворили в 2 л Et2O и отфильтровали. Раствор Et2O промыли водой (2 х х 10000 мл), обезводили (Na2SO4), испарили до сухости и получили 60 г целевого соединения, которое идентифицировано масс-спектрометрией и ЯМР-спектрометрией. Пиридинхлорхромат, замещенный пиридиндихроматом в вышеуказанной процедуре также позволяет получить целевое соединение. Пример 6. 23-оксо-LL–F–28249a. В 1,5 л MeOH нагревом растворили 60 г 5-0-трет-бутилдиметилсилил-23-оксо-LL–F–28249a и при 0оС добавили 30 г п-толуолсульфокислоты в 300 мл MeOH. Эту смесь перемешивали 3 часа и вылили в 6 л насыщенного раствора NaHCO3 в 6 л H2O. После перемешивания смесь экстрагировали 4 л EtOAc и слои выделили. Водный слой насытили NaCl и экстрагировали 2 х 6 л EtOAc. Первый слой EtOAc промыли насыщенным раствором NaCl, объединили с другими экстрактами EtOAc и обезводили (Na2SO4). EtOAc выпарили в вакууме и получили 148,1 г темного остатка. Это сырое вещество после этого хроматографировали ЖХВД на 1200 г SiO2, используя для элюирования 1% изопропанол в СН2Сl2 и контролировали УФдетектором/254 нм фильтром. Фракции 39–42 объединили и выпарили до сухости и получили 12,65 г целевого соединения, которое анализируется следующими данными: Вычислено: для С36Н50О8 С 70,79; Н 8,25 Найдено: С 60,33; Н 8,31 Это целевое соединение дополнительно определяется при помощи масс-спектрометрии и ЯМРспектрометрии. Пример 7. 23-О-метилоксим-LL–F–28249a. В 930 мл сухого диоксана при комнатной температуре добавили 70 г 23-оксо-LL–F–28249a, 11,8 г NaOAC, 11,8 г CH3ONH2 · HCl и 2 мл HOAc. Смесь перемешивали под азотом 3 суток и после отсутствия исходного вещества, по данным ЖХВД, 650 мл диоксана выпарили в вакууме. Остаток влили в 5 л H2O, и продукт экстрагировали CH2Cl2 (4х2 л). Объединенные экстракты промыли H2O, остаток растворили в 1500 мл Et2O раствор промыли водой, обезводили (N2SO4) и выпарили до сухости. Получили 11,84 г целевого соединения, которое идентифицировали масс-спектрометрией и ЯМР-спектрометрией. Оно также анализируется следующим образом: Вычислено для C37H53O8N·1,5 H2O: C 66,64; Н 8,46; N 2,10 Найдено С 66,82; Н 8,13; N 2,32. Это соединение может быть представлено следующей формулой. H3C O N CH3 CH3 O CH3 CH3 H3C O O CH3 OH O H OH CH3 Получение пилюль длительного действия. Пилюли получают в соответствии со следующей формулой. Ингредиент % 23-(О-метилоксим)LL–F–28249a (89% реального вещества) 0,34 Глицеролмоностеарат 15,95 Карнаубский воск 3,96 Барит 79,75 Моностеарат и карнаубский воск смешивают, расплавляют и нагревают до 105 + 5оС. В этот расплав добавляют активный ингредиент и смешивают для однородной суспензии. При непрерывном перемешивании в эту суспензию добавляют барит. Смешивание продолжается, пока не получают однородную сметанообразную массу. Результирующий состав выливают в форму, охлаждают до комнатной температуры и вынимают из формы. Масса полученных пилюль 51–53 г. Пилюля закруглена с обоих концов и имеет размеры: толщина – 3/4 дюйма, ширина – 7/8 дюйма, длина – 3,0 дюйма. Технические данные на глицерoлмоностеарат показывают, что это вещество должно быть белым порошком или шариками, свободными от примесей. Размер частиц не должен превышать 5% на стандартном сите № 20 США и частицы характеризуются кислотным числом 2–3 и влагосодержанием не более 1,5%. Общее содержание моноглицеридов должно превышать 40%, но свободная кислота не должна превышать 1,5%. Карнаубский воск должен быть желтым порошком без примесей. 100% воска должно проходить через стандартное сито № 80 США. Кислотное число воска должно быть 2–6 и растворимое в ацетоне смолистое вещество при 15оС не должно превышать 5,0%. Барит должен быть серым порошком без примесей с объемной плотностью 150 фунтов на куб.фут. Размер частиц должен быть таким, чтобы на стандартном сите № 200 США оставалось не более 4% и не менее 80% проходило через стандартное сито № 325 США. Химический анализ для приемлемого продукта представляет BаSO4 90–94%, SiO2 – 7–8% и Fe2O3 0,1–0,2%. Плотность пилюль по настоящему изобретению должна быть между 2,35 и 2,6 + 0,6. Другие пилюльные композиции получают аналогичным образом и они сведены в таблицу 1. Пример 9. Определение скорости разрушения пилюль настоящего изобретения. Скорости освобождения лекарства для пилюль, обозначенных А, В и С в таблице 1, определяется вначале пробой указанных пилюль для соединения 23-(О-метилоксим)-LL–F–28249a, которые должны вводиться телятам, выбранным для этого теста. Эти пробы показывают, что пилюли, которые должны оцениваться, содержат 0,713, 1035 или 1260 мг 23-(О-метилоксим)-LL–F–28249a, 50–53 г пилюли ломают пополам, взвешивают и орально вводят по 0,5 пилюли каждому теленку. Обработанные телята затем содержатся в загоне и питаются и поятся в соответствии с обычными или стандартными процедурами выращивания скота. Диетой для всех животных является стандартный рацион для скота. В интервалах через 60, 119 и 167 суток после введения четыре животных из каждой обработанной группы умерщвляют, пилюли извлекают и изучают для определения характера поверхности и затем взвешивают. Затем результаты записывают и оценивают. Процедуру повторяют через 119 суток после лечения для второй группы животных из каждой группы лечения и затем повторяют через 167 суток для третьей группы животных из каждой группы лечения. Для удобства результаты, полученные из каждой лечебной группы, четыре теленка в группе, усреднены и представлены в таблице 2. Пример 10. Приготовление препарата пилюли длительного освобождения и его оценка для борьбы с желудочнокишечными глистами и клещами Boophilus microplus у скота. Препараты для пилюль длительного освобождения, содержащие в основном 23-(О-метилоксим)LL–F– 28249a, глицеролмоностеарат карнаубский воск и барит, получают смешиванием соответствующих количеств каждого вещества в смесителе при температуре 80оС в течение 10 минут. После смешивания смесь выгружают и направляют в гранулятор-экструдер и/или непосредственно выгружают в инжекционный пресс. Если проводится гранулирование, то эту смесь затем гранулируют, используя колокольный температурный профиль, который имеет часть охлажденной подачи (50–60оС), часть высокотемпературного перехода (100–110оС) и часть охлажденной дозировки (50–60оС) с прямоточной матрицей 1/8 дюйма, снабженной прерывательной пластиной 20 меш. Температуру матрицы поддерживают 55–60оС. Полученный в результате вытянутый жгут охлаждают воздухом (воздушный поток направлен в отверстие матрицы) и отрезают, используя горячую лобовую фрезу, на гранулы длиной 1/4 дюйма. В случае непосредственной подачи сухой смеси можно использовать систему подачи, такую как Vibra-Screen для подачи вещества в систему литься под давлением, используя систему обогреваемого летника и закрывающегося сопла. Рабочие условия для литьевого формования должны включать температурный профиль колокольной формы, описанный выше для гранулирования, например время заполнения (10– 20с), время литья (10–20с), давление литья 0,5 тонны на кв.дюйм и время выдержки (5–10с), что создает пилюли массой 51 г каждая, плотностью 2,5 г/мсм3 и твердостью по Деламару 77–80 кг. Пилюли, полученные по такому способу, показаны ниже. Составы пилюль, полученные литьем под давлением, вес.% Ингредиент Пилюля I J K L 0,0 3,24 4,84 6,46 23-(О-метилоксим)LL–F–28249a Стеарат глицерина 14,40 14,40 14,40 14,40 Карнаубский воск 3,60 3,60 3,60 3,60 Барит 82,00 78,76 77,16 75,54 (вес в граммах) 0 28,49 42,15 26,49 23-(О-метилоксим)LL–F–28249a Стеарат глицерина 125,28 125,28 125,28 59,04 Карнаубский воск 31,32 31,32 31,32 14,76 Барит 713,60 685,21 671,29 309,71 Для оценки вышеопределенных композиций для борьбы с желудочно-кишечными глистами и клещевыми инвазиями скота провели следующие испытания. 52 теленка абердин-ангусской породы (моложе 1 года) на пастбище выбраны для оценки описанных выше пилюль и обозначенных I, J, K и L. Пилюли содержат 0,713, 1035 или 1260 мг 23-(О-метилоксим)LL–F–28249a, соответственно, на 0,5 пилюли, каждая из которых весит 25 г. В течение недели перед обработкой на телятах провели два раздельных дифференциальных отсчета яиц нематоды и оценили интенсивность клещевых инвазий. Животных заклеймили на ухе, взвесили и отнесли к одной из четырех лечебных групп, 12 телят в каждой группе. Пятую группу из 4 животных также заклеймили на ухе и взвесили. Эту группу используют для изучения осуществимости реинтородукции пилюль, извлеченных после аутопсии другим животным. Дифференциальные отсчеты яиц нематоды проводят через неделю, две недели, 1 месяц и ежемесячно в течение 5 месяцев или до того, как больше нет адекватной борьбы. Полученные данные приведены в таблицах 3 и 4, где можно видеть, что контрольные животные, необработанные в течение первых 67 суток опыта, остаются сильно зараженными в этот период опыта. Затем эти животные обрабатываются левамизолом и нематодные инвазии значительно уменьшаются. Животные, получающие пилюли настоящего изобретения, содержащие 713–1260 мг 23-(О-метилоксим)LL–F–28249a по существу не имеют нематодной инвазии после 28–167 суток обработки. Клещи уничтожаются через одну неделю после обработки пилюлями, содержащими 1035 мг – 1260 мг 23-(О-метилоксим)LL–F–28249a. Животные, принимающие пилюли, содержащие 713 мг активного ингредиента, освобождаются от клещей через две недели. Контрольные животные, должны погружаться в противоклещевой раствор для предотвращения падежа. Обработанные животные освобождаются от клещей на 97 суток или до тех пор, пока не установится холодная погода, при которой исключаются клещевые инвазии на контрольных животных. Пример 11. Оценка пилюль с длительным высвобождением препарата для профилактики псороптоза у крупного рогатого скота. Пилюли, содержащие 375 мг 23-(О-метилоксим)LL–F–28249a на 1/2 пилюли, получили по способу инжекционного формования, описанному в примере 10. Полученные пилюли имели следующий состав вес.% грамм 23-(О-метилоксим)LL–F–28249a Ингредиент 1,53 1,61 Моностеарат глицерина 15,73 16,52 Карнаубский воск 3,93 4,12 Барит 78,81 82,75 100,00 105,00 Подопытному животному давали половину 50-граммовой пилюли, содержащей 750 мг 23-(О-метилоксим)LL–F–28249a. Для опыта отобрали смешанных телок. Животных поместили на сухой площадке и провели с ними все мероприятия по защите от обычных заболеваний. Их бонитировали с помощью серьги и поместили в стойла, чтобы предупредить заражение чесоткой. Затем на каждое животное выпустили живых клещей. Это сделали путем взятия соскоба с сильно зараженного животного и помещения на подопытное животное. Из животных, которых не поместили в коровник, выбрали случайным образом четырех незараженных животных. Затем этим животным давали пилюли по настоящему изобретению и заразили их через неделю. На этих животных заносили клещей (на каждое из них) шесть раз в течение следующих двух недель. Были предприняты меры предосторожности для того, чтобы животные не заразились друг от друга. Соскобы делались через каждую неделю и исследовались в тот же день. Количество клещей подсчитывали с помощью микроскопа, дающего 20–30-кратное увеличение. Пилюли весом 375 мг предотвратили инфицирование псороптозом животных, перенесших шестикратное контрольное заражение. Полученные данные приведены ниже в таблице 5. Пример 12. Оценка пилюль, содержащих 23-(О-метилоксим)LL–F–28249a, для борьбы с вшами и мухой осенней у крупного рогатого скота (таблица 6). Пилюли, испытываемые в этом эксперименте, получены способом инжекционного формования, описанным в примере 10. Полученные пилюли имели следующий состав. I II III Пилюля Ингредиент вес.% грамм вес.% грамм вес.% грамм 23-(О-метилоксим)LL–F–28249a 1,62 6,64 3,24 28,49 4,84 42,15 Моностеарат глицерина 14,40 59,04 14,40 125,28 14,40 125,28 Карнаубский воск 3,60 14,76 3,60 31,32 3,60 31,32 Барит 80,38 329,56 78,76 685,21 77,16 671,29 Для проведения эксперимента пилюли разделили пополам. Пилюля I: содержит 375 мг активного ингредиента на половину пилюли. Пилюля II: содержит 750 мг активного ингредиента на половину пилюли. Пилюля III: содержит 1125 мг активного ингредиента на половину пилюли. Перед началом эксперимента всех животных взвесили, пометили и проверили на наличие вшей. Количество вшей определили визуально по 2–3 проборам в области уха, глаз, морды, пасти, подгрудка, лопатки, линии позвоночника, корня хвоста и бедер. Животных произвольно разделили на группы: 3 подопытных и 1 контрольная по 5 животных в каждой. Группам I, II и III давали пилюли, содержащие экспериментальное соединение, в то время как группа не получала пилюль. Всех животных поместили на площадки в 2 акра и давали им сено древовидной люцерны и минеральные кормовые добавки. Животных обследовали на наличие вшей на 7, 14, 28 день и раз в два месяца в течение испытания. Подсчет количества вшей вели, когда животное фиксировалось за голову и при искусственном освещении. Образцы фекалий отбирались (примерно 10 г) для исследования на наличие нематод на 7, 14, 28 день и через месяц после этого. Эти образцы хранили при температуре -10оС. Все группы, получавшие пилюли (375 мг, 750 мг и 1125 мг), имели малое количество вшей Solinoptes capillatus уже через неделю после обработки. Полное уничтожение вшей Solinoptes capillatus на всех животных, получавших пилюли, было достигнуто в течение 100 дней. Пример 13. Оценка пилюль с длительным выделением препарата для уничтожения Hypoderma spp. у крупного рогатого скота на длительный период времени. Использованные в этом эксперименте пилюли получили путем инжекционного формования, как описано в примере 10. Пилюли имели следующий состав: Ингредиент вес.% грамм 23-(О-метилоксим)1,6 3,2 LL–F–28249a Моностеарат 14,4 28,8 глицерина Карнаубский воск 3,6 7,2 Барит 80,4 160,8 100,0 200,0 В этих экспериментах смешанных породистых животных естественно зараженных Hypoderma spp. первой возрастной стадии случайным образом разделили на группы по 4 животных в каждой. Одну группу оставили в качестве контрольной, а другая группа получала по половине 50–54 г пилюли, содержащей 375 мг 23-(О-метилоксим)LL–F–28249a. По полпилюли давали отелившимся животным с помощью болюсодавателя. После этого эффективность воздействия препарата определяли путем визуального обследования и пальпации боков животного через неделю на предмет выявления присутствия желваков. Лечение препаратом 23-(О-метилоксим)LL–F–28249a в пилюлях было полностью эффективно против Hypoderma spp. На боках животных, получавших пилюли с 375 мг указанного выше препарата в течение 72 дней, не обнаружено личинок; однако у контрольной группы было в среднем 12 (диапазон 4–19) личинок/голова в пиковый момент на 58 день и 8,8 – на 72 день. Пример 14. Оценка пилюль, содержащих 75–1875 мг LL–F–28249a для пролонгированного лечения нематод и клещей у крупного рогатого скота (таблица 7). Пилюли получили следующим образом. Моностеарат и карнаубский воск смешали, расплавили и нагрели до температуры 105 + 5оС. В эту смесь добавили активный ингредиент и перемешали смесь до однородной суспензии. В эту суспензию добавили барит при постоянном перемешивании. Перемешивание продолжали до получения однородной кремообразной смеси. Полученную смесь влили в форму, дали охладиться до комнатной температуры и выгрузили из формы. Полученные пилюли весили 51–53 г. Пилюли с обоих концов имеют куполообразную форму и 3/4 дюйма толщины, 7/8 дюйма ширины и 3,0 дюйма длины. Половину пилюли давали (весом 25,5–27,0 г) животным на пастбище. Эффективность действия препарата наблюдали в течение 120 дней путем определения количества внутренних и внешних паразитов. Ингредиент вес.% грамм вес.% грамм вес.% грамм LL–F–28249a 0,34 5,1 1,69 25,35 8,44 126,6 Моностеарат глицерина 15,95 239,25 15,73 235,95 14,65 219,75 Карнаубский воск 3,96 59,40 3,93 58,95 3,66 54,90 Барит 79,75 1196,25 78,65 1178,75 73,25 1098,75 Пилюля I содержит 75 мг LL–F–28249a на половину пилюли, пилюля II содержит 375 мг LL–F–28249a на половину пилюли, пилюля L содержит 1875 мг LL–F–28249a на половину пилюли. В этом эксперименте животных на пастбище произвольно разделили на группы по 5 животных в каждой группе и пометили. Перед экспериментом фекалии животных обследовали для того, чтобы определить среднее количество яиц нематод на грамм фекалий у подопытных животных. У всех животных оказалось наличие 2700–3000 яиц на 1 грамм фекалий. Испытание начали с того, что каждое животное получило половину пилюли весом 25–27 грамм. В контрольной группе животные получили 3,75 мг/кг веса тела левамизола в начале испытания и на 62 день; другие группы получили половину пилюли I, II или III, которые содержали 75, 375 или 1875 мг LL–F–28249a, соответственно. Затем животных поместили в индивидуальные стойла и обследовали их в течение периода содержания до 120 дней. На 7, 16, 32, 62, 91 и 106 день после дачи пилюли собирали у каждого животного фекалии и определяли количество яиц нематод на грамм фекалий. Полученные данные показывают, что пилюли с содержанием 75 мг действующего ингредиента снижают содержание яиц нематод и нематод до уровня ниже того, который получали после двухразового лечения левамизолом. 375 и 1875 мг пилюли дают 99,9% снижение количества яиц нематод в течение 1 недели и убивают 99,9% нематод. Дополнительные привесы у животных, получавших 375 и 1875 мг пилюли, были высоко статистически значимы. Вес животных, получавших 75 мг пилюли, был равен весу животных, получавших левамизол (таблица 8). Таблица 1 Композиции пилюль с медленным высвобождением препарата Ингредиент A B C D 0,34 1,69 8,44 1,70 15,95 23-(О-метилоксим) LL–F–28249a (89% действ. в-ва) 15,73 14,65 15,70 23-(О-метилоксим) LL–F–28249a (90% действ. в-ва) Моностеарат глицерина Карнаубский воск 3,96 3,93 3,66 3,90 Барит 79,75 100,0 78,65 100,0 73,25 100,0 78,70 100,0 Продолжение табл. 1 Ингредиент E F G H 23-(О-метилоксим) LL–F–28249a (90% действ. в-ва) 1,63 3,26 34,90 6,50 Моностеарат глицерина 14,40 14,40 14,40 14,40 Карнаубский воск 3,60 3,60 3,60 3,60 Барит 80,37 100,0 78,74 10,0 77,10 100,0 75,50 100,0 23-(О-метилоксим) LL–F–28249a (89% действ. в-ва) Таблица 2 Скорость разрушения пилюль состава A, B и С по таблице 1 Среднее содержание 23-(О-метилоксим)LL–F– 28249a (мг) Средний первоначальный вес пилюли (мг) День извлечения пилюли Среднее количество выделяющегося в жел.-киш.тракте 23-(О-метилоксим)LL–F–28249a Средний вес животного за период исследования (кг) Скорость выделения мг/кг/день 23(О-метилоксим)-LL –F– 28249a с 1-го дня до момента Средняя скорость выделения мг/кг/день 23(О-метилоксим)-LL –F– 28249a между (мг/голова/день) 713 713 713 1035 1035 1035 1260 1260 1260 26,7 26,7 27,1 26,2 26,7 26,1 25,8 25,6 25,8 70 119 167 70 119 167 70 119 167 6,07 4,95 3,45 8,59 6,19 5,31 10,41 6,67 7,09 извлечения пилюли 113,4 119,6 122,4 121,8 111,0 129,7 129,0 113,3 129,2 70 и 119 днем и между 119 и 167 днем 0,054 0,041 0,028 0,071 0,056 0,041 0,081 0,059 0,055 – 0,028 0,0014 – 0,025 0,0 – 0,012 0,06 Таблица 3 Оценка пилюль, содержащих 23-(О-метилоксим) LL–F–28249a, с точки зрения, уничтожения нематодной инфекции на длительный период времени День после обработки 0 мг пилюля 713 мг пилюля Средн. Животных WB/Tl Средн. EPG 12/12 11/11 11/11 10/10# 7/7 7/7 3/3 2/3 0 28 44 65 97 116 140 167 Животных WB/Tl 519 1041 1465 2043 108 308 317 717 12/12 12/12 12/12 12/12 8/8 7/8 4/4 4/4 873 0 0 0 0 25 25 0 EPG Продолжение табл. 3 День после обработки 1035 мг пилюля 1260 мг пилюля Средн. Животных WB/Tl Средн. EPG 12/12 12/12 12/12 12/12 8/8 8/8 5/5 3/5 0 28 44 65 97 116 140 167 Животных WB/Tl 552 0 0 0 0 0 0 0 12/12 12/12 12/12 12/12 6/6 6/6 3/3 1/3 581 0 0 0 0 0 0 100 EPG WB/TI = с пилюлей/всего животных. Число контрольных животных, обработанных левамизолом (3,75 мг/кг) на 67 сутки опыта. EPG = яиц нематоды на 1 г фекалий. Таблица 4 Оценка пилюль, содержащих 23-(О-метилоксим)LL–F–28249a, на способность уничтожения нематод у крупного рогатого скота на длительное время 70 119 Конец действия вещества в пилюле, *) мг Количество животных с пилюлей/всего 1260 1035 День забивания животного после обработки 713 0 **) 1260 1035 % уменьшения взрослые личинки 4/4 4/4 100 100 100 100 4/4 4/4 100 4617 (4000–6167) 100 542 (333–667) 3/3 3/3 100 100 100 100 713 0 3/4 3/3 167 713 0 **) 100 674 (67–1155) 98,5 99,3 97,3 100 4/4 2/3 1260 1035 100 1752 (500–2400) 1/3+ 3/5 **) 100 2067 (1467–2533 100 617 (533–1881) Продолжение табл 4. День забивания животного после обработки % уменьшения взрослые личинки взрослые личинки 100 100 70 взрослые личинки 100 99,9 100 100 100 100 100 200 (66–533) 100 35783 (19600–51033) – – – 0 100 665 (310–1072) 100 67 (5–11) 100 100 167 100 100 100 100 100 100 100 100 100 441 (67–756) 100 74 (0–123) 98,8 23959 (18778–32500) 97,2 1322 (433–2533) 100 228 (60–400) 100 120 (0–31) 92,8 100 119 100 100 73,4 99,4 99,5 100 100 100 100 100 100 100 100 100 29567 (14033–59667) 100 400 (33–933) 100 413 (88–880) 100 2 (0–5) 100 10130 (3200–22898) *) На голову (в. 1/2 пилюли [25 грамм]). **) Число нематод: числа в скобках дают диапазон. + У животных с пилюлей нет гельминт. Таблица 5 Среднее количество живых клещей (Psoroptes ovis) на одно животное Дней после обработки Обработка 1 день до обработки 8 16 22 29 Пилюли, содержащие 375 мг 23-(О-метилоксим) ХХ ХХ – – – – 0 0 0 0 LL–F–28249 альфа ХХ ХХ – – – – 0 0 0 0 Контрольные необработанные 274 123 69 1 130 149 66 4 421 50 39 3 757 403 20 9 285 218 6 1 Продолжение табл 5. Обработка Дней после обработки 34 43 47 56 Пилюли, содержащие 375 мг 23-(О-метилоксим) 0 0 0 0 0 0 0 0 LL–F–28249 альфа 0 0 0 0 0 0 0 0 464 Забито Контрольные необработанные Забито 27 5 14 9 16 16 14 16 ХХ = животных, получивших пилюли, заразили через 1 неделю после начала эксперимента; было установлено, что колонии клещей не удерживаются на получавших лечение животных. – = колония клещей не удерживается на животных. Таблица 6 Оценка пилюль, содержащих 75, 375 и 1875 мг LL–F–28249a, на способность убивать нематоды у крупного рогатого скота Среднее количество яиц нематод на 1 г фекалий Обработка Талон Дни 0 7 62 10 (2850) 5 (99,9%) 755 146 Пилюля I (75 мг) 10 (2850) 940 (67%) 205 5 Пилюля II (375 мг) 10 (2850) 0 (100%) 0 5* Пилюля III (1875 мг) 10 (2850) 0 (100%) 0 5** Пилюля III (1875 мг) 10 (2850) 0 (100%) 0 5** (Рекомендованная доза) Левамизол 119 (Левамизол) 0 день и 62 день *1 животное имело 25 яиц нематод на 1 г фекалий; **6 животных имели пилюли и не имели яиц нематод; 4 животных, не получавших пилюли, имеют некоторое количество яиц нематод. Таблица 7 Эффективность пилюль с LL–F–28259a против нематод у крупного рогатого скота % уничтожения нематод Обработка Животное Haemouchus Ostertagia Cooperia Oesophlogostonum 10 92 100 0 25 375 мг пилюля 10 100 100 97 99+ 1875 мг пилюля 110 100 100 99+ 100 Левамизол 10 2325 729 5937 117 75 мг пилюля Контрольная группа, среднее количество глистов (57 дней назад глистов выгнали) Таблица 8 Привесы у крупного рогатого скота, получавшего левамизол 3,75 мг/день на 0 и 62 день, и от пилюль с LL–F–28249a со скоростью выделения 0,37 мг/голова/день; 1,96 мг/голова/день и 3,76 мг/голова/день LL–F–28249a Средние привесы (кг) с 0 дня Обработка Дни 7 62 110 Левамизол (3,75 мг/кг на 0 и 62 день) 7 0 21 Пилюля I 75 мг (0,0031 мг/кг/день) 5 7 34 Пилюля II 375 мг (0,016 мг/кг/день) 6 11 37 Пилюля III (0,031 мг/кг/день) 8 15 40 Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03
ДивитисяДодаткова інформація
Назва патенту англійськоюBolus with sustained release of active ingredient, method for protecting ruminant animals from infestation by helminths, method for preventing, inhibiting, controlling or decreasing infestation of ruminant animals, method for preparing bolus
Автори англійськоюWOOD IRWIN BOYDEN, TOOTHILL RICHARD BOARDMAN, DIETZ JOSEPH CHARLES
Назва патенту російськоюБолюс с пролонгированным выделением активного ингредиента, способ защиты жвачных животных от заражения гельминтами, способ профилактики или угнетения, системного контроля предотвращения или снижения частоты заражения у жвачных животных, способ получения болюсов
Автори російськоюВуд Ирвин Бойден, Тутхилл Ричард Бодман, Диц Джозеф Чарльз
МПК / Мітки
МПК: A61K 9/22, A61K 31/70, A61P 33/00
Мітки: контролю, аб0, виділенням, гельмінтами, інгредієнта, пролонованим, зниження, тварин, захисту, жуйних, запобігання, активного, зараженн, зараження, болюс, жуй, спосіб, пригнічення, профілактики, системного
Код посилання
<a href="https://ua.patents.su/12-37173-bolyus-z-prolonovanim-vidilennyam-aktivnogo-ingrediehnta-sposib-zakhistu-zhujjnikh-tvarin-vid-zarazhennya-gelmintami-sposib-profilaktiki-ab0-prignichennya-sistemnogo-kontrolyu-zniz.html" target="_blank" rel="follow" title="База патентів України">Болюс з пролонованим виділенням активного інгредієнта, спосіб захисту жуйних тварин від зараження гельмінтами, спосіб профілактики аб0 пригнічення, системного контролю зниження або запобігання зараженнь у жуй</a>
Попередній патент: Спосіб одержання антидимної присадки до моторних палив
Наступний патент: Ротаційний віскозиметр
Випадковий патент: Спосіб захисту та відновлення деталей чавунних виробів