Людське моноклональне антитіло, яке специфічно зв’язується з лігандом-1 запрограмованої загибелі клітин (pd-l1)
Номер патенту: 99701
Опубліковано: 25.09.2012
Автори: Пассмор Девід Б., Срінівасан Мохан, Чень Хайбінь, Корман Алан Дж., Селбі Марк Дж., Хуань Хайчунь, Ванг Чангіу
Формула / Реферат
1. Моноклональне антитіло або його антигензв'язувальна частина, які конкурують за перехресне зв'язування з PD-L1 з еталонним антитілом або його еталонною антигензв'язувальною частиною, що містять
(a) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 1, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 11;
(b) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 2, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 12;
(c) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 3, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 13;
(d) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 4, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 14;
(e) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 5, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 15;
(f) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 6, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 16;
(g) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 7, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 17;
(h) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 8, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 18;
(i) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 9, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 19; або
(j) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 10, і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 20,
де варіабельна область важкого ланцюга вказаних моноклонального антитіла або його антигензв'язувальної частини містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії, вибраним з групи, що складається з людського гена зародкової лінії VН 1-18, що має послідовність SEQ ID NO: 101, людського гена зародкової лінії VН 1-69, що має послідовність SEQ ID NO: 102, людського гена зародкової лінії VН 1-3, що має послідовність SEQ ID NO: 103, і людського гена зародкової лінії VН 3-9, що має послідовність SEQ ID NO: 104; і
де варіабельна область легкого ланцюга вказаних моноклонального антитіла або його антигензв'язувальної частини містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії, вибраним з групи, що складається з людського гена зародкової лінії VK L6, що має послідовність SEQ ID NO: 105, людського гена зародкової лінії VK L15, що має послідовність SEQ ID NO: 106, людського гена зародкової лінії VK A27, що має послідовність SEQ ID NO: 107, і людського гена зародкової лінії VK L18, що має послідовність SEQ ID NO: 108.
2. Моноклональне aнтитіло або його антигензв'язувальна частина за п. 1, які зв'язуються з PD-L1 з КD, яка становить 5×10-9 М або менше.
3. Моноклональне aнтитіло або його антигензв'язувальна частина за п. 1, які зв'язуються з PD-L1 з КD, яка становить 2×10-9 М або менше.
4. Антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область важкого ланцюга містить амінокислоти, що мають послідовність SEQ ID NO: 1; а вказана людська варіабельна область легкого ланцюга містить амінокислоти, що мають послідовність SEQ ID NO: 11.
5. Антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область важкого ланцюга містить амінокислоти, що мають послідовність SEQ ID NO: 2; а вказана людська варіабельна область легкого ланцюга містить амінокислоти, що мають послідовність SEQ ID NO: 12.
6. Антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область важкого ланцюга містить амінокислоти, що мають послідовність SEQ ID NO: 3; а вказана людська варіабельна область легкого ланцюга містить амінокислоти, що мають послідовність SEQ ID NO: 13.
7. Mоноклональне антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область важкого ланцюга містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 1-18, що має послідовність SEQ ID NO: 101.
8. Mоноклональне антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область важкого ланцюга містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VН 1-69, що має послідовність SEQ ID NO: 102.
9. Mоноклональне антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область важкого ланцюга містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VН 1-3, що має послідовність SEQ ID NO: 103.
10. Mоноклональне антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область легкого ланцюга містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L6, що має послідовність SEQ ID NO: 105.
11. Mоноклональне антитіло або його антигензв'язувальна частина за п. 1, де вказана варіабельна область легкого ланцюга містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L15, що має послідовність SEQ ID NO: 106.
12. Mоноклональне антитіло або його антигензв'язувальна частина за п. 1, що містять:
(a) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 1-69, що має послідовність SEQ ID NO: 102; і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK A27, що має послідовність SEQ ID NO: 107;
(b) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 3-9, що має послідовність SEQ ID NO: 104; і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L15, що має послідовність SEQ ID NO: 106; або
(c) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 3-9, що має послідовність SEQ ID NO: 104; і варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L18, що має послідовність SEQ ID NO: 108;
де вказане антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1.
13. Mоноклональне антитіло або його антигензв'язувальна частина, що містять:
(a) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 1-18, що має послідовність SEQ ID NO: 101; і
(b) варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L6, що має послідовність SEQ ID NO: 105;
де вказане антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1.
14. Mоноклональне антитіло або його антигензв'язувальна частина, що містять:
(a) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 1-69, що має послідовність SEQ ID NO: 102; і
(b) варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L6, що має послідовність SEQ ID NO: 105;
де вказане антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1.
15. Mоноклональне антитіло або його антигензв'язувальна частина, що містять:
(a) варіабельну область важкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VH 1-3, що має послідовність SEQ ID NO: 103; і
(b) варіабельну область легкого ланцюга, яка містить амінокислоти, що мають послідовність, яка щонайменше на 90 % ідентична послідовності, що кодується людським геном зародкової лінії VK L15, що має послідовність SEQ ID NO: 106;
де вказане антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1.
16. Моноклональне антитіло або його антигензв'язувальна частина, що включають варіабельну область важкого ланцюга, яка містить домени CDR1, CDR2 і CDR3, і варіабельну область легкого ланцюга, яка містить домени CDR1, CDR2 і CDR3, де вказані домени CDR3 варіабельної області важкого ланцюга і варіабельної області легкого ланцюга вибрані з групи, яка складається з:
(a) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 41; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 71, і їх консервативних модифікацій;
(b) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 42; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 72, і їх консервативних модифікацій;
(c) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 43; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 73, і їх консервативних модифікацій;
(d) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 44; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 74, і їх консервативних модифікацій;
(e) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 45; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 75, і їх консервативних модифікацій;
(f) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 46; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 76, і їх консервативних модифікацій;
(g) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 47; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 77, і їх консервативних модифікацій;
(h) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 48; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 78, і їх консервативних модифікацій;
(i) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 49; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 79, і їх консервативних модифікацій; і
(j) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 50; і CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 80, і їх консервативних модифікацій;
де вказані антитіло і його антигензв'язувальна частина специфічно зв'язуються з людським PD-L1.
17. Антитіло або його антигензв'язувальна частина за п. 16, де вказані домени CDR2 варіабельної області важкого ланцюга і варіабельної області легкого ланцюга вибрані з групи, яка складається з:
(a) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 31; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 61, і їх консервативних модифікацій;
(b) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 32; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 62, і їх консервативних модифікацій;
(c) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 33; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 63, і їх консервативних модифікацій;
(d) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 34; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 64, і їх консервативних модифікацій;
(e) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 35; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 65, і їх консервативних модифікацій;
(f) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 36; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 66, і їх консервативних модифікацій;
(g) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 37; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 67, і їх консервативних модифікацій;
(h) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 38; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 68, і їх консервативних модифікацій;
(i) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 39; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 69, і їх консервативних модифікацій; і
(j) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 40; і CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 70, і їх консервативних модифікацій.
18. Антитіло або його антигензв'язувальна частина за п. 17, де вказані домени CDR1 варіабельної області важкого ланцюга і варіабельної області легкого ланцюга вибрані з групи, яка складається з:
(a) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 21; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 51, і їх консервативних модифікацій;
(b) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 22; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 52, і їх консервативних модифікацій;
(c) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 23; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 53, і їх консервативних модифікацій;
(d) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 24; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 54, і їх консервативних модифікацій;
(e) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 25; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 55, і їх консервативних модифікацій;
(f) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 26; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 56, і їх консервативних модифікацій;
(g) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 27; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 57, і їх консервативних модифікацій;
(h) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 28; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 58, і їх консервативних модифікацій;
(i) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 29; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 59, і їх консервативних модифікацій; і
(j) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 30; і CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 60, і їх консервативних модифікацій.
19. Моноклональне антитіло або його антигензв'язувальна частина, що включають варіабельну область важкого ланцюга і варіабельну область легкого ланцюга, вибрані з групи, яка складається з:
(a) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 1, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 11;
(b) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 2, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 12;
(c) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 3, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 13;
(d) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 4, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 14;
(e) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 5, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 15;
(f) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 6, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 16;
(g) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 7, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 17;
(h) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 8, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 18;
(i) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 9, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 19; і
(j) варіабельнoї області важкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 10, і варіабельної області легкого ланцюга, яка містить амінокислотну послідовність, яка щонайменше на 95 % гомологічна амінокислотам, що мають послідовність SEQ ID NO: 20;
де вказане антитіло специфічно зв'язується з PD-L1 з КD, яка становить 1×10-7 М або менше.
20. Моноклональне антитіло або його антигензв'язувальна частина, що включають варіабельну область важкого ланцюга, яка містить домени CDR1, CDR2 і CDR3, і варіабельну область легкоголанцюга, яка містить домени CDR1, CDR2 і CDR3, де домени CDR1, CDR2 і CDR3 варіабельної області важкого ланцюга і варіабельної області легкого ланцюга вибрані з групи, яка складається з:
(a) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 21; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 31; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 41; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 51; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 61; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 71;
(b) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 22; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 32; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 42; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 52; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 62; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 72;
(c) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 23; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 33; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 43; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 53; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 63; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 73;
(d) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 24; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 34; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 44; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 54; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 64; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 74;
(e) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 25; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 35; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 45; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 55; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 65; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 75;
(f) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 26; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 36; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 46; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 56; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 66; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 76;
(g) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 27; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 37; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 47; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 57; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 67; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 77;
(h) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 28; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 38; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 48; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 58; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 68; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 78;
(i) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 29; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 39; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 49; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 59; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 69; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 79; і
(j) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 30; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 40; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 50; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 60; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 70; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 80;
де вказані антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1.
21. Антитіло або його антигензв'язувальна частина за п. 20, які включають:
(a) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 21;
(b) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 31;
(c) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 41;
(d) CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 51;
(e) CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 61; і
(f) CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 71.
22. Антитіло або його антигензв'язувальна частина за п. 20, які включають:
(a) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 22;
(b) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 32;
(c) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 42;
(d) CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 52;
(e) CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 62; і
(f) CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 72.
23. Антитіло або його антигензв'язувальна частина за п. 20, які містять:
(a) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 23;
(b) CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 33;
(c) CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 43;
(d) CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 53;
(e) CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 63; і
(f) CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 73.
24. Моноклональне антитіло або його антигензв'язувальна частина, що містять варіабельну область важкого ланцюга і варіабельну область легкого ланцюга, вибрані з групи, яка складається з:
(а) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 1, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 11;
(b) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 2, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 12;
(c) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 3, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 13;
(d) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 4, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 14;
(e) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 5, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 15;
(f) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 6, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 16;
(g) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 7, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 17;
(h) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 8, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 18;
(i) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 9, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 19; і
(j) варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 10, і варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 20;
де вказані антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1.
25. Антитіло або його антигензв'язувальна частина за п. 24, які включають:
(a) варіабельну область важкого ланцюга, що містить амінокислоти, які мають послідовність SEQ ID NO: 1; і
(b) варіабельну область легкого ланцюга, що містить амінокислоти, які мають послідовність SEQ ID NO: 11.
26. Антитіло або його антигензв'язувальна частина за п. 24, які містять:
(a) варіабельну область важкого ланцюга, що містить амінокислоти, які мають послідовність SEQ ID NO: 2; і
(b) варіабельну область легкого ланцюга, що містить амінокислоти, які мають послідовність SEQ ID NO: 12.
27. Антитіло або його антигензв'язувальна частина за п. 24, які включають:
(a) варіабельну область важкого ланцюга, що містить амінокислоти, які мають послідовність SEQ ID NO: 3; і
(b) варіабельну область легкого ланцюга, що містить амінокислоти, які мають послідовність SEQ ID NO: 13.
28. Моноклональне антитіло або його антигензв'язувальна частина за будь-яким з пп. 1-27, які являють собою антитіло ізотипу IgG1 або IgG4 або його антигензв’язувальну частину.
29. Моноклональне антитіло або його антигензв'язувальна частина за будь-яким з пп. 1-27, які являють собою одноланцюжкове антитіло або його фрагмент.
30. Моноклональне антитіло або його антигензв'язувальна частина за будь-яким з пп. 1-27, які являють собою химерне антитіло або його частину.
31. Моноклональне антитіло або його антигензв'язувальна частина за будь-яким з пп. 1-27, які являють собою гуманізоване антитіло або його частину.
32. Моноклональне антитіло або його антигензв'язувальна частина за будь-яким з пп. 1-27, які являють собою повністю людське антитіло або його частину.
33. Антитіло або його антигензв'язувальна частина за будь-яким з пп. 1-27, яке підвищує:
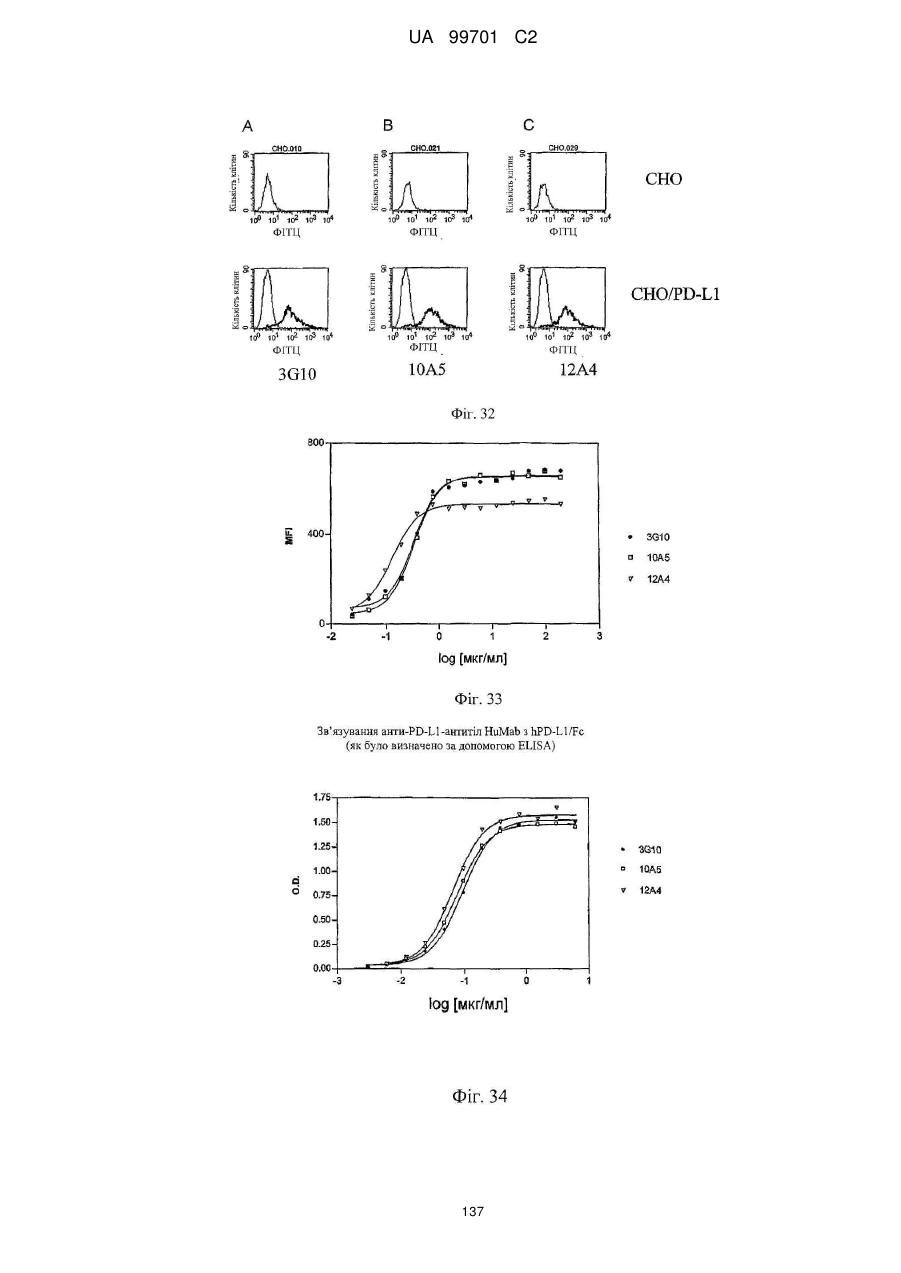
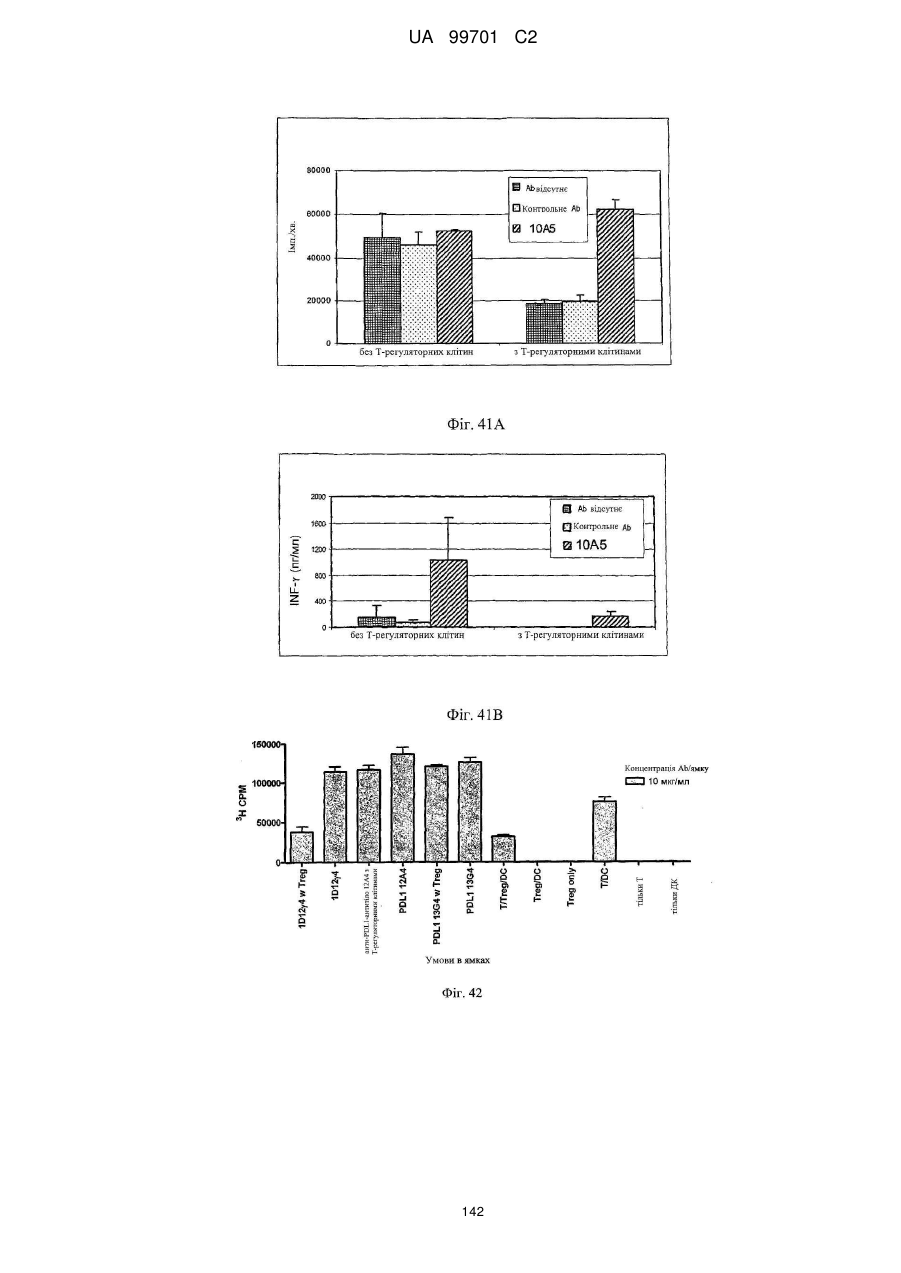
(a) рівень проліферації Т-клітин в аналізі реакцій у змішаній культурі лімфоцитів (РЗКЛ);
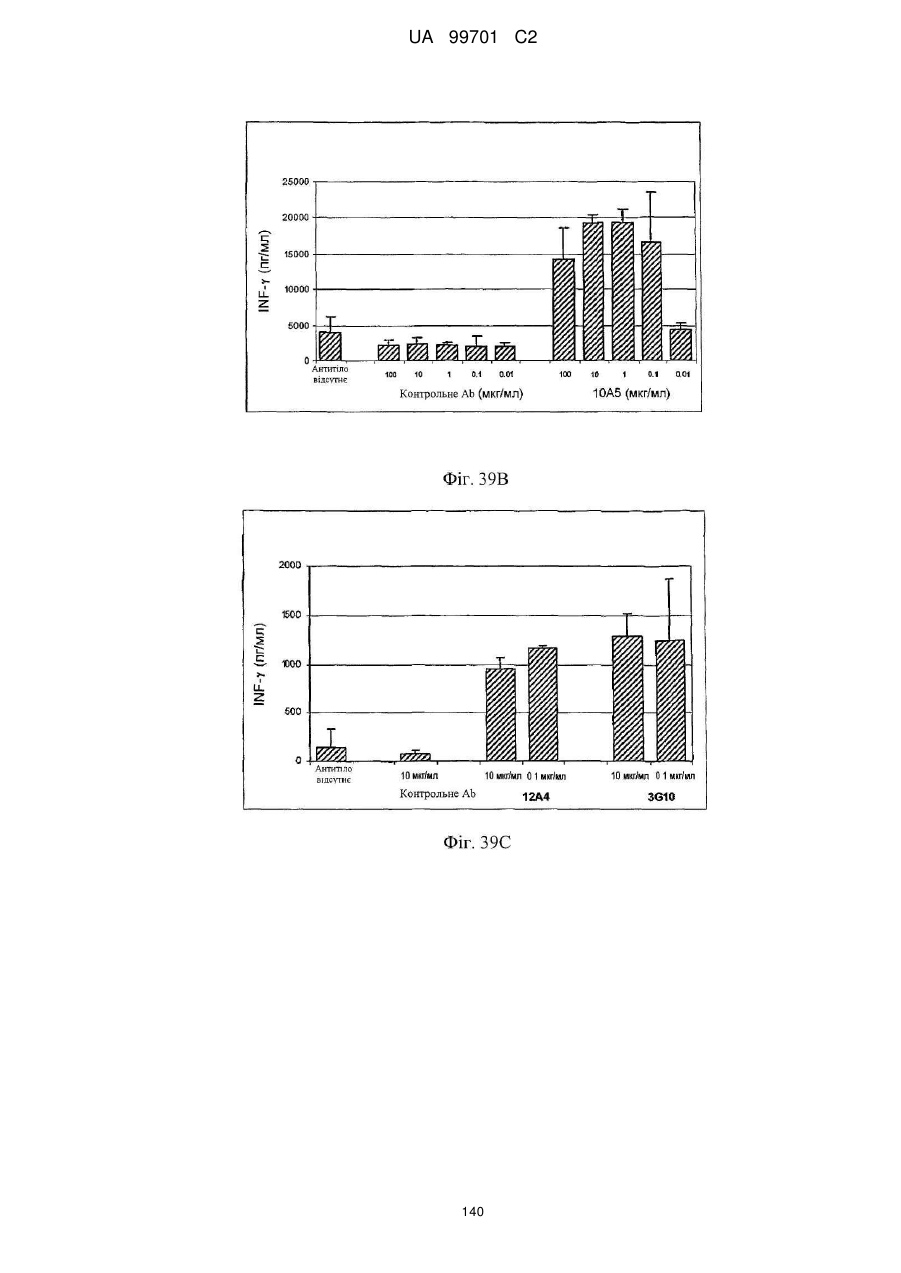
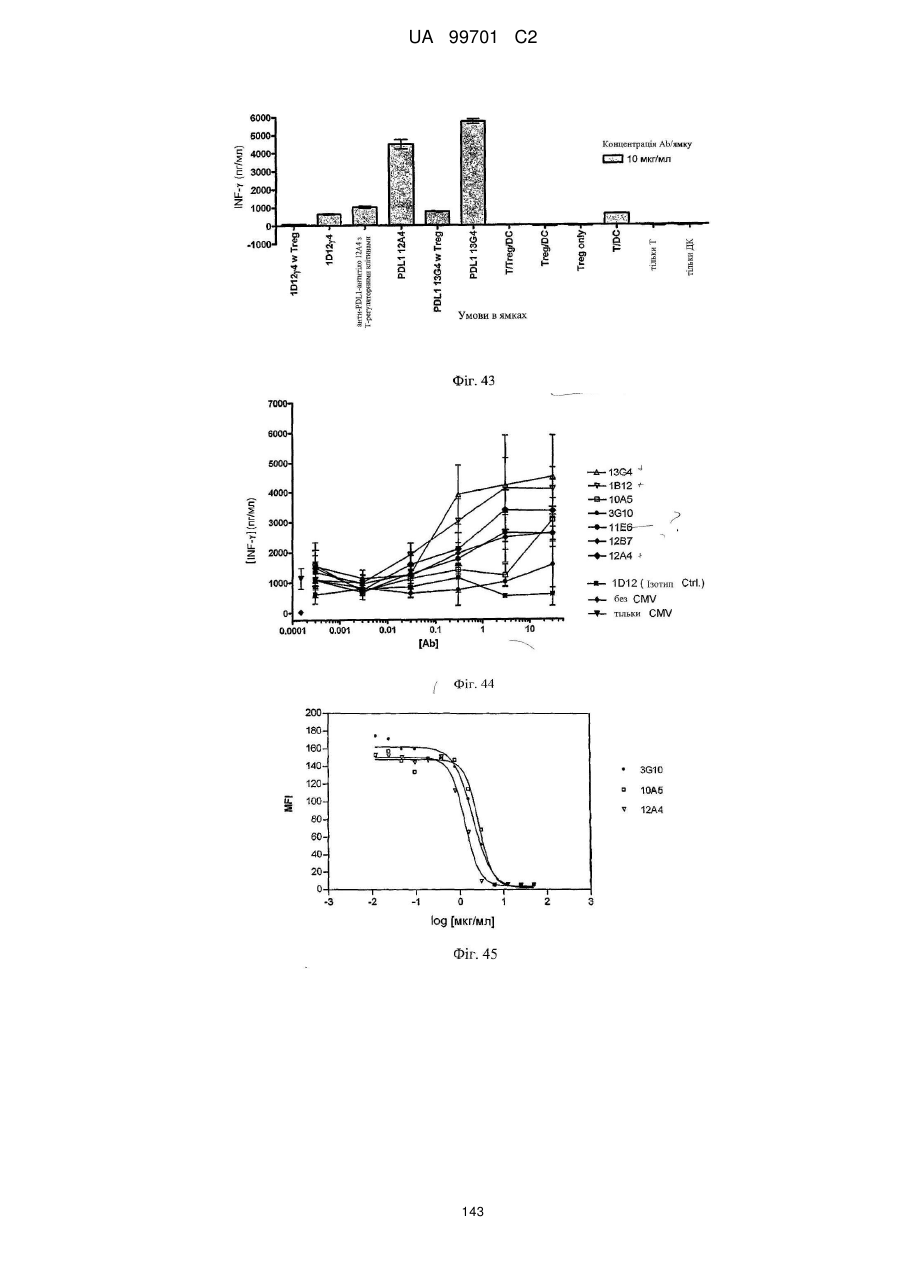
(b) рівень продукування інтерферону-γ в аналізі РЗКЛ; і/або
(c) рівень секреції IL-2 в аналізі РЗКЛ.
34. Композиція, яка містить моноклональне антитіло або його антигензв'язувальну частину за будь-яким з пп. 1-33 і фармацевтично прийнятний носій.
35. Імунокон'югат, який містить моноклональне антитіло або його антигензв'язувальну частину за будь-яким з пп. 1-33, зв'язані з терапевтичним засобом.
36. Імунокон'югат за п. 35, де вказаним терапевтичним засобом є цитотоксин або радіоактивний ізотоп.
37. Композиція, яка містить імунокон'югат за п. 35 або 36 і фармацевтично прийнятний носій.
38. Біспецифічна молекула, яка містить моноклональне антитіло або його антигензв'язувальну частину за будь-яким з пп. 1-33, зв'язані з другою функціональною молекулою, яка має специфічність зв'язування, що відрізняється від специфічності зв'язування вказаного антитіла або його антигензв'язувальної частини.
39. Композиція, що містить біспецифічну молекулу за п. 38 і фармацевтично прийнятний носій.
40. Виділена нуклеїнова кислота, яка кодує моноклональне антитіло або його антигензв'язувальну частину за будь-яким з пп. 1-33.
41. Експресуючий вектор, який містить нуклеїнову кислоту за п. 40.
42. Клітина-хазяїн, яка містить експресуючий вектор за п. 41.
43. Трансгенна миша, яка несе трансгени важкого і легкого ланцюгів людського імуноглобуліну, де у вказаної миші експресується моноклональне антитіло за п. 32.
44. Гібридома, приготовлена з миші за п. 43, де гібридома продукує вказане моноклональне антитіло.
45. Спосіб модуляції імунної відповіді у індивіда, який включає введення вказаному індивіду моноклонального антитіла або його антигензв'язувальної частини за будь-яким з пп. 1-33, так що відбувається модуляція імунної відповіді у вказаного індивіда.
46. Спосіб інгібування росту пухлинних клітин у індивіда, який включає введення вказаному індивіду моноклонального антитіла або його антигензв'язувальної частини за будь-яким з пп. 1-33 так, щоб викликати інгібування росту пухлинних клітин у індивіда.
47. Спосіб за п. 46, де вказаними пухлинними клітинами є клітини злоякісної пухлини, вибраної з групи, яка складається з меланоми, раку нирок, раку передміхурової залози, раку молочної залози, раку товстої кишки і раку легенів.
48. Спосіб за п. 47, де вказаними пухлинними клітинами є злоякісні клітини, вибрані з групи, яка складається з раку кістки, раку підшлункової залози, раку шкіри, раку голови і шиї, злоякісної меланоми шкіри або внутрішньоочної меланоми, раку матки, раку яєчника, раку прямої кишки, раку заднього проходу, раку шлунка, раку яєчок, карциноми фалопієвих труб, карциноми ендометрія, карциноми шийки матки, карциноми піхви, карциноми вульви, хвороби Ходжкіна, неходжкінської лімфоми, раку стравоходу, раку тонкого кишечнику, раку ендокринної системи, раку щитовидної залози, раку паращитовидної залози, раку кори надниркової залози, саркоми м'яких тканин, раку уретри, раку пенісу, хронічного або гострого лейкозу, включаючи гострий мієлоїдний лейкоз, хронічний мієлоїдний лейкоз, гострий лімфобластний лейкоз, хронічний лімфоцитарний лейкоз; солідних пухлин у дітей, лімфоцитарної лімфоми, раку сечового міхура, раку нирок або сечоводу, карциноми ниркової миски, пухлини центральної нервової системи (ЦНС), первинної лімфоми ЦНС, пухлинного ангіогенезу, пухлини хребта, гліоми стовбура головного мозку, аденоми гіпофізу, саркоми Капоші, епідермоїдного раку, плоскоклітинного раку, Т-клітинної лімфоми, злоякісної пухлини, індукованої впливом навколишнього середовища, включаючи злоякісні пухлини, індуковані азбестом, і їх комбінацій.
49. Спосіб лікування інфекційного захворювання у індивіда, який включає введення вказаному індивіду моноклонального антитіла або його антигензв'язувальної частини за будь-яким з пп. 1-33 з метою лікування інфекційного захворювання у вказаного індивіда.
50. Спосіб за п. 49, де вказане інфекційне захворювання являє собою:
(a) захворювання, вибране з групи, яка складається з грипу, герпесу, Giardia, малярії і Leishmania;
(b) патогенну інфекцію, викликану вірусом, вибраним з групи, яка складається з вірусу імунодефіциту людини (ВІЛ), вірусу гепатиту, герпесвірусу, аденовірусу, вірусу грипу, флавівірусу, ECHO-вірусу, риновірусу, вірусу коксаки, коронавірусу, респіраторно-синцитіального вірусу, вірусу паротиту, ротавірусу, вірусу кору, вірусу корової краснухи, парвовірусу, вірусу коров'ячої віспи, вірусу HTLV, вірусу денге, папіломавірусу, вірусу контагіозного молюска, поліовірусу, вірусу сказу, вірусу Джеймстаун-Каньйон (JC) і вірусу арбовірусного енцефаліту;
(c) патогенну інфекцію, викликану бактеріями, вибраними з групи, яка складається з хламідій, рикетсій, мікобактерій, стафілококів, стрептококів, пневмококів, менінгококів і ґонококів, бактерій Klebsiella, Proteus, Serratia, Pseudomonas, Legionella, Diphtheria, Salmonella, Bacilli, холерного токсину, правцевого токсоїду, ботулінічного токсину, токсину сибірської виразки, бактерії, що викликає чуму; бактерії, що викликає лептоспіроз, і бактерії, що викликає хворобу Лайма;
(d) патогенну інфекцію, викликану грибом, вибраним з групи, що складається з Candida, Cryptococcus neoformans, Aspergillus, гриба роду Mucorales, Sporothrix schenkii, Blastomyces dermatitidis, Paracoccidioides brasiliensis, Coccidioides immitis і Histoplasma capsulatum; або
(e) патогенну інфекцію, що викликається паразитом Entamoeba histolytica, Balantidium coli, Naegleria fowleri, Acanthamoeba sp., Giardia lambia, Cryptosporidium sp., Pneumocystis carinii, Plasmodium vivax, Babesia microti, Trypanosoma brucei, Trypanosoma cruzi, Leishmania donovani, Toxoplasma gondi і Nippostrongylus brasiliensis.
51. Спосіб за п. 50, де вірус гепатиту вибирають з групи, яка складається з гепатиту A, гепатиту B, гепатиту C та будь-якої їх комбінації.
52. Спосіб за п. 50, де вірус герпесу вибраний з групи, яка складається з VZV, HSV-1, HAV-6, HSV-II та CMV, вірусу Епштейна-Барр та будь-якої їх комбінації.
53. Спосіб за п. 50, де гриб Candida вибраний з групи, яка складається з Candida albicans, Candida krusei, Candida glabrata, Candida tropicalis та будь-якої їх комбінації.
54. Спосіб за п. 50, де гриб Aspergillus вибраний з групи, яка складається з fumigatus, niger та будь-якої їх комбінації.
55. Спосіб за п. 50, де гриб роду Mucorales вибраний з групи, яка складається з mucor, absidia, rhizophus та будь-якої їх комбінації.
56. Спосіб посилення імунної відповіді на антиген у індивіда, який включає введення вказаному індивіду антигену і моноклонального антитіла або його антигензв'язувальної частини за будь-яким з пп. 1-33 з метою посилення імунної відповіді на вказаний антиген у даного індивіда.
57. Спосіб за п. 56, де вказаним антигеном є пухлинний антиген, вірусний антиген, бактеріальний антиген або антиген патогену.
58. Спосіб лікування або попередження запального захворювання у індивіда, який включає введення вказаному індивіду моноклонального антитіла або його антигензв'язувальної частини за будь-яким з пп. 1-33 для лікування вказаного запального захворювання у даного індивіда.
59. Спосіб за п. 58, де вказаним запальним захворюванням є плoский лишай (ПЛ).
60. Спосіб за будь-яким з пп. 45, 46, 49, 56 та 59, де моноклональне антитіло або його антигензв'язувальна частина являють собою химерне антитіло або його частину.
61. Спосіб за будь-яким з пп. 45, 46, 49, 56 та 59, де моноклональне антитіло або його антигензв'язувальна частина являють собою гуманізоване антитіло або його частину.
62. Спосіб за будь-яким з пп. 45, 46, 49, 56 та 59, де моноклональне антитіло або його антигензв'язувальна частина являють собою повністю людське антитіло або його частину.
63. Спосіб одержання анти-PD-L1-антитіла, який включає:
(і) забезпечення нуклеїнової кислоти, яка кодує антитіло або його антигензв'язувальну частину, що включають послідовність варіабельної області важкого ланцюга антитіла, яка включає домени CDR1, CDR2 і CDR3, і послідовність варіабельної області легкого ланцюга антитіла, яка включає домени CDR1, CDR2 і CDR3, де вказані домени CDR1, CDR2 і CDR3 варіабельної області важкого ланцюга і варіабельної області легкого ланцюга вибрані з групи, яка складається з:
(a) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 21; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 31; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 41; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 51; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 61; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 71;
(b) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 22; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 32; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 42; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 52; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 62; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 72;
(c) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 23; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 33; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 43; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 53; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 63; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 73;
(d) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 24; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 34; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 44; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 54; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 64; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 74;
(e) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 25; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 35; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 45; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 55; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 65; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 75;
(f) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 26; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 36; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 46; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 56; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 66; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 76;
(g) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 27; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 37; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 47; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 57; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 67; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 77;
(h) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 28; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 38; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 48; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 58; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 68; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 78;
(i) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 29; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 39; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 49; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 59; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 69; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 79;
(j) CDR1 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 30; CDR2 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 40; CDR3 варіабельної області важкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 50; CDR1 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 60; CDR2 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 70; CDR3 варіабельної області легкого ланцюга, яка містить амінокислоти, що мають послідовність SEQ ID NO: 80;
(іі) модифікацію нуклеїнової кислоти, яка кодує щонайменше один амінокислотний залишок щонайменше в одній варіабельній області з метою створення нуклеїнової кислоти, яка кодує модифіковане антитіло або його антигензв'язувальну частину, які містять щонайменше одну модифікацію амінокислотної послідовності, де вказані модифіковане антитіло або його антигензв'язувальна частина специфічно зв'язуються з PD-L1; і
(ііі) експресію вказаної модифікованої послідовності антитіла у вигляді білка.
Текст
Реферат: Даний винахід належить до виділених моноклональних антитіл, зокрема до людських моноклональних антитіл, що специфічно зв'язуються з PD-L1 з високою афінністю. Даний винахід належить також до молекул нуклеїнової кислоти, що кодують антитіла відповідно до винаходу, до експресуючих векторів, до клітин-хазяїнів і до способів експресії антитіл відповідно до винаходу. Даний винахід належить також до імунокон'югатів, біспецифічних молекул і до фармацевтичних композицій, що містять антитіла відповідно до винаходу. Даний винахід належить також до способів детектування PD-L1, а також до способів лікування різних захворювань, включаючи злоякісні й інфекційні захворювання, з використанням анти-PD-L1антитіл. UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 Перехресне посилання на родинні заявки У даній заявці вимагається пріоритет попередньої заявки на патент США 60/696426, поданої 1 липня, 2005, яка у всій своїй повноті вводиться в даний опис за допомогою посилання. Попередній рівень техніки Ліганд-1 запрограмованої загибелі клітин (PD-1) являє собою член сімейства CD28 рецепторів, які включають в себе CD28, CTLA-4, ICOS, PD-1 і BTLA. Перші члени цього сімейства, CD28 і ICOS, були виявлені по їх функціональній дії, спрямованій на підвищення рівня проліферації Т-клітин після додавання моноклональних антитіл (Hutloff et al. (1999) Nature 397:263-266; Hansen et al. (1980) Immunogenics 10:247-260). Були ідентифіковані два поверхневих глікопротеїнових ліганди для PD-1, а саме, PD-L1 і PD-L2, і було показано, що ці ліганди інгібують активацію Т-клітин і секрецію цитокінів після зв'язування з PD-1 (Freeman et al. (2000) J. Exp. Med. 192:1027-34; Latchman et al. (2001) Nat. Immunol. 2:261-8; Carter et al. (2002) Eur. J. Immunol. 32:634-43; Ohigashi et al. (2005) Clin. Cancer Res. 11:2947-53). Обидва ліганди PD-L1 (B7-H1) і PD-L2 (B7-DC) є гомологами B7, які зв'язуються з PD-1, але не зв'язуються з іншими членами сімейства CD28 (Blank et al. (2004)). Було також показано, що експресія PD-L1 на клітинній поверхні активується за допомогою стимуляції IFN-γ. Експресія PD-L1 була виявлена при деяких ракових захворюваннях миші і людини, включаючи людські карциноми легень, яєчника і товстої кишки і різні мієломи (Iwai et al. (2002) PNAS 99:12293-7; Ohigashi et al., (2005) Clin. Cancer Res. 11:2947-53). Було висловлене припущення, що PD-L1 відіграє визначену роль у виробленні протипухлинної імунної відповіді шляхом підвищення рівня апоптозу антигенспецифічних Т-клітинних клонів (Dong et al. (2002) Nat. Med. 8:793-800). Було також висловлене припущення, що PD-L1 може брати участь у розвитку запалення слизової тонкої кишки, а інгібування PD-L1 приводить до пригнічення кахексії, асоційованої з колітом (Kanai et al.(2003) J. Immunol. 171:4156-63). Короткий опис суті винаходу Даний винахід належить до виділених моноклональних антитіл, зокрема до людських моноклональних антитіл, які зв'язуються з PD-L1 і мають різні бажані властивості. Такою властивістю є висока афінність зв'язування з людським PD-L1. Крім того, було показано, що антитіла відповідно до винаходу сприяють посиленню проліферації Т-клітин, секреції IFN- і секреції IL-2 у реакції змішаної культури лімфоцитів. В одному зі своїх аспектів, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, де зазначене антитіло має щонайменше одну з наступних властивостей: -7 (a) здатність зв'язуватися з людським PD-L1 з КD, яка складає 1×10 М або менше; (b) здатність підвищувати рівень проліферації T-клітин в аналізі реакцій у змішаній культурі лімфоцитів (РЗКЛ); (c) здатність підвищувати рівень продукування інтерферону-γ в аналізі РЗКЛ; (d) здатність підвищувати рівень секреції IL-2 в аналізі РЗКЛ; (e) здатність стимулювати гуморальну відповідь; або (f) здатність блокувати дію регуляторних Т-клітин на ефекторні T-клітини і/або дендритні клітини. Переважним антитілом є людське антитіло, хоча в альтернативних варіантах здійснення винаходу, може бути використане, наприклад, мишаче антитіло, химерне антитіло або гуманізоване антитіло. У конкретних варіантах винаходу, зазначене антитіло зв'язується з людським PD-L1 з КD, яка -8 -8 -9 складає 5×10 М або менше; з КD, яка складає 1×10 М або менше, з КD, яка складає 5×10 М -9 -8 або менше, з КD, яка складає 1×10 М або менше, або з КD, яка складає від 5×10 М до з КD, яка -8 -10 складає 1×10 М і 1×10 М. В іншому своєму варіанті, даний винахід належить до моноклонального антитіла або до його антигензв‟язувальної частини, де зазначене антитіло конкурує за перехресне зв'язування з PDL1 з відомим антитілом, яке містить (a) варіабельну область людського важкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9 і 10; і (b) варіабельну область людського легкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:11, 12, 13, 14, 15, 16, 17, 18, 19 і 20. У різних варіантах винаходу, зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:1; і 1 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:11; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:2; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:12; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:3; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:13; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:4; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:14; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:5; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:15; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:6; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:16; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:7; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:17; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:8; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:18; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:9; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:19; або зазначене відоме антитіло містить: (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:10; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність SEQ ID NO:20. В іншому своєму аспекті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, які включають в себе варіабельну область важкого ланцюга, яка є продуктом людського гена VH 1-18 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область важкого ланцюга, яка є продуктом людського гена V H 1-69 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область важкого ланцюга, яка є продуктом людського гена VH 1-3 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область важкого ланцюга, яка є продуктом людського гена VH 3-9 або походить від цього продукту, де 2 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область легкого ланцюга, яка є продуктом людського гена V K L6 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область легкого ланцюга, яка є продуктом людського гена VK L15 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область легкого ланцюга, яка є продуктом людського гена VK A27 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. Даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе варіабельну область легкого ланцюга, яка є продуктом людського гена VK L18 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. У своєму конкретному переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе (a) варіабельну область важкого ланцюга, яка кодується людським геном V H 1-18; і (b) варіабельну область легкого ланцюга, яка кодується людським геном V K L6; де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе (a) варіабельну область важкого ланцюга, яка кодується людським геном V H 1-69; і (b) варіабельну область легкого ланцюга, яка кодується людським геном VK L6; де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе (a) варіабельну область важкого ланцюга, яка кодується людським геном V H 1-3; і (b) варіабельну область легкого ланцюга, яка кодується людським геном V K L15; де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе (a) варіабельну область важкого ланцюга, яка кодується людським геном V H 1-69; і (b) варіабельну область легкого ланцюга, яка кодується людським геном VK А27; де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе (a) варіабельну область важкого ланцюга, яка кодується людським геном VH 3-9; і (b) варіабельну область легкого ланцюга, яка кодується людським геном V K L15; де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включає в себе (a) варіабельну область важкого ланцюга, яка кодується людським геном V H 3-9; і (b) варіабельну область легкого ланцюга, яка кодується людським геном V K L18; де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму аспекті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область важкого ланцюга, яка включає в себе послідовності CDR13 CDR2 і CDR3, і варіабельну область легкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, де (a) CDR3 варіабельної області важкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50 і і їхніх консервативних модифікацій; (b) CDR3 варіабельної області легкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80 і їхніх консервативних модифікацій; і (c) зазначене антитіло специфічно зв'язується з людським PD-L1. Переважно, CDR2 варіабельної області важкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40 і їхніх консервативних модифікацій; а CDR2 варіабельної області легкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:61, 62, 63, 64, 3 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 65, 66, 67, 68, 69 і 70 і їхніх консервативних модифікацій. Переважно, CDR1 варіабельної області важкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30 і їхніх консервативних модифікацій; а CDR1 варіабельної області легкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60 і їхніх консервативних модифікацій. У ще одному своєму аспекті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що містять варіабельну область важкого ланцюга і варіабельну область легкого ланцюга, де (a) варіабельна область важкого ланцюга включає в себе амінокислотну послідовність, яка щонайменше на 80% гомологічна амінокислотній послідовності, вибраній з групи, яка складається з SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9 і 10; (b) варіабельна область легкого ланцюга включає в себе амінокислотну послідовність, яка щонайменше на 80% гомологічна амінокислотній послідовності, вибраній з групи, яка складається з SEQ ID NO:11, 12, 13, 14, 15, 16, 17, 18, 19 і 20; і -7 (c) зазначене антитіло зв'язується з людським PD-L1 з КD, яка складає 1×10 М або менше. У переважному варіанті винаходу, зазначене антитіло має щонайменше одну з нижченаведених властивостей: (a) зазначене антитіло підсилює проліферацію Т-клітин в аналізі реакцій у змішаній культурі лімфоцитів (РЗКЛ); (b) зазначене антитіло підвищує рівень продукування інтерферону-γ в аналізі РЗКЛ; або (c) зазначене антитіло підвищує рівень секреції IL-2 в аналізі РЗКЛ. У своїх переважних варіантах, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що містять (a) CDR1 варіабельної області важкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30; (b) CDR2 варіабельної області важкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NО:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40; (c) CDR3 варіабельної області важкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50; (d) CDR1 варіабельної області легкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60; (e) CDR2 варіабельної області легкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70; і (f) CDR3 варіабельної області легкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80; де зазначене антитіло специфічно зв'язується з PD-L1. Переважна комбінація послідовностей зазначеного антитіла включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:21; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:31; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:41; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:51; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:61; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:71. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:22; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:32; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:42; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:52; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:62; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:72. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:23; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:33; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:43; 4 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:53; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:63; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:73. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:24; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:34; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:44; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:54; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:64; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:74. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:25; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:35; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:45; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:55; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:65; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:75. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:26; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:36; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:46; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:56; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:66; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:76. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:27; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:37; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:47; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:57; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:67; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:77. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:28; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:38; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:48; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:58; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:68; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:78. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:29; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:39; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:49; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:59; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:69; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:79. Інша переважна комбінація включає в себе (a) CDR1 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:30; (b) CDR2 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:40; (c) CDR3 варіабельної області важкого ланцюга, що містить послідовність SEQ ID NO:50; (d) CDR1 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:60; (e) CDR2 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:70; і (f) CDR3 варіабельної області легкого ланцюга, що містить послідовність SEQ ID NO:80. Інші переважні антитіла відповідно до винаходу або їх антигензв‟язувальні частини містять (a) варіабельну область важкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9 і 10; і (b) варіабельну область легкого ланцюга, яка включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:11, 12, 13, 14, 15, 16, 17, 18, 19 і 20; де зазначене антитіло специфічно зв'язується з PD-L1. Переважна комбінація послідовностей зазначеного антитіла включає в себе 5 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:1; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:11. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:2; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:12. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:3; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:13. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:4; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:14. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:5; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:15. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:6; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:16. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:7; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:17. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:8; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:18. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:9; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:19. Інша переважна комбінація включає в себе (a) варіабельну область важкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:10; і (b) варіабельну область легкого ланцюга, що містить амінокислотну послідовність SEQ ID NO:20. В іншому своєму аспекті, даний винахід належить до антитіл або до їх антигензв‟язувальних частин, які конкурують з кожним з вищевказаних антитіл за зв'язування з PD-L1. Антитіла відповідно до винаходу можуть бути, наприклад, повнорозмірними антитілами, наприклад, антитілами ізотипу IgG1 або IgG4. Альтернативно, зазначені антитіла можуть являти собою фрагменти антитіл, такі як Fab- або F(ab‟)2-фрагменти, або одноланцюгові антитіла. Даний винахід належить також до імунокон‟югата, який включає в себе антитіло відповідно до винаходу або його антигензв‟язувальну частину, приєднані до терапевтичного засобу, такого як цитотоксин або радіоактивний ізотоп. Даний винахід належить також до біспецифічної молекули, яка включає в себе антитіло відповідно до винаходу або його антигензв‟язувальну частину, приєднані до другої функціональної молекули або до її антигензв‟язувальної частини, 6 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 що мають специфічність зв‟язування, яка відрізняється від специфічності зв'язування зазначеного антитіла. Даний винахід належить також до композицій, які включають в себе антитіло або його антигензв‟язувальну частину, або імунокон‟югат або біспецифічну молекулу і фармацевтично прийнятний носій. Крім того, даний винахід охоплює молекули нуклеїнової кислоти, які кодують антитіла або їх антигензв‟язувальні частини, а також експресуючі вектори, які включають в себе такі нуклеїнові кислоти, і клітини-хазяїни, що містять такі експресуючі вектори. Крім того, даний винахід належить до трансгенних мишей, що мають трансгени, які кодують важкий і легкий ланцюги людського імуноглобуліну, де у зазначеної миші експресується антитіло відповідно до винаходу; а також до гібридом, одержаних від такої миші, де зазначена гібридома продукує антитіло відповідно до винаходу. У ще одному своєму аспекті, даний винахід належить до способу модуляції імунної відповіді у індивіда, який включає в себе введення зазначеному індивіду антитіла відповідно до винаходу або його антигензв‟язувальної частини з метою модуляції імунної відповіді у даного індивіда. Переважно, зазначене антитіло підсилює або стимулює зазначену імунну відповідь, або підвищує рівень її продукування у індивіда. В іншому своєму аспекті, даний винахід належить до способу інгібування росту пухлинних клітин у індивіда, який включає в себе введення зазначеному індивіду терапевтично ефективної кількості анти-PD-L1-антитіла відповідно до винаходу або його антигензв‟язувальної частини. Антитілами, переважними для використання в зазначеному способі, є антитіла відповідно до винаходу, хоча замість анти-PD-L1-антитіл відповідно до винаходу (або в комбінації з такими антитілами) можуть бути використані й інші анти-PD-L1-антитіла. Так, наприклад, у способі інгібування росту пухлини може бути використане химерне, гуманізоване або цілком людське анти-PD-L1-антитіло. В іншому своєму аспекті, даний винахід належить до способу лікування інфекційного захворювання у індивіда, який включає в себе введення зазначеному індивіду терапевтично ефективної кількості анти-PD-L1-антитіла або його антигензв‟язувальної частини. Антитілами, переважними для використання в зазначеному способі, є антитіла відповідно до винаходу, хоча замість анти-PD-L1-антитіл відповідно до винаходу (або в комбінації з зазначеними антитілами) можуть бути використані й інші анти-PD-L1-антитіла. Так, наприклад, у способі лікування інфекційного захворювання може бути використане химерне, гуманізоване або цілком людське анти-PD-L1-антитіло. У ще одному своєму аспекті, даний винахід належить до способу посилення імунної відповіді індивіда на антиген, де зазначений спосіб включає в себе введення зазначеному індивіду: (і) антигену; і (ii) анти-PD-L1-антитіла або його антигензв‟язувальної частини, з метою посилення імунної відповіді у зазначеного індивіда на антиген. Таким антигеном може бути, наприклад, пухлинний антиген, вірусний антиген, бактеріальний антиген або антиген, що походить від патогену. Антитілами, переважними для використання в зазначеному способі, є антитіла відповідно до винаходу, хоча замість анти-PD-L1-антитіл відповідно до винаходу (або в комбінації з такими антитілами) можуть бути використані й інші анти-PD-L1-антитіла. Так, наприклад, у способі посилення імунної відповіді індивіда на антиген може бути використане химерне, гуманізоване або цілком людське анти-PD-L1-антитіло. Даний винахід належить також до способу створення анти-PD-L1-антитіл "другої генерації" на основі послідовностей описаних тут анти-PD-L1-антитіл. Так, наприклад, даний винахід належить до способу створення анти-PD-L1-антитіла, який включає в себе (a) одержання антитіла, що має (і) послідовність варіабельної області важкого ланцюга антитіла, яка включає в себе послідовність CDR1, вибрану з групи, яка складається з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30, послідовність CDR2, вибрану з групи, яка складається з SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40; і послідовність CDR3, вибрану з групи, яка складається з SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50; або (ii) послідовність варіабельної області легкого ланцюга антитіла, яка включає в себе послідовність CDR1, вибрану з групи, яка складається з SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60, послідовність CDR2, вибрану з групи, яка складається з SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70, і послідовність CDR3, вибрану з групи, яка складається з SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80; (b) модифікацію щонайменше одного амінокислотного залишку щонайменше в одній послідовності варіабельної області антитіла, де зазначена послідовність вибрана з групи, яка складається з послідовності варіабельної області важкого ланцюга антитіла і послідовності варіабельної області легкого ланцюга антитіла, де зазначену модифікацію вводять з метою створення щонайменше однієї модифікованої послідовності антитіла; і 7 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 (c) експресію зазначеної модифікованої послідовності антитіла у вигляді білка. Інші відмітні ознаки і переваги даного винаходу будуть очевидні з нижченаведеного докладного опису винаходу і прикладів, які не повинні розглядатися як обмеження винаходу. Зміст усіх публікацій, баз даних Genbank, патентів і опублікованих патентних заявок, цитованих у даній заявці, у всій своїй повноті вводиться в даний опис за допомогою посилання. Короткий опис графічного матеріалу На фігурі 1A представлена нуклеотидна послідовність (SEQ ID NO:81) і амінокислотна послідовність (SEQ ID NO:1) варіабельної області важкого ланцюга людського моноклонального антитіла 3G10. Області CDR1 (SEQ ID NO:21), CDR2 (SEQ ID NO:31) і CDR3 (SEQ ID NO:41) підкреслені, а також зазначені V-, D- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 1В представлена нуклеотидна послідовність (SEQ ID NO:91) і амінокислотна послідовність (SEQ ID NO:11) варіабельної області легкого ланцюга людського моноклонального антитіла 3G10. Області CDR1 (SEQ ID NO:51), CDR2 (SEQ ID NO:61) і CDR3 (SEQ ID NO:71) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 2A представлена нуклеотидна послідовність (SEQ ID NO:82) і амінокислотна послідовність (SEQ ID NO:2) варіабельної області важкого ланцюга людського моноклонального антитіла 12A4. Області CDR1 (SEQ ID NO:22), CDR2 (SEQ ID NO:32) і CDR3 (SEQ ID NO:42) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 2В представлена нуклеотидна послідовність (SEQ ID NO:92) і амінокислотна послідовність (SEQ ID NO:12) варіабельної області легкого ланцюга людського моноклонального антитіла 12A4. Області CDR1 (SEQ ID NO:52), CDR2 (SEQ ID NO:62) і CDR3 (SEQ ID NO:72) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 3A представлена нуклеотидна послідовність (SEQ ID NO:83) і амінокислотна послідовність (SEQ ID NO:3) варіабельної області важкого ланцюга людського моноклонального антитіла 10A5. Області CDR1 (SEQ ID NO:23), CDR2 (SEQ ID NO:33) і CDR3 (SEQ ID NO:43) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 3В представлена нуклеотидна послідовність (SEQ ID NO:93) і амінокислотна послідовність (SEQ ID NO:13) варіабельної області легкого ланцюга людського моноклонального антитіла 10A5. Області CDR1 (SEQ ID NO:53), CDR2 (SEQ ID NO:63) і CDR3 (SEQ ID NO:73) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 4A представлена нуклеотидна послідовність (SEQ ID NO:84) і амінокислотна послідовність (SEQ ID NO:4) варіабельної області важкого ланцюга людського моноклонального антитіла 5F8. Області CDR1 (SEQ ID NO:24), CDR2 (SEQ ID NO:34) і CDR3 (SEQ ID NO:44) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 4В представлена нуклеотидна послідовність (SEQ ID NO:94) і амінокислотна послідовність (SEQ ID NO:14) варіабельної області легкого ланцюга людського моноклонального антитіла 5F8. Області CDR1 (SEQ ID NO:54), CDR2 (SEQ ID NO:64) і CDR3 (SEQ ID NO:74) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 5A представлена нуклеотидна послідовність (SEQ ID NO:85) і амінокислотна послідовність (SEQ ID NO:5) варіабельної області важкого ланцюга людського моноклонального антитіла 10H10. Області CDR1 (SEQ ID NO:25), CDR2 (SEQ ID NO:35) і CDR3 (SEQ ID NO:45) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 5В представлена нуклеотидна послідовність (SEQ ID NO:95) і амінокислотна послідовність (SEQ ID NO:15) варіабельної області легкого ланцюга людського моноклонального антитіла 10H10. Області CDR1 (SEQ ID NO:55), CDR2 (SEQ ID NO:65) і CDR3 (SEQ ID NO:75) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 6A представлена нуклеотидна послідовність (SEQ ID NO:86) і амінокислотна послідовність (SEQ ID NO:6) варіабельної області важкого ланцюга людського моноклонального антитіла 1B12. Області CDR1 (SEQ ID NO:26), CDR2 (SEQ ID NO:36) і CDR3 (SEQ ID NO:46) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 6В представлена нуклеотидна послідовність (SEQ ID NO:96) і амінокислотна послідовність (SEQ ID NO:16) варіабельної області легкого ланцюга людського моноклонального антитіла 1B12. Області CDR1 (SEQ ID NO:56), CDR2 (SEQ ID NO:66) і CDR3 (SEQ ID NO:76) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. 8 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 На фігурі 7A представлена нуклеотидна послідовність (SEQ ID NO:87) і амінокислотна послідовність (SEQ ID NO:7) варіабельної області важкого ланцюга людського моноклонального антитіла 7H1. Області CDR1 (SEQ ID NO:27), CDR2 (SEQ ID NO:37) і CDR3 (SEQ ID NO:47) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 7В представлена нуклеотидна послідовність (SEQ ID NO:97) і амінокислотна послідовність (SEQ ID NO:17) варіабельної області легкого ланцюга людського моноклонального антитіла 7H1. Області CDR1 (SEQ ID NO:57), CDR2 (SEQ ID NO:67) і CDR3 (SEQ ID NO:77) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 8A представлена нуклеотидна послідовність (SEQ ID NO:88) і амінокислотна послідовність (SEQ ID NO:8) варіабельної області важкого ланцюга людського моноклонального антитіла 11E6. Області CDR1 (SEQ ID NO:28), CDR2 (SEQ ID NO:38) і CDR3 (SEQ ID NO:48) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 8В представлена нуклеотидна послідовність (SEQ ID NO:98) і амінокислотна послідовність (SEQ ID NO:18) варіабельної області легкого ланцюга людського моноклонального антитіла 11E6. Області CDR1 (SEQ ID NO:58), CDR2 (SEQ ID NO:68) і CDR3 (SEQ ID NO:78) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 9A представлена нуклеотидна послідовність (SEQ ID NO:89) і амінокислотна послідовність (SEQ ID NO:9) варіабельної області важкого ланцюга людського моноклонального антитіла 12B7. Області CDR1 (SEQ ID NO:29), CDR2 (SEQ ID NO:39) і CDR3 (SEQ ID NO:49) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 9В представлена нуклеотидна послідовність (SEQ ID NO:99) і амінокислотна послідовність (SEQ ID NO:19) варіабельної області легкого ланцюга людського моноклонального антитіла 12B7. Області CDR1 (SEQ ID NO:59), CDR2 (SEQ ID NO:69) і CDR3 (SEQ ID NO:79) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 10A представлена нуклеотидна послідовність (SEQ ID NO:90) і амінокислотна послідовність (SEQ ID NO:10) варіабельної області важкого ланцюга людського моноклонального антитіла 13G4. Області CDR1 (SEQ ID NO:30), CDR2 (SEQ ID NO:40) і CDR3 (SEQ ID NO:50) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 10В представлена нуклеотидна послідовність (SEQ ID NO:100) і амінокислотна послідовність (SEQ ID NO:20) варіабельної області легкого ланцюга людського моноклонального антитіла 13G4. Області CDR1 (SEQ ID NO:60), CDR2 (SEQ ID NO:70) і CDR3 (SEQ ID NO:80) підкреслені, а також зазначені V- і J-сегменти похідних послідовностей зародкової лінії. На фігурі 11 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 3G10 (SEQ ID NO:1) з амінокислотною послідовністю VН 1-18 (SEQ ID NO:101) людської зародкової лінії. На фігурі 12 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 12A4 (SEQ ID NO:2) з амінокислотною послідовністю V Н 1-69 (SEQ ID NO:102) людської зародкової лінії. Послідовність зародкової лінії JH6b розкрита в SEQ ID NO:110. На фігурі 13 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 10A5 (SEQ ID NO:3) з амінокислотною послідовністю VН 1-3 (SEQ ID NO:103) людської зародкової лінії. Послідовність зародкової лінії JH4b розкрита в SEQ ID NO:111. На фігурі 14 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 5F8 (SEQ ID NO:4) з амінокислотною послідовністю VН 1-69 (SEQ ID NO:102) людської зародкової лінії. Послідовність зародкової лінії JH4b розкрита в SEQ ID NO:111. На фігурі 15 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 10H10 (SEQ ID NO:5) з амінокислотною послідовністю V Н 3-9 (SEQ ID NO:104) людської зародкової лінії. Послідовність зародкової лінії JH4b розкрита в SEQ ID NO:111. На фігурі 16 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 1B12 (SEQ ID NO:6) з амінокислотною послідовністю VН 1-69 (SEQ ID NO:102) людської зародкової лінії. Послідовність зародкової лінії JH6b розкрита в SEQ ID NO:110. На фігурі 17 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 7H1 (SEQ ID NO:7) з амінокислотною послідовністю VН 1-69 (SEQ ID NO:102) людської зародкової лінії. Послідовність зародкової лінії JH6b розкрита в SEQ ID NO:110. На фігурі 18 9 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 11E6 (SEQ ID NO:8) з амінокислотною послідовністю V Н 1-69 (SEQ ID NO:102) людської зародкової лінії. Послідовність зародкової лінії JH6c розкрита в SEQ ID NO:112. На фігурі 19 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 12B7 (SEQ ID NO:9) з амінокислотною послідовністю VН 1-69 (SEQ ID NO:102) людської зародкової лінії. Послідовність зародкової лінії JH6b розкрита в SEQ ID NO:110. На фігурі 20 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області важкого ланцюга антитіла 13G4 (SEQ ID NO:10) з амінокислотною послідовністю VН 3-9 (SEQ ID NO:104) людської зародкової лінії. Послідовність зародкової лінії JH4b розкрита в SEQ ID NO:113. На фігурі 21 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 3G10 (SEQ ID NO:11) з амінокислотною послідовністю VK L6 (SEQ ID NO:105) людської зародкової лінії. Послідовність зародкової лінії JK1 розкрита в SEQ ID NO:114. На фігурі 22 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 12A4 (SEQ ID NO:12) з амінокислотною послідовністю VK L6 (SEQ ID NO:105) людської зародкової лінії. Послідовність зародкової лінії JK1 розкрита в SEQ ID NO:115. На фігурі 23 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 10A5 (SEQ ID NO:13) з амінокислотною послідовністю V K L15 (SEQ ID NO:106) людської зародкової лінії. Послідовність зародкової лінії JK2 розкрита в SEQ ID NO:116. На фігурі 24 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 5F8 (SEQ ID NO:14) з амінокислотною послідовністю VK А27 (SEQ ID NO:107) людської зародкової лінії. Послідовність зародкової лінії JK1 розкрита в SEQ ID NO:114. На фігурі 25 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 10H10 (SEQ ID NO:15) з амінокислотною послідовністю VK L15 (SEQ ID NO:106) людської зародкової лінії. Послідовність зародкової лінії JK2 розкрита в SEQ ID NO:116. На фігурі 26 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 1B12 (SEQ ID NO:16) з амінокислотною послідовністю VK L6 (SEQ ID NO:105) людської зародкової лінії. Послідовність зародкової лінії JK1 розкрита в SEQ ID NO:115. На фігурі 27 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 7H1 (SEQ ID NO:17) з амінокислотною послідовністю VK L6 (SEQ ID NO:105) людської зародкової лінії. Послідовність зародкової лінії JK1 розкрита в SEQ ID NO:115. На фігурі 28 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 11E6 (SEQ ID NO:18) з амінокислотною послідовністю VK A27 (SEQ ID NO:107) людської зародкової лінії. Послідовність зародкової лінії JK4 розкрита в SEQ ID NO:117. На фігурі 29 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 11E6a (SEQ ID NO:109) з амінокислотною послідовністю V K A27 (SEQ ID NO:107) людської зародкової лінії. Послідовність зародкової лінії JK4 розкрита в SEQ ID NO:118. На фігурі 30 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 12B7 (SEQ ID NO:19) з амінокислотною послідовністю VK L6 (SEQ ID NO:105) людської зародкової лінії. Послідовність зародкової лінії JK5 розкрита в SEQ ID NO:119. На фігурі 31 проілюстроване зіставлення шляхом вирівнювання амінокислотної послідовності варіабельної області легкого ланцюга антитіла 13G4 (SEQ ID NO:20) з амінокислотною послідовністю VK L18 (SEQ ID NO:108) людської зародкової лінії. Послідовність зародкової лінії JK3 розкрита в SEQ ID NO:120. На фігурах 32A-C представлені результати експериментів, які проведені за допомогою протокової цитометрії і продемонстрували, що людські моноклональні антитіла 3G10, 10A5 і 12A4, спрямовані проти людського PD-L1, зв'язуються з клітинною поверхнею клітин СНО, трансфекованих повнорозмірним людським PD-L1. (A) Графік, побудований за даними протокового цитометричного аналізу для 3G10, (B) для 10A5 і (C) для 12A4. На фігурі 33 представлені результати експериментів, які проведені за допомогою протокової цитометрії і продемонстрували, що людські моноклональні антитіла 3G10, 10A5 і 12A4, спрямовані проти людського PD-L1, зв'язуються з клітинною поверхнею клітин СНО, трансфекованих повнорозмірним людським PD-L1, залежно від концентрації. На фігурі 34 представлені результати експериментів, які проведені за допомогою ELISA і продемонстрували, що людські моноклональні антитіла 3G10, 10A5 і 12A4, спрямовані проти людського PD-L1, зв'язуються з гібридним білком PD-L1-Fc. 10 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 На фігурі 35 представлені результати експериментів, які ілюструють титрування HuMab на + стимульованих людських CD4 -Т-клітинах. На фігурі 36 представлені результати експериментів, які ілюструють титрування HuMab на стимульованих МКПК собакоподібних мавп. На фігурах 37A-C представлені результати експериментів, які проведені за допомогою протокової цитометрії і продемонстрували, що людські моноклональні антитіла 3G10, 10A5 і 12A4, спрямовані проти людського PD-L1, зв'язуються з PD-L1 на клітинній поверхні активованих Т-клітин. (A) Графік, побудований за даними протокового цитометричного аналізу для 3G10, (B) для 10A5 і (C) для 12A4. На фігурі 38 продемонстроване зв'язування HuMab із клітинами ES-2. На фігурах 39A-D представлені результати експериментів, які продемонстрували, що людські моноклональні антитіла проти людського PD-L1 стимулюють проліферацію Т-клітин, секрецію IFN- і секрецію IL-2 в аналізі реакцій у змішаній культурі лімфоцитів. На фігурі 39A представлена гістограма, яка ілюструє проліферацію Т-клітин залежно від концентрації HuMаb 10A5; на фігурі 39B представлена гістограма, яка ілюструє секрецію IFN- залежно від концентрації HuMаb 10A5; на фігурі 39С представлена гістограма, яка ілюструє секрецію IFN-, опосередковувану HuMаb 3G10 і 12A4; на фігурі 39D представлена гістограма, яка ілюструє секрецію IL-2 залежно від концентрації HuMаb 10A5. На фігурі 40 продемонстрований вплив людського анти-PD-L1-антитіла на проліферацію клітин і секрецію IFN- у реакції змішаної культури лімфоцитів (РЗКЛ) з використанням + алогенних дендритних клітин і Т-клітин (ефекторних CD4 -Т-клітин). На фігурах 41A-B представлені результати експериментів, які продемонстрували, що людські моноклональні антитіла проти людського PD-L1 стимулюють проліферацію Т-клітин і секрецію IFN-γ у реакції змішаної культури лімфоцитів (РЗКЛ), що містить регуляторні Т-клітини. На фігурі 41A представлена гістограма, яка ілюструє проліферацію Т-клітин залежно від концентрації HuMаb 10A5; на фігурі 41В представлена гістограма, яка ілюструє секрецію IFN-γ залежно від концентрації HuMаb 10A5. На фігурі 42 продемонстровані результати аналізу на вплив анти-PD-L1-антитіл на проліферацію клітин у реакції змішаної культури лімфоцитів у присутності регуляторних Тклітин. На фігурі 43 продемонстровані результати аналізу на вплив анти-PD-L1-антитіл на продукування цитокінів у реакції змішаної культури лімфоцитів у присутності регуляторних Тклітин. На фігурі 44 продемонстровані результати аналізу на вплив анти-PD-L1-антитіл на секрецію IFN-γ людськими МКПК, стимульованими CMV-лізатом. На фігурі 45 представлені результати експериментів, які проведені за допомогою протокової цитометрії і продемонстрували, що людські моноклональні антитіла проти людського PD-L1 блокують зв'язування PD-L1 із трансфекованими клітинами CHO, що експресують PD-1. На фігурі 46 показано, що анти-PD-L1-антитіла блокують зв'язування PD-1 з IFN-обробленими клітинами ES-2. На фігурі 47 показаний вплив анти-PD-L1-антитіл на ріст пухлини in vivo. Докладний опис винаходу В одному зі своїх аспектів, даний винахід належить до виділених моноклональних антитіл, зокрема до людських моноклональних антитіл, які специфічно зв'язуються з PD-L1. У деяких варіантах винаходу, антитіла відповідно до винаходу мають одну або декілька бажаних функціональних властивостей, таких як висока афінність зв'язування з PD-L1, здатність підсилювати проліферацію Т-клітин, секрецію IFN-γ і/або IL-2 у реакціях змішаної культури лімфоцитів, здатність інгібувати зв'язування PD-L1 з рецептором PD-1, здатність стимулювати гуморальні відповіді і/або здатність блокувати супресорну функцію регуляторних Т-клітин. Додатково чи альтернативно, антитіла відповідно до винаходу походять від конкретних послідовностей важкого і легкого ланцюгів зародкової лінії і/або мають конкретні структурні ознаки, такі як CDR-області, що містять конкретні амінокислотні послідовності. Даний винахід належить, наприклад, до виділених антитіл, до способів одержання таких антитіл, до імунокон‟югатів і до біспецифічних молекул, які містять такі антитіла, а також до фармацевтичних композицій, які містять антитіла, імунокон‟югати або біспецифічні молекули відповідно до винаходу. В іншому своєму аспекті, даний винахід належить до способів інгібування росту пухлинних клітин у індивіда з використанням анти-PD-L1-антитіл. Даний винахід належить також до способів застосування антитіл для модифікації імунної відповіді, а також для лікування захворювань, таких як рак або інфекційне захворювання, або до способів стимуляції 11 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 протективної аутоімунної відповіді або антигенспецифічних імунних відповідей (наприклад, шляхом спільного введення анти-PD-L1-антитіла й антигену, що представляє інтерес). Для кращого розуміння даного винаходу, нижче наводиться визначення деяких термінів. Додаткові визначення наводяться в докладному описі винаходу. Термін "імунна відповідь" означає дію, наприклад, лімфоцитів, антиген-презентуючих клітин, фагоцитарних клітин, гранулоцитів і розчинних макромолекул, продукованих вищеописаними клітинами або клітинами печінки (включаючи антитіла, цитокіни і комплемент), яка приводить до селективного руйнування або деструкції в людському організмі або елімінації з людського організму інвазивних патогенів, клітин або тканин, інфікованих патогенами, ракових клітин або, у випадку аутоімунної відповіді або патологічного запалення, нормальних людських клітин або тканин. Термін "шлях передачі сигналу" означає біохімічний взаємозв'язок між різними молекулами передачі сигналу, які відіграють визначену роль у передачі сигналу від однієї частини клітини в іншу частину клітини. Використовуваний тут термін "рецептор клітинної поверхні" включає в себе, наприклад, молекули і комплекси молекул, здатних приймати сигнал і передавати цей сигнал через плазматичну клітинну мембрану. Прикладом "рецептора клітинної поверхні" відповідно до винаходу є рецептор PD-L1. Використовуваний тут термін "антитіло" означає інтактні антитіла і їх будь-який антигензв‟язувальний фрагмент (тобто "антигензв‟язувальну частину") або їхні окремі ланцюги. Термін "антитіло" означає глікопротеїн, який містить щонайменше два важких ланцюги (H) і два легких ланцюги (L), з'єднаних між собою дисульфідними зв'язками, або їх антигензв‟язувальну частину. Кожен важкий ланцюг складається з варіабельної області важкого ланцюга (скорочено позначуваного тут VН) і константної області важкого ланцюга. Константна область важкого ланцюга складається із трьох доменів, CH1, CH2 і CH3. Кожен легкий ланцюг складається з варіабельної області легкого ланцюга (скорочено позначуваного тут VL) і константної області легкого ланцюга. Константна область легкого ланцюга складається з одного домену C L. VН- і VLобласті можуть бути також підрозділені на гіперваріабельні області, називані комплементарність-визначальними областями (CDR) і чергуються з областями, які є більш консервативними і називаються каркасними областями (FR). Кожна V Н- і VL-область складається з трьох CDR і чотирьох FR, розташованих від амінокінця до карбоксикінця в наступному порядку: FRl, CDR15 FR2, CDR2, FR3, CDR3, FR4. Варіабельні області важкого і легкого ланцюгів містять зв‟язувальний домен, який взаємодіє з антигеном. Константні області антитіл можуть опосередковувати зв'язування імуноглобуліну з тканинами або факторами хазяїна, включаючи різні клітини імунної системи (наприклад, ефекторні клітини) і перший компонент (CIq) класичної системи комплементу. Використовуваний тут термін "антигензв‟язувальна частина" антитіла (або просто "частина антитіла") означає один або кілька фрагментів антитіла, які зберігають здатність специфічно зв'язуватися з антигеном (наприклад, з PD-L1). Було показано, що антигензв‟язувальна функція антитіла може здійснюватися фрагментами повнорозмірного антитіла. Прикладами зв‟язувальних фрагментів, що входять у визначення терміна "антигензв‟язувальна частина" антитіла, є (i) Fab-фрагмент, тобто одновалентний фрагмент, що складається з доменів VL, VН, СL і СН1; (ii) F(ab‟)2-фрагмент, тобто двовалентний фрагмент, що складається з двох Fabфрагментів, зв'язаних у шарнірній області дисульфідним містком; (iii) Fd-фрагмент, що складається з VН- і СН1-доменів; (iv) Fv-фрагмент, що складається з VL- і VН-доменів одного плеча антитіла; (v) dAb-фрагмент (Ward et al, (1989) Nature 341:544-546), що складається з VНдомену; і (vi) ізольована гіперваріабельна область (CDR). Крім того, хоча зазначені два домени Fv-фрагмента, VL і VН, кодуються окремими генами, однак, вони можуть бути приєднані один до одного рекомбінантними методами за допомогою синтетичного лінкера, що дозволяє одержати ці фрагменти у вигляді одного білкового ланцюга, у якому пари V L- і VН-областей утворюють одновалентні молекули (відомі як одноланцюговий Fv (scFv); див., наприклад, Bird et al. (1988) Science 242:423-426; і Huston et al. (1988) Proc. Natl. Acad. Sci. USA 85:5879-5883). Такі одноланцюгові антитіла також входять у визначення терміна "антигензв‟язувальна частина" антитіла. Зазначені фрагменти антитіл одержують стандартними методами, відомими фахівцям, і такі фрагменти скринують на ефективність способом, аналогічним способу скринінгу інтактних антитіл. Використовуваний тут термін "виділене антитіло" означає антитіло, що, по суті, не містить інших антитіл, які мають іншу антигенну специфічність (наприклад, виділене антитіло, що специфічно зв'язується з PD-L1, по суті, не містить антитіл, які специфічно зв'язуються з антигенами, що відрізняються від PD-L1). Однак, виділене антитіло, що специфічно зв'язується з PD-L1, може мати перехресну реактивність з іншими антигенами, такими як молекули PD-L1, 12 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 що походять від інших видів. Крім того, виділене антитіло може, по суті, не містити інші клітинні речовини і/або хімічні речовини. Використовувані тут терміни "моноклональне антитіло" або "композиція моноклональних антитіл" означають препарат молекул антитіла, які мають один і той самий молекулярний склад. Композиція моноклональних антитіл має одну специфічність зв'язування й афінність до конкретного епітопа. Використовуваний тут термін "людське антитіло" означає антитіла, що мають варіабельні області, у яких каркасна і CDR-області походять від послідовностей імуноглобуліну людської зародкової лінії. Крім того, якщо дане антитіло містить константну область, то така константна область також походить від послідовностей імуноглобуліну людської зародкової лінії. Людські антитіла відповідно до винаходу можуть включати амінокислотні залишки, які не кодуються послідовностями імуноглобуліну людської зародкової лінії (наприклад, мутації, внесені за допомогою неспецифічного або сайтспецифічного мутагенезу in vitro, або за допомогою соматичної мутації in vivo). Однак, використовуваний тут термін "людське антитіло" не включає в себе антитіла, у яких у людські каркасні послідовності були введені послідовності CDR, що походять від молекул зародкової лінії ссавців інших видів, таких як миша. Термін "людське моноклональне антитіло" означає антитіла, що мають одну специфічність зв'язування і мають варіабельні області, у яких каркасна область і CDR-області походять від послідовностей імуноглобуліну людської зародкової лінії. В одному з варіантів винаходу, зазначені людські моноклональні антитіла продукуються гібридомами, якими є В-клітини, одержані від трансгенної тварини, яка не є людиною, наприклад, від трансгенної миші, що має геном, який містить людський трансген важкого ланцюга і трансген легкого ланцюга, вбудований у імморталізовану клітину. Використовуваний тут термін "рекомбінантне людське антитіло" включає в себе всі людські антитіла, які були одержані, експресовані, створені або виділені рекомбінантними методами, такі як (a) антитіла, виділені у тварини (наприклад, миші), яка є трансгенною або трансхромосомною по генах людського імуноглобуліну; або гібридоми, одержані від цих тварин (докладно описані нижче), (b) антитіла, виділені з клітин-хазяїнів, трансформованих так, щоб вони експресували людське антитіло, наприклад, із клітин трансфектоми, (c) антитіла, виділені з рекомбінантної комбінаторної бібліотеки людських антитіл, і (d) антитіла, одержані, експресовані, створені або виділені будь-якими іншими методами, які включають в себе сплайсинг послідовностей генів людського імуноглобуліну з іншими послідовностями ДНК. Такі рекомбінантні людські антитіла мають варіабельні області, у яких каркасна область і CDRобласті походять від послідовностей імуноглобулінів людської зародкової лінії. Однак, у деяких варіантах винаходу, такі рекомбінантні людські антитіла можуть бути піддані мутагенезу in vitro (або, у випадку використання тварини, трансгенної по послідовностях людських Ig, соматичного мутагенезу in vivo), а тому, амінокислотні послідовності VН- і VL-областей рекомбінантних антитіл, незважаючи на те, що вони походять від VН- і VL-послідовностей людської зародкової лінії і є родинними таким послідовностям, можуть бути відсутніми у репертуарі антитіл людської зародкової лінії in vivo. Використовуваний тут термін "ізотип" означає клас антитіла (наприклад, IgМ або IgG1), яке кодується генами константної області важкого ланцюга. Використовувані тут терміни "антитіло, що розпізнає антиген" і "антитіло, специфічне до антигену" є синонімами терміна "антитіло, що специфічно зв'язується з антигеном". Термін "похідні людського антитіла" означає будь-яку модифіковану форму людського антитіла, наприклад, кон‟югат антитіла з іншим агентом або антитілом. Термін "гуманізоване антитіло" означає антитіла, у яких послідовності CDR, що походять від зародкової лінії ссавців інших видів, таких як миша, були введені в людські каркасні послідовності. У зазначені людські каркасні послідовності можуть бути внесені додаткові модифікації. Термін "химерне антитіло" означає антитіла, у яких послідовності варіабельної області походять від тварини одного виду, а послідовності константної області походять від тварин інших видів, наприклад, такі антитіла, у яких послідовності варіабельної області походять від мишачого антитіла, а послідовності константної області походять від людського антитіла. Використовуваний тут термін "антитіло, що специфічно зв'язується з людським PD-L1" -7 означає антитіло, що зв'язується з людським PD-L1 з КD, яка складає 1×10 M або менше, більш -8 -8 переважно 5×10 M або менше, ще більш переважно 1×10 M або менше, ще більш переважно -9 -8 -10 5×10 M або менше, а найбільш переважно 1×10 M - 1×10 M або менше. Використовуваний тут термін "Кас" або "Kа" означає швидкість асоціації конкретної взаємодії “антитіло-антиген”, а використовуваний тут термін "Kдис" або "Kd" означає швидкість дисоціації 13 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 конкретної взаємодії "антитіло-антиген”. Використовуваний тут термін "КD" означає константу дисоціації, яку обчислюють виходячи з відношення Кd до Ка (i.e., Kd/Ka) і виражають у вигляді молярної концентрації (M). Величини КD для антитіл можуть бути визначені методами, добре відомими фахівцям. Переважним методом визначення КD антитіла є поверхневий плазмовий ® резонанс, а переважно, метод з використанням біосенсорної системи, такої як система Biacore . Використовуваний тут термін "висока афінність" антитіла IgG означає, що дане антитіло -8 -9 зв'язується з антигеном-мішенню з КD, яка складає 10 M або менше, більш переважно 10 M -10 або менше, а найбільш переважно 10 M або менше. Однак, "висока афінність" зв'язування для антитіл інших ізотипів може варіюватися. Так, наприклад, "висока афінність" зв'язування -7 антитіла ізотипу IgМ означає зв'язування антитіла з КD, яка складає 10 M або менше, більш -8 -9 переважно 10 M або менше, а найбільш переважно 10 M або менше. Використовуваний тут термін "індивід" включає в себе людину або будь-яку тварину, яка не є людиною. Термін "тварина, яка не є людиною" включає в себе всіх хребетних, наприклад, ссавців і нессавців, таких як примати, що не є людиною, вівці, собаки, кішки, коні, корови, кури, амфібії, рептилії і т. п. Різні аспекти даного винаходу більш докладно описані в нижченаведених розділах. Анти-PD-L1-антитіла Антитіла відповідно до винаходу відрізняються за своїми конкретними функціональними ознаками або властивостями. Так, наприклад, зазначені антитіла можуть специфічно зв'язуватися з людським PD-L1. Переважно, антитіло відповідно до винаходу зв'язується з PD-7 L1 з високою афінністю, наприклад, з КD, яка складає 1×10 M або менше. Анти-PD-L1-антитіла відповідно до винаходу мають щонайменше одну або декілька властивостей, вибраних з наступних властивостей: -7 (a) здатність зв'язуватися з людським PD-L1 з КD, яка складає 1×10 М або менше; (b) здатність підвищувати рівень проліферації T-клітин в аналізі реакцій у змішаній культурі лімфоцитів (РЗКЛ); (c) здатність підвищувати рівень продукування інтерферону-γ в аналізі РЗКЛ; (d) здатність підвищувати рівень секреції IL-2 в аналізі РЗКЛ; (e) здатність стимулювати гуморальну відповідь; або (f) здатність блокувати дію регуляторних Т-клітин на ефекторні T-клітини і/або дендритні клітини. -8 Переважно, зазначене антитіло зв'язується з людським PD-L1 з КD, яка складає 5×10 М або -8 -9 менше, з КD, яка складає 1×10 М або менше, з КD, яка складає 5×10 М або менше, з КD, яка -9 -9 -9 складає 4×10 М або менше, з КD, яка складає 2×10 М або менше або із КD, яка складає 1×10 -10 М - 1×10 М або менше. Стандартні аналізи для оцінки здатності антитіл зв'язуватися з PD-L1 відомі фахівцям, включаючи, наприклад, ELISA, вестерн-блот-аналіз і РІА. Придатні аналізи докладно описані в прикладах. Кінетика зв'язування (наприклад, афінність зв'язування) антитіл може бути також ® оцінена за допомогою стандартних аналізів, відомих фахівцям, таких як аналіз Biacore . Моноклональні антитіла 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4. Переважними антитілами відповідно до винаходу є людські моноклональні антитіла 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4, виділені і структурно охарактеризовані як описано в прикладах 1 і 2. Амінокислотні послідовності VН антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO: 1, 2, 3, 4, 5, 6, 7, 8, 9 і 10, відповідно. Амінокислотні послідовності VL антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:11, 12, 13, 14, 15, 16, 17, 18, 19 і 20, відповідно. Беручи до уваги те, що кожне з цих антитіл може зв'язуватися з PD-L1, слід зазначити, що послідовності VН і VL можуть бути "змішані і відповідним чином підібрані" для створення інших PD-L1-зв'язувальних молекул антитіл відповідно до винаходу. Такі "змішані і відповідним чином підібрані" антитіла, що зв'язуються з PD-L1, можуть бути протестовані за допомогою аналізів на зв'язування, описаних вище й у прикладах (наприклад, ELISA). При змішуванні і підборі V Н і VLланцюгів переважно, щоб послідовність VН у конкретній парі VН/VL, була замінена структурно подібною послідовністю VН. Аналогічним чином, переважно, щоб послідовність VL у конкретній парі VН/VL була замінена структурно подібною послідовністю V L. Відповідно до цього, в одному зі своїх аспектів, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:1 , 2, 3, 4, 5, 6, 7, 8, 9 і 10; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:11, 12, 13, 14, 15, 16, 17, 18, 19 і 20; 14 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 де зазначене антитіло специфічно зв'язується з PD-L1, а переважно з людським PD-L1. Переважні комбінації важкого і легкого ланцюгів містять у собі (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:1; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:11; або (а) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:2; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:12; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:3; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:13; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:4; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:14; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:5; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:15; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:6; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:16; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:7; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:17; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:8; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:18; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:9; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:19; або (a) варіабельну область важкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:10; і (b) варіабельну область легкого ланцюга, яка містить амінокислотну послідовність SEQ ID NO:20. В іншому своєму аспекті, даний винахід належить до антитіл, які містять CDR1, CDR2 і CDR3 важкого і легкого ланцюгів антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 або їхньої комбінації. Амінокислотні послідовності CDR1 VН антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30, відповідно. Амінокислотні послідовності CDR2 VН антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40, відповідно. Амінокислотні послідовності CDR3 VН антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50, відповідно. Амінокислотні послідовності CDR1 VK антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60, відповідно. Амінокислотні послідовності CDR2 VK антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70, відповідно. Амінокислотні послідовності CDR3 VK антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 представлені в SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80, відповідно. CDR-області пронумеровані за системою Кебата (Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No 91-3242). Беручи до уваги той факт, що кожне з зазначених антитіл може зв'язуватися з PD-L1, і що специфічність зв'язування з антигеном забезпечується, головним чином, областями CDR1, CDR2 і CDR3, то слід зазначити, що послідовності областей CDR1, CDR2 і CDR3 V Н і послідовності областей CDR1, CDR2 і CDR3 VK можуть бути "змішані і відповідним чином підібрані" (тобто CDR від різних антитіл можуть бути змішані і відповідним чином підібрані, хоча кожне антитіло повинно містити CDR1, CDR2 і CDR3 VН і CDR1, CDR2 і CDR3 VK) з одержанням інших молекул антитіл, що зв'язуються з PD-L1, відповідно до винаходу. Зв'язування таких "змішаних і відповідним чином підібраних" антитіл з PD-L1 може бути протестовано за допомогою аналізів на зв'язування, описаних вище й у прикладах (наприклад, аналізів ELISA і Biacore). При змішуванні і підборі послідовностей CDR VН переважно, щоб послідовності CDR1, CDR2 і/або CDR3 VН у конкретній послідовності VН були замінені структурно подібною(ими) 15 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 послідовністю(ями) CDR. Аналогічним чином, при змішуванні і підборі послідовностей CDR VK переважно, щоб послідовності CDR1, CDR2 і/або CDR3 VK у конкретній послідовності VK були замінені структурно подібною(ими) послідовністю(ями) CDR. Середньому фахівцю в даній галузі очевидно, що нові послідовності VН і VL можуть бути одержані шляхом заміни однієї або декількох послідовностей області CDR VН і/або VL структурно подібними послідовностями, що походять від послідовностей CDR, описаних у даній заявці для моноклональних антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4. Відповідно до цього, в іншому своєму аспекті, даний винахід належить до виділеного моноклонального антитіла або його антигензв‟язувальної частини, що містять (a) CDR1 варіабельної області важкого ланцюга, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80; де зазначене антитіло специфічно зв'язується з PD-L1, а переважно з людським PD-L1. У переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:21; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:31; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:41; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:51; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:61; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:71. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:22; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:32; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:42; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:52; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:62; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:72. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:23; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:33; 16 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність NO:43; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність NO:53; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність NO:63; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність NO:73. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність NO:24; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність NO:34; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність NO:44; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність NO:54; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність NO:64; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність NO:74. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність NO:25; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність NO:35; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність NO:45; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність NO:55; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність NO:65; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність NO:75. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність NO:26; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність NO:36; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність NO:46; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність NO:56; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність NO:66; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність NO:76. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність NO:27; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність NO:37; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність NO:47; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність NO:57; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність NO:67; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність NO:77. 17 SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID SEQ ID UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:28; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:38; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:48; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:58; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:68; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:78. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:29; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:39; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:49; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:59; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:69; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:79. В іншому переважному варіанті винаходу, зазначене антитіло містить: (a) CDR1 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:30; (b) CDR2 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:40; (c) CDR3 варіабельної області важкого ланцюга, що включає в себе послідовність SEQ ID NO:50; (d) CDR1 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:60; (e) CDR2 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:70; і (f) CDR3 варіабельної області легкого ланцюга, що включає в себе послідовність SEQ ID NO:80. Добре відомо, що один домен CDR3, незалежно від домену(ів) CDR1 і/або CDR2, може визначати специфічність зв'язування антитіла з когнатним антигеном, і що, як передбачається, на основі відомої послідовності CDR3 може бути генерована множина антитіл, які мають одну і ту саму специфічність зв'язування. Див., наприклад, публікацію Klimka et al., British J. of Cancer 83(2):252-260 (2000) (де описане продукування гуманізованого анти-CD30-антитіла з використанням тільки CDR3 варіабельного домену важкого ланцюга мишачого анти-CD30антитіла Ki-4); публікацію Beiboer et al., J. Mol. Biol. 296:833-849 (2000) (де описане продукування рекомбінантних антитіл проти епітеліального глікопротеїну-2 (EGP-2) з використанням тільки послідовності CDR3 важкого ланцюга батьківського мишачого анти-EGP2-антитіла MOC-31); публікацію Rader et al., Proc. Natl. Acad. Sci U.S.A. 95:8910-8915 (1998) (де описане продукування панелі гуманізованих антитіл проти інтегрину 3 з використанням CDR3 варіабельного домену важкого і легкого ланцюгів мишачого антитіла проти інтегрину 3 LM609, де кожне з зазначених антитіл містить відмінну послідовність, яка знаходиться за межами домену CDR3 і здатна зв'язуватися з тим же епітопом, з яким зв'язується батьківське мишаче антитіло, і з такою ж афінністю, як і батьківське мишаче антитіло, або з більш високою афінністю); публікацію Barbas et al., J. Am. Chem. Soc. 116:2161-2162 (1994) (де описано, що домен CDR3 відіграє головну роль у зв'язуванні з антигеном); публікацію Barbas et al., Proc. Natl. Acad. Sci. U.S.A. 92:2529-2533 (1995) (де описане вбудовування послідовностей CDR3 важкого ланцюга трьох Fab-фрагментів антитіла (SI-I, SI-40 і SI-32) проти ДНК людської плаценти у важкий ланцюг Fab-фрагмента проти правцевого токсоїду, де зазначене введення приводить до заміни CDR3, присутнього у важкому ланцюзі, і вказує на те, що специфічність зв'язування 18 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 визначається лише одним доменом CDR3); і публікацію Ditzel et al., J. Immunol. 157:739-749 (1996) (де описані дослідження з вбудовування, які показали, що перенесення тільки одного домену CDR3 важкого ланцюга Fab батьківського поліспецифічного антитіла LNA3 у важкий ланцюг Fab моноспецифічного антитіла IgG p313 проти правцевого токсоїду був достатнім для збереження специфічності зв'язування батьківського Fab). Кожна з цих публікацій у всій своїй повноті вводиться в даний опис за допомогою посилання. Відповідно до цього, у деяких своїх аспектах, даний винахід належить до моноклональних антитіл, які містять один або декілька доменів CDR3 важкого і/або легкого ланцюгів, що походять від нелюдського антитіла, такого як мишаче або щуряче антитіло, де зазначене моноклональне антитіло має здатність специфічно зв'язуватися з PD-L1. У деяких варіантах винаходу, такі антитіла відповідно до винаходу, які містять один або декілька доменів CDR3 важкого і/або легкого ланцюгів, що походять від нелюдського антитіла, (a) мають здатність конкурувати за зв'язування з відповідним батьківським нелюдським антитілом; (b) зберігають функціональні властивості зазначеного батьківського антитіла; (c) зв'язуються з таким же епітопом; і/або (d) мають таку ж афінність зв'язування, як і відповідне батьківське нелюдське антитіло. В інших своїх аспектах, даний винахід належить до моноклональних антитіл, які містять один або декілька доменів CDR3 важкого і/або легкого ланцюгів, що походять від першого людського антитіла, такого як, наприклад, людське антитіло, виділене у тварини, яка не є людиною, де зазначене перше людське антитіло має здатність специфічно зв'язуватися з PDL1, і де зазначений домен CDR3 першого людського антитіла замінює домен CDR3 у людському антитілі, що не має здатності специфічно зв'язуватися з PD-L1, у результаті чого утворюється друге людське антитіло, яке має здатність специфічно зв'язуватися з PD-L1. У деяких варіантах винаходу, антитіла відповідно до винаходу, які містять один або декілька доменів CDR3 важкого і/або легкого ланцюгів, що походять від першого людського антитіла, (a) мають здатність конкурувати за зв'язування з відповідним батьківським першим людським антитілом; (b) зберігають функціональні властивості зазначеного батьківського антитіла; (c) зв'язуються з таким же епітопом; і/або (d) мають таку ж афінність зв'язування, як і відповідне батьківське перше людське антитіло. Антитіла, які мають конкретні послідовності зародкової лінії У деяких варіантах винаходу, антитіло відповідно до винаходу містить варіабельну область важкого ланцюга, яка походить від конкретного гена імуноглобуліну важкого ланцюга зародкової лінії, і/або варіабельну область легкого ланцюга, яка походить від конкретного гена імуноглобуліну легкого ланцюга зародкової лінії. Так, наприклад, у своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що містять варіабельну область важкого ланцюга, яка є продуктом людського гена VH 1-18 або похідним цього генного продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область важкого ланцюга, яка є продуктом людського гена VH 1-69 або похідним цього генного продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область важкого ланцюга, яка є продуктом людського гена V H 1-3 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область важкого ланцюга, яка є продуктом людського гена V H 3-9 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область легкого ланцюга, яка є продуктом людського гена VK L6 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область легкого ланцюга, яка є продуктом людського гена VK L15 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому своєму переважному варіанті, даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область легкого ланцюга, яка є продуктом людського гена V K A27 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. В іншому 19 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 своєму переважному варіанті, даний винахід належить також до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що включають в себе варіабельну область легкого ланцюга, яка є продуктом людського гена VK L18 або походить від цього продукту, де зазначене антитіло специфічно зв'язується з PD-L1. У ще одному своєму переважному варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, де зазначене антитіло: (а) містить варіабельну область важкого ланцюга, яка є продуктом або походить від продукту людського гена VН 1-18, 1-69, 1-3 або 3-9 (які кодують амінокислотні послідовності, представлені в SEQ ID NO:101, 102, 103 і 104, відповідно); (b) містить варіабельну область легкого ланцюга, яка є продуктом або походить від продукту людського гена VK L6, L15, A27 або L18 (які кодують амінокислотні послідовності, представлені в SEQ ID NO:105, 106, 107 і 108, відповідно); і (c) специфічно зв'язується з PD-L1, а переважно з людським PD-L1. Прикладом антитіла, що має VН і VK, кодованих генами VH 1-18 і VK L6, відповідно, є 3G10. Прикладами антитіл, що мають VН і VK, кодованих генами VH 1-18 і VK L6, відповідно, є 12A4, 1B12, 7H1 і 12B7. Прикладом антитіла, що має VН і VK, кодованих генами VH 1-3 і VK L15, відповідно, є 10A5. Прикладами антитіл, що мають VН і VK, кодованих генами VH 1-69 і VK А27, відповідно, є 5F8, 11E6 і 11E6a. Прикладом антитіла, що має VН і VK, кодованих генами VH 3-9 і VK L15, відповідно, є 10H10. Прикладом антитіла, що має VН і VK, кодованих генами VH 1-3 і VK L15, відповідно, є 10A5. Прикладом антитіла, що має VН і VK, кодованих генами VH 3-9 і VK L18, відповідно, є 13G4. Використовуване тут людське антитіло містить варіабельні області важкого або легкого ланцюгів, які є "продуктом" або "походять від" конкретної послідовності зародкової лінії, якщо варіабельні області зазначеного антитіла були одержані із системи, у якій використовуються гени імуноглобуліну людської зародкової лінії. Такі системи включають імунізацію трансгенної миші, яка несе гени людського імуноглобуліну, антигеном, що представляє інтерес, або скринінг бібліотеки генів людського імуноглобуліну, представлених на фазі, з використанням антигену, що представляє інтерес. Людське антитіло, яке є "продуктом" послідовності або "походить від" послідовності імуноглобуліну людської зародкової лінії, може бути ідентифіковане шляхом порівняння амінокислотної послідовності людського антитіла з амінокислотними послідовностями імуноглобулінової людської зародкової лінії і добору послідовності імуноглобуліну людської зародкової лінії, що є найбільш подібною (тобто має найбільший % ідентичності) з послідовністю людського антитіла. Людське антитіло, яке є "продуктом" конкретної послідовності імуноглобуліну людської зародкової лінії або "походить від" такої послідовності, може містити амінокислоти, які відрізняються від амінокислот порівнюваної послідовності зародкової лінії, що обумовлено, наприклад, природними соматичними мутаціями або штучним уведенням сайтспрямованої мутації. Однак, амінокислотна послідовність вибраного людського антитіла, звичайно щонайменше на 90% ідентична амінокислотній послідовності, кодованій геном імуноглобуліну людської зародкової лінії, і містить амінокислотні залишки, що дозволяють ідентифікувати дане антитіло як людське антитіло при його порівнянні з амінокислотними послідовностями імуноглобуліну зародкової лінії інших видів (наприклад, з послідовностями мишачої зародкової лінії). У деяких випадках, амінокислотна послідовність людського антитіла може бути щонайменше на 95% або навіть щонайменше на 96%, 97%, 98% або 99% ідентичною амінокислотній послідовності, кодованій геном імуноглобуліну зародкової лінії. У деяких варіантах винаходу, людське антитіло, що походить від конкретної послідовності людської зародкової лінії, має не більше ніж 10 амінокислот, які відрізняються від амінокислот послідовності, кодованої геном імуноглобуліну людської зародкової лінії. У деяких інших варіантах винаходу, зазначене людське антитіло може мати не більше ніж 5 або навіть не більше ніж 4, 3, 2 або 1 амінокислоту, які відрізняються від амінокислот послідовності, кодованої геном імуноглобуліну людської зародкової лінії. Гомологічні антитіла В іншому варіанті здійснення винаходу, антитіло відповідно до винаходу містить варіабельні області важкого і легкого ланцюгів, які включають в себе амінокислотні послідовності, гомологічні амінокислотним послідовностям описаних тут переважних антитіл, де зазначені антитіла зберігають потрібні функціональні властивості анти-PD-L1-антитіл відповідно до винаходу. Так, наприклад, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що містять варіабельну область важкого ланцюга і варіабельну область легкого ланцюга, де 20 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 (a) зазначена варіабельна область важкого ланцюга містить амінокислотну послідовність, яка щонайменше на 80% гомологічна амінокислотній послідовності, вибраній з групи, яка складається з SEQ ID NO:1, 2, 3, 4, 5, 6, 7, 8, 9 і 10; (b) зазначена варіабельна область легкого ланцюга містить амінокислотну послідовність, яка щонайменше на 80% гомологічна амінокислотній послідовності, вибраній з групи, яка складається з SEQ ID NO:11, 12, 13, 14, 15, 16, 17, 18, 19 і 20; -7 (c) зазначене антитіло зв'язується з людським PD-L1 з КD, яка складає 1×10 M або менше; (d) зазначене антитіло підвищує рівень проліферації Т-клітин в аналізі реакцій у змішаній культурі лімфоцитів (РЗКЛ); (e) зазначене антитіло підвищує рівень продукування інтерферону-γ в аналізі РЗКЛ; (f) зазначене антитіло підвищує рівень секреції IL-2 в аналізі РЗКЛ; (g) зазначене антитіло стимулює виробляння гуморальних відповідей; і (h) зазначене антитіло блокує дію регуляторних Т-клітин на ефекторні Т-клітини і/або на дендритні клітини. В інших варіантах винаходу, амінокислотні послідовності VН і/або VL можуть бути на 85%, 90%, 95%, 96%, 97%, 98% або 99% гомологічні вищевказаним послідовностям. Антитіло, що має області VН і VL, які є у високому ступені (тобто на 80% або більше) гомологічними областям VН і VL вищевказаних послідовностей, можуть бути одержані шляхом мутагенезу (наприклад, сайтспрямованого або ПЦР-опосередкованого мутагенезу) молекул нуклеїнової кислоти, що кодують послідовності SEQ ID NO:25, 26, 27, 28, 29 і 30, з наступним тестуванням кодованого модифікованого антитіла на збереження його функцій (тобто функцій, зазначених вище в пунктах (c)-(h)) за допомогою описаних тут функціональних аналізів. Використовуваний тут термін "відсоток гомології двох амінокислотних послідовностей" еквівалентний терміну "відсоток ідентичності двох послідовностей". Відсоток ідентичності двох послідовностей залежить від числа положень ідентичних амінокислот у цих двох послідовностей (тобто % гомології = # ідентичних амінокислот у даних положеннях/загальне число положень х 100) з урахуванням числа пробілів і довжини кожного пробілу, які необхідно ввести для оптимального зіставлення двох послідовностей шляхом вирівнювання. Порівняння послідовностей і визначення відсотка ідентичності двох послідовностей може бути здійснене за допомогою математичного алгоритму, описаного нижче в необмежуючих прикладах. Відсоток ідентичності двох амінокислотних послідовностей може бути визначений за допомогою алгоритму E. Meyers і W. Miller (Comput. Appl. Biosci., 4:11-17 (1988)), що був введений у програму ALIGN (version 2.0), з використанням таблиці "ваг" залишків PAM120, штрафу на пробіл-подовження = 12, і штрафу на пробіл-пропуск = 4. Крім того, відсоток ідентичності двох амінокислотних послідовностей може бути визначений за допомогою алгоритму Needleman і Wunsch (J. Mo. Biol. 48:444-453 (1970)), що був введений у програму GAP, яка входить у пакет програм GCG (доступних на сайті www.gcg.com), з використанням або матриці Blossum 62, або матриці PAM250 і "ваг" пробілів-пропусків, що складають 16, 14, 12, 10, 8, 6, або 4, і "ваг" довжин (ділянок), що складають 1, 2, 3, 4, 5 або 6. У деяких випадках, послідовності білка відповідно до винаходу можуть бути також використані як "запитувана послідовність" з метою пошуку в загальнодоступних базах даних, наприклад, для ідентифікації родинних послідовностей. Такий пошук може бути проведений за допомогою програми XBLAST (version 2.0) Altschul, et al. (1990) J. Mo. Biol. 215:403-10. Пошук білків BLAST може бути здійснений за допомогою програми XBLAST, де при "ваговому коефіцієнті" = 50 і довжині "слова" = 3, можуть бути одержані амінокислотні послідовності, гомологічні послідовностям молекул антитіл відповідно до винаходу. Для здійснення вирівнювання з пробілами з метою зіставлення послідовностей може бути використана програма Gapped BLAST, описана Altschul et al., (1997) Nucleic Acids Res. 25(17):3389-3402. При роботі з програмами BLAST і Gapped BLAST можуть бути використані параметри за замовчуванням, встановлені у відповідних програмах (наприклад, XBLAST і NBLAST). Див. www.ncbi.nlm.nih.gov. Антитіла з консервативними модифікаціями У деяких варіантах винаходу, антитіло відповідно до винаходу містить варіабельну область важкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, і варіабельну область легкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, де одна або кілька зазначених послідовностей CDR мають конкретні амінокислотні послідовності, одержані на основі послідовностей описаних тут переважних антитіл (наприклад, 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4), або їхні консервативні модифікації, і де зазначені антитіла зберігають потрібні функціональні властивості анти-PD-L1-антитіл відповідно до винаходу. Відповідно до цього, даний винахід належить до виділеного моноклонального 21 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 антитіла або до його антигензв‟язувальної частини, що містять варіабельну область важкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, і варіабельну область легкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, де (a) послідовність CDR3 варіабельної області важкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з амінокислотних послідовностей SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50 і їхніх консервативних модифікацій; (b) послідовність CDR3 варіабельної області легкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з амінокислотних послідовностей SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80 і їхніх консервативних модифікацій; -7 (c) зазначене антитіло зв'язується з людським PD-L1 з КD, яка складає 1×10 M або менше; (d) зазначене антитіло підвищує рівень проліферації Т-клітин в аналізі реакцій у змішаній культурі лімфоцитів (РЗКЛ); (e) зазначене антитіло підвищує рівень продукування інтерферону-γ в аналізі РЗКЛ; (f) зазначене антитіло підвищує рівень секреції IL-2 в аналізі РЗКЛ; (g) зазначене антитіло стимулює виробляння гуморальних відповідей; і (h) зазначене антитіло блокує дію регуляторних Т-клітин на ефекторні Т-клітини і/або дендритні клітини. У переважному варіанті винаходу, зазначена послідовність CDR2 варіабельної області важкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з амінокислотних послідовностей SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40 і їхніх консервативних модифікацій; а послідовність CDR2 варіабельної області легкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з амінокислотних послідовностей SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70 і їхніх консервативних модифікацій. В іншому переважному варіанті винаходу, зазначена послідовність CDR1 варіабельної області важкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з амінокислотних послідовностей SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30 і їхніх консервативних модифікацій; а послідовність CDR1 варіабельної області легкого ланцюга включає в себе амінокислотну послідовність, вибрану з групи, яка складається з амінокислотних послідовностей SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60 і їхніх консервативних модифікацій. Використовуваний тут термін "консервативні модифікації послідовності" означає амінокислотні модифікації, які не здійснюють значного впливу або впливу на зв‟язувальні властивості антитіла, що містить амінокислотну послідовність. Такими консервативними модифікаціями є амінокислотні заміни, додавання і делеції. Модифікації можуть бути введені в антитіло відповідно до винаходу стандартними методами, відомими фахівцям, такими як сайтспрямований мутагенез і ПЦР-опосередковуваний мутагенез. Консервативними амінокислотними замінами є заміни, у яких даний амінокислотний залишок замінений амінокислотним залишком, який має аналогічний бічний ланцюг. Сімейства амінокислотних залишків, які мають аналогічні бічні ланцюги, відомі фахівцям. Такі сімейства включають амінокислоти з основними бічними ланцюгами (наприклад, лізин, аргінін, гістидин), амінокислоти з кислотними бічними ланцюгами (наприклад, аспарагінова кислота, глутамінова кислота); амінокислоти з незарядженими полярними бічними ланцюгами (наприклад, гліцин, аспарагін, глутамін, серин, треонін, тирозин, цистеїн, триптофан); амінокислоти з неполярними бічними ланцюгами (наприклад, аланін, валін, лейцин, ізолейцин, пролін, фенілаланін, метіонін); амінокислоти з бета-розгалуженими бічними ланцюгами (наприклад, треонін, валін, ізолейцин) і амінокислоти з ароматичними бічними ланцюгами (наприклад, тирозин, фенілаланін, триптофан, гістидин). Таким чином, один або кілька амінокислотних залишків в областях CDR антитіла відповідно до винаходу можуть бути замінені іншими амінокислотними залишками, які належать до сімейства амінокислотних залишків, що мають аналогічні бічні ланцюги, і таке модифіковане антитіло може бути протестоване на збереження його функцій (тобто функцій, зазначених вище в пунктах (c)-(h)) за допомогою описаних тут функціональних аналізів. Антитіла, які зв'язуються з таким же епітопом, як і анти-PD-L1-антитіла відповідно до винаходу В іншому своєму варіанті, даний винахід належить до антитіл, які зв'язуються з таким же епітопом на людському PD-L1, як і анти-PD-L1-антитіла відповідно до винаходу (тобто антитіла, які мають здатність конкурувати з кожним з моноклональних антитіл відповідно до винаходу за перехресне зв'язування з PD-L1). У переважних варіантах винаходу, еталонним антитілом, використовуваним у дослідженнях на конкуренцію за перехресне зв'язування, може бути моноклональне антитіло 3G10 (що має послідовності VН і VL, представлені в SEQ ID NO:1 і 11, відповідно), або моноклональне антитіло 12A4 (що має послідовності V Н і VL, представлені в 22 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 SEQ ID NO:2 і 12, відповідно), або моноклональне антитіло 10A5 (що має послідовності V Н і VL, представлені в SEQ ID NO:3 і 13, відповідно), або моноклональне антитіло 5F8 (що має послідовності VН і VL, представлені в SEQ ID NO:4 і 14, відповідно), або моноклональне антитіло 10H10 (що має послідовності VН і VL, представлені в SEQ IDNO:5 і 15, відповідно), або моноклональне антитіло 1B12 (що має послідовності VН і VL, представлені в SEQ ID NO:6 і 16, відповідно), або моноклональне антитіло 7H1 (що має послідовності V Н і VL, представлені в SEQ ID NO:7 і 17, відповідно), або моноклональне антитіло 11E6 (що має послідовності V Н і VL, представлені в SEQ ID NO:8 і 18, відповідно), або моноклональне антитіло 12B7 (що має послідовності VН і VL, представлені у SEQ ID NO:9 і 19, відповідно), або моноклональне антитіло 13G4 (що має послідовності VН і VL, представлені в SEQ ID NO:10 і 20, відповідно). Такі конкуруючі за перехресне зв'язування антитіла можуть бути ідентифіковані по їх здатності конкурувати за перехресне зв'язування з 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4 у стандартних аналізах на зв'язування з PD-L1. Так, наприклад, аналіз BIAcore, аналіз ELISA або протоковий цитометричний аналіз можуть бути використані для ілюстрації конкуренції за перехресне зв'язування з антитілами відповідно до винаходу. Здатність тестованого антитіла інгібувати зв'язування, наприклад, 3G10 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4 з людським PD-L1 продемонструвала, що тестоване антитіло може конкурувати з антитілами 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4 за зв'язування з людським PD-L1, а, тому воно зв'язується з тим же епітопом на людському PD-L1, з яким зв'язуються антитіла 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4. У переважному варіанті винаходу, антитіло, що зв'язується з тим же епітопом на людському PDL1, з яким зв'язуються антитіла 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4, являє собою людське моноклональне антитіло. Такі людські моноклональні антитіла можуть бути одержані і виділені як описано в прикладах. Сконструйовані і модифіковані антитіла Антитіло відповідно до винаходу може бути також одержане з використанням антитіла, яке має одну або декілька описаних тут послідовностей VН і/або VL як вихідний матеріал для конструювання модифікованого антитіла, де зазначене модифіковане антитіло може мати властивості, що відрізняються від властивостей вихідного антитіла. Антитіло може бути сконструйоване шляхом модифікації одного або декількох залишків в одній або обох варіабельних областях (тобто VН і/або VL), наприклад, в одній або декількох областях CDR і/або в одній або декількох каркасних областях. Додатково чи альтернативно, антитіло може бути сконструйоване шляхом модифікації залишків у константній(их) області(ях), наприклад, з метою зміни ефекторної(их) функції(й) зазначеного антитіла. Одним із придатних методів конструювання варіабельних областей є приєднання CDR. Антитіла взаємодіють з антигеном-мішенню переважно за допомогою амінокислотних залишків, які локалізовані в шести гіперваріабельних областях (CDR) важкого і легкого ланцюгів. З цієї причини, амінокислотні послідовності CDR в окремих антитілах мають більші відмінності, ніж послідовності, розташовані за межами цих CDR. Оскільки послідовності CDR є відповідальними за більшість взаємодій антитіло-антиген, то можуть бути експресовані рекомбінантні антитіла, які імітують властивості конкретних природних антитіл, шляхом конструювання експресуючих векторів, що включають в себе послідовності CDR, які походять від специфічних природних антитіл, приєднаних до каркасних послідовностей іншого антитіла з іншими властивостями (див., наприклад, Riechmann, L. et al. (1998) Nature 332:323-327; Jones, P. et al. (1986) Nature 321:522-525; Queen, C. et al. (1989) Proc. Natl. Acad. See. U.S.A. 86:10029-10033; Патент США 5225539, Winter і патенти США № 5530101, 5585089, 5693762 і 6180370, Queen et al.). Відповідно до цього, в іншому своєму варіанті, даний винахід належить до виділеного моноклонального антитіла або до його антигензв‟язувальної частини, що містять варіабельну область важкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, що мають амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30, SEQ ID NО: 31, 32, 33, 34, 35, 36, 37, 38, 39 і 40 і SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50, відповідно, і варіабельну область легкого ланцюга, яка включає в себе послідовності CDR1, CDR2 і CDR3, що мають амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NО: 51, 52, 53, 54, 55, 56, 57, 58, 59 і 60, SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70 і SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80, відповідно. Таким чином, зазначені антитіла містять послідовності CDR VН і VL моноклональних антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 або 13G4, а також вони можуть містити різні каркасні послідовності цих антитіл. Такі каркасні послідовності можуть бути одержані з загальнодоступних баз даних ДНК або відомих послідовностей, які включають послідовності генів антитіл зародкової лінії. Так, 23 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, послідовності ДНК зародкової лінії, які включають в себе гени варіабельної області людського важкого і легкого ланцюгів, можна знайти в базі даних послідовностей людської зародкової лінії "VBase" (доступної в Інтернеті на сайті www.mrc-cpe.cam.ac.uk/vbase), а також у публікаціях Kabat, E. A., et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health і Human Services, NIH Publication No 91-3242; Tomlinson, I. M., et al. (1992) "The Repertoire of Human Germline VH Sequences Reveals about Fifty Groups of VH Segments with Different Hypervariable Loops" J. MoI. Biol. 227:776-798; і Cox, J. P. L. et al. (1994) "A Directory of Human Germline VH Segments Reveals a Strong Bias in their Usage" Eur. J. Immunol. 24:827-836; зміст яких у всій своїй повноті вводиться в даний опис за допомогою посилання. Білкові послідовності антитіла порівнювали з послідовностями білків, які є в компільованій базі даних, із застосуванням методів пошуку подібності послідовностей, називаних Gapped BLAST (Altschul et al. (1997) Nucleic Acids Research 25:3389-3402), що добре відомі фахівцям. BLAST являє собою евристичний алгоритм, у якому при статистично значимому зіставленні шляхом вирівнювання послідовності антитіла з послідовністю бази даних, вирівнювані "слова", імовірно, містять пари сегментів з високими "ваговими коефіцієнтами" (HSP). Пари сегментів, "вагові коефіцієнти" які не можуть бути поліпшені шляхом подовження або усічення, називаються "найкращими збігами". Коротко, нуклеотидні послідовності на початку послідовності VBASE (vbase.mrc-cpe.cam.ac.uk/vbasel/list2.php) були трансльовані, а область між каркасними областями FR1-FR3, включно, зберігалася. Послідовності бази даних мають середню довжину в 98 залишків. Дублікати послідовностей, що мають точні відповідності всій довжині білка, були вилучені. Пошук білків у BLAST, проведений з використанням blastp зі стандартними параметрами за замовчуванням, за винятком "фільтра" для послідовностей низької складності, що був "відключений", і матриці замін BLOSUM62, виявив 5 найкращих збігів з одержанням пар подібних послідовностей. Ці нуклеотидні послідовності транслювали у всіх шести рамках зчитування, і рамка зчитування без стоп-кодонів у сегменті відповідної послідовності бази даних розглядалася як послідовність, що має, цілком ймовірно, найкращий збіг. Це, у свою чергу, було підтверджено за допомогою програми tblastx, що входить у пакет BLAST. Ця програма дозволяє транслювати послідовності антитіла у всіх шести рамках зчитування і порівнювати ці трансльовані послідовності з нуклеотидними послідовностями VBASE, динамічно трансльованими у всіх шести рамках зчитування. Ідентичність являє собою точні відповідності між послідовністю антитіла і послідовністю білка в базі даних протягом усієї довжини даної послідовності. Позитивні "ваги" (ідентичність + відповідність замін) означають лише ідентичності амінокислотних замін, що надаються матрицею замін BLOSUM62. Якщо послідовність антитіла відповідає двом послідовностям у базі даних з тим же ступенем ідентичності, то збіг з найбільшою позитивною "вагою" повинен розглядатися як найкращий збіг послідовностей. Переважними каркасними послідовностями, що можуть бути використані в антитілах відповідно до винаходу, є послідовності, які мають структурну подібність з каркасними послідовностями, використовуваними у вибраних антитілах відповідно до винаходу, наприклад, має подібність з каркасними послідовностями VН 1-18 (SEQ ID NO:101) і/або каркасними послідовностями VН 1-69 (SEQ ID NO:102), і/або каркасними послідовностями VН 1-3 (SEQ ID NO:103), і/або каркасними послідовностями VН 3-9 (SEQ ID NO:104), і/або каркасними послідовностями VK L6 (SEQ ID NO:105), і/або каркасними послідовностями VK L15 (SEQ ID NO:106), і/або каркасними послідовностями VK А27 (SEQ ID NO:107), і/або каркасними послідовностями VK L18 (SEQ ID NO:107), використовуваним у переважних моноклональних антитілах відповідно до винаходу. Послідовності CDR1, CDR2 і CDR3 V Н і послідовності CDR1, CDR2 і CDR3 VK можуть бути приєднані до каркасних областей, ідентичних послідовностям, виявленим у гені імуноглобуліну зародкової лінії, від якого походить дана каркасна послідовність, або послідовності CDR можуть бути приєднані до каркасних областей, що містять одну або кілька мутацій у порівнянні з послідовностями зародкової лінії. Так, наприклад, було виявлено, що в деяких випадках може виявитися переважним введення мутацій у положення залишків у каркасних областях з метою збереження або посилення антигензв‟язувальної здатності антитіла (див., наприклад, патенти США 5530101; 5585089; 5693762 і 6180370, Queen et al.). Модифікація варіабельної області іншого типу являє собою мутацію амінокислотних залишків в областях CDR1, CDR2 і/або CDR3 VН і/або VK, яку вводять з метою поліпшення однієї або декількох зв‟язувальних властивостей (наприклад, афінності) антитіла інтерес, що представляє. Сайтспрямований мутагенез або ПЦР-опосередкований мутагенез може бути проведений для введення мутації(й), і їхній вплив на зв'язування антитіла або інша функціональна властивість, що представляє інтерес, може бути оцінене в in vitro або in vivo 24 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 аналізах, описаних вище й у прикладах. Переважними є консервативні модифікації (обговорювані вище). Такими мутаціями можуть бути амінокислотні заміни, додавання або делеції, однак, переважними є заміни. Крім того, звичайно в область CDR вводять не більше ніж одну, дві, три, чотири або п'ять модифікацій залишків. Відповідно до цього, в іншому своєму варіанті, даний винахід належить до виділених моноклональних антитіл проти PD-L1 або до їх антигензв‟язувальних частин, що включають в себе варіабельну область важкого ланцюга, яка містить (a) область CDR1 VН, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30, або амінокислотну послідовність, що має одну, дві, три, чотири або п'ять амінокислотних замін, делецій або додавань у порівнянні з SEQ ID NO:21, 22, 23, 24, 25, 26, 27, 28, 29 і 30; (b) область CDR2 VН, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40, або амінокислотну послідовність, що має одну, дві, три, чотири або п'ять амінокислотних замін, делецій або додавань у порівнянні з SEQ ID NO:31, 32, 33, 34, 35, 36, 37, 38, 39 і 40; (c) область CDR3 V Н, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50, або амінокислотну послідовність, що має одну, дві, три, чотири або п'ять амінокислотних замін, делецій або додавань у порівнянні з SEQ ID NO:41, 42, 43, 44, 45, 46, 47, 48, 49 і 50; (d) область CDR1 VK, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60, або амінокислотну послідовність, що має одну, дві, три, чотири або п'ять амінокислотних замін, делецій або додавань у порівнянні з SEQ ID NO:51, 52, 53, 54, 55, 56, 57, 58, 59 і 60; (e) область CDR2 VK, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70, або амінокислотну послідовність, що має одну, дві, три, чотири або п'ять амінокислотних замін, делецій або додавань у порівнянні з SEQ ID NO:61, 62, 63, 64, 65, 66, 67, 68, 69 і 70; і (f) область CDR3 V K, що включає в себе амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO: 71, 72, 73, 74, 75, 76, 77, 78, 79 і 80, або амінокислотну послідовність, що має одну, дві, три, чотири або п'ять амінокислотних замін, делецій або додавань у порівнянні з SEQ ID NO:71, 72, 73, 74, 75, 76, 77, 78, 79 і 80. Сконструйованими антитілами відповідно до винаходу є антитіла, у яких в V Н і/або в VK були зроблені модифікації каркасних залишків з метою поліпшення властивостей даного антитіла. Звичайно, такі модифікації в каркасних областях вводять з метою зниження імуногенності антитіла. Так, наприклад, одним з методів є введення "зворотної мутації" одного або декількох каркасних залишків у відповідну послідовність зародкової лінії. Більш конкретно, антитіло, що було піддано соматичній мутації, може містити каркасні залишки, які відрізняються від залишків послідовності зародкової лінії, від якої походить дане антитіло. Такі залишки можуть бути ідентифіковані шляхом порівняння каркасних послідовностей антитіла з послідовностями зародкової лінії, від яких походить дане антитіло. Так, наприклад, як описано нижче, у каркасні області анти-PD-L1-антитіл 3G10, 12A4, 10A5, 5F8, 10H10, 1B12, 7H1, 11E6, 12B7 і 13G4 був введений ряд амінокислотних замін, а тому послідовності цих областей відрізняються від послідовностей батьківської зародкової лінії. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, соматичні мутації можуть бути піддані "зворотній мутації" з одержанням послідовності зародкової лінії, наприклад, за допомогою сайтспрямованого мутагенезу або ПЦР-опосередковуваного мутагенезу. Зіставлення шляхом вирівнювання послідовності VН-області антитіла 3G10 з послідовністю V Н 1-18 батьківської зародкової лінії представлено на фігурі 11. Зіставлення шляхом вирівнювання послідовності V Нобласті антитіла 12A4 з послідовністю VН 1-69 батьківської зародкової лінії представлено на фігурі 12. Зіставлення шляхом вирівнювання послідовності VН-області антитіла 10A5 з послідовністю VН 1-3 батьківської зародкової лінії представлено на фігурі 13. Зіставлення шляхом вирівнювання послідовності VН-області антитіла 5F8 з послідовністю VН 1-69 батьківської зародкової лінії представлено на фігурі 14. Зіставлення шляхом вирівнювання послідовності VН-області антитіла 10Н10 з послідовністю VН3-9 батьківської зародкової лінії представлено на фігурі 15. Зіставлення шляхом вирівнювання послідовності V Н-області антитіла 1В12 з послідовністю VН 1-69 батьківської зародкової лінії представлено на фігурі 16. Зіставлення шляхом вирівнювання послідовності V Н-області антитіла 7Н1 з послідовністю VН 169 батьківської зародкової лінії представлено на фігурі 17. Зіставлення шляхом вирівнювання послідовності VН-області антитіла 11Е6 з послідовністю VН 1-69 батьківської зародкової лінії представлено на фігурі 18. Зіставлення шляхом вирівнювання послідовності VН-області антитіла 12В7 з послідовністю VН 1-69 батьківської зародкової лінії представлено на фігурі 19. 25 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 Зіставлення шляхом вирівнювання послідовності VН-області антитіла 13G4 з послідовністю VН 3-9 батьківської зародкової лінії представлено на фігурі 20. Так, наприклад, у 3G10, амінокислотним залишком #79 (у FR3) V Н є валін, а відповідним залишком у послідовності VН 1-18 зародкової лінії є аланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, соматичні мутації можуть бути піддані "зворотній мутації" з одержанням послідовності зародкової лінії, наприклад, за допомогою сайтспрямованого мутагенезу або ПЦР-опосередковуваного мутагенезу (наприклад, залишок #79 (залишок #13 у FR3) у VН антитіла 3G10 може бути підданий "зворотній мутації" шляхом заміни валіну на аланін). В іншому прикладі, для 12A4, амінокислотним залишком #24 (у FR1) V Н є треонін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є аланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #24 у VН антитіла 12A4 може бути підданий "зворотній мутації" шляхом заміни треоніну на аланін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 12A4, амінокислотним залишком #27 (у FR1) V Н є аспарагінова кислота, а відповідним залишком у послідовності VН 1-69 зародкової лінії є гліцин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #27 у VН антитіла 12A4 може бути підданий "зворотній мутації" шляхом заміни аспарагінової кислоти на гліцин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 12A4, амінокислотним залишком #95 (у FR3) V Н є фенілаланін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є тирозин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #95 (залишок #29 у FR3) у VН антитіла 12A4 може бути підданий "зворотній мутації" шляхом заміни фенілаланіну на тирозин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 5F8, амінокислотним залишком #24 (у FR1) є валін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є аланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #24 у VН антитіла 5F8 може бути підданий "зворотній мутації" шляхом заміни валіну на аланін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 5F8, амінокислотним залишком #28 (у FR1) є ізолейцин, а відповідним залишком у послідовності VН 1-69 зародкової лінії є треонін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #28 у VН антитіла 5F8 може бути підданий "зворотній мутації" шляхом заміни ізолейцину на треонін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 10H10, амінокислотним залишком #24 (у FR1) є валін, а відповідним залишком у послідовності VН3-9 зародкової лінії є аланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #24 у VН антитіла 10H10 може бути підданий "зворотній мутації" шляхом заміни валіну на аланін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 10H10, амінокислота може бути введена за амінокислотним залишком #97 (у FR3). Такою амінокислотою є валін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, амінокислота, уведена за залишком #97 у VН антитіла 10H10, може бути піддана "зворотній мутації" з видаленням валіну. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 1В12, амінокислотним залишком #24 (у FR1) є треонін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є аланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #24 у VН антитіла 1В12 може бути підданий "зворотній мутації" шляхом заміни треоніну на аланін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 1В12, амінокислотним залишком #27 (у FR1) є аспарагінова кислота, а відповідним залишком у послідовності VН 1-69 зародкової лінії є гліцин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #27 у VН антитіла 1В12 може бути підданий "зворотній мутації" шляхом заміни аспарагінової кислоти на гліцин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. 26 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому прикладі, для 1В12, амінокислотним залишком #95 (у FR3) є фенілаланін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є тирозин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #95 (залишок #29 у FR3) у VН антитіла 1В12 може бути підданий "зворотній мутації" шляхом заміни фенілаланіну на тирозин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 7Н1, амінокислотним залишком #24 (у FR1) є треонін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є аланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #24 у VН антитіла 7Н1 може бути підданий "зворотній мутації" шляхом заміни треоніну на аланін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 7Н1, амінокислотним залишком #77 (у FR3) є треонін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є серин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #72 (залишок #11 у FR3) у VН антитіла 7Н1 може бути підданий "зворотній мутації" шляхом заміни треоніну на серин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 11Е6, амінокислотним залишком #78 (у FR3) є аланін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є треонін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #78 (залишок #12 у FR3) у VН антитіла 11Е6 може бути підданий "зворотній мутації" шляхом заміни аланіну на треонін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 12В7, амінокислотним залишком #13 (у FR1) є глутамінова кислота, а відповідним залишком у послідовності VН 1-69 зародкової лінії є лізин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #13 у VН антитіла 12В7 може бути підданий "зворотній мутації" шляхом заміни глутамінової кислоти на лізин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 12В7, амінокислотним залишком #30 (у FR1) є аспарагін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є серин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #30 у VН антитіла 12В7 може бути підданий "зворотній мутації" шляхом заміни аспарагіну на серин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 12В7, амінокислотним залишком #77 (у FR3) є аспарагін, а відповідним залишком у послідовності VН 1-69 зародкової лінії є серин. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #377 (залишок #11 у FR3) у VН антитіла 12В7 може бути підданий "зворотній мутації" шляхом заміни аспарагіну на серин. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 12В7, амінокислотним залишком #82 (у FR3) є аспарагінова кислота, а відповідним залишком у послідовності VН 1-69 зародкової лінії є глутамінова кислота. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #82 (залишок #16у FR3) у V Н антитіла 12В7 може бути підданий "зворотній мутації" шляхом заміни аспарагінової кислоти на глутамінову кислоту. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. В іншому прикладі, для 13G4, амінокислотним залишком #27 (у FR1) є ізолейцин, а відповідним залишком у послідовності VН 1-69 зародкової лінії є фенілаланін. Для повернення послідовностям каркасної області конфігурацій, які вони мали у вихідній зародковій лінії, наприклад, залишок #27 у VН антитіла 13G4 може бути підданий "зворотній мутації" шляхом заміни ізолейцину на фенілаланін. Такі антитіла зі "зворотними мутаціями" також входять в об‟єм даного винаходу. Модифікація каркасної області іншого типу включає в себе мутацію одного або декількох залишків у каркасній або області навіть в одній або декількох областях CDR, що вводиться з метою видалення Т-клітинних епітопів для зниження потенційної імуногенності антитіла. Цей метод також називається "деімунізацією" і докладно описаний у публікації заявки на патент США № 2003/0153043, Carr et al. Крім модифікацій або як альтернатива модифікаціям, що вводяться в каркасні області або в області CDR, антитіла відповідно до винаходу можуть бути сконструйовані так, щоб вони мали 27 UA 99701 C2 5 10 15 20 25 30 35 40 45 50 55 60 модифікації в Fc-області, які звичайно приводять до зміни однієї або декількох функціональних властивостей даного антитіла, таких як час напівжиття в сироватці, фіксація комплементу, зв'язування з Fc-рецептором і/або антигензалежна клітинна цитотоксичність. Крім того, антитіло відповідно до винаходу може бути хімічно модифіковане (наприклад, до такого антитіла можуть бути приєднані одна або кілька хімічних груп) або воно може бути модифіковане для зміни рівнів його глікозилування, що також здійснюють з метою зміни однієї або декількох функціональних властивостей антитіла. Кожний з цих варіантів винаходу більш докладно описаний нижче. Залишки в Fc-області пронумеровані відповідно до Європейської нумерації за Кебатом. В одному з варіантів винаходу, шарнірну область CH1 модифікують зі зміною числа цистеїнових залишків у цій області, наприклад, для їхнього збільшення або зниження. Цей метод докладно описаний у патенті США № 5677425, Bodmer et al. Число цистеїнових залишків у шарнірній області CH1 змінюють, наприклад, для полегшення збирання легкого і важкого ланцюгів або для підвищення або зниження стабільності антитіла. В іншому варіанті винаходу, шарнірну область Fc антитіла піддають мутації для зменшення біологічного часу напівжиття даного антитіла. Більш конкретно, одну або кілька амінокислотних мутацій вводять в область стику доменів CH2-CH3 шарнірні Fc-фрагмента, для того, щоб дане антитіло мало порушену здатність зв'язуватися зі стафілококовим білком А (SpА) у порівнянні зі здатністю до зв'язування нативної шарнірної області Fc-фрагмента з SpА. Цей метод докладно описаний у патенті США № 6165745, Ward et al. В іншому варіанті винаходу, зазначене антитіло модифікують з метою збільшення його біологічного часу напівжиття. Для цього можуть бути застосовані різні методи. Так, наприклад, можуть бути введені одна або декілька з нижченаведених мутацій: T252L, T254S, T256F, як описано в патенті США № 6277375, Ward. Альтернативно, для збільшення біологічного часу напівжиття, зазначене антитіло може бути модифіковане в області CH1 або CL, так, щоб воно містило епітоп зв'язування з рецептором "порятунку", що походить від двох "петель" домену CH2 у Fc-області IgG, як описано в патентах США № 5869046 і 6121022, Presta et al. В інших варіантах винаходу, Fc-область модифікують шляхом заміни щонайменше одного амінокислотного залишку іншим амінокислотним залишком з метою зміни ефекторної(их) функції(й) антитіла. Так, наприклад, одна або кілька амінокислот, вибраних з амінокислотних залишків 234, 235, 236, 237, 297, 318, 320 і 322, можуть бути замінені іншим амінокислотним залишком так, щоб дана заміна приводила до зміни афінності даного антитіла стосовно ефекторного ліганду, але зі збереженням антигензв‟язувальної здатності батьківського антитіла. Ефекторним лігандом, стосовно якого може бути змінена афінність антитіла, може бути, наприклад, Fc-рецептор або компонент Cl комплементу. Цей метод докладно описаний у патентах США № 5624821 і 5648260, Winter et al. В іншому прикладі, одна або кілька амінокислот, вибраних з амінокислотних залишків 329, 331 і 322, можуть бути замінені іншими амінокислотними залишками так, щоб дана заміна приводила до зміни здатності даного антитіла зв'язуватися з CIq і/або до зниження або усунення комплементзалежної цитотоксичності (CDC). Цей метод докладно описаний у патенті США № 6194551, Idusogie et al. В іншому прикладі, один або кілька амінокислотних залишків у положеннях амінокислот 231 і 239 модифікують з метою зміни здатності антитіла до фіксації комплементу. Цей метод докладно описаний у публікації заявки PCT WO 94/29351, Bodmer et al. У ще одному прикладі, Fc-область модифікують з метою підвищення здатності антитіла опосередковувати антитілозалежну клітинну цитотоксичність (ADCC) і/або з метою підвищення афінності даного антитіла до Fc-рецептора шляхом модифікації однієї або декількох амінокислот у наступних положеннях: 238, 239, 248, 249, 252, 254, 255, 256, 258, 265, 267, 268, 269, 270, 272, 276, 278, 280, 283, 285, 286, 289, 290, 292, 293, 294, 295, 296, 298, 301, 303, 305, 307, 309, 312, 315, 320, 322, 324, 326, 327, 329, 330, 331, 333, 334, 335, 337, 338, 340, 360, 373, 376, 378, 382, 388, 389, 398, 414, 416, 419, 430, 434, 435, 437, 438 або 439. Цей метод докладно описаний у публікації заявки PCT WO 00/42072, Presta. Крім того, сайти зв'язування на людських IgG1 для FcRI, FcRII, FcRIII і FcRn були картовані, і були описані варіанти з поліпшеною здатністю до зв'язування (див. Shields, R.L. et al. (2001) J. Biol. Chem. 276:65916604). Було показано, що специфічні мутації в положеннях 256, 290, 298, 333, 334 і 339 приводять до підвищення рівня зв'язування з FcRIII. Крім того, було показано, що нижченаведені комбінації мутацій: T256A/S298A, S298A/E333A, S298A/K224A і S298A/E333A/K334A приводять до підвищення рівня зв'язування з FcRIII. У ще одному варіанті винаходу розглядаються зміни рівня глікозилування антитіла. Так, наприклад, може бути одержане неглікозиловане антитіло (тобто антитіло, що не містить 28
ДивитисяДодаткова інформація
Назва патенту англійськоюHuman monoclonal antibody that specifically binds to programmed death ligand 1 (pd-l1)
Автори англійськоюKorman, Alan, J., Selby, Mark, J., Wang, Changyu, Srinivasan, Mohan, Passmore, David, B., Huang, Haichun, Chen, Haibin
Назва патенту російськоюЧеловеческое моноклональное антитело, которое специфически связывается с лигандом-1 запрограммированной гибели клеток (pd-l1)
Автори російськоюКорман Алан Дж., Селби Марк Дж., Ванг Чангиу, Сринивасан Мохан, Пассмор Дэвид Б., Хуан Хайчунь, Чень Хайбинь
МПК / Мітки
МПК: C12N 15/13, A61K 39/395, C12N 5/20, A61P 35/00, C07K 16/28
Мітки: клітин, pd-l1, специфічно, антитіло, моноклональне, запрограмованої, загибелі, людське, зв'язується, яке, лігандом-1
Код посилання
<a href="https://ua.patents.su/146-99701-lyudske-monoklonalne-antitilo-yake-specifichno-zvyazuehtsya-z-ligandom-1-zaprogramovano-zagibeli-klitin-pd-l1.html" target="_blank" rel="follow" title="База патентів України">Людське моноклональне антитіло, яке специфічно зв’язується з лігандом-1 запрограмованої загибелі клітин (pd-l1)</a>
Попередній патент: Спосіб приготування імморталізованої людської клітинної лінії
Наступний патент: Спосіб одержання езетимібу й проміжних продуктів, використовуваних у цьому способі
Випадковий патент: Застосування монокристалів купрум йодиду-пентатіосилікату cu7sis5i як матеріалу мембрани іоноселективного електрода для визначення купруму в кислих розчинах