Фармацевтична композиція, що містить естер темозоломіду
Формула / Реферат
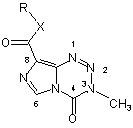
1. Сполука 3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат загальної формули (І):
 , І
, І
де X являє собою О або S;
R являє собою заміщений або незаміщений С3~С10 алкіл з нерозгалуженим або розгалуженим ланцюгом, С3~С10 циклоалкіл, С3~С10 алкеніл з нерозгалуженим або розгалуженим ланцюгом або С3~С10 алкініл з нерозгалуженим або розгалуженим ланцюгом;
та R може мати замісник(и), де вказаний замісник(и) може являти собою С1~С6 алкіл, С1~С6 алкокси, С1~С6 алкілтіогрупу, С1~С6 алкіламіногрупу, феніл або феніл, заміщений галогеном.
2. Сполука за п. 1, де вказана сполука вибрана з групи, що складається з:
метил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
етил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
пропіл-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
бутил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
1-метилбутил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
1-етилбутил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
1-етилпропіл-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
1-етиламіл-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
1-метилгексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-3-карбоксилату,
2-метилгексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
3-метилгексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
4-мeтилгeкcил-3,4-дигiдpo-3-мeтил-4-oкcoiмiдaзo[5,l-d]-l,2,3,5-тeтpaзин-8-карбоксилату,
5-метилгексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
1-метилгептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
2-мeтилгeптил-3,4-дигiдpo-3-мeтил-4-oкcoiмiдaзo[5,1-d]-1,2,3,5-тeтpaзин-8-карбоксилату,
З-метилгептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
4-метилгептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
5-метилгептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
6-метилгептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
aмiл-3,4-дигiдpo-3-мeтил-4-oкcoiмiдaзo[5,l-d]-l,2,3,5-тeтpaзин-8-карбоксилату,
н-гексил-3,4-дигiдpo-3-мeтил-4-oкcoiмiдaзo[5,l-d]-l,2,3,5-тeтpaзин-8-карбоксилату,
ізогексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
циклогексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату,
гептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату та
октил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату.
3. Сполука за п. 2, де вказана сполука являє собою н-гексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат.
4. Фармацевтична композиція, що має протипухлинну активність, яка відрізняється тим, що містить терапевтично ефективну кількість однієї чи більше із сполук за будь-яким з пп. 1-3 як активний інгредієнт, разом з традиційними фармацевтично прийнятними носіями.
5. Фармацевтична композиція за п. 4, яка відрізняється тим, що вказана композиція може містити один або більше фармацевтично прийнятних компонентів кислотної природи.
6. Фармацевтична композиція за п. 5, яка відрізняється тим, що вказаний компонент кислотної природи вибраний з групи, що складається з олеїнової кислоти, стеаринової кислоти, лінолевої кислоти, фумарової кислоти, бензойної кислоти, винної кислоти, сорбінової кислоти, молочної кислоти, лимонної кислоти, оцтової кислоти та ЕДТА.
7. Фармацевтична композиція за будь-яким з пп. 4-6, яка відрізняється тим, що вказана композиція додатково може містити один або більше фармацевтично прийнятних С3~С8 третинних спиртів або вторинних спиртів, або їх естерних або ефірних похідних.
8. Фармацевтична композиція за будь-яким з пп. 4-7, яка відрізняється тим, що вказаний активний інгредієнт вводять пацієнтам в дозі 0,1~200 мг/кг маси тіла/добу.
9. Фармацевтична композиція за п. 8, яка відрізняється тим, що вказаний інтервал доз активного інгредієнта становить 1~20 мг/кг маси тіла/добу.
10. Фармацевтична композиція за п. 4, яка відрізняється тим, що вказана композиція може бути виготовлена в будь-якій з фармацевтично прийнятних лікарських форм.
11. Фармацевтична композиція за п. 10, яка відрізняється тим, що вказана композиція може бути виготовлена в трансдермальній лікарській формі для місцевого застосування або в лікарській формі для перорального застосування.
12. Фармацевтична композиція за п. 11, яка відрізняється тим, що вказана трансдермальна лікарська форма для місцевого застосування являє собою трансдермальний пластир для місцевого застосування.
13. Фармацевтична композиція за п. 12, яка відрізняється тим, що вказаний трансдермальний пластир являє собою пластир з контрольованим вивільненням матричного типу, пластир з контрольованим вивільненням по типу резервуара твердої речовини або пластир з контрольованим вивільненням по типу резервуара рідкої речовини.
14. Фармацевтична композиція за п. 13, яка відрізняється тим, що вказаний трансдермальний пластир являє собою пластир з контрольованим вивільненням по типу резервуара твердої речовини, в якому водна фаза являє собою воду та масляна фаза являє собою одну або більше субстанцій, вибраних з групи, що складається з олеїнової кислоти, ізопропілміристату, лауринової кислоти, воску, цетилового спирту, стеарилового спирту, рідкого парафіну, вазеліну, безводного ланоліну, стеаринової кислоти, бавовняної олії, рицинової олії та ліноленової кислоти.
15. Фармацевтична композиція за п. 14, яка відрізняється тим, що вказана масляна фаза являє собою олеїнову кислоту або ізопропілміристат.
16. Фармацевтична композиція за п. 13, яка відрізняється тим, що вказаний трансдермальний пластир являє собою пластир з контрольованим вивільненням по типу резервуара, що містить непроникну матрицю, рідкий лікарський засіб, мембрану, що сповільнює швидкість вивільнення, PSAs та шар вивільнення, де:
непроникна матриця являє собою одну або більше субстанцій, вибраних з групи, що складається з поліетилену, полівінілхлориду, нітрогліцерину, полідиметилсилоксану, полівінілпіролідону, полівінілового спирту, комплексу поліетеноксиду, поліетиленгліколю, монометилового ефіру поліетиленгліколю або диметилового ефіру поліетиленгліколю, поліетиленгліколю сукцинату та вітаміну Е ТПГС, бавовни та вовни;
вказана мембрана, що сповільнює швидкість вивільнення, вибрана з групи, що складається з мембрани із співполімеру етилену та вінілацетату, мембрани з поліуретану або мембрани з глікольдіацетату; та
вказаний PSAs вибраний з групи, що складається з чутливої до тиску полісилоксанової смоли або чутливої до тиску поліакрилатної смоли.
17. Фармацевтична композиція за п. 16, яка відрізняється тим, що вказана матриця являє собою поліетилен або полівінілхлорид.
18. Фармацевтична композиція за п. 13, яка відрізняється тим, що вказаний трансдермальний пластир для місцевого застосування являє собою пластир з контрольованим вивільненням матричного типу, де допоміжна клейка матриця лікарського засобу вибрана з групи, що складається з полівінілхлориду, поліакрилату, полідиметилсилоксану, полівінілпіролідону, полівінілового спирту, водного гелю, що виготовлений з гелю, полівінілпіролідону, комплексу полівінілпіролідону та поліетиленоксиду, монометилового ефіру поліетиленгліколю або диметилового ефіру поліетиленгліколю, поліетиленгліколю сукцинату та BE ТПГС.
19. Фармацевтична композиція за п. 18, яка відрізняється тим, що допоміжна липка матриця лікарського засобу являє собою поліакрилат.
20. Фармацевтична композиція за п. 10, яка відрізняється тим, що вказана лікарська форма являє собою таблетку, пігулку, диспергований порошок, капсулу, гранулу, емульсію, розчин, суспензію, сироп, твердий супозиторій для вагінального або ректального введення.
21. Спосіб одержання композиції за пп. 14 або 15, який відрізняється тим, що в ньому здійснюють наступні стадії:
зважування відповідної кількості сполуки за п. 1 як активного інгредієнта та подрібнення до стану тонкого порошку, ретельне перемішування водної фази, масляної фази, поверхнево-активної речовини та необхідних носіїв з подальшим змішуванням з подрібненим порошком лікарського засобу, одержану суміш змішують та мелють з одержанням мікроемульсії; додавання до суміші відповідної кількості мембрани, що сповільнює швидкість вивільнення, та чутливої до тиску клейкої субстанції з ретельним перемішуванням; дегазація шляхом збереження тепла з використанням водяної бані та розподіл на поліетиленовій матриці; сушіння та розрізання на маленькі шматочки з одержанням вказаного пластира з контрольованим вивільненням по типу резервуара твердої речовини.
Текст
1. Сполука 3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат загальної формули (І): R 2 (19) 1 3 циклогексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилату, гептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилату та октил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилату. 3. Сполука за п. 2, де вказана сполука являє собою н-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат. 4. Фармацевтична композиція, що має протипухлинну активність, яка відрізняється тим, що містить терапевтично ефективну кількість однієї чи більше із сполук за будь-яким з пп. 1-3 як активний інгредієнт, разом з традиційними фармацевтично прийнятними носіями. 5. Фармацевтична композиція за п. 4, яка відрізняється тим, що вказана композиція може містити один або більше фармацевтично прийнятних компонентів кислотної природи. 6. Фармацевтична композиція за п. 5, яка відрізняється тим, що вказаний компонент кислотної природи вибраний з групи, що складається з олеїнової кислоти, стеаринової кислоти, лінолевої кислоти, фумарової кислоти, бензойної кислоти, винної кислоти, сорбінової кислоти, молочної кислоти, лимонної кислоти, оцтової кислоти та ЕДТА. 7. Фармацевтична композиція за будь-яким з пп. 46, яка відрізняється тим, що вказана композиція додатково може містити один або більше фармацевтично прийнятних С3~С8 третинних спиртів або вторинних спиртів, або їх естерних або ефірних похідних. 8. Фармацевтична композиція за будь-яким з пп. 47, яка відрізняється тим, що вказаний активний інгредієнт вводять пацієнтам в дозі 0,1~200 мг/кг маси тіла/добу. 9. Фармацевтична композиція за п. 8, яка відрізняється тим, що вказаний інтервал доз активного інгредієнта становить 1~20 мг/кг маси тіла/добу. 10. Фармацевтична композиція за п. 4, яка відрізняється тим, що вказана композиція може бути виготовлена в будь-якій з фармацевтично прийнятних лікарських форм. 11. Фармацевтична композиція за п. 10, яка відрізняється тим, що вказана композиція може бути виготовлена в трансдермальній лікарській формі для місцевого застосування або в лікарській формі для перорального застосування. 12. Фармацевтична композиція за п. 11, яка відрізняється тим, що вказана трансдермальна лікарська форма для місцевого застосування являє собою трансдермальний пластир для місцевого застосування. 13. Фармацевтична композиція за п. 12, яка відрізняється тим, що вказаний трансдермальний пластир являє собою пластир з контрольованим вивільненням матричного типу, пластир з контрольованим вивільненням по типу резервуара твердої речовини або пластир з контрольованим вивільненням по типу резервуара рідкої речовини. 14. Фармацевтична композиція за п. 13, яка відрізняється тим, що вказаний трансдермальний пластир являє собою пластир з контрольованим вивільненням по типу резервуара твердої речовини, в якому водна фаза являє собою воду та мас 89795 4 ляна фаза являє собою одну або більше субстанцій, вибраних з групи, що складається з олеїнової кислоти, ізопропілміристату, лауринової кислоти, воску, цетилового спирту, стеарилового спирту, рідкого парафіну, вазеліну, безводного ланоліну, стеаринової кислоти, бавовняної олії, рицинової олії та ліноленової кислоти. 15. Фармацевтична композиція за п. 14, яка відрізняється тим, що вказана масляна фаза являє собою олеїнову кислоту або ізопропілміристат. 16. Фармацевтична композиція за п. 13, яка відрізняється тим, що вказаний трансдермальний пластир являє собою пластир з контрольованим вивільненням по типу резервуара, що містить непроникну матрицю, рідкий лікарський засіб, мембрану, що сповільнює швидкість вивільнення, PSAs та шар вивільнення, де: непроникна матриця являє собою одну або більше субстанцій, вибраних з групи, що складається з поліетилену, полівінілхлориду, нітрогліцерину, полідиметилсилоксану, полівінілпіролідону, полівінілового спирту, комплексу поліетеноксиду, поліетиленгліколю, монометилового ефіру поліетиленгліколю або диметилового ефіру поліетиленгліколю, поліетиленгліколю сукцинату та вітаміну Е ТПГС, бавовни та вовни; вказана мембрана, що сповільнює швидкість вивільнення, вибрана з групи, що складається з мембрани із співполімеру етилену та вінілацетату, мембрани з поліуретану або мембрани з глікольдіацетату; та вказаний PSAs вибраний з групи, що складається з чутливої до тиску полісилоксанової смоли або чутливої до тиску поліакрилатної смоли. 17. Фармацевтична композиція за п. 16, яка відрізняється тим, що вказана матриця являє собою поліетилен або полівінілхлорид. 18. Фармацевтична композиція за п. 13, яка відрізняється тим, що вказаний трансдермальний пластир для місцевого застосування являє собою пластир з контрольованим вивільненням матричного типу, де допоміжна клейка матриця лікарського засобу вибрана з групи, що складається з полівінілхлориду, поліакрилату, полідиметилсилоксану, полівінілпіролідону, полівінілового спирту, водного гелю, що виготовлений з гелю, полівінілпіролідону, комплексу полівінілпіролідону та поліетиленоксиду, монометилового ефіру поліетиленгліколю або диметилового ефіру поліетиленгліколю, поліетиленгліколю сукцинату та BE ТПГС. 19. Фармацевтична композиція за п. 18, яка відрізняється тим, що допоміжна липка матриця лікарського засобу являє собою поліакрилат. 20. Фармацевтична композиція за п. 10, яка відрізняється тим, що вказана лікарська форма являє собою таблетку, пігулку, диспергований порошок, капсулу, гранулу, емульсію, розчин, суспензію, сироп, твердий супозиторій для вагінального або ректального введення. 21. Спосіб одержання композиції за пп. 14 або 15, який відрізняється тим, що в ньому здійснюють наступні стадії: зважування відповідної кількості сполуки за п. 1 як активного інгредієнта та подрібнення до стану тон 5 89795 6 кого порошку, ретельне перемішування водної фази, масляної фази, поверхнево-активної речовини та необхідних носіїв з подальшим змішуванням з подрібненим порошком лікарського засобу, одержану суміш змішують та мелють з одержанням мікроемульсії; додавання до суміші відповідної кількості мембрани, що сповільнює швидкість вивільнення, та чутливої до тиску клейкої субстанції з ретельним перемішуванням; дегазація шляхом збереження тепла з використанням водяної бані та розподіл на поліетиленовій матриці; сушіння та розрізання на маленькі шматочки з одержанням вказаного пластира з контрольованим вивільненням по типу резервуара твердої речовини. Даний винахід відноситься до галузі медицини. Більш конкретно, даний винахід стосується похідних темозоломід-8-карбоксилату, способу їх одержання, композицій на їх основі та застосування похідних і композицій у виробництві лікарського засобу для лікування пухлини, конкретно, застосування сполуки і композиції в препараті для перорального або трансдермального застосування, призначеному для лікування пухлини, такої як карцинома шкіри, карцинома мозку та лімфома. Темозоломід (в даному описі має назву "ТМЗ"), алкілувальний засіб для лікування карциноми, володіє протипухлинною біологічною активністю широкого спектру дії [L.Н. Tsang, et al. Cancer Chemother Pharmacol. 27 (1991): 342-346], і зокрема, володіє біологічною активністю, придатною для лікування нейрогліоми (карцинома мозку) та злоякісної меланоми (карцинома шкіри). У деяких західних країнах ТМЗ в капсулах зареєстрований для застосування в лікуванні злоякісної нейрогліоми. WO 0057867 описує спосіб застосування ТМЗ в циклічний схемі. ТМЗ в капсулах також зареєстрований для клінічного застосування в Китаї. Фаза II клінічних випробувань показала, що ТМЗ володіє здатністю виліковувати злоякісну меланому [N.М. Bleehen, et al. J. Clin. Oncol. 13 (1995): 910-913], а нещодавні клінічні випробування фази III виявили, що з точки зору лікування злоякісної меланоми ТМЗ має таку ж активність, як дакарбазин [М.R. Middleton, et al. J. Clin. Oncol. 18 (2000): 158-166], навіть з подібними побічними ефектами, такими як лейкоцитопенія, нудота, блювання, випадіння волосся, червоні висипи та закріп. Крім того, пероральне введення ТМЗ продемонструвало мієлотоксичність, що обмежує дозу [А.М. Heimberger, et al. Clin. Can. Res. 6 (2000): 4148-4153]. Попереднє дослідження різних лікарських форм продемонструвало, що інтратекальне ін'єкційне введення розчину ТМЗ може зменшити побічні ефекти [J. Н. Sampson, et al. Clin. Can. Res. 5 (1999): 1183-1188]. Схоже, що препарат ТМЗ для трансдермального введення є ідеальним для вилікування карциноми шкіри, особливо на ранніх стадіях. Кілька досліджень довели, що місцеве застосування тореміфену в місці карциноми може забезпечувати високі місцеві концентрації при зниженні системної концентрації [L. Soe, et al. Cancer Chemother. Pharmacol., 39 (1997): 513-520], що сприяє зниженню системної токсичності. Загалом, підшкірне введення обумовлюється як бар'єром шкіри, так і фізико-хімічними властивостями лікарського засобу. Нестабільність і нерозчинність вказаного лікарського засобу переш коджають введенню його в лікарські форми. Наприклад, опубліковані в WO0057867 дослідження показали, що його лікарського засобу проникати крізь штучну шкіру (силіконова мембрана), шкіру людини та шкіру щура робить неможливим введення даного лікарського засобу в препарати для трансдермального введення. Зважаючи на це, сфера застосування ТМЗ буде істотною мірою обмежена. Раніше з метою модифікації структури були синтезовані численні похідні, більшість з яких стосувалася заміни групи при атомі азоту №3 та модифікації групи при атомі азоту амідної групи №8. Загальна формула, описана в ЕР0252682 (1987), заявляє метил-, етил-, пропіл- та бутилтемозоломід-8-карбоксилати, але не розкриває їх фармакологічну дію та активність з точки зору лікування різних видів карциноми. З іншого боку, сполуки імідазо[5,1-d]-1,2,3,5тетразин-4-ону, звичайно представлені ТМЗ, мають спільну рису настільки низької розчинності, що вони тільки з великими зусиллями можуть бути розчинені в будь-яких розповсюджених розчинниках, таких як етилацетат, дихлорметан та вода. Вони демонструють слабку розчинність (приблизно 1~5%) в суміші органічного розчинника та води, наприклад, у водному розчині оцтової кислоти, ацетонітрилу, ацетону, метанолу або етанолу, з концентрацією 1~10%. Навіть в апротонному полярному розчиннику ДМСО їх розчинність становить приблизно 5%. Крім того, іншою особливістю даних сполук є їх нестабільність, що виявляється не просто в їх чутливості до дії світла, але більш того, в їх чутливості до лужних середовищ із значенням рН більше 7 та середовищ, що містять нуклеофільні групи, наприклад, сполуки, що містять амідогенні, гідроксильні та меркаптогрупи. Наприклад, середовище із значенням рН більше 7 призведе до швидкого розкладу та зміни кольору (червоний) вказаних сполук; те ж саме може відбуватися в метанолі та етанолі. Таким чином застосування метанолу та етанолу як солюбілізаторів у виробництві препаратів є обмеженим. Отже, дуже бажаним виглядає створення нової біологічно активної сполуки і пошук способів підвищення її стабільності та розчинності для використання у фармацевтичній промисловості. Таким чином, об'єктом даного винаходу є одержання похідних 3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату загальної формули (І) та способи їх одержання, а також композиції, що містять вказані похідні і способи одержання таких композицій. 7 Винахідниками було виявлено, що похідні 3,4дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5тетразин-8-карбоксилату загальної формули (І) та композиції, що їх містять, володіють протипухлинною активністю і будуть використовуватися для лікування різних видів карциноми, особливо карциноми шкіри, карциноми мозку та лімфатичної карциноми, тощо. Таким чином, іншим об'єктом винаходу є застосування похідних 3,4-дигідро-3метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилату загальної формули (І) та композицій, що їх містять, у виробництві лікарських засобів для лікування різних видів карциноми, де вказані види карциноми включають карциному шкіри, карциному мозку та лімфатичну карциному, тощо. Інший об'єкт винаходу полягає в пропонуванні різноманітних препаратів, що володіють біологічною протипухлинною активністю та містять похідні темозоломід-8-карбоксилату загальної формули (І) як активний(і) інгредієнт(и), особливо препарати для перорального застосування і трансдермальні пластирі для місцевого застосування (проникнення крізь шкіру). Вказані трансдермальні пластирі для місцевого застосування включають пластир з контрольованим вивільненням матричного типу, пластир з контрольованим вивільненням по типу резервуару твердої речовини або пластир з контрольованим вивільненням по типу резервуару рідкої речовини. Структура вказаного 3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату за даним винаходом представлена загальною формулою (І) наступним чином: де X являє собою О або S; R являє собою заміщений або незаміщений С3~С10 алкіл з нерозгалуженим або розгалуженим ланцюгом, С3~С10 циклоалкіл, С3~С10 алкеніл з нерозгалуженим або розгалуженим ланцюгом або С3~С10 алкініл з нерозгалуженим або розгалуженим ланцюгом; Додатково, R може містити замісник(и), де вказані замісник(и) можуть являти собою С1~С6 алкіл, С1~С6 алкокси, С1~С6 алкілтіогрупу, С1~С6 алкіламіногрупу, феніл або феніл, заміщений галогеном. Переважно, X являє собою О. У викладеному вище визначенні термін С3~С10 алкіл з нерозгалуженим або розгалуженим ланцюгом в даному описі являє собою насичений вуглеводневий радикал з нерозгалуженим або розгалуженим ланцюгом, що містить 3-10 атомів вуглецю, наприклад пропіл, бутил, аміл, гексил, 89795 8 гептил, октил, ноніл або децил і т.п. та всі їх ізомери, такі як ізопропіл, ізобутил, трет-бутил, ізогексил або ізо-гептил, і т.д. Переважний R вибраний з групи, що складається з метилу, етилу, пропілу, ізопропілу, н-бутилу, 1-метил-пропілу, 2метил-пропілу, амілу, 1-метил-бутилу, 2-метилбутилу, 3-метил-бутилу, гексилу, 1-метил-амілу, 2метил-амілу, 3-метил-амілу, 4-метил-амілу, гептилу, 1-метил-гексилу, 2-метил-гексилу, 3-метилгексилу, 4-метил-гексилу, 5-метил-гексилу, октилу, 1-метил-гептилу, 2-метил-гептилу, 3-метилгептилу, 4-метил-гептилу, 5-метил-гептилу, 6метил-гептилу, 1-етил-пропілу, 1-етил-бутилу, 1етил-амілу, 2-етил-амілу або 3-етил-амілу. Більш переважний R являє собою н-гексил, ізогексил та циклогексил. Найбільш переважний R являє собою н-гексил. У відповідності до описаних вище груп, похідні ТМЗ-8-карбонової кислоти включають: метил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилат; етил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилат; пропіл-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилат; бутил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилат; 1-метил-бутил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 1-eтил-бyтил-3,4-дигiдpo-3-мeтил-4oкcoiмiдaзo[5,1-d]-1,2,3,5-тeтpaзин-8-карбоксилат; 1-етил-пропіл-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 1-eтил-aміл-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 1-метил-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 2-метил-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 3-мeтил-гeкcил-3,4-дигiдpo-3-мeтил-4oкcoiмiдaзo[5,1-d]-1,2,3,5-тeтpaзин-8-карбоксилат; 4-мeтил-гeкcил-3,4-дигiдpo-3-мeтил-4oкcoiмiдaзo[5,1-d]-1,2,3,5-тeтpaзин-8-карбоксилат; 5-метил-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 1-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 2-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 3-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 4-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 5-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 6-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; аміл-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилат; н-гексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилат; циклогексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; ізогексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; 9 гептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилат та октил-3,4-дигідро-3-метил-4-оксоімідазо [5,1d]-1,2,3,5-тетразин-8-карбоксилат. Більш переважними є н-гексил-3,4-дигідро-3метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилат, ізогексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат та циклогексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат; найбільш переважним є н-гексил-3,4-дигідро-3метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилат. У наведеному вище визначенні загальної формули термін С3~С10 циклоалкіл в даному описі означає циклічний насичений вуглеводневий радикал, що містить 3-10 атомів вуглецю, такий як циклопропіл, циклобутил, циклоаміл, циклогексил, циклогептил, циклооктил, циклононіл або циклодецил, і т.д. У наведеному вище визначенні загальної формули термін С3~С10 алкенільний ланцюг означає вуглеводневий радикал, що містить 1, 2 або 3 ненасичені подвійні зв'язки та 3-10 атомів вуглецю, такий як пропеніл, бутеніл, пентеніл, гексеніл, гептеніл та гептадієніл, і т.д. У наведеному вище визначенні загальної формули термін С3~С10 алкінільний ланцюг означає вуглеводневий радикал, що містить 1, 2 або 3 ненасичених потрійних зв'язки та 3-10 атомів вуглецю, такий як пропініл, бутиніл, пентиніл, гексиніл та гептиніл, і т. д. У наведеному вище визначенні загальної формули термін С1~С6 алкіл, як визначено вище, означає алкіл з нерозгалуженим або розгалуженим ланцюгом, що містить 1-6 атомів вуглецю, такий як метил, етил, пропіл, бутил, аміл, гексил і т.п., та також всі їх ізомери. У наведеному вище визначенні загальної формули термін С1~С6 алкокси означає алкіл, наведений вище, що містить атом кисню, такий як метокси, етокси, пропокси, бутокси, пентокси, гексилокси і т.п., та всі їх ізомери. У наведеному вище визначенні загальної формули термін С1~С6 алкілтіогрупа означає алкоксил, наведений вище, в якому атом кисню замінений на атом сірки, такий як метилтіо, етилтіо, пропілтіо, бутилтіо, амілтіо, гексилтіо і т.п., та всі їх ізомери. У наведеному вище визначенні загальної формули термін С1~С6 алкіламіногрупа означає аміногрупу, що містить один або два алкільних радикали, як визначено вище, таку як метиламіно, етиламіно, диметиламіно, бутиламіно, аміламіно, гексиламіно і т.п., та всі їх ізомери. У наведеному вище визначенні загальної формули термін галоген означає фтор, хлор, бром або йод. Сполуки загальної формули (І) одержують за наступним способом. При перемішуванні ТМЗ змішують з концентрованою сірчаною кислотою. Натрію нітрит розчиняють у воді і потім по краплях додають до описаної вище суміші на льодяній бані при температурі нижче 15°С, після чого перемішують при кімнатній 89795 10 температурі протягом ночі. До одержаної суміші безперервно додають лід та охолоджують на льодяній бані протягом 1 год. Одержаний твердий продукт ТМЗ кислоту відокремлюють фільтрацією та сушать під вакуумом. Суміш безводних ДМФА та ТГФ впорскують у колбу, заповнену ТМЗ кислотою та Pybrop, і перемішують до повного розчинення твердої речовини, після чого в умовах льодяної бані додають 4диметиламінопіридин (DMAP). Далі відповідну кількість безводного вуглеводневого спирту або меркаптану впорскують до одержаної суміші та продовжують реакцію протягом 30 хвилин, після чого перемішують при кімнатній температурі протягом ночі. Після завершення реакції суспензію фільтрують крізь лійку Бюхнера. Одержаний маточник піддають дистиляції; до залишку додають лід та екстрагують етилацетатом (10мл×3). Етилацетатні фракції об'єднують та сушать за допомогою безводного магнію сульфату. Етилацетат видаляють за допомогою роторного випарювача з одержанням залишку. Залишок, що являє собою кінцевий продукт, далі очищують на колонці з силікагелем та одержують цільову сполуку після випаровування розчинників. Продукт ідентифікований за допомогою ІЧспектра, 1Н-ЯМР, 13С-ЯМР та МС. У відповідності до іншого аспекту винаходу, пропонуються композиції, що містять вказані похідні 3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилату, та способи їх одержання. Фармацевтичні композиції за винаходом володіють протипухлинною активністю, причому вказані композиції містять терапевтично ефективну кількість однієї чи більше сполук загальної формули (І), як активні інгредієнти, разом з традиційними фармацевтично прийнятними носіями. Вказані фармацевтично прийнятні носії являють собою носії, відомі з рівня техніки, такі як рідкі або тверді допоміжні речовини, розбавлювачі, зволожувальні засоби, консерванти, засоби для маскування смаку та барвники, і т.д. Композиції за винаходом включають одну або більше сполук вказаної загальної формули (І), як активний(і) інгредієнт(и). Переважні сполуки загальної формули (І) вибрані з групи, що складається з: метил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилату, етил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилату, пропіл-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилату, бутил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилату, 1-метил-бутил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 1-етил-бутил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 1-етил-пропіл-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 1-етил-аміл-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 11 1-метил-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 2-метил-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 3-мeтил-гeкcил-3,4-дигiдpo-3-мeтил-4oкcoiмiдaзo[5,1-d]-1,2,3,5-тeтpaзин-8-карбоксилату, 4-метил-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 5-мeтил-гeкcил-3,4-дигiдpo-3-мeтил-4oкcoiмiдaзo[5,1-d]-1,2,3,5-тeтpaзин-8-карбоксилату, 1-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 2-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 3-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 4-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 5-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, 6-метил-гептил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, аміл-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3,5-тетразин-8-карбоксилату, н-гексил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилату, iзо-гексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, циклогексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилату, гептил-3,4-дигідро-3-метил-4-оксоімідазо[5,1d]-1,2,3,5-тетразин-8-карбоксилату та октил-3,4-дигідро-3-метил-4-оксоімідазо[5,1-d]1,2,3)5-тетразин-8-карбоксилату. Більш переважними сполуками є н-гексил-3,4дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5тетразин-8-карбоксилат, iзо-гексил-3,4-дигідро-3метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилат та циклогексил-3,4-дигідро-3-метил-4оксоімідазо[5,1-d]-1,2,3,5-тетразин-8-карбоксилат. Найбільш переважною сполукою є н-гексил-3,4дигідро-3-метил-4-оксоімідазо[5,1-d]-1,2,3,5тетразин-8-карбоксилат. Додатково, композиції за винаходом можуть включати фармацевтично прийнятні компоненти кислотної природи, наприклад, допоміжні речовини кислотної природи, які використовуються в фармацевтичній промисловості, такі як олеїнова кислота, стеаринова кислота, ліноленова кислота, фумарова кислота, бензойна кислота, винна кислота, сорбінова кислота, молочна кислота, лимонна кислота, оцтова кислота, ЕДТА, і т.д. Такі субстанції кислотної природи виконують роль стабілізатора для сполук загальної формули (І). Винахідниками також було виявлено, що розчинність та кількість в середовищі ТМЗ-8карбоксилату, активного інгредієнта композицій, буде збільшуватися при додаванні 0,5-20% (мас), переважно 1-10% (мас.) фармацевтично прийнятного вторинного спирту або третинного спирту, на базі загальної маси композиції. Причому, переважним спиртом є С3~С8 вторинний спирт або третинний спирт, такий як ізопропанол, ізобутиловий спирт, ізоаміловий спирт, mpew-бутиловий спирт або їх естерні похідні або ефірні похідні, такі як 89795 12 тригліцерид та полігліколєвий ефір. Тим часом, вказані субстанції можуть використовуватися як солюбілізатор для композиції та лікарських форм іншого типу, що містять похідні ТМЗ-8карбоксилату або інші імідазо[5,1-d]-1,2,3,5тетразин-4-они. Композиція за винаходом може бути виготовлена у будь-якій з традиційних фармацевтичних лікарських форм. Конкретно, лікарські форми розробляють на базі наступних факторів: бажаний ефект, властивості активних інгредієнтів, дозування, вік, стать і стан захворювання пацієнтів. Вказані лікарські форми включають лікарські форми, придатні для введення, наприклад, таблетку, пігулку, диспергований порошок, капсулу, гранулу, емульсію, розчин, суспензію, сироп, твердий супозиторій для вагінального або ректального введення, а також пластир для місцевого застосування. Переважною є трансдермальна лікарська форма для місцевого застосування або лікарська формула для перорального застосування. Найбільш переважною є трансдермальна лікарська форма для місцевого застосування. Композиція та всі її лікарські форми за винаходом можуть бути виготовлені за будь-яким способом, добре відомим в галузі фармації. У відповідності до винаходу, одна з лікарських форм, придатних для похідних 3,4-дигідро-3метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилату, являє собою препарат для перорального застосування, в тому числі тверді та рідкі препарати, зокрема тверді препарати для перорального застосування включають таблетку, пігулку, диспергований порошок, капсулу та гранули, і т.д. В ході процесу виготовлення твердих лікарських форм, біологічно активний агент, похідні ТМЗ-8карбоксилату, може не бути змішаний з іншими інгредієнтами, або може бути змішаний щонайменше з одним інертним розбавлювачем, в тому числі кальцію карбонатом, крохмалем, альгіновою кислотою або лактозою, і т.д., та з субстанцією кислотної природи, такою як фумарова кислота, винна кислота, сорбінова кислота та лимонна кислота, і т.д., які можуть бути додані до лікарської форми. На додаток до описаних вище компонентів, інші компоненти можуть бути включені в лікарські форми, наприклад, змащувальна речовина, така як стеарат магнію. Крім того, похідні ТМЗ-8карбоксилату можуть бути введені в рідкі лікарські форми для перорального застосування, в тому числі емульсію, розчин, суспензію та сироп, і т.д. У згаданих вище рідких лікарських формах завжди присутня водна рідина, яка містить поверхневоактивну речовину або рідкий парафін як інертні розбавлювачі. Крім інертних розбавлювачів, також можуть бути включені інші добавки, наприклад, зволожувальні агенти, суспендувальні агенти, такі як полівінілпіролідон (ПВП), підсолоджувальні агенти, агенти для маскування смаку, консерванти та ароматизатори. Іншою фармацевтичною лікарською формою, придатною для введення похідних 3,4-дигідро-3метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилату, є супозиторій, в тому числі твердий супозиторій для вагінального та ректального вве 13 дення. Окрім традиційних допоміжних речовин, з метою забезпечення пролонгованого та контрольованого вивільнення вказаний супозиторій загалом включає полімер, що розкладається в біологічному середовищі, такий як полімолочна кислота (PLGA), поліангідрид та полі(змішаний ангідрид) ((поліангідридний співполімер полі(1,3-біс-(nкарбоксифеноксипропан)-ко-(себациновый ангідрид) або (CPP:SA)). Зважаючи на властивості похідних 3,4-дигідро3-метил-4-оксоімідазо[5,1-d]-1,2,3,5-тетразин-8карбоксилату, здатних проникати крізь шкіру, найбільш переважними лікарськими формами для них є трансдермальні лікарські форми для місцевого застосування, в тому числі настоянка, суспензія, емульсія, мазь, гель, супозиторій, плівка та пластир, і т.д. Як правило, трансдермальні лікарські форми для місцевого застосування включають такі допоміжні речовини, як масляне середовище, поверхнево-активна речовина і т.п. Вказане масляне середовище, яке використовується в трансдермальних лікарських формах для місцевого застосування, вибирають з групи, що складається з олеїнової кислоти, ізопропілміристату (ІПМ), лауринової кислоти, воску, цетилового спирту, стеарилового спирту, рідкого парафіну, вазеліну, безводного ланоліну, стеаринової кислоти, бавовняної олії, рицинової олії, ліноленової кислоти і тригліцериду, тощо. Вказану широко застосовувану поверхнево-активну речовину вибирають з групи, що складається з фосфоліпіду, субстанції по типу Myrj, субстанції по типу Brij, субстанції по типу Твіну, акацієвої камеді, трагакантової камеді, глютину та вітаміну Ε ТПГС (BE ТПГС), і т.д. Переважні трансдермальні пластирі ТМЗ-8карбоксилату для місцевого застосування діляться на дві групи: резервуарного та матричного типу. Матричний тип може бути поділений на єдину матрицю (AM) та поліматрицю (РМ). Тип резервуару включає систему резервуару рідини (LRS) і систему резервуару твердої речовини (SRS), яка складається з багатошарової липкої (MLA) та багатошарової полімерної матриці (MLM). В основному, трансдермальні лікарські форми ТМЗ-8карбоксилатів для місцевого застосування як матричного типу, так і резервуарного типу істотною мірою включають: матрицю, полімерні матеріали, резервуар лікарського засобу (розчин або суспензію лікарського засобу), мембрану, що сповільнює швидкість вивільнення, чутливі до тиску клейкі речовини (PSAs) та шар вивільнення для захисту PSAs. Додаткове обговорення наведено нижче. Пластир типу резервуару твердої рідини: матриця являє собою прозору та стабільну мікроемульсію та її лікарські форми, утворені водною фазою, масляною фазою та поверхнево-активними речовинами при різних співвідношеннях, що поділяються на пластир типу резервуару рідини і типу резервуару твердої речовини. У вказаному пластирі типу резервуару твердої речовини як масляна фаза може бути вибрана олеїнова кислота або ізопропілміристат (ІПМ), а також лауринова кислота, віск, цетиловий спирт, стеариловий спирт, рідкий парафін, вазелін, безводний ланолін, стеари 89795 14 нова кислоти, бавовняна олія, рицинова олія та ліноленова кислота можуть бути вибрані для створення масляної фази. Переважна масляна фаза для пластиру типу резервуару твердої речовини ТМЗ-8-карбоксилату за винаходом являє собою ізопропілміристат (ІПМ) або олеїнову кислоту, переважна водна фаза являє собою воду, та переважна поверхнево-активна речовина являє собою BE ТПГС та лимонну кислоту. Пластир контрольованого вивільнення типу резервуару для рідини виготовляють шляхом термічного топлення непроникної матриці (або так званої матриці), рідкого лікарського засобу, мембрани, що сповільнює швидкість вивільнення, PSAs та шару вивільнення. Структура кожної частини пластиру типу резервуару рідини ТМЗ-8-карбоксилату за винаходом є наступною: Матриця, тобто непроникна матриця, загалом може бути синтезованою з полімерних матеріалів, що володіють проникністю або непроникністю, таких як поліестер, поліетилен, полівінілхлорид (ПВХ), полі(вініліденхлорид) (ПВДХ) та поліуретан, і т. д., а також з природних полімерних матеріалів, таких як бавовна або вовна, тощо. Матриця за винаходом може бути вибрана з групи, що складається з ПВХ, нітрогліцерину (Transdermal®), полідиметилсилоксану (Nitrodisc®), ПВП, полівінілового спирту (Nitro-Dur® І), комплексу поліетеноксиду, ПЕГ, всіх похідних ПЕГ, таких як монометиловий ефір поліетиленгліколю або диметиловий ефір поліетиленгліколю, поліетиленгліколь сукцинат (ТПГС) та BE ТПГС, і т.д. Переважними є поліетилен, полівінілхлорид, ПВДХ, поліуретан або бавовна. Переважно, мембрана, що сповільнює швидкість вивільнення, являє собою мембрану, утворену співполімером етилену та вінілацетату, або гомогенні мембрани, такі як мембрана з поліуретану та мембрана з глікольдіацетату. PSAs являє собою унікальну біоадгезивну, переважно чутливу до тиску полісилоксанову або чутливу до тиску поліакрилатну смолу. Пластир контрольованого вивільнення типу резервуару за винаходом може бути виготовлений за способом, що включає наступні стадії: зважування відповідної кількості н-гексил-ТМЗ-8карбоксилату та подрібнення його до стану тонкого порошку, додавання водної фази, такої як вода, масляної фази, такої як олеїнова кислота і т.д., та поверхнево-активної речовини, такої як BE ТПГС і т.д.; ретельне змішування; додавання подрібненого лікарського засобу, помел одержаної суміші з утворенням мікроемульсії; з наступним додаванням мембрани, що сповільнює швидкість вивільнення, такої як мембрана, утворена співполімером етилену та вінілацетату, та відповідної кількості PSAs, ретельне перемішування; дегазацію шляхом збереження тепла з використанням водяної бані та розподіл на поліетиленовій матриці; сушіння та розрізання на маленькі шматочки з одержанням цільового продукту. Вказані пластирі матричного типу за винаходом з єдиною клейкою матрицею виготовляють за 15 способом, що включає наступні стадії: диспергування лікарського засобу в PSAs, з якого буде здійснюватися контрольоване вивільнення лікарського засобу. Особливості системи контрольованого вивільнення: тонший об'єм, більш простий технічний процес та легша промислова відтворюваність. Склад допоміжних речовин клейкої матриці лікарського засобу за винаходом вибирають з групи, що складається з природних або синтетичних полімерів, в тому числі полівінілхлориду, поліакрилату, полідиметилсилоксану, та гідрофільних полімерів, таких як ПВП, полівініловий спирт, водний гель, виготовлений з гелю (наприклад, Prostep®), комплексу ПВП та поліетеноксиду, ПЕГ та його похідних, таких як монометиловий ефір поліетиленгліколю або диметиловий ефір поліетиленгліколю, поліетиленгліколь сукцинату та BE ТПГС. Переважним є поліакрилат. Звичайно, вказаний ТМЗ-8-карбоксилат вводять в дозах 0,1~200мг/кг маси тіла/день, переважно, 1~20мг/кг маси тіла/день. Дослідження розчинності в ліпідах, стабільності та розчинності ТМЗ-8-карбоксилату Дослідження показали, що в порівнянні з ТМЗ, розчинність похідних ТМЗ-8-карбоксилату в ліпідах є значно кращою. Наприклад, якщо брати Log P як стандарт, Log Ρ для ТМЗ становить -0,66, тоді як Log Ρ для н-гексил-ТМЗ-8-карбоксилату становить 2,56. Це означає, що н-гексил-ТМЗ-8-карбоксилат являє собою ідеальний лікарський засіб для місцевого трансдермального застосування (спосіб вимірювання Log Ρ див. у Leo and Hansch. Chemical Reviews 71 No.6, December 1971 (Partition Coefficients and Their Uses, Leo Α., Hansch C. and Elkins D.). Винахідниками було виявлено, що стабільність може бути істотно збільшена у випадку похідних ТМЗ-8-карбоксилату окремо або разом з іншими імідазо[5,1-d]-1,2,3,5-тетразин-4-онами в кислих умовах (рН 1~6,5), одержаних додаванням фармацевтично прийнятних компонентів кислотної природи. Отже, стабільність активних інгредієнтів буде істотною мірою підвищуватися, якщо похідні ТМЗ-8-карбоксилату будуть застосовуватися як активні інгредієнти в рідкій лікарській формі, такій як настоянка, суспензія, емульсія та ін'єкційні лікарські форми, а також в твердій лікарській формі, такій як мазь, супозиторій та плівка. Вказані субстанції кислотної природи включають олеїнову кислоту, стеаринову кислоту, ліноленову кислоту, фумарову кислоту, бензойну кислоту, винну кислоту, сорбінову кислоту, молочну кислоту, лимонну кислоту, оцтову кислоту, ЕДТА і т.п. Крім того, винахідниками також було виявлено, що розчинність та кількість ТМЗ-8карбоксилату, активного інгредієнта композиції, в середовищі буде збільшуватися при додаванні 0,5%~20% фармацевтично прийнятного вторинного спирту або третинного спирту, такого як ізопропанол, ізобутиловий спирт, ізоаміловий спирт, трет-бутиловий спирт або їх естерні або ефірні похідні, такі як тригліцерид, полігліколевий ефір. Відповідно, вторинний спирт або третинний спирт, такий як ізопропанол, ізобутиловий спирт, ізоаміловий спирт, трет-бутиловий спирт, і т. д. може 89795 16 використовуватися як солюбілізатор в композиції, що містить похідні ТМЗ-8-карбоксилату та інші імідазо[5,1-d]-1,2,3,5-тетразин-4-они. Одержані дані підтверджують, що винахід забезпечує протипухлинну композицію, яка містить одне або більше похідних ТМЗ-8-карбоксилату, фармацевтично прийнятні речовини кислотної природи, необов'язково містить фармацевтично прийнятний вторинний спирт або третинний спирт та їх похідні, а також фармацевтично прийнятні допоміжні речовини та/або носії. Винахід також пропонує різноманітні препарати, виготовлені на основі композиції за винаходом. Наступні експерименти з дослідження фармацевтичної активності метил-ТМЗ-8-карбоксилату, бутил-ТМЗ-8-карбоксилату та н-гексил-ТМЗ-8карбоксилату in vitro проти карциноми наведені з метою ілюстрації їх ефективності. Дослідження здатності ТМЗ-8-карбоксилату вбивати пухлинні клітини in vitro Експеримент проводили для метил-ТМЗ-8карбоксилату, бутил-ТМЗ-8-карбоксилату, нгексил-ТМЗ-8-карбоксилату та ТМЗ кислоти, яка відома як активна сполука проти карциноми, з використанням ін'єкції фторурацилу (10мл:0,25г, придбаний у Xudong Pharmaceutical Co. Ltd, номер серії 000612 ), як лікарського засобу для позитивного контролю. Штами ракових клітин, які використовували в експериментах, включали НСТ-8 (клітини карциноми ободової кишки людини), А549 (клітини карциноми легень людини), MCF-7 (клітини карциноми молочної залози людини), Веl-7402 (клітини карциноми печінки людини), BGC-823 (клітини карциноми шлунку людини) та MV3 (клітини меланоми людини). Лікарські засоби та реактиви ТМЗ кислота являє собою білий порошок; метил-ТМЗ-8-карбоксилат, бутил-ТМЗ-8-карбоксилат та н-гексил-ТМЗ-8-карбоксилат, білі лускаті кристали, одержували за способом, описаним у Прикладі 2; фторурацил для ін'єкцій (10мл:0,25г): як лікарський засіб для позитивного контролю, виробник Xudong Pharmaceutical Co. Ltd, номер серії 000612; RPMI: виробник GIBCO; теляча сироватка: виробник Sijiqing bio-engineer material Co. Ltd, Hangzhou; та МТТ: виробник Bebco. Штами клітин Всі штами ракових клітин - НСТ-8, А549, MCF7, Bel-7402, BGC-823, MV3 та В16 - були вирощені і культури перенесені з Institute of Materia Medica, Chinese Academy of Medical Sciences та Peking Union Medical College. Прилад: BIORAD 550 для мічення ферментів. Метод: Використовували пробу відновлення солі тетразолію [3-(4,5-диметилтіазол-2-іл)-2,5-дифенілтетразолію бромід, МТТ]. Всі культивовані клітини карциноми збирали, готували суспензію клітин 4 1×10 /мл в розчині для культивування RPMI 1640, що містить 10% телячої сироватки, та інокулювали в 96-ячейкові планшети для культивування, 100мкл на ячейку (містить 1000 ракових клітин). Після проходження 24 год культивування в термосному інкубаторі з 5% СО2 при температурі 37°С додавали лікарські засоби. В дослідженні брала 17 89795 участь група холостого контролю, лікарським засобом для позитивного контролю був фторурацил. Досліджувані лікарські засоби були розділені на п'ять груп з різними концентраціями, які досліджувалися в трьох паралельних повтореннях. Культури клітин вміщували до термосного інкубатору з 5% СО2 при температурі 37°С для культивування протягом 4 днів. Розчин культивування відкидали та додавали 100мкл розчину МТТ (0,4мг/мл, виготовлений в RPMI 1640) на ячейку і продовжували культивування протягом 4 год при температурі 37°С. Супернатант відкидали та додавали 150мкл диметилсульфоксиду для розчинення гранул Fomazan. Після обережного перемішування вимірювали значення оптичної густини за допомогою 18 приладу для мічення ферментів BIORAD 550 при довжині хвилі 540нм та довжині хвилі порівняння 450нм. Результати Дані інгібування клітин наносили на графік та будували криву залежності "доза-реакція", за якою обчислювали 50% інгібувальну концентрацію ІС50 (див. Таблицю 1 та Таблицю 2). Результат (див. Таблицю 1) продемонстрував, що інтервали ІС50 чотирьох лікарських засобів (метил-ТМЗ-8-карбоксилат, бутил-ТМЗ-8-карбоксилат, н-гексил-ТМЗ-8-карбоксилат та ТМЗ кислота) становили для вибраних штамів клітин 10~30мкг/мл, причому не спостерігалося значних відмінностей між ними з точки зору дії на клітини. Таблиця 1 Загибель пухлинних клітин (метод МТТ) Штами клітин MV3 MCF-7 Веl-7402 А549 НСТ-8 BGC-823 Фторурацил 0,427 0,629 0,495 0,126 0,606 0,722 ІС50 ТМЗ кисло- н-Гексил-ТМЗ-8та карбоксилат 14,625 8,835 14,911 19,995 16,957 27,203 >19,5 26,632 18,525 28,644 >19,5 >19,5 Вплив місцевого застосування гексил-ТМЗ-8карбоксилату на ріст ксенотрансплантованої меланоми людини у голих мишей МУЗ Гексил-ТМЗ-8-карбоксилат був вибраний як репрезентативна сполука для дослідження впливу похідних ТМЗ-8-карбоксилату на ріст ксенотрансплантованої меланоми людини у голих мишей MV3. Гексил-ТМЗ-8-карбоксилат розчиняли в ДМСО з одержанням розчину 50мг/мл. Здійснювали ксенотрансплантацію меланоми людини голим мишам BALB/c-nu і дозволяли їй рости. Коли пухлина досягала об'єму 100~300мм3, всіх тварин поділяли на дві групи у відповідності до розміру пухлини, по 8 мишей в кожній групі. З вказаних двох груп одна являла собою групу лікарського засобу, в якій здійснювали лікування нанесенням розчину гексил-ТМЗ-8-карбоксилату; інша група служила контролем, де пухлини росли природним чином. В групі лікарського засобу його застосовували шляхом нанесення в місці пухлини та навколишньої області (2см×2см) двічі на день (один раз в суботу та неділю). Кожного разу, коли розчин висихав, нанесення повторювали 1-2 рази. Середня добова доза введеного миші гексил-ТМЗ-8карбоксилату загалом становила приблизно 20мг. Об'єм пухлини у миші вимірювали двічі на тиждень, таким чином, щоб спостерігати та реєструвати її ріст в динаміці. Коли пухлини в контрольній групі досягай визначеного об'єму, всі миші були забиті, пухлини були витягнуті та зважені, був обчислений ступінь інгібування росту. Проліферацію пухлини (Т/С(%)) обчислювали з використанням відносного об'єму пухлини в двох групах. Метил-ТМЗ-8карбоксилат 8,827 17,665 25,304 27,001 28,369 >19,5 Бутил-ТМЗ-8карбоксилат 7,568 16,558 24,368 25,336 27,359 >19,5 Об'єм пухлини (TV) обчислювали за наступним рівнянням: 2 Довжина×ширина ÷2 Відносний об'єм пухлини обчислювали за наступним рівнянням: Vt/Vо де Vо являє собою TV, виміряний в точці часу, в якій тварин розподіляли в окремі клітини, та Vt являє собою TV, виміряний в подальшому в кожній точці часу. t-тест застосовували для порівняння статистичної відмінності між двома групами для багатьох показників, таких як маса пухлини, TV та RTV. Відносну швидкість проліферації пухлини (Т/С(%)) застосовували як показник протипухлинної біологічної активності, яку обчислювали наступним чином: Група лікарськог о засобу (Т ) RTV T / C(%) 100 Контрольна група (C) RTV Критерії оцінки ефекту: Ефект оцінювали за допомогою статистичного аналізу. Ефект вважали недостовірним, якщо Т/С (%) становило більше 60, та вважали достовірним, якщо Т/С (%) становило ≤60 при р
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical composition comprising temozolomide ester
Автори англійськоюWang Yongfeng
Назва патенту російськоюФармацевтическая композиция, которая содержит эстер темозоломида
Автори російськоюВан Йонфен
МПК / Мітки
МПК: A61K 31/41, A61P 35/00, C07D 487/04
Мітки: композиція, темозоломіду, естер, містить, фармацевтична
Код посилання
<a href="https://ua.patents.su/15-89795-farmacevtichna-kompoziciya-shho-mistit-ester-temozolomidu.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція, що містить естер темозоломіду</a>
Попередній патент: Плавлений литий вогнетривкий продукт і спосіб його застосування
Наступний патент: Ламіновані будівельні матеріали
Випадковий патент: Вітроенергетична установка мілінського ю.м.












