Композиція для катетера та її застосування
Формула / Реферат
1. Композиція для видалення фібрин-зв'язаних згустків крові з катетера, яка містить виключно нехелатуючі засоби: воду, фібринолітично ефективну кількість активатора плазміногену й антисептично ефективну кількість бактеріостатичного органічного спирту.
2. Композиція за п. 1, яка відрізняється тим, що активатор плазміногену являє собою тканинний активатор плазміногену або урокіназу.
3. Композиція за п. 2, яка відрізняється тим, що активатор плазміногену являє собою t-PA нативної послідовності, урокіназу нативної послідовності, ретеплазу або тенектеплазу.
4. Композиція за п. 3, яка відрізняється тим, що активатор плазміногену являє собою t-PA нативної послідовності або тенектеплазу.
5. Композиція за будь-яким з пп. 1-4, яка відрізняється тим, що органічний спирт являє собою бензиловий спирт, ізопропанол або етанол.
6. Композиція за будь-яким з пп. 1-5, яка відрізняється тим, що органічний спирт являє собою бензиловий спирт.
7. Композиція за будь-яким з пп. 1-6, яка відрізняється тим, що фібринолітично ефективна кількість активатора плазміногену складає від 0,1 до 10 мг/мл, а антисептично ефективна кількість органічного спирту складає від 0,5 до 1,2 % (об./об.).
8. Композиція за будь-яким з пп. 1-7, яка відрізняється тим, що фібринолітично ефективна кількість активатора плазміногену складає від 0,3 до 4 мг/мл.
9. Композиція за будь-яким з пп. 1-8, яка відрізняється тим, що вода, яка містить спирт, являє собою бактеріостатичну воду для ін'єкцій або являє собою бактеріостатичний нормальний сольовий розчин.
10. Спосіб видалення фібрин-зв'язаних згустків крові з катетера, який містить такі згустки крові, що включає контактування катетера з композицією за будь-яким з пп. 1-9 протягом не менше 5 днів.
11. Спосіб за п. 10, який відрізняється тим, що катетер контактує з композицією протягом 6-15 днів.
12. Катетер, вмочений, просочений і/або імпрегнований композицією за будь-яким з пп. 1-9.
13. Катетер за п. 12, що являє собою постійний катетер.
14. Мультисекційний контейнер, що включає відсік, який містить фібринолітично ефективну кількість активатора плазміногену, відсік, який містить воду, яка містить антисептично ефективну кількість бактеріостатичного органічного спирту, причому відсіки містять виключно нехелатуючі засоби; а також містить інструкції по змішуванню вмісту обох відсіків і по використанню отриманої суміші для видалення фібрин-зв'язаних згустків крові з катетера, що містить такі згустки крові.
15. Контейнер за п. 14, який відрізняється тим, що активатор плазміногену являє собою тканинний активатор плазміногену або урокіназу.
16. Контейнер за п. 15, який відрізняється тим, що активатор плазміногену являє собою t-PA нативної послідовності, урокіназу нативної послідовності, ретеплазу або тенектеплазу.
17. Контейнер за п. 16, який відрізняється тим, що активатор плазміногену являє собою t-PA нативної послідовності або тенектеплазу.
18. Контейнер за будь-яким з пп. 14-17, який відрізняється тим, що органічний спирт являє собою бензиловий спирт, ізопропанол або етанол.
19. Контейнер за будь-яким з пп. 14-18, який відрізняється тим, що органічний спирт являє собою бензиловий спирт.
20. Контейнер за будь-яким з пп. 14-19, який відрізняється тим, що фібринолітично ефективна кількість активатора плазміногену складає від 0,1 до 10 мг/мл, а антисептично ефективна кількість органічного спирту складає від 0,5 до 1,2 %(об./об.).
21. Контейнер за будь-яким з пп. 14-20, який відрізняється тим, що фібринолітично ефективна кількість активатора плазміногену складає від 0,3 до 4 мг/мл.
22. Контейнер за будь-яким з пп. 14-21, який являє собою комплект, де кожний відсік являє собою окремий контейнер.
23. Контейнер за будь-яким з пп. 14-21, який являє собою шприц з кількома відсіками.
24. Контейнер за будь-яким з пп. 14-23, який відрізняється тим, що вода, яка містить спирт, являє собою бактеріостатичну воду для ін'єкцій або являє собою бактеріостатичний нормальний сольовий розчин.
25. Мультисекційний контейнер, що включає відсік, який містить від 0,1 до 10 мг/мл t-PA нативної послідовності або тенектеплази, і відсік, який містить воду, яка містить від 0,5 до 1,2 % (об./об.) бензилового спирту, ізопропанолу або етанолу, причому відсіки містять виключно нехелатуючі засоби; а також містить інструкції по змішуванню вмісту обох відсіків і по використанню отриманої суміші для видалення фібрин-зв'язаних згустків крові з катетера, що містить такі згустки крові.
Текст
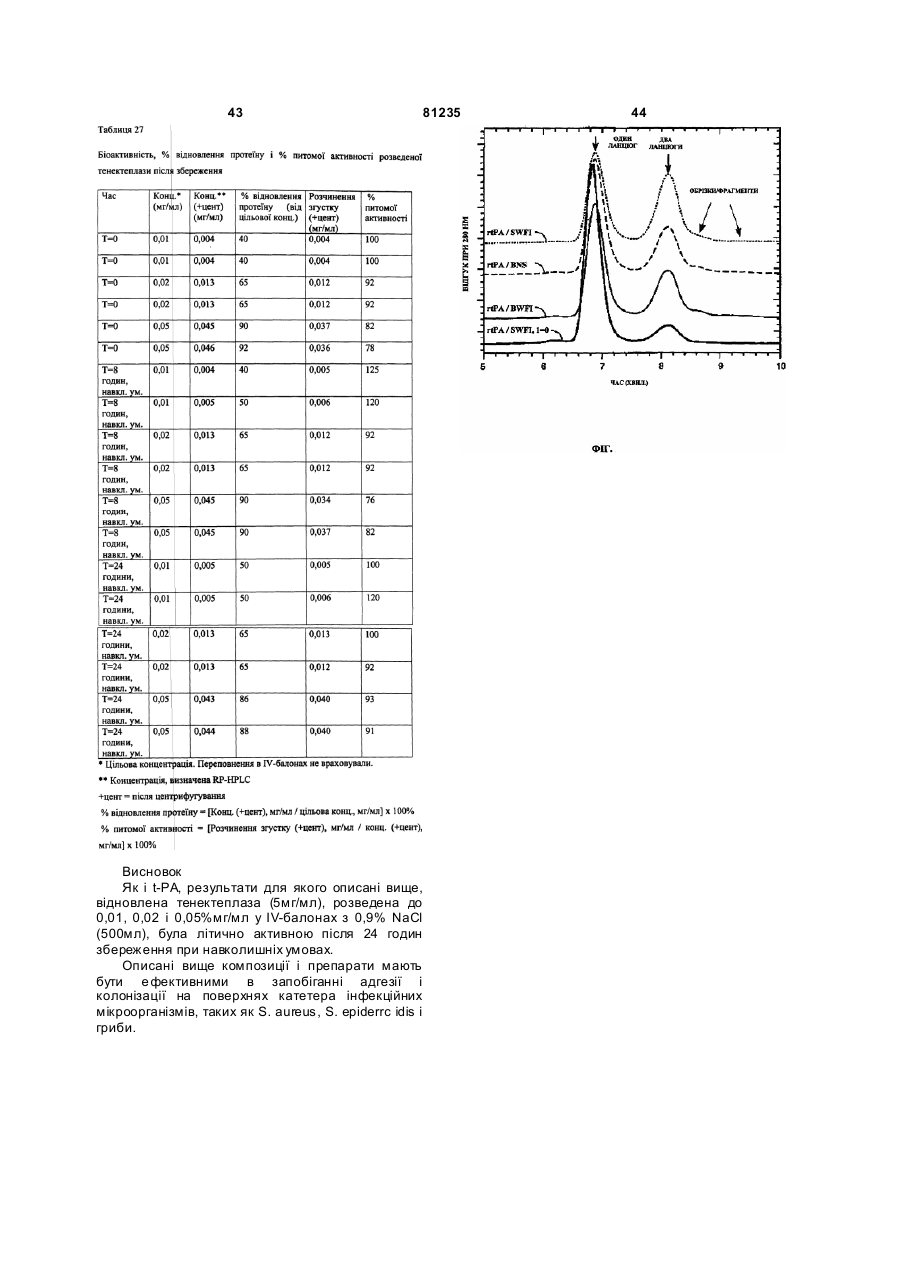
2 (19) 1 3 будь-яким з пп. 1-9 протягом не менше 5 днів. 11. Спосіб за п. 10, який відрізняється тим, що катетер контактує з композицією протягом 6-15 днів. 12. Катетер, вмочений, просочений і/або імпрегнований композицією за будь-яким з пп. 1-9. 13. Катетер за п. 12, що являє собою постійний катетер. 14. Мультисекційний контейнер, що включає відсік, який містить фібринолітично ефективну кількість активатора плазміногену, відсік, який містить воду, яка містить антисептично ефективну кількість бактеріостатичного органічного спирту, причому відсіки містять виключно нехелатуючі засоби; а також містить інструкції по змішуванню вмісту обо х відсіків і по використанню отриманої суміші для видалення фібрин-зв'язаних згустків крові з катетера, що містить такі згустки крові. 15. Контейнер за п. 14, який відрізняється тим, що активатор плазміногену являє собою тканинний активатор плазміногену або урокіназу. 16. Контейнер за п. 15, який відрізняється тим, що активатор плазміногену являє собою t-PA нативної послідовності, урокіназу нативної послідовності, ретеплазу або тенектеплазу. 17. Контейнер за п. 16, який відрізняється тим, що активатор плазміногену являє собою t-PA нативної послідовності або тенектеплазу. 18. Контейнер за будь-яким з пп. 14-17, який відрізняється тим, що органічний спирт являє собою бензиловий спирт, ізопропанол або етанол. 81235 Даний винахід відноситься до області медичних пристроїв для тривалого введення, зокрема, катетерів, а також до області способів і конструкцій для промивки, закріплення, 4 19. Контейнер за будь-яким з пп. 14-18, який відрізняється тим, що органічний спирт являє собою бензиловий спирт. 20. Контейнер за будь-яким з пп. 14-19, який відрізняється тим, що фібринолітично ефективна кількість активатора плазміногену складає від 0,1 до 10 мг/мл, а антисептично ефективна кількість органічного спирту складає від 0,5 до 1,2 %(об./об.). 21. Контейнер за будь-яким з пп. 14-20, який відрізняється тим, що фібринолітично ефективна кількість активатора плазміногену складає від 0,3 до 4 мг/мл. 22. Контейнер за будь-яким з пп. 14-21, який являє собою комплект, де кожний відсік являє собою окремий контейнер. 23. Контейнер за будь-яким з пп. 14-21, який являє собою шприц з кількома відсіками. 24. Контейнер за будь-яким з пп. 14-23, який відрізняється тим, що вода, яка містить спирт, являє собою бактеріостатичну воду для ін'єкцій або являє собою бактеріостатичний нормальний сольовий розчин. 25. Мультисекційний контейнер, що включає відсік, який містить від 0,1 до 10 мг/мл t-PA нативної послідовності або тенектеплази, і відсік, який містить воду, яка містить від 0,5 до 1,2 % (об./об.) бензилового спирту, ізопропанолу або етанолу, причому відсіки містять виключно нехелатуючі засоби; а також містить інструкції по змішуванню вмісту обох відсіків і по використанню отриманої суміші для видалення фібрин-зв'язаних згустків крові з катетера, що містить такі згустки крові. заправляння і нанесення покриття на ці медичні пристрої. Винахід також відноситься до фармацевтичних препаратів, що застосовуються для збільшення потоку в катетері і запобігання 5 81235 6 виникненню інфекції в катетерах, які схильні до вплинути на поверхневі характеристики пристрою. фібринових відкладень або містять згустки на Труднощі, що виникають при забезпеченні основі фібрину. ефективного антибактеріального захисту, Системи доставки широко використовуються в посилюються розвитком патогенів, що мають медицині в якості пристроїв для введення рідких стійкість до ліків. речовин, які можуть включати лікарські або У наш час стандартний догляд за поживні речовини, або інші активні речовини, в васкулярними катетерами включає промивку певну ділянку організму пацієнта. Такі системи порожнини катетера антикоагулянтом, таким як часто включають використання катетерів, які в гепарин, для запобігання коагуляції крові багатьох випадках вводять хірургічним шляхом всередині і навколо наконечника катетера і або внутрішньовенно і вшивають для тривалого створення перешкод потоку рідин через катетер. застосування бажаної речовини. Типові системи Крім того, гепарин не має антибактеріальної дії і, включають центральні катетери, які можуть бути до того ж, при недостатньому контролі, він може використані для загального парентерального завести антикоагуляційний процес дуже далеко, харчування (TPN), що використовується, створивши небезпеку кровотечі. Гепарин також наприклад, при синдромі укороченої товстої кишки може призвести до утворення антитіл, що (для продовження життя), з ризиком сепсису або викликають серйозний розлад, що називається ендокардиту. Такі системи також включають гепарин-індукованою тромбоцитопенією (HIT), яка катетери і дренажі, що використовуються в виснажує тромбоцити і додатково збільшує перитонеальному діалізі у пацієнтів з небезпеку кровотечі. Таким чином, інфекції і термінальною нирковою недостатністю, яка у разі тромбозна закупорка як і раніше становлять інфікування може призвести до перитоніту з поширену проблему, незважаючи на серйозними наслідками. профілактичне використання гепаринових Інтраваскулярні катетери відносяться до промивок. Необхідне пильне вивчення патогенезу і найбільш поширених медичних пристроїв. Такі мікробіології інфекцій, зумовлених центральними катетери за допомогою стандартних операцій венозними катетерами, для ефективного усунення поміщають у васкулярну систему пацієнта для цієї проблеми. різних процедур і часто залишають на місці Staphylococcus epidermidis та S. aureus протягом тривалого часу. Один з типів систем спричиняють 75% інфекцій, зумовлених доставки, що використовуються протягом центральними венозними катетерами (CVC). Види декількох років при лікуванні різних розладів у Candida спричиняють ще 10-15% таких інфекцій. людей, включає резервуар або камеру малого Було виявлено, що використання об'єму, що імплантується підшкірно під фасцію з антистафілококових антибіотиків для запобігання прямим доступом через катетер до цим інфекціям знижує CVC-зумовлені бактерійні кардіоваскулярної системи. Такі системи відомі як інфекції, але тільки за рахунок збільшення ступеня системи портів. Оскільки порт і інтраваскулярний грибкових (Candida) інфекцій. катетер є прямими шляхами з навколишнього Спостерігається також кореляція між середовища в кровообіг пацієнта, присутність тромбоутворенням та інфікуванням. По суті, катетера або порту створює значний і постійний фібринова оболонка, що поступово покриває потенціал для попадання мікроорганізмів в внутрішню і зовнішню поверхні катетера, поглинає кровообіг пацієнта. постійні васкулярні катетери. Ця фібринова В наш час загальновизнаним є те, що таке оболонка розвиває такі організми, як Staphylococci використання постійних катетерів у терапевтичних, і Candida з підвищеною здібністю адгезії до хірургічни х, гінекологічних, урологічних і інших поверхні катетера. На відміну від цих мікробних пацієнтів може призвести до серйозного видів, грамнегативні бацили не показують інфікування сечостатевих шляхів. Практикуючі істотного зчеплення з фібрином і фібронектином. лікарі розробили безліч методик, що стосуються Таким чином, склад, що зупиняє утворення введення, використання, прикріплення і видалення фібрину, був би особливо корисний для пристроїв рідинного регулювання і інших операцій, запобігання колонізації Staphylococci, Candida і т.п. що проводяться з катетерами. Майже всі ці на ділянках постійних катетерів. операції мають на меті запобігання проникнення Після введення лікарського препарату в мікроорганізмів в кровообіг пацієнта. організм пацієнта через катетер лікар звичайно Було розроблено ряд методик для зниження здійснює введення промивального розчину, який ризику інфікування, які використовують в може включати антикоагулянт, такий як гепарин. медичних пристроях антибактеріальні засоби, але Промивальний розчин повинен витіснити жодна з них не показала повністю задовільних лікарський препарат з катетера таким чином, щоб результатів в клінічних випробуваннях. Ці пристрої забезпечити доставку всієї дози, і залишитися в переважно забезпечують ефективні рівні деякій кількості в катетері, щоб кров пацієнта не антибактеріального засобу протягом всього проходила в катетер і не утворювала згусток, який періоду використання пристрою. Подібне може засмітити отвір катетера. Таким чином, коли уповільнене вивільнення може бути таким, якого катетер знадобиться наступного разу, добре важко досягти, оскільки може бути потрібен промитий катетер буде повністю вільним і готовим спеціальний механізм розподілу для чергового використання. антибактеріального засобу протягом тривалого [Root et al., Antimicrob. Agents Chemother.. 32: періоду часу, і введення достатніх кількостей 1627-1631 (1988)] опублікували дослідження дії в антибактеріального засобу може негативно катетерах динатрій-етилендіамінтетраоцтової 7 81235 8 кислоти (ЕДТА), сполуки, що є добре відомою солі для запобігання інфекції і коагуляції крові своїми хелатуючими властивостями in vivo і що всередині або поблизу медичного протезного широко використовується в якості антикоагулянту пристрою після введення цього пристрою в тіло in vitro. У [патенті США №5,363,754] описане пацієнта. У [ЕР 1,040,841] описане запобігання застосування фармацевтичних композицій суміші тромбозу і/або бактерійному зростанню на міноцикліну і ЕДТА для підтримки порту катетера контактуючій з рідиною поверхні системи доставки порожнім. У [патенті США №5,091,442] описані шляхом контактування цієї поверхні з рідиною, що трубчасті вироби, такі як презервативи і катетери з запобігає тромбозу, яка містить антикоагулянт протимікробними властивостями, зумовлені тауролідин і/або таурултам. У [ЕР 882,461] введенням в них неіонного слаборозчинного описаний медичний пристрій, що має як протимікробного препарату, такого як триклозан. фізіологічну, так і протимікробну активність, який Цей протимікробний препарат може бути включає основний матеріал і плівкове покриття із розподілений у всьому виробі або в його покритті. зшитого полімеру, утворене на поверхні основного У [патенті США №5,362,754] описаний матеріалу, при цьому і фізіологічно активна фармацевтичний препарат, що включає речовина, і протимікробна речовина пов'язані з міноциклін і ЕДТА для підтримки катетера вільним. плівкою покриття. У [патенті США №5,362,754] описане використання У [публікації Boorgu et al., ASAIO J., 46 (6): 767суміші міноцикліну і ЕДТА (М-ЕДТА) для підтримки 770 (Nov. 2000)] описана додаткова порту катетера вільним. антибіотична/антикоагулянтна блокуюча терапія У [роботі Purchase et al., Nephron, 58: 119-20 при лікуванні бактеріємії, пов'язаної з (1991)] для цієї мети описано використання використанням пристроїв доступу, що кальцієвих комплексонів, включаючи цитрат. У імплантуються підшкірно для гемодіалізу. До [роботі Butuovic et al., Artif. Organs. 22: 945-7 пристрою прикріпляють два катетери, які (1998)] показано, що цитрат і полігелін, що є імплантують у верхню порожнисту вен у або праве замінником плазми, який отримують з кісток передсердя. Антибіотична/антикоагулянтна крупної рогатої худоби, мають однакову блокуюча терапія включає вливання антибіотика і ефективність з гепарином в підтримці катетера антикоагулянту в пристрій. [Див. також Schwartz et вільним. У лекції на 30-му щорічному засіданні al., Journal of Clinical Oncology.. 8(9):1591-1597 Американського Нефрологічного Товариства, що (1990) і Kamal et al., JAΜΑ, 265(18):2364-2368 відбулося 2-5 листопада 1997 в Антоніо, Техас, (1991)]. Sodemann et al. повідомили, що видалення [Wiernikowski et al., Am J. Pediatr Hematol катетерів через інфекцію можна уникнути завдяки Oncol. 11(2): 137-140 (1991)] показують, що постійному застосуванню концентрованої суміші бактеріостатичні промивальні сольові розчини гентаміцина/цитрата. ефективніше запобігають інфекції катетера, ніж Однак один з цитратних кальцієвих звичайний сольовий розчин. [Vercaigne et al., комплексонів для діалізних катетерів, під маркою Pharmacotherapy. 20: 394-9 (2000)] оцінювали гепарин в поєднанні з антибіотиками як блокуючий TRICITRASOLÔ , має певні недоліки. Деякі пацієнти скаржаться на короткочасну втрату розчин для запобігання інфекції. У [роботі Patel et al., Thromb Hemost. 82: 1205-6 (1999)] описане смакових відчуттів відразу після ін'єкції цитрату. Є успішне використання слабкодозованого r-гирудіна недавнє повідомлення FDA (Управління по для рецидивного тромбозу діалізного катетера у санітарному нагляду за якістю харчових продуктів і пацієнта з гепарин-індукованою медикаментів, США) про випадок смерті пацієнта незабаром після ін'єкції цитрату для блокування тромбоцитопенією. [Darouiche et al., Nutrition. 11(4) (suppl): 26S-29S (1997)] повідомляють, що катетера [Stas et al., Nephrol Dial Transplant. 1£: запобігання васкулярної катетер-зумовленої 1521-1522 (2001)]; FDA випустило попередження інфекції може бути забезпечене шляхом по застосуванню антикоагулянту triCitrasol використання протимікробних засобів, що (торгова марка) для діалізних катетерів. FDA Talk Paper T00-16,14 April 2000. включають застосування місцевих дезінфектантів, таких як хлоргексидін, використання насичених У [патенті США №5,019,096] описані стійкі до сріблом підшкірних манжет (для CVC інфекції медичні пристрої, що включають короткочасного використання), промивку катетерів синергічну комбінацію солі срібла (наприклад, комбінацією протимікробних і протитромбозних сульфадіазину срібла) і хлоргексидіну. У [патенті США №5,772,640] описані полімерні медичні засобів і нанесення на катетери покриття з антисептичних (хлоргексидін і сульфадіазин вироби, що включають антибактеріальні засоби, срібла) або протимікробних засобів (міноциклін і хлоргексидін і триклозан. У [патенті США ріфампін). №5,362,754] описане запобігання утворенню Антибактеріальні блокуючі розчини глікокаліксу на катетері за рахунок нанесення покриття з ЕДТА і/або міноцикліну, що запобігає використовуються для очищення катетерів. Наприклад, в [патенті США №6,174,537] описанo бактерійним і грибковим інфекціям. У [патенті США промивальний розчин для катетерів. [Див. також №6,258,797] описаний спосіб запобігання інфекції Sodermann et al. Blood Purif.. 12: 251-254 (2001) або сепсису в системах катетерів і портів шляхом використання протимікробного блокуючого відносно DIALOCKÔ і CLS; the TUBEXÔ Heparin розчину та уролідина або таурултама. Lock Flush Solution (Wyeth-Ayerst); і Henrickson et У [патенті США №6,166,007] описані al., J. Clin Oncol.. IS: 1269-1278 (2000)] про протимікробні блокуючі речовини, що включають запобігання CVC-зумовлених інфекцій і похідні тауринаміду і карбонові кислоти і/або їх тромботичних явищ з використанням 9 81235 10 ванкоміцин/ципрофлоксацин/гепаринового засобу, з неглікопептидним протимікробним промивального розчину. засобом, таким як тетрациклінові антибіотики, для CVC з м'якою манжетою, що імплантуються, утворення покриття медичного пристрою і інгібування інфекції катетера. Переважні комбінації такі як QUINTON PERMCATHÔ CVC (Quinton включають міноциклін або інший неглікопептидний Instrument Co., Seattle, WA), все частіше протимікробний препарат разом з ЕДТА, ЕГТА, використовуються у пацієнтів з нирковою ДТПА, ТТГ, гепарином і/або гірудином в недостатністю в термінальній стадії, як засіб постійного доступу. Головними обмеженнями їх фармацевтично прийнятному розріджувачі. У [патенті США №6,187,768] також описане застосування, крім інфекцій, є тромбоз і використання протимікробного засобу і неадекватний кровоток. Для запобігання цим антикоагулянту, антитромботичного засобу або ускладненням звичайно використовують гепарин хелатуючого засобу для підтримки вільними для заправляння центральних венозних катетерів постійних медичних пристроїв, таких як катетери, і QUINTON PERMC ATHÔ між сеансами діалізу. для запобігання інфекціям, викликаним [Schenk et al., Amer. J. Kidney Diseases. 35: 130зростанням бактерій в катетерах. 136 (Jan. 2000)] показали, що рекомбінантний Незважаючи на вищеописані досягнення, існує тканинний активатор плазміногену (rt-PA) виявився необхідність в нетоксичному способі видалення краще за гепарин для заправляння QUINTON фібрин-зв'язаних кров'яних згустків з катетерів, PERMCATHÔ між сеансами діалізу. Однак Schenk зокрема, постійних медичних пристроїв. Також et al. використали 2мг альтеплази в поєднанні з існує необхідність в запобіганні утворення і SWFI (стерильна вода для ін'єкцій, фармакопея видалення фібрину з таких пристроїв, оскільки США), що не запобігало зростанню бактерій. певні бактерії містять ділянки скріплення, зокрема, Закупорка або блокування центральних схильні до зчеплення з фібрином. венозних пристроїв доступу (CVAD) внаслідок Даний винахід відноситься до розчинів, утворення кров'яного згустку (тромбу) всередині унікальних по своїй здатності задовольняти або у наконечнику катетера CVAD являють собою вищеописані вимоги, не заснованих на поширену проблему, яка може перешкоджати антикоагуляціонної, протитромботичної або застосуванню такого виду терапії у пацієнтів. хелатуючої дії і без використання антибіотиків, до Оцінки показують, що закупорюються 25% CVAD, яких ссавці можуть розвивати стійкість. Даний при цьому найбільш поширена етіологія включає винахід вирішує проблеми, викладені вище, тромбоз [Наіге et al., Thromb. Haemost 72: 543-547 шляхом використання активатора плазміногену в (1994); Rubin, J. Clin. Oncol.. 1: 572-573 (1983); поєднанні з дезінфектантом, що використовується Lokich et al., J. Clin. Oncol.. 2: 710-717 (1985)]. В в якості консерванту, в основному, органічному 1994 році Наіге et al., вище, провели двічі сліпе, спирту, що має цю здатність. Отримана перспективне, рандомізоване випробування композиція не тільки має фібринолітичну урокінази в порівнянні з альтеплазою (t-PA) в активність, але і запобігає зростанню патогенів, дисфункціональних катетерах, які за даними зокрема, в закупорених катетерах, і відповідає рентгенографії виявилися закупореними тромбом. стандартам USP (фармакопея США). Катетери обробляли 2мг альтеплази або 10000Од. Область винаходу викладена в формулі урокінази, які залишали в пристрої на 2 години. винаходу. Зокрема, в першому аспекті даний Після 1-2 обробок альтеплаза відновлювала винахід відноситься до композиції, що функцію більшої кількості катетерів, ніж урокіназа застосовується для видалення фібрин-зв'язаних (89% проти 59% (р=0,013)). згустків крові з катетера, який містить воду, 4 вересня 2001р. Управління США по фібринолітично ефективну кількість активатора санітарному нагляду за якістю харчових продуктів і плазміногену і антисептично ефективну кількість медикаментів (FDA) схвалило тромболітичний бактеріостатичного органічного спирту, при цьому засіб CATHFLOÔ ACTIVASEÒ (альтеплаза) t-PA композиція не включає хелатуючий засіб. для відновлення функції CVAD, що оцінюється за Ò У наступному аспекті винахід відноситься до здатністю відбирати кров. CATHFLOÔ ACTIVASE комплекту, що складається з кількох відсіків, t-PA випускається в 2-мг одноразових ампулах, є включаючи, відсік, який містить фібринолітично єдиним тромболітичним препаратом, що серійно ефективну кількість активатора плазміногену, випускається, який застосовується для цієї мети, і відсік, який містить воду, що включає пропонує медичним працівникам розумний спосіб антисептично ефективну кількість обробки при ускладненнях CVAD, які можуть бактеріостатичного органічного спирту, при цьому ускладнювати догляд за пацієнтом. Одна ампула жоден із відсіків не містить хелатуючо го засобу, і CATHFLOÔ t-PA містить 2,2мг альтеплази, 77мг Lінструкції по змішуванню вмісту обох відсіків і по аргінину, 0,2мг емульгатору POLYSORBATE 80Ô і використанню отриманої суміші для видалення фосфорну кислоту для створення рН ~7,3. фібрин-зв'язаних згустків крові з катетера, що Т-РА зв'язували з іншими матеріалами, містить такі згустки крові. відмінними від васкулярних катетерів. [Див., У наступному аспекті винахід відноситься до наприклад, Zhou et al., J. Control Release. 55: 281комплекту, що складається з кількох відсіків, 295 (1998); Greco et al., Ann Vase. Surg. 9: 140-145 включаючи відсік, який містить від ~0,1 до (1995) і Woodhouse et al., Biomaterials. 17: 75-77 ~10мг/мл t-PA нативної послідовності або (1996)]. тенектеплази і відсік, який містить воду, що У [патенті США №5,688,516] описане включає від ~0,5 до ~1,2% (об./об.) бензилового використання вибраних комбінацій хелатуючого спирту, ізопропанолу або етанолу, при цьому засобу, антикоагулянту, або антитромботичного 11 81235 12 жоден з відсіків не містить хелатуючого засобу, і Вираз "препарат" або "композиція" тут інструкції по змішуванню вмісту обох відсіків і по відноситься до композиції, розчину, складу і т.п., використанню отриманої суміші для видалення що являє собою суміш інгредієнтів, описаних фібрин-зв'язаних згустків крові з катетера, що вище. містить такі згустки крові. Вираз "контакт", "контактування" і т.п. Переважна кількість бензилового спирту, що є означають вплив на реагент будь-яким способом, тут переважним спиртом, складає біля 0,8-1,1%. наприклад, шляхом покриття, інкубування і т.д. Цей діапазон і більш широкий діапазон 0,5-1,2% Вираз "покриття", "покритий" і т.д. тут достатній для інгібування зростання мікробів, але відносяться до вмочення, просочення і/або зберігає стабільність і функцію активатора імпрегнування катетеру композицією, описаною плазміногену. Перевага цих спиртів полягає в тут. тому, що вони не приводять до розвитку стійкості Вираз "бактеріостатичний органічний спирт" до антибіотиків. означає органічний спирт, що є дезінфектантом, У наступному варіанті здійснення винахід що використовується як антисептик, і не відноситься до способу видалення фібринкласифікується як антибіотик або такий, що зв'язаних згустків крові з катетера, що містить такі відноситься до класу антибіотиків. Дезінфектанти, згустки крові, що включає контактування катетера що є хімічними препаратами, які iнгібують або з вищеописаною композицією щонайменше вбивають мікроорганізми, визначені в [Basic and протягом 5 днів. Clinical Pharmacology. 8th edition (2001), Section VII. У наступному варіанті здійснення винахід Chemotherapeutic Drags. Chapter 50. Miscellaneous відноситься до катетера, покритого вищеописаною Antimicrobial Agents - Disinfectants, Antiseptics, and композицією. Sterilants]. Консерванти, являють собою хімічні Фіг. показує обрізані хроматограми SEC для препарати, що використовуються для запобігання розведених зразків rt-PA (1мг/мл в BWFI, BNS і псування препаратів мікробами. Дезінфектанти SWFI) після 14 днів зберігання при 37°3 в скляних використовуються як антисептики для запобігання пробірках. надмірного зростання бактерій і грибків в Визначення фармацевтичних препаратах. Вони повинні бути У даному описі вираз "катетер" відноситься до ефективними в запобіганні зростання медичного пристрою, що звичайно виготовляється мікроорганізмів, які можуть в них міститися, і з конструкційних полімерів, таких як поліуретан, повинні мати достатню розчинність і стабільність, силікон або інші подібні полімери медичного щоб залишатися активними, як описано в призначення для доставки ліків і відбору крові. Такі [Ellenhorn's Medical Toxicology 2nd Ed (1997), катетери включають широку різноманітність Section IV. Chemicals. Chapter 57. Antiseptics and постійних медичних пристроїв, таких як сечовий Disinfectants]. Приклади таких органічних спиртівкатетер, васкулярний катетер, зокрема, CVC або антисептиків включають етанол, ізопропанол і периферичний внутрішньовенний катетер, бензиловий спирт, що є тут переважними, при артеріальний катетер, трахеальний катетер, цьому бензиловий спирт найбільш переважний. катетер Свана-Ганза, гемодіалізний катетер, Бензиловий спирт, що є гідрофобним, може пупковий катетер, підшкірний нетунельований руйнува ти стінки кліток і мембрани силіконовий катетер, тунельований центральний мікроорганізмів, денатурувати білки і інактивува ти венозний катетер з манжетою, підшкірний ферменти. центральний венозний порт і т.п. Вираз "бактеріостатична вода для ін'єкцій" або Вираз "васкулярний катетер" відноситься до "BWFI" відноситься до суміші води і змінних катетера, що вводиться у васкулярну систему, і кількостей бензилового спирту, а також до води, включає периферичні катетери і CVC, пристрої з що не містить інших інгредієнтів, по визначенню манжетами для тривалого застосування і фармакопеї США (USP). короткострокового застосування, пристрої без Вираз "стерильна вода для ін'єкцій" або манжет і порти, що імплантуються. CVC, або "SWFI" тут означає тільки стерильну воду без центральні венозні пристрої доступу (CVAD), інших інгредієнтів. включають центральні катетери, що вводяться Вираз "нормальний сольовий розчин" або "NS" периферично (лінії РІСС), зовнішні пристрої з тут означає суміш води з відповідною кількістю манжетами, катетери без манжет, нетунельовані і (наприклад, 0,9% (вага/об.)) хлориду натрію, без підшкірно нетунельовані катетери, гемодіалізні інших інгредієнтів. (HD) катетери і порти. Вираз "бактеріостатичний нормальний Переважними катетерами в даному винаході є сольовий розчин" або "BNS" тут відноситься до постійні катетери, такі як CVC, переважно стерильної води з відповідною кількістю тунельований CVC з манжетою, периферичний (наприклад, 0,9% (вага./об.)) хлориду натрію і з внутрішньовенний катетер, артеріальний катетер, відповідною кількістю (тобто, антисептично катетер Свана-Ганза, гемодіалізний катетер, ефективним) бактеріостатичного органічного пупковий катетер, підшкірний нетунельований спирту, такого як бензиловий спирт, без інших силіконовий катетер або підшкірний центральний інгредієнтів. венозний порт. Також переважним є сечовий Вираз "активатор плазміногену" тут означає катетер або перитонеальний катетер. Крім того, фібринолітичний одно- або двухланцюговий переважними є внутрішньовенний катетер, активатор плазміногену, включаючи активатор зокрема, виготовлений з біомедичного поліуретану сечового плазміногену в нативній або варіантній або силікону, або васкулярний катетер. формі, тканинний активатор плазміногену в 13 81235 14 нативній формі, такій як альтеплаза t-PA від ~4,5 до 6,5. Композиція звичайно має фізіологічний рівень рН. Якщо необхідно, рН може ACTTVASEÒ , або у варіантній формі, такій як r-ΡΑ бути відрегульована доданням кислоти або (ретеплаза; RETAVASEÒ , Centocor, Inc.) і основи, наприклад, мінеральної кислоти, такої як тенектеплаза (інваріант t-PA, який позначається соляна кислота, або, переважно, кислоти, що не T103N, N117Q, К296А, Н297А, R298A, R299A, що викликає ацидоз, такий як оцтова, яблучна або випускається під маркою TNKASEÔ компанією молочна кислота. Інші способи регулювання рН, Genentech, Inc. і описаний, наприклад, в [патенті відомі фахівцям, також можуть бути використані. США №5,612,029]), а також урокіназа (наприклад, Ò Тест для з'я сування, чи є кількість активатора ABBOKINASE ; Abbott), яка може являти собою плазміногену в композиції фібринолітично існуючу в природі нативну молекулу або варіант ефективною, може бути проведений, наприклад, урокінази, що має фібринолітичну функцію для шляхом in vitro аналізу розчинення згустку, розчинення згустків в кров і запобігання наприклад, як описано нижче в Прикладах. накопичення і видалення фібрину. Переважно, Антисептично ефективна кількість спирту активатор плазміногену являє собою t-PA нативної може бути визначена, наприклад, шляхом тесту на послідовності, фібринолітичний варіант t-PA, протимікробну ефективність, викладеного нижче в урокіназу нативної послідовності або Прикладах. Переважно, кількість активатора фібринолітичний варіант урокінази. Більш плазміногену складає біля 0,1-10мг/мл, а переважно, активатор плазміногену являє собою tантисептично ефективна кількість органічного PA нативної послідовності, фібринолітичний спирту переважно складає біля 0,5-1,2% (об./об.). варіант t-PA або урокіназу нативної послідовності. Більш переважно, фібринолітично ефективну Ще більш переважно, активатор плазміногену кількість активатора плазміногену складає біля являє собою t-PA нативної послідовності або 0,3-5 мг/мл, ще більш переважно біля 0,5-4мг/мл, і фібринолітичний варіант t-PA. Ще більш найбільш переважно біля 1-3мг/мл. Найбільш переважно, варіант t-PA являє собою переважна кількість органічного спирту складає тенектеплазу або ретеплазу. Найбільш біля 0,8-1,1% (об./об.). переважно, активатор плазміногену являє собою tКомпозицію по винаходу переважно піддають PA нативної послідовності або тенектеплазу. умовам, в яких будь-які мікроорганізми, що Вираз "хелатуючий засіб" тут означає засіб, містяться в ній стають по суті нежиттєздатними, і що використовується для хелатування, такий як заповнюють нею ємність, що герметизується, таку етілендіамінтетраоцтова кислота (ЕДТА), DMSA як шприц, пробірку із закритою мембраною або (димеркаптосукцинова кислота), дефероксамін, ампулу, по суті стійку до проникнення димеркапрол, цитрат цинку, TRICITR ASOLÔ мікроорганізмів. Переважно, ємність, що (цитратний кальцієвий комплексон), комбінації герметизується містить аліквоту промивального вісмуту і цитрату, пеніциламін, сукцимер або розчину, достатню для виконання однієї етідронат. Інші хелатуючі засоби включають процедури промивки катетера. Для спеціальних етіленгликоль-біс-(бета-аміноетіловий ефір)цілей може бути переважна загальна ємність, що Ν,Ν,Ν',Ν'-тетраоцтову кислоту (EGTA) і містить достатню кількість розчину для дозування діетілентриамінпентаоцтову кислоту (DTPА) і її кількох аліквот, призначених для окремих солі, а також динатрію кальцію едетат, процедур промивки катетера. триетілентетраміну дигідрохлорід і речовини, що Спосіб промивки внутрішньовенного катетера хелатують двовалентні катіони металів, таких як включає приготування змішаного розчину, Са, Mg, Mn, Fe і Zn. описаного вище, і контактування катетера з таким Моделі здійснення винаходу розчином щонайменше протягом двох годин. Даний винахід відноситься до композицій, що Спосіб включає заповнення маніпуляційного використовуються для видалення фібринрідинного пристрою, переважно шприца, зв'язаних згустків крові з катетера, який містять аліквотою розчину, достатньої для виконання воду, фібринолітично ефективну кількість процедури промивки катетера. Переважна активатора плазміногену і антисептично кількість для промивальної процедури звичайно ефективну кількість бактеріостатичного складає від 1 до 3мл. Потім виконавець фіксує органічного спирту. Композиція не містить шприц в цільовому інтраваскулярному катетері, хелатуючого засобу. що вимагає промивки, і вводить розчин в катетер, Вода переважно містить, по-перше, таким чином виконуючи процедуру промивки. бактеріостатичний органічний спирт. Існує чотири Описаний спосіб може бути використаний для основні типи розріджувачів, що використовуються видалення наявних згустків крові практично з для розбавлення або розведення лікарських будь-якого тунельованого або нетунельованого препаратів: BWFI, SWFI, BNS і NS. Даний винахід катетера. Як частина режиму обслуго вування включає тільки бактеріостатичні розріджувачі, катетера, промивка катетера найбільш переважно тобто, BWFI і BNS. Переважно, вода, що містить повинна виконуватися з використанням композиції, спирт, являє собою бактеріостатичну воду для описаної тут, наприклад, раз в тиждень, один раз в ін'єкцій або бактеріостатичний нормальний 4 дні, один раз кожні два дні, раз в день сольовий розчин. (приблизно кожні 24 години), два рази в день, рН композиції, що описується тут, повинна кожні чотири години або з потреби, відповідно до бути придатною для біологічного використання. потреб пацієнта, відомих досвідченому Звичайно композиція або розчин по даному практикуючому лікареві. Режим промивки катетера винаходу має рН в діапазоні від ~3 до 7, може просто перебувати в одній промивці при переважно від ~3,5 до 6,5 і найбільш переважно 15 81235 16 кожній зміні катетера. У переважному варіанті потім розводять водою для отримання зручного здійснення способу катетер повинен промиватися для використання розчину. Комплект може частіше, з 4-часовими інтервалами, композицією, включати додатковий контейнер, адаптований для описаною тут. прийняття вмісту двох відсіків. Пакет, описаний Хоч спосіб по винаходу відноситься до тут, може являти собою комплект, в якому кожний введення композиції в катетери, вже встановлені відсік є окремим контейнером, таким як пробірка на цільовій ділянки, досвідченим фахівцям буде або ампула, або пакет може являти собою шприц зрозуміло, що контактування або покриття з кількома відсіками. катетера композицією поза тілом пацієнта може Різні особливості і аспекти винаходу запобігти відкладенню фібрину на такій поверхні додатково представлені в прикладах, описаних після імплантації катетера і скоротити ділянки нижче. Оскільки ці приклади приведені лише для бактерійного зростання. Таким чином, поверхні ілюстрації використання винаходу в межах його катетерів, наприклад, гемодіалізних катетерів, області, вони не повинні розглядатися як можуть бути заздалегідь оброблені композицією, обмежуючі область винаходу. Всі приведені тут що описується тут. Катетер може бути оброблений літературні джерела включені в дану заявку у композицією заздалегідь, а після введення може вигляді посилань. зазнавати періодичних промивок. Приклад 1 (Порівняльний) Приватні приклади катетерів, які можуть бути Короткий опис виготовлені і покриті композицією по винаходу, Тест, описаний нижче, проводили для оцінки перелічені вище. У способі покриття активатор протимікробних властивостей 2мг/мл t-PA плазміногену, вода і спирт використовуються в ACTIVASEÒ, розведеного в SWFI. Цей зразок таких кількостях, щоб їх комбінація в обробленому показав невідповідність вимогам тесту на виробі мала істотну фібринолітичну і антисептичну протимікробну ефективність USP. активність. В одному з варіантів здійснення Тест на протимікробну ефективність USP катетер являє собою поліуретановий або Цей тест використовують для оцінки силіконовий катетер (або виготовлений з подібних ефективності антисептика в препараті або для полімерів), оброблений (тобто, шляхом вмочення оцінки власної протимікробної здатності активного або просочення) просочувальним розчином, інгредієнту. Цей тест описаний в [USP 24, описаним вище. Потім поверхню катетера, що "Microbiological Tests/(51) Antimicrobial представляє інтерес, піддають впливу композиції Effectiveness Testing, стор.1809-1811]. протягом періоду часу, достатнього для утворення А. Матеріали і основне обладнання композицією плівки або покриття на контактуючій з 1. Пробні мікроорганізми включали Escherichia нею поверхні пристрою. Оскільки композиція являє coli, ATCC 8739, Pseudomonas aeruginosa, ATCC собою рідину, вона повинна висохти на поверхні 9027, Staphylococcus aureus, ATCC 6538, Candida пристрою протягом достатнього часу для albicans, ATCC 10231, i Aspergillusniger, ATCC утворення плівки. 16404. Кількість описаної тут композиції, що 2. Середовища, добавки і основне обладнання вводиться в катетер, має вистачати для його включали: заповнення. Такі пристрої, якщо вони є Соєво-триптиказний агар (TSA) гемодіалізними катетерами, звичайно мають Декстрозний агар Сабуро (SDA) внутрішній об'єм в діапазоні від ~0,1 до ~10мл. Ці Сольовий розчин, буферізований фосфатом цифри, безумовно, будуть варіюватися в (PBS), стерильний, рН 7,2±0,2 залежності від довжини і діаметру трубки Тільні 50-мл конічні пробірки пристрою, які, серед іншого, можуть залежати від Стерильні тампони і серологічні піпетки розміру тіла пацієнта. Спектрофотометр Якщо з катетера треба видалити фібринЛічильник колоній мікроорганізмів, Quebec або зв'язані згустки крові, катетер може контактувати з еквівалентний розчином, описаним тут, протягом щонайменше 5 Термостати при 2-8°С, 22,5±2,5°С, і 32,5±2,5°С днів, переважно біля 6-15 днів. В. Методика У наступному варіанті здійснення винахід 1. Отримання інокуляту: відноситься до комплекту або пакету. У одному з Готували суспензію кожного мікроорганізму варіантів, комплект або пакет включає для отримання приблизної концентрації 1´108 контейнерний пристрій, такий як шприц з колоніеутворюючих одиниць (CFU)/мл. Кожну з відсіками, що включає щонайменше два окремих п'яти конічних пробірок, що містять 10мл зразку, відсіки. Один відсік або контейнер містить інокулювали 0,05мл одного з пробних фібринолітично ефективну кількість активатора мікроорганізмів з отриманням вихідної плазміногену, такого як t-PA, а другий відсік або концентрації від 1´105CFU/мл до 1´106CFU/мл контейнер містить воду, що включає антисептично тестового препарату. Ви хідну популяцію ефективну кількість бактеріостатичного життєздатних організмів в кожному тестовому органічного спирту. Як і композиція, жоден відсік препараті розраховували на основі концентрації не містить хелатуючого засобу. Пакет також мікроорганізмів в кожному стандартизованому включає інструкції по змішуванню вмісту обох інокуляті методом Pour Plate (глибинного посіву). відсіків і по використанню отриманої суміші для Цей метод являє собою стандартну видалення фібрин-зв'язаних згустків крові з мікробіологічну методику визначення кількості катетера, який містить такі згустки крові. t-PA може мікроорганізмів у тестовому зразку. Тестовий мати форму сухого ліофілізованого порошку, який зразок розбавляють стерильним сольовим 17 81235 18 розчином і відмірюють піпеткою в стерильну чашку виконували в двох примірниках з отриманням Петрі. Потім в чашку Петрі наливають середнього значення для кожного розплавлений агар (поживну середу), змішують із стандартизованого інокуляту. Ви хідну зразком і інкубують при стандартизованій концентрацію кожного пробного мікроорганізму у температурі і часі. Цей метод забезпечує тестовому препараті розраховували з отримання колоній, які формуються у всьому агарі використанням наступного рівняння: - не тільки на поверхні. Біля 10мл зразка залишили неінокульованим в 1 S´ одній конічній пробірці як негативний контрольний P досвід. При Τ = 7 днів, 14 днів і 28 днів популяцію кожного мікроорганізму в інокульованих зразках і в де негативному контрольному досвіді визначали S = середня концентрація мікроорганізму в методом глибинного посіву - підтвердженим стандартизованій суспензії (1,0´108CFU/мл) методом чашкового підрахунку мікроорганізмів. І = об'єм інокуляту (0,05мл) Умови інкубації для методу глибинного посіву Ρ = об'єм тестового препарату (10мл) представлені в Табл. 1. 7. Зберігання зразків і тестові інтервали 2. Перевірка достовірності методу глибинного Інокульовані контейнери і негативний посіву: контрольний досвід інкубували при 22,5±2,5°С із Провели серію розведень зразка 1:10 і 1:100 з захистом від світла. З кожного контейнеру отриманням розбавлених концентрацій. 1-мл відбирали зразки через проміжки часу, вказані в порцію кожної розбавленої концентрації зразка Табл.2. Чашковий підрахунок інокульованих ввели в кожну з 5 чашок Петрі. Для кожної зразків і негативного контрольного досвіду розбавленої концентрації зразка у відповідну проводили методом глибинного посіву. Ча шковий чашку Петрі додали 0,1-мл аліквоти, що містить підрахунок виконували в двох примірниках. біля 1´103CFU/мл кожного пробного Використали умови середовища і інкубації, мікроорганізму. Паралельно той же об'єм представлені в Табл.1. інокуляту кожного мікроорганізму ввели в кожну з двох пластин без розбавлених концентрацій зразка для підтвердження кількості мікроорганізмів. 15-20-мл порції розплавленого Умови інкубації для методу глибинног агару, що підтримується при ~45°С, додали в кожну чашку і обережно перемісили вміст Мікроорганізм Відповідна середа Температура круговими рухами. Чашки залишили для твердіння Е. соlі АТСС 8739 TSA 32,5 і інкубували, як показано в Табл.1. P. aemginosa АТСС 9027 TSA 32,5 3. Приготування зразка S. aureus АТСС 6538 TSA 32,5 10мл зразка ввели в кожну з п'яти пробірок. З. аlbісаns АТСС 10231 SDA 22,5 Кожну пробірку позначили "ЕС", "PA", "SA", "С А" A. niger АТСС 16404 SDA 22,5 або "AN", так щоб для кожного пробного мікроорганізму була призначена одна пробірка. 10мл зразка ввели в одну пробірку, позначену як негативний контрольний досвід. У Час відбору зразків для парентеральних альтернативному варіанті, на етапах введення і маркірування в кожну пробірку вводили 20мл зразка. 0г 6г 4. Визначення біонавантаження По USP (бактерії, дріжджові і плісняві гриби) NA NA З використанням негативного контрольного По ЕР (бактерії) R R досвіду визначали біонавантаження зразка По ЕР (дріжджові і плісняві гриби) R NA методом глибинного посіву. Використали умови середовища і інкубації, представлені в Табл.1. NA = не проводиться 5. Інокуляція зразка R = проводиться 0,05мл кожної суспензії мікроорганізму ЕР - фармакопея Європи інокулювали при 1´108CFU/мл у відповідну пробірку, що містить 10мл зразка. Об'єм С. Критерії відповідності суспензіонного інокуляту становив 0,5% об'єму 1. Для достовірності випробування пробними зразка. Суміш ретельно перемісили шляхом мікроорганізмами концентрація пробних струшування. Кінцева концентрація тестового мікроорганізмів в кожному тестовому препараті препарату склала біля 5,0´105CFU/мл. У складала від 1´105CFU/мл до 1´106CFU/мл. У альтернативному варіанті, якщо в кожній пробірці зразках, випробуваних перевіреним методом був використаний об'єм 20мл зразка, на етапі чашкового підрахунку мікроорганізмів, виявленого інокуляції вводили 0,1мл кожної пробної суспензії. біонавантаження не було. 6. Підтвердження вихідної концентрації 2. Для достовірності методу чашкового Чашковий підрахунок для кожного підрахунку мікроорганізмів середнє підраховане стандартизованого інокуляту (1,0´108CFU/мл) значення здобутого інокуляту при кожному рівні виконували методом глибинного посіву. розведення повинно бути більше або рівним 50% Використали умови середовища і інкубації, середнього значення для відповідного представлені в Табл.1. Чашковий підрахунок контрольного досвіду. Якщо середнє підраховане 19 81235 20 значення отриманого інокуляту при розведенні глибинного посіву. Середнє значення вилікуваного складає менше ніж 50%, всі підраховані значення інокуляту при розведенні зразка 1:10 було більше при цьому розведенні вважаються або рівно 50% середнього значення відповідного недостовірними. контрольного досвіду (Табл.6). D. Інтерпретація Для P. aeraginosa і S. aureus логарифмічне 1. По USP зниження відносно розрахованої вихідної Для бактерій має спостерігатися зниження по концентрації було більше або дорівнює величині шкалі десятеричного логарифму не менше 1,0 1,3 через 7 днів, менше 3,0 через 14 днів і більше відносно вихідної підрахованої кількості через 7 або дорівнює 3,6 через 28 днів (Табл. 7 і 8). днів, не менше 3,0 відносно вихідної кількості Для дріжджових і пліснявих грибів через 14 днів, а через 28 днів не повинно бути логарифмічне зниження відносно розрахованої збільшення відносно кількості, визначеної через 14 вихідної концентрації було більше або дорівнює днів. 0,6 через 7 днів, більше або дорівнює 1,0 через 14 Для дріжджових і пліснявих грибів не повинно днів і більше або дорівнює 1,6 через 28 днів (Табл. бути збільшення відносно вихідної підрахованої 7 і 8). кількості через 7, 14 і 28 днів. "Відсутність збільшення" означає не більше 0,5 логарифмічних одиниць вище попередньої виміряної величини. 2. По ЕР Розрахункові вихідні концентрації пробних м Критерії оцінки протимікробної активності для парентеральних препаратів представлені в Табл.3 Пробний мікроорганізм Концентрація суспензії (CFU/мл) Розраху у вигляді логарифмічного зниження кількості P. aeruginosa 7,7´107 життєздатних мікроорганізмів відносно величини, Ε. coli 1,2´108 отриманої для інокуляту. S. aureus 3,9´107 С. albicans 7,2´107 Таблиця 3 A. niger 1,2´108 Критерії ЕР для оцінки протимікробної активності для парентеральних препаратів Бактерії Бактерії Гриби Гриби Критерії* А В А В 6г 2 Логарифмічне зниження 24г 7 днів 3 Середовище 1 3 - TSA 2 - SDA 14 Бiонавантаження зразка в методі глибинн днів 28 днів NR Кількість CFU, отримана при розведенні 1:10 Nl Nl 0 1 Nl 0 NR = не отримано Nl = Відсутність збільшення. "Відсутність збільшення" означає не більше 0,3 логарифмічних одиниць Середня кількість отриманого інокуляту в методі вище попередньо виміряної величини. *Критерій А виражає рекомендовану ефективність, яка має бути досягнута. У виправданих випадках, коли критерій А не може бути досягнутим, наприклад,Пробний мікроорганізм Середня кількість CFU Середня кількість через підвищений ризик негативних реакцій, має інокульоване при розве бути задоволений критерій В. P. aeruginosa 65 4 Ε. coli 93 11 Тест з t-PA ACTIVASEÒ і SWFT S. aureus 43 5 А. Матеріали. обладнання і методика С. albicans 84 7 Зразок являв собою 2 г/мл t-PA альтеплазу A. niger 59 4 ACTIVASEÒ в пробірці з SWFI, що не містить бензилового спирту. Пробні мікроорганізми і всі середовища, добавки і основне обладнання відповідали переліченим для попереднього тесту. Методика Мікробна популяція протягом 28 д відповідала методиці, описаній для попереднього тесту, а умови інкубації - приведеним в Табл.1. Вихідна отримана 7 днів (CFU/м Пробний мікроорганізм Критерії відповідності і інтерпретація відповідали кількість (CFU/мл) описаним для попереднього тесту. P. aeruginosa 3,9´105 6,3´103 5 Результати Ε. coli 6,0´10 1,2´105 Розраховані вихідні концентрації пробних 5 S. aureus 2,0´10 9,1´103 мікроорганізмів в кожному тестовому препараті 5 С. albicans 4,6 >4,8 23 81235 24 відповідності і інтерпретація відповідали описаним В одному з пропонованих способів в Прикладі 1. заправлення розчин CATHFLOÔ ACTIVASEÒ Результати (альтеплази), отриманий шляхом розведення Результати були ідентичними наведеним в 2,2мг ліофілізованого порошку 2,2мл 0,9% Табл.4 і Табл.5 для розрахованої вихідної бензилового спирту в стерильної концентрації пробних мікроорганізмів в кожному бактеріостатичній воді для ін'єкцій (концентрація тестовому препараті (від 1´105 до 1´106 CFU/мл) і 1мг/мл) може бути введений усередину для біонавантаження в зразку в методі глибинного васкулярного катетеру в обсязі, рівному посіву (відсутність наявного біонавантаження). заправному обсягу порожнини катетера. Потім Метод чашкового підрахунку мікроорганізмів розчин може бути аспірирован з катетера перед підтверджували з використанням методу використанням катетера в медичних цілях глибинного посіву. Середня кількість отриманого Приклад 4 інокуляту при розведенні зразка 1:10 було більше Короткий опис або рівно 50% середнього значення відповідного Тестування проводили, як описано вище для контрольного досвіду (Табл.12). Для бактерій тесту на протимікробну ефективність, для оцінки логарифмічне зниження відносно розрахованої ефективності 1,0% бензилового спирту в якості вихідної концентрації було більшим 3,3 через 7 антисептику в 2мг/мл t-PA ACTIVASEÒ відповідно днів і більше 4,3 через 14 і через 28 днів (Табл. 10 до вимог USP. Цей зразок показав відповідність і 11). Для дріжджових і пліснявих грибів вимогам тесту USP на протимікробну логарифмічне зниження відносно розрахованої ефективність. вихідної концентрації було більшим або Матеріали, обладнання і методика дорівнювало 3,6 через 7 днів і більше 4,6 через 14 Зразок являв собою ACTIVASEÒ t-PA (2мг/мл) і через 28 днів (Табл. 10 і 11). в пробірці з 1,0% бензилового спирту. Зокрема, роздріджувачем служила стерильна вода з Таблиця 12 додаванням відповідної кількості бензилового спирту до кінцевої концентрації 1,0%. Середня кількість отриманого інокуляту в методімікроорганізми відповідали описаним в Пробні глибинного посіву Прикладі 1. Середня кількість CFU Середня кількість добавки і основне обладнання Середній відсоток Середовища, CFU Пробний мікроорганізм інокульованого отриманого при описаним в 1:10 отримання (%) відповідали розведенні Прикладі 1. P. aeruginosa 65 Методика, що використовується 89 58 відповідала описаної 91 Прикладі 1, а умови інкубації в Ε. coli 93 97 відповідали в Табл.1. S. aureus 43 43 вказаним 100 Критерії відповідності і інтерпретація відповідали описаним С. albicans 84 76 90 в Прикладі 38 1. A. niger 59 65 Результати Результати були ідентичними наведеним 13 Таблиця в Табл.4 і Табл.5 для розрахованої вихідної концентрації пробних мікроорганізмів в кожному Мікробна популяція протягом 28 днів тестовому препараті (від 1´105 до 1´10бCFU/мл) і зразку в Вихідна розрахована 7для біонавантаження в(CFU/мл) методі глибинного Пробний мікроорганізм днів (CFU/мл) 14 днів 28 днів (CFU/мл) посіву (відсутність наявного біонавантаження). кількість (CFU/мл) Метод чашкового
ДивитисяДодаткова інформація
Назва патенту англійськоюCatheter composition and uses thereof
Автори англійськоюSemba Charles P.
Назва патенту російськоюКомпозиция для катетера и ее применение
Автори російськоюСемба Чарлз П.
МПК / Мітки
МПК: A61M 31/00, A61K 38/49, A61M 37/00, A61K 38/00, A61M 21/00, A61K 31/45
Мітки: застосування, композиція, катетера
Код посилання
<a href="https://ua.patents.su/22-81235-kompoziciya-dlya-katetera-ta-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Композиція для катетера та її застосування</a>
Попередній патент: Авіаційний газотурбінний двигун
Наступний патент: Анкерне кріплення
Випадковий патент: Черв'ячна передача