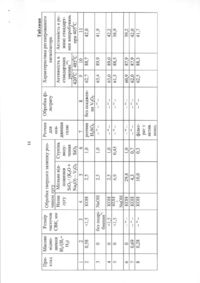
Спосіб одержання n-заміщених 2,6-діалкілморфолінів та застосування каталізатора для одержання третинного аміну
Номер патенту: 75126
Опубліковано: 15.03.2006
Автори: Хулльманн Міхаель, Герлах Тілль, Руб Лотар, Куше Андреас, Кесхаммер Штефан, Хеннінгсен Міхаель
Формула / Реферат
1. Спосіб одержання N-заміщених 2,6-діалкілморфолінів загальної формули І
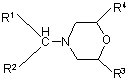 ,(І)
,(І)
у якій
R1 і R2 незалежно один від одного являють собою водень, алкіл або циклоалкіл
або R1 і R2 разом з атомом вуглецю, з яким вони зв'язані, утворюють 5-14-членний карбоцикл, а
R3 і R4 незалежно один від одного являють собою алкіл або циклоалкіл, взаємодією принаймні однієї карбонільної сполуки загальної формули II
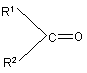 ,(ІІ)
,(ІІ)
у якій R1 і R2 мають вказані вище значення принаймні з одним морфоліном загальної формули III
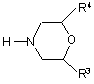 ,(ІІІ)
,(ІІІ)
у якій R3 і R4 мають вказані вище значення у присутності водню і принаймні одного металовмісного каталізатора, який відрізняється тим, що активний компонент каталізатора містить принаймні 50 мас.% металу(ів) платинової групи.
2. Спосіб за п.1, який відрізняється тим, що застосовують каталізатор, активний компонент якого містить від 1 до 100 мас.% Pd, до 60 мас.% Pt та до 50 мас.% принаймні ще одного металу, вибраного з групи, яка включає Ru, Rh, Os, Ir, Се, La та їх суміші.
3. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що застосовують каталізатор на носії.
4. Спосіб за п. 3, який відрізняється тим, що як носій використовують ZrO2.
5. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що застосовують каталізатор, який містить від 0,1 до 10 мас.% Pd і від 0 до 5 мас. % Pt.
6. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що R1 і R2 разом з атомом вуглецю, з яким вони зв'язані, утворюють 6-12-членний карбоцикл, який може містити один, два або три замісники, незалежно один від одного, вибраних із групи, яка включає алкіл, алкоксигрупу, алкілтіогрупу, циклоалкіл і циклоалкілалкіл.
7. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що R3 і R4 незалежно один від одного являють собою С1-С4алкільні групи.
8. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що R3 і R4 незалежно один від одного являють собою метил.
9. Спосіб за будь-яким з попередніх пунктів, який відрізняється тим, що як сполуку загальної формули І використовують N-(циклододецил)-2,6-диметилморфолін.
10. Застосування каталізатора за будь-яким з пп. 1-5 для одержання третинного аміну взаємодією принаймні однієї карбонільної сполуки принаймні з одним вторинним аміном у присутності водню.
Текст
1. Спосіб одержання N-заміщених 2,6діалкілморфолінів загальної формули І C2 2 (19) 1 3 Даний винахід стосується способу одержання N-заміщених 2,6-діалкілморфолінів, який здійснюється взаємодією карбонільної сполуки з вторинним аміном шляхом відновного амінування. Третинні аміни утворюють клас важливих сполук, які знаходять найширше промислове застосування. Тому існує нагальна потреба в розробці гранично простих у здійсненні способів, які дозволяли б одержувати третинні аміни з найбільш доступних компонентів з високим виходом і високою вибірністю відносно потрібної цільової сполуки. З гетероциклічних третинних амінів, наприклад, Nзаміщені тетрагідро-1,4-оксазини (морфоліни) застосовуються для захисту рослин. У [К.Н. König і ін., Angewandte Chemie 77, 1965, стор.327-333], описані N-заміщені тетрагідро-1,4оксазини і їх застосування як фунгіцидних сполук, які мають ефективну дію проти грибів, що уражують культурні рослини. За методикою, запропонованою авторами вищезгаданої публікації, ці сполуки можна одержувати, наприклад, дегідратуючою циклізацією відповідних біс(2-гідроксіетил)амінів. У заявці DE-A 2543279 також описується спосіб одержання N-заміщених тетрагідро-1,4оксазинів, який здійснюється одно- або двостадійною циклізацією і гідруванням N-заміщених біс(2гідроксіалкіл)амінів. Недолік вищевказаного способу полягає в необхідності використовувати вихідні речовини, пов'язані зі значними витратами на їх одержання. У заявці DE-A 19720475 описаний спосіб одержання N-алкіл-2,6-діалкілморфолінів двостадійним синтезом, який передбачає одержання оксазолідину взаємодією відповідних альдегідів або кетонів із двохатомними спиртами вторинних амінів у присутності кислого іоніту і наступне перетворення оксазолідину в присутності водню і каталізатора гідрування. Безпосереднє одержання третинних амінів з карбонільних сполук і особливо з кетонів і вторинних амінів вважається в принципі процесом, пов'язаним з істотними труднощами, оскільки він, як правило, не забезпечує досить високого виходу цільових сполук, для виділення яких потрібні відповідно значні витрати. У заявці DE-A 3321712 описуються похідні 2,6транс-диметилморфоліну і їх застосування як фунгіцидів. За запропонованою у цій заявці методикою N-(циклододецил)-2,6-диметилморфолін (додеморф), наприклад, одержують двостадійним синтезом, який передбачає взаємодію циклододеканону і 2,6-транс-диметилморфоліну в присутності n-толуолсульфонової кислоти з утворенням Nциклододеценіл-2,6-транс-диметилморфоліну і його наступне гідрування в присутності Pd/Cкаталізатора. У заявці ЕР-А 0271750 описані 4-заміщені циклогексиламіни, які мають фунгіцидну дію, одержувати які можна, наприклад, відновним амінуванням циклогексанонів вторинним аміном у присутності відповідного відновника. Як придатні для цих цілей відновники у заявці вказані водень, мурашина кис 75126 4 лота і комплексні гідриди, такі як ціанборогідрид натрію. Каталізатори ж, які можна використовувати при відновному амінуванні в присутності водню, у вказаній заявці не описані. Крім того, цей варіант реакції не підтверджений відповідним прикладом здійснення винаходу. У заявці DE-А 2118283 описується спосіб одержання вторинних або третинних аліфатичних або циклоаліфатичних амінів, який здійснюється взаємодією аліфатичної або циклоаліфатичної карбонільної сполуки з аміаком або первинним, відповідно вторинним аміном у присутності водню і каталізатора гідрування, при цьому як каталізатор використовують суміш срібла і паладію на носії зі спеченого матеріалу. Один з істотних недоліків даного способу полягає у високих витратах, пов'язаних з використанням срібного каталізатора. Крім того, вихід цільових сполук, так само як і вибірність у відношенні цих сполук вимагають безумовного удосконалювання. Виходячи з вищевикладеного, в основу даного винаходу була покладена задача розробити більш ефективний спосіб одержання N-заміщених 2,6діалкілморфолінів. При цьому синтез повинен відбуватися виходячи з карбонільних сполук і вторинних амінів за одностадійним механізмом. Крім цього такий спосіб переважно повинен забезпечити можливість одержання третинних амінів з високим виходом і високою вибірністю відносно до необхідних цільових сполук. При створенні винаходу несподівано було встановлено, що вказану вище задачу вдається вирішити за допомогою способу одержання Nзаміщених 2,6-діалкілморфолінів, який полягає в тому, що принаймні одну карбонільну сполуку піддають взаємодії принаймні з одним похідним морфоліну в присутності водню іпринаймні одного металовмісного каталізатора, активний компонент якого складається в основному з металів платинової групи, шляхом відновного амінування. Об'єктом винаходу відповідно до цього є спосіб одержання N-заміщених 2,6-діалкілморфолінів загальної формули І у якій R1 і R2 незалежно один від одного являють собою водень, алкіл або циклоалкіл або R1 і R2 разом з атомом вуглецю, з яким вони зв'язані, утворюють 5-14-членний карбоцикл, а 3 4 R і R незалежно один від одного являють собою алкіл або циклоалкіл, взаємодією принаймні однієї карбонільної сполуки загальної формули II 5 75126 6 піримідиніл або піразиніл. у якій R1 і R2 мають вказані вище значення, Заміщені гетероарильні групи містять перевапринаймні з одним морфоліном загальної формужно 1, 2 або 3 замісники, вибраних із групи, яка ли III включає алкіл, алкоксигрупу, карбоксил, карбоксилат, -SO3H, сульфонат, NE1E2, алкілен-NE1E2, трифторметил і галоген. Наведені вище пояснення щодо алкільних груп стосуються відповідно і алкокси- й алкілтіогруп. Під групами NE1E2 переважно маються на увазі Ν,Ν-диметил, Ν,Ν-діетил, Ν,Ν-дипропіл, Ν,Νдіізопропіл, Ν,Ν-ди-н-бутил, Ν,Ν-ди-трет-бутил, Ν,Ν-дициклогексил або Ν,Ν-дифеніл. у якій R3 і R4 мають вказані вище значення, у Галоген означає фтор, хлор, бром і йод, переприсутності водню і принаймні одного металовмісважно фтор, хлор і бром. ного каталізатора, який відрізняється тим, що акКарбоксилат і сульфонат у контексті даного тивний компонент каталізатора складається в осопису являють собою похідне функціональної груновному з металів платинової групи. пи карбонової кислоти, відповідно функціональної У контексті даного опису під поняттям "алкіл" групи сульфонової кислоти, насамперед карбоксимаються на увазі прямоланцюгові і розгалужені лат або сульфонат металу, функціональну групу алкільні групи. Переважно мова при цьому йде про ефіру карбонової кислоти або сульфонової кислопрямоланцюгові або розгалужені С1-С20алкільні, ти, функціональну групу аміду карбонової кислоти переважно С1-С12алкільні, особливо переважно або сульфонової кислоти. С1-С8алкільні і найбільш переважно С1-С4алкільні Активний компонент каталізатора, який викогрупи. Як приклади подібних алкільних груп можна ристовується відповідно до винаходу, складаєтьназвати метил, етил, пропіл, ізопропіл, н-бутил, 2ся, як зазначалося вище, в основному з металів бутил, втор-бутил, трет-бутил, н-пентил, 2-пентил, платинової групи, тобто Ru, Rh, Pd, Os, Ir, Pt і їх 2-метилбутил, 3-метилбутил, 1,2-диметилпропіл, сумішей. Переважно застосовувати каталізатор, 1,1-диметилпропіл, 2,2-диметилпропіл, 1активний компонент якого не містить головним етилпропіл, н-гексил, 2-гексил, 2-метилпентил, 3чином срібла. метилпентил, 4-метилпентил, 1,2-диметилбутил, Переважно застосовувати каталізатор, актив1,3-диметилбутил, 2,3-диметилбутил, 1,1ний компонент якого містить диметилбутил, 2,2-диметилбутил, 3,3- від 1 до 100мас.%, переважно від 10 до диметилбутил, 1,1,2-триметилпропіл, 1,2,299мас.%, Pd, триметилпропіл, 1-етилбутил, 2-етилбутил, 1-етил- від 0 до 60мас.%, переважно від 1 до 2-метилпропіл, н-гептил, 2-гептил, 3-гептил, 255мас.%, Pt і етилпентил, 1-пропілбутил, октил, ноніл і децил. - від 0 до 50мас.%, наприклад від 0,1 до Заміщені алкільні групи містять переважно 1, 40мас.%, принаймні ще одного металу, насампе2, 3, 4 або 5, насамперед 1, 2 або 3, замісники. Ці ред вибраного з групи, яка включає Ru, Rh, Os, Іr, замісники можуть бути вибрані, наприклад, із груСе, La і їхньої суміші. пи, яка включає циклоалкіл, арил, гетарил, галоУ запропонованому у винаході способі переген, ОН-, SH-, алкокси-, алкілтіогрупу, NE1E2, важно застосовувати каталізатор, нанесений на (NE1E2E3)+, карбоксил, карбоксилат, -SO3H, сульвідповідний носій. Як придатні для таких цілей фонат, нітро- і ціаногрупу. носії можуть використовуватися в принципі звиУ випадку циклоалкільної групи переважно чайні, відомі фахівцям у даній галузі матеріали. До мається на увазі С6-С12циклоалкільна група, така них належать серед інших вуглецевмісні матеріаяк циклогексил, циклогептил, циклооктил, циклоли, такі як активоване вугілля, карбід кремнію, подецил або циклододецил. Особливо переважні з лімерні носії, металеві носії, наприклад з високояних циклогексил і циклододецил. кісної сталі, оксиди алюмінію, діоксиди кремнію, У тих випадках, коли циклоалкільна група засилікати, алюмосилікати, такі як цеоліти, пемза, міщена, вона містить переважно 1, 2, 3, 4 або 5, діатомова земля, кізельгель, гідроталькіт, діоксиди насамперед 1, 2 або 3, замісники. Ці замісники титану, діоксиди цирконію, оксид цинку, оксид магможуть бути вибрані з групи, яка включає алкіл, нію, а також їх комбінації і суміші. При необхідності алкокси-, алкілтіо-, ОН-, SH-групу, циклоалкіл, цидо матеріалів носіїв можуть додаватися оксиди клоалкілалкіл, нітро-, ціаногрупу і галоген. лужних і/або лужноземельних металів. Особливо Під поняттям "арил" переважно маються на увазі феніл, толіл, ксиліл, мезитил, нафтил, анпереважно використовувати в цих цілях -Аl2О3, траценіл, фенантреніл, нафтаценіл і насамперед Аl2О3, SiO2, ТiО2, ZrO2 і їх суміші. Найбільш перефеніл або нафтил. важним з них є ΖrO2. Носії можуть мати в принципі Заміщені арильні групи містять переважно 1, будь-яку звичайну форму, наприклад, їх можна 2, 3, 4 або 5, насамперед 1, 2 або 3 замісники. Ці застосовувати у вигляді екструдатів (джгутів), замісники можуть бути вибрані з групи, яка вклюсферичних гранул, зерняток, таблеток, кілець, сідчає алкіл, алкоксигрупу, карбоксил, карбоксилат, ло- або гантелеподібних виробів, тканин, переплетрифторметил, -SO3H, сульфонат, NE1E2, алкілентеної структури, монолітів, кульок, порошку і т.д. NE1E2, нітро-, ціаногрупу і галоген. При здійсненні способу в періодичному режимі Під поняттям "гетарил" маються на увазі перепереважно застосувати носії у вигляді порошку. важно піроліл, піразоліл, імідазоліл, індоліл, карЗастосовувані в способі за винаходом каталібазоліл, піридил, хінолініл, акридиніл, піридазиніл, затори можна одержувати за загальновідомими 7 75126 8 методами, наприклад просоченням носія розчинапор за розмірами вирішального значення не мають ми сполук або комплексами використовуваних і можуть змінюватися в широких межах. металів. Як сполуки металів (попередників) придаОсобливо переважно в способі за винаходом тні, наприклад, солі металів, такі як нітрати, нітрозастосовувати каталізатор, який містить від 0,1 до зилнітрати, галогеніди, карбонати, карбоксилати, 10мас.% Pd, у кожному випадку в перерахунку на металеві комплекси, такі як ацетилацетонати, гамасу активного компонента і носія. Переважно логенові комплекси, наприклад хлорвмісні комплекаталізатор містить Pt у кількості 0-5мас.%, наприкси, комплекси з аміном і т.д. Для нанесення споклад 0,1-4мас.%. Особливо переважні каталізатолук металів на носій можна використовувати, ри, які містять як активний компонент лише один наприклад, метод спільного осадження або просоPd. чення. При використанні декількох сполук металів Запропонований у винаході спосіб дозволяє останні можна наносити одночасно або послідовекономічним і ефективним шляхом одержувати за но. При цьому послідовність, у якій наносять актиодностадійним механізмом N-заміщені 2,6вні компоненти, як правило, може бути будь-якою. діалкілморфоліни. При цьому цільові сполуки, як Придатними розчинниками для одержання каталіправило, одержують з високим виходом і високою заторів просоченням є вода й органічні розчиннивибірністю. Одна з переваг запропонованого у ки, такі як спирти, наприклад метанол і етанол, винаході способу полягає в можливості одержання ароматичні вуглеводні, такі як бензол і толуол, N-заміщених 2,6-діалкілморфолінів також при поаліфатичні розчинники, такі як гексан, гептан і т.п., дачі едуктів з високою витратою, тобто при всіх циклоаліфатичні розчинники, такі як гексан, і інші. умовах забезпечений високий вихід продуктів з Нанесені на носій паладійвмісні каталізатори одиниці об'єму за одиницю часу. Ще одна переваодержують переважно просоченням носія розчига способу за винаходу полягає в тому, що він доном Рd(NО3)2, РdСІ2, H2РdСl2, Pd-ацетилацетонату зволяє одержувати N-заміщені 2,6і т.п. Після просочення носій доцільно піддавати діалкілморфоліни у вигляді чистих ізомерів. сушінню при температурі в основному в інтервалі Переважно для одержання N-заміщених 2,6від порядку 50 до 200°С, переважно від 100 до діалкілморфолінів використовувати кетон загаль150°С. Після сушіння носій при необхідності можна ної формули II, де R1 і R2 разом з атомом вуглецю, кальцинувати. Температура при цьому знаходитьз яким вони зв'язані, утворюють 6-12-членний карся, як правило, в інтервалі від 200 до 600°С, перебоцикл, який може містити один, два або три заміважно від 400 до 500°С. Тривалість кальцинування сники, незалежно один від одного вибраних із груможе змінюватися в широких межах і становити, пи, яка включає алкіл, алкоксигрупу, алкілтіогрупу, наприклад, від порядку 1 до 10 годин, переважно циклоалкіл і циклоалкілалкіл. Особливо переважвід 1,5 до 5 годин. Для переведення попередників ною сполукою формули II є циклододеканон. в активний компонент каталізатор можна обробляR3 і R4 у формулі III незалежно один від одного ти звичайним відновником, таким як водень. При переважно являють собою С1-С4алкільні групи. цьому до відновника при необхідності можна доОсобливо переважно R3 і R4 означають обидва мішувати інертні гази, такі як азот або аргон. Темметил. пература при відновленні знаходиться переважно Запропонований у винаході спосіб придатний в інтервалі від порядку 100 до 500°С, особливо насамперед для одержання N-(циклододецил)-2,6переважно від 200 до 300°С. Якщо для одержання диметилморфоліну (додеморфу). застосовуваних відповідно до винаходу каталізаТемпература реакції знаходиться переважно в торів як попередник використовують сполуку меінтервалі від 100 до 300°С. Тиск при перебігу реаталу, яка термічно легко розкладається, то подібні кції становить переважно від 5 до 300 бар, особсполуки, як правило, вже в умовах кальцинування ливо переважно від 10 до 250 бар. розкладаються на елементарні метали або оксидні Запропонований у винаході спосіб можна здійсполуки металів, що дозволяє в принципі виклюснювати без використання розчинників або у причити необхідність наступного відновлення. сутності відповідного розчинника. З переліку можПісля сушіння і/або кальцинування і/або відноливих розчинників можна назвати воду, спирти, влення при необхідності можна проводити притакі як метанол і етанол, прості ефіри, такі як менаймні ще одну операцію з обробки. До таких опетил-трет-бутиловий ефір, прості циклічні ефіри, рацій належать, зокрема, пасивування, наприклад такі як тетрагідрофуран, кетони, такі як ацетон і за допомогою кисню, до якого в разі потреби може метилетилкетон, і ряд інших. Особливо переважно бути домішаний інертний газ. Пасивування доцільзастосовувати як розчинник морфолін, який виконо проводити при одержанні каталізаторів на осристовується як едукт. При цьому морфолін можна нові металів, оксиди яких також мають каталітичну використовувати в 100-кратному молярному надактивність. лишку відносно до амінового компонента. Інші способи одержання каталізаторів, які заЗапропонований у винаході спосіб можна здійстосовуються відповідно до винаходу, відомі фахіснювати як у періодичному, так і в безперервному вцям у даній галузі. Як приклади можна назвати режимі. Переважно працювати в безперервному напилювання з парової фази, металізацію, іоноорежимі. бмінний спосіб і інші. Для здійснення способу за винаходу можуть Відповідно до одного з рекомендованих варіавикористовуватися звичайні, відомі фахівцям апантів здійснення винаходу каталізатор відновлюють рати і пристрої, придатні для роботи під високим in situ за допомогою водню і переводять таким тиском, такі, наприклад, як автоклави або трубчасшляхом в активну форму. ті реактори. Переважно застосовувати каталізатор Поверхня каталізатора, об'єм пор і розподіл у вигляді стаціонарного (нерухомого) шару або в 9 75126 10 якій-небудь іншій формі, придатній для викорисПриклад 2 (Рd/ZrO2-каталізатор) тання у вигляді вбудовуваного елемента. РеакційУ даному прикладі працювали аналогічно до ну камеру при цьому доцільно розміщати у вертиприкладу 1, з тією, однак, відмінністю, що викорискальному положенні. Реакцію переважно товували чистий цис-2,6-диметилморфолін і проводити пропусканням реагентів через шар каPd/ZrO2-каталізатор (вміст паладію 0,9%). При тій талізатора низхідним потоком і висхідним потоком. же температурі і швидкості подачі і після відділенВихідні речовини при цьому переважно подавати ня 2,6-диметилморфоліну реакційна суміш містила таким чином, щоб практично весь шар каталізато94,4% додеморфу, а також 0,7% циклододеканону. ра повністю був покритий рідиною. Ці значення відповідають перетворенню, що доріЩе одним об'єктом винаходу є застосування внює 99,3%, і вибірності, що дорівнює 95%. вищеописаного каталізатора для одержання треПриклад 3 (Pd/ZrO2-каталізатор) тинного аміну взаємодією принаймні однієї карбоУ даному прикладі працювали аналогічно до нільної сполуки принаймні з одним вторинним аміприкладу 2, з тією, однак, відмінністю, що швидном у присутності водню. кість подачі була вдвічі вищою (720мл/год), а темНижче винахід більш докладно пояснюється пература становила 240°С. Після відділення 2,6на прикладах, які не обмежують його обсяг. диметилморфоліну реакційна суміш містила 92,2% Приклади додеморфу, а також 2,6% циклододеканону. Ці Приклад 1 (порівняльний Pd/Ag-каталізатор) значення відповідають перетворенню, що дорівУ розташований вертикально трубчастий реанює 97,4%, і вибірності, що дорівнює 95%. ктор поміщали 500мл каталізатора, який містив 5% Приклад 4 (Pd/Pt, ZrO2-каталізатор) Ag2O і 0,4% Pd на SiO2-Hocii. При температурі У даному прикладі працювали аналогічно до 220°С і тиску водню 100 бар знизу накачували наприкладу 1, з тією, однак, відмінністю, що викорисгріту до 220°С суміш з однієї частини цис-2,6товували чистий цис-2,6-диметилморфолін і диметилморфоліну, однієї частини транс-2,6Ра/Рt/ZrО2-каталізатор (вміст паладію 0,4%, вміст диметилморфоліну і 0,39 частини циклододеканоплатини 0,4%). При температурі 230°С і витраті ну при витраті 360мл/год. На виході реакційна су180мл/год реакційна суміш після відділення 2,6міш після видалення з неї у вакуумі 2,6диметилморфоліну містила 95,6% цис-додеморфу диметилморфоліну містила 89,6% додеморфу, а при повній відсутності циклододеканону. Ці знатакож 2,3% циклододеканону. Ці значення відповічення відповідають перетворенню, що дорівнює дають перетворенню, що дорівнює 97,3%, і вибір100%, і вибірності, що дорівнює 95%. ності, що дорівнює 91%. Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA method of producing the n-substituted 2,6-dialkyl morpholines and use of catalyst for producing tertiary amine
Назва патенту російськоюСпособ получения n-замещенных 2,6-диалкилморфолинов и применение катализатора для получения третичного амина
МПК / Мітки
МПК: C07D 265/30, C07D 295/033, C07D 295/03, C07D 295/023, C07B 61/00
Мітки: n-заміщених, застосування, аміну, 2,6-діалкілморфолінів, спосіб, третинного, каталізатора, одержання
Код посилання
<a href="https://ua.patents.su/5-75126-sposib-oderzhannya-n-zamishhenikh-26-dialkilmorfoliniv-ta-zastosuvannya-katalizatora-dlya-oderzhannya-tretinnogo-aminu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання n-заміщених 2,6-діалкілморфолінів та застосування каталізатора для одержання третинного аміну</a>
Попередній патент: Спосіб керування потужністю для обслуговування багатоточкового з’єднання у системі зв’язку (варіанти) та пристрій для його здійснення (варіанти)
Наступний патент: 1,4-біс-[2-арил(гетарил)оксазол-4-іден-5-он]бензоли, які проявляють властивості органічних люмінофорів зеленого світіння
Випадковий патент: Спосіб одержання суміші ізомерів циперметрину або цифлутрину