Лікарський засіб для лікування хронічного обструктивного захворювання легень
Формула / Реферат
1. Лікарський засіб для лікування хронічного обструктивного захворювання легень, який включає похідне карбостирилу формули (1):
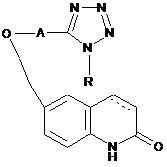 , (1)
, (1)
де:
А представляє нижчу алкіленову групу, R представляє циклоалкільну групу і зв'язок між положеннями 3 і 4 карбостирильного скелета є одинарним зв'язком або подвійним зв'язком,
або його сіль і пробукол як активні інгредієнти.
2. Лікарський засіб за п. 1, в якому похідним карбостирилу є 6-[4-(1-циклогексил-1Н-тетразол-5-іл)бутокси]-3,4-дикарбостирил або його сіль.
3. Застосування похідного карбостирилу або його солі, представлених в п. 1 або 2, і пробуколу при приготуванні лікарського засобу для лікування хронічного обструктивного захворювання легень.
4. Спосіб лікування хронічного обструктивного захворювання легень, який включає введення потребуючому такого лікування пацієнту ефективної кількості похідного карбостирилу або його солі, як вони представлені в п. 1 або 2, і пробуколу.
Текст
1. Лікарський засіб для лікування хронічного обструктивного захворювання легень, який включає похідне карбостирилу формули (1): N (13) N N H 95830 R O , (1) Даний винахід стосується лікарського засобу для лікування хронічного обструктивного захворювання легень, зокрема лікарського засобу для лікування хронічного обструктивного захворювання легень (ХОЗЛ), що включає як активні інгредієнти похідне карбостирилу формули (1): де А являє собою нижчу алкіленову групу і зв'язок між положеннями 3 і 4 карбостирильного скелету є одинарним зв'язком або подвійним зв'язком, або його сіль; і пробукол. Похідні карбостирилу формули (1) або їх солі і спосіб їх одержання описані в JP-63-20235-B і JP55-35019-A. Відомо також, що сполуки мають інгібуючу агрегацію тромбоцитів дію, інгібуючу фосфодіестеразу (PDE) дію, противиразкову, гіпотензивну дію і протизапальну дію і використовуються як антитромботичний агент, лікарська речовина, що поліпшує мозкову кровопостачання, протизапальний агент, противиразковий лікарський препарат, антигіпертензивний лікарський препарат, протиастматичний лікарський препарат, інгібітор (11) A UA O N де: А представляє нижчу алкіленову групу, R представляє циклоалкільну групу і зв'язок між положеннями 3 і 4 карбостирильного скелета є одинарним зв'язком або подвійним зв'язком, або його сіль і пробукол як активні інгредієнти. 2. Лікарський засіб за п. 1, в якому похідним карбостирилу є 6-[4-(1-циклогексил-1Н-тетразол-5іл)бутокси]-3,4-дикарбостирил або його сіль. 3. Застосування похідного карбостирилу або його солі, представлених в п. 1 або 2, і пробуколу при приготуванні лікарського засобу для лікування хронічного обструктивного захворювання легень. 4. Спосіб лікування хронічного обструктивного захворювання легень, який включає введення потребуючому такого лікування пацієнту ефективної кількості похідного карбостирилу або його солі, як вони представлені в п. 1 або 2, і пробуколу. (19) N 2 C2 1 3 фосфодіестерази і т.д. Крім того, відомо, що сполуку використовуються також як лікарський засіб для лікування алергічних захворювань (JP-5320050-A). Далі, відомі також сполуки як лікарський засіб для лікування ХОЗЛ (JP-10-175864-А). ХОЗЛ (хронічне обструктивне захворювання легень) в даний час є четвертою з найбільш поширених причин смертей в Америці, яка іде за серцевою недостатністю, ішемічним інсультом і раком. ХОЗЛ має тенденцію зростати в світі, незважаючи на той факт, що інші захворювання зменшуються, і на додаток кількість потенційних пацієнтів з ХОЗЛ дуже велика. Таким чином, можна передбачувати, що ця кількість буде зростати все більше і більше протягом часу. Причини ХОЗЛ включають аномальну запальну реакцію на куріння, шкідливий газ, такий як забруднене повітря, або шкідливі мікрочастинки, і таким чином ХОЗЛ є захворюванням, що характеризується прогресуючим обмеженням потоку повітря в зв'язку з хронічним обструктивним бронхітом і емфіземою. У даний час бронходилататори, такі як антихолінергічний агент і агоніст рецептора (2, використовуються клінічно як лікарський засіб для лікування ХОЗЛ, однак, лікарські засоби не вийдуть за межі паллиативной терапії, і, таким чином, не є базовими лікарськими засобами для лікування ХОЗЛ. Додатково, протизапальний агент, що зазвичай використовується при гострому нападі хвороби, є стероїдним лікарським препаратом, корисність якого, однак, ще не була задовільно вивчена. Інвазія в запалених клітинах легень є одним з головних факторів хронічного запалення при ХОЗЛ, і, додатково, окиснювальний стрес, викликаний запаленими клітинами, клітинами легень, пошкодженими запаленими клітинами або самою речовиною, що викликала порушення, також пов'язані з хронічним запаленням. Тому, є очікуваним, що регуляція анімального окиснювального стресу, викликаного в осередку запалення, може пригнітити хронічне запалення, і тому повинен бути розроблений новий лікарський засіб, що запобігає розвитку патології. Крім того, відомо, що в легені, яка є осередком запалення при ХОЗЛ, еластаза, що вивільняється з нейтрофіла, який проникає в легеневі альвеоли, суттєво пов'язана з настанням емфіземи, і також відомо, що нейтрофільна еластаза в крові інкапсулюється антитрипсином (α1-ΑΤ). Тому при такому окислювальному стресі α1-ΑΤ окиснюється, і інактивується, внаслідок чого нейтрофільна еластаза не інактивується, даючи початок порушення тканин. Таким чином, можна вважати, що лікарський засіб для регуляції такого окиснювального стресу буде запобігати розвитку патології. Як модельна тварина патології при ХОЗЛ може служити тварина, яка страждає емфіземою, викликаною тим, що тварина протягом тривалого періоду зазнавала впливу сигаретного диму, або введенням тварині інтратрахеально різних протеаз, таких як еластаза підшлункової залози свині (РРЕ) і еластаза нейтрофіла людини, і тварина, яка страждає емфіземою через легеневий розлад/запалення при стимулюванні її різними хімічними речовинами, такими як LPS, хлорид кадмію, 95830 4 двоокис азоту, озон і неорганічний пил. У доповнення використовували також мишей з пороками, що мимовільно виникли, які легко захворюють емфіземою, таких як Tight Skin (Tsk +/-) і Pallid (C57BL/6J ра+/ра+) або генно-модифікованих мишей, таких як Transgenic і Gene Targeting. Таким чином, хоча деякі лікарські засоби для лікування ХОЗЛ, як згадано вище, використовувалися клінічно, все ще є потреба в більш ефективному лікарському засобі для лікування ХОЗЛ, оскільки сучасні лікарські засоби не вийдуть за межі паліативної терапії. Автори даного винаходу інтенсивно вивчили новий лікарський засіб для лікування ХОЗЛ і виявили, що комбінація або комбінований лікарський препарат з похідного карбостирилу наведеної вище формули (1), особливо 6-[4-(1-циклогексил- 1Нтетразол-5-іл)бутокси]-3,4-дикарбостирилу (цилостазолу) або його солі і пробуколу надає чудову синергетичну дію для лікування ХОЗЛ. Особливо, комбінація також має деякі впливи, які зменшують побічні ефекти кожного лікарського засобу, пригнічують напади, які вимагають введення стероїда, сильно поліпшують стан при ХОЗЛ і зменшують дозу стероїда для системного застосування. У доповнення, комбінація або комбінований лікарський препарат може вводитися протягом тривалого періоду завдяки її швидкій дії і низькій токсичності. Крім того, вже відомо, що цилостазол виявляє бронходилататорну дію, і, отже, можна вважати, що ця дія може ефективно працювати на поліпшення стану при ХОЗЛ при лікуванні комбінацією або комбінованим лікарським препаратом. Даним винаходом є корисний лікарський засіб для лікування ХОЗЛ з точки зору безпечного лікування. Даний винахід пропонує лікарський засіб для лікування хронічного обструктивного захворювання легень, що включає похідне карбостирилу загальної формули: в якій А представляє нижчу алкіленову групу, R представляє циклоалкільну групу і зв'язок між положеннями 3 і 4 карбостирильного скелету є одинарним зв'язком або подвійним зв'язком, або його сіль, і пробукол як активні інгредієнти. Даний винахід також пропонує лікарський засіб для лікування хронічного обструктивного захворювання легень, що включає 6-[4-(1-циклогексил-1Нтетразол-5-іл)бутокси]-3,4-дикарбостирил (цилостазол) або його сіль і пробукол як активні інгредієнти. Даний винахід також пропонує лікарський засіб для лікування хронічного обструктивного захворювання легень, що включає вищезазначені інгредієнти. 5 Даний винахід також пропонує композицію для лікування хронічного обструктивного захворювання легень, що включає вищезазначені інгредієнти. Даний винахід пропонує також використання похідного карбостирилу або його солі, як згаданий вище, і пробуколу при приготуванні лікарського засобу для лікування хронічного обструктивного захворювання легень. Даний винахід пропонує також спосіб лікування хронічного обструктивного захворювання легень, який включає введення потребуючому такого лікування пацієнту ефективної кількості похідного карбостирилу або його солі, як згадано вище, і пробуколу. Згідно з даним винаходом дуже ефективно використати проти ХОЗЛ похідне карбостирилу (1), особливо 6-[4-(1-циклогексил-1Н-тетразол-5іл)бутокси]-3,4-дикарбостирил (цилостазол) або його сіль, разом з пробуколом. Фіг.1 показує комбінований ефект впливу на розмір легеневих альвеол з використанням експериментальної моделі ХОЗЛ на мишах, оброблених еластазою. Похідним карбостирилу, яке включене як інгредієнт в комбінований лікарський препарат або використовується в комбінованому введенні, є похідне тетразолілалкоксидигідрокарбостирилу формули: де: А представляє нижчу алкіленову групу, R представляє циклоалкільну групу і зв'язок між положеннями 3 і 4 карбостирильного скелету є одинарним зв'язком або подвійним зв'язком, або його сіль. У наведеній вище формулі (1) циклоалкільна група включає циклоалкільні групи С3-С8, такі як циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. Нижча алкіленова група включає алкіленові групи С1-С6, такі як метилен, етилен, пропілен, тетраметилен, бутилен і пентилен, з яких переважним є тетраметилен. Переважно похідним карбостирилу є 6-[4-(1 циклогексил-1 Н-тетразол-5-іл)бутокси]-3,4дикарбостирил, який був випущений на ринок під торговою назвою цилостазол як антитромботичний агент. Похідне карбостирилу (1) може бути легко перетворено на його сіль, обробкою його фармацевтично прийнятною кислотою. Кислоти включають, наприклад, неорганічні кислоти, такі як хлористоводнева кислота, сірчана кислота, фосфорна кислота і бромистоводнева кислота, і органічні кислоти, такі як щавлева кислота, малеїнова кислота, фумарова кислота, яблучна кислота, винна кислота, лимонна кислота і бензойна кислота. 95830 6 Ці похідні карбостирилу (1) і їх солі і способи їх одержання розкриті в JP-55-35019-А (релевантному патенту США 4277479). Інший активний інгредієнт, пробукол, є сполукою, що має хімічну назву 4,4'-ізопропілідендитіобіс[2,6-ди-трет-бутилфенол], і вже був випущений на ринок як антигіперліпідемічний агент. Відомо також, що ця сполука має активність інгібувати продукування окисленого ліпопротеїну низької щільності (LDL) (див. J. Clin. Invest, 77, p. 641, 1986). Ці активні інгредієнти, похідне карбостирилу (1) і пробукол, можуть бути введені разом або по окремості, в один і той самий час або в різний час. Ці інгредієнти зазвичай можуть бути використані в звичайних фармацевтичних формах. Так, ці інгредієнти можуть бути приготовані в одній дозованій формі або в окремих дозованих формах. Доза цих активних інгредієнти не обмежена точно визначеним інтервалом. Похідні карбостирилу (1) або їх солі можуть бути використані в кількості від 50 до 200 мг/добу для дорослого (маса тіла 50 кг), яка може вводитися за один прийом на добу або за два або декілька прийомів на добу. Пробукол може бути використаний в кількості від 100 до 1000 мг/добу для дорослого (маса тіла 50 кг), яка може вводитися за один прийом на добу або за два або декілька прийомів на добу, але переважно за два або декілька прийомів на добу. Коли ці інгредієнти приготовані в єдиній дозованій формі, їх вводять в співвідношенні від 25 до 10 масових частин пробуколу на 1 масову частину похідного карбостирилу (1) або його солі. Комбінований лікарський препарат може включати суму інгредієнти 0,1-70% мас. на препарат, не обмежуючись цим. Кожна дозована форма, використана для комбінованого лікарського препарату або для комбінації за даним винаходом, включає, наприклад, дозовані форми, наведені в JP-10-175864-A, і зазвичай пероральну тверду дозовану форму, таку як таблетки або капсули, і пероральну рідку дозовану форму, таку як сиропи і еліксири, парентеральну дозовану форму, таку як ін'єкції, і лікарська форма для інгаляції. Препарати за винаходом, такі як таблетки, капсули, рідина для перорального введення можуть бути приготовані звичайним методом. Таблетки можуть бути приготовані змішуванням активного інгредієнта (активних інгредієнтів) із звичайними фармацевтичними носіями, такими як желатин, крохмаль, лактоза, стеарат магнію, тальк, камедь і т.п. Капсули можуть бути приготовані змішуванням активного інгредієнта (активних інгредієнти) з інертними фармацевтичними наповнювачами або розріджувачами і заповненням твердих желатинових капсул або м'яких капсул сумішшю. Пероральні рідкі препарати, такі як сиропи або еліксири, готують змішуванням активного інгредієнта (активних інгредієнти) з підсолоджувачами (наприклад, сахарозою), консервантами (наприклад, метилпарабеном, пропілпарабеном), барвниками, ароматизаторами і т.п. Препарати для парентерального введення також можуть бути приготовані звичайним методом, наприклад, розчиненням активного 7 інгредієнта (активних інгредієнти) за даним винаходом в стерильному водному носії, переважно у воді або сольовому розчині. Переважний рідкий препарат, придатний для парентерального введення, готують розчиненням добової дози згаданих вище активних інгредієнтів у воді і органічному розчиннику і далі в поліетиленгліколі, що має молекулярну вагу від 300 до 5000, в яку переважно введений лубрикант, такий як натрійкарбоксиметилцелюлоза, метилцелюлоза, полівінілпіролідон і полівініловий спирт. Переважно вищезгадані рідкі препарати можуть додатково включати дезінфектанти (наприклад, бензиловий спирт, фенол, тимерозал), фунгіцид і далі, необов'язково, ізотонічний агент (наприклад, сахарозу або хлориди натрію), місцеве знеболювальне, стабілізатор, буфер і т.п. Приймаючи до уваги збереження стабільності, препарат для парентерального введення може бути поміщений в капсули з подальшим видаленням водного середовища звичайним методом ліофілізації. Препарат може бути відновлений в рідкий препарат розчиненням у водному середовищі при використанні. Лікарські форми для інгаляції можуть бути приготовані звичайним методом. Тобто, лікарські форми для інгаляції можуть бути приготовані шляхом перетворення активної сполуки в порошок або в рідкий стан, підмішування її в пропелент і/або носій для інгаляції і зарядження сумішшю відповідного інгалятора. Зазвичай механічний інгалятор може бути використаний, коли активна сполука є порошком, і такий інгалятор як розпилювач, може бути використаний, коли сполука є рідиною. У доповнення, лікарська форма для інгаляції може, необов'язково, включати сурфактант, масло, ароматизатор, циклодекстрин або його похідне, яке використовують, якщо потрібно. Приклади вищезазначених додаткових агентів включають, але не обмежуються цим, агенти, які розкриті в JP-10-175864-A. Приклад 1 Вплив комбінації цилостазол/пробукол на легеневий розлад у мишей C57BL/6J, оброблених еластазою, продукованою нейтрофілами людини Методика експерименту Тварини: використовувалися самиці мишей C57BL/6J (вік 5 тижнів), які були придбані у Charles River Laboratories Japan Inc. Групи за складом: наступні 5 груп: Група без обробки (нормальний контроль): n=4. Група, оброблена еластазою (контрольна група): n=6. Група, оброблена еластазою з введенням 0,3% цилостазолу: n=6. Група, оброблена еластазою з введенням 0,5% пробуколу: n=6. Група, оброблена еластазою з введенням 0,5% пробуколу + 0,3% цилостазолу: n=6. Самиці мишей C57BL/6J (вік 5 тижнів) були розділені на вказані групи типовою довільною вибіркою (використовуючи програмний продукт SAS R 8.11) на основі маси тіла кожної на початковий день введення. Незабаром після розділення на групи корм MF був даний необробленій групі і кон 95830 8 трольній групі, і змішаний корм, до якого цилостазол і/або пробукол був доданий в заданому співвідношенні, був даний обробленим лікарським засобом групам у вільному годуванні. На 7-ие доби після початку введення еластазу, продуковану нейтрофілом людини (Elastin Products Co. Inc.), інтратрахеально вводили в дозі 20 Е/50 мкл анестезованим фенобарбіталом мишам через гортані, використовуючи розпилювач (Penn-Century Inc.). Через три тижні після введення еластази тварини були умертвлені кровопусканням з черевної порожнистої вени під ефірною анестезією, і потім були повністю видалені їх легені, які були зафіксовані перфузією 10% нейтральним формаліновим буферним розчином. Легеневу тканину, фіксовану формаліном, фіксували парафіном, нарізали тонкими зрізами і забарвлювали барвником Mason Trichrome і барвником НЕ в Biopathology Institute Co., Ltd. Оцінку патологічних тканин проводили, базуючись на середньому лінійному перекритті їх легеневих альвеол, яке є об'єктивним показником порушення легеневих альвеол (M.S.Dunnill, Тогах (1962); 17, 320). Статистичний аналіз Для того, щоб вивчити ефект введення лікарських засобів по окремості комбінованого введення, статистично аналізували наступні групи: 1) Оброблена еластазою група (контрольна група) 2) Група з введенням 0,3% цилостазолу 3) Група з введенням 0,5% пробуколу 4) Група з введенням 0,3% цилостазолу + 0,5% пробуколу Для того, щоб оцінити комбінований ефект, проводили двофакторний аналіз відхилень між обробленою еластазою групою і групою з введенням цилостазолу, групою з введенням пробуколу або групою з комбінованим введенням, щоб оцінити кожну взаємодію. Були проведені тести Dunnett'a групи з введенням цилостазолу і групи з введенням пробуколу по відношенню до групи, обробленої еластазою. У доповнення також були проведені тести Dunnett'a групи з введенням цилостазолу і групи з введенням пробуколу по відношенню до групи з комбінованим введенням. Всі тести оцінювали з двостороннім критерієм з рівнем значущості 5%. Тест проводили, використовуючи комп'ютерну програму SAS (SAS Institute Japan, R 8.11). Комбінований ефект впливу на середнє лінійне перекриття легеневих альвеол при моделі ХОЗЛ у оброблених еластазою мишей Всі результати для групи з введенням 0,3% цилостазолу (116,9±14,3 мкм), групи з введенням 0,5% пробуколу (86,2±4,8 мкм), і групи з введенням (0,3% цилостазолу + 0,5% пробуколу) (67,5±3,7 мкм) показали значні інгібувальні ефекти в порівнянні з результатом для обробленої еластазою групою (контрольною групою, 178,8±22,4 мкм) (середня величина ± стандартне відхилення, Ρ0,01), і крім того результат для групи з комбінованою обробкою показав ефект значного поліпшення з досягненням такого ж рівня, як у необробленої групи (51,4+1,9 мкм). 9 При порівнянні між кожним введенням однієї сполуки і комбінованим введенням, комбіноване введення показало більш значний ефект зниження середнього лінійного перекриття легеневих альве Комп’ютерна верстка І. Скворцова 95830 10 ол, ніж показало введення тільки однієї сполуки у групи з введенням 0,5% пробуколу, або у групи з введенням 0,3% цилостазолу (фіг. 1). Підписне Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMedicament for the treatment of chronic obstructive pulmonary disease
Автори англійськоюYabuuchi, Yoichi, Kotosai, Kounori
Назва патенту російськоюЛекарственное средство для лечения хронического обструктивного заболевания легких
Автори російськоюЯбуути Йоити, Котосаи Коунори
МПК / Мітки
МПК: A61K 31/095, A61P 11/00, A61K 31/4704
Мітки: обструктивного, захворювання, легень, хронічного, засіб, лікування, лікарський
Код посилання
<a href="https://ua.patents.su/5-95830-likarskijj-zasib-dlya-likuvannya-khronichnogo-obstruktivnogo-zakhvoryuvannya-legen.html" target="_blank" rel="follow" title="База патентів України">Лікарський засіб для лікування хронічного обструктивного захворювання легень</a>
Попередній патент: Стенд для дослідження сили тертя у ковзунах візка вантажного вагона
Наступний патент: Зернолущилка качанів кукурудзи
Випадковий патент: Спосіб діагностики розвитку атеросклерозу









