Спосіб одержання магнію сульфату гептагідрату із сольового розчину
Номер патенту: 75034
Опубліковано: 26.11.2012
Автори: Яворський Віктор Теофілович, Перекупко Тамара Вікторівна, Блажівський Костянтин Іванович, Перекупко Аркадій Вікторович, Максимович Ігор Євстафійович
Формула / Реферат
Спосіб одержання магнію сульфату гептагідрату з сольового розчину, що включає концентрування розчину його випарюванням з кристалізацією натрію хлориду, розділення одержаної суспензії та охолодження рідкої фази з кристалізацією магнію сульфату гептагідрату, який відрізняється тим, що як сольовий розчин використовують розчин хвостосховища калійного виробництва, концентрування розчину його випарюванням здійснюють на 40 %, після розділення одержаної суспензії рідку фазу охолоджують до кімнатної температури з кристалізацією калійно-магнієвих солей, їх відфільтровують і сушать з одержанням калімагнезії, а відфільтрований розчин охолоджують до (мінус 3 - мінус 5)°С з кристалізацією магнію сульфату гептагідрату, його наступним фільтруванням і репульпаційним промиванням насиченим розчином магнію сульфату в кількості 1-2 т на 1 т магнію сульфату гептагідрату.
Текст
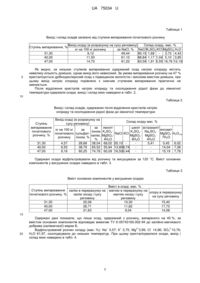
Реферат: Спосіб одержання магнію сульфату гептагідрату з сольового розчину включає концентрування розчин хвостосховища калійного розчину випарюванням. Потім розділяють одержану суспензію, а рідку фазу охолоджують з кристалізацією калійно-магнієвих солей. Після їх відфільтровують і сушать з одержанням калімагнезії. Відфільтрований розчин охолоджують з кристалізацією магнію сульфату гептагідрату. Потім фільтрують та промивають насиченим розчином магнію сульфату. UA 75034 U (54) СПОСІБ ОДЕРЖАННЯ МАГНІЮ СУЛЬФАТУ ГЕПТАГІДРАТУ ІЗ СОЛЬОВОГО РОЗЧИНУ UA 75034 U UA 75034 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель належить до хімічної технології неорганічних речовин, зокрема технологій перероблення сольових розчинів з одержанням магнію сульфату гептагідрату, який використовують у сільському господарстві як добриво, у виробництві синтетичних миючих засобів, кормових дріжджів, шкіряній, хімічній, металургійній, будівельній, целюлозно-паперовій, текстильній, радіоелектронній і харчовій галузях промисловості та медицині. Відомий спосіб одержання магнію сульфату гептагідрату [А.с. 40386 НРБ, МКИ C01F5/40. Метод за получаване на магнезиев сулфат хептахидрат / X.X. Баларев, Д.Л. Спасов, B.C. Мавров, С.К. Танев, Г.Г. Георгиева, Б.Г. Керемедчиева; 30.12.1986], який включає 3 концентрування морської води або розсолу до густини 1275-1284 кг/м їх випарюванням, кристалізацію натрію хлориду, відділення осаду, охолодження розчину до 0-(-5)°С з виділенням у тверду фазу магнію сульфату гептагідрату. Але за цим способом одержують магнію сульфат гептагідрат низької чистоти, який містить не більше 85 мас. % MgSO4·7H2O, до 12 мас. % домішок натрію і магнію хлоридів, і не відповідає вимогам чинних технічних умов до цього продукту. Відомий спосіб [Патент № 2056356 RU, МКИ C01F5/40; Способ извлечения сульфата магния / Л.М. Пасевьева, Г.Г. Багиров, B.C. Грищенко, А. Ходжамамедов, Б. Джумамурадов, А. Колатова; 20.03.1996], який включає вилуговування водою магнію сульфату з природного епсоміту за температури 25-75 °C, відділення нерозчинного залишку, висолювання продукту з одержаного розчину хлоридмагнієвим розсолом, який додають у кількості 0,06-0,29 т на 1 т епсоміту, охолодження пульпи до кімнатної температури та відділення осаду магнію сульфату гептагідрату. Проте в цьому способі необхідно використовувати специфічну сировину - природний епсоміт, який одержують басейновим способом з морської води або ропи солених озер, та концентровані чисті розчини магнію хлориду, які після висолювання продукту забруднюються домішками, що містить природний епсоміт. Це потребує подальшого очищення розчинів після висолювання, значно ускладнює спосіб і знижує його економічність. Запропоновано підземне захоронення розчинів хвостосховищ калійних виробництв на велику глибину у вичерпані шари виробіток природного газу поблизу Калуш-Голинського родовища калійних руд [Манюк О.Р., Семчук Я.М. Підземне захоронення високомінералізованих розсолів та основні заходи захисту від забруднень навколишнього середовища // Екологічна безпека.-2008. - № 1. - С. 37-42]. Але в цьому способі не передбачено використання таких розчинів як дешевої початкової сировини для одержання цінних продуктів. Найближчим за технічною суттю і досягнутому результату є спосіб одержання магнію сульфату гептагідрату із сольового розчину, що включає концентрування розчину його випарюванням, кристалізацію натрію хлориду, розділення одержаної суспензії та охолодження рідкої фази з кристалізацією магнію сульфату гептагідрату. Як сольовий розчин використовують розсіл озера Сиваш, що містить (мас. %): MgSO4 9,76; MgCl2 14,06; КСl 2,94; NaCl 5,72 [Позин М.Е. Технология минеральных солей. - Ч.1. - Л.: Химия, 1974. - С. 302]. Однак одержаний за цим способом магнію сульфат гептагідрат має низьку чистоту і не відповідає вимогам чинних технічних умов до цього продукту. Крім того, не передбачено виділення з розсолу в тверду фазу калійно-магнієвих солей, які забруднюють цільовий продукт, ще більше знижуючи його чистоту. В основу корисної моделі поставлена задача створити такий спосіб одержання магнію сульфату гептагідрату із сольового розчину, в якому використання нової сировини і здійснення нових стадій процесу забезпечило б одержання кондиційного магнію сульфату гептагідрату і супутнього продукту - кондиційного калійно-магнієвого добрива (калімагнезії), тим самим покращити техніко-економічні показники процесу одержання цільового продукту (знизити його собівартість, підвищити рентабельність і прибутковість перероблення початкового розчину) та поліпшити екологічну ситуацію в районі калійних виробництв Прикарпаття за рахунок утилізації відпрацьованих розчинів хвостосховищ. Поставлена задача вирішується тим, що у способі одержання магнію сульфату гептагідрату із сольового розчину, який включає концентрування розчину його випарюванням, кристалізацію натрію хлориду, розділення одержаної суспензії та охолодження рідкої фази з кристалізацією магнію сульфату гептагідрату, згідно з корисною моделлю, як сольовий розчин використовують розчин хвостосховища калійного виробництва, випарювання розчину здійснюють на 40 %, після відділення кристалів натрію хлориду рідку фазу охолоджують до кімнатної температури з кристалізацією калійно-магнієвих солей, їх відфільтровують і сушать з одержанням калімагнезії, а відфільтрований розчин охолоджують до (мінус 3 - мінус 5)°С з кристалізацією магнію 1 UA 75034 U 5 10 15 20 25 30 35 40 45 50 сульфату гептагідрату, його наступним фільтруванням і репульпаційним промиванням насиченим розчином магнію сульфату в кількості 1-2 т на 1 т магнію сульфату гептагідрату. Запропонований спосіб порівняно з найближчим аналогом дає змогу залучити у виробництво магнію сульфату гептагідрату новий вид сировини - відпрацьовані розчини хвостосховищ калійних виробництв, які досі не знаходили застосування, і покращити екологічну ситуацію в районі калійних виробництв Прикарпаття. Використання цих розчинів, які містять іони + + 2+ 2Na , К , Mg , Сl і SO4 , дає змогу, крім основного продукту, одержати супутній продукт калійно-магнієве добриво (калімагнезію), що значно знижує собівартість основного продукту, підвищує рентабельність і прибутковість перероблення початкового розчину. Репульпаційне промивання одержаного осаду магнію сульфату гептагідрату насиченим розчином магнію сульфату за співвідношення Т:Р=1:1-1:2 забезпечує одержання кондиційного продукту, який відповідає вимогам ТУ 6-46-2319883-09-2001 "Магния сульфат гептагидрат технический" і ТУ 2141-016-32496445-00 "Магния сульфат гептагидрат". Приклад 1 100 кг розчину, відібраного на глибині 5 м південної ділянки Стебницького хвостосховища, + + 2+ 2який містить (мас. %): Na 6,84; К 2,65; Mg 2,13; Cl 13,49; SO4 7,84 і Н2О 67,05, концентрують випарюванням на 40 % з кристалізацією натрію хлориду. Суспензію розділяють, одержуючи 11,96 кг осаду, який містить (мас. %): NaCl 88,84; K2SO4 1,17; КСl 1,04; MgSO4 5,10; Н2О 3,85, і + + 2+ 248,04 кг рідкої фази складу (мас. %): Na 5,54; К 5,25; Mg 4,18; Сl 14,54; SO4 15,14; Н2О 55,35. Одержану рідку фазу охолоджують до кімнатної температури з кристалізацією 8,73 кг калійномагнієвих солей складу (мас. %): K2SO4·MgSO4·4H2O 55,94; NaCl 13,90; КСl 8,74; MgSO4·7H2O 14,04; Н2Огігр 7,38, їх відфільтровують і сушать за температури 120 °C, одержуючи 7,38 кг калімагнезії, яка містить (мас. % у розрахунку на суху речовину): К2О 26,71; MgO 11,82; Сl 17,73, і відповідає вимогам чинних ТУ 6-05743160.002-94 до калімагнезії марки Б. 3 + + Відфільтрований розчин в кількості 39,31 кг з густиною 1300 кг/м складу (мас. %): Na 5,57; К 2+ 22,75; Mg 3,99; Сl 14,96; SO4 10,76; Н2О 61,97, охолоджують до температури мінус 3 °C, унаслідок чого кристалізується 5,87 кг магнію сульфату гептагідрату складу (мас. %): MgSO4·7H2O 87,10; NaCl 2,53; КСl 0,88; MgCl2·6H2O 3,34; Н2Огігр 6,15, який відфільтровують, змішують із 5,87 кг насиченого розчину магнію сульфату і здійснюють репульпаційне промивання. Одержують 5,23 кг промитого магнію сульфату гептагідрату складу (мас. %): MgSO4·7H2O 97,772; NaCl 0,039; КСl 0,342; MgCl2·6H2O 0,029; Н2Огігр 1,818, який відповідає вимогам ТУ 6-46-2319883-09-2001 до магнію сульфату гептагідрату технічного. Приклад 2 Відфільтрований розчин, одержаний аналогічно до прикладу 1, в кількості 39,31 кг з 3 + + 2+ 2густиною 1300 кг/м складу (мас. %): Na 5,57; К 2,75; Mg 3,99; Сl 14,96; SO4 10,76; Н2О 61,97, охолоджують до температури мінус 5 °C, унаслідок чого кристалізується 6,10 кг магнію сульфату гептагідрату складу (мас. %): MgSO4·7H2O 86,89; NaCl 1,86; КСl 0,82; MgCl2·6H2O 3,95; Н2Огігр 6,48, який відфільтровують, змішують із 6,10 кг насиченого розчину магнію сульфату і здійснюють репульпаційне промивання. Одержують 5,43 кг промитого магнію сульфату гептагідрату складу (мас. %): MgSO4·7H2O 97,536; NaCl 0,029; КСl 0,320; MgCl2·6H2O 0,041; Н2Огігр 2,074, який відповідає вимогам ТУ 6-46-2319883-09-2001 до магнію сульфату гептагідрату технічного. Приклад 3 Відфільтрований магнію сульфат гептагідрат, одержаний аналогічно до прикладу 2, в кількості 6,10 кг складу (мас. %): MgSO4·7H2O 86,89; NaCl 1,86; КСl 0,82; MgCl2·6H2O 3,95; Н2Огігр 6,48, змішують з 12,20 кг насиченого розчину магнію сульфату і здійснюють репульпаційне промивання. Одержують 5,41 кг промитого магнію сульфату гептагідрату складу (мас. %): MgSO4·7H2O 97,924; NaCl 0,017; КСl 0,130; MgCl2·6H2O 0,030; Н2Огігр 1,899, який має вищу чистоту порівняно з продуктом, одержаним в умовах прикладу 2, і відповідає вимогам ТУ 2141016-32496445-00 до магнію сульфату гептагідрату. У табл. 1 наведено дані досліджень випарювання початкового розчину до різних ступенів випарювання. 2 UA 75034 U Таблиця 1 Вихід і склад осадів залежно від ступеня випарювання початкового розчину Ступінь випарювання, % 31,30 40,00 47,00 5 Вихід осаду (в розрахунку на суху речовину) Склад осаду, мас. % кг на 100 кг розчину за NaCl, % NaCl K2SO4 КСl MgSO4 Н2О 9,12 49,44 90,15 1,69 3,73 4,43 11,50 61,10 88,84 1,17 1,04 5,10 3,85 14,70 61,22 63,59 1,91 5,55 16,76 12,19 Як видно, за низьких ступенів випарювання одержаний осад натрію хлориду містить невелику кількість домішок, однак вихід його невисокий. За умови випарювання розчину на 47 % кристалізується дрібнодисперсний осад з підвищеною вологістю і високим вмістом домішок, при цьому вихід натрію хлориду порівняно з нижчим ступенем випарювання практично не змінюється. Після відділення кристалів натрію хлориду та охолодження рідкої фази до кімнатної температури одержали осади, вихід і склад яких наведено в табл. 2. 10 Таблиця 2 Вихід і склад осадів, одержаних після відділення кристалів натрію хлориду та охолодження рідкої фази до кімнатної температури Вихід осад) (в розрахунку на суху речовину) Ступінь випарювання за кг на 100 кг за початкового іоном початкового сульфатрозчину, % калію, розчину іоном, % % 31,30 4,57 28,68 38,04 40,00 6,50 38,79 65,52 47,00 9,16 60,25 74,78 Склад осаду мас. % леоніт шеніт астраханіт K2SO4· K2SO4· Na2SO4· NaCl КСl MgSO4· MgSO4· MgSO4· 4H2O 6H2O 4H2O 68,02 20,10 5,41 55,94 13,90 8,74 60,09 16,50 0,44 епсоміт MgSO4· Н2Огігр 7H2O 0,45 14,04 15,19 6,02 7,38 7,78 Одержані осади відфільтровували від розчину та висушували за 120 °C. Вміст основних компонентів у висушених осадах наведено в табл. 3. Таблиця 3 Вміст основних компонентів у висушених осадах Ступінь випарювання калію в перерахунку на початкового розчину, % калію оксид і суху речовину 31,30 22,06 40,00 26,71 47,00 21,63 Вміст в осаді, мас. % магнію в перерахунку на хлору в перерахунку магнію оксид і суху на суху речовину речовину 10,30 15,40 11,82 17,73 9,04 14,08 15 20 Одержані дані показали, що лише осад, одержаний з розчину, випареного на 40 %, за вмістом основних компонентів відповідає вимогам ТУ 6-05743160.002-94 до калійно-магнієвого добрива (калімагнезії) марки Б. + + 2+ 2Відфільтрований розчин складу (мас. %): Na 5,57; К 2,75; Mg 3,99; Сl 14,96; SO4 10,76; Н2О 61,97, охолоджували до низьких температур. При цьому кристалізувалися осади, вихід і склад яких наведено в табл. 4. 3 UA 75034 U Таблиця 4 Вихід і склад осадів, які кристалізувалися з відфільтрованого розчину за низьких температур Температура, °C +5 0 -3 -5 -10 5 Вихід вологого осаду кг на 100 кг за магнію розчину сульфатом, % 10,72 34,36 13,85 44,01 14,93 47,16 15,53 48,94 21,83 66,88 Склад осаду, мас. % епсоміт бішофіт NaCl КСl MgSO4·7H2O MgCl2·6H2O 88,40 1,50 0,65 3,10 87,61 2,14 0,94 3,23 87,10 2,53 0,88 3,34 86,89 1,86 0,82 3,95 84,48 2,54 4,01 3,40 H2Oгiгp 6,35 6,08 6,15 6,48 5,49 Як свідчать наведені результати, у всьому дослідженому температурному інтервалі в тверду фазу виділяється епсоміт. Вихід солі різко зростає з пониженням температури і за температури -10 °C досягає найвищого значення, проте чистота одержаного продукту при цьому істотно. зменшується. Одночасно зниження температури до -10 °C негативно впливає на економічність процесу. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 10 15 20 Спосіб одержання магнію сульфату гептагідрату з сольового розчину, що включає концентрування розчину його випарюванням з кристалізацією натрію хлориду, розділення одержаної суспензії та охолодження рідкої фази з кристалізацією магнію сульфату гептагідрату, який відрізняється тим, що як сольовий розчин використовують розчин хвостосховища калійного виробництва, концентрування розчину його випарюванням здійснюють на 40 %, після розділення одержаної суспензії рідку фазу охолоджують до кімнатної температури з кристалізацією калійно-магнієвих солей, їх відфільтровують і сушать з одержанням калімагнезії, а відфільтрований розчин охолоджують до (мінус 3 - мінус 5) °С з кристалізацією магнію сульфату гептагідрату, його наступним фільтруванням і репульпаційним промиванням насиченим розчином магнію сульфату в кількості 1-2 т на 1 т магнію сульфату гептагідрату. Комп’ютерна верстка В. Мацело Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of magnesium sulphate heptahydrate from salt solution
Автори англійськоюYavorskyi Viktor Teofilovych, Perekupko Tamara Viktorivna, Blazhivskyi Kostiantyn Ivanovych, Maksymovych Ihor Yevstafiiovych, Perekupko Arkadii Viktorovych
Назва патенту російськоюСпособ получения магния сульфата гептагидрата из солевого раствора
Автори російськоюЯворский Виктор Теофилович, Перекупко Тамара Викторовна, Блажевский Константин Иванович, Максимович Игорь Евстафиевич, Перекупко Аркадий Викторович
МПК / Мітки
МПК: C01F 5/40
Мітки: сольового, сульфату, гептагідрату, магнію, одержання, спосіб, розчину
Код посилання
<a href="https://ua.patents.su/6-75034-sposib-oderzhannya-magniyu-sulfatu-geptagidratu-iz-solovogo-rozchinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання магнію сульфату гептагідрату із сольового розчину</a>
Попередній патент: Пристрій для видалення co2 із відпрацьованих газів з установок для виробництва чавуну
Наступний патент: Теплообмінник витий
Випадковий патент: Спосіб внесення мікроелементу цинку на посівах сої