Металокоплексополіорганосилоксани, що містять триядерні комплекси іонів 3d-металів та алюмінію, як адсорбенти з бактерицидними властивостями і спосіб їх одержання
Номер патенту: 18977
Опубліковано: 25.12.1997
Формула / Реферат
1. Металокомплексополіорганосилоксани, що містять триядерні комплекси іонів 3d-металів та алюмінію загальної формули
L -донорний атом кисню, азоту або сірки слідуючих лігандів:
1,4,8,11 - тетраазациклотетрадекан (cyclam) (І)
5,7,12,14 - тетраметил - 1,4.8,11 -тетраазациклотетрадекан (ТМС)
як адсорбенти з бактерицидними властивостями.
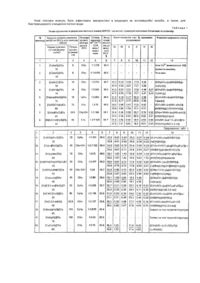
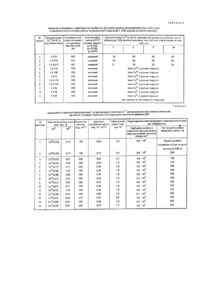
2. Спосіб одержання металокомплексо-поліорганосилоксанів, що містять триядерні комплекси іонів 3d-перехідних металів та алюмінію, який відрізняється тим, що розчин, що містить відповідну комплексну сіль 3d-перехідного металу концентрації від 1,33 * 10-2 до 3,79 · 10-2 моль/л та сіль алюмінію (IIІ) концентрації від 2,67 · 10-2 до 1,07 · 10-1 моль/л при інтенсивному перемішуванні додають до розчину органосиліконату натрію порціями, що не перевищують 0,05 частини об'єму органосиліконату натрію, до досягнення співвідношення в суміші Іони 3d-металу: іони алюмінію (III): органосиліконат = 1 :(2—3) : (75-375) моль/моль/моль з послідуючим введенням в суміш розчину кислоти для утворення гелю, визріванням одержаного гелю, його відмивкою та сушкою.
Текст
Винахід відноситься до хімії кремнійорганічних сполук і, зокрема, до синтезу металокомплексополіорганосилоксанів, що мають біологічну активність. Ці речовини можуть бути використані в хімічній та медичній промисловості, біотехнології, а також фармакології для стримування росту хвороботворних мікроорганізмів, в якості бактерицидних засобів. Відомі сполуки - мідьвміщуючі металокомплексополіорганосилоксани Сu -МКПОС використовуються як адсорбенти, що мають бактерицидні властивості. Ці сполуки є найбільш близькими до заявляємих за структурою та призначенням. Вони характеризуються розвиненою поверхнею, пористою структурою та селективністю по відношенню до адсорбатів різної природи. Але цим речовинам властиві певні недоліки: для них питома поверхня не перевищує 130 м /г, внаслідок чого вони характеризуються недостатньо високою здатністю стримувати ріст хвороботворних мікроорганізмів (недостатні бактерицидні властивості). Крім цього, для відомих сполук спостерігається зниження бактерицидних властивостей на протязі деякого часу за рахунок вимивання іонів металів із матриці при контакті із субстратом. Суть винаходу полягає у синтезі метало-комплексополіорганосилоксанів, що мають високорсзвинену поверхню, міцно закріплені в кремнійорганічній матриці іони 3d-перехідних металів та, в результаті цього, високі бактерицидні властивості. Рішення поставленої технічної задачі досягається одержанням нових металокомплексополіорганосилоксанів, що містять у своєму складі триядерн! комплекси Зс)-ме-талів та алюмінію (III) загальної формули L - донорний атом кисню, азоту або сірки слідуючих лігандів: 1,4,8,11 - тетраазациклодекан (cyclam)(a) та 5,7,12,14 - тетраметил - 1,4,8,11 -тетраазациклотетрадекан (ТМС)(б) Сполуки формули (1) та способи їх одержання відомі не були. Спосіб одержання сполук (1) полягає в тому, що розчин, вміщуючий відповідну комплексну сіль 3dперехідного металу концентрації в розчині від 1,33 · 10~2до3,79 · 10"2 моль/л та сіль алюмінію (III) концентрації від 2,67 · 10-2 до 1,07 · 10-1 моль/л(попередньо одержали шляхом змішування відповідних розчинів солі 3dметалу та солі алюмінію (III) при інтенсивному перемішуванні додають до розчину органосиліконату натрію порціями, що не перевищують 0,05 частини об'єму органосиліконату натрію, до досягнення співвідношення в суміші Іони 3d-металу: іони алюмінію (III): органосиліконат = 1 :(2—3) : (75-375) моль/моль/моль з послідуючим введенням в суміш розчину кислоти для утворення гелю, визріванням одержаного гелю, його відмивкою та сушкою. Концентрація кислоти, час визрівання гелю, процеси відмивки та сушки такі ж як і при синтезі відомих Сu МКПОС. При здійсненні способу істотне значення має порядок додавання реагентів, тому що його зміна не дозволяє одержати речовини, що характеризуються стехіометричним складом, відображеним формулою (І) та відтворюваними властивостями. Суть винаходу пояснюється прикладами 1-20. Як вихідні були використані такі "реактиви: 1) розчин у 5н водному NaOH метил-, етил-, феніл- або вінілсиліконат натрію RSi(OH)2ONa (загальна назва - органосиліконат натрію - ОСН) концентрації 6,0 моль/л: 2) водні розчини відповідних комплексних солей вищевказаних металів концентрації 0,16 моль/л; 3) водний розчин Al2(SO4)3 концентрації 0,32 моль/л: 4) водний розчин 5н H 2SO4. Приклад 1. До 100 мл розчину метилсиліконату натрію при інтенсивному перемішуванні додавали порціями попередньо змішані 5 мл розчину AI2(SO4) 3 з 10 мл розчину CuSO4. Одержаний розчин має синє забарвлення. Після цього проводили процес поліконденсації додаванням 5н H2SO4 до утворення однорідного гелю, який залишали визрівати при кімнатній температурі на протязі 20 годин, потім гель подрібнювали на невеликі шматочки та відмивали дистильованою водою до нейтральної реакції і відсутності реакції на домішки сульфат-іонів. Відмитий гель висушували на повітрі при 25°С до утворення склоподібного твердого продукту блакитного кольору, Вихід готового продукту по відношенню до вихідного метилсилікоиату натрію склав 99,4%. Аналогічно були проведені синтези за прикладами 2-20, кількість взятих для цього вихідних реагентів наведені в таблиці 1. Дослідним шляхом встановлено, що стехіометричний склад та властивості речовин забезпечуються незмінними при варіюванні концентрацій відповідно: ОСН (від 3 до 6 моль/л); AI2(SO4) 3 (від 2,67 · 10-2 до 1,07 * 10-1 моль/л); ML (комплекс металу) (від 1,33 · 10-2 до 3,79 · 10-2 моль/л), при умові витримування такого співвідношення: ML : АІ3+ : ОСН = 1: (2-3) : (75-375) моль/моль/ моль. Наведені в табл.1 результати хімічного аналізу на вміст елементів добре узгоджуються з наведеним складом сполук. Вміст кремнію визначали ваговим методом у вигляді SiO2· Визначення іонів мегалута алюмїнію(ІІІ) у поліорганосилоксанах проводилося атомно-абсорбціиним методом. Калібровочний графік будували на фоні постійної (10 г/л) концентрації органосиліконату натрію. Далі кількість досліджуваного адсорбенту вибирали так, щоб розчин, який аналізують, вміщував таку ж кількість відповідного органосиліконату натрію. Наважку речовини, що містить, у своєму складі комплексні іони 3d-перехідного металу та іони AI3+ розчиняли у 40% водному розчині NaOH при нагріванні та розбавляли кількісно у мірній колбі. Інтенсивність спектральних ліній металів реєстрували атомно-абсорбційним спектрофотометром AAS-3. Аналіз на С, Η, Ν проводили за допомогою елементного аналізатора фірми Карло Fp6a (Італія). Про стан іонів d-металів в синтезованих сполуках робили висновок на основі даних електронної спектроскопії (спектри відбиття в області 300-800 нм записували на спектрофотометрі "Specord Μ 40"). ІЧ спектроскопії (ЛОМО, "ИКС-29"). а також даних ЕПР (спектрофотометр SE/x-2544) з робочою частотою 9400 МГц при температурі 77k. На основі даних електронних спектрів відбиття нових та відомих сполук робили висновок щодо будови координаційного вузла вбудованого комплексу 3d-метапу. На рис, наведені електронні спектри відбиття сорбентів з вбудованими комплексами 3d-перехідних металів, що відповідають табл. 1. Для серії МКПОС з вбудованими комплексами Сu2+ дослідили спектри ЕПР. Проведений комплекс досліджень дозволив встановити, що в залежності в(д будови введеного комплексу та кількості фрагментів.(RSiO15); АІО 1,5(Н2 О); АІО(ОН) 2 утворюються МКПОС такої будови якщо L - монодентатні ліганди: ОН-; Н2О; NH3; NH2CH2CH3; ТiO; ДМСО. R — C 2H5- ; C2H 2-; C6H5-; СН2=СНМ - всі ви щезгадані метали. L - бідентатні ліганди: en, pn, асас, NH2CH2CH2OH, а також (ОН-+ ДМSО). L - 2 en; 2pn: 2acac; 2NH2CH2CH2OH; k.l.k -tet; cyclam; TMC. L - всі ви щезгадані в загальній формулі ліганди. Наприклад, із електронних спектрів відбиття {(C6H5SiO1,5)268[AIO(OH)2 ]2CuNH3)2} (табл.1, зразок 4) можна зробити висновок, що хромофор Сu2+ тетрагонально викривлений та вміщує чо тири атоми кисню та два атоми азоту [СuO4N2] (положення смуг поглинання в області 670-700 нм). З іншого боку, для Сu(NH3)2 - МКПОС. що не вміщують іонів алюмінію (III) (табл.2), іони міді (II) безпосередньо вбудовані в кремнійорганічну матрицю і сигнал ЕПР в цьому випадку не фіксується Із-за малого часу релаксації. Якщо ввести у склад сполуки іони алюмінію (НІ), утворюються спочатку бі а при досягненні співвідношення 1:2 І триядерні комплекси При цьому час релаксації збільшується і стає можливим спостереження спектрів ЕПР для таких сполук . Дійсно, при введенні в склад сполук іонів алюмінію (III) з'являється сигнал ЕПР (g11 = 2,348, g 1 = 2,043, g 0 = 2,150). При цьому спостерігається добра кореляція між відносним вмістом Іонів алюмінію (III) в сполуках та інтенсивністю сигналу ЕПР. При досягненні співвідношення Сu2+ : АІ3+ =1:2 моль/моль інтенсивність сигналу ЕПР досягає максимальної величини, і при подальшому збільшенні вмісту алюмінію (III) не змінюється (табл.2). При цьому досягається найбільш міцне закріплення іонів Сu2+ у структурі матриці і вони вже не вимиваються дією 10%-го розчину аммоніаку (табл.2). При подальшому збільшенні відносного вмісту іонів Аl + їх надлишок вбудовується в структур у матриці. і не впливає на стан як іонів міді (II), так і інших іонів За-металів, що входять до складу нових сполук, хоча позначається на пористій структурі одержаних сполук - сорбентів. На основі хімічного аналізу та даних ЕСП (рис.) зроблено висновок щодо будови хромофору вбудованих комплексів 3d-металів в заявлених сорбентах (номери зразків відповідають табл.1). Крім цього, на основі ЕСВ було зроблено висновок щодо геометричної будови хромофору та його магнітних властивостей: Нові речовини що заявляються, являють собою кремнійорганічні просторово-зшиті матриці, що містять вбудовані триядерні комплекси 3d-металів та алюмінію, що включають об'ємні структурні фрагменти, які регулярно повторюються І описуються заявляемою формулою, тобто характеризуються постійним стехіометричним складом. Наявність матрічної структури обумовлює розвинену пористу стр уктур у та повну нерозчинність у воді, водно-органічних та відомих органічних розчинниках. В табл. 3 наведені адсорбційно-структурні характеристики металокомплек-сополіорганосилоксанів, що містять бі- та триядерні комплекси 3d-металів та алюмінію (III). На основі цих даних слідує висновок, що введення Іонів ΑΙ 3+, крім ефекту закріплення в матриці Іонів 3d-перехІдних металів, дозволяє одержати тонкопористі сорбенти з розвиненою питомою поверхнею, що визначає високий адсорбційний потенціал і, як наслідок, високу адсорбційну активність одержаних сполук. Дослідження бактерицидних властивостей нових сполук та їх порівнення з аналогічними властивостями відомих Сu-МКПОС показали (табл.3), що сполуки які включають у свій склад Бі- та триядерні комплекси Іонів 3d-металів та алюмінію (III), характеризуються сорбційною ємністю по відношенню до патогенних мікроорганізмів у 1,7 - 2,0 рази більшою ніж відомі Сu-МКПОС, а час повної загибелі мікроорганізмів скорочується у 1,8 - 3,5 рази. Аналіз сукупності даних відносно властивостей нових речовин показує, що введення саме бі- та (або) триядерних комп лексів іонів 3d-металів та алюмінію (III) до складу нових сполук дозволяє досягти поставленої мети: одержати металокомплексо-поліорганосилоксани Із міцно закріпленними в структурі матриці іонами 3d-металів, які мають високорозвинену поверхню та бактерицидні властивості. Крім того, встановлено, що в результаті слабкого зв'язування іонів Cu(ll) при контакті відомих сполук із субстратом відбувається їх вимивання із матриці та перехід у розчин, що може призвести до попадання Іонів Cu(ll) в організм та виникненню патологій. ЦІ якості, котрих позбавлені заявляємі нові сполуки, перешкоджають використанню відомих речовин у медицині та біотехнологі). Властивості нових сполук дозволяють рекомендувати їх, на відміну від відомих, як сорбенти для знезаражування рідинних біосубстратів та, в тому числі, питної води. Таким чином, заявляємі речовини відрізняються новим складом та будовою, тобто відповідають критерію новизни. ЦІ відмінності істотні, тому що саме включення в матричну структур у нових сполук триядерних комплексних Іонів ви щеперелічених 3d-металів та алюмінію (III) дозволяє одержати оптимальні адсорбційноструктурні характеристики та високі бактерицидні властивості. Нові сполуки можуть бути ефективно використані в медицині як антимікробні засоби, а також для бактерицидного очищення питної води.
ДивитисяДодаткова інформація
Назва патенту англійськоюMetal-complex polyorganosiloxanes, comprising trinuclear complexes of 3d-мmetals and aluminum ions, as adsorbents having bactericidal properties and a process for obtaining thereof
Автори англійськоюShevchenko Yurii Mykolaiovych
Назва патенту російськоюМеталлокоmплексополиорганосилоксаны, содержащие трехъядерные комплексы ионов 3d-металлов и алюминия, в качестве адсорбентов с бактерицидными свойствами и способ их получения
Автори російськоюШевченко Юрий Николоаевич
МПК / Мітки
МПК: A01N 55/02, A01N 55/10, A01P 1/00, C08G 77/00
Мітки: властивостями, спосіб, бактерицидними, комплекси, триядерні, адсорбенти, металокоплексополіорганосилоксани, іонів, алюмінію, одержання, 3d-металів, містять
Код посилання
<a href="https://ua.patents.su/7-18977-metalokopleksopoliorganosiloksani-shho-mistyat-triyaderni-kompleksi-ioniv-3d-metaliv-ta-alyuminiyu-yak-adsorbenti-z-baktericidnimi-vlastivostyami-i-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Металокоплексополіорганосилоксани, що містять триядерні комплекси іонів 3d-металів та алюмінію, як адсорбенти з бактерицидними властивостями і спосіб їх одержання</a>
Попередній патент: Коагулююча суміш для зневоднення осадів стічних вод
Наступний патент: Клей
Випадковий патент: Спосіб теплової ізоляції металевого розплаву в ковші