Реагент для очищення природних та стічних вод коагуляцією, спосіб його одержання і спосіб очищення води із його використанням
Номер патенту: 109947
Опубліковано: 26.10.2015
Автори: Супрунчук Володимир Ілліч, Алексеєв Олександр Федорович, Нижник Тарас Юрійович
Формула / Реферат
1. Реагент для очищення природних та стічних вод коагуляцією на основі сполуки титану, який відрізняється тим, що як сполуку титану він містить неорганічну та/або органічну сіль та/або оксисіль чотиривалентного титану у вигляді розчину в полярному органічному розчиннику з вмістом титану 0,1-200 г/дм3 в перерахунку на діоксид титану.
2. Реагент за п. 1, який відрізняється тим, що як неорганічну сіль титану він містить сіль кислоти, яку вибирають з ряду, що включає соляну, сірчану, азотну, фосфорну, карбонатну, хлорну та хлорнуватисту кислоти або їх суміші.
3. Реагент за п. 1, який відрізняється тим, що як органічну сіль титану він містить сіль кислоти, яку вибирають з ряду, що включає оцтову, лимонну, яблучну та молочну кислоти або суміш таких солей.
4. Реагент за п. 1, який відрізняється тим, що як органічну сіль титану він містить сполуку титану зі спиртом, який вибирають з ряду, що включає етиловий, ізопропіловий і бутиловий спирти або суміш таких солей.
5. Реагент за будь-яким з пп. 1-4, який відрізняється тим, що він містить полярний органічний розчинник, який вибирають з ряду, що включає етиловий, бутиловий, ізопропіловий, ізоаміловий, полівініловий спирти, пропіленгліколь, гліцерин, ацетон, діетиловий, діізопропіловий, метил-третбутиловий етер, етиловий естер оцтової кислоти та триетиленамін або їх суміш.
6. Спосіб одержання реагенту для очищення природних та стічних вод змішуванням компонентів, що входять до його складу згідно з п. 1, який відрізняється тим, що процеси змішування компонентів і затарювання готового продукту проводять в умовах обмеження доступу вологи в зони змішування і затарювання.
7. Спосіб за п. 6, який відрізняється тим, що процес змішування проводять у герметичному реакторі з відводом тепла, що виділяється.
8. Спосіб за п. 6 або п. 7, який відрізняється тим, що розчинник попередньо зневоднюють до вмісту вологи не більше 15 %.
9. Спосіб очищення природних та стічних вод, який включає змішування титанового коагулянта з водою при інтенсивному перемішуванні, відстоювання та відділення осаду, який відрізняється тим, що як коагулянт використовують реагент за п. 1, який вводять безпосередньо в очищувану воду в кількості, що забезпечує дозу 0,02-10,0 мг/дм3 в перерахунку на діоксид титану.
Текст
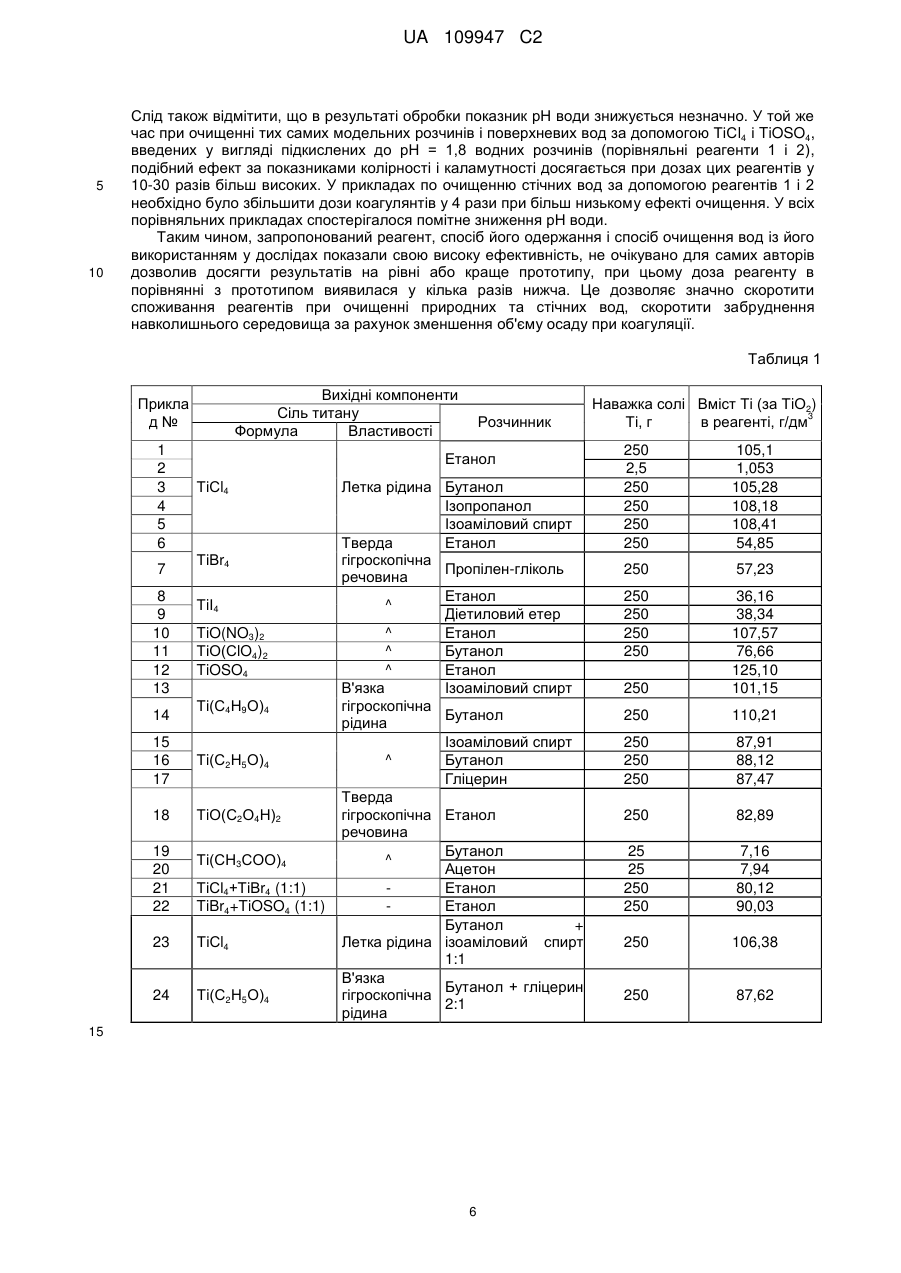
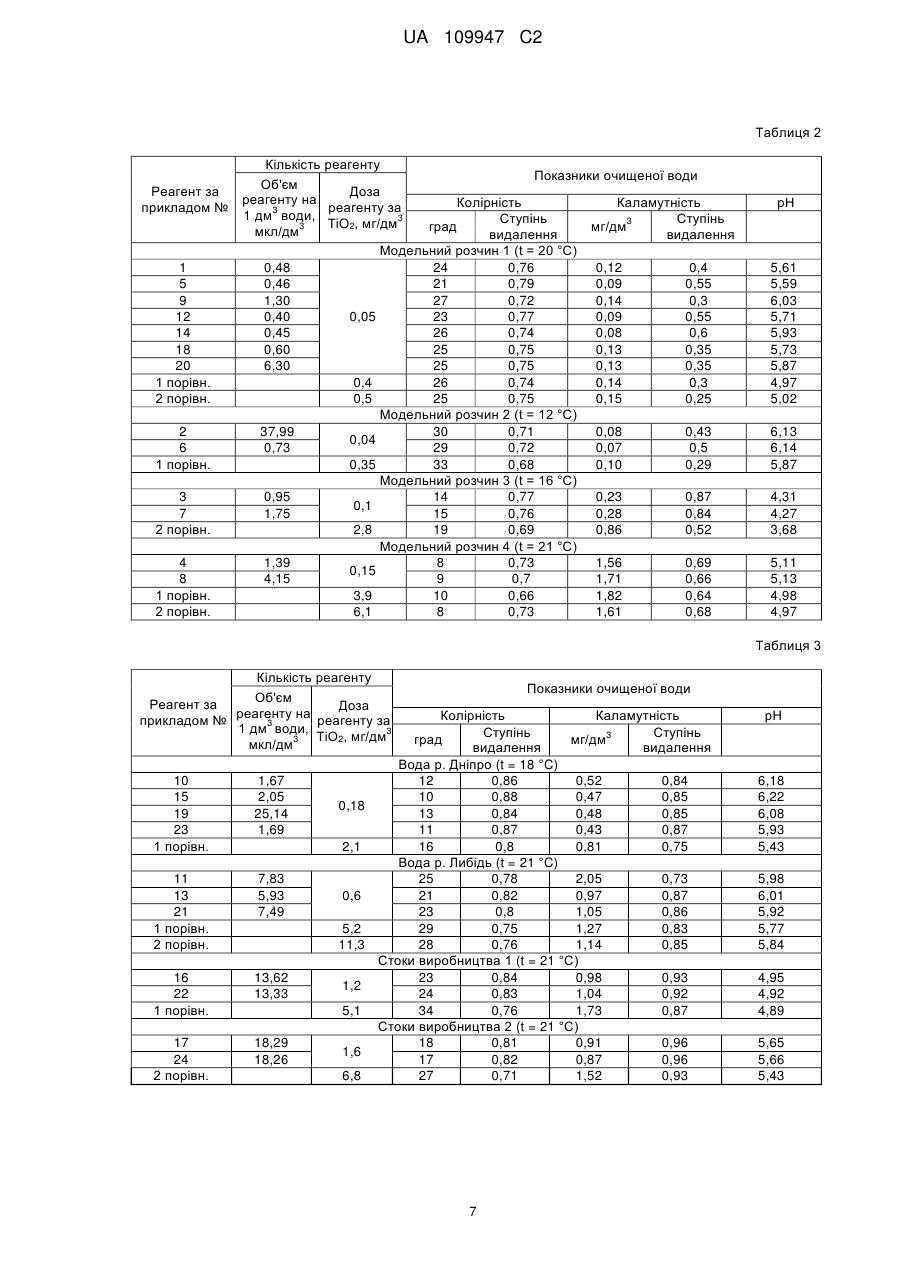
Реферат: Заявлена група винаходів, серед яких реагент для очищення природних та стічних вод коагуляцією, спосіб його одержання і спосіб очищення вод з його використанням. Група винаходів належить до галузі очищення природних та стічних вод від забруднень природного та техногенного походження із застосуванням коагулянтів і може бути використана для вирішення проблем водопостачання і охорони навколишнього середовища. Заявлений реагент для очищення природних та стічних вод коагуляцією на основі сполук титану містить як сполуку титану неорганічну та/або органічну сіль та/або оксисіль чотиривалентного титану у вигляді 3 розчину в полярному органічному розчиннику з вмістом титану 0,1-200 г/дм у перерахунку на діоксид титану. Реагент одержують шляхом змішування компонентів, які входять до його складу, при цьому процес змішування компонентів і затарювання готового продукту проводять в умовах обмеження доступу вологи у зони змішування і затарювання. Реагент застосовують для очищення природних і стічних вод шляхом змішування реагенту з очищуваною водою при інтенсивному перемішуванні з подальшим відстоюванням та відділенням осаду. Реагент 3 вводять безпосередньо в очищувану воду в дозах від 0,02 до 10 мг/дм очищуваної води. UA 109947 C2 (12) UA 109947 C2 UA 109947 C2 5 10 15 20 25 30 35 40 45 50 55 60 Група винаходів належить до галузі очищення природних і стічних вод від забруднюючих сполук природного і техногенного походження із використанням коагулянтів і може бути застосована для вирішення проблем водопостачання та охорони навколишнього середовища. Використання солей титану як реагентів для водоочищення вперше було запропоновано [Upton W.V., Buswell A.M., Industrial and Engineering Chemistry, 1937, 29(8), P. 870-871] в 30-х роках минулого сторіччя. Автори показали, що сульфат титану легко коагулює при низьких температурах та більш ефективно знижує колірність, ніж сульфат алюмінію. Проте, можливо через високу вартість солей титану, протягом тривалого часу спеціалісти по водоочищенню не виявляли до нього значної зацікавленості. На межі минулого і теперішнього сторіч, коли загострилися питання екології, підвищилися вимоги до ступеня очищення природних та стічних вод від органічних сполук, важких металів, мікроорганізмів та інших забруднень, коагулянти на основі алюмінію та заліза, що застосовуються у технології водопідготовки, виявилися недостатньо ефективними, особливо за низьких температур оброблюваної води, а відносно велика залишкова кількість цих токсичних реагентів у воді після очищення створює додаткові ускладнення для виконання вимог екології. В цих умовах стали актуальними і активізувались пошуки нових коагулянтів, і в тому числі, коагулянтів, що містять сполуки титану. В патенті RU № 2087425, МПК6 C02F 1/52, C01F 7/74, опубл. 20.08.1997 г., запропоновано спосіб одержання реагенту для очищення природних та стічних вод шляхом обробки гідроксидів металів II, III та VIII груп періодичної системи елементів кислим титановмісним розчином при температурі не нижче 60 °С і співвідношенні між титаном і металом (або сумішшю металів) рівним 1:0.5-0.7. Показана ефективність одержаного реагенту у вигляді суміші гідроксихлоридів титану і алюмінію чи заліза, чи магнію, чи їх суміші при очищенні природних і стічних вод від важких металів та завислих речовин. Композиція ще більш складного складу запропонована у патенті RU № 2179954, МПК7 C02F 1/52, опубл. 27.02.2002 г. У патенті описана група винаходів, що включає 3 варіанти складу коагулянта для очищення природних та стічних вод і 4 варіанти способу його одержання. Багатокомпонентний коагулянт містить як основу сполуки чотиривалентного титану з високою коагулюючою здатністю та принаймні одну сполуку металу I-IV та VIII груп періодичної системи елементів, а також принаймні одну сполуку V групи періодичної системи елементів при співвідношенні титану і суми металів, рівному 1:(0,1-30). Композиція може містити також сполуку тривалентного титану. Вказані сполуки можуть бути у вигляді гідроксиду, оксиду, солі (хлориду, сульфату, карбонату, фосфату) титану або у вигляді суміші цих сполук. Одержують коагулянт обробкою суміші сполук металів кислим титановмісним розчином при безперервному перемішуванні і нагріванні протягом 2,5-4,5 годин у дві чи три стадії при ступінчатому підвищенні температури від 10 до 120 °С і різних швидкостях нагрівання на кожній стадії, забезпечуючи на 1-й стадії розчинення сполук металів, а на другій і третій стадіях полімеризацію суміші. Багатокомпонентність та багатоваріантність складу та способу синтезу відомого титанового коагулянта дозволяє вибрати оптимальний коагулянт для конкретного типу очищуваної води із досягненням високого ступеня очищення природних і стічних вод. Відомий також багатокомпонентний титановий коагулянт, що містить оксиди, гідроксиди, сульфати, оксигідросульфати, хлориди, оксигідрохлориди титану, алюмінію та кремнію, взяті у перерахунку на оксиди у співвідношенні, % мас.: - оксид алюмінію не більше 76,5, - оксид титану не менше 10,6, - оксид кремнію не менше 5,9, - домішки сполук сірки, заліза, кальцію, хлору не більше 0,5, - вода не більше 7,4. [Патент RU № 2367618, МПК6 C02F 1/52, опубл.20.09.2009 г.] Такий реагент показав свою ефективність і рекомендований для доочищення нафтовмісних пластових солоних вод до води питної якості після двостадійної флотації та пом'якшення. Однією з переваг сполук титану є їх низька токсичність і практична відсутність розчинності у воді продуктів гідролізу, що обумовлює їх перевагу з точки зору екології у порівнянні з широко застосовуваними в наш час алюмінієвими та залізовмісними коагулянтами. Проте описані вище багатокомпонентні титанові коагулянти містять велику кількість сполук інших металів (у тому числі алюмінію та заліза), що можуть стати джерелом вторинного забруднення очищуваної води. Загальним недоліком відомих багатокомпонентних титановмісних коагулянтів є також складність їх складу та технології їх одержання. Тому такі реагенти не знайшли широкого вжитку в практиці водопідготовки. 1 UA 109947 C2 5 10 15 20 25 30 35 40 45 50 55 60 В той же час, враховуючи високі коагулюючі властивості сполук титану і екологічну безпечність продуктів гідролізу, спеціалісти в нинішній час не відмовляються від розробки титанових коагулянтів, проте, намагаючись спростити технологію їх одержання та застосування, звертають увагу на більш прості за складом композиції і навіть індивідуальні сполуки титану. Останнім часом спеціалісти досліджують коагуляційну ефективність тетрахлориду і сульфату титану для визначення можливості застосування цих титанових солей у водоочищенні. В статті авторів Vi-Fan Wu, Wen Liu та ін., що опублікована в «Water research» № 45, 2011 г. с. 3704-3711, описані результати вивчення процесу коагуляції сульфату титану у дозах 0,03-0,3 ммоль/л в дистильованій воді і в суспензіях каолінової глини, що моделюють води з середньою (50-100 мг/л) та низькою (9,8-19,7 мг/л) каламутністю. В суспензії добавляли також бікарбонат натрію від 0 до 120 мг СаСО3/л для моделювання лужності. Автори показали, що найбільш ефективним діапазоном для коагуляції Ti(SO4)2 є рН від 4 до 6 і гарна коагуляція може бути досягнута навіть при дозах 0,03-0,04 ммоль/л (2,4-3,2 мг ТіО2/л) та в діапазоні лужності від 0,06 ммоль/л (15 мг СаСО 3/л) до 0,20 ммоль/л (45 мг СаСО3/л). Для створення оптимальних умов коагуляції Ti(SO4)2 в кислих водах автори додавали необхідну кількість 1,05 М розчину гідроксиду натрію, а в суспензії з високою лужністю (більше 50 мг СаСО3/л) сумісно із коагулянтом вводили 0,5 М розчин сірчаної кислоти. Проведення процесу коагуляції із середньою та низькою каламутністю при оптимальних умовах забезпечувало досягнення доброго ефекту освітлення (залишкова каламутність менше 1,74 мг/л) при дозах Ti(SO4)2 0,07-0,14 ммоль/л (5,6-11,2 мг ТіО2/л). Зроблені авторами на основі лабораторних досліджень висновки про можливу ефективність Ti(SO4)2 для видалення із води природних органічних речовин і зниження каламутності підтверджені експериментами на пілотній установці з очищення води з річки Янцзи (каламутність 23,2-28,4 мг/л, лужність 80-89 мг СаСО3/л, рН = 7,0-7,8, температура 23 °С). 3 Процес очищення води проводили на установці продуктивністю 160 м /добу, що включала перегородчастий коагулятор, вертикальний відстійник та піщаний фільтр. Використовували коагулятор лабораторного типу із часом перебування в ньому води 20 хвилин при швидкості -1 перемішування 25-80 с . При дозах Ti(SO4)2 16-32 мг/л (5,6-10,4 мг ТіО2/л) і регулюванні рН = 5,4-5,6 каламутність води на виході із відстійника складала 1,86-3,25 мг/л, а ступінь видалення кольоровості складав 54-57 %. Таким чином, було показано, що сульфат титану може викликати ефективну коагуляцію в слабокислому середовищі при дозах, які можна співставити з такими для зазвичай використовуваних коагулянтів, і, за думкою авторів, є підходящим реагентом для покращення коагуляції при очищенні поверхневих вод з низькою лужністю або для очищення деяких стічних вод. Мамченко А.В. із співавторами [Химия и технология воды, 2010 г., т. 32, № 3. - С. 309-323] (прототип) провели дослідження ефективності коагулянтів на основі титану (TiOSO4 та ТіСl4) на -3 моделі природної води з такими постійними показниками: іонна сила - 5,5x10 , жорсткість 4,0 3 3 мг-екв/дм , каламутність - 5 мг/дм (введення дисперсії каоліну), колірність - 30° (додавання 3 розчину гумату натрію), а значення рН (5,5-10) та лужності (0,5-5,0 ммоль/дм ) варіювали, додаючи розчини НСl, KОН і NaHCO3. Для підготовки коагулянтів готували концентровані 3 (близько 1,5 моль/дм ) розчини TiOSO4, ТіСl4 і Аl2(SО4)з і як робочі використовували розведені 3 (0,6 г-екв Me/дм ) розчини зі значенням рН 0,9, 0,6 і 1,8, відповідно. Процес очищення води проводили наступним чином: в модельну систему дозували коагулянт у вигляді свіжоприготованого робочого розчину, перемішували у двостадійному режимі: 2 хв. при 250 об/хв. і 10 хв. при 90 об/хв. (режим аналогічний тому, який використовується у виробничих умовах на Деснянський водопровідній станції м. Києва) і залишали відстоюватись протягом години. Після відстоювання визначали каламутність, лужність і значення рН, після чого воду фільтрували і визначали показники якості очищеної води. Проведені дослідження по визначенню оптимальних доз коагулянтів для досягнення 3 задовільного ефекту очищення води (каламутність у відстояній воді не більше 2 мг/дм , залишковий вміст металу нижче ГДК, колірність не вища за 20°) залежно від рН і лужності оброблюваної води показали, що в умовах проведених експериментів титанові солі більш ефективні, ніж сульфат алюмінію при очищенні води з невисокою лужністю (менше 5 3 ммоль/дм ) і рН менше 7,0 або більше 9,0, тобто в тих умовах, в яких сульфат алюмінію не працює. В той же час в оптимальній для сульфату алюмінію області рН = 7-9 при середніх значеннях лужності, каламутності, колірності води і температурі 18-20 °С цей реагент 3 забезпечує той же самий ступінь очищення при дозах 0,081-0,098 мг-екв/дм , тобто на 20 і 50 % 3 3 менших, ніж у титанілсульфату (0,102-0,12 мг-екв/дм ) і хлориду титану (0,113-0,145 мг-екв/дм ). 2 UA 109947 C2 5 10 15 20 25 30 35 40 45 50 55 Таким чином, проведені лабораторні дослідження, хоча й мають певні протиріччя отриманих результатів та рекомендацій, дають певні орієнтири для розробки технології очищення природних вод і промислових стоків із використанням як коагулянтів індивідуальних солей титану. Проте при створенні промислових технологій необхідно враховувати деякі особливості солей титану, такі, як гігроскопічність (для твердих солей), леткість (для рідин) і властиву їм усім дуже високу швидкість гідролізу у воді. Леткість і гігроскопічність солей титану ускладнює процеси їх зберігання і транспортування, оскільки вимагає виконання умов герметичності при затарюванні, зберіганні, використанні. Через високу швидкість гідролізу титанових солей дозування їх безпосередньо в очищувану воду небажане, оскільки важко досягти гарного розподілення коагулянта у воді: сіль гідролізує раніше, ніж досягається якісне її змішування з водою по всьому об'єму для забезпечення найкращого захоплення домішок та найбільш повного використання коагулянта. Використання для дозування попередньо приготованих робочих водних розчинів коагулянта не вирішує цієї проблеми, оскільки гідроліз відбувається вже при приготуванні робочого розчину, що призводить до втрат коагулянта та утворенню продуктів гідролізу, які можуть закорковувати дозуюче обладнання, виводячи його з ладу. Для попередження гідролізу робочі водні розчини готують в умовах значного зниження рН додаванням кислот. Так, у прототипі в робочому розчині TiOSO4 забезпечували рН = 0,9, а у розчині ТіСl4 - рН = 0,6. Використання таких робочих розчинів забезпечує більш рівномірне розповсюдження м при дозуванні в очищувану воду, однак внесення значних кількостей кислоти може знижувати лужну ємність води, вимагаючи додаткового внесення підлужуючих агентів. Крім того для приготування, зберігання та дозування таких розчинів потрібні корозійно- і кислотостійке обладнання. Все це ускладнює технологію і апаратурне оформлення процесу очищення води при використанні титанових коагулянтів. Задачею групи винаходів є спрощення процесу коагуляційного очищення води на стадії підготовки і дозування титанового коагулянта з одночасним підвищенням ефективності застосовуваного реагенту. Поставлена задача вирішена запропонованою групою винаходів, що включає новий склад реагенту для коагуляційного очищення природних та стічних вод, спосіб його одержання і спосіб очищення вод із застосуванням нового реагенту. Запропонований реагент для очищення природних та стічних вод коагуляцією містить сполуку чотиривалентного титану, вибрану із широкого кола його органічних та/або неорганічних та/або оксисолей, у вигляді її розчину в полярному органічному розчиннику з 3 вмістом титану від 0,1 до 200 г/дм у перерахунку на диоксид титану. Як неорганічну сіль титану запропонований реагент містить сіль кислоти, обраної з ряду, який включає в себе соляну, сірчану, азотну, фосфорну, карбонатну, хлорну і хлорнуватисту кислоти або їх суміші. Як органічну сіль титану реагент містить сіль кислоти, вибраної з ряду, який включає оцтову, лимонну, яблучну та молочну кислоти або сполуки титану зі спиртом, вибраним з ряду, який включає етиловий, ізопропіловий та бутиловий спирти або їх суміші. Як розчинник у складі запропонованого реагенту використовують органічний розчинник, вибраний з широкого кола таких розчинників: етиловий, бутиловий, ізопропіловий, ізоаміловий, полівініловий спирти, пропіленгліколь, гліцерин, ацетон, діетиловий, діізопропіловий, метилтретбутиловий етер, етиловий естер оцтової кислоти та триетиленамін або їх суміші. Запропонований реагент одержують змішуванням компонентів, які входять до його складу, в необхідному співвідношенні, проте, у зв'язку гігроскопічністю солей титану та небажаним гідролізом при попаданні значної кількості вологи, процес змішування компонентів і затарювання готового продукту ведуть в умовах обмеження доступу вологи (з повітря або у складі розчинника, який додають). Це досягається шляхом попереднього зневоднення розчинника (до вмісту вологи менше 15 %) та/або забезпечення герметичності апаратури, особливо при використанні летких сполук титану. Запропонований спосіб очищення води із застосуванням нового реагенту відрізняється від використаної у прототипі традиційної технології коагуляційного очищення, що включає підготовку робочого розчину коагулянта, його дозування в очищувану воду, інтенсивне перемішування, відстоювання та фільтрацію, тим, що коагулянт вносять (дозують) 3 безпосередньо в очищувану воду в дозах (від 0,02 до 10 мг/дм ) значно менших, ніж у відомих способах очищення із застосуванням відомих титанових коагулянтів. 3 UA 109947 C2 5 10 15 20 25 30 35 40 45 50 55 Використання як коагулянтів в процесах водопідготовки індивідуальних солей титану у вигляді розчинів в полярних органічних розчинниках дозволяє значно розширити асортимент титанових коагулянтів, спростити технологію процесу очищення води на стадії підготовки і дозування коагулянта, оскільки запропонований реагент вводиться безпосередньо в очищувану воду, а не у вигляді попередньо приготованих кислих робочих розчинів, при цьому не відбувається значного зниження рН та лужної ємності оброблюваної води та нема необхідності у використанні корозійно- та кислотостійкого обладнання. Запропонований реагент практично не взаємодіє із вологим повітрям, що також спрощує його використання і дозування, а після розповсюдження у воді його органічна складова вже не протидіє процесу гідролізу титанової солі і гідроліз протікає швидко та ефективно, чим забезпечується досягнення більш високих показників якості водоочищення. В наведених нижче прикладах очищення вод з різним характером забруднень показана висока ефективність запропонованих реагентів, яка проявляється у значному зниженні ефективних доз реагентів у порівнянні із дослідженими в прототипі титановими солями (ТіСl4 та TiOSO4), що застосовуються у вигляді кислих водних розчинів. Досягнутий ступінь зниження доз коагулянта при очищенні поверхневих вод (у 10-30 раз) є непередбачуваним результатом навіть для авторів винаходу. Нижче наведені приклади реалізації заявленої групи винаходів. У прикладах №№ 1-24 представлено спосіб одержання та конкретний склад одержаних зразків запропонованого реагенту, а в прикладах з очищення модельних (приклад № 25), поверхневих (приклад № 26) та стічних (приклад № 27) вод, наведено основні технологічні параметри процесів коагуляції і показники якості очищеної води, що підтверджують ефективність нового реагенту. Приклади №№ 1-24 Для одержання зразків запропонованого реагенту використовували різноманітні солі титану у вигляді хімічних реактивів вітчизняного виробництва (ТіСl4, TiOSO4 - виробництва ОАО «Титан»), а також реактивів категорії «ч» і «чда» з каталогів фірм «Мерк» та «Алдріч». Полярні органічні розчинники використовували вітчизняного і закордонного виробництва категорії «ч». Процес одержання зразків реагенту проводили в атмосфері очищеного і висушеного азоту, створеній у герметичному реакторі, обладнаному мішалкою та охолоджуючою водною 3 сорочкою. В реактор вміщували 1 дм розчинника та переносили з герметичної ємності розраховану кількість титановоїсолі. Розчинники із високим вмістом вологи попередньо зневоднювали до вмісту вологи не вище 15 %. Компоненти перемішували з одночасним відводом тепла, що виділяється, циркулюючою у сорочці водою, охолодженою до 6 °С. Процес вели до повного розчинення солі. У всіх прикладах одержали однорідні прозорі або злегка опалесцюючі рідини, при находженні яких у відкритій ємності на повітрі (вологість 78 %, t = 19 °С) протягом не менше двох годин не спостерігалося ніяких змін, які б свідчили про те, що відбувається гідроліз. Точний вміст титану у готовому реагенті визначали ваговим методом, осаджуючи його у вигляді ТіО2 шляхом гідролізу солі за допомогою розчину NH4OH. Данні щодо використаних вихідних компонентів, якісного і кількісного складу одержаних за прикладами 1-24 зразків запропонованого реагенту наведено в табл. 1. Вміст титану в зразках реагенту приведено в перерахунку на ТіО2. Наведені приклади здійснення винаходу вказують на можливість одержання достатньо стійких за часом рідких реагентів на основі різноманітних солей або суміші солей титану з використанням широкого кола розчинників у великому діапазоні вмісту активної речовини. Для підтвердження ефективності одержаних реагентів при коагуляційному очищенні води та визначення основних параметрів процесу проводили досліди по очищенню вод із різноманітним характером забруднень (приклади 25, 26 і 27). Приклад № 25 У даному прикладі зразки реагенту застосували для очищення розчинів, що моделюють води з різними показниками колірності, каламутності і рН, при температурному режимі 12-21 °С. Для одержання модельних розчинів у дистильовану воду вносили препарат гумату натрію виробництва фірми «Алдрич» (для моделювання природної колірності) і стандартну суспензію каоліну в необхідних кількостях (моделювання каламутності). рН регулювали шляхом додавання 0,05 М розчину НСl. Було одержано 4 варіанти розчинів з такими характеристиками: 4 UA 109947 C2 Колірність, град. Модельний розчин 1 Модельний розчин 2 Модельний розчин 3 Модельний розчин 4 5 10 15 20 25 30 35 40 45 50 98 102 62 30 Каламутність, 3 мг/дм 0,20 0,14 1,78 5,10 рН 6,54 7,40 4,75 5,50 Модельний розчин 1 за характеристиками подібний водам у застійних водоймах (болотах та повільно текучих річках) у літньо-осінній період, для яких характерні висока колірність, низька каламутність, трохи кислий рН. Такі води вимагають для очищення великих доз традиційних коагулянтів. Модельний розчин 2 за своїми характеристиками подібний до води у застійних водоймах у весняний період. Для них характерні висока колірність і низька каламутність. Очищення такої води вимагає високих доз традиційних коагулянтів і не завжди дозволяє досягнути задовільного результату. Модельний розчин 3 за своїми характеристиками подібний до побутових стоків після первинного очищення. Для них характерна відносно невисока колірність, достатньо висока каламутність та низьке значення рН. Для очищення таких вод за допомогою традиційних коагулянтів потрібно введення значних доз підлужуючих реагентів. Модельний розчин 4 за показниками колірності, каламутності і рН подібний одному з варіантів модельної системи у відомому способі очищення стічних вод [А.В. Мамченко и др. Химия и технология воды, 2010 г., т. 32, № 3, с. 309-323]. Завданням коагуляційного очищення таких вод, як правило, є доведення до придатності для споживання людьми, тобто до відповідності основних показників вимогам СанПіН 2.2.4-171-10 для питної води: колірність не більше 30 градусів кобальтово-біхроматної шкали, каламутність 3 не більше 2,9 мг/дм . Процес коагуляції проводили у ємностях об'ємом 1,5 л, які були оснащені мішалками, куди 3 вносили 1 дм очищуваної води і додавали реагент з числа одержаних за прикладами №№ 124, у кількості, розрахованій виходячи з попередньо визначеної ефективної дози. Суміш перемішували у 2-х стадійному режимі: 0,5 хв. при 250 об/хв. і 10 хв. при 20 об/хв., а потім відстоювали протягом години, спостерігаючи утворення та осідання пластівців ТіО2. Після цього воду відділяли від осаду і визначали каламутність, колірність і значення рН очищеної води. Паралельно проводили очищення тої ж води, застосовуючи як коагулянт свіжоприготований водний розчин ТіСl4, підкислений НСl до рН = 1,8 з вмістом титану (у перерахунку на ТіО2) 105,2 3 г/дм (порівняльний реагент 1) чи водний розчин TiOSO4, підкислений H2SO4 до рН = 1,8 із 3 вмістом титану (у перерахунку на ТіО2) 125,6 г/дм (порівняльний реагент 2). Основні параметри процесу коагуляції і показники якості очищеної води наведені у табл. 2. Приклад № 26 У даному прикладі проводили очищення природних вод, відібраних із поверхневих джерел водопостачання з високим рівнем забруднення: з річки Дніпро у весняний період (колірність 83 3 градуси, каламутність 3,22 мг/дм , рН = 6,67) і річки Либідь у літній період (колірність 116 3 градусів, каламутність 7,54 мг/дм , рН = 6,15). Задача очищення - доведення основних показників очищеної води до відповідності вимогам стандартів для питної води. Приклад № 27 Запропонований реагент застосували для коагуляційного очищення виробничих стічних вод 3 із високим вмістом органічних речовин: колірність 140 градусів, каламутність 13,51 мг/дм , рН = 5,61 (стоки виробництва 1) і стоків з великим вмістом заліза (більше 80 г/л): колірність 93 3 градуси, каламутність 21,55 мг/дм , рН = 6,21 (стоки підприємства 2). Стоки підприємства 1 - це суміш побутових стоків та стоків цеху фарбування, а стоки виробництва 2 - суміш побутових стічних вод та стоків цеху металообробки і травлення. Метою очищення виробничих стічних вод, за звичай, є доведення їх показників до відповідності нормам, що встановлені для вод, які скидаються у каналізацію. Процеси коагуляції зразками запропонованого реагенту, а також із застосуванням порівняльних реагентів у прикладах № 26 і № 27 проводили, як описано у прикладі № 25, а дані щодо зразків, доз реагентів та результатів очищення вод наведені в табл. 3. Наведені в табл. № 2 і № 3 дані щодо результатів коагуляційного очищення вод (з рН = 4,757,4) із застосуванням нового реагенту вказують, що у всіх випадках досягнуто високої ефективності видалення забруднень і за показниками каламутності і колірності очищена вода задовольняє вимогам, що встановлені для питної води, навіть у випадку обробки стічних вод. 5 UA 109947 C2 5 10 Слід також відмітити, що в результаті обробки показник рН води знижується незначно. У той же час при очищенні тих самих модельних розчинів і поверхневих вод за допомогою ТіСl4 і TiOSO4, введених у вигляді підкислених до рН = 1,8 водних розчинів (порівняльні реагенти 1 і 2), подібний ефект за показниками колірності і каламутності досягається при дозах цих реагентів у 10-30 разів більш високих. У прикладах по очищенню стічних вод за допомогою реагентів 1 і 2 необхідно було збільшити дози коагулянтів у 4 рази при більш низькому ефекті очищення. У всіх порівняльних прикладах спостерігалося помітне зниження рН води. Таким чином, запропонований реагент, спосіб його одержання і спосіб очищення вод із його використанням у дослідах показали свою високу ефективність, не очікувано для самих авторів дозволив досягти результатів на рівні або краще прототипу, при цьому доза реагенту в порівнянні з прототипом виявилася у кілька разів нижча. Це дозволяє значно скоротити споживання реагентів при очищенні природних та стічних вод, скоротити забруднення навколишнього середовища за рахунок зменшення об'єму осаду при коагуляції. Таблиця 1 Вихідні компоненти Сіль титану Формула Властивості Прикла д№ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 Розчинник Етанол ТіСl4 ТіВr4 ТiІ4 TiO(NO3)2 ТіО(СlO4)2 TiOSO4 Ті(С4Н9О)4 15 16 17 Тi(С2Н5О)4 18 ТiО(С2О4Н)2 19 20 21 22 Ті(СН3СОО)4 23 ТіСl4 24 Тi(С2Н5О)4 ТіСl4+ТіВr4 (1:1) TiBr4+TiOSO4 (1:1) Летка рідина Бутанол Ізопропанол Ізоаміловий спирт Тверда Етанол гігроскопічна Пропілен-гліколь речовина Етанол ^ Діетиловий етер ^ Етанол ^ Бутанол ^ Етанол В'язка Ізоаміловий спирт гігроскопічна Бутанол рідина Ізоаміловий спирт ^ Бутанол Гліцерин Тверда гігроскопічна Етанол речовина Бутанол ^ Ацетон Етанол Етанол Бутанол + Летка рідина ізоаміловий спирт 1:1 В'язка Бутанол + гліцерин гігроскопічна 2:1 рідина 15 6 Наважка солі Вміст Ті (за ТiО2) 3 Ті, г в реагенті, г/дм 250 2,5 250 250 250 250 105,1 1,053 105,28 108,18 108,41 54,85 250 57,23 250 250 250 250 250 36,16 38,34 107,57 76,66 125,10 101,15 250 110,21 250 250 250 87,91 88,12 87,47 250 82,89 25 25 250 250 7,16 7,94 80,12 90,03 250 106,38 250 87,62 UA 109947 C2 Таблиця 2 Кількість реагенту Показники очищеної води Об'єм Реагент за Доза реагенту на Колірність Каламутність прикладом № реагенту за 3 1 дм води, 3 Ступінь Ступінь 3 ТiO2, мг/дм 3 град мг/дм мкл/дм видалення видалення Модельний розчин 1 (t = 20 °C) 1 0,48 24 0,76 0,12 0,4 5 0,46 21 0,79 0,09 0,55 9 1,30 27 0,72 0,14 0,3 12 0,40 0,05 23 0,77 0,09 0,55 14 0,45 26 0,74 0,08 0,6 18 0,60 25 0,75 0,13 0,35 20 6,30 25 0,75 0,13 0,35 1 порівн. 0,4 26 0,74 0,14 0,3 2 порівн. 0,5 25 0,75 0,15 0,25 Модельний розчин 2 (t = 12 °C) 2 37,99 30 0,71 0,08 0,43 0,04 6 0,73 29 0,72 0,07 0,5 1 порівн. 0,35 33 0,68 0,10 0,29 Модельний розчин 3 (t = 16 °C) 3 0,95 14 0,77 0,23 0,87 0,1 7 1,75 15 0,76 0,28 0,84 2 порівн. 2,8 19 0,69 0,86 0,52 Модельний розчин 4 (t = 21 °C) 4 1,39 8 0,73 1,56 0,69 0,15 8 4,15 9 0,7 1,71 0,66 1 порівн. 3,9 10 0,66 1,82 0,64 2 порівн. 6,1 8 0,73 1,61 0,68 рН 5,61 5,59 6,03 5,71 5,93 5,73 5,87 4,97 5,02 6,13 6,14 5,87 4,31 4,27 3,68 5,11 5,13 4,98 4,97 Таблиця 3 Кількість реагенту Об'єм Реагент за Доза реагенту на прикладом № реагенту за 3 1 дм води, 3 ТіО2, мг/дм 3 мкл/дм 10 15 19 23 1 порівн. 1,67 2,05 25,14 1,69 11 13 21 1 порівн. 2 порівн. 7,83 5,93 7,49 16 22 1 порівн. 13,62 13,33 17 24 2 порівн. 18,29 18,26 Показники очищеної води Колірність Каламутність Ступінь Ступінь 3 град мг/дм видалення видалення Вода р. Дніпро (t = 18 °C) 12 0,86 0,52 0,84 10 0,88 0,47 0,85 0,18 13 0,84 0,48 0,85 11 0,87 0,43 0,87 2,1 16 0,8 0,81 0,75 Вода р. Либідь (t = 21 °C) 25 0,78 2,05 0,73 0,6 21 0,82 0,97 0,87 23 0,8 1,05 0,86 5,2 29 0,75 1,27 0,83 11,3 28 0,76 1,14 0,85 Стоки виробництва 1 (t = 21 °C) 23 0,84 0,98 0,93 1,2 24 0,83 1,04 0,92 5,1 34 0,76 1,73 0,87 Стоки виробництва 2 (t = 21 °C) 18 0,81 0,91 0,96 1,6 17 0,82 0,87 0,96 6,8 27 0,71 1,52 0,93 7 рН 6,18 6,22 6,08 5,93 5,43 5,98 6,01 5,92 5,77 5,84 4,95 4,92 4,89 5,65 5,66 5,43 UA 109947 C2 ФОРМУЛА ВИНАХОДУ 5 10 15 20 25 30 1. Реагент для очищення природних та стічних вод коагуляцією на основі сполуки титану, який відрізняється тим, що як сполуку титану він містить неорганічну та/або органічну сіль та/або оксисіль чотиривалентного титану у вигляді розчину в полярному органічному розчиннику з 3 вмістом титану 0,1-200 г/дм в перерахунку на діоксид титану. 2. Реагент за п. 1, який відрізняється тим, що як неорганічну сіль титану він містить сіль кислоти, яку вибирають з ряду, що включає соляну, сірчану, азотну, фосфорну, карбонатну, хлорну та хлорнуватисту кислоти або їх суміші. 3. Реагент за п. 1, який відрізняється тим, що як органічну сіль титану він містить сіль кислоти, яку вибирають з ряду, що включає оцтову, лимонну, яблучну та молочну кислоти або суміш таких солей. 4. Реагент за п. 1, який відрізняється тим, що як органічну сіль титану він містить сполуку титану зі спиртом, який вибирають з ряду, що включає етиловий, ізопропіловий і бутиловий спирти або суміш таких солей. 5. Реагент за будь-яким з пп. 1-4, який відрізняється тим, що він містить полярний органічний розчинник, який вибирають з ряду, що включає етиловий, бутиловий, ізопропіловий, ізоаміловий, полівініловий спирти, пропіленгліколь, гліцерин, ацетон, діетиловий, діізопропіловий, метил-третбутиловий етер, етиловий естер оцтової кислоти та триетиленамін або їх суміш. 6. Спосіб одержання реагенту для очищення природних та стічних вод змішуванням компонентів, що входять до його складу згідно з п. 1, який відрізняється тим, що процеси змішування компонентів і затарювання готового продукту проводять в умовах обмеження доступу вологи в зони змішування і затарювання. 7. Спосіб за п. 6, який відрізняється тим, що процес змішування проводять у герметичному реакторі з відводом тепла, що виділяється. 8. Спосіб за п. 6 або п. 7, який відрізняється тим, що розчинник попередньо зневоднюють до вмісту вологи не більше 15 %. 9. Спосіб очищення природних та стічних вод, який включає змішування титанового коагулянта з водою при інтенсивному перемішуванні, відстоювання та відділення осаду, який відрізняється тим, що як коагулянт використовують реагент за п. 1, який вводять 3 безпосередньо в очищувану воду в кількості, що забезпечує дозу 0,02-10,0 мг/дм в перерахунку на діоксид титану. 35 Комп’ютерна верстка Д. Шеверун Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Назва патенту англійськоюReactant for purification of natural and waste water by coagulation, process for preparation thereof and water purification method using thereof
Автори англійськоюNyzhnyk Taras Yuriiovych, Suprunchuk Volodymyr Illich, Alekseiev Oleksandr Fedorovych
Назва патенту російськоюРеагент для очистки природных и сточных вод коагуляцией, способ его получения и способ очистки воды с его использованием
Автори російськоюНижник Тарас Юрьевич, Супрунчук Владимир Ильич, Алексеев Александр Федорович
МПК / Мітки
МПК: C01G 23/00, C02F 1/52, B01J 21/06
Мітки: природних, води, коагуляцією, очищення, вод, використанням, стічних, реагент, спосіб, одержання
Код посилання
<a href="https://ua.patents.su/10-109947-reagent-dlya-ochishhennya-prirodnikh-ta-stichnikh-vod-koagulyaciehyu-sposib-jjogo-oderzhannya-i-sposib-ochishhennya-vodi-iz-jjogo-vikoristannyam.html" target="_blank" rel="follow" title="База патентів України">Реагент для очищення природних та стічних вод коагуляцією, спосіб його одержання і спосіб очищення води із його використанням</a>
Попередній патент: Масообмінний апарат
Випадковий патент: Спосіб управління електроприводами неперервної технологічної лінії обробки металу тиском