Спосіб одержання імуногену, який стимулює імунну систему людини, зараженої hiv
Текст
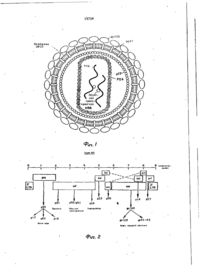
Способ получения иммуногена, стимулирующего иммунную систему человека, зараженного HIV, заключающийся в том, что зараженные HIV клетки выращивают в сре де RPMI 1640 в присутствии эмбриональной сыворотки крупного рогатого скота, 5-7дневный супернатант фильтруют, к фильтрату добавляют/?-прапиолактон и инкубируют в течение 5 ч при 37°С и рН среды, 7,2-7.4. после чего замораживают, облучают гаммалучами, размораживают, концентрируют, пропуская через миллипоровые полисульфоновые фильтры, очищают вначале центрифугированием с 30%-ной сахарозой, затем центрифугированием в градиенте 30-45%ной сахарозы, а целевой продукт получают ресуспендированием полученного осадка в PBS буфере при концентрации 1 мл на 10 л исходного вещества. С > Настоящее изобретение относится к борьбе с ретровирусами, более конкретно к способу получения иммуногена, стимулирующего иммунную систему человека, зараженного HIV. На дату приоритета данного изобретения патентная и научно-техническая литература не содержит сведений о получении высокоэффективного средства для борьбы с ретровирусами, преимущественно ретровирусом HIV. Задачей изобретения является создание высокоэффективного средства для борьбы с ретровирусами, преимущественно ретровирусом HIV. Поставленная задача решается предлагаемым способом получения стимулирующего иммунную систему человека, зараженного HIV, заключающимся в том, что зараженные HIV клетки выращивают в сре де RPMI 1640 в присутствии эмбриональной сыворотки крупного рогатого скота. 5-7дневный супернатант фильтруют, к фильтрату добавляют/J-пропиолактон и инкубируют в течение 5 часов при 37°С и рН среды 7,27,4, после чего замораживают, облучают гамма-лучами, размораживают, концентрируют, пропуская через миллипоровые полисульфоновые фильтры, очищают вначале центрифугированием с 30%-ной сахарозой, затем центрифугированием в градиенте 3045%-ной сахарозы, а целевой продукт получают ресуспендированием полученного осадка в PBS буфере при концентрации 1 мл на 10 л исходного вещества. Для пояснения изобретения приводятся фиг. 1-4, причем на фиг.1 представлена схематическая модель HIV. Как показано на фиг.2. геном РНК HIV кодирует три основных структурных гена: со СО 13734 4 Полоски по Вестерну с пятнами иммуногена pal и env, которые фланкированы на в результате скрининга гомологичными сыоґюик концах длинными концевыми дупливоротками человека. кациями (LTR) Ген ддд кодирует специфические белки ядра, р55. рЗЭ, р24, р17 и р15. Как показано схематически на фиг.З. выГены доД кодируют обратную транскриптазу 5 сокие уровни антитела против др160/120 рВ5/р51 и протеазу рЗІ. Гены en у кодируют (наружная оболочка), которые присутствуют гликопротеин наружной мембраны др120 и в бессимптомной фазе заражения HIV, такего предшественник др1ВО, а также трансже продолжают существовать в симптомной м^мбпанный гликопротеин др41. Некоторые фазе. Уровень антитела р24 в бессимптоми? геков являются чрезвычайно вариабель- 10 ной фазе является высоким, но, по-видимоными, в частности, гены епу. Кроме того, му, снижается в с и м п т о м н о й фазе. существуют пять других генов, не присутстАналогично, HIV-сероположительные сывовующих в других ретровирусах, которые лиротки содержат антитело, которое ингибирубо вовлечены в транскрипционную или ет функцию обратной транскриптазы. У трансляционную регуляцию, либо кодируют 15 пациентов, в которых антитело против обдругие структурные белки. Структура гена ратной транскриптазы присутствует на выHIV известна. Она описана Ратнером и др. соких уровнях, попытки относительно Nature. 313, стр. 277 (1985). выделения вируса менее часто положительны, нежели у тех, в которых оно отсутствует. HIV присоединяется к клеткам хозяина путем взаимодействия мембранных гликоп- 20' Поэтому следует, что уменьшение клеточных ротеинов с поверхностным рецептором и гуморальных иммуноэащитных факторов, клетки. Оказывается, что при контакте HIVc таких, как Т4-клетки и антитела против GAG, клеткой Т4 протеин др120 взаимодействует включая анти~р24, и антитела против рої, с рецептором CD4. Вирусная оболочка завключая антитело против обратной транстем сливается с клеточной мембраной и 25. криптазы, связано с развитием HIL до спивнутреннее ядро вируса входит в зараженда. ную клетку, где транскрипция РНК в вирус Используемый в данном описании терДНК катализируется обратной транскриптамин "HIV" включает типы 1 и 2 и является зой. Провирус может оставаться в клетке в синонимом HTUHII. LAV-1 и LAV-2. H I V O T латентной форме в течение нескольких ме- 30 носится к вирусу в общем смысле и включает сяцев или лет, и все это время зараженный все формы, подтипы и вариации. индивидуум является бессимптомным. ОдИспользуемый в данном описании тернако, если вирус позднее активируется, вымин "белок наружной оболочки" относится к зывая вирусную репликацию и той части мембранного глілкопротеина реиммуносупрессию, индивидуум будет затем 35 тровируса, которая выступает за пределы восприимчивым к условно-патогенным зарамембраны, в противоположность трансмемжениям, включая рак, ассоциируемым со бранному белку, др41. Белок наружной обоспидом. лочки HIV является синонимом др120 и его предшественника дрібО. На фиг.З представлено схематическое воспроизведение уровня некоторых антител 40 . Используемый в данном описании термин и антигенов, присутствующих в развитии из "др120" или "др160/120" относится к гликопробессимптомного состояния до состояния теинам, имеющим либо антигенную специфичARC (связанный со спидом комплекс) и до ность, либо биологическую функцию белка спида у HIV - сероположительных пациеннаружной оболочки; др160. как полагают, являтов, зараженных HIV. 45 ется предшественником др120. На фиг.? представлены результаты анаИспользуемый в данном описании терлиза по Вестерну иммуногена по примеру 1, мин "генный продукт" относится к полипепкоторые показывают, что"ом свободен от тиду или белку, который кодируется геном. белков наружной оболочки при скрининге Термин, как предполагают, включает в себя гомологичными и гетерологичными сыворот- 50 белковые производные, такие, как гликопроками, которые содержат высокие титры антеины. Понятно, что в аминокислотную потитела против белков наружной оболочки. А; следовательность генного продукта могут Коммерческие полоски по Вестерну с пятнабыть внесены ограниченные модификации ми HIV в результате скрининга гетерологичбез нарушения биологической функции или иыми сыворотками шимпанзе; Б: Полоски по 55 иммуногенности генного продукта, и только Вестерну с пятнами иммуногена в результачасть первичной последовательности может те скрининга гетерологичными сыворотками потребоваться для иммуногенности. шимпанзе; В: Коммерческие полоски с HIVИдентификация HIV-специфических гепятнами по Бестерну в результате скрининнов и генных продуктов основана на термига гомологичными сыворотками человека; Г; нологии HIV типа 1, представленной на 13734 фиг.1. Предполагается, однако, что ссылка на специфический ген или"генный продукт Н1\/типа 1, на основе его молекулярной массы, будет также включать соответствующий ген или генный продукт HIV типа 2 и, когда присутствует гомологичный ген, другие ретровирусы. Генные продукты других типов и родов могут иметь незначительно отличающиеся молекулярные массы. Например, gp41 HIV типа 1 эквивалентен дрЗб типа 2, тогда как др120 типа 1 соответствует дМЗО типа 2. HIV можно культивировать из пробы периферической крови зараженных индивидуумов. Например, одноядерные клетки из периферической крови, такие, как лимфоциты, могут быть получены путем наслоения пробы гепаринизированной венозной крови по градиенту плотности Ficoll-Hypaque и центрифугирование пробы. Одноядерные клетки затем собирают, активируют, например, фитогемагглютинином, в течение двухтрех дней и культивируют в подходящей среде, предпочтительно заполненной интерлейкином 2. Вирус может быть обнаружен либо анализом на обратную транскриптазу, анализом с захватом антигена для р24, иммунофлюоресценцией, либо электронной микроскопией для обнаружения присутствия вирусных частиц в клетках. Все эти методы хорошо известны специалистам в данной области. После выделения вирус может быть включен в другие клетки. 6 Для иммунизации человека или ШИРОполучаемый предлагаемым г.погобом иммуноген применяется вместе со вспомогательными веществами. Но он может также применяться в своей водной форме без вспомогательного вещества. При этом дозу выбирают так, чтобы она была иммунологически эффективной, и она, как правило, составляет от 1 до 100 мкг белка, предпочтительно, около 30 мкг белка Активную иммунизацию осуществляют и, предпочтительно, повторяют раз с минимальным интервалом, по меньшей мере, 90 дней, хотя дополнительные ревакцинации могут подходить в соответствии с изменениями в уровне иммунной активности на основе, например, уменьшения количества антител против HIV-генным продуктом, другим, нежели белки наружной оболочки Такую иммунизацию предпочтительно осуществляют первоначально путем внутримышечной иньекции с последующей внутрикожной иньекцией, хотя может быть использована любая комбинация внутрикожной и внутримышечной инъекции ТНОГО 5 10 15 20 25 30 Важно использовать неинфекционную вакцину с тем, чтобы избежать проникнове- 35 ния инфекции в хозяина. Различные методы хорошо известны для придания болезнетворному организму неинфекционности. Вирус можно инактивировать или сделать репликационно-недостаточным. Пред- 40 почтительно, однако, обрабатывать его комбинацией бета-пропиолактона и гаммаизлучения. При этом /?-пропиолзктон должен находиться в контакте с вирусом, как минимум, 2,5 ч. С тем, чтобы полностью уда- 45 лить какой-либо остаточный бета-пропиолактон, бета-пропиолактон должен оставаться в растворе в течение, как минимум, пяти часов при температуре 37°С. Выделенный вирус затем обрабатывают 50 так, чтобы удалить белки наружной оболочки, Такое удаление предпочтительно осуществляют неоднократными замораживанием и оттаиванием вируса в сочетании с физическими методами, которые вызывают набуха- 55 ние и сокращение вирусных частиц, хотя также можно использовать другие физические и нефизические методы, такие, как разрушение ультразвуком, в отдельности или в сочетании друг с другом. Предпочтительно, иммунокомпетентность или иммунную активность сероположительного индивидуума определяют перед иммунизацией с тем, чтобы определить подходящий путь лечения. В качестве метода такого определения сыворотки пациентов подвергают скринингу на присутствие антител против р24 (например, при помощи иммуноферментного твердофазного анализа), антитела против обратной транскриптазы и/или уровня клеток Т4 при помощи хорошо известных методов. Пациенты, проявляющие индикаторы низкой иммунокомпетентности, например, низкие титры р24 или антитела против обратной транскриптазы или низкие количества клеток Т4, являются подходящими кандидатами для пассивной иммунотерапии, предпочтительно, в сочетании (проводимой перед или совместно) с активной иммунизацией. Серонегативные индивидуумы могут быть вакцинированы с тем, чтобы вызвать иммунозащитные факторы для предотвращения инфекции. Предпочтительно, вакцину вводят первоначально путем внутримышечной инъекции с последующим введением бустера, осуществляемым либо внутримышечно, либо внутрикожно. Физиологически эффективная доза содержит предпочтительно от 1 до 100 мкг, от 1 до 100 мкг, и более предпочтительно, около 30 мкг иммуногена. Вакцину предпочтительно вводят в сочетании с адъювантом, т.е. вспомогательным веществом, наиболее предпочтительно, адьювэнтом для обеспечения 13734 8 мораживают при температуре -70°С. Замо• роженный супернатант затем подвергают гамма-облучению кобальтом мощностью 4 5 MR. 5 Раствор супернатанта затем оттаивают и концентрируют путем 40-кратной фильтрации через выполненные с молярной массой 100 000 фильтры. Концентрат подают в снабженные мешалкой колбы Т-21, предвари10 тельно обработанные 70%-ным иэопропанолом. и центрифугируют при 28000 об/мин в течение часа. Супернатант удаляют и осадок повторно суспендируют в содержащем ЭТУК натриевом буфере до об15 щего конечного объема приблизительно 24 мл 4 мл этой суспензии расслаивают над 8 мл 30%-ной сахарозы в полиалломерных пробирках, предварительно обработанных 70%-ным изопропанолом, и центрифугиру20 ют в течение одного часа при 28000 об/мин. Супернатант сливают из 30%-ной сахарозы и осадок ресуспендируют в указанном натриевом буфере. Градиент в ультрасветлых центрифуж25. ных пробирках, предварительно обработанных 70%-ным изопропанолом, Такие антиидиотипные антитела могут устанавливают путем прибавления 3 мл быть получены методами, хорошо известны45%-й сахарозы в пробирку и наложения ми в данной области. сверху 6 мл 30%-й сахарозы. 3 мл вышеопиИзобретение иллюстрируется следую30 санной суспензии наслаивают на раствор. щими примерами. Пробирки центрифугируют в течение 60 мин Пример 1. Получение вирусных частиц, при 28000 об/мин. свободных от белков наружной оболочки. Клетки, зараженные штаммом HIV No. Раствор над слоями при 35%-м перехо-. Hz 321 (выделившимся из плазмы 26-летней де отсасывают пипеткой и сливают. Слои из африканской женщины из Заира) выращива- 35 всех пробирок соединяют в одной коничеют в среде А, состоящей из RPMI 1640 с ской пробирке и разбавляют в соотношении 10%-ной эмбриональной сыворотки крупно1:10 фосфатсодержащим буферным солего рогатого скота, 25 мМ буфера HEPES, 50 вым раствором. Раствор центрифугируют в мкг/мл гентамицина и 100 мгк/мл стрептополиалломерных пробирках, предварительмицина. 40 но обработанных 70 %-ным изопропанолом, Культуры увеличивают в объеме путем в течение 1 ч при 28000 об/мин. Супернаподачи исходных клеток в центрифужные тант удаляют и осадки в пробирках ресуспробирки и доведения объема приблизипеидируют в указанном фосфатсодержащим тельно до 8 л добавкой предварительно набуферном растворе при концентрации 1 мл гретой среды А. При этом степень 45 н а 10 л исходного вещества. ~ разведения составляет приблизительно 1:5. Альтернативно, особенно, когда иммуЗатем осуществляют второе разведение в ноген получают в больших количествах, стасоотношении 1:3. СупернаЧант от 5-7-дневдию облучения можно осуществлять после ной суспензии HIV-зараженных клеток объединения слоев. Затем вирус расслаивафильтруют через фильтр размером 0,45 50 ют на градиенте 15-50%-й сахарозы. Вимкм. Свежеприготовленный раствор 1:40 русные слои объединяют и бета-пропиолактона прибавляют к суперресуспендируют в вышеуказанном фосфатнатанту до конечной концентрации 1:4000. содержащем буферном растворе. Вирус Раствор инкубируют в течение 5 ч при темцентрифугируют при 28000 об/мин в течепературе 37°С и рН поддерживают на уров- 55 ние 1 ч и ресуспендируют в упомянутом не 7,2-7.4. буферном растворе до конечной концентЧерез 5 ч 20 мл раствора супернатанта рации, равной 1,0 мг/мл. удаляют с тем, чтобы определить уровень Количество имеющегося белка опредеинфективности и количество оставшегося ляют в соответствии с методом Бредфорда бета-пропиолэктона Затем супернатант за(см. Anaf. Biochem 72 стр. 248, 1976 г). получения препарата типа "вода в масле". Различные подходящие адьювэнты хорошо известны в данной области Кроме того, поскольку антитела против qp 1B0/120 могут содействовать вирусной абсорбции клетками, эти специфические антитела могут быть удалены из пациента, зараженною HIV, перед иммунотерапией. Иммуносорбентные колонки выполненные из полых целлюлозных волокон, модифицируют с тем, чтобы ковалентно связать лиганды, реакционноспасобные с антитепами противдр 160/120 Такие лиганды включают антигены др 160/120, полученные из очищенных гликопротеинов, которые в свою очередь получены из только что собранных вирусных частиц или из культурального супернатанта HIV-продуцирующих Т4-лимфоцитов. Альтернативно, такие лиганды могут быть получены методами рекомбинантной ДНК с использованием трансфецировэнных клеток. Альтернативно, идиотипы, реакционноспособные с антителами против др 160/120 могут быть использованы для этих целей. 13734 10 Как показано на фиг.4, коммерческие Белок разбавляют вышеуказанным фосполоски с имеющимися на них белками HIV фатсодержащим буферным раствором до подвергнутые скринингу с гетерогоіичной концентрации, равной 1.0мг/мл. сывороткой (шимпанзе А86-С и А-3) и содерУровень остаточного бета-пропиолактона в иммуногене определяют с использова- 5 жащие высокие титры антител против белков н а р у ж н о й оболочки, др 160/120 нием к а п и л л я р н о г о га з о - ж и д к о с т н о г о являются негативными (нероакционноспохроматографа. При этом приготовляют стансобными) на полосках, полученных при анадартные растворы бета-пропиолактона и лизе полученного вышеописанным образом масляной кислоты, имеющие концентрации между I и 500 частями на миллион. Пробы 10 иммуногена, свободного от нар/жной оболочки. Гомологические человеческие сывообъемом 2 мкм вводят в капиллярный хромаротки (003 и 010), содержащие высако-титры тограф в соответствии с рекомендацией изантител против белков наружной оболочки, готовителя. Предел обнаружения составляет др 160/120, являются реакционноспособны0,1 ч/милл. Иммуноген содержит менее, чем 0,05 ч/милл, бетэ-пропиолактона. 15 ми с коммерческими полосками но негативными с полосками, полученными из Восемь проб иммуногена анализируют иммуногена, свободного от наружной обона содержание бета-пропиолактона капиллочки. Как гомологические, так и гетерологилярной газовой хроматографией, используя ческие сыворотки вступают во масляную кислоту в качестве внутреннего взаимодействие с другими генными продукстандарта. Используют следующие хрома- 20 тами HIV. тографические условия: колонка: 30 м х 0,25 мм, кварцевое стекло, открытая, трубчатая; Отсутствие белков наружной оболочки стационарная фаза: 100%-ный цианопрона предлагаемом иммуногене подтверждапил-кремний; температура ввода пробы ют электронной микроскопией. К иммучо140°С; рабочая температура: 70° С/1 мин, 25 г е н н о м у п р е п а р а т у последовательно 20° С/мин до 130°С; методика.ввода пробы: добавляют 2,5%-ный глутаральдегид и осминерасщепляющая. При вышеприведенных евый ангидрид, дегидратируют с помощью условиях время удерживания бета-пропиорастворов этанола разных концентраций и лактона и масляной кислоты соответствует заливают в EPON-812. Тонкие шлифы пол7,52 мин и 6,70 мин, соответственно. Ввод 2 30 учают с помощью прибора LKB Microtome мкл 1 ч/милл, раствора бета-пропиолактона (фирма LKB, Упсала, Швеция) с использоваприводит к получению пика, который может нием алмазного скальпеля. Толщина шлибыть измерен количественно Концентрация фов составляет 60 нм. Шлифы окрашивают 1 ч/милл раствора до 1/10 его объема упауранилацетатом и лимоннокислым свинцом, риванием растворителя при температуре 35 наблюдают и фотографируют с использова40°С при пониженном давлении не привонием электронного микроскопа марки Цейс дит к ощутимой потери бета-пропиолактона, 109. Служащие в качестве контроля клетки, Предел обнаружения после концентрации зараженные HIV, подготовляют с использосоставляет 0,1 ч/милл./0,1 мкг/мл. ванием той же методики. При этом обнаруж и в а ю т , что и м м у н о г е н не имеет 40 темно-окрашенную наружную оболочку, коС тем, чтобы подтвердить то, что иммуторая присуща контрольным пробам и котоноген свободен от белков наружной оболочрая отражает др 160/120 на вирусной ки, иммуноген вначале разделяют на поверхности. 11,0%-ных полиариламидных гелях с применением додецилсульфата натрия в соответ- 45 Пример 2. Иммунотерапия сероположиствии со способом Лэммли, см. Nature 227, тельных индивидуумов. стр. 680,1970 г). Очищенный материал затем Девять пациентов, сероположительных переносят на нитроцеллюлозную бумагу в к HIV, лечат иммунотерапией при даче имсоответствии с методом, предложенным Тамуногена по примеру 1. При этом иммуноген убином и др. (см. Proc, Nature. Acad. Sci., 76, 50 эмульгируют в соотношении 1:1 в неполном стр. 4350, 1979 г.) и иммуноокрашивают в адъюванте Фройнда в эмульсификаторе соответствии с методом, предложенным марки Spex 8000MixerMiH инофирмы Спекс Цанг и др. (см. Meth. Enzymalogy. 92. стр. Индастриз Инк., США. 1,0 мл раствора, со377, 1983 г.). Как можно видеть на фиг.4, держащего 100 мкг белка, вводят внутримыпятна полученного таким образом иммуно- 55 шечно Бустер 100 мкг белка без адъюванта гена не имеют полосу, соответствующую вводят через 90 дней путем внутрикожной др 120/160, как указано в контрольных инъекции. испытаниях, при взаимодействии с сывоПрисутствие вируса HIV в лимфоцитах ротками, содержащими высокие титры периферической крови пациентов опредеанти-др 160/120. ляют как до, так и после иммунизации путем 11 12 13734 из которых HIV выделен перед иммунизасокультивирования вместе со свежепригоцией, не проявляют выделяемый вирус товленными лимфоцитами периферической вплоть до 12 недели после иммунизации. грпви, стимулированными фитогемагглютиПациенты 008 и 009 не являются переносчинином и интерлеикином-2 в соответствии с ками вируса вплоть до 8 недели после иммуметодом Галло и др. (см J СИп Microb , 25, н и з а ц и и . Все четыре этих п а ц и е н т а стр. 1291, 1987 г.) Оборудование для обнапроявляют высокие титры анти-р24 (>1:5000) ружения присутствия антигенов HIV, таких, и антитела против обратной транскриптазы как р24, коммерчески доступно {например, (> 1:1000) перед иммунизацией. Остальные от инофирмы Е И. Дю-Пон энд Де-Немурс Ко., Инк, США). Каждого пациента обследу- 10 пять пациентов, которые проявляют низкие титры анти-р24 и антитела против обратной ют три раза перед иммунизацией и через транскриптазы перед иммунизацией, про2.4.6,8,12 и 14 недель после иммунизации. должают проявлять выделяемый вирус поВ следующей таблице представлены ресле иммунизации. зультаты исследований. Пациенты 010 и 003, .15 Иммунологические и вирусологические профили у сероположительных к HIV пациентов перед и после иммунизации ' ^ Пациент Цитологический Иммунологический анализ Вирусологический анализ „ анализ Т-4 После Перед Анти АОТ 1 } НА2> Перед После (недели) р24 2 4 6 8 12 003 51В 671 250000 2560 40 + 010 229 297 500000 10240 80 371 16000 2560 80 _ 288 4+ _ 008 + 009 219 261 8000 2560 80 + 001 296 280 3200 640 40 198 3200 20 40 + 237 - ++ + + 004 + + + + + 007 261 ?77 400 20 20 005 180 259 200 80 10 + + + + + 228 98 170 20 + + + , ' Антитело против обратной транскриптазы ' Нейтрализующее антитело. * 14 + + + + + + + + + 13734 gp!20 Иемйранэ UPID Обратная транскриптаза Р66 Геном HIV 9 1 і і і 1 1 1 tat Ц^ gag 5* LTR { рЗ( •jt^ Протеаза p24 pl5 r • p23 р66/р5І P 34 Обратили Энюнуклеаэа t p2O p(4 % erf 3' LTR env art I ялр* tat 80f рої < _-jart] 1 gpl 60 9РІ2О &елки нарулпоЯ p27 (киво-осип Антитело против р24 Антиооолочка и нейтрализующее антитело }Ь-^--Н-^—X Н Антитело против обратной транскриптазы X * X Антиген р24 со о. л Т1 AC R Бессимптомно Фиг. 3 Спид 13734 A Б Aae-c A~3 9p160 '9РІ20 9P160 9РІБ0 ЭР120 рбв P55 P66 рбб P55 ЭР41 P39 P39 P31 P24 P31 p17 P24 P21 PI5 Pt7 P15 003 010 9P160 gp120 t 003 010 9P1B0 gp!20 9P150 9P12O рбб P55 *. P39 pee рбв P55 P31 1 p39 P24 P21 РІ7 P1S p31 P27 Фиг, Упорядник Замовлення 4121 Техред М.Моргентал pf5 Коректор М, Керецман Тираж Підписне Державне патентне відомство України, 254655, ГСП. КиТв-53, Львівська пл., 8 Відкрите акціонерне товариство "Патент", м. Ужгород. вул.ГагарІна 101
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 39/12
Мітки: спосіб, стимулює, людини, одержання, імунну, зараженої, імуногену, систему
Код посилання
<a href="https://ua.patents.su/10-13734-sposib-oderzhannya-imunogenu-yakijj-stimulyueh-imunnu-sistemu-lyudini-zarazheno-hiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання імуногену, який стимулює імунну систему людини, зараженої hiv</a>
Попередній патент: Електроліт залізнення
Наступний патент: Спосіб виробництва етилового спирту
Випадковий патент: Контейнер