Спосіб одержання похідних тіазолу або їх солей приєднання кислот, 5-хлор-3-тіоціанато-2-алканон та спосіб його одержання
Номер патенту: 34443
Опубліковано: 15.03.2001
Автори: Карбоніц Дежьо, Хейя Гергей, Дьюре Карой, Міхаловіч Дьордь, Кішш Пал, Боней Іштван, Хусар Чаба, Сабо Ержебет, Кеварі Арпад, Бутткаі Ілдіко, Бан Карой, Лєдніцкі Ласло, Гараці Шандор, Неймет Аттіла, Морас Ференц, Шютьо Міхай, Дьорі Петер, Молнар Ержебет, Салай Ержебет, Палоші Ендре, Свобода Іда, Гьонці Чаба, Шпербер Ференц
Текст
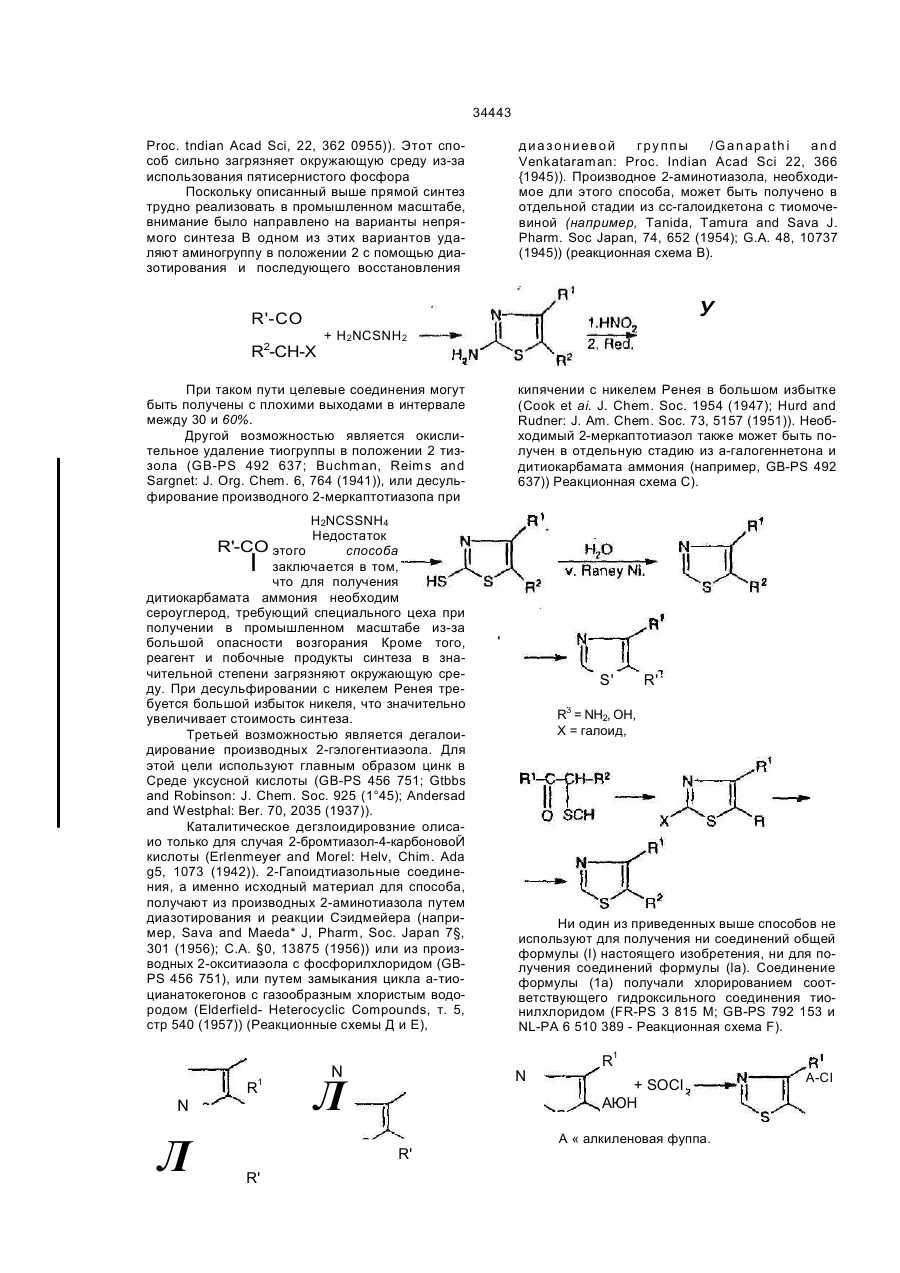
1 Способ получения производных тиаэола общей формулы сн, т. где R означает Сг-5-алкил с прямой цепью, замещенный атомом хлора в положении 2, или их солей присоединения кислот, отличающийся тем, что проводят взаимодействие 5-хлор-З-тиоцианато-2-алканона общей формулы R--- СН----С~СН, SCN (IV) в органическом растворителе с газообразным хлористым водородом чтобы получить 2-хлор-4-метил-5-(2-хлоралкил)тиазол общей формулы N R сн, СІ а затем гидрируют соединение общей формулы (II) в присутствии металлического катализатора в органическом растворителе, чтобы получить 4-метил-5-(2хлоралкил) тиазол общей формулы (I), где R имеет указанные ранее значения, и не обязательно превращают соединение общей формулы (I), где R имеет указанные значения, или его гидрохлоридную соль известным способом в другую соль присоединения кислоты, или выделяют свободное соединение общей формулы (I) где R имеет указанные ранее значения, из его соли присоединения кислоты 2 Способ по п 1, отличающийся тем, что R яв ляется 2-хлорэтипом 3 Способ по п 1, отличающийся тем, что в ка честве металлического катализатора при гидри ровании используют палладий на активирован ном угле, не обязательно содержащий селен 4 Способ по пп 1-3, отличающийся тем. что проводят гидрирование в присутствии связываю щего кислоту агента, предпочтительно в при сутствии триэтиламина 5 Способ по пп 1-4, отличающийся тем, что в качестве органического растворителя исполь зуют алифатические спирты, сложные эфиры жирных кислот, образованные алифатическими спиртами ароматические углеводороды или простые эфиры с открытой цепью 6 Способ по пп 1-5, отличающийся тем. что проводят гидрирование при атмосферном или более высоком давлении но не выше, чем при давлении 0 7 МПа 7 Способ по пп 1-6, отличающийся тем, что проводят реакцию замыкания цикла соединений общей формулы (IV) в соединения общей форму лы (II) в безводном несмешивающемся с водой растворителе, который не растворяет воду, пред почтительно в бутилацетате 8 Способ по пп 1-7. отличающийся тем, что проводят реакцию замыкания цикла соединений общей формулы (IV) в соединений общей форму см о г со О) 34443 лы (II) при температуре в интервале от 0пС до 100°С 9 Способ по п 1, отличающийся тем, что соединения формулы (IV) получают взаимодействием соединения (V) сн—с—сн3 где R - С?-5 - алкил с прямой цепью, замещенный атомом хлора в положении 2. 11 Соединение по п 10, где R является 2хлорэтипом 12 Способ получения 5-хлор-3-тиоцианато-2-эпканон общей формулы (IV) по пп. 10 или 11, от личающийся тем, что проводят взаимодействие соединения общей формулы (V) R о (V), где R имеет указанные значения, с неорганическим тиоцианатом и без выделения из реакционной смеси вводят во взаимодействие нз следующей стадии по п. 1 10. 5-хлор-З-тиоцианато-2-алканон общей формулы (IV) R- СН—С—СН3 SCN Настоящее изобретение относится к способу получения 4-метил-5-(2-хлоралкил)-тиаэопов общей формулы .СИ, N где R означает Сг-«-апкип с прямой цепью, замещенный атомом хлора в положении 2, с помощью частично известных промежуточных продуктов. Соединение общей формулы Із R---- СН—С—СН3 CI (V) с неорганическим тиоцианатом. 13 Способ по п. 12, отличающийся тем, что неорганический тиоцианат выбран среди тиоциа-ната натрия, тиоцианата калия и тиоцианата аммония. 14. Способ по п. 12 или 13, отличающийся тем, что процесс проводят в присутствии растворителя, такого как алифатические спирты, алифатические кетоны, сложные эфиры жирных кислот с алифатическими спиртами или вода. работе по способам первого типа 2-незамещенный тиазоп получают в одну стадию. В соответствии со способами второго типа получают производные тиагола, содержащие легко удапяемый заместитель в положении 2, и удаляют этот заместитель во второй стадии. Согласно способам первого типа тиазольное кольцо образуется при взаимодействии галоидированного кетона или альдегида, которые галоидированы 8 а-положении, или альдегида с тиоформзмидом (Elderfield, R.C.: Heterocyclic Compounds, т. 5, стр. 516 (1957)) (Реакционная схема А). , HCSNH, N FV-CO 2 R СН2-СН2-С! и его соли присоединения кислот (Клометиаэюл) является терапевтически широко применяемым активным ингредиентом антиконвульсивных и седативных средств. Соединение формулы (fa) первоначально было описано в 1935 г. (J. Am Chem. Soc. §7, 1876 (1935)). Его гидрохлоридная и этандисульфонвтная соли были описаны в GBPS792 158 Его фосфонатнзи соль известна из US-PS3 639 415. Известные способы получения производных тиаэола. незамещенных в положении 2, могут быть разделены иа два основных типа При сн-х R1 и R2 = алкил, арил или водород; X - галоид. Этот тип способов дает хороший вывод только в некоторых случаях (Buchman and Richardson: J. Am Chem. Soc. 67, 395 (1945); Erne, Ramires and Burger: Helv. Chem. Asta 34, 143 (1951)). Другим недостатком этого способа является трудность получения чистого тиоформамида. Для преодоления этого затруднения получение тиоформэмида проводят в реакционной смеси из формамида и пятисернистого фосфора, но этот способ является успешным только в некоторых случаях (Ganapathi and Venkataraman' 34443 Proc. tndian Acad Sci, 22, 362 0955)). Этот способ сильно загрязняет окружающую среду из-за использования пятисернистого фосфора Поскольку описанный выше прямой синтез трудно реализовать в промышленном масштабе, внимание было направлено на варианты непрямого синтеза В одном из этих вариантов удаляют аминогруппу в положении 2 с помощью диазотирования и последующего восстановления д и а з о н и ев о й г ру п п ы / G a n ap a t h i and Venkataraman: Proc. Indian Acad Sci 22, 366 {1945)). Производное 2-аминотиазола, необходимое дли этого способа, может быть получено в отдельной стадии из сс-галоидкетона с тиомочевиной (например, Tanida, Tamura and Sava J. Pharm. Soc Japan, 74, 652 (1954); G.A. 48, 10737 (1945)) (реакционная схема В). У R'-CO R2-CH-X + H2NCSNH2 При таком пути целевые соединения могут быть получены с плохими выходами в интервале между 30 и 60%. Другой возможностью является окислительное удаление тиогруппы в положении 2 тиззола (GB-PS 492 637; Buchman, Reims and Sargnet: J. Org. Chem. 6, 764 (1941)), или десульфирование производного 2-меркаптотиазопа при H2NCSSNH4 Недостаток R'-CO этого способа заключается в том, что для получения дитиокарбамата аммония необходим сероуглерод, требующий специального цеха при получении в промышленном масштабе из-за большой опасности возгорания Кроме того, реагент и побочные продукты синтеза в значительной степени загрязняют окружающую среду. При десульфировании с никелем Ренея требуется большой избыток никеля, что значительно увеличивает стоимость синтеза. Третьей возможностью является дегалоидирование производных 2-гэлогентиаэола. Для этой цели используют главным образом цинк в Среде уксусной кислоты (GB-PS 456 751; Gtbbs and Robinson: J. Chem. Soc. 925 (1°45); Andersad and Westphal: Ber. 70, 2035 (1937)). Каталитическое дегзлоидировзние олисаио только для случая 2-бромтиазол-4-карбоновоЙ кислоты (Erlenmeyer and Morel: Helv, Chim. Ada g5, 1073 (1942)). 2-Гапоидтиазольные соединения, а именно исходный материал для способа, получают из производных 2-аминотиазола путем диазотирования и реакции Сэидмейера (например, Sava and Maeda* J, Pharm, Soc. Japan 7§, 301 (1956); C.A. §0, 13875 (1956)) или из производных 2-окситиаэола с фосфорилхлоридом (GBPS 456 751), или путем замыкания цикла а-тиоцианатокегонов с газообразным хлористым водородом (Elderfield- Heterocyclic Compounds, т. 5, стр 540 (1957)) (Реакционные схемы Д и Е), кипячении с никелем Ренея в большом избытке (Cook et ai. J. Chem. Soc. 1954 (1947); Hurd and Rudner: J. Am. Chem. Soc. 73, 5157 (1951)). Необходимый 2-меркаптотиаэол также может быть получен в отдельную стадию из а-галогеннетона и дитиокарбамата аммония (например, GB-PS 492 637)) Реакционная схема С). I 1 R N Л N Л R' 3 R = NH2, ОН, X = галоид, Ни один из приведенных выше способов не используют для получения ни соединений общей формулы (I) настоящего изобретения, ни для получения соединений формулы (la). Соединение формулы (1а) получали хлорированием соответствующего гидроксильного соединения тионилхлоридом (FR-PS 3 815 М; GB-PS 792 153 и NL-PA 6 510 389 - Реакционная схема F). N R' R' S' R1 + SOCI АЮН А « алкиленовая фуппа. A-CI 34443 Дпя Клометиазола формулы (!а) был описан способ, в соответствии с которым окисляют подходящее 2-меркаптопроизводное перекисью водорода (CH-PS 200 24В) 2-Хпор-4-метил-5-(2-хлорэтил)-тиазол формулы вестными вообще способами Они также могут быть получены при взаимодействии соединений общей формулы (IV) с водной минеральной кислотой и превращении полученных таким образом 2-окси-4-метил-5-(2-хлоралкил)тиазопов общей формулы -СН, (Acta Pharm, Suec. 8, с 49 (1982) и 2-окси-4-метил-5-(2-хлорэтил)-тиазол формулы (Ufa) (Acta Pharm Suec |9, с 37 (1982) являются известными соединениями Однако ни одно из этих соединений не было заявлено как подходящий промежуточный продукт для получения соединения формулы ((а) Во всех общих формулах R имеет указанные выше значения. Неожиданно мы обнаружили, что при взаимодействии известного 3,5-дихлор-2-алханона общей формулы (V) R - СН - С - СН3 С) (III) (Па) СН2-СН2-С1 О с неорганическим изотиоцианатом и превращении З-тиоцианато-5- хлор-2-алканона общей формулы полученного таким образом, а 2-хлор-4-метил-5(2-хлорэлкил)тиаэол общей формулы в соединения общей формулы (И) с помощью гапоидирующего агента с последующим гидрированием последних в соединений общей формулы (1). как описано выше Наше изобретение основано на следующих положениях в соединениях общей формулы (V) реактивность заместителя - хлора в а-положении по отношению к карбонильной группе превосходит реактивность других хлорных заместителей на конце цепи до такой степени, что получают исключительно соединения общей формулы (IV), не наблюдается образования ни дитиоцианзтокетона, ни изотиоцианатокетона даже в следовых количествах Получение соединений общей формулы (И), содержащих тиаэольное кольцо, из соединений общей формулы (IV) не является очевидным из литературных данных Удаление заместителя - хлора 8 тиаэольном кольце из дихпоридных соединений общей формулы (И) при селективном гидрировании является неожиданным и неочевидным, поскольку неактивность хлорного заместителя в конце цепи не может быть ожидаемой для специалиста в этой области Превращение соединений общей формулы (IV) в производные 2-окситиаэола общей формулы (III) предпочтительно в присутствии фосфорной кислоты, потом галоидирование соединений общей формулы (Ш) небольшим избытком галоидирующего агента в наиболее подходящем растворителе осуществляется со значительными технологическими и экологическими преимуществами. Способ, описанный в примерах настоящего изобретения, является новым и представляет собой альтернативный синтетический путь, который не может быть выьеден из известных способов получения Клометиазола общей формулы (1а) Ниже приводится выгодный вариант способа настоящего изобретения для синтеза соединения общей формулы (І а) Соединение формулы (И) с газообразным хлористым водородом в органическом растворителе, с последующим гидрированием последнего в присутствии металлического катализатора в органическом растворителе, получают с хорошим выходом 4-метил-б (2-хлоралкип)тиазолы общей формулы (I) высокой чистоты лри выделении их из реакционной смеси известными способами предпочтительно в виде их гидрохлоридов Соединения общей формулы (I) могут быть превращены в их соли присоединения кислот из СІ - СНг - СН2 - СН - С - СН3 (IVa) SCN получают из известного соединения формулы CI - СН 2 - СН г - СН - С - СН 3 СІ О (Va) 34443 (Ada Cnem Hung. 3 157 (1953)) в воде, в органическом растворителе или в смеси воды и органи* ческого растворителя, с помощью неорганических тиоцианатов, предпочтительно тиоцианатов натрия, калия или аммония Наиболее предпочтительно используют органический растворитель, например, ацетон, метилэтипкетон, этилаМетат, метанол, этанол, иэопропилацетат или этилпропионэт Реакция может быть проведена при температуре в интервале от 20 до 1О0°С, предпочтительно при температуре кипения растворителя, с эквивалентным количеством или незначительным (1-5% мольн.) избытком неорганического роданида Дихлорпроизводное общей формулы (На) получают при взаимодействии соединения формулы (IVa), растворенного в органическом растворителе, с безводным газообразным хлористым водородом. В качестве растворителя наиболее предпочтительна используют иесмвшивэющиеся с водой простые и сложные эфиры, которые нерастворимы в воде, например, этилацетат, бутилацетат или дииэопропиловый эфир Предпочтительно также могут быть использованы низшие алифатические спирты, например, метанол, этанол, н-пропанол, иэопропанол или бутанол, низшие жирные кислоты, например, уксусная или пропионовая кислота, или галоидированные углеводороды, например, четыреххлористый углерод, хлороформ или 1,2М-дихлорэтан. Реакцию проводят при температуре в интервале от 0 до 100°С, предпочтительно от 0 до 40°С. Селективное гидрирование соединения формулы (На) проводят в присутствии металлического катализатора в органическом растворителе. Металлическим катализатором предпочтительно является палладий на активированном угле или палладий, содержащий селен (Примеры 1, 3 и 5 опубликованной заявки РСТ No 89(2429), также могут быть использованы катализаторы, содержащие родий или рутений В качестве органического растворителя могут быть использованы низшие «лифатические спирты, например, метанол, этанол, н-пропанол или иэопропанол, низшие сложные эфиры алифатических карбоновых кислот, например, этилацетзт, бутилацетат, метилацетат, изопропилацетат или этилпропионат, ароматические углеводороды, например, бензол или толуол, или простые эфиры с открытой целью, например, целлоэольв, метилцеллозольв, бутилцеллоэольв, диметилцеллозольв или диглим. Гидрирование можно проводить при атмосферном давлении или при слегка повышенном давлении (0.05-0,7 МПа). Расщепляющий хлористый водород связывается с образованием тиаэольного производного формулы (fa), затем оно может быть также извлечено в форме гидрохлорида формулы (la) Во время гидрирования в качестве связывающего кислоту агента может быть применен щелочной гидроксид, например, гидроксид натрия или калия или органическое основание, нап ример, триэтиламин, затем получают само основное соединение формулы (!а) При получении соединения формулы (Ша) а-тмоцианатокетон формулы (fVa) обрабатывают водной фосфорной кислотой, в этом стлше нет необходимости в органическом растворителе и не возникает проблемы коррозии в противоположность известным реагентам уксусная кислота-концентрированная серная кислота или уксусная кислота-концентрированная соляная кислота Кроме того, во время обработки реакционной смеси не образуется опасных для окружающей среды побочных продуктов Реакцию проводят при температуре в интервале от 50 до 120°С, предпочтительно от 90 до 100°С При гзлоидировэнии соединений формулы (Ша) в качестве галоидирующего агента используют галоидные соединения фосфора, например, фосфорилхлорид, пягихлористый фосфор или треххлористый фосфор. 6 качестве органического растворителя могут быть использованы предпочтительно галоидированные алифатические углеводороды, например, 1,2-дихлорэтан, 1,1,2-трихлорэтан, трихлорэтилен или 1.1.2.2-тетрахпорэтан, ароматические углеводороды, например, бензол, толуол или ксилол, особенно предпочтительно, галоидированные ароматические углеводороды, например, хлорбензол, 1,2-дихлорбензол или 1,2,4-трихлорбензол Реакцию проводят при температуре в интервале от 80 до 150°С, предпочтительно от 100 до 140°С Другие соединения общих формул (І), (II), (It!) и (IV) предпочтительно могут быть по-./чены по описанным выше способам Получение соединений общей формулы (V) описано в примерах, когда не имеется ссылок на литературные данные Настоящее изобретение раскрыто более детально в следующих неограничивающих его примерах Пример 1. Прибавляют 77.8 г (0.5 моля) 3,5-дихлор-2лентанона (полученного согласно Acta Chim Hung 3. 157 (1953)) к раствору 49.9 г (0,513 моля) роданида калия в 500 мл ацетона. Раствор кипятят при перемешивании в течение 4 часов. Реакционную смесь охлаждают до комнатной температуры, отфильтровывают осадок хлористого калия и промывают ацетоном Фильтрат выпаривают, остаток растворяют в бензоле и бензольный раствор промывают 3 раза водой После сушки над сульфатом натрия бензол отгоняют Получают 62,2 г (93%) 3-тиоцианато-5-хлор-2лентанона в виде красного масла. После разгонки при пониженном давлении получают светложелтое масло, его точка кипения равна 112°С при давлении 26,6 Па, п^3 «1,5110 Согласно инфракрасному спектру он не содержит какоголибо изотиоцианата. Анализ для формулы CeHeCfNOS: Вычисл.%: С 40,56, Н 4,53, N 7,88. CI 19,95, S 18,04. 34443 ИК и ЯМР-спектры подтверждают структуру По данным газовой хроматографии содержание продукта превышает 95%. Пример 7. Растворяют 25 г (0,14 мопя) 3-тиоцианато5-хлор-2-лентанона в 170 см3 бутилацетате, насыщенного газообразным хлористым водородом. В реакционную смесь вводят газообразный хлористый водород до насыщения при охлаждении льдом, поддерживая температуру ниже 10°С. После насыщения реакционную смесь перемешивают еще 20 минут при охлаждении, затем температуру медленно повышают до 40°С Реакционную смесь перемешивают при этой температуре 20 минут и после охлаждения до комнатной температуры выливают на лед Устанавливают величину рН смеси между 7 и 8 при добавлении 40%-го раствора гидроксида натрия Затем смесь обрабатывают, как описано в примере 6. Получают 20,8 г (76%) 2-хлор-4-метил-5-(2хлорэтил)-тиаэола, который идентичен во всех отношениях продукту примера 6. Пример 8. Работают по методике примера 7 с тем исключением, что вместо бутилацетата используют абсолютный этанол. После окончания реакции смесь выпаривают в вакууме и прибавляют к . остатку воду и 20%-й раствор гидроксида натрия до величины рН 7. Затем работают по методике примера 7, Получают 17 г (62%) 2-хлор-4-метил-5(2-хлорэтил)-тиазола, который идентичен во всех отношениях продукту примера 6 Пример 9. Работают по методике примера 6 с той разницей, что вместо этилацетата используют диизопропиловый эфир. Получают 14 г (74%) 2-хлор4-метил-5-(2-хлорэтил)-тиазола, который идентичен во всех отношениях продукту примера 6 Пример 10. Работают по методике примера 8 с той разницей, что вместо абсолютного этанола используют ледяную уксусную кислоту. Получают 20,2 г (73,5%) 2-хлор-4-метил-5-{2-хлорэтил)-тиазопа, который идентичен во всех отношениях продукту примерз 6. Пример 11. Работают по методике примера в с той разницей, что вместо этилацетата используют четыреххпористый углерод. Получают 12 г (61%) 2-хлор4-метил-5-(2-хпорзтил)-тмазола, который идентичен во всех отношениях продукту примера б. Найдено, %• С 41,25, Н 4,59. N 8,13, CI 20,32, S 17,90 Данные ЯМР подтверждают структуру. Пример 2. Раствор 155,5 г (1 моль) 3,5-дихлор-2-пентанона с 83 г (1,025 моля) роданида натрия в 1 п метипэтилкетона кипятят 1 час при перемешивании. Затем работают по методике примера 1. Попучают 171 г (96,2%) 3-тиоцианато-5-хлор-2-пентаиона, который поспе перегонки идентичен во всех отношениях продукту примера 1. Пример 3. Суспензию 7,8 г (0,05 Моля) 3,5-дихлор-2пентзнона с 3,9 г (0,051 моля) роданида аммония в 50 см3 метил этил квтона кипятят 1 час при перемешивании Затем работают по методике примера 1. Получают 8,5 г (95,5%) 3-тиоцианато-5-хлор-2пентанона, который после перегонки идентичен во всех отношениях продукту примера 1. Пример 4. Раствор 7.8 г (0,05 моля) 3,5-дихлор-2-лентанона с 4.15 г (0,051 моля) роданида натрия в 3 50 см этанола кипятят 2 часа при перемешивании. Затем работают по методике примера 1. Получают 7,7 г (87%) 3-тиоциэнэто-5-хлор-2-пентанона, который идентичен во всех отношениях продукту примера 1 поспе перегонки. Пример 5. К раствору 4,86 г (0,05 моля) роданида калия в 10 см3 воды прибавляют 7,8 г (0,05 моля) 3,5-дихлор-2-лентанонэ и перемешивают реакционную смесь 3 часа при температур® 80°С. После охлаждения отделяют выделившееся масло и водную фазу встряхивают дважды каждый раз с 20 см3 бензола Отделенное масдо объединяют с бензольным раствором, промывают водой и сушат над сульфатом натрия. После фильтрации и выпаривания получают 7,4 г (83,5%) Э-тиоцианато-5-хлор-2-пентанонз, который после переюкки идентичен во всех отношениях продукту примера 1. Пример 6. Раствор 17,7 г (0,1 мопя) З-тиоцианато-5хлор-2-пеятвнона в 170 см3 безводного этипацетата насыщают газообразным хлористым водородом. Температуру реакционной смеси поддерживают ниже 10°С при охлаждении льдом. Полученный раствор оставляют на ночь при комнатной температуре. На следующий день раствор выпивают на лед и устанавливают величину его рН между 6 и 7 с помощью 20%-ного растэора гидроксида натрия Разделяют фазы и водную фазу встряхивают со 150 смэ этилацетзта. Объединенные этилацетатные растворы промывают до нейтральной реакции водой и 5%-м раствором бикарбоната натрия, сушат над сульфатом натрия. После отгонки растворителя остаток разгоняют при пониженном давлении, получают 14,8 г (75,5%) 2-хлор-4-метил-5-(2-хлорэтил)-тиазола в виде саетло-желтого" масла. Точка кипения 104°С при давлении 40 Па, Пс? =1,5505. Анализ для формулы CeH7Ct2NS: Пример 12. Прибавляют 355,5 г (2 моля) перегнанного 3-тиоцианато-5-хлор-2- пентанона к 360 см3 85%й фосфорной кислоты при перемешивании. Повышают температуру реакционной смеси до 95°С на водяной бане в течение примерно 1 часа, а затем перемешивают 1,5 часа при температуре между 95 и 100°С. Коричневый раствор охлаждают до 20°С и выливают в 660 см3 воды. После 1,5 часов перемешивания отфильтровывают выпавшие в осадок бежевые кристаллы, промывают до нейтральной реакции водой и сушат в вакууме при температуре 60°С. Получают 337 f (95%) светло-бежевых кристаллов 2-окси-4-метил-5-{2-хлорэтип)-тиазола, т.пл. 151-152°С. Пос Вычисл. %: С 36.70, Н 3,39, N 7,14, С\ 36,15, S 16,35. Найдено, %: С 37,01, Н 3,71, N 7,48. CI 35,40, S 15,97. 6 34443 ле перекристаллизации из бетона точка плавления равна 157-15В°С Анализ для CeHeCINOS Вычисп % С 40,56. Н 4,53, Н 7.88, S 18.04, CI 19,95 Найдено % С 40,74, Н 4.52, N 7,57. S 17,94, CI 19,68 Структура соединений подтверждена также данными ИК и ЯМР-спектров Пример 13. Работают по методике примера 12, используя неперегнанный 3-тиоцианато-5-хлор-2-пентзнон (содержание 80% по данным газовой хроматографии) Получают 234 г (66%) 2-окси-4-метил5- (2-хлорэтил)-тиазола, который плавится при 141-146°С Пример 14. Суспензию 177.6 г (1 моль) 2-окси-4-м столбу-хлорэти л )-тиазол а в 530 см3 безводного хлорбензола нагревают при перемешивании до 100°С Вливают в раствор 306,6 г (2 моля) фосфорилхлорида в течение 30 минут, затем перемешивают при температуре 125~13О°С до тех пор, пока не прекратится выделение хлористого водорода (около 2 часов) Реакционную смесь охлаждают до 20°С, затем ее выливают на 1,5 кг льда Разделяют фазы, водную фазу дважды экстрагируют 200 см3 хлорбензола каждый раз Объединенные фазы, содержащие хлорбензол, промывают не содержащей кислоты водой а затем 5%-м раствором бикарбоната натрия и выпаривают при пониженном давлении Коричневый остаток фракционируют в вакууме Получают 145 г (74%) 2-хлор-4-метил-5-(2-хлорзтип)-тиаэопа. Точка кипения равна 102°С при давлении 53,2 Па, ng? = 1,5512, ng> = 1,5468. Чистота 99,4% (по данным газовой хроматографии) Анализ для CeHrCkNS: Вычисл % С 36,70. Н 3.59, И 7,14, CI 36,15, S 16,35 Найдено, % С 36,98, Н 3,68, N 7,28, С1 35,70, S 16,05. Структура соединения также подтверждается данными ИК и ЯМР-спектров Пример 15. К раствору 83 г (0,32 мопя) 2-хлор-4-метил-5-(2-хлорзтил)-тиазола в 630 см3 96%-го этанола прибавляют 9 г влажмого катализатора палладия на угле (содержание палладия 8%). Смесь гидрируют при атмосферном давлении Окончание реакции определяется по прекращению поглощения водорода. После фильтрации катализатора раствор выпаривают, остаток растворяют в воде и раствор нейтрализуют бикарбонатом натрия г (90%) А тепля Ъ (?хлорэтип) тиязола уогорый во всех отношение идентичпн продукту примера 15 Пример 17. Работают по методике примера 15 с той разницей, что вместо этанола испольтуют метанол Получают 42.9 г (83%) 4-метил-5-{2~ хлорэл1Л}-тиазолз. который идентичен оо всех отношениях продукту примера 15 Пример 18 Рабсают по методике примера 15 с той разницей, что после выпаривания отделяют твердый остаток Получают 61 5 г (97%) 4-метил-5-(2хлорзтил)-тиазола гидрохлоридз После перекристаллизации из безводного этанола его точка плавления равна 13Є—!37°С Анализ для CeHgCbNS: Вычисп % С 36,37, Н 4,58, N 7,07, Cf 35,79 Найдено, % С 36,18, Н 4,52. N 7,10, CI 35,89 Пример 19. Работают по методике примера 15 с той разницей что к раствору, полученному после фильтрации катализатора, прибавляют ацетон и отфильтровывают выпавшее в осадок твердое вещество Получают 59,4 г (93,7%) 4-метил-5-
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of the thiazole derivatives or acid addition salts thereof, 3-thiocyanato-5-chloro-2-alkanone and a process for its preparation
Автори англійськоюPalosi Endre, Korbonits Dezso, Molnar Erzsebet, Szvoboda Ida, Heja Gergely, Kiss Pal, Goenczi Csaba, Morasz Ferenc, Ledniczky Laszlo, Szabo Erzsebet, Gyoeri Peter, Szalay Erzsebet, Sperber Ferenc, Huszar Csaba, Mihalovics Gyoergy, Nemeth Attila, Sue Mihaly, Gyuere Karol, Bone Istvan, Ban Karoly, Buttkai Iidiko, Koevari Arpad, Garaczy Sandor
Назва патенту російськоюСпособ получения производных тиазола или их солей присоединения кислот, 2-алканон и способ его получения
Автори російськоюПалоши Эндре, Карбониц Дежьо, Молнар Эржебет, Воля Ида, Хейя Гергей, Кишш Упал, Гьонци Чаба, Морас Ференц, Ледницки Ласло, Сабо Эржебет, Дьори Петер, Салай Эржебет, Шпербер Ференц, Хусар Чаба, Михалович Дьордь, Неймет Аттила, Шютьо Михай, Дьюре Карей, Боней Иштван, Бан Карей, Бутткаи Илдико, Кевари Арпад, Гараци Шандор
МПК / Мітки
МПК: C07D 277/22, C07D 277/32, C07C 331/00, C07D 277/20, C07D 277/34
Мітки: 5-хлор-3-тіоціанато-2-алканон, одержання, тіазолу, солей, приєднання, похідних, спосіб, кислот
Код посилання
<a href="https://ua.patents.su/10-34443-sposib-oderzhannya-pokhidnikh-tiazolu-abo-kh-solejj-priehdnannya-kislot-5-khlor-3-tiocianato-2-alkanon-ta-sposib-jjogo-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних тіазолу або їх солей приєднання кислот, 5-хлор-3-тіоціанато-2-алканон та спосіб його одержання</a>
Попередній патент: Ступеневий вимикач (варіанти)
Наступний патент: Шприц-ампула
Випадковий патент: Спосіб відновлення регенераційних розчинів натрій-катіонного пом'якшення води