Спосіб неінвазійного визначення концентрації глюкози в крові людини та пристрій для його реалізації
Номер патенту: 78817
Опубліковано: 25.04.2007
Автори: Войтович Ігор Данилович, Корсунський Володимир Мусійович
Формула / Реферат
1. Спосіб неінвазійного визначення концентрації глюкози в крові пацієнта, який передбачає підготовку вибраної ділянки тіла пацієнта до вимірювання, в тому числі створення передумов для неінвазійної зміни кровонаповнення цієї ділянки, просвічування її напрямленим світловим пучком, до складу якого входить випромінювання з довжиною хвилі ![]() , характерною для поглинання глюкозою, збирання частини світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, вимірювання спектральних інтенсивностей потрібних складових, зміну кровонаповнення досліджуваної ділянки тіла, при зміненому кровонаповненні просвічування тієї ж досліджуваної ділянки тіла тим же світловим пучком, збирання частини світла, яке пройшло крізь досліджувану ділянку тіла або зворотно розсіяне нею, вимірювання спектральних інтенсивностей потрібних складових, обчислення з використанням отриманих результатів концентрації глюкози та виведення її для зчитування, який відрізняється тим, що при підготовці до вимірювання на першу чи середню фалангу пальця руки пацієнта накладають еластичну надувну манжету і кінцеву фалангу того ж пальця приводять в оптичний контакт з вимірювальним приладом, в ході операції вимірювання спектральних інтенсивностей вимірюють лише спектральну інтенсивність
, характерною для поглинання глюкозою, збирання частини світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, вимірювання спектральних інтенсивностей потрібних складових, зміну кровонаповнення досліджуваної ділянки тіла, при зміненому кровонаповненні просвічування тієї ж досліджуваної ділянки тіла тим же світловим пучком, збирання частини світла, яке пройшло крізь досліджувану ділянку тіла або зворотно розсіяне нею, вимірювання спектральних інтенсивностей потрібних складових, обчислення з використанням отриманих результатів концентрації глюкози та виведення її для зчитування, який відрізняється тим, що при підготовці до вимірювання на першу чи середню фалангу пальця руки пацієнта накладають еластичну надувну манжету і кінцеву фалангу того ж пальця приводять в оптичний контакт з вимірювальним приладом, в ході операції вимірювання спектральних інтенсивностей вимірюють лише спектральну інтенсивність ![]() частини світла з довжиною хвилі
частини світла з довжиною хвилі ![]() в спектральній смузі, характерній для поглинання глюкозою, кінцеву фалангу пальця додатково просвічують пучком світла з довжиною хвилі
в спектральній смузі, характерній для поглинання глюкозою, кінцеву фалангу пальця додатково просвічують пучком світла з довжиною хвилі ![]() , яке добре поглинається гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном, зі світла, яке пройшло крізь тканину пальця пацієнта або зворотно розсіяне нею, збирають лише ту частину, яка виходить з пальця на певній відстані від місця входу і під певним кутом до поверхні шкіри, вимірюють лише спектральну інтенсивність
, яке добре поглинається гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном, зі світла, яке пройшло крізь тканину пальця пацієнта або зворотно розсіяне нею, збирають лише ту частину, яка виходить з пальця на певній відстані від місця входу і під певним кутом до поверхні шкіри, вимірюють лише спектральну інтенсивність ![]() частини світла з довжиною хвилі
частини світла з довжиною хвилі ![]() , кровонаповнення досліджуваного пальця пацієнта неінвазійно змінюють шляхом зміни тиску в накладеній на нього манжеті; після цього повторюють просвічування досліджуваної фаланги пальця пучком світла з довжиною хвилі
, кровонаповнення досліджуваного пальця пацієнта неінвазійно змінюють шляхом зміни тиску в накладеній на нього манжеті; після цього повторюють просвічування досліджуваної фаланги пальця пучком світла з довжиною хвилі ![]() і пучком світла з довжиною хвилі
і пучком світла з довжиною хвилі ![]() , в результаті чого вимірюють спектральні інтенсивності світла
, в результаті чого вимірюють спектральні інтенсивності світла ![]() та
та ![]() , концентрацію глюкози в крові пацієнта обчислюють за формулою
, концентрацію глюкози в крові пацієнта обчислюють за формулою
![]() ,
,
де ![]() - концентрація гемоглобіну в крові пацієнта, яка має бути відомою,
- концентрація гемоглобіну в крові пацієнта, яка має бути відомою,
![]() - константи, які визначають при калібруванні або обчислюють за іншим алгоритмом, який дає близькі результати.
- константи, які визначають при калібруванні або обчислюють за іншим алгоритмом, який дає близькі результати.
2. Спосіб за п. 1, який відрізняється тим, що довжина хвилі ![]() належить набору (506,5±7) нм, (523±7) нм, (549±7) нм, (569±7) нм або (586±7) нм, а довжина хвилі
належить набору (506,5±7) нм, (523±7) нм, (549±7) нм, (569±7) нм або (586±7) нм, а довжина хвилі ![]() належить ближньому інфрачервоному діапазонові від 1000 до 2700 нм і може бути взята з набору 1575, 1765 і 2270±20 нм або між 2080 нм та 2200 нм.
належить ближньому інфрачервоному діапазонові від 1000 до 2700 нм і може бути взята з набору 1575, 1765 і 2270±20 нм або між 2080 нм та 2200 нм.
3. Спосіб за п. 1 або 2, який відрізняється тим, що світловий пучок для просвічування досліджуваної фаланги пальця як при нормальному, так і зміненому кровонаповненні, є модульованим за амплітудою і при збиранні частини світла, яке пройшло крізь досліджувану ділянку тіла або зворотно розсіяне нею та при вимірюванні інтенсивностей потрібних складових як при нормальному, так і зміненому кровонаповненні, виділяють та вимірюють лише синхронно модульовану частину світла.
4. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що до та після зміни кровонаповнення групи операцій по просвічуванню досліджуваної фаланги пальця і вимірюванню спектральних інтенсивностей з обома довжинами хвилі ![]() та
та ![]() повторюють по кілька разів, результати серій вимірювань осереднюють, щоб позбутися або значно зменшити вплив шумових факторів, і в операції обчислення концентрації глюкози використовують осереднені значення спектральних інтенсивностей
повторюють по кілька разів, результати серій вимірювань осереднюють, щоб позбутися або значно зменшити вплив шумових факторів, і в операції обчислення концентрації глюкози використовують осереднені значення спектральних інтенсивностей ![]() ,
, ![]() ,
, ![]() та
та ![]() .
.
5. Пристрій для неінвазійного визначення концентрації глюкози в крові пацієнта, який містить вузол фіксації об'єкта вимірювання, що дає можливість змінювати кровонаповнення об'єкта вимірювання; джерело світла, випромінювання якого містить світло з довжиною хвилі ![]() , характерною для поглинання глюкози, схему живлення та керування джерелом світла, перший волоконно-оптичний світловод для спрямування світла з довжиною хвилі
, характерною для поглинання глюкози, схему живлення та керування джерелом світла, перший волоконно-оптичний світловод для спрямування світла з довжиною хвилі ![]() від джерела до вибраної ділянки шкіри пацієнта, другий волоконно-оптичний світловод для збирання частини світла з довжиною хвилі
від джерела до вибраної ділянки шкіри пацієнта, другий волоконно-оптичний світловод для збирання частини світла з довжиною хвилі ![]() , яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до фотоприймача, чутливого до світла з довжиною хвилі
, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до фотоприймача, чутливого до світла з довжиною хвилі ![]() , який перетворює світловий потік на пропорційний електричний сигнал, електронні підсилювачі, входами підключені до відповідних фотоприймачів, аналого-цифровий перетворювач (АЦП), входи якого підключені до виходів електронних підсилювачів, мікропроцесор, до якого підключений вихід АЦП і в пам'яті якого містяться програми обчислення концентрації глюкози, керування роботою пристрою та видачею інформації, індикаторне табло, приєднане інформаційною шиною до мікропроцесора, та блок живлення, який відрізняється тим, що вузол фіксації об'єкта вимірювання являє собою вимірювальне ложе для пальця пацієнта, на котрому проводять вимірювання, оснащене еластичним надувним кільцем-манжетою; джерело світла випромінює також світло з довжиною хвилі
, який перетворює світловий потік на пропорційний електричний сигнал, електронні підсилювачі, входами підключені до відповідних фотоприймачів, аналого-цифровий перетворювач (АЦП), входи якого підключені до виходів електронних підсилювачів, мікропроцесор, до якого підключений вихід АЦП і в пам'яті якого містяться програми обчислення концентрації глюкози, керування роботою пристрою та видачею інформації, індикаторне табло, приєднане інформаційною шиною до мікропроцесора, та блок живлення, який відрізняється тим, що вузол фіксації об'єкта вимірювання являє собою вимірювальне ложе для пальця пацієнта, на котрому проводять вимірювання, оснащене еластичним надувним кільцем-манжетою; джерело світла випромінює також світло з довжиною хвилі ![]() , яке добре поглинається гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; для спрямування цього світла до вибраної ділянки шкіри пацієнта введено третій волоконно-оптичний світловід; для збирання частини світла з довжиною хвилі
, яке добре поглинається гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; для спрямування цього світла до вибраної ділянки шкіри пацієнта введено третій волоконно-оптичний світловід; для збирання частини світла з довжиною хвилі ![]() після його взаємодії з досліджуваною ділянкою тіла пацієнта введено четвертий волоконно-оптичний світловід, який передає зібране світло до додаткового фотоприймача, чутливого до світла з довжиною хвилі
після його взаємодії з досліджуваною ділянкою тіла пацієнта введено четвертий волоконно-оптичний світловід, який передає зібране світло до додаткового фотоприймача, чутливого до світла з довжиною хвилі ![]() ; в стінку вимірювального ложа виведені кінці 1-го, 2-го, 3-го та 4-го світловодів, які при вимірюванні оптично контактують з пальцем, додатково введено блок керування тиском в манжеті, який пневматично з'єднаний з манжетою і може бути керованим від мікропроцесора, в пам'яті мікропроцесора міститься програма обчислення концентрації глюкози.
; в стінку вимірювального ложа виведені кінці 1-го, 2-го, 3-го та 4-го світловодів, які при вимірюванні оптично контактують з пальцем, додатково введено блок керування тиском в манжеті, який пневматично з'єднаний з манжетою і може бути керованим від мікропроцесора, в пам'яті мікропроцесора міститься програма обчислення концентрації глюкози.
6. Пристрій за п. 5, який відрізняється тим, що джерела світла виконані як світлодіоди або напівпровідникові лазери.
7. Пристрій за п. 5 або 6, який відрізняється тим, що до складу схеми живлення та керування джерелом світла входять модулятори інтенсивності випромінювання, а до складу електронних підсилювачів - синхронні демодулятори, причому модулятори та демодулятори керуються мікропроцесором.
8. Пристрій за будь-яким із пп. 5 - 7, який відрізняється тим, що перед фотоприймачами встановлено світлофільтри, які пропускають до них лише світло з відповідною вузькою спектральною смугою.
9. Пристрій за будь-яким із пп. 5 - 8, який відрізняється тим, що до його складу входять також клавіатура і блок зв'язку з зовнішньою ЕОМ, а в пам'яті мікропроцесора містяться також програми взаємодії через клавіатуру з користувачем та через блок зв'язку з зовнішньою ЕОМ.
10. Пристрій за будь-яким із пп. 5 - 9, який відрізняється тим, що блок керування тиском в манжеті складається з ресивера, міні-компресора, манометра, триходового клапана, автоматично керованого від мікропроцесора, та з'єднувальних трубок.
Текст
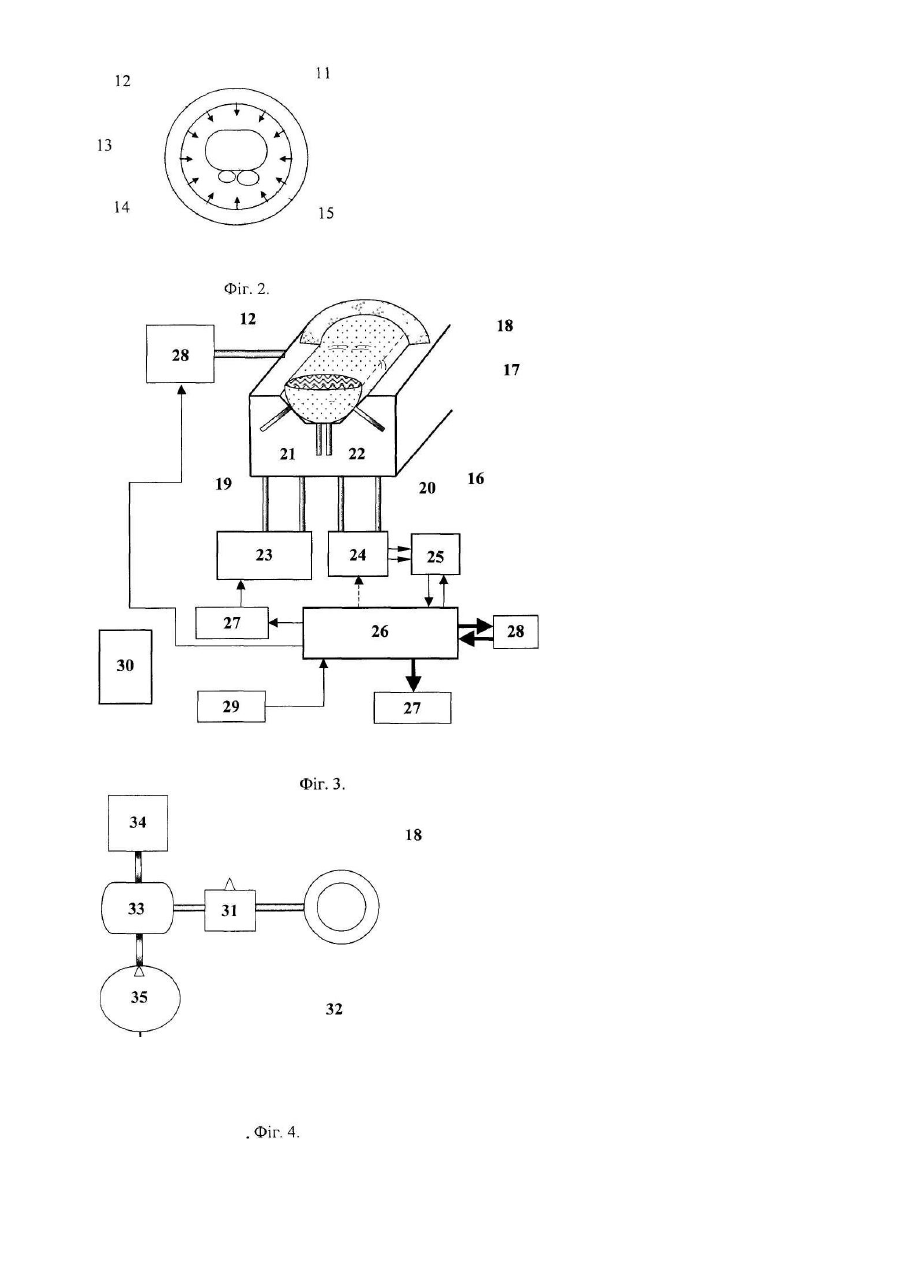
Винахід відноситься до галузі медичної вимірювальної техніки й може бути застосований при створенні приладу для нетравмуючого неінвазійного вимірювання концентрації глюкози в крові людини - приладу, який хворі на діабет люди могли б повсякденно безболісно багаторазово використовувати для самоконтролю та коригування доз інсуліну. У другій половині XX століття, коли захворювання на діабет досягли масштабів епідемії, розробка такого приладу стала світовою проблемою. Починаючи з 70-х років цією проблемою займаються чимало фірм та науково-технічних закладів більшості розвинених країн. Спочатку увагу було зосереджено на розробці поляриметричних приладів, бо до цього вже понад 100 років для визначення концентрації цукру в розчинах широко використовували поляризаційні цукрометри. Їх дія ґрунтується на особливій властивості молекул глюкози повертати площину поляризації світла [К.Джерасси. Дисперсия оптического вращения.Μ., 1962; Волкова Е.В. Поляризационные измерения. - М., Изд. стандартов, 1974; Zirk К., Potzschke Η., Barnicol W.K.R., А Minitiaturisable High Sensitive Polarimeter as Detector of an Implantable Glucose Probe. Biomedizinische Technik, Vol. 46, 2001, No. 6 та 10]. Поляриметричні способи вимірювання концентрації глюкози в крові людини розробляються та патентуються ще й досі [U.S. Patent №№ 4169676, 4350163, 4427889, 4586513, 4655225, 4498774, 5398681, 6188477, RP Patent №2088896, 2112937 і інші]. Проте задовільного результату на цьому шляху досягти ще не вдалося. З кінця 80-х років почались інтенсивні розробки спектрофотометричних способів, в яких використовують специфіку спектра поглинання глюкози в інфрачервоній області [Swiss Patent №612271, U.S. Patent №4169676, 4655255, 4975581, 5028787, 5077476, 5086229, 5115133, 5178142, 5179951, 5267152, 5313941, 5361758, 5424545, 5433197, 5743262, 5750994, 5782755, 5830112, 5974337, 6016435, 6026314, 6031233, 6061582, 6064898, PCT Application WO 99/43255, United States Patent Application №20020151773, №20030023152, №20030023152, №20040162470, №20040181132, №20040225206]. Мабуть, найбільше просунулись у їх розробці американські фірми Futrex Inc. та Biocontrol Technology, які розробили відповідно неінвазійні глюкосенсори "Dream Beam" та "Diasensor". Проте й вони так і не отримали дозволу на широке застосування, бо результати їх клінічних випробувань виявилися незадовільними. З багатьох патентів на спектрофотометричні способи вимірювання концентрації глюкози в крові людини пошлемось лише на 3, які за сукупністю суттєвих ознак є найближчими до нашого винаходу. В [європейському патенті №0160768 А1 (аналог)] пропонується спектрофотометричний спосіб неінвазійного визначення глюкози в тканинах тіла, при якому обрану ділянку тіла пацієнта опромінюють світлом від напрямленого джерела, збирають світловий потік, що пройшов або дифузно відбився від певного об'єму тіла під шкірою, перетворюють цей світловий потік у відповідні електричні сигнали. Вказане зібране світло складається щонайменше з однієї спектральної смуги 1-го роду ("вимірювальної") з довжиною хвилі l G, типової для спектру поглинання глюкози, і щонайменше з однієї спектральної смуги 2-го роду ("опорної") з довжиною хвилі l R, типовою для фонового поглинання тіла, на якій поглинання глюкози відсутнє або є незначним. Величини виміряних електричних сигналів I G та I R відповідно "вимірювальної" та "опорної" спектральної смуг, подають на комп'ютер, з допомогою котрого за наперед заданим алгоритмом обчислюють концентрацію глюкози, і виводять її для зчитування. В патенті вказується, що спектральні смуги 1-го та 2-го роду знаходяться у ближньому інфрачервоному (БІЧ) діапазоні довжин хвилі від 1000 до 2700нм, l G може бути взята з набору 1575, 1765, 2100 і 2270 ± 15нм. В способі-аналозі пропонується також вимірювати спектральні інтенсивності світла, зворотно розсіяного від першого об'єму тіла, з розташованого безпосередньо під шкірою, в якому "кількість глюкози мала або незначна", і в "більш цікавому для аналізу" другому об'ємі тіла, розташованому глибше під шкірою. Вважається, що результат їх віднімання є більш репрезентативним для визначення глюкози. Спільними ознаками цього способу-аналога і запропонованого нами способу є такі операції: обрану ділянку тіла пацієнта приводять в оптичний контакт з вимірювальним пристроєм; цю ділянку неінвазійно крізь шкіру просвічують напрямленим світловим пучком, до складу якого входить випромінювання з довжиною хвилі l G в спектральній смузі поглинання глюкозою, цей світловий пучок є модульованим за інтенсивністю; збирають частину світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею; виділяють з неї лише потрібну спектральну складову; вимірюють спектральну інтенсивність виділеної частини світла; використовуючи виміряні значення спектральних інтенсивностей, за певним алгоритмом обчислюють концентрацію глюкози і виводять її для зчитування. Причинами, які заважають вирішенню поставленої задачі, є у способі-аналозі те, що не виправдовується вихідне припущення відносно того, що в об'ємі тіла, розташованому безпосередньо під шкірою, кількість глюкози є незначною, а головне те, що в способі-аналозі не враховується об'ємна доля фактично присутньої в тканині крові, тобто ступінь кровонаповнення просвічуваної тканини. Іншим аналогом є спосіб, описаний в [патенті США №6097975]. В ньому обрану ділянку тіла пацієнта приводять в оптичний контакт з вимірювальним приладом; подають до неї імпульс світла через оптоволоконний світловід; з допомогою іншого оптоволоконного світловоду збирають частину світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею; з допомогою світлофільтра виділяють з неї спектральну складову, що належить смузі, характерній для поглинання глюкозою; вимірюють інтенсивність цієї спектральної складової; вимірюють (в тій же спектральній смузі) інтенсивність світла, поданого до шкіри пацієнта; порівнюють отримані результати вимірювань; на цій основі з допомогою мікропроцесора за наперед закладеною в його пам'ять програмою визначають кількість світла, поглинутого глюкозою в тілі пацієнта, і обчислюють концентрацію глюкози. Спільними ознаками цього способу-аналога і запропонованого нами способу є такі операції: обрану ділянку тіла пацієнта приводять в оптичний контакт з вимірювальним пристроєм; подають до неї імпульс світла і неінвазійно крізь шкіру просвічують напрямленим світловим пучком, до складу якого входить випромінювання з довжиною хвилі l G в спектральній смузі поглинання глюкозою; збирають частину світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею; виділяють з неї потрібну спектральну складову; вимірюють спектральну інтенсивність виділеної складової зібраного світла; використовуючи виміряні значення спектральних інтенсивностей, з допомогою мікропроцесора за наперед закладеною в його пам'ять програмою обчислюють концентрацію глюкози і виводять її для зчитування. Причинами, що заважають вирішенню поставленої задачі, є в способі-аналозі те, що відсутні операції, які давали б змогу врахувати значне розсіювання і "фонове" поглинання введеного світла живою тканиною, а головне, які б давали змогу врахувати об'ємну долю крові в тканині, тобто ступінь кровонаповнення просвічуваної ділянки тіла. Найближчим до нашого винаходу за сукупністю суттєвих ознак є спосіб, описаний в [патентній заявці США №20020123677]. Цей спосіб взятий нами як спосіб-прототип. В способі-прототипі обрану ділянку тіла пацієнта приводять в оптичний контакт з вимірювальним приладом та створюють передумови для неінвазійної зміни кровонаповнення цієї ділянки; світло в діапазоні довжин хвилі від 0,8мкм до 2,5мкм поділяють на вузькі спектральні складові й опромінюють об'єкт вимірювання кожною з них через оптоволоконний світловід; з допомогою іншого оптоволоконного світловоду збирають частину світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею; вимірюють інтенсивності усіх спектральних складових і обчислюють спектр поглинання; шляхом стискання досліджуваної ділянки тіла (пальця) гумовим кільцем приводять її в так званий "гемостатичний стан", простіше кажучи, змінюють її кровонаповнення; знову шляхом повторення описаних вище операцій вимірюють спектр поглинання. Далі шляхом віднімання спектра поглинання в "нормальному стані" від спектра поглинання в "гемостатичному стані" обчислюють "спектр поглинання крові"; на цій основі з допомогою мікропроцесора за наперед закладеною в його пам'ять програмою і визначають концентрацію глюкози. Спільними ознаками способу-прототипу і запропонованого нами способу є такі операції: вибрану ділянку тіла пацієнта готують до вимірювання, в тому числі створюють передумови для неінвазійної зміни кровонаповнення цієї ділянки, просвічують її напрямленим світловим пучком, до складу якого входить випромінювання з довжиною хвилі l G, характерною для поглинання глюкозою, збирають частину світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, вимірюють спектральні інтенсивності відповідних складових, змінюють кровонаповнення досліджуваної ділянки тіла, знову просвічують її напрямленим світловим пучком, до складу якого входить випромінювання з довжиною хвилі l G, характерною для поглинання глюкозою, збирають частину світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, вимірюють спектральні інтенсивності відповідних складових, обчислюють з використанням отриманих результатів концентрацію глюкози та виводять її для зчитування. Причинами, що заважають вирішенню поставленої задачі, є в способі-прототипі те, що стискування пальця за допомогою гумового кільця не забезпечує регульованої зміни кровонаповнення (адже товщина різних пальців людини і пальців різних людей є різною), фактична величина зміни кровонаповнення не реєструється. А це не дає змоги коректно обчислити концентрацію глюкози в крові. В основу даного винаходу покладено задачу знайти такий не інвазійний спосіб вимірювання концентрації глюкози в крові людини, в якому шляхом введення додаткових неінвазійних операцій та вимірювань можна було б врахувати фактичну зміну кровонаповнення просвічуваної ділянки тіла і на цій основі значно коректніше визначити концентрацію глюкози в крові людини. Розв'язок поставленої задачі досягається тим, що: - при підготовці до вимірювання обрану ділянку тіла, наприклад, кінцеву фалангу пальця, приводять в оптичний контакт з вимірювальним пристроєм і створюють передумови для регульованої неінвазійної зміни її кровонаповнення, наприклад, на середню фалангу цього ж пальця накладають еластичне надувне кільцеманжету; - крізь шкіру просвічують обрану ділянку тіла сконцентрованим пучком світла, напрямленим перпендикулярно до шкіри, яке має довжину хвилі kG , характерну для поглинання глюкозою; - зі світла, яке пройшло крізь тканину обраної ділянки тіла пацієнта або зворотно розсіяне нею, збирають ту частину, яка виходить з тіла на певній відстані від місця входу і під певним кутом до поверхні шкіри; - вимірюють спектральну інтенсивність N(1)G цієї частини світла; - просвічують ту ж частину тіла напрямленим пучком світла з іншою довжиною хвилі l Н, характерною для поглинання гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; - збирають ту частину цього світла, яка виходить з тіла на заданій відстані від місця входу і під заданим кутом до поверхні шкіри, наприклад, перпендикулярно до неї; - вимірюють спектральну інтенсивність N(1)H цієї частини світла; - після цього неінвазійно змінюють кровонаповнення обраної ділянки тіла шляхом зміни тиску в накладеній на першу чи середню фалангу того ж пальця манжеті; - знову просвічують обрану ділянку тіла сконцентрованим пучком світла, напрямленим перпендикулярно до шкіри, яке має довжину хвилі l G, характерну для поглинання глюкозою; - зі світла, яке пройшло крізь тканину обраної ділянки тіла пацієнта або зворотно розсіяне нею, збирають ту частину, яка виходить з тіла на певній відстані від місця входу і під певним кутом до поверхні шкіри; - вимірюють спектральну інтенсивність N(2)G цієї частини світла; - просвічують ту ж частину тіла напрямленим пучком світла з іншою довжиною хвилі l Η, характерною для поглинання гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; - збирають ту частину цього світла, яка виходить з тіла на заданій відстані від місця входу і під заданим кутом до поверхні шкіри, наприклад, перпендикулярно до неї; - вимірюють спектральну інтенсивність N(2)H цієї частини світла; - концентрацію глюкози в крові пацієнта обчислюють за формулою (20), яка буде наведена нижче; - виводять знайдене значення для зчитування. Відмітними ознаками запропонованого способу є те, що при підготовці до вимірювання на першу чи середню фалангу пальця руки одягають еластичне надувне кільце-манжету; після вимірювання спектральної інтенсивності N(1)G тієї частини світла, яка виходить з тіла на певній відстані від місця входу і під певним кутом до поверхні шкіри, ту ж ділянку тіла додатково просвічують напрямленим пучком світла з довжиною хвилі l Η, характерною для поглинання гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; зі світла, яке пройшло крізь тканину обраної ділянки тіла пацієнта або зворотно розсіяне нею, збирають лише ту частину, яка виходить з неї на певній відстані від місця входу і під певним кутом до поверхні шкіри; додатково вимірюють спектральну інтенсивність N(1)H виділеної частини світла з довжиною хвилі l Η; кровонаповнення обраної ділянки тіла пацієнта після вимірювання спектральної інтенсивності N(1)H змінюють контрольовано шляхом зміни тиску в накладеній манжеті; при зміненому кровонаповненні знову просвічують обрану ділянку тіла сконцентрованим пучком світла, яке має довжину хвилі l G, характерну для поглинання глюкозою; зі світла, яке пройшло крізь тканину обраної ділянки тіла пацієнта або зворотно розсіяне нею, збирають ту частину, яка виходить з тіла на певній відстані від місця входу і під певним кутом до поверхні шкіри; вимірюють спектральну інтенсивність N(2)G цієї частини світла; просвічують ту ж частину тіла напрямленим пучком світла з іншою довжиною хвилі l Η, характерною для поглинання гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; збирають ту частину цього світла, яка виходить з тіла на заданій відстані від місця входу і під заданим кутом до поверхні шкіри, наприклад, перпендикулярно до неї; вимірюють спектральну інтенсивність N(2)H цієї частини світла; маючи значення спектральних інтенсивностей N(1)G, N(1)H, N(2)G, N(2)H, обчислюють концентрації глюкози в крові пацієнта за формулою, яка буде наведена нижче. Саме сукупність відмітних ознак дозволяє розв'язати поставлену задачу. Вимірювання спектральних інтенсивностей світла з довжиною хвилі l Η, характерною для поглинання загальним гемоглобіном крові (це в основному оксигемоглобін та відновлений гемоглобін), дозволяє коректно врахувати фактичні зміни кровонаповнення просвічуваної ділянки тіла. Справа в тому, що гемоглобін присутній тільки в крові, його нема поза кровоносним руслом. Концентрація саме загального гемоглобіну в крові однакова в усіх ділянках тіла, і тому він є природним індикатором змін кровонаповнення. А от глюкоза присутня не тільки у крові, але й поза кровоносним руслом, особливо у м'язових клітинах, де її кількість може коливатись у значних межах. Тому в звичайних умовах не можна визначити, яка частина світлового потоку поглинається глюкозою, розчиненою безпосередньо в крові, а яка - глюкозою, що знаходиться поза кровоносним руслом. Керована зміна кровонаповнення пальця призводить до зміни поглинання світлового потоку як гемоглобіном, так і саме тією частиною глюкози, яка розчинена в крові. А кількість глюкози поза кровоносним руслом при швидкій зміні кровонаповнення не встигає помітно змінитись. Тому отримані дані дають змогу обчислити концентрацію глюкози саме в крові. При цьому абсолютні значення кровонаповнення знати не обов'язково. Застосування мікропроцесора дозволяє робити потрібні обчислення в режимі on-line. Виділення зі світла, зворотно розсіяного тканиною тіла пацієнта, лише тієї його частини, яка виходить на певній відстані від місця входу і під певним кутом до поверхні шкіри, дозволяє значно покращити коректність вимірювань. Бо, якщо цього не робити, то у вихідному світловому потоці присутні частини світла, які пройшли в тілі людини дуже різні відстані, і, як наслідок, вимірюється спектральна інтенсивність змішаного світлового потоку, до якого, строго кажучи, не можна застосовувати відомий експоненціальний закон поглинання світла Ламберта-Бера. Отже, для коректного визначення концентрації глюкози в тілі людини потрібна сукупність усіх вказаних відмітних ознак. Точність вимірювання запропонованим способом додатково помітно покращується тим, що: - світловий пучок модулюють за інтенсивністю, і при вимірюванні інтенсивностей N(1)G, N(1)H , N(2)G, N(2)H, виділяють та вимірюють спектральні інтенсивності лише модульованої частини світла; - до та після зміни кровонаповнення вимірювання інтенсивностей N(1)G, N(1)H, N(2)G, N(2)H, повторюють по декілька разів, результати кожної серії вимірювань осереднюють і при обчисленні глюкози в крові пацієнта використовують осереднені значення спектральних інтенсивностей N(1)G, N(1)H, N(2)G та N(2)H. Модуляція інтенсивності зондуючого світлового пучка та вимірювання спектральної інтенсивності лише модульованої частини світла дають змогу позбутись також впливу паразитного зовнішнього засвічування. А кількаразове повторення вимірювань та осереднення результатів кожної серії вимірювань дозволяють позбутися або значно зменшити вплив усіх шумових факторів. Запропонований спосіб додатково конкретизується також тим, що: - довжина хвилі l G належить ближньому інфрачервоному діапазонові від 1000 до 2700нм і може бути взята з набору 1575, 1765 і 2270 ± 20нм або між 2080нм та 2200нм; - довжина хвилі l Η належить наборові (506,5±7)нм, (523±7)нм, (549±7)нм, (569±7)нм або (586±7)нм. Саме вказані довжини хвилі є найзручнішими. Розкриємо детальніше сутність запропонованого способу. Зазвичай неінвазійними спектрофотометричним, поляриметричним (та й іншими відомими) методами, строго кажучи, вимірюється не безпосередньо концентрація тієї чи іншої речовини в крові людини, а концентрація цієї речовини, усереднена по зондованому об'ємові тканини. Це відноситься як до глюкози, так і до гемоглобіну, і до інших біологічно важливих речовин. З гемоглобіном справа простіша. Оскільки він присутній тільки в крові і не виходить з кровоносного русла назовні, то його середня концентрація в тканині сHt пропорційна до його концентрації в крові с Н [див. патентну заявку України №2002021460]: (1) сHt=сНj де j - кровонаповнення тканини, тобто відношення об'єму крові, фактично присутньої в тканині, до об'єму всієї тканини, або іншими словами - об'ємна доля крові в тканині. Тому вимірювана спектрофотометричним методом концентрація гемоглобіну в тканині напряму залежить від кровонаповнення цієї тканини. Глюкоза, на відміну від гемоглобіну, як вже зазначалось, присутня не лише в крові, але й поза кровоносним руслом, особливо у м'язових клітинах. Тому усереднена концентрація глюкози в тканині с Gt задається іншою формулою (2) cGt=cGj+cGo де cG - концентрація глюкози в крові людини; cGo - концентрація глюкози поза кровоносним руслом. Зазвичай кровонаповнення пальця становить 2-3 об'ємних %. І якщо концентрація глюкози в крові cG навіть у 40 разів вища за cGo, то й тоді все одно доданки cGj і cGo порівнянні. Тому ігнорування cGo може приводити до значних похибок. Врахувати наявність глюкози поза кровоносним руслом можна, визначивши середню концентрацію глюкози в тканині для двох різних рівнів кровонаповнення (cGt(1)) та (cGt(2)). Позначаючи кровонаповнення в першому випадку через j1, а в другому через j2 і враховуючи те, що концентрації глюкози в крові та в клітинах поза кровоносним руслом від кровонаповнення не залежать, можна записати (3) cGt(1)=cGj1+cGo (4) cGt(2)=cGj2+cGo Звідси (5) cG=(cGt(2)-cGt(1))/(j2-j1) Найпростіший спосіб регульовано змінити рівень кровонаповнення кінцівки відомий медицині давно. Це накладання на вході в кінцівку еластичної надувної манжети. Якщо тиск, що створюється манжетою, нижчий за систолічний артеріальний тиск крові, але вищий за тиск крові у венозних судинах, то кров через артеріальні судини під манжетою продовжує надходити до кінцівки (у нашому випадку до кінцевої фаланги пальця), але відтікати через стиснуті зовні венозні судини вже не може. В результаті кровонаповнення пальця контрольовано зростає доти, доки тиск крові у венозних судинах не зрівняється з тиском, створеним манжетою. Досвід показує, що кровонаповнення може зрости у декілька разів. Коли з манжети випустити повітря і зняти таким чином зовнішній тиск на венозні судини, зайва венозна кров швидко відтікає з пальця, і кровонаповнення повертається до норми. Важливою обставиною є також те, що живі біологічні тканини мають складну структуру, а тому оптично є дуже неоднорідними. Крім поглинання, в них має місце значне розсіювання світла, яке варіює при переході від однієї ділянки тіла до іншої, від однієї особи до іншої, що значно ускладнює задачі аналізу. В тканині, як правило, крім речовини-аналіту присутня значна кількість інших біоречовин, які створюють "фон" поглинання; від нього не завжди просто відділити поглинання саме аналіту. Проходження світла крізь біотканину описується моделлю багатократних розсіювань, яка досить складна для підрахунків. З наявних експериментальних даних і комп'ютерного моделювання методом Монте-Карло випливає, що, коли світло входить в тканину у вигляді вузького пучка («світловий зонд»), то зворотно розсіяне світло розподіляється по досить великій площі на поверхні тканини. Спостерігається дифузно розмита кругла пляма. В наближенні геометричної оптики можна казати про траєкторії проходження світла в тканині. Можуть мати місце декілька його розсіювань на великі кути. Найкоротший теоретично можливий шлях світла в тканині в цьому випадку дорівнює відстані (х) між точками входу й виходу світла. Але імовірність розсіювань на великі кути набагато менша за імовірність розсіювань на малі кути. Тому найбільш імовірними є траєкторії проходження світла, обумовлені багатократними його розсіюваннями на малі кути. Якщо світловий зонд входить по нормалі до поверхні тіла і ми відбиратимемо для вимірювання світловий пучок, який виходить теж по нормалі до поверхні тіла, то пучок найбільш імовірних траєкторій групується навколо траєкторії, близької до дуги кола. Такий пучок траєкторій фахівці називають «бананом». Тільки при використанні гостросфокусованого світлового зонду з малим кутом розходження, при фіксованому напрямкові його входу в тіло і при фіксованому напрямкові виходу вимірюваного розсіяного пучка світла з тіла середньостатистичний шлях S світла в тканині є більш-менш фіксованим і пропорційним до відстані x між вхідним та вихідним пучками, яка задається відповідною конструкцією приладу. І тільки за таких обставин можна користуватись відомим експоненціальним законом послаблення інтенсивності світла, який називають законом Ламберта-Бера. Розглянемо детальніше проходження світла крізь живу тканину і виведемо формулу для обчислення концентрації глюкози в крові пацієнта. Застосовуватимемо такі позначення: l G - довжина хвилі світла при вимірюванні поглинання глюкозою; l Η - довжина хвилі світла при вимірюванні поглинання гемоглобіном; FGі, F Ні - інтенсивності світла відповідно з довжинами хвиль l G і l Η при вході в тканину; FG, F Н - інтенсивності світла відповідно з довжинами хвиль l G і l Η при виході з тіла; SG, SH - середні довжини шляху, який проходить світло відповідно з довжинами хвиль l G і l Η між входом в тканину й виходом з неї; KsG, KsH - коефіцієнти послаблення світла, зумовлені розсіюванням тканиною, на довжинах хвиль l G і l Η відповідно; kG - питомий коефіцієнт поглинання глюкози на довжині хвилі l G; kН - питомий коефіцієнт поглинання гемоглобіну на довжині хвилі l Η; KbG, KbH - коефіцієнти "фонового" поглинання світла на довжинах хвилі l G і l Η відповідно; Ζ - множник, який враховує загальні втрати світла, пов'язані з тим, що ми збираємо для вимірювань лише частину зворотно розсіяного тілом світла. За законом Ламберта-Бера на довжині хвилі l G для двох різних рівнів кровонаповнення мають місце співвідношення: (6) FG(1)=FGiΖехр[-(KsG(1)+KbG(1)+kGcGt(1))sG] (7) FG(2)=FGiΖехр[-(KsG(2)+KbG(2)+kGcGt(2))sG] Тут враховано те, що питомий коефіцієнт поглинання глюкозою kG не залежить від кровонаповнення. Мало залежить від кровонаповнення і коефіцієнт розсіювання світла тканиною (KsG(1)»KsG(2)). Але в коефіцієнтах "фонового" поглинання KbG(1) і KbG(2) варто явно виділити ті складові, які залежать від кровонаповнення тканини j1 і j2 (8) KbG(1)=Kbo+(kwcw+kHGсH)j1 (9) KbG(2)=Kbo+(kwcw+kHGсH)j2 де Kbo - коефіцієнт "фонового" поглинання усіма компонентами тканини, які знаходяться поза кровоносним руслом, при довжині хвилі l G; kw - питомий коефіцієнт поглинання води при довжині хвилі l G; cw - концентрація води в крові; kHG - питомий коефіцієнт поглинання гемоглобіну при довжині хвилі l G. Ці величини (Kbo, kw, cw, kHG) не залежать від кровонаповнення тканини. У виразах (8) і (9) враховані лише ті компоненти крові, які суттєво поглинають світло з довжиною хвилі l G; в разі необхідності можуть бути враховані й інші. Якщо поділити (6) на (7) з урахуванням (3), (4), (8) і (9), то отримаємо (10) FG(1)/F G(2)=ехр[(kwcw+kHGcH+kGcG)(j2-j1)] звідки cG={(lп(F G(1)/F G(2))/[(kGsG(j2-j1)]}(11) [(kwcw+kHGcHb)/kG] У цій формулі параметри kG, kw , kHG є фізичними константами відповідно глюкози, води і гемоглобіну, sG - константою, яка визначається конструкцією приладу, cw і сН - параметри складу крові, які для конкретного пацієнта є стабільними. Тепер розкриємо, як можна визначити різницю кровонаповнень (j2-j1) у формулі (11). Для цього запишемо рівняння, аналогічні рівнянням (6) і (7), але на цей раз для світла з довжиною хвилі l Η (теж для двох рівнів кровонаповнення j2 і j1): (12) FG(1)=F HiZexp[-(KsH(1)+KbH(1)+kHCHt(1))sH] (13) FG(2)=F HiZexp[-(KsH(2)+KbH(2)+kHCHt(2))sH] Коефіцієнт розсіювання світла KsH та фонового поглинання KbH тканиною тіла дуже мало залежать від кровонаповнення тканини (бо всі інші компоненти тканини, крім крові, залишаються незмінними). Тому можна вважати, що KsH(1)=KsH(2) і KbH(1)=KbH(2). Від кровонаповнення не залежить і питомий коефіцієнт поглинання світла гемоглобіном KН. Основною складовою крові, крім гемоглобіну, є вода. Але вона на довжині хвилі l Η є прозорою і практично не поглинає світло. А концентрація інших складових крові є настільки малою порівняно з водою та гемоглобіном, що їх поглинанням можна тут знехтувати. Тоді, відповідно до (1) (14) cHt(1)=cHj1 (15) cHt(2)=cHj2 Поділимо (12) на (13) (16) FG(1)/F H(2)=ехр[KsH(cHt(2)-сHt(1))] звідки з урахуванням (14) і (15) знаходимо (17) j2-j1=ln(F H(1)/F H(2))/(kHGсHbsН) Підставивши (17) в (11), отримаємо наступну формулу для визначення концентрації глюкози в крові cG=сHА{В[ln(F G(1)/FG(2))/ln(F H(1)/F H(2))]-1}-С (18) де A=kHG/kG, B=s H/sG, C=kwcw/kHG (19) - константи, які можна визначати при калібруванні приладу. Після аналого-цифрового перетворення відношення світлових потоків замінюються відношеннями отриманих відповідних двійкових кодів N(1)G, N(2)G, N(1)H, N(2)H,. І ми приходимо до остаточної розрахункової формули: cG=сНА{В[In(NG(1)/NG(2))/In(NH(1)/NH(2))]-1}-С (20) Величину сН концентрації гемоглобіну в крові беруть з медичної картки пацієнта чи одноразово визначають іншим способом, бо вона з часом практично не змінюється, або змінюється досить повільно. її заносять у пам'ять мікропроцесора, який потім автоматично використовує її при обчисленнях. Оновлення значення с H можна проводити раз на 3-4 місяці й лише у необхідних випадках (це встановлює лікар) частіше. Розглянемо два приклади можливої реалізації запропонованого способу. Приклад 1. На Фіг.1 зображено у поперечному розрізі оптичну голівку 1 з виїмкою 2 для пальця пацієнта, кінцеву фалангу 3 пальця пацієнта, ніготь 4. В стінку оптичної голівки 1 виведено оптоволоконні світловоди 5, 6, 7 і 8. При підготовці до вимірювання кінцеву фалангу пальця 3 кладуть у виїмку 2 і тим самим приводять в оптичний контакт зі світловодами 5, 6, 7 і 8. Також створюють передумови для неінвазійної зміни кровонаповнення пальця, наприклад, на плече цієї ж руки накладають еластичну надувну манжету, які зазвичай використовують при вимірюванні артеріального тиску. Далі через світловід 5 неінвазійно, крізь шкіру, просвічують ділянку кінцевої фаланги пальця сконцентрованим пучком світла, напрямленим перпендикулярно до шкіри. Довжина хвилі цього світла l G=2100нм належить спектральній смузі поглинання глюкозою. Зі світла, яке пройшло крізь тканину пальця пацієнта, за допомогою оптоволокна 6 збирають ту частину, яка виходить з пальця на певній відстані від місця входу перпендикулярно до поверхні шкіри. Найімовірніша траєкторія проходження цього світла зображена на Фіг.1 пунктирною кривою 9. Вимірюють спектральну інтенсивність NG(1) цієї частини світла. Далі через оптоволокно 7 просвічують ту ж кінцеву фалангу пальця пучком світла, теж напрямленим ортогонально до шкіри. Це світло з довжиною хвилі l Η=549нм добре поглинається гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном. За допомогою оптоволоконного світловода 8 збирають ту частину цього світла, яка виходить з пальця перпендикулярно до поверхні шкіри на заданій відстані від місця входу. Ця відстань значно менша відстані між світловодами 5 та 6, бо концентрація гемоглобіну в тканині пальця значно більша за концентрацію глюкози. Вимірюють спектральну інтенсивність NH(1) цієї частини світла. Після цього неінвазійно змінюють кровонаповнення досліджуваного пальця шляхом накачування повітря в накладену на руку манжету, наприклад, до 60мм рт. cт. Зачекавши 10-30с, доки кровонаповнення кінцівки руки помітно зросте (це видно за її почервонінням-посинінням), повторюють групу попередніх операцій, в результаті котрих вимірюють значення спектральних інтенсивностей світла NG(2) та NH(2) при значно вищому кровонаповненні. З допомогою мікропроцесора за формулою (20) обчислюють концентрацію глюкози в крові пацієнта. Приклад 2. При підготовці до вимірювання кінцеву фалангу пальця З кладуть у виїмку 2 і тим самим приводять в оптичний контакт зі світловодами 5, 6, 7 і 8. Передумови для неінвазійної зміни кровонаповнення пальця створюють, накладаючи на першу фалангу цього ж пальця еластичну надувну кільцеву манжету. На Фіг.2 схематично зображено поперечний переріз першої фаланги пальця 11 з надітим на неї гумовим надувним кільцем 12, яке локально стискує палець з усіх боків (умовно це зображено стрілочками). Через м'яку тканину пальця тиск передається на кістку 13, артеріальні та венозні судини 14 та 15. Спочатку повітря з гумового кільця випущене, і кров вільно циркулює в пальці, підтримуючи його звичайне кровонаповнення. Далі виконують такі самі операції вимірювання спектральних інтенсивностей NG(1) та NH(1), як і в прикладі 1. Лише порядок їх може бути змінений (спочатку вимірюється NH(1), а вже потім NG(1)). Після цього в гумове кільце впускають повітря під тиском 80мм рт. cт. Зачекавши 5-10с, поки кінцева фаланга пальця додатково наповниться кров'ю, повторюють вимірювання спектральних інтенсивностей NH(2) та NG(2). За формулою (20), обчислюють концентрацію глюкози в крові пацієнта й виводять отримане значення для зчитування. Аналогами запропонованого нами пристрою для неінвазійного вимірювання концентрації глюкози в крові людини, призначеного для реалізації вищеописаного способу, є пристрої, описані у патентах, згаданих при обгрунтуванні способу. В [європейському патенті №0160768 А1] описано пристрій-аналог, який складається з джерела світла, що спрямовується на ділянку тіла пацієнта. Спектральний склад цього світла є таким, що дозволяє йому проникати крізь шкіру в область під поверхнею шкіри, де може бути виміряна концентрація глюкози і від якої світло може бути зібране після часткового поглинання, залежного від концентрації глюкози. До складу пристрою-аналога входять також вузол збирання світла, яке пройшло крізь або дифузно відбите від вказаної області; детектори для перетворення зібраного світла в електричні сигнали окремо для кожної щонайменше з двох спектральних смуг (одна з яких вимірювальна, інша - опорна); обчислювальний вузол для перетворення вказаних електричних сигналів на результат вимірювання глюкози і видачі його в зручному для зчитування вигляді. Пристрій містить також вузол неперервного або ступінчастого варіювання кута падіння світла на тіло, вказані варіації призводять до варіації глибини області під шкірою, з якої збирається світло після поглинання. Вказаний вузол складається з дзеркальця, що може зміщуватись відносно світлового пучка. Його позиція змінює кут падіння світла на тіло. Зворотно розсіяне від тіла світло збирається через одну й ту ж область шкіри, якою б не була позиція дзеркала. Вузол збирання світла складається з інтегруючої відбиваючої поверхні у вигляді напівсфери, вказана поверхня покрита з середини золотом або шаром сульфату барію. Спільними ознаками цього аналога і запропонованого нами пристрою є: джерело світла, випромінювання якого містить світло з довжиною хвилі l G, характерною для поглинання глюкозою; вузол для спрямування цього світла від джерела до вибраної ділянки шкіри пацієнта; вузол для збирання частини світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до фотоприймача, чутливого до світла з довжиною хвилі l G, який перетворює світловий потік на пропорційний електричний сигнал; електронні підсилювачі; обчислювальний вузол для перетворення вказаних електричних сигналів на результат вимірювання глюкози і видачі його в зручному для зчитування вигляді. Причинами, що заважають вирішенню поставленої задачі в пристрої-аналозі, є те, що в ньому вузол для збирання частини світла, яке провзаємодіяло з досліджуваною ділянкою тіла пацієнта, збирає світло, яке виходить через поверхню шкіри в занадто широкому діапазоні кутів. Це не дозволяє однозначно говорити ні про глибину проникнення цього світла в тіло, ні про довжину його шляху в тілі. Ще більш важливим є те, що в ньому відсутні елементи й зв'язки, які дозволяють врахувати зміни кровонаповнення просвічуваної ділянки тіла, і в пам'ять обчислювального вузла закладено не зовсім коректну програму обчислення концентрації глюкози. В [патенті США №6097975] описано інший пристрій-аналог, до складу якого входять: джерело світла, випромінювання якого містить світло з довжиною хвилі l G в діапазоні між 2080нм та 2200нм, що добре поглинається глюкозою; вимірювальний канал, що складається з першого світлофільтра, який пропускає вузькосмугове світло в межах вказаного діапазону довжин хвилі, першого фотодетектора, здатного вимірювати світло, пропущене вказаним світлофільтром, з першого підсилювача імпульсів та з першого аналого-цифрового перетворювача (АЦП); перший оптоволоконний вузол, здатний передавати світло від джерела світла до шкіри пацієнта, приймати зворотно розсіяне пацієнтом світло й передавати це світло до вимірювального каналу; опорний канал, що складається з другого світлофільтра, другого фотодетектора, другого підсилювача імпульсів та другого АЦП, кожний з яких є ідентичним відповідному елементу вимірювального каналу; другий оптоволоконний вузол, здатний передавати світло від джерела світла до опорного каналу; і вузол обробки (мікропроцесор), здатний порівнювати виходи вимірювального та опорного каналів для кількісного визначення інтенсивності світла, що поглинається глюкозою крові пацієнта. Спільними ознаками цього пристрою-аналога і запропонованого нами пристрою є: джерело світла, випромінювання якого містить світло з довжиною хвилі l G, що добре поглинається глюкозою; оптоволоконний вузол для спрямування цього світла від джерела до вибраної ділянки шкіри пацієнта; оптоволоконний вузол для збирання частини світла, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до фотоприймача, чутливого до світла з довжиною хвилі l G, який перетворює світловий потік на пропорційний електричний сигнал; електронні підсилювачі, входом підключені до відповідного фотоприймача; АЦП, входи якого підключені до виходів електронних підсилювачів; вузол обробки (мікропроцесор) для перетворення вказаних електричних сигналів на результат вимірювання глюкози і видачі його в зручному для зчитування вигляді. Причинами, що заважають вирішенню поставленої задачі в пристрої-аналозі, є те, що в ньому відсутні елементи й зв'язки, які дозволяють врахувати дуже суттєві «фонове» поглинання та розсіювання світла, зміни кровонаповнення просвічуваної ділянки тіла, і в пам'ять вузла обробки закладено не зовсім коректну программу обчислення концентрації глюкози. Найближчим до нашого винаходу за сукупністю суттєвих ознак є пристрій, описаний в [патентній заявці США №20020123677]. Цей пристрій узято нами як пристрій-прототип. До складу пристрою-прототипу входять: вузол фіксації об'єкта вимірювання; вузол ближнього інфрачервоного (БІЧ) опромінювання з неперервним поділом діапазона довжин хвилі від 0,8 до 2,5мкм на вузькі спектральні інтервали, який по черзі опромінює об'єкт вимірювання кожним з них; вузол фотоелектричного перетворення для прийому та перетворення світла, що пройшло крізь або відбите від об'єкта; і вузол розрахунку концентрації глюкози в крові шляхом аналізу спектра поглинання. Вузол фіксації об'єкта вимірювання може викликати застій крові шляхом стискування фаланги пальця гумовим кільцем. Вузол БІЧ опромінювання складається з джерела світла, акусто-оптичного перенастроюваного осциляторного фільтра, високочастотного (ВЧ) вібратора для створення вібрацій у вказаному фільтрі та ВЧ генератора напруги для подачі високої частоти на вказаний вібратор. Вузол фотоелектричного перетворення для прийому та перетворення світла складається зі світлосприймаючого елемента для прийому світла, що пройшло крізь об'єкт вимірювання, і елемента, який перетворює його в сигнали спектра поглинання. Вузол розрахунку концентрації глюкози в крові складається з аналізатора форми спектра поглинання та обчислювача (мікропроцесора). Спільними ознаками пристрою-прототипа і запропонованого нами пристрою є: (7) вузол фіксації об'єкта вимірювання, що має можливість змінювати кровонаповнення цього об'єкта; (2) джерело світла, випромінювання якого містить світло з довжиною хвилі l G, характерною для поглинання глюкози, (3) схема живлення та керування джерелом світла, (4) перший волоконно-оптичний світловід для спрямування світла з довжиною хвилі l G від джерела до вибраної ділянки шкіри пацієнта, (5) другий волоконно-оптичний світловід для збирання частини світла з довжиною хвилі l G, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до (6) фотоприймача, чутливого до світла з довжиною хвилі l G, який перетворює світловий потік на пропорційний електричний сигнал, (7) електронні підсилювачі, входом підключені до відповідного фотоприймача, (8) аналого-цифровий перетворювач (АЦП), входи якого підключені до виходів електронних підсилювачів, (9) мікропроцесор, до якого підключений вихід АЦП і в пам'яті якого містяться програми обчислення концентрації глюкози та видачі інформації, (10) індикаторне табло, приєднане інформаційною шиною до мікропроцесора, та (77) блок живлення. Причинами, що заважають вирішенню поставленої задачі в пристрої-прототипі, є те, що в ньому стискування пальця за допомогою гумового кільця не забезпечує регульованої зміни кровонаповнення (адже товщина різних пальців людини і пальців різних людей є різною). Відсутні елементи та зв'язки для вимірювання фактичної зміни кровонаповнення, що не дає змоги коректно обчислити концентрацію глюкози в крові. В основу даного винаходу поставлено задачу шляхом введення у пристрій додаткових елементів та зв'язків між ними врахувати поточне кровонаповнення просвічуваної ділянки тіла, дозовано змінювати його і на цій основі значно коректніше обчислити концентрацію глюкози в крові людини; ліквідувати значні відхилення, пов'язані з фізіологічними змінами кровонаповнення, повністю реалізувати описаний вище спосіб визначення концентрації глюкози в крові людини. Розв'язок поставленої технічної задачі досягається тим, що запропонований пристрій складається з - вимірювального ложа для пальця пацієнта, на котрому провадяться вимірювання, яке оснащене еластичним надувним кільцем-манжетою; - джерела світла, випромінювання якого містить світло з довжиною хвилі l G, що добре поглинається глюкозою, і світло з довжиною хвилі l Η, яке добре поглинається гемоглобіном, причому однаково обома його головними формами (відновленим гемоглобіном і оксигемоглобіном); - схеми живлення та керування джерелом світла; - з 1 -го волоконно-оптичного світловода для спрямування світла з довжиною хвилі l G від джерела до вибраної ділянки шкіри пацієнта; - 2-го волоконно-оптичного світловода для збирання частини світла з довжиною хвилі l G, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до - 1-го фотоприймача, чутливого до світла з довжиною хвилі l G, який перетворює світловий потік на пропорційний електричний сигнал; - з 3-го волоконно-оптичного світловода для спрямування світла з довжиною хвилі l Η від джерела до вибраної ділянки шкіри пацієнта; - 4-го волоконно-оптичного світловода для збирання частини світла з довжиною хвилі l Η, яке пройшло крізь досліджувану ділянку тіла пацієнта або зворотно розсіяне нею, і для передачі цього світла до - 2-го фотоприймача, чутливого до світла з довжиною хвилі l Η, який перетворює світловий потік на пропорційний електричний сигнал; - кінці 1-го, 2-го, 3-го та 4-го світловодів виведені в стінку вимірювального ложа, де вони оптично контактують з пальцем; - з 1-го електронного підсилювача, входом підключеного до 1-го фотоприймача; - з 2-го електронного підсилювача, входом підключеного до 2-го фотоприймача; - з аналого-цифрового перетворювача (АЦП), входи якого підключені до виходів електронних підсилювачів; - з мікропроцесора, до якого підключений вихід АЦП і в пам'яті якого містяться програми обчислення концентрації глюкози, керування роботою пристрою та видачею інформації; - з блока управління тиском в манжеті, який пневматично з'єднаний з манжетою і може бути керованим від мікропроцесора; - з індикаторного табло, приєднаного інформаційною шиною до мікропроцесора, та - з блоку живлення. Параметри пристрою та точність визначення концентрації глюкози в крові пацієнта додатково покращуються, якщо: - як джерела світла з довжинами хвилі l G та l Η застосовуються лазерні світлодіоди або напівпровідникові лазери; - довжина хвилі l G належить ближньому інфрачервоному діапазонові від 1000 до 2700нм і може бути взята з набору 1575, 1765 і 2270 ± 20нм або між 2080нм та 2200нм; - довжина хвилі l Η належить набору (506,5±7)нм, (523±7)нм, (549±7)нм, (569±7)нм або (586±7)нм; - до складу схеми живлення та керування джерелом світла також входять модулятори інтенсивності випромінювання, до складу електронних підсилювачів - синхронні демодулятори, модулятори та демодулятори керуються від мікропроцесора; - перед фотоприймачами встановлено світлофільтри, які пропускають до кожного з них лише світло з відповідною вузькою спектральною смугою, наприклад, перед 1-м фотоприймачем - шириною 15-20нм, а перед 2-м фотоприймачем - шириною 5-8нм; - до складу пристрою входять також клавіатура для керування режимами роботи пристрою і блок зв'язку з зовнішньою ЕОМ, а в пам'яті мікропроцесора містяться також програми взаємодії через клавіатуру з користувачем та через блок зв'язку з зовнішньою ЕОМ. Блок управління тиском в манжеті складається з невеличкого ресивера, мінікомпресора, манометра, трьохходового клапана, автоматично керованого від мікропроцесора, та з необхідних з'єднувальних трубок. Відмітними ознаками запропонованого пристрою є те, що він порівняно з прототипом додатково має в своєму складі джерело світла з довжиною хвилі l Η, яке добре поглинається гемоглобіном, причому однаково обома його головними формами - відновленим гемоглобіном і оксигемоглобіном; третій волоконно-оптичний світловід для спрямування цього світла до обраної ділянки шкіри пацієнта; четвертий волоконно-оптичний світловід для збирання частини світла з довжиною хвилі l Η після його взаємодії з обраною ділянкою тіла пацієнта, який передає зібране світло до 2-го фотоприймача, чутливого до світла з довжиною хвилі l Η; до складу вимірювального ложа входить еластичне надувне кільце-манжета для надівання на палець пацієнта, на котрому провадяться вимірювання; в стінку вимірювального ложа виведені кінці 1-го, 2-го, 3-го та 4-го світловодів, які при вимірюваннях оптично контактують з пальцем; блок управління тиском в манжеті, який пневматично з'єднаний з манжетою і може бути керованим від мікропроцесора; в пам'яті мікропроцесора міститься програма обчислення концентрації глюкози за формулою (20) або за іншим алгоритмом, який дає практично ті ж самі результати. Саме сукупність відмітних ознак дозволяє розв'язати поставлену задачу. Наявність додаткового джерела світла з довжиною хвилі l Η, яке добре поглинається загальним гемоглобіном крові, 3-го й 4-го волоконно-оптичних світловодів, 2-го фотоприймача й 2-го електронного підсилювача, вимірювального ложа, в стінку якого виведені кінці 1-го, 2-го, 3-го та 4-го світловодів, які оптично контактують з пальцем, дозволяє коректно врахувати зміни кровонаповнення просвічуваної ділянки тіла. Наявність у складі вимірювального ложа еластичного надувного кільця-манжети, наявність блоку управління тиском в манжеті, який пневматично з'єднаний з манжетою і може бути керованим від мікропроцесора - дозволяють керовано змінювати кровонаповнення пальця і відтак коректно визначати, яка частина світлового потоку поглинається глюкозою, розчиненою безпосередньо в крові, і відділити її від глюкози, що знаходиться поза кровоносним руслом. Застосування мікропроцесора дозволяє керувати роботою пристрою і робити потрібні обчислення в режимі on-line. А занесення в пам'ять мікропроцесора програми обчислення за формулою (20) або за іншим алгоритмом, який дає практично ті ж самі результати, дозволяє отримати коректне значення концентрації глюкози саме в крові пацієнта. Блок-схема запропонованого пристрою наведена на Фіг.3. До неї входить вимірювальне ложе 16 для пальця пацієнта 17, оснащене еластичним надувним кільцем-манжетою 18. В стінки вимірювального ложа 16 виведені кінці 1-го, 2-го, 3-го та 4-го оптоволоконних світловодів (19, 20, 21 та 22 відповідно), які оптично контактують з пальцем. Інший кінець 1-го оптоволоконного світловода 19 оптично приєднаний до джерела світла 23, до того його виходу, через котрий виходить випромінювання з довжиною хвилі l G. А інший кінець 3-го оптоволоконного світловода 21 оптично приєднаний до того виходу джерела світла 23, через котрий виходить випромінювання з довжиною хвилі l Η. Інший кінець 2-го оптоволоконного світловода 20 оптично приєднаний до 1-го фотодетектора в блоці фото детекторів та електронних підсилювачів 24, а інший кінець 4-го оптоволоконного світловода 22 - до 2-го фотодетектора в тому ж блоці. Виходи 1-го та 2-го електронних підсилювачів підключені до входів АЦП 25. Вихід та вхід керування АЦП підключені до мікропроцесора 26, в пам'яті якого містяться програми обчислення концентрації глюкози, керування роботою пристрою та видачею інформації. Один з виходів мікропроцесора 26 підключено до схеми живлення та керування джерелом світла 27, інший - до блоку управління тиском в манжеті 28, який пневматично з'єднаний з манжетою 18. Одна інформаційна шина мікропроцесора 26 з'єднує його з індикаторним табло 27, інша - зі схемою взаємодії з зовнішньою ПЕОМ 28. Входи мікропроцесора 26 підключені також до міні-клавіатури 29. Очевидні з'єднання блоку живлення 30 з усіма електронними блоками пристрою на Фіг.3 для спрощення не зображені. Більш точні й надійні результати вимірювань можна отримати, якщо до складу схеми живлення та керування джерелом світла 27 входять також модулятори інтенсивності світла, а до складу електронних підсилювачів в блоці 24 входять також синхронні демодулятори, модулятори та демодулятори керовані від мікропроцесора 26 (цей зв'язок зображений пунктирною стрілкою). Якщо випромінювання джерела світла 23 недостатньо монохроматичне, то в блоці 24 перед фотоприймачами встановлено світлофільтри, які пропускають до кожного з них лише світло з відповідною вузькою спектральною смугою. На Фіг.4 показано один з можливих варіантів виконання блоку управління тиском в манжеті 28. Тут зображено трьохходовий клапан 31, керований або вручну, або автоматично від мікропроцесора 26. Один кінець клапана через з'єднувальну трубку 32 пневматично підключений до кільця-манжети 18, другий кінець - до ресивера 33, а третій кінець має вихід в атмосферу. Тиск в ресивері 33 контролюється мініатюрним манометром 34. Створення потрібного тиску в ресивері 33 забезпечується невеличким мінікомпресором 35, який може бути ручним (наприклад, звичайна гумова "груша") або автоматично діючим і запускатися від мікропроцесора 26. Внутрішній об'єм ресивера 33 набагато більший за внутрішній об'єм кільця-манжети 18 (напр., 200мл та 5-10мл відповідно). Запропонований пристрій для неінвазійного вимірювання концентрації глюкози в крові людини функціонує так. Перед вимірюваннями за допомогою компресора 35 в ресивер 33 нагнітається повітря до досягнення заданого тиску (наприклад, 60мм рт. ст.), який контролюється манометром 34. Трьохходовий клапан 31 пневматично з'єднує еластичне кільце-манжету 18 з атмосферою так, що в отвір кільця-манжети 18 може легко входити палець. При підготовці до вимірювання пацієнт просуває свій палець 17 крізь отвір кільця-манжети 18, кладе пучку пальця 17 на вимірювальне ложе 16 і натискає кнопку „Пуск" на клавіатурі 29. Мікропроцесор 26 через схему керування джерелом світла 27 вмикає джерело світла з довжиною хвилі l G, за наперед заданою програмою модулює інтенсивність його випромінювання і одночасно керує демодуляцією відповідного світлового сигналу в блоці 24. Двійковий код (NG(1)) виміряної спектральної інтенсивності запам'ятовується. Далі мікропроцесор 26 через схему керування джерелом світла 27 вимикає перше і вмикає друге джерело світла з довжиною хвилі l Η. Проводиться вимірювання другої спектральної інтенсивності і запам'ятовується и двійковий код ΝΗ(1). Після цього за сигналом від мікропроцесора 26 клапан 31 перекриває вихід кільця-манжети 18 в атмосферу і приєднує його до ресивера 33. Тиск у манжеті 18 зростає до заданого рівня. Вона, в свою чергу, створює такий же тиск на першу чи середню фалангу пальця. В результаті кровонаповнення пальця починає зростати. Мікропроцесор організує періодичне вимірювання спектральної інтенсивності в каналі вимірювання концентрації гемоглобіну, тобто на довжині хвилі l Η. Коли ця спектральна інтенсивність стабілізується, мікропроцесор 26 запам'ятовує відповідний код NH(2), організує вимірювання спектральної інтенсивності на довжині хвилі l G і запам'ятовує відповідне значення NQ(2). Після закінчення вимірювань мікропроцесор 26 подає сигнал на керований клапан 31, який перекриває вихід кільця-манжети 18 до ресивера 33 і відкриває вихід в атмосферу. Зайве повітря виходить з манжети, і пацієнт може вільно вийняти палець з вимірювального ложа. Мікропроцесор 26 розраховує концентрацію глюкози в крові пацієнта за формулою (20) і виводить отримане значення на індикаторне табло 27. Порядок вимірювань може бути й іншим. Пацієнт просуває свій палець 17 через кільце-манжету 18, вручну за допомогою клапана 31 перекриває її вихід в атмосферу, відкриває вихід до ресивера 33 і з допомогою компресора 35 нагнітає в ресивер 33 повітря до досягнення потрібного тиску. Відтік крові з пальця перекривається, і його кровонаповнення починає зростати. Коли палець достатньо почервоніє, користувач натискає кнопку „Пуск" на клавіатурі 29. Пристрій вимірює значення NG(1) та NH(1) і подає користувачеві звуковий сигнал. Тоді пацієнт вручну перемикає вихід кільця-манжети 18 на атмосферу. Повітря виходить з неї, відкриваючи можливість відтоку крові з пальця. Коли палець достатньо „побіліє", тобто прийде в звичайний стан, пацієнт знову натискає кнопку „Пуск" на клавіатурі 29. Пристрій вимірює значення NG(1) та NH(1) і далі діє, як описано раніше. Подальше функціонування пристрою залежить від режиму роботи, заданого користувачем за допомогою клавіатури 29. Це може бути запам'ятовування результату в енергонезалежній пам'яті, видача результату через схему взаємодії 28 і послідовний канал зв'язку на зовнішню ПЕОМ чи в медичну комп'ютерну мережу та інші сервісні функції. Запропонований пристрій може бути реалізований в промислових умовах. Як джерела світла можна використати промислові світлодіоди чи напівпровідникові лазери. Потрібні оптоволоконні світловоди та фото детектори теж випускаються промисловістю. Виготовлення еластичного гумового кільця-манжети та блоку управління тиском в манжеті теж не викликає труднощів. Приблизно такі ж вузли широко застосовують в приладах домашнього вжитку для напівавтоматичного вимірювання артеріального тиску. Для реалізації всіх інших електронних блоків застосовується стандартна мікроелектронна елементна база промислового виготовлення. Такий неінвазійний пристрій чекають мільйони хворих на діабет в усіх країнах світу.
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for noninvasive measurement of glucose blood content and device for its realization
Автори англійськоюVoitovych Ihor Danylovych
Назва патенту російськоюСпособ неинвазивного определения концентрации глюкозы в крови человека и устройство для его реализации
Автори російськоюВойтович Игорь Данилович
МПК / Мітки
МПК: G01N 33/49, A61B 5/1455
Мітки: спосіб, пристрій, неінвазійного, глюкози, концентрації, визначення, крові, людини, реалізації
Код посилання
<a href="https://ua.patents.su/10-78817-sposib-neinvazijjnogo-viznachennya-koncentraci-glyukozi-v-krovi-lyudini-ta-pristrijj-dlya-jjogo-realizaci.html" target="_blank" rel="follow" title="База патентів України">Спосіб неінвазійного визначення концентрації глюкози в крові людини та пристрій для його реалізації</a>
Попередній патент: Мийний засіб для дезактивації
Наступний патент: Оптичний коноскопічний пристрій для вимірювання рельєфу поверхні
Випадковий патент: Спосіб лікування менінгококцемії у дітей