Алкіламінокетони
Номер патенту: 37199
Опубліковано: 15.05.2001
Автори: Йоганнес Ебі, Сінез Жолідон, Олів'є Моран, Філіп Гюєррі
Формула / Реферат
1. Алкиламинокетоны формулы I
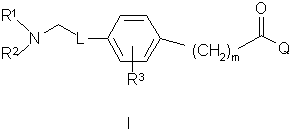
где m, L, Q, R1, R2 и R3 имеют такие значения, которые соответствуют следующим соединениям:
4-[[б-(аллилметиламино) гексил] окси]-3,4'-дибромбензофенон,
4-[[4-(аллилметиламино) 2-бутенил] окси]-3,4'-дибромбензофенон,
3-хлор-4'-йод-4-[[б"(аллилметиламино) гексил] окси] бензофенон,
4'-бром-3-хлор-4-[[6-(аллилметиламино) гексил] окси] бензофенон,
2,4-[[(4-диметиламино)-2-бутенил] окси]-3,4-дибромбензофенон,
4-[[4-(диметиламино)-2-бутенил] окси]-3-хлорбензофенон,
4'-бром-3-хлор-4-[[6-(диметиламино) гексил] окси] бензофенон,
3,4-дихлорфенил-4'-[(диметиламино) метил]-4-бифенилкетон,
4'-[(аллилметиламино) метил]-4-бифенил-3,4-дихлорфенилкетон,
(RS)-4'-(диметиламинометил)-4-бифенил-2,6-диметил-5-гептенилкетон,
п-бромфенил-2-хлор-4'-[(диметиламино) метил]-4-бифенилкетон,
4'- [(диметиламино) метил] -4-бифенилпропилкетон,
[4-[6-(аллилметиламино)-гексилокси]-фенил]-(4-бромфенил)-метанон,
[4-[4-(аллилметиламино)-бутокси]-фенил]-(4-бромфенил)-метанон,
[4-[6-(аллилметиламино)-гексилокси]-3-фторфенил]-(4-бромфенил)-
метанон,
[4-[6-(аллилметиламино)-гексилокси]-2-фторфенил]-(4-бромфенил)-
метанон,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-(4-
трифторметилфенил)-метанон,
(Ε)- [4- [4-(аллилметиламино)-бут-2-енилокси] -3 -фторфенил] -(4-бромфенил)-метанон,
(Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-5-метилгексан-1-он,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-(4-йодфенил)-метанон,
(Е)-1-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-5-метилгексан-1 -он,
(Е)-[4- [4-(аллилметиламино)-бут-2-енилокси] -3 -фторбензоил] -бензонитрил,
(Е)-4-[4-[4-(аллилметиламино)-бут-2-енилокси]-бензоил]-бензонитрил,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-(2,6-дифторфенил)-метанон,
(Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-5-метилгекс-4-ен-1-он,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-2-фторфенил]-(4-бромфенил)-метанон,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-(4-фторфенил)-метанон,
(Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-3 -фторфенил ]-6-метилгепт-5-ен-2-он,
(Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-1-(4-бромофенил)-этанон,
(Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси)-фенил]-1-(4-бромфенил)-этанон,
(Е)-(4-бромфенил)-[4-[4-(этилметиламино)-бут-2-енилокси]-фенил]-метанон,
4'-[(аллилметиламино)-метил]-2-хлор-4-бифенил-п-бромфенилкетон,
и их фармацевтически приемлемые соли присоединения кислот.
2. Алкиламинокетоны формулы I по п.1, обладающие снижающим содержание холестерина действием.
Приоритет по пунктам:
14.07.93 - по п.2 и по п.1 формулы, а именно:алкиламинокетоны формулы I, которые соответствуют следующим соединениям:
4-[[6-(аллилметиламино) гексил] окси]-3,4´дибромбензофенон,
4-[[4-(аллилметиламино)-2-бутенил] окси]-3,4'-дибромбензофенон,
3-хлор-4'-йод-4-[[6-(аллилметиламино) гексил] окси ]-бензофенон,
4'-бром-3-хлор-4-[[6-(аллилметиламино) гексил] окси]-бензофенон,
2,4-[[4-(диметиламино)-2-бутенил] окси]-3,4'-дибромбензофенон,
4-[[4-(диметиламино)-2-бутенил] окси] -3 -хлорбензрфенон,
4'-бром-3-хлор-4-[[6-(диметиламино) гексил] окси]-бензофенон,
3,4-дихлорфенил-4'-[(диметиламино) метил]-4-бифенилкетон,
4'-[(аллилметиламино) метил] -4-бифенил-3,4-дихлорфенилкетон,
(RS)-4-(диметиламинометил)-4-бифенил-2,6-диметил-5-гептанилкетон,
п-бромфенил-2-хлор-4'-[(диметиламино)метил]-4-бифенилкетон,
4'-[(диметиламино) метит]-4-бифенилпропилкетон,
и их фармацевтически приемлимые соли присоединения кислот;
28.04.94 - по п. 2 и по п. 1 формулы, а именно:алкиламинокетоны формулы I, которые соответствуют следующим соединениям:
(Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-5-метилгексан-1-он,
(Е)-1 -[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-5-метилгексан-1 -он,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -3 -фторбензоил] -бензонитрил,
(Е)-4-[4-[4-(аллилметиламино)-бут-2-енилокси]-бензоил]-бензонитрил,
(Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси] -фенил] -5 -метилгекс-4-ен-1-он,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил] -(2,6-дифторфенил)-метанон,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-2-фторфенил]-(4-бромфенил)-метанон,
(Ε)-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-(4-фторфенил)- метанон,
(Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-6-метилгепт-5-ен-2-он,
(Е)-2-[4- [4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил] -1 -(4-бромофенил)-этанон,
(Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-(4-бромфенил)-этанон,
(Е)- [4-[4-(аллилметиламино)-бут-2-енилокси] -фенил] -(4-йодфенил)-метанон,
[4-[6-(аллилметиламино)-гексилокси]-фенил]-(4-бромфенил)-метанон,
[4-[4-(аллилметиламино)-бутокси]-фенил]-(4-бромфенил)-метанон,
[4-[6-(аллилметиламино)-гексилокси]-3-фторфенил]-(4-бромфенил)-метанон,
[4-[6-(аллилметиламино)-гексилокси] -2-фторфенил] -(4-бромфенил)-метанон,
(Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил] -(4-трифторметилфенил)-метанон,
(Ε)-[4- [4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-(4-бромфенил)-метанон,
(Е)-(4-бромфенил)- [4-[4-(этилметиламино)-бут-2-енилокси]-фенил]-метанон,
4'-[(аллилметиламино)метил]-2-хлор-4-бифенил-п-бромфенилкетон
и их фармацевтически приемлемые соли присоединения кислот.
Текст
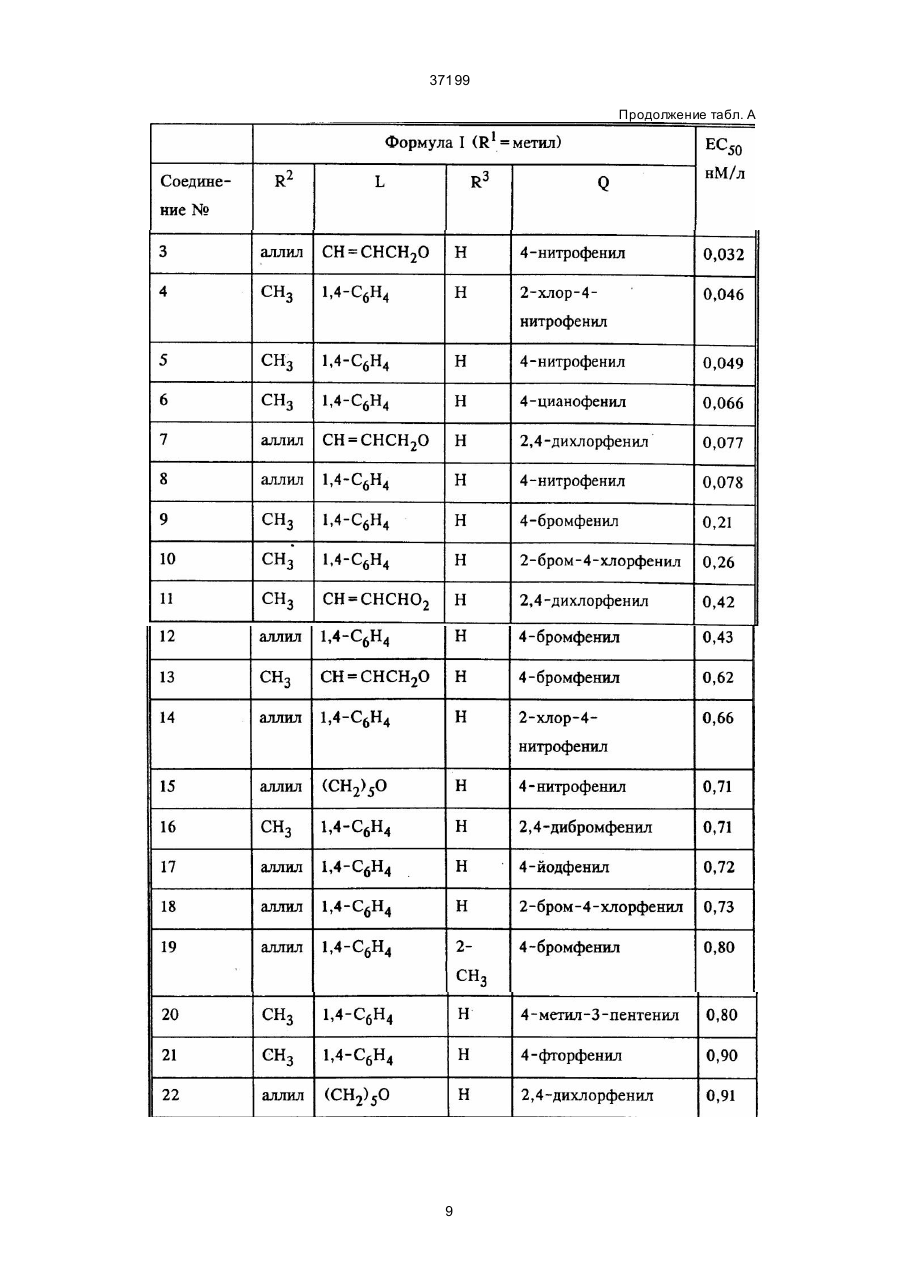
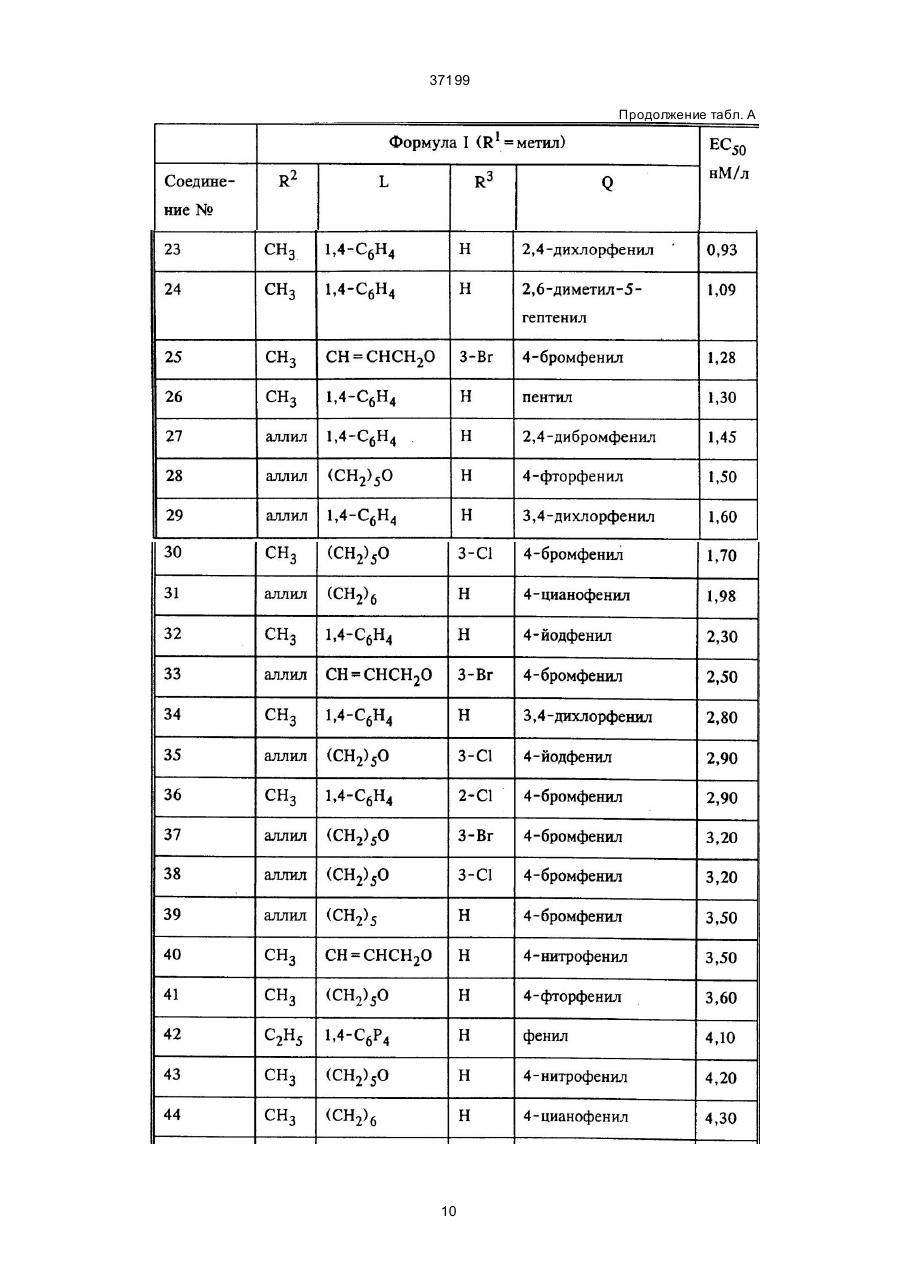
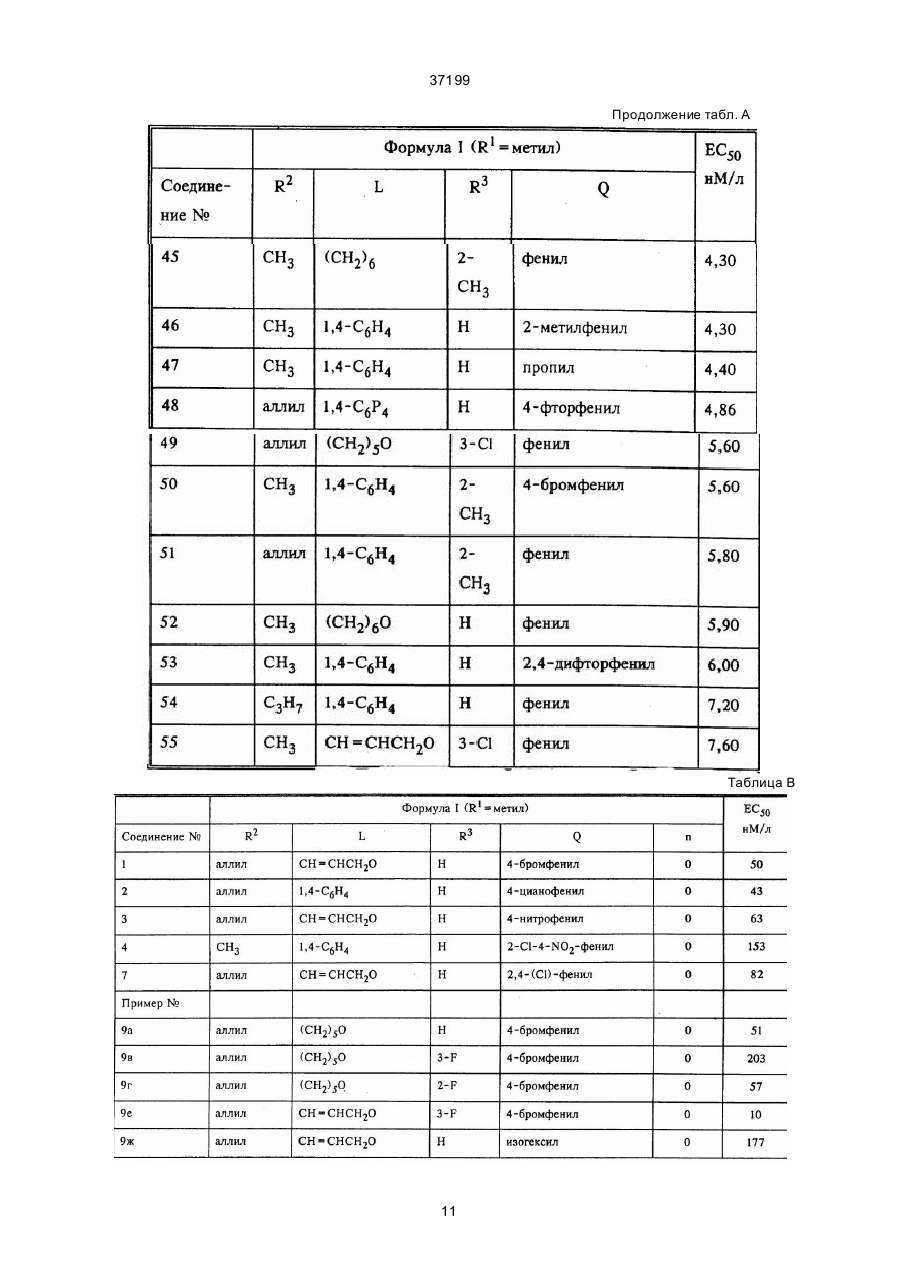
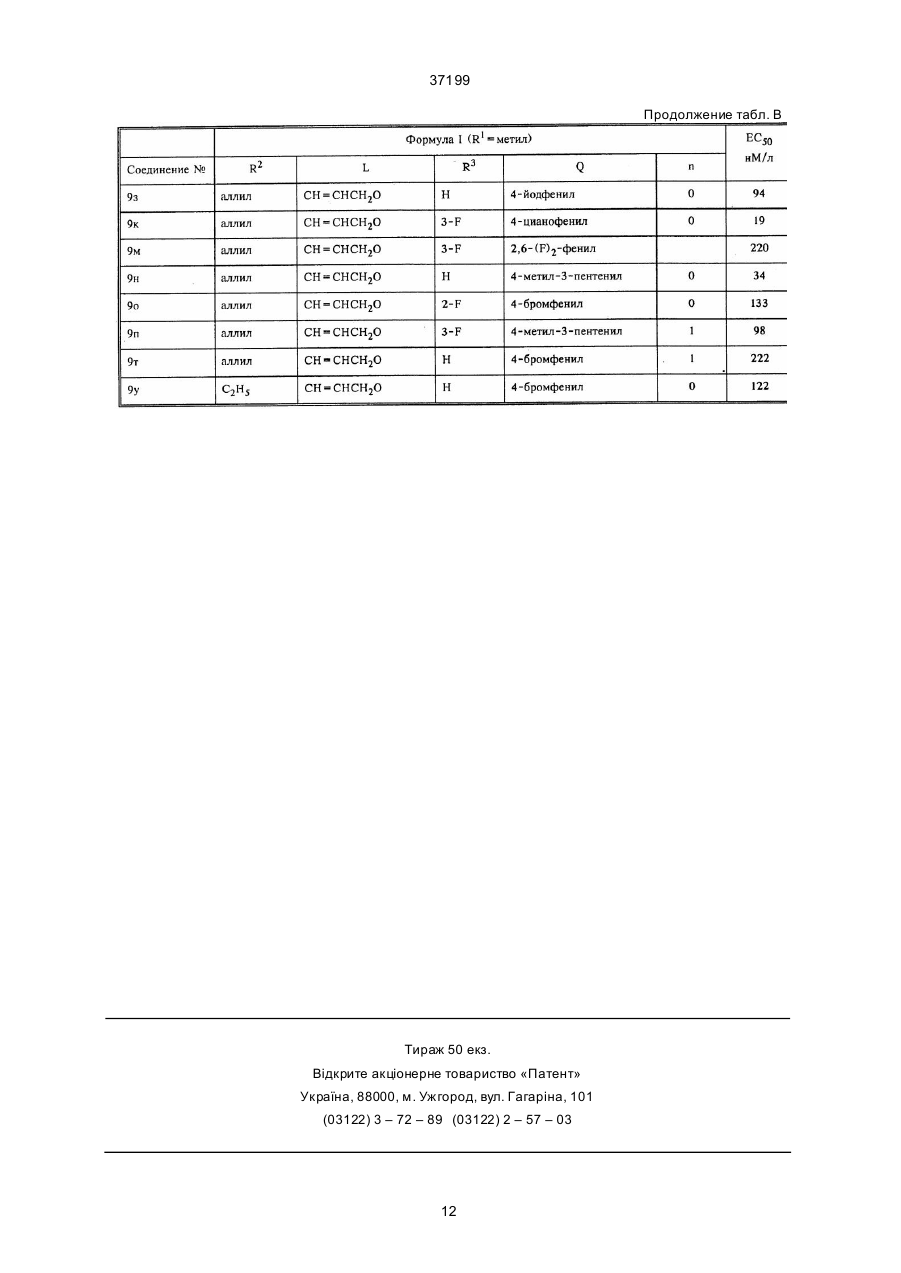
1. Алкиламинокетоны формулы I C2 (54) АЛКIЛАМIНОКЕТОНИ 37199 2,4-[[4-диметиламино)-2-бутенил]окси]-3,4'-дибромобензофе нон, 4-[[4-диметиламино)-2-бутенил]окси]-3- хлорбензофе нон, 4'-бром-3-хлор-4-[[6-(диметиламино)гексил]окси]бензофе нон, 3,4-дихлорфенил-4'-[(диметиламино)метил]-4-бифе нилкетон, 4'-[(аллилметиламино)метил]-4-бифенил-3,4-дихлорфе нилкетон, (RS)-4-(диметиламинометил)-4-бифенил-2,6-диметил-5-гепта нилкетон, п-бромфе нил-2-хлор-4'-[(диметиламино)метил]-4бифенилкетон, 4'-[(диметиламино)метил]-4-бифенилпропилкетон, и их фар мацевтически приемлемые соли присоединения кислот; 28.04.94 – по п.2 и по п.1 формулы, а именно: алкиламинокетоны формулы I, которые соответствуют сле дующим соединениям: (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]-5 -метилгексан-1-он, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-3фтор фенил]- 5-метилгексан-1-он, (Е)-[4 -[4-(а лли лметиламино )-бут-2 -ени локси ]3-фторбензоил]- бензонитрил, (Е)-4-[4-[4-(аллилметиламино)-бут-2-енилокси]-бензоил]-бензонитрил, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]- 5-метилгекс-4-ен-1-он, (Е)-[4-[4 -(аллилмети ламин о)-бут-2-е нилокси ]3-фторфенил]- (2,6-дифторфе нил)-метанон, (Е)-[4-[4 -(аллилмети ламино)-бут-2 -енилокси]-2 фтор фенил]- (4-бромофе нил)-метанон, (Е)-[4-[4-(аллилмети ламино)-бут-2-енилокси]-фенил]-(4-фторфе нил) -метанон, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-3фтор фенил]-6- метилгепт-5-ен-2-он, (Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси]-3фтор фенил]-1- (4-бромофенил)-этанон, (Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил]- (4-бромофенил)-этанон, (Е)-[4-[4-(а ллилметила мино)-бут-2-енилокси]-фенил]- (4-йодофенил)-метанон, [4-[6-аллилметиламино)-гексилокси]-фенил]- (4-бромофенил)-метанон, [4-[4-(аллилмети ламино)-бутокси]-фенил]- (4-бромофенил)-метанон, [4-[6-(а ллилметила мино)-гексилокси]-3-фтор фенил]- (4-бромофенил)-метанон, [4-[6-(а ллилметила мино)-гексилокси]-2-фтор фенил]- (4-бромофенил)-метанон, (Е)-[4-[4-(а ллилметила мино)-бут-2-енилокси]-фенил]- (4-трифторметилфе нил)-метанон, (Е)-[4-[4-(аллилмети ламино)-бут-2-енилокси]–3фтор фенил]- (4-бромофе нил)-метанон, (Е)-(4-бромофенил)-[4-[4-(этилметиламино)-бут-2енилокси]-фенил]- мета нон, 4'-[(аллилметиламино)метил]-2-хлор-4-бифенил-пбромофе нилкетон, и их фар мацевтически приемлемые соли присоединения кислот. _______________________ R5 представляет собой Н либо, если R обозначает Н, Н или га логен, и применимые в фармацевтике аддитивные соли кислот при получении лекарственных препаратов, снижающи х содержание холестерина в крови. Изобретение относится далее к следующим новым соединениям, соответствующим фор муле I: 4-[[6-(аллилметиламино)гексил]окси]-3-хлорбензофенон, 4-[ [6-(аллилметиламино)гексил]окси] -3,4'-дибромбензофенон, 4-[[4-(аллилметиламино)-2-бутенил] окси] -3,4'дибромбензофенон, 3-хлор-4'-йод-4-[[6-(аллилметиламино)гексил] окси] бензофенон, 4'-бром-3-хлор-4-[[6-(аллилметиламино) гексил] окси] бензофенон, 2,4-[[(4-диметиламино)-2-бутенил]окси]-3,4'дибромбензофенон, 4-[[4-(дим е тилам ино )-2 -буте ни л]окси ]-3хлорбензофенон, 4'-бром-3-хлор-4-[[6-(диметиламино)гексил] окси]бензофенон, 3,4-дихлорфенил-4'-[(диметиламино)метил] -4-бифенилилкетон, 4'-[(аллилметиламино)метил]-4-бифенилил3,4-дихлорфенилкетон, (RS)-4'-(диме тиламин омети л)-4-бифе ни л2,6-диметил-5-гептенилкетoн, Настоящее изобретение относится к применению соединений формулы I где один из R1 и R2 обозначает С 1-7-алкил, а другой обозначает С 1-7-алкил либо С 2-6-алкенил-метил, L обозначает при определенных условиях связанный через О-атом с фенильной группой C1-11-алкилен либо С 2-11-алкенилен, или L обозначает 1,4-фе нилен, n обозначает 0 либо, если L содержит Oатом, n обозначает 0 или 1, Q обозначает С1-7-алкил, С2-10-алкенил либо груп пу фор мулы Q': Q’ R представляет собой Н, галоген, СF3, CN либо NO2, R3 и R4 представляют собой Н, С1-4-алкил либо галоген и 2 37199 р-бромфе нил-2-хлор-4'-[(диметиламино) метил] -4-бифенилилкетон, 4'-[(диметиламино)метил]-4-бифенилил-пропилкетон, [4-[6-(аллилметиламино)-гексилокси]-фе нил] - (4-бромфе нил) -метанон, [4-[4-(аллилметиламино)-бутокси]-фенил](4-бромфе нил) -метанон, [4 -[6 -(а лли лм ети лами но )-гекси локси ]-3 фторфенил] - (4-бромфенил) -метанон, [4-[6 -(а лли лм ети лам ин о)-гексилокси ]-2фторфенил] - (4-бромфенил) -метанон, (Е)- [4-[4- (аллилметиламино)-бут-2-енилокси] -фе нил] -(4-трифторметилфе нил) -метанон, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -3-фторфе нил] -(4-бромфе нил) -метанон, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси] -фе нил] -5-метилгексан-1-он, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -фе нил]-(4-йодфе нил) -метанон, (Е)-1-[4-(аллилметиламино)-бут-2-енилокси] -3-фторфе нил] -5-метилгексан-1-он, (Е)-[4-[4-(аллилметиламино) -бут-2-енилокси] -3-фторбензоил] -бензонитрил, (Е)-4-[4-[4-(аллилметиламино)-бут-2-енилокси] -бензоил] -бензонитрил, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -3-фторфе нил] -(2,6-дифторфе нил) -метанон, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси] -фе нил] -5-метилгекс-4-ен-1-он, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] 2-фторфе нил]-(4-бромфенил) -метанон, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -фе нил] -(4-фторфе нил) -метанон, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси] -3-фторфенил] -6-метилгепт-5-ен-2-он, (Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси] -3-фторфенил] -1-(4-бромфе нил) -этанон, (Е)-2-[4-[4-(аллилметиламино)-бут-2-енилокси) -фе нил] -1- (4-бромфенил) -этанон, (Е)-(4-бромфе нил)-[4-[4-(этилметиламино) бут-2-е нилокси] -фе нил] -метанон, 4'-[(аллилметиламино)метил]-2-хлор-4-бифенилил-р-бромфенилкетон, 4'-[(аллилметиламино)метил]-4-бифенил-4метил-3-пентенилкетон. Названия "алкил"и "алкилен" обозначают неразветвленные либо разветвленные, насыщенные углеводородные радикалы с одной или двумя свободными валентностями, как метил, этил, пропил, изобутил и трет.-бутил, соответственно метилен, пентаметилен и гексаметилен. Названия "алкенил" и "алкенилен" обозначают неразветвленные либо разветвленные, содержащие двойную связь углеводородные радикалы с одной или двумя свободными валентностями, как винил и пропенил, соответственно пропенилен. В качестве применимых в фармацевтике аддитивных солей кислот рассматриваются соли соединений I неорганических и органических кислот, как НСl, НВг, H2S04, НNО3, лимонная кислота, уксусная кислота, янтарная кислота, фумаровая кислота, винная кислота, метансульфокислота и ртолуолсульфо кислота. Предпочти тельными соединениями формулы I являются те из них, в которых n равно 0, a R5 обозначает Н. К предпочтительным соединениям формулы I относятся далее такие, где а) R1 обозначает метил, а R2 обозначает метил, этил, пропил либо аллил и/или б) L представляет собой группу -СН СНСН2О-, прежде всего в транс-форме, = -(СН2)5-, -(СН2)6-, -(СН2)3 О-, -(СН2) 5О-, -(СН2)6О- либо 1,4-фенилен. и/или в) R3 обозначает Н, Вr, Cl, F ли бо СН 3 и/или г) Q обозначает пропил, пентил, изогексил, 4-метил-3-пентенил либо 2,6-диметил-5-гептенил или д) Q представляет собой группу Q', в которой R обозначает Н, Br, Cl, F, J, СF3, CN либо NO2 и/или R4 обозначает Н, Br, Cl, F либо СНз и/или R5 обозначает Н либо F. Особенно предпочтительны соединения формулы I, где а) L представляет собой C5-11-алкилен либо С5-11-алкиленокси, прежде всего -(СН2)6- либо -(СН2)5О-; С3-11-алкениленокси, прежде всего -СН СНСН2О-, либо 1,4-фенилен и/или = б) R3 обозначает Н либо галоген и/или в) Q представляет собой С 2-10-алкенил, прежде всего 4-метил-3-пентенил; либо группу Q', в которой R обозначает CN, NO2 ли бо галоген, прежде всего Br, Cl либо F, а R4 обозначает Н либо Cl, в частности те соединения формулы I, где а) R1 обозначает метил, а R2 обозначает метил либо аллил и/или б) L представляет собой -(СН2)5О-, -СН СНСН2О- либо 1,4-фенилен и/или = в) R3 обозначает Н либо F и/и ли г) Q представляет собой 4-метил-3-пентенил либо группу Q', в которой R обозначает Br, Cl, CN либо NO2, R4 обозначает Н либо Сl, а R5 обозначает Н. Примерами предпочтительных соединений являются транс-4-[ [4- (аллилметиламино)-2-бутенил]окси] -4'-бромбензофенон, транс-4-[[4-(аллилметиламино)-2-бутенил] окси] -4' -нитробензофенон, р- [[4'- [(аллилметиламино)метил]-4-бифенилил]карбонил] бензонитрил, 2-хлор-4-нитрофенил-4'-[(диметиламино) метил] -4-бифенилил-кетон, транс-4-[[4-(аллилметиламино)-2-бутенил] окси]-2',4'-дихлоробензофенон, [4-[6-(аллилметиламино)-гексилокси]-фенил] (4-бромфе нил) -метанон, [4 -[6 -(а лли лм ети лами но )-гекси локси ]-3фторфенил]-(4-бромфе нил)-метанон, [4 -[6 -(а лли лм ети лами но )-гекси локси ]-2фторфенил] - (4-бромфенил) -метанон, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -3-фторфе нил] -(4-бромфе нил) -метанон, (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фе нил] -5-метил-гекс-4-ен-1-он, (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси] -2-фторфе нил] - (4-бромфе нил) -метанон. Соединения формулы I и и х со ли могут быть получе ны так, как это описывается в патентах США № 5106878, 5137920 и 5177067. Те соединения, которые в этих патентах не указаны особо, являются предметом настоящего изобретения. 3 37199 Получение таких новых соединений описано в нижеследующи х примерах. растворов, эмульсий или суспензий. Для изготовления таких препаратов биологически активное вещество можно смешивать с инертными в фармакологическом отношении, неорганическими либо органическими носителями. В качестве носителей для таблеток, лаковых таблеток, драже и твердожелатиновых капсул можно использовать, например, лактозу, к укурузный крахмал, тальк, стеариновую кислоту или ее соли. Для мягкожелатиновых капсул в качестве носителей пригодны, например, расти тельные масла, воск или жиры; однако в зависимости от специфических свойств биологически активного вещества для мягкожелатиновых капсул вообще не требуется никаких носителей. Для приготовления растворов и спиртов в качестве носителей пригодны, например, вода, сахароза, инвертный сахар и глюкоза. Фармацевтические препараты могут, кроме того, содержать еще и консерванты, агенты растворения, стабилизаторы, смачивающие агенты, эмуль гаторы, сладкие вещества, красители, ароматические вещества, соли для изменения осмотического давления, буферы, оболочки или антиокислители. Они могут содержать также и другие, ценные в терапевтическом отношении вещества. Как уже упоминалось выше, снижающие содержание холестерина лекарственные средства, содержащие одно из соединений формулы I или применимую в фармацевтике соль такого соединения, также являются предметом настоящего изобретения, предметом изобретения является далее способ получения таких лекарственных средств, отличающийся тем, что одно или несколько из вышеназванных биологически активных веществ и при определенных условиях одно или несколько других цен ных в те рапевтическом отношении веществ используют для изготовления галеновых препаратов. Как уже упоминалось выше, эти биологически активные вещества могут применяться для борьбы или предуп реждения таких заболеваний, как гиперхо лестеринемия и атеросклероз. Их дозировка может варьироваться в широких пределах и при этом, естественно, в каждом отдельном случае должны учитываться индивидуальные особенности пациентов. В принципе при оральном введении суточная доза должна составлять от приблизительно 2 мг до приблизительно 2 г, предпочти тельно от приблизительно 10 до приблизительно 100 мг. При этом суточную дозу можно разделить на один, два либо три приема, например, во время приема, соответственно приемов пищи. В нижеследующих примерах описывается получе ние неизвестных до настоящего времени соединений формулы I. Пример 1. В раствор из 34,5 г 1,6-дибромгексана, 9,9 г 3-хлор-4-гидроксибензофенона и 1,6 г бромида тетрабути ламмония в 100 мл хлористого метилена добавляют 100 мл 10%-ного водного натрового ще лока. Гетерогенную смесь перемешивают в течение ночи при комнатной температуре. Органическую фа зу отделяют, сушат над сульфа том натрия и выпаривают. После хро матографии остатка на силикагеле с помощью гексана/этилового эфира уксусной кислоты 7:3 получают 4-[(6-бромгексил)окси]-3-хлорбензофенон, Тпл 58° С. Соединения I и их со ли обладают эффективным действием по снижению содержания холестерина в крови и поэтому могут применяться для борьбы, соответственно профилактики гиперхо лесте ринемии и атеросклероза, обусловливающи х большую часть сердечно-сосудистых заболеваний. Для доказательства эффективности соединений I и их солей по снижению содержания холестерина в крови был осуществлен модифицированный D.L.Brasaemle и Attie A.D. (Biotechniques 6, 1988, 418-419) эксперимент, проведенный M.Krieger (Anal. Biochem. 135, 1983, 383-391). В этом эксперименте используется способность ингибиторов синтеза холестерина защищать клетки СНО-К1 (клетки яичников китайского хомяка) от цитотоксических эффектов в полиеновых антибиотиках груп пы амфо терицина В. Ингибирование синте за холесте рина проявляется через защиту живых клеток, и эта защи та, в свою очередь, выражается числом сохранившихся живых клеток по сравнению с необработанными клетками. Значения ЕС 50 в нМ/л в приведенной ниже таблице А соответствуют концентрации, при которой выживают 50% клеток. В описанном выше эксперименте для 2,4дифтopфeнил-4'-[(aллилмeтилaмино)метил]-4-бифенилилкетон-гидрохлорида выявленное значение ЕС50 составляло 4,00 нМ/л. Для дальнейшего подтверждения эффективности соединений формулы I и их солей по снижению содержания холестерина работали аналогично эксперименту, описанному в Journ. Biol. Chem. 256 (1981) 11923-11931. При этом ингибирование синте за холестерина в гепатомных клетках человека (Нер G2) определяли на основе параллельно индуцированной регуляции LDL-рецептора (LDL = липопротеид низкой плотности). Клетки высевали на микротитрационные планше ты и обрабатывали ингибитором синтеза холестерина. Концентрацию LDL-рецептора определяли по ELISA-методике (ферментный иммуносорбентный тест), причем С7LDL-анти тело применяли в качестве первичного анти тела. Значения ЕС50 в нМ/л, представленные в нижеследующей таблице В, соответствуют концентрации ингибитора синте за холестерина, при которой активность рецептора по сравнению с контролем (т.е. необработанными клетками) повышается на 50%. Положения 2, соответственно 3 заместителя R3 в приведенных выше таблицах А и В соответствуют орто-, соответственно метаположению по отношению к содержащей ся в формуле Iгр уппе -(CH2)nC(O)Q. Токсичность этих сое динений незначительна, однако соединение № 20, например, имеет ЛД50 1250-2500 мг/кг при введении внутрь мышам. Соединения формулы I и их соли могут применяться в качестве биологически активных веществ в фармацевтических препарата х. Эти фармацевтические препараты вводятся оральным путем, например, в виде таблеток, лаковых таблеток, драже, твердо- и мягкожелатиновых капсул, 4 37199 Раствор из 3,0 г получен ного бензофенона в 30 мл этанола нагревают с 16 мл 33%-ного раствора N-аллилметиламина в этаноле в те чение 1,5 ч в трубке под давлением до 90° С. После охлаждения смесь сливают на во ду и трижды экстрагируют ук сусным эфиром. Высушен ные над сульфа том натрия органические фазы выпаривают и остаток хроматографируют с помощью гексана/уксусного эфира (7:3) на окиси алюминия до нейтральной реакции. В результате получают 4-[[6-(аллилметиламино)гексил]окси] -3-хлорбензофе-нон, Тпл гидрохлорида 133° С. Пример 2. Аналогично примеру 1 получают а) из 3,4'-дибром-4-гидроксибензофенона, через 4-[(6-бромгексил)окси]-3,4'-дибромбензофенон, Тпл 97°С, 4-[[6-(аллилметиламино)гексил]окси]-3,4'-дибромбензофенон, Тпл гидрохлорида 126-127°С, б) из 3,4'-дибром-4-гидроксибензофенона и транс-1,4-дибромбутена, через 4-[(4-бром-2-бутенил]окси]-3,4'-дибромбензофенон, 4-[[4-(аллилметиламино)-2-бутенил]окси] -3,4'-дибромбензофенон, Тпл гидрохлорида 115-116° С. в) из 3-хлор-4'-йод-4-гидроксибензофенона и 1,6-дибромгексана, через 3-хлор-4'-йод-4- [(6бромгексил)окси] бензофенон, 3-хлор-4'-йод-4[[6-(аллилметиламино)гексил]окси] бензофенон, который переводят в гидрохлорид, МС: m/е 511 (M+, 2,4%), 484 (2%), 482 (4%), 231 (2,5%), 154 (3,3%), 84 (100%), г) через 4' -бром-3-хлор-4-[(6-бромгексил)окси] бензофенон (пример 3в), 4'-бром-3-хлор-4- [6(аллилметиламино)гексил]окси] бензофенон, который переводят в гидрохлорид, МС: m/е 465 (М+, 2%), 463 (1,5%), 436 (4%), 434 (3%), 155 (3%), 134 (4%), 84 (100%). Пример 3. Аналогично примеру 1 получают а) через 4-[(4-бром-2-бутенил)окси]-3,4'-дибромбензофенон (пример 2б) с диметиламином вместо N-аллилметиламина, 2,4-[[(4-диметиламино)-2-бутенил]окси]-3,4'-дибромбензофенон, который переводят в гидрохлорид, Тпл 166-167°С, б) из 3-хлор-4-гидроксибензофенона и 1,4дибромбутена, через 4-[(4-бром-2-бутенил)окси]-3хлорбензофенон, Тпл 96-97°С, 4-[[4-(диметиламино)-2-бутенил]окси]-3-хлорбензофенон, который переводят в гидрохлорид, Тпл 195° С, в) из 4'-бром-3-хлор-4-гидроксибензофенона и 1,6-дибромгексана, через 4'-бром-3-хлор-4-[(6бромгексил)окси] бензофенон, 4'-бром-3-хлор-4[[6-(диметиламино)гексил]окси] бензофенон, который переводят в гидрохлорид, MC: m/e 402 (M+ Cl, 0,2%), 185 (1,3%), 183 (1,6%), 155 (2%), 128 (4%), 58 (100%). Пример 4. а) 35 мл нитробензола охлаждают в ледяной ванне, после чего последовательно обрабатывают 5,2 г хло ристого алюминия и 5,0 г 4-метилбифенила. Смесь доводят до комнатной температуры и затем обрабатывают 7,7 г 3,4-дихлорбензоилхлорида. Смесь перемешивают при комнатной температуре, сливают на воду и экстрагируют с помощью хлористого метилена. Экстракт вымывают 2Н соляной кислотой и водой, сушат над сульфотом магния и выпаривают. Остаток хроматографируют на силикагеле с помощью толуо ла/уксусного эфира 9:1. В результате получают 3,4-дихлорфенил-4'-метил-4-бифенилилкетон. б) Смесь из 5,0 г 3,4-дихлорфе нил-4'-метил4-бифенилилкетона, 2,7 г N-бромсукцинимида и 20 мг азаизобутиронитрила в 70 мл четыреххлористого углерода нагревают с обратным холодильником до кипения. Выпавший осадок отфильтровывают и фильтрат выпаривают. Остаток перекристаллизовывают из толуо ла/циклогексана. В результате получают 3,4-ди хлорфе нил-4'-бромметил-4-бифенилилкетон. в) 1,0 г 3,4-дихлорфенил-4'-бромметил-4-бифенилилкетона и 20 мл 33%-ного раствора диметиламина в этаноле нагревают в те чение 4 ч до кипения, после чего смесь выпаривают. Остаток растворяют в простом эфире и обрабатывают эфирным раствором хлористого водорода. Выпавший в осадок гидрохлорид отфильтровывают и сушат. В результате получают 3,4-дихлорфенил-4'[(диметиламино) метил] - 4-бифенилилкетон-гидрохлорид, Тпл 223° С. Пример 5 1,0 г 3,4-дихлорфенил-4'-бромметил-4-бифенилилкетона, 1,5 мл N-аллилметиламина и 0,84 г карбоната калия в 25 мл этанола нагревают в течение 4 ч с обратным холодильником до кипения. Смесь выпаривают и остаток экстрагируют с помощью простого эфира. Экстракты сушат над сульфа том магния и обрабатывают эфирным раство ром хлористого водорода. Выпавший в осадок гидрохлорид отфильтровывают и сушат. В результате получают 4'-[(аллилметиламино) метил] - 4 бифенилил -3,4-дихлорфенилкетон - гидрохлорид, Тпл 160° С. Пример 6. Раствор из реагента Гриньяра, полученного из 344 мг магния и 2,27 г 1,4-дибромбензола в 15 мл ТГФ, по каплям добавляют в суспензию из 2 г 4-бром-N,N-диметилбензиламина и 158 мгтетракистрифенилфосфин палладия в 10 мл ТГФ. При этом добавку производят при комнатной температуре и в атмосфере аргона. После окончания добавки смесь еще в течение 5 ч нагревают до кипения и затем выпаривают при пониженном давлении. После этого обрабатывают простым эфиром и насыщенным раствором хлористого аммония и водную фа зу отделяют. Эту последнюю экстрагируют с помощью простого эфира. Органические экстракты вымывают насыщенным раствором хло ристого натрия, сушат над суль фатом магния и выпаривают. Остаток очищают посредством хроматографии на силикагеле при одновременном элюировании с помощью хлористого метилена/метанола 9:1. В результате получают 4'-бром-N,Nдиметилбифенилметанамин, Тпл 60-62° С. б) Раствор из реагента Гриньяра, полученного из 0,94 г 4'-бром-N,N-диметилбифенилметанамина и 146 мг магния в 5 мл ТГФ, по каплям добавляют в раствор из 1,07 г питронеллаля в 10 мл ТГФ. При этом добавку производят при комнатной температуре и в атмосфере аргона. Затем смесь в течение 6 ч перемешивают при комнатной температуре, после чего гидролизуют 50 мл насыщенного раствора хлористого аммония. Затем экстрагируют с помощью простого эфира. Экстракты сушат над сульфатом магния и выпаривают их. После хроматографии на 5 37199 силикагеле с помощью хлористого метилена/метанола 9:1 в качестве элюента получают (RS)-4'-[(диметиламинометил)-4-бифенилил]-a-(2,6-диметил-5-гептенил)-метанол, МС m/e: M+ 365 (21%), 321 (19%), 280 (36%), 58 (100%). в) Раствор из 406 мг ДМСО в 2 мл хлористого метилена добавляют в раствор из 327 мг хлористо го оксалила в 10 мл хлористого метилена при -70° С. Реакционную смесь перемешивают в течение 2 мин, после чего добавляют раствор из 810 мг продукта из б) в 5 мл хлористого метилена. Перемешивание продолжают еще в те чение 15 мин и затем реакционную смесь обрабатывают при -70° С 1,18 г триэтиламина. После этого реакционной смеси дают нагреться до комнатной температуры и затем обрабатывают водным раствором карбоната натрия. Водную фазу экстрагируют с помощью хлористого метилена. Органические фа зы соединяют, вымывают насыщенным раствором хлористого натрия и сушат над сульфа том магния. В полученный после фильтрации и выпаривания продукт до бавляют го рячий раствор из 263 мг фумаровой кислоты в 5 мл этанола. Выпавший в осадок фумарат перекристаллизовывают из этанола. В результате получают (RS)-4'-(диметиламинометил)-4-бифенил-2,6-диметил-5-гептенилкетонфумарат, Тпл 116-123° С. Пример 7. а) Аналогично тому, как это описано в примере 6а), из 4-бромтолуо ла и 3-хлорбромбензола получают 3-хлор-4'-метилбифенил, Тпл 110-115° С/20Па. б) Смесь из 4,76 г 3-хлор-4'-метилбифенила, 2,94 г гексаметилентетрамина и 30 мл трифторуксусной кислоты в течение 5 дней нагревают с обратным холодильником до кипения. Затем реакционную смесь концентрируют и обрабатывают ледяной водой, после чего перемешивают в течение 15 мин, преобразуют с помощью карбоната натрия в основание и экстрагируют простым эфиром. После выпаривания эфирных экстрактов и хроматографии остатка на силикагеле с помощью хло ристого метилена/метанола 9:1 в качестве элюента получают 2-хлор-4-(4'-метилфе нил)бензальдегид, Ткип 210-215° С/25Па. в) Аналогично примерам 6б) и 6в) из 2-хлор4-(4'-метилфенил)бензальдегида и 1,4-дибромбензола получают р-бромфе нил-2-хлор-4'-метил-4-бифенилкетон в ви де бесцветного масла, МС m/е: 386 (М +, 46%), 306 (9%), 229 (100%). г) Аналогично примеру 4б) из р-бромфе нил2-хлор-4'-метил-4-бифенилкетона получают 4' бромметил-2-хлор-р-бромфенил-4-бифенилкетон. д) Аналогично примеру 4в) путем обработки 4'-бромметил-2-хлор-р-бромметил-4-бифенилкетона диметиламином, а затем хлористым водородом получают р-бромфе нил-2-хлор-4'-[(диметиламино) метил] -4-бифенилилкетон-гидрохлорид, Тпл 189-191° С. Пример 8. Раствор реагента Гриньяра, полученного из 228 мг магния и 1,42 г n-пропиламида в 10 мл ТГФ, добавляют по каплям в раствор из 1,16 г 4'-[(диметиламино)метил]-N-метокси-N-метил-4-бифенилкарбоксамида в 10 мл ТГФ при 0° С в атмосфе ре аргона. После окончания добавки смесь продолжают перемешивать еще в течение 5 ч при комнатной температуре и затем выпаривают при пониженном давлении. После этого обрабатывают хло ристым метиленом и насыщенным раствором хло ристого аммония и отделяют водную фа зу. Эту последнюю экстрагируют с помощью хлористого метилена. Органические экстракты вымывают насыщенным раствором хлористого натрия, сушат над сульфатом магния и выпаривают. Остаток очищают посредством хроматографии на силикагеле при одновременном элюировании с помощью хло ристого метилена/метанола 95:5. После обменной реакции с фумаровой кислотой в этаноле получают 4'- [(диметиламино) метил] -4-бифенилпропилкетонфумарат, Тпл от 155-156° С. Пример 9. Исходные материалы А) Смесь из 41 г 4-гидроксибензойной кислоты и 400 мл гексаметилдисилазана нагревают в течение 2 ч с обратным холодильником, затем охлаждают, концентрируют и растворяют в 400 мл хло ристого метилена. После добавки 3 капель ДМФ добавляют 28 мл хло ристо го оксалила. Смесь перемешивают, затем концентрируют и сушат. Полученный хлорид кислоты суспендируют с 31 г N,О-диметилгидроксиламин-гидрохлорида в 520 мл хлористого метилена и при 0°С в течение 2 ч обрабатывают 73 мл N-метиленморфолина. В течение ночи нагревают, растворяют в уксусном эфире и вымывают водой, 10%-ным водным раствором KHSO4 и насыщенным водным раствором NаНСО3. Ор ганическую фа зу сушат, отфильтровывают и вы паривают. В ре зульта те получают 76 г N-метокси-N-метилтриметилсиланилоксибензамида, МС: m/е 238 (M+-CH3). Б) Аналогично тому, как это описано выше в разделе А), получают Ба) из 4-гидроксифенилуксусной кислоты Nметок си-N-метил-2-(4-триметилсиланилоксифенил)-ацетамид, МС: m/е 267 (М+), 252 (M+-CH3). Бб) из 3-фтор-4-гидроксифенилуксусной кислоты N-метокси-N-метил-2-(3-фтор-4-триметилсиланилоксифенил)-ацетамид, МС: m/е 285 (М+). В) К реагенту Гриньяра, получен ному из 1 г магния и 5,7 г 1-бром-4-метил-3-пентена, по каплям добавляют при 0°С раствор из 6,3 г N-метокси-N-метилтриметилсиланилоксибензамида. Реакцию продолжают в те чение ночи при комнатной температуре и при перемешивании. Затем обрабатывают 10%-ным водным раствором KHSO4, после чего экстрагируют с помощью уксусного эфира. Ор ганическую фазу вы мывают 10%-ным водным раствором NaCl до нейтральной реакции, затем сушат и концентрируют. Си лильную груп пу отщепляют в 10%-ном водном ТГФ с помощью 1Н соляной кислоты. За тем растворяют в хло ристом метилене, сушат и концентрируют. После хроматографии на силикагеле при элюировании с помощью хлористо го метилена/0,5% метанола получают 2,1 г 1-(4-гидроксифенил)-5-метил-гекс-4ен-1-она. МС: m/е 204 (М+). Г) Аналогично тому, как это описано в разделе В), из N-метокси-N-метил-2-(3-фтор-4-триметилсиланилоксифенил)-ацетамида (раздел Бб)) получают 1-(3-фтор-4-гидроксифенил)-6-метил-гепт-5-ен-2-он, МС: m/е 236 (М+). Д) Раствор из 45 мл n-бутиллития (1,6М в гексане) по каплям добавляют в охлажденную до 6 37199 -78°С суспензию из 18,2 г 1,4-дибромбензола в 140 мл ТГФ. Затем при -78°С добавляют по каплям 10 г N-метокси-N-метил-2-(3-фтор-4-триметилсиланилоксифенил)-ацетамида (раздел Бб)) в 35 мл ТГФ. Реакционую смесь перемешивают в течение 2 ч при -78°С, затем оставляют реагировать в те чение 1 ч при комнатной температуре и при перемешивании. После разбавления уксусным эфиром вымывают 10%-ным водным раствором KHSO4, насыщенным раствором NaHCO3 и 10%-ным водным раствором NaCI. После экстракции с помощью уксусного эфира органические фазы сушат и концентрируют. Затем с помощью 105 мл ТГФ, 11 мл Н2O и 5 капель 1Н НСl отщепляют силильную груп пу. После концентрирования, растворения в хлористом метилене, сушки и хроматографии на силикагельной колонке с помощью хлористо го метилена/0,5% метанола в качестве элюента получают 9,2 г 1-(4-бромфенил)-2-(3-фтор-4гидроксифе-нил)-этанона. МС: m/e 308 (М+, 1 Br). E) Аналогично тому, как это описано в разделе Д), из N-метокси-N-метил-2-(4-триметилсиланилоксифенил)-ацетамида (раздел Ба)) получают 1-(4-бромфенил)-2-(4-гидроксифенил)-этанон, МС: m/e 290 (М+, 1Вr). Ж) 14 мл нитробензола охлаждают в ледяной ванне и затем последовательно смешивают с 3,8 г AlCl 3 и 3,7 г хло рида 5-метилгексановой кислоты в 5 мл нитробензола. Смесь перемешивают в течение ночи, после чего сливают на ледяную воду и экстрагируют с помощью хлористого метилена. Экстракты вымывают водой и 10%-ным водным раствором NaCI, затем сушат и концентрируют и после этого кристаллизуют с помощью пентана. В результате получают 5,3 г 1-(3-фтор-4метоксифенил)-5-метилгексан-1-она, МС: m/e 238 (М+). 3) Аналогично тому, как это описано в разделе Ж), получают: За) из 4-бром-бензоилхлорида и 2-фторанизола (4-бромфенил)-(3-фтор-4-метоксифенил)-метанон, Тпл 142-143° С, 3б) из 4-циано-бензоилхлорида и 2-фторанизола 4-(3-фтор-4-метоксибензоил)-бензонитрил, Тпл 132,5-133° С, 3в) из 4-бром-бензоилхлорида и 3-фторанизола (4-бромфенил)-(2-фтор-4-метоксифенил)-метанон, МС: m/e 308 (М+, 1 Br), 3г) из 2,6-дифторбензоилхлорида и 2-фторанизола (2,6-дифторфе нил)-(3-фтор-4-метоксифенил)-метанон, Тпл 79-83° С. И) Раствор из 3,9 г (2,6-дифторфенил)-(3фтор-4-метоксифенил)-метанона (раздел Зг) в 30 мл уксусной кислоты перемешивают с 20 мл водного 62%-ного раствора НВr при 125° С, затем выпаривают, после чего продолжают выпаривание с помощью толуо ла и растворяют в ук сусном эфире. Органическую фазу вы мывают насыщенным водным раствором NaHCO3 и 10%-ным раствором NaCI, после чего сушат. В результате получают 3,6 г (2,6-дифторфе нил)-(3-фтор-4-гидроксифенил)-метанона, МС: m/e 252 (М+). Кб) из (4-бромфе нил)-(2-фтор-4-метоксифенил)-метанона (раздел 3в) (4-бромфенил)-(2фтор-4-гидроксифенил)-метанон, МС: m/е 294 (М+, 1 Br), Кв) из анизола и хлорида 5-метилгексановой кислоты через 1-(4-метоксифенил)-5-метилгексан1-он непосредственно 1-(4-гидроксифенил)-5-метилгексан-1-он, МС: m/е 206 (М+). Л) Раствор из 50 г 4-(3-фтор-4-метоксибензоил)-бензонитрила в 550 мл хлористого метилена обрабатывают при 5° С 70 мл ВВr3 и перемешивают при комнатной температуре. При охлаждении льдом добавляют по каплям 1 л 1М NaOH. Затем экстрагируют с помощью насыщенного водного раствора NH4Cl и хлористого метилена. Органическую фа зу вымывают водой и сушат. После перекристаллизации из простого эфира получают 34 г 4-(3-фтор-4-гидроксибензоил)-бензонитрила, Тпл 168,5-169,5° С. Продукты Аналогично примеру 1 получают: а) из 4'-бром-4-гидрокси бензофенона и 1,6-дибромгексана, че рез 4'-бром-4-[(6-бромгексил)окси]бен зофенон и п утем реакции с N-аллилметила мином [4-[6-(аллилметила мино)-гексилокси]-фе нил]-(4 -бромфе нил)-метанон гидробромид, Тпл 117-119°С , б) из 4'-бром-4-гидроксибензофенона и 1,4дибромбутана, через 4'-бром-4- [(6-бромбутил)окси]бензофенон и путем реакции с N-аллилметиламино [4-[4- (аллилметиламино) -бутокси] -фе нил] (4-бромфе нил) -метанонгидробромид, Тпл 149151°С, в) из (4-бромфе нил)-(3-фтор-4-гидроксифенил)-метанона (раздел Ка) и 1,6-дибромгексана, через [4-(6-бромгексил)-3-фторфенил] -(4-бромфенил)-метанон и путем реакции с N-аллилметиламином [4-[6-(аллилметиламино)-гексилокси]-3фторфенил]-(4-бромфе нил)-метанон, который переводят в гидрохлорид, МС: m/е 447 (М +, 1 Br), г) из (4-бромфенил) -(2-фтор-4-гидроксифенил)-метанона (раздел Кб) и 1,6-дибромгексана, через [4-(6-бромгексил)-2-фторфе нил] -(4бромфе нил) -метанон и путем реакции с N-аллилметиламином [4-[6-(аллилметиламино) -гексилокси]-2-фторфе нил]-(4-бромфенил)-метанон, который переводят в гидрохлорид, Тпл 106-109° С, д) из 4'-трифторметил-4-гидроксибензофенона и (Е)-1,4-дибромбутена, через (Е) - [4-[4-бромбут-2енилокси]-фенил]-(4-трифторметилфенил)-метанон и путем реакции с N-аллилметиламином (Е)-[4-[4(аллилметиламино)-бут-2-енилокси]-фенил]-(4-трифторметилфенил)-метанон, который переводят в гидрохлорид, МС: m/е 390 (М + Н +), е) из (4-бромфе нил)-(3-фтор-4-гидроксифенил)-метанона (раздел Ка) и (Е)-1,4-дибромбутена, через (Е)- [4-(4-бромбут-2-енилокси)-3-фторфе нил] -(4-бромфенил)-метанон и путем реакции с N-аллилметиламином (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-(4-бромфе нил)метанон, который переводят в гидрохлорид, МС: m/е 418 (М+Н+, 1 Вr), ж) из 1-(4-гидроксифенил)-5-метилгексан-1она (раздел Кв) и (Е)-1,4-дибромбутена, через (Е)1-[4-[4-бромбут-2-ен илокси ]-фени л]-5 -метилгексан-1-он и путем реакции с N-аллилметиламином (Е)-1- [4- [4-(аллилметиламино)-бут-2-енилокси] К) Аналогичным путем получают: Ка) из (4-бромфенил)-(3-фтор-4-метоксифенил)-метанона (раздел 3а)) (4-бромфенил)-(3фтор-4-гидроксифенил)-метанон, Тпл 183-184° С, 7 37199 фе нил] -5-метилгексан-1-он, который переводят в гидрохлорид, Тпл 105-106° С, з) из (4-гидроксифенил)-(4-йодфенил)-метанона и (Е)-1,4-дибромбутена, через (Е)-[4-[4бромбут-2-енилокси]-фе нил]-(4-йодфенил)-метанон и путем реакции с N-аллилметиламином (Е)[4-[4-(аллилметиламино)-бут-2-енилокси]-фенил](4-йодфе нил)-метанон, который переводят в гидрохлорид, Тпл 152-153° С, и) из 1-(3-фтор-4-метоксифенил)-5-метилгексан-1-она (раздел Ж), че рез 1-(3-фтор-4-гидроксифенил)-5-метилгексан-1-он и (Е)-1-[4-бромбут-2енилокси]-3-фторфе нил]-5-метилгексан-1-он и путем реакции с N-аллилметиламином (Е)-1- [4-(аллилметиламино)-бут-2-енилокси]-3-фторфе нил]-5метилгексан-1-он, который выделяют в виде гидробромида, Тпл 106-107°С, к) из 4-(3-фтор-4-гидроксибензоил)-бензонитрила (раздел Л) с помощью (Е)-1,4-дибромбутена, через (Е)-4-[4-(4-бромбут-2-е нилокси)-3фторбензоил]-бензонитрил и путем реакции с Nаллилметиламином (Е)-[4-[4-(аллилметиламино)бут-2-е нилокси]-3-фторбензоил]-бензонитрил, МС: m/е 364 (М+), л) из 4-(4-гидроксибензоил)-бензонитрила с помощью (Е)-1,4-дибромбутена, через (Е)-4-[4-(4бромбут-2-енилокси)-бензоил]-бензонитрил и путем реакции с N-аллилметиламином (Е)-4-[4- [4(аллилметиламино)-бут-2-енилокси]-бензоил]-бензонитрил, МС: m/е 346 (М +), м) из (2,6-дифторфенил)-(3-фтор-4-гидроксифенил)-метанона (раздел И) и (Е)-1,4-дибромбутена, через (Е)-[4-[4-бромбут-2-е нилокси]-3-фторфе нил] -(2,б-дифторфенил)-метанона и путем реакции с N-аллилметиламином (Е)- [4- [4-(аллилметиламино)-бут-2-енилокси] -3-фторфе нил] -(2,6дифторфе нил)-метанон, который выделяют в ви де гидробромида, Тпл 1,2°С, н) из 1-(4-гидроксифенил)-5-метилгекс-4-ен1-она (раздел В) и (Е)-1,4-дибромбутена, через (Е)-1-[4-[4-бромбут-2-енилокси]-фе нил]-5-метилгекс-4-ен-1-он и путем реакции с N-аллилметиламином (Е)-1-[4-[4-(аллилметиламино)-бут-2-енилокси]-фе нил]-5-метилгекс-4-ен-1-он, который выделяют в ви де фумарата, МС: m/е 327 (М +), о) из (4-бромфе нил)-(2-фтор-4-гидроксифенил)-метанона (раздел Кб) и (Е)-1,4-дибромбутена, через (Е)-[4-[4-бромбут-2-енилокси]-2фторфенил]-(4-бромфе нил)-метанон и путем реакции с N-аллилметиламином (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-2-фторфенил]-4-бромфе нил)-метанон, который выделяют в виде гидрохлорида, Тпл 88-92° С, п) из 4-фтор-4'-гидроксибензофенона и (Е)1,4-дибромбутена, через (Е)-[4-[4-бромбут-2енилокси]-фе нил]-(4-фторфенил)-метанон и путем реакции с N-аллилметиламином (Е)-[4-[4-(аллилметиламино)-бут-2-енилокси]-фе нил]-(4-фторфенил)-метанон, который выделяют в виде гидрохлорида, МС: m/е 338 (М-Н+), р) из 1-(3-фтор-4-гидроксифенил)-6-метилгепт-5-ен-2-она (раздел Г) и (Е)-1,4-дибромбутена, через (Е)-1-[4-[4-бромбут-2-енилокси]-3-фторфенил] -6-метилгепт-5-ен-2-он и путем реакции с N-аллилметиламином (Е)-1-[4-[4-(аллилметиламино)-бут-2енилокси]-3-фторфе нил]-6-метилгепт-5-ен-2-он, который выделяют в виде фумарата, МС: m/е 359 (М+), с) из 1- (4-бромфенил) -2- (3-фтор-4-гидроксифенил)-этанона (раздел Д) и (Е)-1,4-дибромбутена, через (Е)-2-[4-[4-бромбут-2-енилокси]-3фторфенил]-(4-бромфе нил)-этанон и путем реакции с N-аллилметиламином (E)-2-[4-[4-(аллилметиламино)-бут-2-енилокси]-3-фторфенил]-(4-бромфе нил)-этанон, который выделяют в виде гидрохлорида, Тпл 114-116° С, т) из 1-(4-бромфенил)-2-(4-гидроксифенил)-этанона (раздел Еа) и (Е)-1,4-дибромбутена, через (Е)-2-[4-(4-бромбут-2-енилокси)-фeнил]-1-(4-бромфенил)-этанон и путем реакции с N-аллилметиламином(Е)-2 -[4 -[4-(аллилметила мино)-бут-2-енилокси)-фенил-]-1-(4-бромфенил)-этанон, который выделяют в виде гидрохлорида, Тпл 150-153oС, у) из 4'-бром-4-гидроксибензофенона и (Е)1,4-дибромбутена, через (Е)-[4-(4-бромбут-2енилокси)-фенил]-(4-бромфе нил)-метанон и путем реакции с N-этилметиламином (Е)- (4-бромфенил) –[4-[4-(этилметиламино)-бут-2-енилокси]-фе нил] метанонгидробромид, Тпл 171,5° С (распад). Пример 10. Аналогично примеру 4в) путем обработки 4'бромметил-2-хлор-р-бромфенил-4-бифенилкетона N-аллилиметиламином получают 4' [(аллилметиламино)метил]-2-хлор-4-бифенилил-р-бромфе нилкетон, МС: m/е 453 (М+, 1 Вr). Пример 11. Аналогично примеру 8 из 5-бром-2-метилпентена и 4'-[(N-аллилметиламино)метил] -N-метил-4-бифенилкарбоксамида получают 4'- [(аллилметиламино)метил]-4-бифенил-4-метил-3-пентенилкетон, МС: m/е 347 (М+). Пример галенова препарата. Твердожелатиновая капсула содержит, например, 3,125, 6,25, 12,5, 25 либо 50 мг соединения формулы I или его со ли и тонкокристаллическую лактозу до общего ве са 580-590 мг. Таблица А 8 37199 Продолжение табл. А 9 37199 Продолжение табл. А 10 37199 Продолжение табл. А Таблица В 11 37199 Продолжение табл. В Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03 12
ДивитисяДодаткова інформація
Назва патенту англійськоюAlkylaminoketones
Автори англійськоюJohannes AEBI, Philip Guerry, SYNESE Jolidon, Olivier Morand
Назва патенту російськоюАлкиламинокетоны
Автори російськоюЙоганнес Эби, Филипп Гюерри, Синез Жолидон, Оливье Моран
МПК / Мітки
МПК: A61P 9/10, C07C 217/22, A61P 3/06, A61K 31/277, A61K 31/135, C07C 217/18, C07C 255/56, C07C 225/00, A61K 31/137, A61K 31/24, C07C 217/46, A61K 31/138
Мітки: алкіламінокетони
Код посилання
<a href="https://ua.patents.su/12-37199-alkilaminoketoni.html" target="_blank" rel="follow" title="База патентів України">Алкіламінокетони</a>
Попередній патент: Спосіб одержaння плівки розплаву гранулята на поверхні
Наступний патент: Спосіб одержання практично безпилового гранулята з тетрагідро-3,5-диметил-1,3,5-тіадіазин-2-тіону, практично безпиловий гранулят та спосіб знезаражування грунту
Випадковий патент: Спосіб пластики глибокого дефекту покривних тканин стопи та гомілки