Стійкі солі похідних 3,3-дифенілпропіламінів та спосіб їх одержання (варіанти)
Формула / Реферат
1. Сполуки загальної формули І
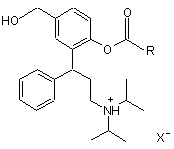 , І
, І
у якій R є С1-С6алкілом, С3-С10циклоалкілом, заміщеним або незаміщеним фенілом, а X- - відповідний кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти.
2. Сполуки за п.1, які відрізняються тим, що X- у кожному випадку є кислотним естером гідрохлоридної кислоти, гідробромідної кислоти, фосфатної кислоти, сульфатної кислоти, нітратної кислоти, оцтової кислоти, пропіонової кислоти, пальмітинової кислоти, стеаринової кислоти, малеїнової кислоти, фумарової кислоти, щавлевої кислоти, янтарної кислоти, DL-яблучної кислоти, L-(-)-яблучної кислоти, D-(+)-яблучної кислоти, DL-винної кислоти, L-(+)-винної кислоти, D-(-)-винної кислоти, лимонної кислоти, L-аспарагінової кислоти, L-(+)-аскорбінової кислоти, D-(+)-глюкуронової кислоти, 2-оксопропіонової кислоти (пірувинної кислоти), фуран-2-карбонової кислоти (муцинової кислоти), бензойної кислоти, 4-гідроксибензойної кислоти, саліцилової кислоти, ванільної кислоти, 4-гідроксицинамової кислоти, галової кислоти, гіпурової кислоти (N-бензоїлгліцин), ацетосечової кислоти (N-ацетилгліцин), флоретинової кислоти (3-(4-гідроксифеніл)-пропіонової кислоти), фталевої кислоти, метансульфонової кислоти або оротової кислоти.
3. Сполуки за пп. 1 або 2, які відрізняються тим, що мають загальну формулу 2
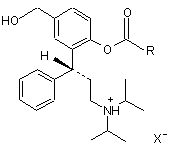 , 2
, 2
у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним або заміщеним фенілом, а X- - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти.
4. Сполуки за п. 3, які відрізняються тим, що X- у кожному випадку є кислотним естером гідрохлоридної кислоти, гідробромідної кислоти, фосфатної кислоти, сульфатної кислоти, нітратної кислоти, оцтової кислоти, пропіонової кислоти, пальмітинової кислоти, стеаринової кислоти, малеїнової кислоти, фумарової кислоти, щавлевої кислоти, янтарної кислоти, DL-яблучної кислоти, L-(-)-яблучної кислоти, D-(+)-яблучної кислоти, DL-винної кислоти, L-(+)-винної кислоти, D-(-)-винної кислоти, лимонної кислоти, L-аспарагінової кислоти, L-(+)-acкорбінової кислоти, D-(+)-глюкуронової кислоти, 2-оксопропіонової кислоти (пірувинної кислоти), фуран-2-карбонової кислоти (муцинової кислоти), бензойної кислоти, 4-гідроксибензойної кислоти, саліцилової кислоти, ванільної кислоти, 4-гідроксицинамової кислоти, галової кислоти, гіпурової кислоти (N-бензоїлгліцин), ацетосечової кислоти (N-ацетилгліцин), флоретинової кислоти (3-(4-гідроксифеніл)-пропіонової кислоти), фталевої кислоти, метансульфонової кислоти або оротової кислоти.
5. Сполуки за пп. 3 або 4, які відрізняються тим, що ними є гідрофумарат ізомасляного естеру R-(+)-2-(3-(діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу, гідрат гі-дрохлориду ізомасляного естеру R-(+)-2-(3-(діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу.
6. Сполуки за пп. 3 або 4, які відрізняються тим, що R - циклопропіл, циклобутил, циклопентил, циклогексил, 4-(1-циклопропілметаноїлокси)-феніл, 4-(1-циклобутилметаноїлокси)-феніл, 4-(1-циклогексилметаноїлокси)-феніл або 4-(2,2-диметилпропаноїлокси)-феніл, а Х- є хлоридом.
7. Сполуки за пп. 1-6, які відрізняються тим, що мають форму сипучого матеріалу.
8. Спосіб одержання сполук загальної формули І
 , І
, І
у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним або заміщеним фенілом, а Х- - відповідний кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти, який відрізняється тим, що
а) сполуку формули III
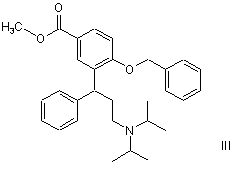
розщеплюють гідрувальним засобом з утворенням сполуки формули V
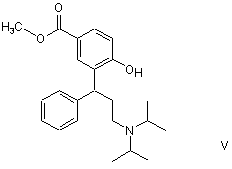 ,
,
після чого
b) отриману так сполуку формули V перетворюють відновником з утворенням сполуки формули VI
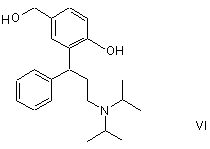 ,
,
яку
с) перетворюють ацилувальним засобом з утворенням сполуки формули А
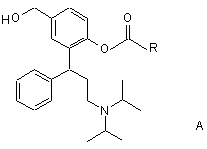 ,
,
де R визначено вище, яку
d) перетворюють фізіологічно сумісною неорганічною або органічною кислотою з утворенням сполуки формули І
 , І
, І
у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним або заміщеним фенілом, а X- - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти.
9. Спосіб за п. 8, який відрізняється тим, що для одержання сполуки загальної формули І використовують гідрохлоридну кислоту, гідробромідну кислоту, фосфатну кислоту, сульфатну кислоту, нітратну кислоту, оцтову кислоту, пропіонову кислоту, пальмітинову кислоту, стеаринову кислоту, малеїнову кислоту, фумарову кислоту, щавлеву кислоту, янтарну кислоту, DL-яблучну кислоту, L-(-)-яблучну кислоту, D-(+)-яблучну кислоту, DL-винну кислоту, L-(+)-винну кислоту, D-(-)-винну кислоту, лимонну кислоту, L-аспарагінову кислоту, L-(+)-аскорбінову кислоту, D-(+)-глукуронову кислоту, 2-оксопропіонову кислоту (пірувинну кислоту), фуран-2-карбонову кислоту (муцинову кислоту), бензойну кислоту, 4-гідроксибензойну кислоту, саліцилову кислоту, ванільну кислоту, 4-гідроксицинамову кислоту, галову кислоту, гіпурову кислоту (N-бензоїлгліцин), ацетосечову кислоту (N-ацетилгліцин), флоретинову кислоту (3-(4-гідроксифеніл)-пропіонову кислоту), фталеву кислоту, метансульфонову кислоту або оротову кислоту.
10. Спосіб одержання сполук загальної формули 2
 , 2
, 2
у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним або заміщеним фенілом, а Х- - відповідний кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти, який відрізняється тим, що
а) сполуку формули 3
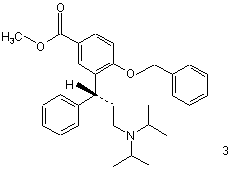
розщеплюють гідрувальним засобом з утворенням сполуки формули 5
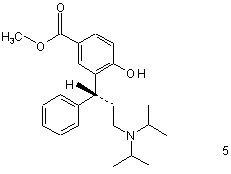 ,
,
після чого
b) отриману таким чином сполуку формули 5 перетворюють відновником з утворенням сполуки формули 6
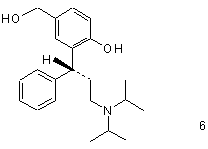 ,
,
яку
с) перетворюють ацилувальним засобом з утворенням сполуки формули 1
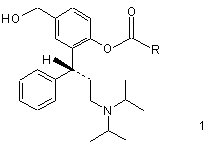 ,
,
де R визначено вище, яку
d) перетворюють фізіологічно сумісною неорганічною або органічною кислотою з утворенням сполуки формули 2
 , 2
, 2
у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним або заміщеним фенілом, а Х- - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти.
11. Спосіб за п. 10, який відрізняється тим, що для одержання сполуки загальної формули 2 використовують гідрохлоридну кислоту, гідробромідну кислоту, фосфатну кислоту, сульфатну кислоту, нітратну кислоту, оцтову кислоту, пропіонову кислоту, пальмітинову кислоту, стеаринову кислоту, малеїнову кислоту, фумарову кислоту, щавлеву кислоту, янтарну кислоту, DL-яблучну кислоту, L-(-)-яблучну кислоту, D-(+)-яблучну кислоту, DL-винну кислоту, L-(+)-винну кислоту, D-(-)-винну кислоту, лимонну кислоту, L-аспарагінову кислоту, L-(+)-аскорбінову кислоту, D-(+)-глюкуронову кислоту, 2-оксопропіонову кислоту (пірувинну кислоту), фуран-2-карбонову кислоту (муцинову кислоту), бензойну кислоту, 4-гідроксибензойну кислоту, саліцилову кислоту, ванільну кислоту, 4-гідроксицинамову кислоту, галову кислоту, гіпурову кислоту (N-бензоїл-гліцин), ацетосечову кислоту (N-ацетилгліцин), флоретинову кислоту (3 -(4-гідроксифеніл)-пропіонову кислоту), фталеву кислоту, метансульфонову кислоту або оротову кислоту.
12. Спосіб за пп. 8-11, який відрізняється тим, що як гідрувальний засіб, переважно, використовують нікель Ренея/Н2 у метанолі як розчинник.
13. Спосіб за пп. 8-11, який відрізняється тим, що як відновник використовують NaBH4/EtOH, а переважно LiАlН4/тетрагідрофуран.
14. Спосіб за пп. 8-11, який відрізняється тим, що як засіб ацилування використовують ізобутирилхлорид, а як основу - триетиламін.
15. Спосіб за пп. 10-14, який відрізняється тим, що сполуку загальної формули 6 перетворюють еквівалентом ізобутирилхлориду у присутності триетиламіну, використовуючи один з відповідних розчинників - етилацетат, дихлорметан, тетрагідрофуран, ацетонітрил або толуол, регіо- та хемоселективно, у R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілізобутират.
16. Спосіб за пп. 10-15, який відрізняється тим, що ізомасляний естер R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу та фумарову кислоту або гідрохлоридну кислоту перетворюють з утворенням відповідної солі.
17. Спосіб за пп. 10-13 для виготовлення ізомасляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу, який відрізняється тим, що фенольну естерифікацію R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенолу (6) проводять без додавання зовнішньої основи, тим, що розчини (6) додають краплями у розчини ізобутиратхлориду, що містять щонайменше 1 молярний еквівалент води, для безпосереднього отримання відповідного стабільного, гідратовмісного гідрохлориду.
Текст
Представлений винахід стосується високо чистих, кристалічних, стабільних сполук нових похідних 3,3дифенілпропіламінів у формі їх солей, способу виробництва їх та високо чистих, стабільних, проміжних продуктів. З документу РСТ/EР99/03212 відомі нові похідні 3,3-дифенілпропіламінів. Це цінні проліки для лікування невтримання сечі та інших спазматичних ускладнень, які охоплюють нестачу активних речовин, наявну при неадекватному поглинанні активної. речовини біологічними мембранами або їх небажаному метаболізмі. Крім того ці нові проліки мають поліпшені фармакокінетичні характеристики порівняно з оксибутиніном та толтеродином. Кращі сполуки з групи цих нових похідних 3,3-дифенілпропіламінів є естерами аліфатичних або ароматичних карбонових кислот загальної формули А, наведеної нижче у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним чи заміщеним фенілом. Вони можуть існувати як оптичні ізомери, як рацемічні суміші та у формі своїх індивідуальних енантіомерів. Сполуки структурної формули А, однак, мають низьку розчинність у воді. Це обмежує їх пероральну біопридатність. Під кінець, моноестери структури, яку показано у формулі А, мають тенденцію до інтрамолекулярноїтрансестерифікації. Протягом довгого періоду зберігання тому вміст сполуки зі структурою загальної формули А зменшує зростання діестерів і можна детектувати вільні діоли. Загалом солі сполук загальної формули А можна отримати, якщо розчини сполук формули А (основний компонент) очищають розчинами кислот у придатних розчинниках, але солі, отримані у формі твердого продукту, можуть бути взагалі аморфними та/або гігроскопічними і їх не можна безпосередньо кристалізувати зі звичайних розчинників Такі солі мають неадекватну хімічну стабільність при отриманні фармацевтичних препаратів як цінні фармацевтично активні речовини. Несподівано, зараз виявлено, що вищезгаданих недоліків можна позбавитися, якщо сполуки зі структурою загальної формули А, коли їх ви готовлено певним реакційним процесом, перетворюють фізіологічно сумісною неорганічною або органічною кислотою загальної формули Н-Х, в якій "Х-" представляє відповідний кислотний залишок, у їх відповідну сіль загальної формули І Проблемою представленого винаходу є тому отримання високо чистих кристалічних стабільних сполук нових похідних 3,3-дифенілпропіламінів у формі їх солей, що позбавляють від встановлених недоліків та добре придатні для використання у фармацевтично-технічних композиціях і можуть бути переробленими у них. Крім того, проблемою представленого винаходу с спосіб виробництва таких висок чистих кристалічних стабільних сполук у формі їх солей, а також високо чистих стабільних інтермедіатів. Кінцевою проблемою винаходу є спосіб виробництва вищезгаданих сполук з високим виходом продуктів за цим способом та можливістю отримати відповідні інтермедіати хемо- або регіоселективно. Цю проблему розв'язано тим, що запропоновані високо чисті кристалічні стабільні сполуки 3,3дифенілпропіламінів у формі їх солей загальної формули І у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним чи заміщеним фенілом, а "Х-" представляє відповідний кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти. Згідно з метою винаходу солі загальної формули І можуть містити відповідний кислотний залишок "Х-" нижченаведених кислот: гідрохлоридна кислота, гідробромідна кислота, фосфатна кислота, сульфатна кислота, нітратна кислота, оцтова кислота, пропіонова кислота, пальмітинова кислота, стеаринова кислота, малеїнова кислота, фумарова кислота, щавлева кислота, янтарна кислота, DL-яблучна кислота, L-(-)-яблучна кислота, и-(+)-яблучна кислота, DL-винна кислота, L-(+)-винна кислота, D-(-)-винна кислота, лимонна кислота, Lаспарагінова кислота, L-(+)-аскорбінова кислота, D-(+)-глюкуронова кислота, 2-оксопропіонова кислота (пірувинна кислота), фуран-2-карбонова кислота (муцинова кислота), бензойна кислота, 4-гідроксибензойна кислота, саліцилова кислота, ванільна кислота, 4-гідроксицинамова кислота, галова кислота, гіпурова кислота (Н-бензоїл-гліцин), ацетсечова кислота (N-ацетилгліцин), флоретинова кислота (3-(4 гідроксифеніл)-пропіонова кислота), фталева кислота, метансульфонова кислота або оротова кислота. Згідно з головною метою винаходу крім того запропоновано сполуки загальної формули 2 з Rконфігурацією у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним чи заміщеним фенілом, а "Х-" відповідний кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти. Згідно з головною метою винаходу сполуки у формі їх солей загальної формули 2 можуть містити відповідний кислотний залишок "Х-" нижченаведених кислот: гідрохлоридна кислота, гідробромідна кислота, фосфатна кислота, сульфатна кислота, нітратна кислота, оцтова кислота, пропіонова кислота, пальмітинова кислота, стеаринова кислота, малеїнова кислота, фумарова кислота, щавлева кислота, янтарна кислота, DL-яблучна кислота, L-(-)-яблучна кислота, D-(+)-яблучна кислота, DL-винна кислота, L-(+)-винна кислота, D-(-)-винна кислота, лимонна кислота, Lаспарагінова кислота, L-(+)-аскорбінова кислота, D-(+)-глюкуронова кислота, 2-оксопропіонова кислота (пірувинна кислота), фуран-2-карбонова кислота (муцинова кислота), бензойна кислота, 4-гідроксибензойна кислота, саліцилова кислота, ванільна кислота, 4-гідроксицинамова кислота, галова кислота, гіпурова кислота (Н-бензоїл-гліцин), ацетсечова кислота (N-ацетилгліцин), флоретинова кислота (3-(4гідроксифеніл)-пропіонова кислота), фталева кислота, метансульфонова кислота або оротова кислота. Кращими сполуками представленого винаходу є солі: гідрофумарат R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілізомасляного естеру та гідрат гідрохлориду R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідрокси-метилфенілізомасляного естеру. Крім того, кращими є сполуки, в яких R-циклопропіл, циклобутил, циклопентил, циклогексил, 4-(1-циклопропіл-метаноїлокси)-феніл, 4-(1-циклобутил-метаноїлокси)-феніл, 4-(1-циклогексил-метаноїлокси)-феніл або 4-(2,2-диметил-пропаноїлокси)-феніл, а X- означає хлорид. Особливу перевагу представляють хлорид [(R)-3-(2-{1-{4-(1-циклопропіл-метаноілокси)-феніл]метаноїлокси}-5-гідроксиметил-феніл)-3-фенілпропіл]-діізопропіл-амонію, хлорид [(R)-3-(2-{1-[4-(1циклобутил-метаноїлокси)-феніл]-метаноїлокси}-5-гідроксиметил-феніл)-3-феніл-пропіл]-діізопропіламонію, хлорид [(R)-3-(2-{1-{4-(1-циклогексил-метаноїлокси)-феніл]-метаноїлокси}-5-гідроксиметил-феніл)-3феніл-пропіл]-діізопропіл-амонію, хлорид [(R)-3-(2-{1-(4-(2,2-диметил-пропаноїлокси)-феніл]-метаноїлокси}5-гідроксиметил-феніл)-3-феніл-пропіл]-діізопропіл-амонію, хлорид {(R)-3-[2-(1-циклопропіл-метаноїлокси)5-гідроксиметил-фенілі-3-феніл-пропіл}-діізопропіл-амонію, хлорид {(R)-3-{2-(1-циклобутил-метаноїлокси)-5гідроксиметил-феніл]-3-феніл-пропіл}-діізопропіл-амонію, хлорид {{R)-3-[2-(1-циклопентил-метаноїлокси)-5гідроксиметил-феніл]-3-феніл-пропіл}-діізопропіл-амонію та хлорид {(R)-3-[2-(1-циклогексил-метаноїлокси)5-гідроксиметил-феніл)-3-феніл-пропiл}-діізопропіл-амонію. Для сполук представленого винаходу вираз "алкіл" переважно встановлено для гід-рогенової групи з лінійним чи розгалуженим ланцюгом, що має 1-6 С-атоми. Особливо переважними є метил, етил, пропіл, ізопропіл, бутил, ізобутил, пентил та гексил. Вираз "циклоалкіл" означає циклічні гідрогенові групи, що мають 3-10 атомів гідрогену, що можуть також містити придатні замісники замість атомів гідрогену. Вираз "феніл" означає групу С6Н5-, що може бути заміщеною або незаміщеною. Придатними замісниками можуть бути, наприклад, алкіл, алкоксил, галоген, нітрогрупа та аміногрупа. Вираз "алкоксил" з огляду на алкільний компонент має таке ж значення, як наведене вище для "алкілу". Придатними галогенами є атоми флуору, хлору, брому та йоду Представлений винахід також включає способи виготовлення сполуки згідно з винаходом загальної формули І, а також цінних інтермедіатів. Спосіб характеризується хемо- та регіоселективністю. Сполуки загальної формули III, у яких R є С1-С6алкілом, С3-С10циклоалкілом або не-заміщеним чи заміщеним фенілом, а X" - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти, виробляють так а) сполуку формули III розщеплюють гідру вальним засобом з утворенням сполуки формули V після чого b) отриману сполуку формули V перетворюють відновником у сполуку формули VІ яку с) перетворюють ацилувальним засобом у сполуку формули А, в якій R визначено вище, яку d) перетворюють фізіологічно сумісною неорганічною або органічною кислотою з утворенням сполуки формули І у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним чи заміщеним фенілом, а X" - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти. Згідно з винаходом, для виготовлення сполуки загальної формули І використовують такі кислоти: гідрохлоридна кислота, гідробромідна кислота, фосфатна кислота, сульфатна кислота, нітратна кислота, оцтова кислота, пропіонова кислота, пальмітинова кислота, стеаринова кислота, малеїнова кислота, фумарова кислота, щавлева кислота, янтарна кислота, DL-яблучна кислота, L-(-)-яблучна кислота, D-(+)яблучна кислота, DL-винна кислота, L-(+)-винна кислота, D-(-)-винна кислота, лимонна кислота, Lаспарагінова кислота, L-(+)-аскорбінова кислота, D-(+)-глюкуронова кислота, 2-оксопропіонова кислота (пірувинна кислота), фуран-2-карбонова кислота (муцинова кислота), бензойна кислота, 4-гідроксибензойна кислота, саліцилова кислота, ванільна кислота, 4-гідроксицинамова кислота, галова кислота, гіпурова кислота (Н-бензоїл-гліцин), ацетсечова кислота (N-ацетилгліцин), флоретинова кислота (3-(4гідроксифеніл)-пропіонова кислота), фталева кислота, метансульфонова кислота або оротова кислота. Згідно з переважною розробкою винаходу описано спосіб виготовлення сполуки загальної формули 2 з R-конфігурацією у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним чи заміщеним феніл, а Х- - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти, таким чином а) сполуку формули 3 розщеплюють гідрувальним засобом з утворенням сполуки формули 5 після чого b) отриману сполуку формули 5 перетворюють відновником у сполуку формули 6 яку с) перетворюють засобом ацилування з одержанням сполуки формули 1 у якій R визначено вище, яку d) перетворюють фізіологічно сумісною неорганічною або органічною кислотою з утворенням сполуки формули 2 у якій R є С1-С6алкілом, С3-С10циклоалкілом або незаміщеним чи заміщеним фенілом, а Х- - кислотний залишок фізіологічно сумісної неорганічної або органічної кислоти. Переважно для одержання сполуки загальної формули 2 згідно зі способом використовують такі кислоти: гїдрохлоридна кислота, гідробромідна кислота, фосфатна кислота, сульфатна кислота, нітратна кислота, оцтова кислота, пропіонова кислота, пальмітинова кислота, стеаринова кислота, малеїнова кислота, фумарова кислота, щавлева кислота, янтарна кислота, DL-яблучна кислота, L-(-)-яблучна кислота, D-(+)-яблучна кислота, DL-винна кислота, L-(+)-винна кислота, D-(-)-винна кислота, лимонна кислота, Lаспарагінова кислота, L-(4-)-аскорбінова кислота, D-(+)-глюкуронова кислота, 2-оксопропіонова кислота (пірувинна кислота), фуран-2-карбонова кислота (муцинова кислота), бензойна кислота, 4-гідроксибензойна кислота, саліцилова кислота, ванільна кислота, 4-гідроксицинамова кислота, галова кислота, гіпурова кислота (Н-бензоїл-гліцин), ацетсечова кислота (N-ацетилгліцин), флоретинова кислота (3-(4гідроксифеніл)-лропіонова кислота), фталева кислота, метансульфонова кислота або оротоеа кислота. Особливо переважно на основі кристалічного метилового естеру R-(-)-4-бензилокси-3-(3діізопропіламіно-1-феніл-пропіл)бензойної кислоти виготовляють високочистий кристалічний інтермедіат, метиловий естер R-(-)-3-(3-діізопропіламiно-феніл-пропіл)-4-гідрокси-бензойної кислоти, який відновлюють до R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенолу, а під кінець ацилують придатним способом та далі перетворюють фізіологічно сумісною неорганічною або органічною кислотою при самовільній кристалізації у відповідну високочисту кристалічну стабільну сіль. Залежно від використаного хлорангідриду отримують сполуки загальної формули 1 у якій R є С1-С6алкілом, зокрема ізопропілом, С3-С10циклоалкілом або незаміщеним чи заміщеним фенілом. Для одержання сполуки згідно з винаходом у формі їх солей вирішальними є особливий реакційний процес через певні проміжні етапи та придатні для індивідуального впізнання інтермедіати. Це пояснено, використовуючи реакційну діаграму 1 (дивися Фіг.1), в якій описано перетворення сполук з R-конфігурацiею, але без цього обмеження При цьому: 3=метиловий естер R-(-)-4-бензилокси-3-(3-діізопропіламіно-1-феніл-пропіл)-бензойної кислоти 4=R-(+)-[4-бензилокси-3-(3-діізопропіламіно-1-феніл-пропіл)-феніл]-метанол 5=метиловий естер R-(-)-3-(3-діізопропіламіно-феніл-пропіл)-4-гідрокси-бензойноі кислоти 6=R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-пдроксиметилфенол 1=R-(+)-2-(3-діізопропіламіно-1 -фенілпропіл)-4-гідроксиметилфеніл-ізомасляний естер 2а=гідрофумарат R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідрокси-метилфеніл-ізомасляного естеру 2b=гідрат гідрохлориду R-(+)-2-(3-діізопропіламіно-1-феніллропіл)-4-пдроксиметилфеніл-ізомасляного естеру. Згідно реакційного процесу, поясненого у втіленні на підготовчому етапі метиловий естер 3 (R-(-)-4бензилокси-3-(3-діізопропіламіно-1-феніл-пропіл)-бензойної кислоти) виготовляють у кристалічно чистій формі. Використовуючи звичайні засоби, як-то ВВr3, АІСІ3 , але переважно водень з нікелем Ренея у метанолі як розчиннику, при кімнатній температурі (кг), на підготовчому етапі З розщеплюють у метиловий естер {R-()-3-(3-діiзопропіламіно-феніл-пропіл)-4-гідрокси-бензойної кислоти, 5. Це дає високочисту кристалічну форму (температура плавлення 143,7°С). Під кінець, використовуючи придатний відновник, як-то NaBr4/EtOH, переважно LiAIH4, 5 відновлюють у інертному розчиннику при низькій температурі (-78°С- +10°С) та отримують сполуку 6, [R-{+)-2-(3діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенол). Сполуку 6 отримують у високочистому стані i її можна кристалізувати з придатного розчиннику, як-то етилацетат. Безбарвний компактний гранульований матеріал має температур плавлення 102,3°С. Це є неочікуваним тим, що сполуку 6 у рівні те хніки описано як аморфну тверду речовину. Сполуку 6 далі ацилують з дуже гарним виходом, регіо- та хемоселективністю у фенольний естер. Цю реакцію проводять при кімнатній температурі або низькій температурі еквівалентом хлорангідриду у присутності основи у придатному розчиннику. Придатними розчинниками є етилацетат, дихлорметан, тетрагідрофуран, ацетонітрил або толуол. Реакцію переважно проводять з ізобутирилхлоридом як хлорангідридом, та триети-ламіном як основою, при вищезгаданих температурах. Далі отриманий 1, ізомасляний естер (R-(+)-2-(3-діізопропіламіно-1фенілпропіл)-4-гідроксиметилфенілу), має таку чистоту, що з розчинами фумарової кислоти у придатних розчинниках починається самовільна кристалізація з утворенням гідрофумарату 2а. Ця сіль має високу температур у плавлення 103°С, є стабільною при кімнатній температурі, є негігроскопічною і не містить кристалізуючих засобів. її можна перекристалізовувати так часто, як потрібно. Якщо замість фумарової кислоти використовують безводну гідрохлоридну кислоту, наприклад, як ефірний розчин, також відбувається утворення солі кристалічного продукту 2b, отриманого гідрату гідрохлориду ізомасляного естеру (R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметил фенілу. Після подальшої перекристалізації продукт 2b має температуру плавлення 97-106°С. Під кінець, продукт 2b можна особливо гарно отримувати наступними варіантами реакції інверсії, починаючи зі сполуки 6 на діаграмі реакцій 1. Продукт 2b можна тому отримати без додавання додаткової зв'язуючої кислоту основи, як пояснено у наступному. Розчини 6, (R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенолу), додають краплями у розчини ізобутиратхлориду так, щоб в умовах придатної полярності швидко викристалізовується безводний продукт 2b. 2b є дуже гігроскопічним. Якщо вищезазначені реакції проводять у вологому розчиннику, що містить щонайменше один молярний еквівалент води, отримують стабільний кристалічний продукт 2b з вмістом гідрату, що має вищезгадані характеристики плавлення. Сполуки згідно з винаходом загальних формул 1 та 2 підхожі як сипучий матеріал. Особливу перевагу мають високочисті сполуки загальних формул III, V, VI, 3, 5, 6 та 7, які можна отримати. Сполука формули III Сполука формули V Сполука формули VI Сполука формули 3 Сполука формули 5 Сполука формули 6 Сполука формули 7 хлорид [(R)-3-(2-{1-[4-(2,2-диметил-пропаноїлокси)-феніл]-метаноїлокси}-5-{1-[4-(2,2-диметилпропаноїлокси)-феніл]-метаноїлоксиметил}-феніл)-3-феніл-пропіл]-діізолропіл-амонію. Вищезгадані сполуки 111, V, VI, 3, 5, 6 та 7 особливо добре використовувати у кожному випадку як високочисті, кристалічні стабільні інтермедіати у виробництві фармацевтично корисних сполук. Особливу перевагу мають сполуки для використання в якості інтермедіатів у виробництві гідрофумарату ізомасляного естеру R-(+)-2-(3-діізопролілзміно-1-фенілпролiл)-4-лдроксиметилфенілу, гідрату пдрохлориду ізомасляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу. Під кінець, спосіб можна здійснити особливо кращим шляхом перетворенням сполуки загальної формули 6 (дивися діаграму реакцій 1) еквівалентом ізобутирилхлориду у присутності триетиламіну, використовуючи один з відповідних розчинників: етилацетат, дихлорметан, тетрагідрофуран, ацетонітрил або толуол, регіо- та хемоселективно, у ізо-масляний естер R-{+)-2-(3- діізопропіламіно-1-фенілпропіл)-4гідроксиметилфенілу. Згідно з винаходом ізомасляний естер R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4гідроксиметилфенілу є особливо придатним для перетворення фумаровою кислотою або гідрохлоридною кислотою з утворенням відповідної солі. Наступні втілення пояснюють винахід. Експеримент I. Загальне Усі сполуки повністю охарактеризовано 1Н та 13С ЯМР-спектроскопією (Bruker DPX 200). Встановлені хімічні зсуви у 13С Я МР-спектрах (50МГц, у чнм) стосуються резонансів розчиннику СDСІ3 (77,10чнм). Дані 1 Н ЯМР (CDCI3 ; 200МГц, чнм) стосуються тетраметил-силану як внутрішнього стандарту). Тонкошарову хроматографію (DC, наведено Rf) проводили на силікагелевих плівках Е. Merck 5 x10см (60F254), та плями проявляли флуоресценцією видалених ділянок або розпиленням лужного розчину перманганату калію. Абсорбентними системами були: (1), н-гексан / ацетон / триетиламін (70/20/10,% за масою); (2), толуол/ацетон/метанол/оцтова кислота (70/5/20/5, % за масою). Оптичне обертання вимірювали на довжині хвилі 589,3нМ (D-лінія натрію), при кімнатній температурі, використовуючи етанол як розчинник (поляриметр: Perkin Elmer, тип 241), температури плавлення (у °'С) не коректували та визначали на приладі Mettler FP, або ди ференційним термоаналізом (DSC) на приладі Perkin Eimer, модель DSC7, використовуючи програму оцінки "Pyris". Виміри у видимому та ультрафіолетовому світлі проводили на спектрофотометрі моделі Lambda 7 (Perkin-Elmer) при товщині шару 1см. Специфічне поглинання визначали для 1% розчину (А1%-1см ) ІЧ спектри реєстрували на спектрометрі Perkin-Elmer FT1R Series 1610 (розділення 4см -1). Газову хроматографію/мас спектрометрію (ГХ-МС, значення m/z та відносну стосовно основного іона інтенсивність (%)) визначали на потрійному мас-спектрометрі Finnigan TSQ 700 способом виміру при позитивній (Р-СІ) або негативній (N-CI) хімічній іонізації з метаном або аміаком як реагентним газом або Іонізацією електронним ударом, Пдрокси-сполуки вимірювали як похідні триметилсилілового етеру. Сполучені рідинна хроматографія/мас спектрометрія (РХ-МС): Water Integrity System, Thermabeam Mass Detector (El, 70eB), значення m/z та відносну інтенсивність (%) дано у кількісних межах 50-500о.а.м.. II. Втілення Арабські числа у дужках (3), (4), (5), (6) стосуються ідентичних позначок у діаграмі реакцій 1. 1. Виготовлення метилового естеру R-(-)-4-бензилокси-3-(3-діізопропіламiно-1-феніл-пропіл)-бензойної кислоти (3) Розчин гідрохлориду R-(-)-4-бензилокси-3-(3-діізопропіламіно-1-феніл-лропіл)-бензойної кислоти (2,30кг, 4,77моль) у 26,4л метанолу та 0,25л концентрованої сульфатної кислоти гріють протягом 16 годин з рециклуванням. Далі третю частин у розчиннику відганяли, охолоджували та при перемішуванні змішували з 5кг льоду та 2,5л 25% водного розчину карбонату натрію. Осад спочатку екстрагували 15л, а далі ще 5л дихлор-метану. Органічні фази очищали та концентрували на роторному випарнику досуха. Отримували 1,99кг (90,7% від теоретичного) темно-жовтого масла чистотою приблизно 90% (DC, ЯМР). DC (1): 0,58 13 С-ЯМР (СDСІ3): 20,55, 20,65, 36,83, 41,84, 43,83, 51,82, 70,12, 111,09, 122,46, 125,28, 127,49, 128,02, 128,35, 128,50, 129,22, 129,49, 133,20, 136,39, 144,51, 159,87, 167,09. Перекристалізація 69,0 масляного сировинного матеріалу розчиняли у 150мл киплячого метанолу. Після додавання 15мл дистильованої води це залишали при 0°С, після чого осаджувалися безбарвні кристали, які відфільтровували, промивали невеликою кількістю холодного метанолу та сушили у вакуумі. Вихід: 41,8г(60,6 % від теоретичного) безбарвних кристалів, температура плавлення 89,8°С; [І] n20=-30,7 (с=1,0, етанол). 2. Виготовлення R-(+)-[4-бензилокси-3-(3-діізопропіламіно-1-феніл-пропілфеніл]-метанолу (4) Сирий продукт (3) (28г) розчиняють у 230мл чистого діетилового етеру та при перемішуванні додають краплями у суспензію 1,8г алюмогідриду літію у діетиловому етері (140мл). Через 18 годин перемішування при кімнатній температурі додають 4,7мл води у формі крапель. Органічну фазу відділяють, сушать безводним сульфатом натрію, фільтрують та концентрують на роторному випарнику досуха. Отримують 26г (98,9% від теоретичного) R-(+)-[4-бензилокси-3-(3-діізопропіламіно-1-феніл-пропіл)-феніл]-метанолу (4) як безбарвне масло. DC (2): 0,32; [I]n 20=+6,3 (с=1,0, етанол). 13 С-ЯМР (СDСІ3): 20,53, 20,61, 36,87,41,65,44,14, 48,82, 65,12, 70,09, 111,80, 125,77, 125,97, 126,94,127,55, 128,08,128,37,128,44,133,27,134,05,134,27, 137,21,144,84. 3. Виготовлення метилового естеру R-(-)-3-(3-діізопропіламіно-феніл-пропіл)-4-гідрокси-бензойної кислоти (5) До перемішуваної суспензії 5гнікелю Ренея (промивали водою, далі метанолом) у 200мл метанолу, додають 10г (21,8ммоль) метилового естеру R-(-)-4-бензилокси-3-{3-діізопропіламіно-1-феніл-пропіл)6ензойної кислоти (3). Після недовгого нагрівання для повного розчинення (3), апаратуру поміщають в атмосферу водню. Через три години перемішування при звичайному тиску та кімнатній температурі, тонкошарова хроматографія показала повне перетворення. Осад промивають азотом та після додавання деякої кількості активного вугілля фільтрують. Після концентрації метанольного розчину на роторному випарнику 6,0г(75% від теоретичного) метиловий естер R-(-)-3-(3-діізопропіламінофеніл-пропіл)-4-гідроксибензойної кислоти (5) залишається у формі безбарвних кристалів чистотою 99,6% (ВЕРХ). Температура плавлення 143,7°С; DSC 144,7eC [I]D20=-26,6 (С=0,93, етанол) 13 С-ЯМР (СDСІ3): 18,74, 19,21, 19,62, 33,12, 39,68, 42,36, 48,64, 51,42, 117,99, 120,32, 126,23, 127,81, 128,85,129,39, 130,26,132,21, 144,06,162,43, 167,35. 4. Виготовлення R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4гідроксиметилфенолу (6) а) початок з проміжного етапу (4), R-(+)-[4-бензилокси-3-(3-діізопропіламіно-1-феніл-пропіл)-феніл]метанол R-(+)-[4-бензилокси-3-(3-діізопропіламіно-1-феніл-пропiл)-феніл]-метанол (19,7г, 45,7ммоль) розчиняють у 220мл метанолу та нікелю Ренея (5г). Апаратур у промивають газуватим воднем та осад перемішують до двох діб при кімнатній температурі. Після додавання ще 5г нікелю Ренея, перемішування продовжують ще дві доби при кімнатній температурі в атмосфері водню, а потім відфільтрують від каталізатору та концентрують досуха на роторному випарнику. Маслянистий блідо-жовтий залишок розчиняють у 100мл діетилового етеру, промивають двічі 100мл води кожного разу, суша ть сульфатом натрію, фільтрують та концентрують досуха. 14,1г (90,4% від теоретичного) R-(+)-2-(3-діізопропіламіно-1фенілпропіл)-4-гідроксиметилфенолу отримують у формі кремової, аморфної твердої речовини. Стосовно перекристалізації дивися с). b) початок з проміжного етапу (5); метиловий естер R-(-)-3-(3-діізопроліламіно-феніл-проліл)-4-гідроксибензойної кислоти Розчин 370мг (1,0ммоль) метилового естеру R-(-)-3-(3-діiзопропіламіно-феніл-пропіл)-4-гідроксибензойної кислоти у 20мл безводного тетрагідрофурану повільно додають краплями при кімнатній температурі у перемішуван у суміш сухо го тетрагідрофурану (10мл) та 1М розчину алюмогідриду літію у тетрагідрофурані (3мл) (в захисній атмосфері азоту). Надлишок гідриду розкладають додаванням краплями насиченого розчину карбонату натрію. Після відділення органічної фази її концентрують на роторному випарнику та далі сушать у високому вакуумі. Отримують 274мг (74% від теоретичного) блідо-жовтого масла, що повільно твердне у аморфну масу. c) Перекристалізація: Сирий продукт 6 (1,0г) розчиняють у етилацетаті та знов концентрують на роторному випарнику. Діол, вивільнений при цьому від чужинних розчинників (діетиловий етер або тетрагідрофуран, дивися вище), має 1,5мл етилацетату, доданого при легкому нагрівання. Перемішування проводять до прозорості розчину, а потім охолоджують при кімнатній температурі та додають кілька затравочних кристалів. їх о тримують очисткою сирого 6 за допомогою ВЕРХ, збиранням головної фракції, концентрацією цього та сушкою залишку протягом кількох годин у високому вакуумі. При чітко визначеному початку кристалізації, суміш залишають при - 10°С. Кристали відсмоктують холодними та сушать у вакуумі. Отримують безбарвні кристали з виходом 84%. Температура плавлення 102,3°С DC (1): 0,57 [I]D20=+21,3 (с=1,0, етанол). 13 С-ЯМР (СDСІ3): 19,58, 19,96, 33,30, 39,52, 42,10, 48,00, 65,40, 118,58, 126,31, 126,57, 127,16, 127,54, 128,57,132,63, 132,83, 144,55,155,52. 5. Виготовлення ізомасляного естеру R-(+)-2-(3-діізопроліламіно-1-фенілпропiл)-4-гідроксиметилфенолу (1) Розчин R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенолу (6) (65,0г, 190,3ммоль) та триетиламіну (20,4г, 201,7ммоль) у 750мл дихлорметану має розчин ізобутиратхлориду (23,4г, 201,7ммоль) у 250мл дихлорметану, доданого при перемішуванні та охолодженні. Після додавання перемішують ще 15 хвилин при 0°С, далі протягом 30 хвилин при кімнатній температурі та далі почергово промивають водою (250мл) та 5% водним розчином гідрокарбонату натрію. Органічну фазу відділяють та концентрують на роторному випарнику досуха. Ізомасляний естер R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4гідроксиметилфенілу отримують як безбарвне в'язке масло; вихід: 77,1г(98,4 % від теоретичного). DC (І): 0,26; [I]D22=+2.7 (с=1,0, етанол). 13 С-ЯМР (CDCI3):19,01, 19,95, 20,59, 21,12, 34,28, 36,89, 41,88, 42,32, 43,90, 48,78, 64,68, 122,57, 125,59, 126,16, 126,86, 127,96, 128,54, 136,88, 138,82, 143,92, 147,90, 175,96. 6. Виготовлення гідрофумарату ізомасляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу. Розчин 41,87г(102ммоль) ізомасляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4гідроксиметилфенілу у 90мл 2-бутаноні має фумарову кислоту (11,81г, 102ммоль), додану при нагріванні. Після розчинення кислоти, циклогексан (20-30мл) повільно додають при перемішуванні до початку помутніння. Безбарвний гомогенний осад спочатку залишають протягом 18 годин при кімнатній температурі, та далі протягом кількох годин при 0°С. безбарвні кристали, що осадилися відсмоктують, промивають невеликою кількістю циклогексану/2-бутанону (90:10, об'ємн.%)та сушать у вакуумі при 30°С. 44,6г (83,1% від теоретичного) Отримують гідрофумарат ізомасляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)4-гідроксиметилфенілу у формі безбарвних пластівців. Температура плавлення 98,8°С, друга кристалізація з того ж розчиннику забезпечує продукт з температурою плавлення 103°С. [I]n 20=+6,0 (с=1,0, етанол). Елементарний аналіз: Розраховано для C30H41NO7 (молекулярна маса 527,66) С 68,29%, Н 7,83%, N 2,65%, 0 21,2%, виявлено С 68,29%, Н 7,90%, N 2,72%, 0 21,0%. Виміри у видимому та ультрафіолетовому світлі при å у нм (А1%1см ): 191 (1306), 193 (1305), 200 (1143), 220 (456). ІЧ-спектр: 3380, 2978, 2939, 2878, 2692, 2514, 1756, 1702, 1680, 1618, 1496, 1468, 1226, 1040, 1019,806, 1 Н-ЯМР (СDСІ3): 1,198, 1,285, 1,287 (СН3); 2,541 (СНС=О ); 3,589 (NCH); 4,585 (CH2OH); 6,832 (=СН, фумарат); 6,84-7,62 (арил, =СН). 13 С-ЯМР (CDCI3): 17,79, 18,95, 19,16 (СН3); 31,63 (СНСН2); 34,09 (СН-С=О ); 41,87 (СНСН2); 45,83 (NCH2); 54,29 (NCH); 63,78 (ОСН2); 122,23, 126,48, 126,77, 127,56, 140,46, 140,52, 142,35, 147,54 (Арил СН); 135,54 (=СН, фумарат); 170,48 (С=О, фумарат); 175,62 (i-Pr-C=O). MC у прямому впуску, m/z (%): 411 (1), 396 (9), 380 (1), 223 (2), 165 (2), 114 (100), 98 (4), 91 (3), 84(3), 72 (10), 56 (7). 7. Виготовлення гідрату гідрохлориду ізомасляного естеру R-(+)-2-(3-діізопропіла міно-1-феніл пропіл)-4-гідроксиметил фенілу Розчин масляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу (8,54г, 25,0ммоль) у 50мл дихлорметану повільно додають краплями при 0°С у перемішуваний розчин ізобутиратхлориду (2,66г, 25,0ммоль) у 100мл дихлорметану. Через годину охолодження видаляють, та знов перемішують протягом додаткової години. Після видалення летючих компоненти у вакуумі на роторному випарнику залишається безбарвна аморфно-тверда піна. Цей залишок розчиняють у ацетоні (17мл), додають 0,45-0,50г води та діетиловий етер (приблизно 20-25мл) до початку помутніння. Після недовгої обробки ультразвуком кристалізація починається самовільно і при перемішуванні повільно додають ще 80мл діетилового етеру. Осаджені безбарвні кристали відсмоктують та сушать протягом ночі у вакуумі пентоксидом фосфору. Отримують 10,5г (93,7% від теоретичного) безбарвного кристалічного гідрату гідрохлориду ізомасляного естеру R-(+)-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілу з чистотою 97,0% (ВЕРХ). Температура плавлення 97,1°С. [І]о=+4,3 (с=1,03, етанол) 13 С-ЯМР (CDCI3): 16,94, 17,35, 18,24, 18,40, 18,87, 19,05, 31,20, 33,99, 41,64, 45,41, 54,18, 54,42, 63,83, 122,25, 126,50, 126,70, 126,96, 127,34, 128,60, 133,80, 140,55, 142,17, 147,68, 175,79. 8. Фенольний моноестер Загальну обробку описано для виготовлення фенольних моноестерів У розчин 120,3 мг (0,352ммоль) R-(+)-2-(3-діiзо-проліламіно-1-фенілпропіл)-4-пдроксифенолу (6) у 5мл дихлорметану при перемішуванні при 0°С додають краплями розчин кислоти хлорид (0,352ммоль) у 2мл дихлорметану. Далі додають триетиламін-дихлорметан (49,1мкл/0,353ммоль-2мл). Через 18 годин при кімнатній температурі тонкошарова хроматографія виявляє, що перетворення є повним. Осад промивають послідовно 5мл вод, водною 0,1Н гідрохлоридною кислотою, 5мл 5% водного розчину гідрокарбонату натрію, 5мл води, сушили сульфатом натрію та після фільтрування концентрують досуха. Далі його сушать у високому вакуумі до постійної маси. Наступні сполуки, як приклад, виробляють, використовуючи цей спосіб: R=СН2СН(СН3)2 R-(+)-3-метилмасляної кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4-гідрокси метилфеніловий естер Безбарвне масло, 70% вихід та >95% чистоти (ЯМР). 13 С-ЯМР (СDСІ3): 20,45, 20,59, 22,54, 25,70, 36,74, 42,18, 43,27, 43,96, 48,90, 64,67, 122,66, 125,60, 126,20, 126,79, 127,95, 128,37, 136,83, 138,86, 143,83, 147,82, 171,37. DC (1):0,76. R=СН2С(СН 3)з R-(+)-3,3-диметилмасляної кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4-гідроксиметилфеніловий естер, вільна основа Безбарвне масло, 69,7% вихід та >95% чистоти (ЯМР). 13 С-ЯМР (СDСІ3): 20,40, 20,53, 29,73, 30,99, 36,62, 42,17, 44,01, 47,60, 49,01, 64,65, 122,64,125,60,126,20, 126,80, 127,96, 128,36,136,85,138,90, 143,80, 147,82,170,55. DC (1): 0,75. R=(СН3)3С Гідрохлорид R-(+)-3-півалової кислоти-2-(3-діізопропiламіно-1-феніл-пропіл)-4-гідроксиметилфенілового естеру Безбарвні кристали, температура плавлення 165-6°С. 13 С-ЯМР (D MSO-d6=39,7чнм): 16,52, 16,68, 17,98, 18,11, 26,87, 31,46, 41,71, 45,33, 53,89, 53,98, 62,65, 122,61, 122,97, 125,94, 126,09, 126,57, 126,75, 127,87, 128,58, 131,80, 134,94, 141,02, 142,69, 147,17, 155,32, 163,92, 176,21. R=С-С3Н5 Гідрохлорид R-(+)-циклопропанкарбонової карбонової кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилфенілового естеру. Безбарвна воскоподібна речовина. 13 С-ЯМР (DMSO-d6=39,7чнм): 173,02, 172,49, 172,37, 153,10, 147,12, 142,72, 142,03, 140,78, 136,60, 134,79, 134,35, 129,55, 129,13, 128,80, 128,67, 127,87, 126,96, 126,74, 125,94, 125,84, 124,37, 123,71, 122,80, 62,64, 53,92, 45,34 41,65, 31,44, 18,05, 16,66, 12,84, 9,58, 9,28, 8,49, 7,89. Гідрохлорид R-(+)-циклобутанкаобонової кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилФенілового естеру Безбарвна воскоподібна речовина. 13 С-ЯМР (DMSO-d6=39,7чнм): 173,53, 147,12, 142,81, 140,74, 134,77, 128,65, 127,81, 126,74, 125,99, 125,87, 122,75, 62,63, 53,92, 45,34, 41,42, 37,38, 31,54, 25,04, 24,92, 18,03, 16,68, 16,61. R=С-С5Н9 Гідрохлорид R-(+)-циклопентанкарбонової кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилфенілового естеру Безбарвна воскоподібна речовина. 13 С-ЯМР (D MSO-d6=39,7чнм): 174,80, 147,22, 142,86, 140,76, 134,72, 128,66,127,80, 126.73, 126,04, 125,88, 122,71, 62,62, 53,94, 45,37, 43,24, 41,39, 31,54, 29,78, 29,59, 25,64, 25,59, 18,07, 16,64. R=С-С6Н11 Гідрохлорид R-(+)-циклогексанкарбонової кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилфенілового естеру Безбарвна воскоподібна речовина. 13 С-ЯМР (DMSO-d6=39,7чнм): 174,08, 147,15, 142,85, 140,77, 134,78, 128,66, 127,77, 126.74, 126,06, 125,87, 122,69, 62,61, 53,91, 45,36, 42,26 41,24, 31,53, 28,74, 28,62, 25,48, 25,04, 24,98, 18,05, 16,67, 16,60. R=4-(C 2H5CO2)-C6H4 Гідрохлорид R-{+)-4-етилкарбонілокси-бензойної кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилфенілового естеру Безбарвні кристали, температура плавлення 195-8°С. 1 Н-ЯМР (DMSO-d6): 9,87 (s, 1Н може бути заміщеним D2O, NH), 8,19-8,12 (m, 2H, Феніл-Н), 7,55 (d, J=1,0Гц, 1Н, Феніл-Н3), 7,41-7,13 (m, 9H, Феніл-Н), 5,28 (br s, 1H може бути заміщеним D 2O, ОН), 4,53 (s, 2Н, СН2), 4,23 (t, J=7,6Гц, 1Н, СН), 3,61-3,50 (m, 2H, 2хСН(СН 3)2), 2,97-2,74 (m, 2Н, СН2), 2,67 (q, J=7,4Гц, 2Н, СН2), 2,56-2,43 (m, 2Н, СН2), 1,23-1,13(m, 15Н, 2хСН(СН3)2, СН3). R=4-(і-С3Н7СО2)-С6Н4 Гідрохлорид R-(+)-4-(ізопропілкарбонiлокси)-бензойної кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилфенілового естеру Безбарвні кристали, температура плавлення 202-4°С. 1 Н-ЯМР (DMSO-d6): 9,73 (s, 1Н може бути заміщеним D2O, NH), 8,19-8,12 (m, 2H, Феніл-Н), 7,55 (d, J=1,4Гц, 1Н, Феніл-Н3), 7,42-7,14 (m, 9Н, Феніл-Н), 5,27 (br s, 1H може бути заміщеним D 2O, ОН), 4,53 (s, 2Н, СН2), 4,23 (t, J=7,5Гц, 1Н, СН), 3,61-3,50 (m, 2H, 2хСН(СН 3)2), 2,99-2,78 (m, 3Н, СН2, СН(СН3)2), 2,54-2,47 (m, 2Н, СН2), 1,29-1,13 (m, 18Н, 3хСН (СН3)2). R=4-(t-C 4H9CO2)-C6H4 R-(+)-4-(трет-бутилкарбонілокси)-бензойної кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4гідроксиметилфеніловий естер, вільна основа. Безбарвне масло. 1 Н-ЯМР (DMSO-d6): 8,19-8,12 (m, 2H, феніл-Н), 7,45-7,33 (m, 3H, феніл-Н), 7,25-7,09 (m, 7Н, феніл-Н), 5,20 (t, J=5,6Гц, 1Н, ОН), 4,50 (d, J=5,6Гц, 2Н, СН2), 4,20 (t, J=7,5Гц, 1Н, СН), 2,95-2,80 (m, 2Н, 2хСН(СН3)2), 2,38-2,25 (m, 2Н, СН2), 2,09-2,03 (m, 2Н, СН2), 1,33 (s, 9Н, (СН3)3), 0,82-0,76 (m, 12Н, 2хСН(СН 3)2). Гідрохлорид: безбарвні крисmали, mемпераmура плавлення 165-6°С. 1Н-ЯМР (CDCl3): 8,22-8,16 (m, 2Н, феніл-Н), 8,02 (d, J=1,8Гц, 1Н, феніл-Н), 7,27-7,02 (m, 9H, феніл-Н), 4,83-4,60 (m, 2Н, СН2), 4,01-3,94 (m, 1Н, СН), 3,66-3,54 (m, 2Н) 3,18-2,80 (m, 3Н), 2,53-2,44 (m, 1Н) (2 х СН 2, 2хСН(СН3)2) 1,43-1,25 (m, 21Н, (СН3)3. 2хСН(СН3)2). R=4-(с-С3Н6СО2)-С6Н4 Гідрохлорид R-(+)-4-(циклопропілкарбонілокси)-бензойної кислоти-2-(3-діізопропіламіно-1-фенілпропіл)-4-гiдроксиметилФенілового естеру Безбарвні кристали, температура плавлення 208-213°С. 1 Н-ЯМР (DMSO-d6): 9,04 (s, 1Н може буmи заміщеним D2O, NH), 8,15-8,09 (m, 2H, феніл-Н), 7,53 (d, 1H, феніл-НЗ), 7,42-7,13 (m, 9H, феніл-Н), 5,25 (brs, 1H може буmи заміщеним D2O, ОН), 4,52 (s, 2Н, СН2), 4,23 (t, J=7,5Гц, 1Н, СН), 3,62-3,53 (m, 2Н, 2xСН(СН3)2), 3,05-2,70 (m, 2Н, СН2), 2,51-2,37 (m, 2Н, СН2), 2,01-1,89 (m, 1Н, циклопропіл-СН), 1,20-1,05 (m, 16Н, 2xСН(СН3)2, 2xциклопропіл–СН2). 13 С-ЯМР (DMSO-d6=39,7чнм): 172,71, 163,93, 154,92, 147,16, 142,69, 141,03, 134,97, 131,76, 128,60, 127,86, 126,76, 126,56, 126,06, 125,94, 122,95, 122,65, 62,65, 54,00, 53,89, 45,33, 41,63, 31,49, 18,10, 17,98, 16,69, 16,51, 12,86, 9,52. R=4-(с-С4Н7СО2)-С6Н4 Гідрохлорид R-(+)-4-(циклобутилкарбонілокси)-бензойної кислоти-2-(3-діізопропіламіно-1-фенiл-пропіл)4-гідроксиметилфенілового естеру Безбарвні кристали, температура плавлення 201-6°С. 1 Н-ЯМР (DMSO-d 6): 9,50 (s, 1Н може бути заміщеним D2O, NH), 8,17-8,12 (m, 2H, феніл-Н), 7,54 (d, J=1,4Гц, 1Н, феніл-Н3), 7,42-7,14 (m, 9Н, феніл-Н), 5,25 (br s, 1H може бути заміщеним D2O, ОН), 4,52 (s, 2H, CH2), 4,23 (t, J=7,5Гц, 1H, СН), 3,62-3,47 (m, 3Н, циклобутил-СН), 2хСН(СН3)2), 3,00-2,70 (m, 2Н, СН2), 2,51-2,26 (m, 6Н, СН2, 2хциклобутил-СН 2), 2,10-1,85 (m, 2Н, циклобутил-СН2), 1,22-1,12 (m, 12Н, 2хСН(СН3)2). R=4-(с-С6Н11СО2)-С6Н4 Гідрохлорид R-(+)-4-(ииклогексилкарбонілокси)-бензойної кислоти-2-(3-діізопропіламіно-1-фенілпропіл)-4-гідроксиметилфенілового естеру Безбарвні кристали, температура плавлення 212-217°С. 1 Н-ЯМР (D MSO-d6): 9,34 (s, 1H, може буmи заміщеним D 2O, NH), 8,16-8,12 (m, 2H, феніл-Н), 7,54 (d, J=1,4Гц, 1Н, феніл-Н3), 7,39-7,14 (m, 9H, Феніл-Н), 5,26 (t, 1H, може бути заміщеним D 2O, ОН), 4,53 (d, J=4,2Гц, 2Н, СН2), 4,22 (t, J=7,5Гц, 1Н, СН), 3,62-3,48 (m, 2Н, 2xСН(СН3)2), 3,00-2,60 (m, 3Н, циклогексилСН), СН2), 2,51-2,40 (m, 2Н, СН2), 2,07-1,98 (m, 2Н, циклогексил-СН 2), 1,80-1,11 (m, 20Н, 4xциклогексилСН2), 2xСН(СН3)2) 9. Ідентичні діестери Загальну обробку описано для виготовлення ідентичних діестерів у розчин 7,30г (21,4ммоль) R-(+)-2-(3-діізо-пропіламіно-1-фенілпропіл)-4-гідроксифенолу (6) у 100мл дихлорметану при перемішуванні при 0°С додають краплями розчин хлорангідриду (49,2ммоль) у 50мл дихлорметану. Далі додають триетиламін-дихлорметан (6,86мл/ 49,2ммоль-50мл). Через 1-3 години при кімнатній температурі тонкошарова хроматографія виявляє, що перетворення є повним. Осад промивають послідовно відповідно 100мл води, водною 0,1Н гідрохлоридною кислотою, 5мл 5% водного розчину гідрокарбонату натрію, 5мл води, сушать сульфа том натрію та після фільтрування концентрують досуха. Далі це суша ть у високому вакуумі до постійної маси. Наступні сполуки, як приклад, виробляють, використовуючи цей спосіб: R=Метил R-(-)-оцтової кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4-ацетоксиметил-феніловий естер, вільна основа Блідо-жовте масло, чистота (ВЕРХ): 95,2%. 13 С-ЯМР (CDCI3): 20,36, 20,69, 20,94, 20,99, 36,41, 42,27, 43,69, 48,79, 65,89, 122,89, 126,28, 127,17, 127,92, 128,36, 133,69, 136,95, 143,61, 148,46,168,97, 170,76. LC-MC: 425 (15%, М+), 410 (97%), 382 (4%), 308 (3%), 266 (7%), 223 (27%), 195 (13%), 165(8%), 114(100%). [a]D20=-33,1 (с=І, CH 3CN). DC (1): 0,79. R=Циклогексил R-(+)-циклогексанкарбонової кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4циклогексилкарбонілоксиметил-феніловий естер Блідо-жовте масло, чистота (ЯМР): >95%. 13 С-ЯМР (CDCI3): 20,30, 25,17, 25,58, 25,73, 28,97, 29,12, 41,70, 43,15, 44,03, 48,64, 65,37, 122,67, 125,88, 126,24, 127,06, 127,31, 127,90, 128,37, 134,03, 136,85, 143,55, 148,33, 174,20,175,72. DC (1): 0,96. R=Ізопропіл R-(+)-ізобутират-2-(3-діізопропіламiно-1-феніл-пропіл)-4-ізобутирилоксиметил-феніловий естер Вільна основа: блідо-жовте масло, чистота (ВЕРХ): 95,6%. 13 С-ЯМР (CDCI3): 18,96, 19,08, 20,59, 33,98, 34,20, 36,86, 41,72, 43,72, 48,72, 65,58, 122,65, 126,19, 126,73, 127,91, 128,11, 128,36, 133,91, 136,96, 143,81, 148,41, 175,15, 176,77. DC (1): 0,74. Гідрофумарат: безбарвний сироп, чистота 94,4% за ВЕРХ. 13 С-ЯМР (CDCI3): 17,89, 18,07, 18,94, 18,97, 19,07, 31,22, 33,93, 34,13, 41,78, 45,62, 53,93, 65,33, 122,93, 126,82, 127,45, 127,53, 127,91, 128,75, 134,74, 135,29, 135,42, 142,04, 148,44, 170,24, 175,71, 176,79. R=4-(t-C 4H9CO2)-C6H4 Гідрохлорид R-4-(трет-бутилкарбонілокси)-бензойної кислоти-2-(3-діізопропіламіно-1-феніл-пропіл)-4(4-трет-бутилкарбонілоксиметил-бензойної кислоти)фенілового естеру Безбарвні кристали, температура плавлення 105-7°С. 13 С-ЯМР (D MSO-d6): 16,49, 16,71, 17,97, 18,06, 26,84, 31,36, 38,45, 41,70, 45,24, 53,79, 53,96, 55,09, 66,11, 122,47, 122,62, 123,59, 126,42, 126,83, 127,21, 127,70, 127,88, 128,02, 128,62, 131,17, 131,86, 134,48, 135,64, 142,52, 148,35, 154,86, 155,39, 163,80, 165,09, 176,14, 176,19. 10. Змішані діестери R’ відрізняється від R” Загальну обробку описано для виготовлення змішаних діестерів У розчин 5,30ммоль фенольного моноестеру загальної формули А у 40мл дихлор-метану при перемішуванні при 0°С додають краплями розчин хлорангідриду (5,83ммоль) у 15мл дихлорметану. Далі додають триетиламін-дихлорметан (0,589g/5,82ммоль-15мл). Через 18 годин при кімнатній температурі тонкошарова хроматографія виявляє, що перетворення є повним. Осад промивають послідовно відповідно 50мл води, водною 0,1Н-гідрохлоридною кислотою, 5мл 5% водного розчину гідрокарбонату натрію, 5мл води, сушать сульфатом натрію та після фільтрування концентрують до суха. Далі це сушать у високому вакуумі до постійної маси. Наступні приклад виробляють, використовуючи цей спосіб R'=СН(СН3)2 R"=СН3 R-(+)-ізобутират-2-(3-діізопропіламіно-1-феніл-пропіл)-4-ацетоксиметил-феніловий естер Безбарвне масло. DC (1): 0,56 13 С-ЯМР (СDСІ3): 19,12, 20,65, 21,05, 34,24, 37,02, 41,79, 43,79, 48,72, 65,98, 122,75, 125,98, 126,22,127,94, 128,39,128,84,133,55, 137,04, 143,84,148,58, 170,84,175,18. Гідрохпорид: безбарвні кристали 13 С-ЯМР (CDCI3): 16,89, 17,04, 18,31, 18,92, 20,95, 31,49, 34,07, 41,64, 46,17, 54,55, 65,49, 122,91, 126,61, 126,93, 127,48, 127,83, 128,74, 134,50, 134,88, 141,61, 148,44, 170,67,175,63. [a]D20=+14,6(c=1, CHCI3).
ДивитисяДодаткова інформація
Назва патенту англійською3,3-diphenylpropylamines derivatives stable salts and a method for the preparation thereof (variants)
Назва патенту російськоюСтойкие соли производных 3,3-дифенилпропиламинов и способ их получения (варианты)
Автори російськоюMeese, Claus
МПК / Мітки
МПК: C07C 215/00, A61P 13/00, A61P 13/06, C07B 61/00, C07C 219/00, A61K 31/24, C07C 213/00, C07C 229/38
Мітки: 3,3-дифенілпропіламінів, стійкі, солі, одержання, варіанти, спосіб, похідних
Код посилання
<a href="https://ua.patents.su/12-73324-stijjki-soli-pokhidnikh-33-difenilpropilaminiv-ta-sposib-kh-oderzhannya-varianti.html" target="_blank" rel="follow" title="База патентів України">Стійкі солі похідних 3,3-дифенілпропіламінів та спосіб їх одержання (варіанти)</a>
Попередній патент: Закупорювальний вузол для пляшки із вмістом високоякісного напою
Наступний патент: Спосіб визначення липкості фотополімеризаційноздатних матеріалів і пристрій для його реалізації
Випадковий патент: Спосіб оцінювання стану техногенно трансформованого середовища з використанням морфологічних маркерів синантропних видів рослин












