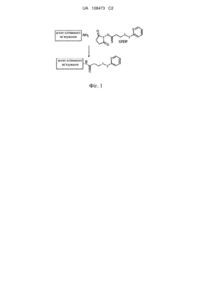
Кон’югати, їхнє одержання і застосування в терапії
Номер патенту: 108473
Опубліковано: 12.05.2015
Автори: Бушар Ерве, Чжан Цзидун, Брен Марі-Прісцилл, Коммерсон Ален
Формула / Реферат
1. Похідне криптофіцину формули (II):
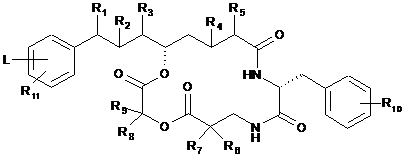 , (II)
, (II)
в якій:
R1 означає атом галогену і R2 означає групу -ОН або (С1-С4)алканоїлоксигрупу;
або R1 і R2 разом утворюють епоксидну ланку;
R3 означає (С1-С6)алкільну групу;
R4 і R5 обидва означають Н або разом утворюють подвійний зв'язок СН=СН між С13 і С14;
R6 і R7 означають, незалежно один від одного, Н або (С1-С6)алкільну групу;
R8 і R9 означають, незалежно один від одного, Н або (С1-С6)алкільну групу;
R10 означає принаймні один замісник фенільного кільця, вибраний із: Н, групи -ОН, (С1-С4)алкокси, атома галогену або ж групи -NH2, -NH(C1-C6)aлкіл або -N(С1-С6)алкіл2;
R11 означає принаймні один замісник фенільного кільця, вибраний із Н або (С1-С4)алкільної групи;
L означає лінкер у положенні орто- (о-), мета- (м-) або пара- (п-), переважно у пара-положенні, фенільного кільця, що несе ланку GCR1, що вибирають із формул:
-G'X(CR13R14)t(OCH2CH2)y(CR15R16)uQGCR1;
-G'X(CR13R14)t(OCH2CH2)yY'-(CR15R16)uQGCR1;
-G'X(CR13R14)t(CR17=CR18)(CR15R16)u(OCH2CH2)uQGCR1;
-G'X(CR13R14)t(OCH2CH2)y(CR17=CR18)(CR15R16)uQGCR1;
-G'X(CR13R14)t-фeнiл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-фурил-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-оксазоліл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-тiaзoлiл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-тієніл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-iмiдaзoлiл-(CR15R16)uY'QGCR1;
-G'Х(С13R14)t-піперазиніл-CO(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-піперидинілметил-NH12-CO(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-піперидиніл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-піперидиніл-NR12-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-триазоліл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-триазоліл-(CR15R16)uY'QGCR1;
-G'X(CR13R14)t-феніл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-фурил-(CR15R16)uQGCR1;
-G'X(CR13R14)t-oксазоліл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-тіазоліл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-тієніл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-імідазоліл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-піперазиніл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-пiпepидинiл-(CR15R16)uQGCR1;
-G'X(CR13R14)t-піперидинілметил-NR12-(CR15R16)uQGCR1;
-G'X(CR13R14)t-піперидиніл-NR12-(CR15R16)uQGCR1;
-G'X(CR13R14)t-триазоліл-(CR15R16)uQGCR1;
або
-G''Y(CR13R14)t(OCH2CH2)y(CR15R16)uQGCR1;
-G''Y(CR13R14)t(OCH2CH2)y-Y'-(CR15R16)uQGCR1;
-G''Y(CR13R14)t(CR17=CR18)(CR15R16)u(OCH2CH2)yQGCR1;
-G''Y(CR13R14)t(OCH2CH2)y(CR17=CR18)(CR15R16)uQGCR1;
-G''Y(CR13R14)t-феніл-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-фypил-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-оксазоліл-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-тіазоліл-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-тієніл-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-імідазоліл-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-піперазиніл-CO(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-піперидинілметил-NR12-CO(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-пiпepидинiл-(CR15R16)uY'QGCR1;
-G"Y(CR13R14)t-піперидиніл-NR12-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-триазоліл-(CR15R16)uY'QGCR1;
-G''Y(CR13R14)t-феніл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-фурил-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-оксазоліл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-тіазоліл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-тієніл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-імідазоліл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-піперазиніл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-піперазиніл-(CR15R16)uQCCR1;
-G''Y(CR13R14)t-піперидиніл-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-піперидинілметил-NR12-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-піперидиніл-NR12-(CR15R16)uQGCR1;
-G''Y(CR13R14)t-тpиaзoлiл-(CR15R16)uQGCR1;
в яких:
G' позначає групу -СН=СН- або -(СН2)n-;
G" позначає групу -(СН2)n-;
n позначає ціле число від 1 до 6;
X позначає простий зв'язок або групу -СО-, -СОО- або -CONR12-, причому група CO зв'язана з G';
Y позначає групу -О-, -ОСО-, -ОСОО-, -OCONR12-, -NR12-, -NR12CO, -NR12CONR'12, -NR12COO- або -S(O)q-, причому атом О або група NR12 зв'язані з G";
q позначає ціле число, що означає 0, 1 або 2;
Y' позначає групу -О-, -ОСО-, -ОСОО-, -OCONR12-, -NR12-, -NR12CO-, -NR12CONR'12, -NR12COO-, -S(O)q-, -CO-, -COO - або -CONR12-;
R12, R'12, R13, R14, R15, R16, R17 і R18 означають, незалежно один від одного, Н або (С1-С6)алкільну групу;
t, u і у позначають цілі числа від 0 до 20, причому t+u+y повинна бути вища або дорівнювати 1;
у разі лінкеру формули -G'Y(CR13R14)t(OCH2CH2)y-Y'-(CR15R16)uQGCR1, якщо у означає 0, a Q означає простий зв'язок, то u не може означати 0;
Q означає простий зв'язок, (С1-С10)алкіленову групу або групу (ОСН2СН2)i, де і означає ціле число від 1 до 20, конкретніше від 1 до 10, ще конкретніше від 1 до 8 або від 1 до 6 і ще конкретніше від 2 до 5;
GCR1 означає -SZa, -C(=O)-ZbRb, 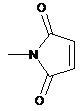 або
або 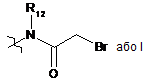 , де R12 означає Н або (С1-С6)алкіл, конкретніше метил;
, де R12 означає Н або (С1-С6)алкіл, конкретніше метил;
або L вибирають із формул:
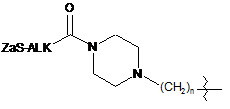 ;
; 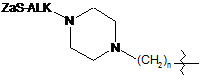 ;
; 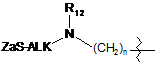 ;
;
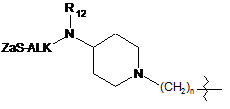 ;
; 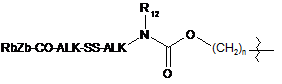 ;
;
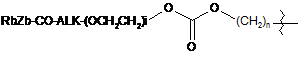 ;
; 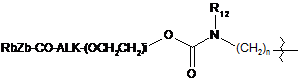 ;
;
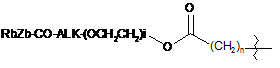 ;
; 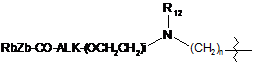 ;
;
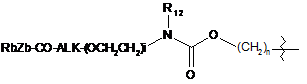 ;
; 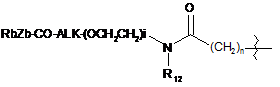 ;
;
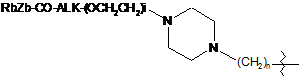 ;
; 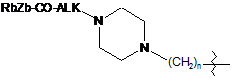 ;
;
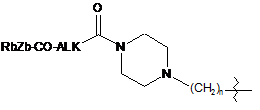 ;
; 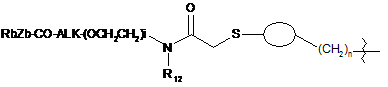 ;
;
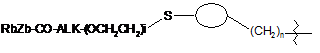 ;
; ![]() ;
;
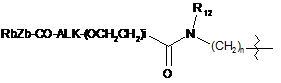 ;
; 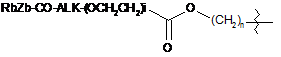 ;
;
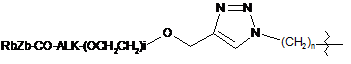 ;
;  ;
;
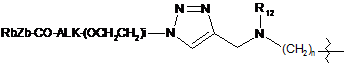 ;
; 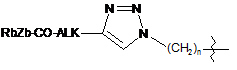 ;
;
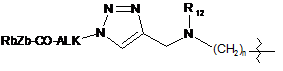 ;
; ![]() ;
;
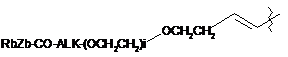 ;
; ![]() ;
;
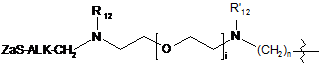 ;
;  ;
;
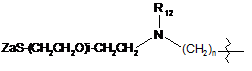 ;
; 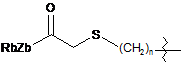 ;
; 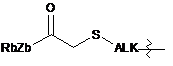 ;
;
-ALK-SZa або -(CH2)n-SZa,
в яких:
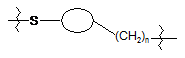 означає одну з наступних груп:
означає одну з наступних груп:
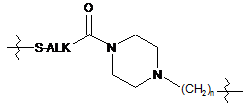 ;
; 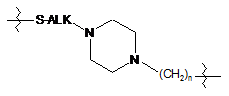 ;
; 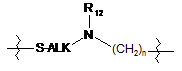 ;
;
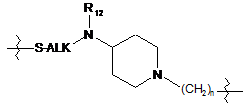 ;
; 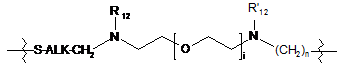 ;
;
 ;
;  ;
; ![]() або
або ![]() ;
;
n позначає ціле число від 1 до 6;
ALK позначає (С1-С12)алкіленову групу;
R12 і R'12 позначають, незалежно один від одного, Н або (С1-С6)алкільну групу, конкретніше метильну;
і означає ціле число від 1 до 20, конкретніше від 1 до 10, ще конкретніше від 1 до 8 або від 1 до 6 і ще конкретніше від 2 до 5.
2. Похідне криптофіцину за п. 1, в якому R10 означає принаймні один замісник фенільного кільця, вибраний із: Н, групи ОН, (С1-С4)алкокси, атома галогену.
3. Похідне криптофіцину за п. 1 або 2, в якому GCR1 означає -SZa або -С(=О)-ZbRb.
4. Похідне криптофіцину за будь-яким з пп. 1-3, в якому 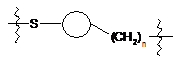 означає одну з 7 наступних груп:
означає одну з 7 наступних груп:
 ;
; 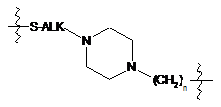 ;
;
 ;
;
 ;
;
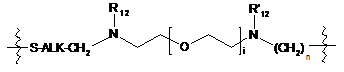 ;
;
 ;
;
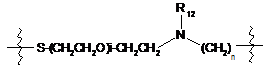 .
.
5. Похідне криптофіцину за будь-яким з пп. 1-4, в якому n дорівнює 1.
6. Похідне криптофіцину за п. 1, в якому L вибраний із:
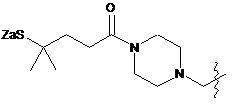 ;
; 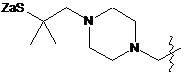 ;
; 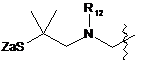 ;
;
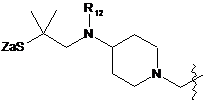 ;
; 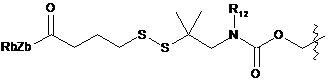 ;
;
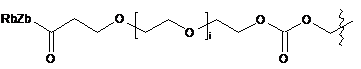 ;
;
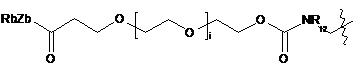 ;
;
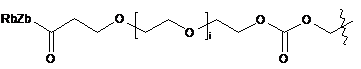 ;
;
 ;
;
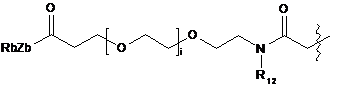 ;
;
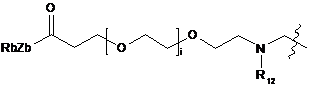 ;
;
 ;
;  ;
;
 ;
;
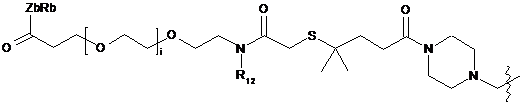 ;
;
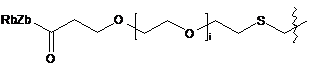 ;
;
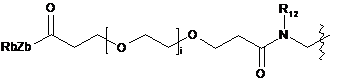 ;
;
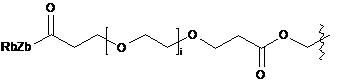 ;
;
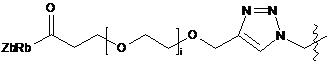 ;
;
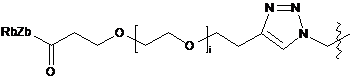 ;
;
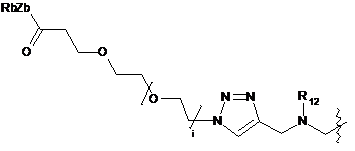 ;
; 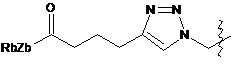 ;
;
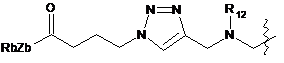 ;
;
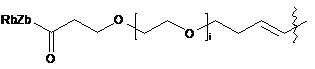 ;
;
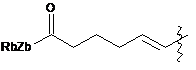 ;
; 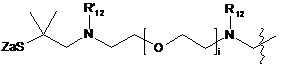 ;
;
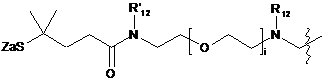 ;
;
 ;
;
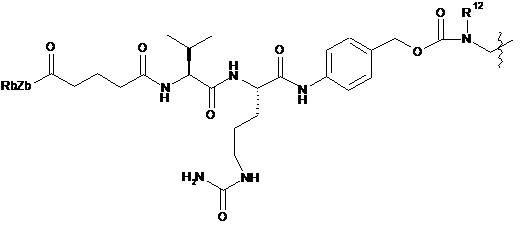 ;
;
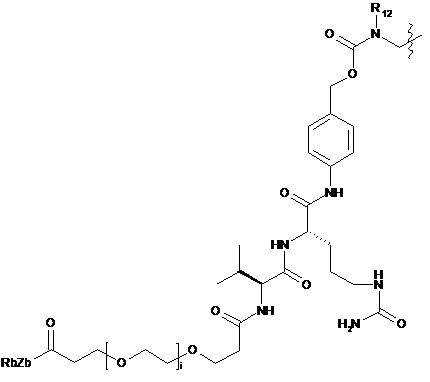 ;
;
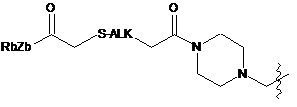 ;
; 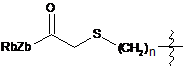 ;
;
-CH2SZa; -ALK-SZa;
R12 і R'12 означають, незалежно один від одного, Н або (С1-С6)алкільну групу, конкретніше метильну;
і означає ціле число від 1 до 20, конкретніше від 1 до 10, ще конкретніше від 1 до 8 або від 1 до 6 і ще конкретніше від 2 до 5;
Za означає Н або групу -SRa, причому Ra означає групу (С1-С6)алкіл, (С3-С7)циклоалкіл, арил, гетероарил або (С3-С7)гетероциклоалкіл;
Zb означає простий зв'язок, -О- або -NH-, причому Rb означає Н або групу (С1-С6)алкіл, (С3-С7)циклоалкіл, арил, гетероарил або (С3-С7)гетероциклоалкіл.
7. Похідне криптофіцину за п. 1, в якому L вибраний із:
 ;
; 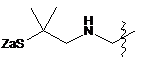 ;
; 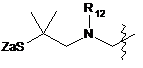 ;
;
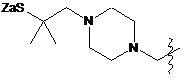 ;
; 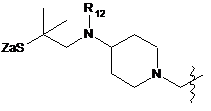 ;
;
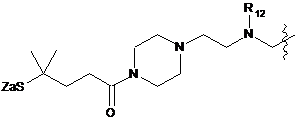 ;
;  ;
;
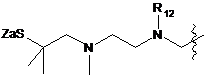 ;
;
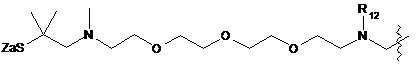 ;
;
 ;
; 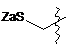 ;
;
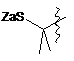 ;
; 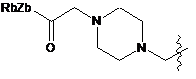 ;
; 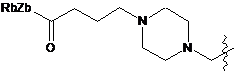 ;
;
 ;
; 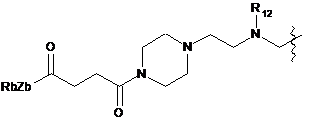 ;
;
 ;
;
 ;
;
 ;
;
 ;
; 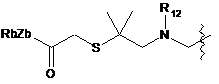 ;
;
 ;
;
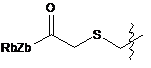 ;
; 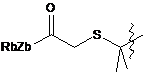 ;
; 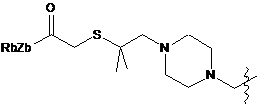 ;
;
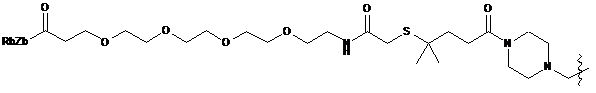 ;
;
 ;
; 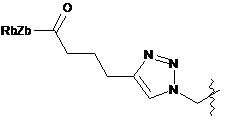 ;
;
 ;
;
 ;
;  ;
;
 ;
;
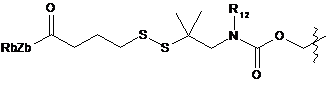 ;
;
 ;
;
 ;
;
 ;
;
 ;
;
 ;
;
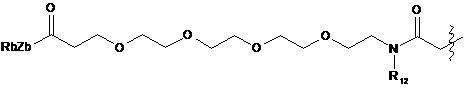 ;
;
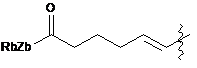 ;
;
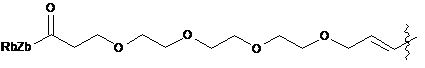 ;
;
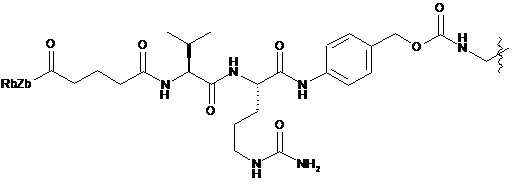 ;
;
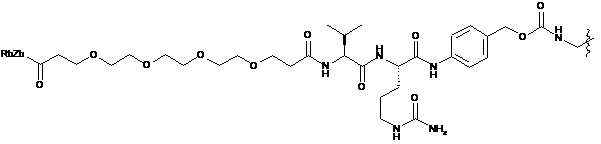 ;
;
R12 означає Н або (С1-С6)алкільну групу, конкретніше метильну.
8. Похідне криптофіцину за п. 7, в якому R12 означає Н.
9. Похідне криптофіцину за п. 7, в якому R12 означає (С1-С6)алкіл, конкретніше метил.
10. Похідне криптофіцину за будь-яким з пп. 1-9, в якому Za означає Н або -S(С1-С6)алкіл, зокрема -SMe, або -S-гетероарил, зокрема 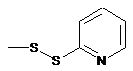 , або ZbRb означає -О(С1-С6)алкіл, -ОН, -ОСН3, -ОСН2СН=СН2,
, або ZbRb означає -О(С1-С6)алкіл, -ОН, -ОСН3, -ОСН2СН=СН2, 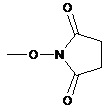 або
або  , або катіон
, або катіон 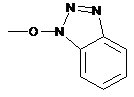 , або групу
, або групу 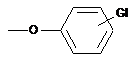 , в якій G1 означає принаймні одну електроноакцепторну групу, або ж в якому -C(=O)ZbRb означає
, в якій G1 означає принаймні одну електроноакцепторну групу, або ж в якому -C(=O)ZbRb означає 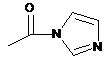 .
.
11. Похідне криптофіцину за будь-яким з пп. 1-10, описане однією з наступних формул, причому L знаходиться, переважно, у пара-положенні:
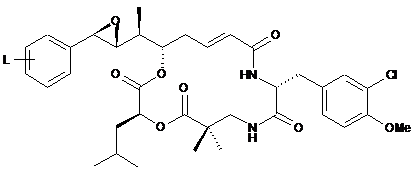 ,
,
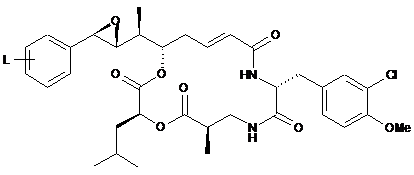 ,
,
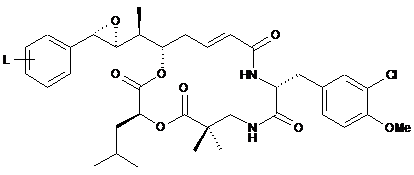 ,
,
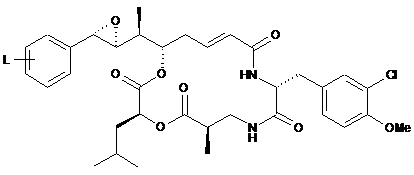 ,
,
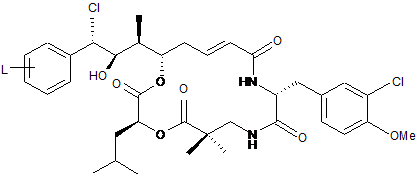 ,
,
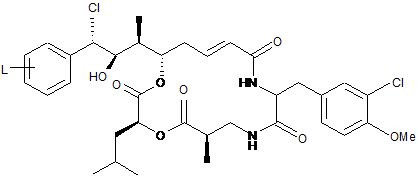 ,
,
 ,
,
 .
.
12. Похідне криптофіцину за п. 1, вибране з:
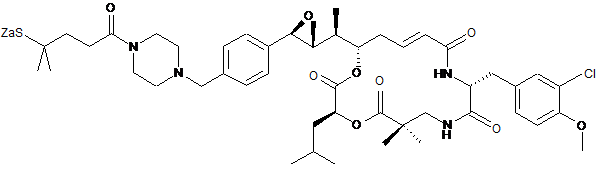 ,
,
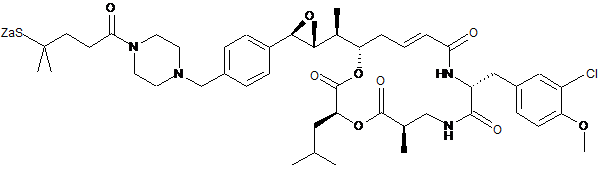 ,
,
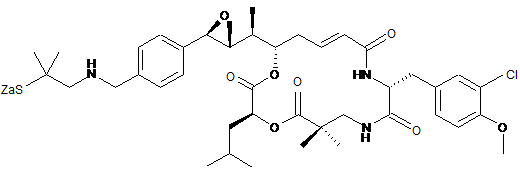 ,
,
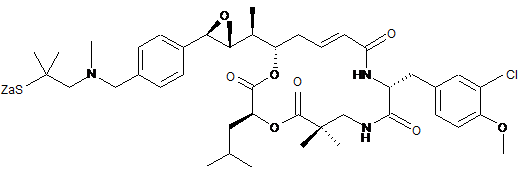 ,
,
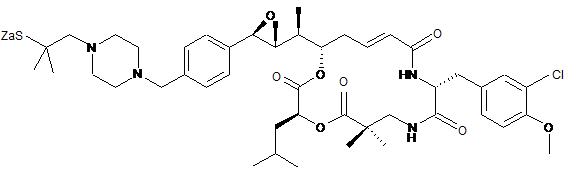 ,
,
 ,
,
 ,
,
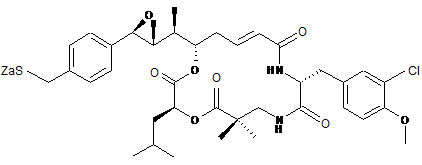 ,
,
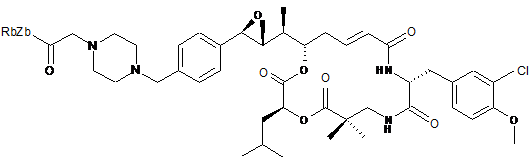 ,
,
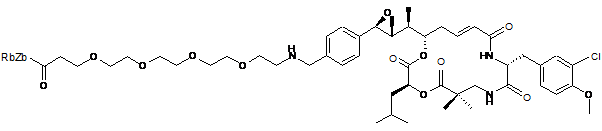 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
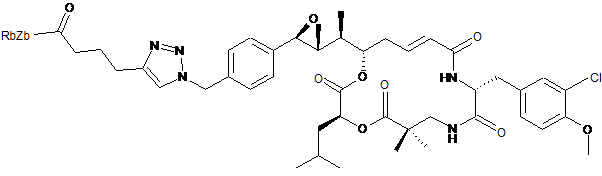 ,
,
 ,
,
 ,
,
 ,
,
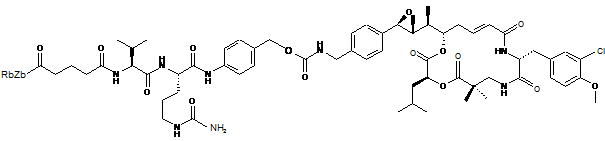 ,
,
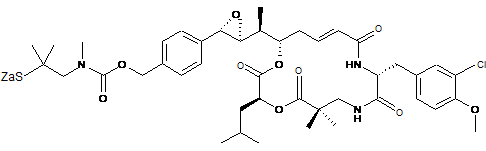 ,
,
причому Za, Zb і Rb визначені в п. 1 або 10.
13. Похідне криптофіцину формули (III):
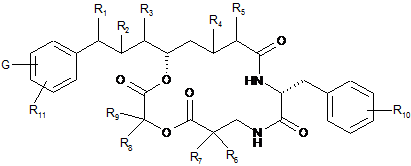 ,
,
в якій групи R1-R11 мають такі ж значення, які зазначені в п. 1, 11 або 12, і G означає групу -(CH2)nY, що знаходиться в орто- (о-), мета- (м-) або пара- (п-) положенні фенільного кільця, що несе ланку CR1, переважно в пара-положенні, причому
n є цілим числом від 1 до 6, a Y означає -N3; -NR12-CH2-C=CH, в якому R12 означає Н або (С1-С6)алкільну групу; -OMs; -ОС(=О)-О-(4-нітрофеніл), 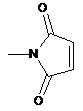 або
або 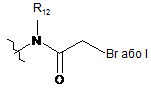 , де R12 означає Н або (С1-С6)алкіл, конкретніше метил.
, де R12 означає Н або (С1-С6)алкіл, конкретніше метил.
14. Похідне криптофіцину за п. 13, в якому Y означає -N3; -NR12-CH2-C=CH, де R12 означає Н або (С1-С6)алкіл; - OMs або -ОС(=О)-О-(4-нітрофеніл).
15. Похідне криптофіцину за будь-яким з пп. 1-13, в якому агентом клітинного зв'язування є ліганд, білок, антитіло, конкретніше моноклональне антитіло, фрагмент білка або антитіла, пептид, олігонуклеотид або олігосахарид.
16. Спосіб одержання агента клітинного зв'язування, з яким зв'язано принаймні одне похідне криптофіцину, агента, що називають кон'югатом, який полягає в тому, що:
(і) вводять у контакт і піддають взаємодії водний розчин агента клітинного зв'язування, необов'язково забуференого, і розчин похідного криптофіцину, такого, як визначений в одному з пп. 1-16;
(іі) потім, необов'язково, відділяють кон'югат, одержаний на стадії (і), від похідного криптофіцину, що не прореагував, і/або агента клітинного зв'язування і/або від агрегатів, що можливо утворилися.
17. Спосіб за п. 16, в якому:
в присутності похідного криптофіцину, що містить реакційноздатну хімічну групу GCR1 типу -SZa, агент клітинного зв'язування містить:
дисульфідні хімічні групи, якщо GCR1 означає -SH;
тіольні хімічні групи, якщо GCR1 означає -SZa, де Za≠H;
малеімідо або йодацетамідо хімічні групи, якщо GCR1 означає -SH;
- у присутності похідного криптофіцину, що містить реакційноздатну хімічну групу GCR1 типу -C(=O)-ZbRb, піддають взаємодії похідне криптофіцину з амінофункціями агента клітинного зв'язування, зокрема ε-аміногрупами, що знаходяться на бічних ланцюгах лізинових залишків (Lys) антитіла;
- у присутності похідного криптофіцину формули (III), в якій G=-(CH2)nY, агент клітинного зв'язування містить групи -SH, якщо Y=-Cl або -малеімідо, групи -СºСН, якщо Y=-N3, або карбоксильні групи, якщо Y=-OH або -NH2;
- у присутності похідного криптофіцину, що містить реакційноздатну хімічну групу GCR1 типу мелеіміду або галогенацетамідо, агент клітинного зв'язування містить тіольні хімічні групи.
18. Спосіб за п. 16 або 17, в якому:
- у присутності похідного криптофіцину, що містить реакційноздатну хімічну групу GCR1 типу -SZa, агент клітинного зв'язування модифікують за допомогою модифікуючого агента, вибраного зі сполуки формули 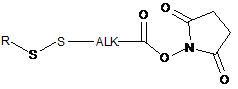 , в якій R означає групу (С1-С6)алкіл, арил, гетероарил, (С3-С7)циклоалкіл, (С3-С7)гетероциклоалкіл і ALK означає (С1-С6)алкіленову групу;
, в якій R означає групу (С1-С6)алкіл, арил, гетероарил, (С3-С7)циклоалкіл, (С3-С7)гетероциклоалкіл і ALK означає (С1-С6)алкіленову групу;
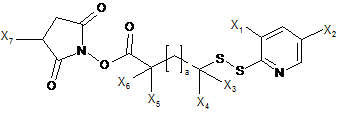 , пегильований аналог формули
, пегильований аналог формули
 або сульфоновий аналог формули
або сульфоновий аналог формули
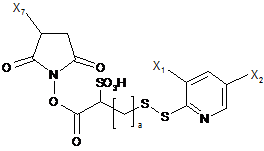 ,
,
в яких Х3, Х4, Х5, Х6 означають Н або (С1-С6)алкільну групу,
Х1 і Х2 означають -Н, -CONX8X9, NO2,
Х8 і Х9 означають Н або (С1-С6)алкільну групу,
Х7 означає -SO3-M+ або Н, або ж групу четвертинного амонію, і
а означає ціле число від 0 до 4, і
b означає ціле число від 0 до 2000;
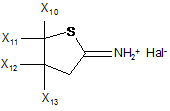 , в якій:
, в якій:
Hal означає атом водню;
Х10 означає атом галогену або групу СООХ14, нітро, (С1-С8)алкіл, незаміщений або галогенований, (С1-С8)алкокси, незаміщений або галогенований, (С2-С8)алкеніл, незаміщений або галогенований, (С2-С8)алкініл, незаміщений або галогенований, (С3-С8)циклоалкіл, незаміщений, арил, незаміщений або заміщений від одного до трьох замісниками, вибраними з аміно, атома водню, (С1-С8)алкілу, незаміщеного або галогенованого, (С1-С8)алкокси, незаміщеного або галогенованого;
кожен із Х11, X12, Х13 означає, незалежно, атом водню або може означати Х3;
або Х10 і Х11 разом утворюють (С2-С5)алкіленовий цикл, незаміщений або заміщений від однієї або п'яти (С1-С4)алкільними групами;
або Х10 або Х11 разом із Х12 утворюють (С1-С5)алкіленовий цикл, незаміщений або заміщений від однієї до п'яти (С1-С4)алкільними групами;
і Х14 означає -Н або (С1-С8)алкільну групу;
- у присутності похідного криптофіцину, що містить реакційноздатну хімічну групу GCR1 типу -SH, агент клітинного зв'язування модифікують за допомогою модифікуючого агента, вибраного з сукцинімідил-4-(N-малеімідометил)циклогексан-1-карбоксилату; сульфосукцинімідил-4-(N-малеімідометил)циклогексан-1-карбоксилату;
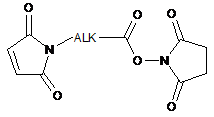 ;
; 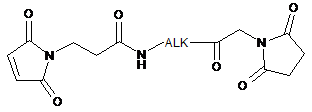 ;
;
 ;
;
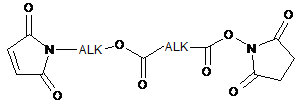 ;
;
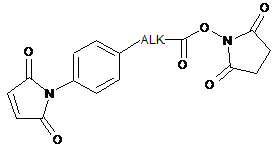 ;
;
 ,
,
причому ALK означає (С1-С12)алкіленову групу і b означає ціле число між 0 і 2000;
 ;
; 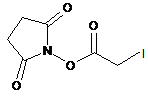 ;
;
сукцинімідил-N-бромацетату; сукцинімідил-3-(N-бромацетамідо)пропіонату;  причому b є цілим числом між 0 і 2000.
причому b є цілим числом між 0 і 2000.
19. Кон'югат, що одержується способом за одним із пп. 16-18.
20. Кон'югат за п. 19, який відрізняється тим, що DAR, що визначається на основі розшифрування HRMS-спектра, вище 1, переважно між 2 і 10, конкретніше між 2 і 7.
21. Кон'югат за п. 19, який відрізняється тим, що DAR, який визначається за допомогою УФ-спектрофотометра, вище 0,5, переважно вище 1, переважніше між 1 і 10, ще більш переважно між 2 і 7, причому DAR розраховують за рівнянням:
DAR=CD/CA,
в якому:
CD=[(εAλ1´Aλ2)-(εAλ2´Aλ1)]/[(εDλ2´εAλ1)-(εAλ2´εDλ1)],
CΑ=[Αλ1-(CD´εDλ1)]/εΑλ1
i
Аl1 і Аl2 означають відповідні смуги поглинання розчину кон'югата на довжинах хвиль l1 і l2, відповідно;
eDl1 і eDl2 означають коефіцієнти молярного поглинання похідного криптофіцину перед кон'югуванням відповідно на двох довжинах хвиль l1 і l2, згадані коефіцієнти виміряні зі сполуками формули (II) типу -SZa, де Za=-SMe, або типу -C(=O)-ZbRb, де ZbRb=-OMe або -ОСН2-СН=СН2;
eAl1 і eAl2 означають коефіцієнти молярного поглинання голого антитіла перед кон'югуванням відповідно на двох довжинах хвиль l1 і l2.
22. Кон'югат за п. 21, в якому l1=280 нм, а l2 вибраний із діапазону специфічних довжин хвиль 246-252 нм.
23. Розчин кон'югата, що одержується згідно зі способом за одним із пп. 16-18 і містить кон'югат, такий, як він визначений в одному з пп. 19-22.
24. Застосування похідного криптофіцину за будь-яким з пп. 1-13 для одержання агента клітинного зв'язування, з яким з'єднане принаймні одне похідне криптофіцину.
25. Застосування похідного криптофіцину формули (III):
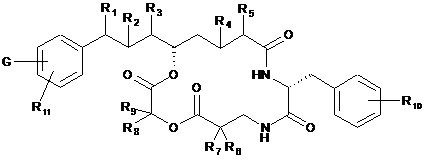 , (III)
, (III)
в якій:
G означає групу -СН=СН2 або -(CH2)nY, що знаходиться в орто- (о-), мета- (м-) або пара- (п-) положенні фенільного кільця, що несе ланку CR1, переважно у пара-положенні;
Y означає -ОН; -Сl; -N3; -NH2; -SH; -COOH; -NR12-CH2-CºCH, де R12 означає Н або (С1-С6)алкільну групу, конкретніше метильну групу; -OGP, де GP означає відхідну групу; -ОС(=О)-О-(4-нітрофеніл); -малеімідо;
або формули
 ,
,
де групи R1-R11 мають такі ж значення, як в п. 1, 11 або 12, і
n є цілим числом від 1 до 6,
для одержання агента клітинного зв'язування, з яким з'єднане принаймні одне похідне криптофіцину.
26. Застосування похідного криптофіцину, вибраного з наступних похідних:
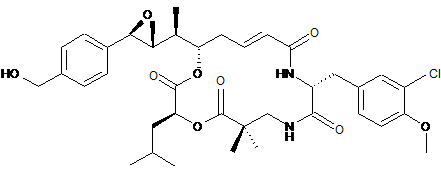 ,
,
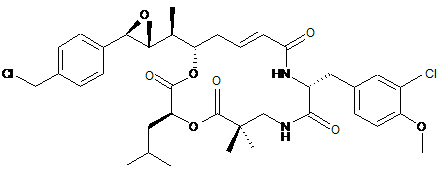 ,
,
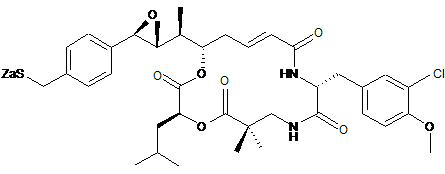 ,
,
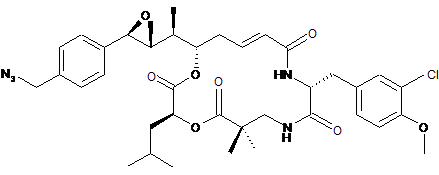 ,
,
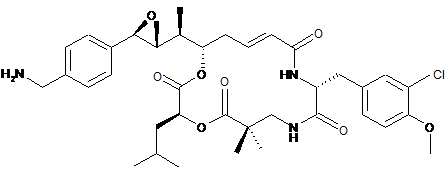 ,
,
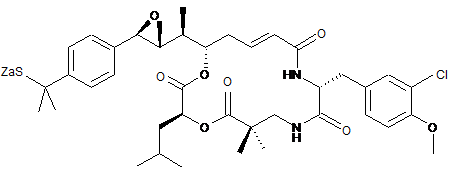 ,
,
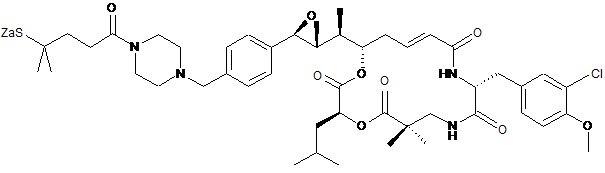 ,
,
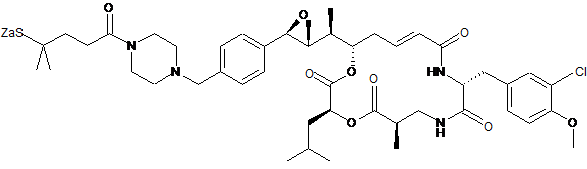 ,
,
 ,
,
 ,
,
 ,
,
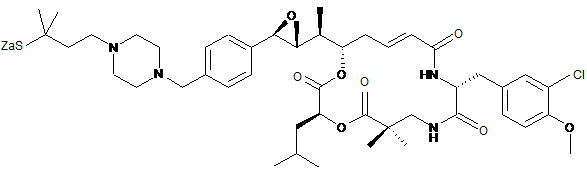 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
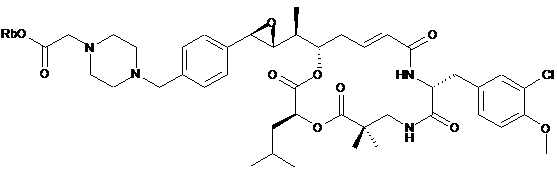 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
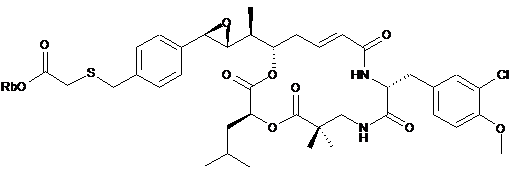 ,
,
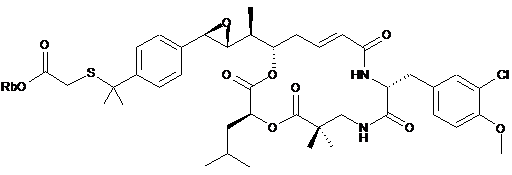 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
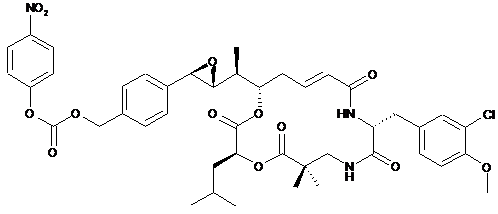 ,
,
 ,
,
 ,
,
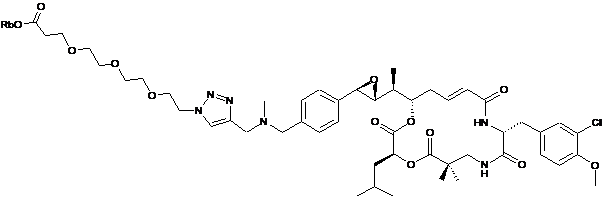 ,
,
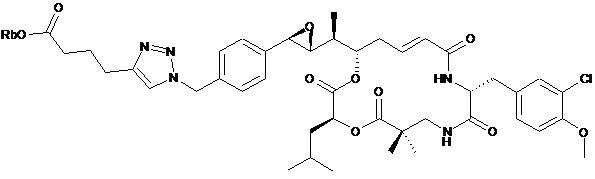 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
де Za, Zb і Rb такі, як визначено в п. 1 або 10,
для одержання агента клітинного зв'язування, з яким з'єднане принаймні одне похідне криптофіцину.
27. Похідне криптофіцину формули:
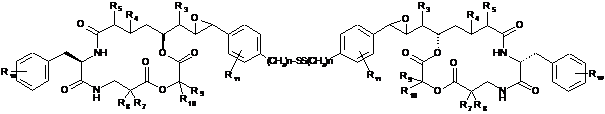 ,
,
де групи R1-R11 мають такі ж значення, як в п. 1, 11 або 12, і n є цілим числом від 1 до 6.
28. Похідне криптофіцину за будь-яким з пп. 1-14 для застосування як протиракового агента.
29. Кон'югат за пп. 19-22 для застосування як протиракового агента.
30. Розчин кон'югата за п. 23 для застосування як протиракового агента.
31. Застосування похідного криптофіцину за будь-яким з пп. 1-14 для одержання протиракового лікарського засобу.
32. Застосування кон'югата будь-яким з пп. 19-22 для одержання протиракового лікарського засобу.
33. Застосування розчину кон'югата за п. 23 для одержання протиракового лікарського засобу.
Текст
Реферат: Винахід стосується агента клітинного зв'язування, з яким з'єднано принаймні одне похідне криптофіцину формули (І), в якій: R1 означає атом галогену і R2 означає групу -ОН, ацильну групу, що походить від амінокислоти АА, або (С1-С4)алканоїлоксигрупу; або R1 і R2 разом утворюють епоксидну ланку; АА означає амінокислоту природного або неприродного походження; R3 означає (С1-С6)алкільну групу; R4 і R5 обидва означають Н або разом утворюють подвійний зв'язок СН=СН між С13 і С14; R6 і R7 означають, незалежно один від одного, Н або (С1-С6)алкільну групу; R8 і R9 означають, незалежно один від одного, Н або (С1С6)алкільну групу; R10 означає принаймні один замісник фенільного кільця, вибраний із: Н, групи -ОН, (С1-С4)алкокси, атома галогену або ж групи -NH2, -NН(С1-С6)алкілу або -N(С1-С6)алкіл2; R11 означає принаймні один замісник фенільного кільця, вибраний із Н або (С1-С4)алкільної групи; причому агент клітинного зв'язування і похідне криптофіцину ковалентно сполучені, а зв'язок знаходиться в орто- (о-), мета- (м-) або пара- (п-) положенні фенільного кільця, що несе ланку CR1. UA 108473 C2 (12) UA 108473 C2 UA 108473 C2 5 10 15 20 25 30 35 Даний винахід стосується кон’югованих криптофіцинів, фармацевтичних композицій, що їх містять, і застосування їх у терапії, зокрема, як протиракових агентів. Винахід стосується також способу одержання цих сполук, а також самих похідних криптофіцинів. Галузь техніки Криптофіцини є вторинними метаболітами, що стосуються класу депсипептидних макроциклів, що продукуються ціанобактеріями виду Nostoc. Їх назва пов’язана з тим, що ці сполуки є високо цитотоксичними сполуками стосовно дріжджів виду Cryptococcus. Перший представник цього класу молекул, криптофіцин-1 (С-1), був виділений у 1990 році з ціанобактерії Nostoc sp (ATCC 53789) (Eiβler S., et al., Synthesis 2006, 22, 3747-3789). Структура, загальна формула і нумерація атомів вуглецю в цих сполуках, такі, як описано в заявці WO 98/08505, і наведені нижче: Криптофіцини С-1 і С-52, що характеризуються наявністю епоксидної функціональної групи, показаної нижче, мають протиракові властивості. Клінічні випробування були проведені на ракові легень, фаза II, із С-52 (LY 355073): див. Edelman M.J. et al., Lung Cancer 2003, 39, 197199; Sessa C. et al., Eur. J. Cancer 2002, 38, 2388-96. Сам криптофіцин С-55, що є проліками С52, характеризується наявністю хлоргідринової функціональної групи замість і на місці епоксидної функціональної групи (Bionpally R.R., et al., Cancer Chemother Pharmacol 2003, 52, 25-33). С-55 виявив себе дуже активним продуктом, але нестабільним у розчині. Описані також похідні типу хлоргідрин-гліцинатних похідних, такі як сполука С-55 Gly, для збільшення стабільності (Liang J., et al., Investigational New Drugs 2005, 23, 213-224). Технічне завдання Хімія кон’югатів відома протягом декілька років і була застосована для вивчення декількох сімейств цитотоксичних сполук, таких, як, наприклад, майтансиноїди (WO 04103272), таксани (WO 06061258), томайміцини (WO 09016516), лептоміцини (WO 07144709), СС-1065 і його аналоги (WO 2007102069); див. також про кон’югировані сполуки: Monneret С., et al., Bulletin du Cancer, 2000, 87(11), 829-38; Ricart A.D. et al., Nature Clinical Practice Oncology 2007, 4, 245-255. Однак ця хімія не займалася похідними криптофіцину, кон’югованих з антитілами або іншими агентами клітинного зв’язування. Технічне завдання, яке пропонує вирішити даний винахід, полягає в наданні нових кон’югатів на основі похідних криптофіцину, а також нових похідних криптофіцину, здатних до кон’югування. Рівень техніки Документи ЕР 0830136 і WO 98/08505 описують похідні криптофіцинів, але не описують кон’юговані криптофіцини. Заявка WO 98/08505 описує похідні криптофіцинів формули (А): 1 UA 108473 C2 , в якій Ar може означати групу Ar формули: , в якій R54 означає Н, групу (С1С6)алкіл, (С1-С6)алкіл(R57,R57,R57), арил, феніл, гетероциклоалкіл, атом галогену, СOOR 57, PO3H, SO3H, SO2R58, NR59R60, NHOR61, NHOR61, CN, NO2, OR62, CH2OR62, CH2NR96R96, (C15 C6)алкілOR100, , SR63; R55 і R56 означають Н, групу (С1-С6)алкіл, С(R57,R57,R57), арил, феніл, гетероциклоалкіл, атом галогену, СOOR 57, PO3H, SO3H, SO2R58, NR59R60, NHOR61, NHCHR61, CN, NO2, OR62, CH2OR62, CH2OCOR95, CH2NR96R96, (С1-С6)алкілОR100, (С1С6)алкілNR59,R60. Заявка WO 98/08505 описує, зокрема, наступні сполуки: (сполука 24, схема 4) 10 (сполука 33, схема 5) 2 UA 108473 C2 5 10 15 20 , які характеризуються кінцевою групою -NHC(=О)Ot-Bu. Однак заявка WO 98/08505 не конкретизує, що ці сполуки можуть бути кон’юговані або використовуються для кон’югування. US 2007/0213511 описує імунокон’югати каліхеаміцину. Серед них згадується MYLOTARG® (або СМА-676), який є імунокон’югатом каліхеаміцину, що використовується для лікування AML (анти-CD33-каліхеаміцин). Про кон’югати див. також: WO 2006/042240. Al-awar R.S., et al., J. Med. Chem. 2003, 46(14), 2985-3007 і Al-awar R.S., et al., Mol. Cancer Ther. 2004, 3(9), 1061-1067 описують похідні криптофіцину, а також оцінюють їхню активність in vivo. WO 08010101 описує моноклональне антитіло проти EphA2, а також відповідні кон’югати, що включають одну або декілька молекул цитотоксичної сполуки, зв’язаної(их) із моноклональним антитілом. WO 08047242 описує моноклональне антитіло проти CD38, а також відповідні кон’югати, що включають одну або декілька молекул цитотоксичної сполуки, зв’язаної(их) із моноклональним антитілом. Цитотоксична сполука може бути вибрана з майтансіноїдів, таксанів, томайміцинів, лептоміцинів, СС-1065 і його аналогів. WO 2009/126934 описує антитіла проти CD70 та їхні кон’югати з цитотоксичними сполуками; серед цитотоксичних сполук названий криптофіцин. WO 2009/134976 описує кон’югати з оптимальною мірою заміщення для подачі необхідної кількості цитотоксичних сполук у клітину; серед цитотоксичних сполук названий криптофіцин. WO 2005/116255 описує кон’югати аптамерів із цитотоксичною сполукою, якою може бути криптофіцин (див.[0037] і Таблицю 2), причому лінкер може включати ПЕГ-ланцюжок ([0038]). Зокрема, описаний криптофіцин Cryp-NH2 формули: 3 UA 108473 C2 5 10 15 20 25 30 35 40 , а також його кон’югати на основі аптамерів із наступними лінкерами: NHS-ПЕГ-еритритол, pNP-ПЕГ-еритритол, NHS-ПЕГ-октаПЕГ, pNP-ПЕГ-октаПЕГ і ПЕГ-comb (Таблиці 3 і 4). Природа ланцюга на фенільному кільці (-СН2О-С(=О)-СМе2-СН2NH-…) відрізняється від того, що запропоновано в даному винаході. WO 2006/096754 також описує кон’югати аптамерів із цитотоксичною сполукою, якою також може бути криптофіцин. WO 2009/002993 описує кон’югати цитотоксичної сполуки формули B-L-A, що включають гідрофільний лінкер, наприклад, лінкер формули: Цитотоксичною сполукою може бути криптофіцин (с.46), при цьому не уточнене місце приєднання лінкеру. Прикладом кон’югованої сполуки є ЕС0262: в якої лінкер і місце його приєднання відрізняються від тих, які запропоновані в даному винаході. Визначення Мають на увазі під: - кон’югатом: агент клітинного зв’язування, з яким ковалентно з’єднана, принаймні, одна молекула цитотоксичної сполуки; - агентом клітинного зв’язування (або по-англійському “cell binding agent"): молекулу, що має спорідненість до біологічної мішені: це можливо, наприклад, ліганд, білок, антитіло, конкретніше, моноклональне антитіло, фрагмент білка або антитіла, пептид, олігонуклеотид, олігосахарид. Функція агента клітинного зв’язування полягає в тому, щоб спрямовувати біологічно активну сполуку, таку як цитотоксична сполука, до біологічної мішені. Переважно, щоб агент клітинного зв’язування не був аптамером; - біологічною мішенню: антиген (або групу антигенів), локалізований переважно на поверхні ракових або стромальних клітин, асоційованих із цією пухлиною; цими антигенами можуть бути, наприклад, рецептор фактора росту, онкогенний продукт або мутований ген-“супресор пухлини”, молекула, пов’язана з ангіогенезом, адгезивна молекула; - лінкером: сукупність атомів, що дозволяє ковалентно з’єднати цитотоксичну сполуку з агентом клітинного зв’язування; - алкільною групою: вуглеводневу аліфатичну насичену групу, що одержується видаленням атома водню з алкану. Алкільна група може бути лінійною або розгалуженою. Як приклад можна назвати групи: метил, етил, пропіл, ізопропіл, бутил, ізобутил, трет-бутил, пентил, 2,2диметилпропіл, гексил; - циклоалкільною групою: циклічну алкільну групу, що містить 3-8 атомів вуглцю, вбудованих у циклічну структуру. Як приклад можна назвати групи: циклопропіл, циклобутил, циклопентил, циклогексил; - гетероциклоалкільною групою: циклоалкільну групу, що містить, принаймні, один гетероатом (О, S, N), вбудований у цикл і зв’язаний з атомами вуглецю, що утворюють цикл; - алкоксигрупою: О-алкільну групу, в якій алкільна група така, як визначена вище; - алканоїлоксигрупою: О-СО-алкільну групу, в якій алкільна група така, як визначено вище; - алкіленовою групою: двовалентну насичену групу бруто-формули -CNH2n-, що одержується видаленням двох атомів водню з алкану. Як приклад можна назвати метиленову (-СН2-), етиленову (-СН2СН2-), пропіленову (-СН2СН2СН2-), бутиленову (-СН2СН2СН2СН2-), гексиленову 4 UA 108473 C2 5 10 15 20 25 30 35 40 45 (-СН2СН2СН2СН2СН2СН2-) групу або наступні розгалужені групи ; - переважно, алкіленова група відповідає формулі -(CH2)n-, де n означає ціле число; - у діапазон величин включені граничні значення (наприклад, діапазон типу “n від 1 до 6” або “між 1 і 6” включені граничні значення 1 і 6). Абревіатура, що використовується AcOEt: етилацетат; ALK: група (С1-С12)алкілен, конкретніше, (С1-С6)алкілен, конкретніше, у вигляді -(CH2)n-, де n означає ціле число від 1 до 12, переважно, від 1 до 6; aq.: водний; ССМ: хроматографія в тонкому шарі (по-англійському TLC); CMS: метансульфонілхлорид; крипто означає ланку формули , зокрема, крипто означає одне з похідних криптофіцину D 1-D8, описаних нижче, або похідне криптофіцину згідно з будь-яким прикладом; Rf: коефіцієнт утримування; DAR: ступінь заміщення (drug-antibody ratio); DBU: 1,8-діазабіцикло[5.4.0]ундец-7-ен; DCC: N,Nдициклогексилкарбодиімід; DCM: дихлорметан; DEAD: діетилазодикарбоксилат; DIC: N,Nдіізопропілкарбодиімід; DIPEA: N,N-діізопропілетиламін; DMA: диметилацетамід; DMAP: 4диметиламінопіридин; DME: диметоксіетан; DMF: диметилформамід; ДМСО: диметилсульфоксид; EEDQ: 2-етокси-1-етоксикарбоніл-1,2-дигідрохінолін; EDCl: N-(3диметиламінопропіл)-N-етилкарбодиімід; EDTA: етилендіамінтетраоцтова кислота; екв.: еквівалент; Fmoc: флуоренілметоксикарбоніл; HOBt: 1-гідроксибензотриазол; HEPES: 4-(2гідроксіетил)-1-піперазинетансульфонова кислота; mCPBA: м-хлорпербензойна кислота; NHS: N-гідроксисукцинімід; NMP: N-метилпіролідинон; АТ: атмосферний тиск; РАВАС: “карбонат пара-амінобензилового спирту”; ЗТ: знижений тиск; SEC: ексклюзивна стерична хроматографія; SPE: твердофазна екстракція; КТ: кімнатна температура; TBDMS: трет-бутилдиметилсиліл; ТСЕР: гідрохлорид трис-(2-карбоксіетил)фосфіну; ТЕА: триетиламін; TFA: трифтороцтова кислота; TIPS: триізопропілсиліл; ТHF: тетрагідрофуран; tR: час утримування. Детальний опис винаходу Винахід стосується агента клітинного зв’язування, з яким з’єднане, принаймні, одне похідне криптофіцину формули (I): , в якій: * R1 означає атом галогену і R2 означає групу -ОН, ацильну групу, що походить від амінокислоти АА, або (С1-С4)алканоїлоксигрупу; або R1 і R2 разом утворюють епоксидну ланку; - АА означає амінокислоту природного або не природного походження; * R3 означає (C1-С6)алкільну групу; * R4 і R5 обидва означають Н або разом утворюють подвійний зв’язок СН=СН між С13 і С14; * R6 і R7 означають, незалежно один від одного, Н або (С1-С6)алкільну групу; * R8 і R9 означають, незалежно один від одного, Н або (С1-С6)алкільну групу; * R10 означає, принаймні, один замісник фенільного кільця, вибраний із: Н, групи -ОН, (С1С4)алкокси, атома галогену або ж групи -NH2, -NH(C1-C6)алкіл або -N(C1-C6)алкіл2; * R11 означає, принаймні, один замісник фенільного кільця, вибраний із Н або (С1С4)алкільної групи; при цьому агент клітинного зв’язування і похідна криптофіцину ковалентно сполучені, і місце їх Сполука знаходиться в орто(о)-, мета(м)- або пара(п)- положенні на фенільному кільці, що несе ланку CR1. орто(о)-, мета(м)- або пара(п)-положення: 5 UA 108473 C2 5 10 15 20 25 30 35 40 45 R1 означає атом галогену, конкретніше, Cl. R3 означає (С1-С6)алкільну групу, конкретніше, Ме; R6 і R7 означають, незалежно один від одного, Н або (С1-С6)алкільну групу; конкретніше, вони означають, незалежно один від одного, Н або групу Ме. R8 і R9 означають, незалежно один від одного, Н або (С1-С6)алкільну групу; конкретніше, R8 означає Н і R9 означає ізобутил. R10 являє собою, принаймні, один замісник фенільного кільця, вибраний із Н, групи -ОН, (С1С4)алкоксигрупи, атома галогену. Це може бути також група -NH2, -NH(C1-C6)алкіл або -N(C1C6)алкіл2, така як, наприклад, -NH2 або -NMe2, переважно, у положенні 3 або 4 фенільного кільця. Конкретніше, на фенільному кільці є два замісники в положенні 3 і 4. Переважно, ними є 3-Cl і 4-метокси. R11 являє собою, принаймні, один замісник фенільного кільця, вибраний із Н або (С1-С4)алкільної групи; конкретніше, Н. У конкретнішому випадку, можна вибрати один із замісників R 1-R11 серед тих, які описані в прикладах. Кожний замісник R1-R11 може також прийняти одну з просторових конфігурацій (наприклад, R або S або ж Z або Е), як описано в прикладах. АА означає амінокислоту природного або не природного походження. Мова може йти про α, β або γ амінокислоту. Можна назвати, зокрема, наступні амінокислоти: аланін (Ala), β-аланін, 2аміно-2-циклогексилоцтову кислоту, 2-аміно-2-фенілоцтову кислоту, аргінін (Arg), аспартамову кислоту (Asp), цистеїн (Cys), глутамін (Gln), глутамінову кислоту (Glu), гліцин (Gly), гістидин (His), ізолейцин (Ile), лейцин (Leu), лізин (Lys), метіонін (Met), фенілаланін (Phe), пролін (Pro), серин (Ser), треонін (Thr), триптофан (Trp), тирозин (Tyr), валін (Val), γ-аміномасляну кислоту, α,α-диметил-γ-аміномасляну кислоту, β,β-диметил-γ-аміномасляну кислоту, орнітин (Orn), цитрулін (Cit), а також захищені форми згаданих амінокислот (наприклад, ацетилом, формілом, тозилом, нітро). Переважно, мова йде про природну амінокислоту. Конкретніше, про гліцин. R1 і R2 можуть також разом утворювати епоксидну ланку. Зв’язування похідної криптофіцину з агентом клітинного зв’язування здійснюється через лінкер L, що займає орто(о)-, мета(м)- або пара(п)-положення на фенільному кільці, що несе ланку CR1; так, похідна криптофіцину, здатна до кон’югування, має формулу (II): . Місце зв’язування з агентом клітинного зв’язування знаходиться на іншому кінці лінкеру L на рівні реакційноздатної групи, що є на агентові клітинного зв’язування. Так, L містить, принаймні, одну хімічну реакційноздатну групу (GCR1) навпроти хімічної реакційноздатної групи (GCR2), що є на агентові клітинного зв’язування. Взаємодія між GCR1 і GCR2 забезпечує зв’язування сполуки формули (II) з агентом клітинного зв’язування за допомогою утворення ковалентного зв’язку. Таким шляхом похідне криптофіцину формули (II) здатне кон’югуватися з агентом клітинного зв’язування. Похідні криптофіцину згідно з даним винаходом, у тому числі похідні криптофіцину згідно з прикладами, можуть існувати у формі основ або кислотно-адитивних солей із кислотами, зокрема, із фармацевтично прийнятними кислотами. Як приклади групи GCR1 можна назвати: (i) реакційноздатну групу -SZa, в якій Za означає Н або групу -SRa, де Ra означає групу (С1С6)алкіл, (С3-С7)циклоалкіл, арил, гетероарил або (С3-С7)гетероциклоалкіл; (ii) реакційноздатну групу -C(=О)-ZbRb, в якій Zb означає простий зв’язок, -О- або -NH-, конкретніше, -О-, і Rb означає Н або групу (С1-С6)алкіл, (С3-С7)циклоалкіл, арил, гетероарил або (С3-С7)гетероциклоалкіл; або І (iii) одну з наступних реакційноздатних груп: - Cl, -N3, -OH, -NH2, реакційноздатну малеімідо 6 UA 108473 C2 або галогенацетамідогрупу, конкретне, Ме, у разі сполук формули (III): , де R12 означає Н або (С1-С6)алкіл, більш , або І 5 10 що містить групу G=-(CH2)nY, де Y=-Cl, -N3, -OH, -NH2, означає Н або (С1-С6)алкіл, конкретніше, Ме; або І або (iv) реакційноздатну малеімідоабо галогенацетамідогрупу , де R12 означає Н або (С1-С6)алкіл, більш конкретне, Ме. Конкретніше, -SZa може означати -SH або -SS(C1-C6)алкіл, зокрема, -SSMe, або -SSгетероарил, зокрема, або (Х1 і Х2 визначені нижче). Конкретніше, -ZbRb може означати -ОН, -ОСН3, -ОСН2СН=СН2, групу або або 20 25 30 або , в якій Gl означає, принаймні, одну електронно-акцепторну групу, таку як -NO2 або -Hal, зокрема, -F. Мова може йти, наприклад, про наступні групи: 15 , де R12 . Іншим типом групи -С(=О)ZbRb є наступна: або . Реакційноздатні групи -SH і мають хорошу реакційноздатність. Конкретніше, група GCR1 може бути вибрана з тих груп, які описані в прикладах. Як приклад GCR2 можна назвати ε-аміногрупи лізинів, що знаходяться на бічних ланцюгах лізинових залишків, які є на поверхні антитіла, сахаридні групи з’єднувального ланцюга або тіольні групи цистеїнів, що утворюються відновленням дисульфідних міжланцюгових зв’язків (Garnett M.C., et al., Advanced Drug Delivery Reviews 2001, 53, 171-216). Останнім часом з’явилися інші технічні рішення, такі як введення цистеїнів шляхом мутації (Junutula J.R. et al., Nature Biotechnology 2008, 26, 925-932; WO09026274) або введення амінокислот не природного походження іншими хімічними методами (Graaf A.J. et al., Bioconjugate Chem. 2009, Publication Date (Web): лютий, 3, 2009 (Review); DOI: 10.1021/bc800294a; WO 2006/069246 і згідно Chin J.W., et al., JACS 2002, 124, 9026-9027 (технологія ReCode®)). Всі ці варіанти зв’язування з антитілами, що використовуються, можна застосовувати до всіх відомих агентів клітинного зв’язування залежно від їхньої структури. Можна також хімічно модифікувати агент клітинного зв’язування так, щоб можна було ввести нові хімічні реакційноздатні групи GCR2. Так, фахівцеві відомо, яким шляхом можна 7 UA 108473 C2 5 10 15 модифікувати антитіло за допомогою модифікуючого агента (див., зокрема, WO 2005/077090, с.14). Модифікація дозволяє поліпшити реакцію кон’югування і використати більш різноманітні види груп GCR1. Модифікуючі агенти, що дозволяють вводити дисульфідні групи Модифікуючим агентом може бути активований складний ефір NHS формули , в якій R означає групу (С1-С6)алкіл, арил, гетероарил, (С3-С7)циклоалкіл, (С3-С7)гетероциклоалкіл, і ALK означає (С1-С6)алкіленову групу; наприклад, можна використати N-сукцинімідилпіридилтіопропіонат (SPDP) або N-сукцинімідилпіридилтіобутират (SPDB) або Nгідроксисукцинімідиловий складний ефір 4-(2-піридилтіо)бутанової кислоти для того, щоб ввести реакційноздатні дитіопіридильні групи GCR2 (див. Bourdon M.A., et al., Biochem. J. 1978, 173, 723-737; US 5208020), які потім можна ввести у взаємодію з хімічною реакційноздатною групою GCR1 типу -SH, що знаходиться на лінкері похідного криптофіцину, з утворенням нового зв’язку -S-S- (див. приклад 9 кон’югата, що має дисульфідний зв’язок). N-гідроксисукцинімідна група взаємодіє переважно з аміногрупами, що є на антитілі, з утворенням амідних зв’язків. Інший приклад модифікуючого агента описаний в WO 2004/016801 з формулою , або це пегильований аналог формули , описаний у WO 2009/134976, або сульфоновий аналог 20 25 формули , описаний у WO 2009/134977, в яких: - Х3, Х4, Х5, Х6 означають Н або (С1-С6)алкільну групу, - Х1 і Х2 означають -Н, -СОNХ8Х9, -NO2, причому X8 і X9 означають Н або (С1-С6)алкільну групу, + - Х7 означає -SO3-Mабо Н або четвертину амонієву групу, - а означає ціле число від 0 до 4 і b означає ціле число від 0 до 2000, переважно, від 1 до 200; а і b можуть приймати будь-які значення між 0 і 4 або між 0 і 2000, відповідно. Модифікуючі агенти, що дозволяють вводити малеімідні групи Іншим прикладом модифікуючого агента є сукцинімідил-4-(N-малеімідометил)циклогексан-1карбоксилат (SMCC), аналогічна до нього сполука описана в ЕР 0306943, або сульфо-SMCC (сульфосукцинімідил-4-(N-малеімідометил)циклогексан-1-карбоксилат). Як інші приклади можна назвати: 30 , таку, як N-сукцинімідил-3-малеімідопропаноат; , така, як N-сукцинімідил-6-(3-малеімідопропіонамідо)гексаноат; , де b означає ціле число між 0 і 2000, переважно, між 1 і 200 (b може приймати будь-які значення між 0 і 2000), таку, як N-сукцинімідил-3-(2-{2-[3-малеімідопропіоніламіно]етоксі}етокси)пропаноат або SM(ПЕГ)2; , таку, 8 як N-сукцинімідилмалеімідоетилсукцинат; UA 108473 C2 , таку, як N-сукцинімідил-4-(4-малеімідофеніл)бутаноат або, таку, як Nсукцинімідил-3-малеімідобензоат. Модифікуючі агенти, що дозволяють вводити тіольні групи Іншим прикладом модифікуючого агента, описаного в WO 90/06774, є сполука формули 5 10 15 20 , в якій: - Hal означає атом галогену; - Х10 означає атом галогену або групу СООХ 14, нітрогрупу, незаміщений або галогенований (С1-С8)алкіл, незаміщений або галогенований (С1-С8)алкоксил, незаміщений або галогенований (С2-С8)алкеніл, незаміщений або галогенований (С2-С8)алкініл, незаміщений (С3-С8)циклоалкіл, арил, незаміщений або заміщений від одного до трьох замісниками, вибраними з аміно, атома галогену, незаміщеної або галогенованної (С1-С8)алкільної групи, незаміщеного або галогенованого (С1-С8)алкокси; - кожен із Х11, Х12, Х13 означає, незалежно, атом водню або може означати Х 3; - або Х10 і Х11 разом утворюють (С2-С5)алкіленовий цикл, незаміщений або заміщений від однієї до п’яти групи(ами) (С1-С4)алкіл; - або Х10 або Х11 утворюють разом із Х12 (С1-С5)алкіленовий цикл, незаміщений або заміщений від однієї до п’яти групами (С1-С4)алкіл; і Х14 означає -Н або (С1-С8)алкільну групу. Переважно, Hal означає атом хлору або брому. У наведеній нижче таблиці показані можливі значення для Х10-Х13: 9 UA 108473 C2 Переважним прикладом імінотіолану є наступний: . Модифікуючі агенти, що дозволяють вводити галогенацетамідні групи Іншим прикладом модифікуючого агента є сукцинімідил-4-(N-йодацетил)амінобензоат або аналогічні сполуки, серед яких сукцинімідил-N-йодацетат (SIA) (SIAB), 5 (SВAР), 10 , сукцинімідил-N-бромацетат (SВA), або сукцинімідил-3-(N-бромацетамідо)пропіонат або аналогічна пегильована сполука, описана в WO 2009/134976 , де b має зазначені вище значення. На Фігурах 1 і 2 проілюстрований спосіб модифікації аміногрупи агента клітинного зв’язування за допомогою SPDP або переважного вищезазначеного імінотіолану. Таким шляхом можна вводити в агент клітинного зв’язування дисульфідні (-SSR) групи GCR2, зокрема, групи піридилдисульфідні: або , у випадку, коли GCR1 означає -SH. Аналогічно до цього, можна ввести в агент клітинного зв’язування тіольні (SН) групи GCR2, наприклад, за допомогою імінотіолану, у випадку, коли GCR1 означає 15 дисульфід (тобто GCR1=-SZa, де ZaН, наприклад, Za ). В обох випадках ковалентний зв’язок, що утворюється внаслідок реакції між GCR1 і GCR2, являє собою дисульфідний зв’язок, що розщеплюється. Можливо також, у випадку, коли GCR1 означає -SH, ввести на поверхню агента клітинного зв’язування групи GCR2 типу малеімідо йодацетамідо 20 або галогенацетамідо (наприклад, бром- або ). І, навпаки, можна ввести в агент клітинного зв’язування тіольні (-SН) групи GCR2, наприклад, за допомогою імінотіолану, у випадку, коли GCR1 означає або . У цьому випадку, ковалентний зв’язок, що утворюється внаслідок реакції між GCR1 і GCR2, являє собою сульфідний зв’язок, що не розщеплюється. 10 UA 108473 C2 11 UA 108473 C2 5 10 g: число функціональних груп GCR2 на модифікованому агентові клітинного зв’язування; d: число похідних криптофіцину, зв’язаних з агентом клітинного зв’язування MAb L*=такий фрагмент лінкеру L, що містить GCR1=-SZa щоб L=-L*SZa Конкретніше, у випадку, коли GCR1 стосується типу, описаного вище в (iii), можна хімічно модифікувати агент клітинного зв’язування за допомогою відповідного модифікуючого агента або ввести амінокислоту/амінокислоти не природного походження для введення відповідних функціональних груп GCR2. Наприклад: - у випадку функціональної групи -N3: GCR2 може бути групою -CН; - у випадку функціональної групи -ОН або -NH2: GCR2 може бути карбоксильною групою; - у випадку функціональної групи -Cl: GCR2 може бути групою -SH. 12 UA 108473 C2 У випадку, коли GCR1 означає реакційноздатну групу малеімідо або гелогенацетамідо , де R12 означає Н або (С1-С6)алкіл, конкретніше, Ме, похідне криптофіцину може бути представлене нижчеописаною формулою (IIa) або (IIb): 5 (L* означає такий фрагмент лінкеру, щоб L=-L*-малеімідо або L=-L*-галогенацетамідо). Похідним криптофіцину з серії С-52 і С-1 може бути одне з наступних похідних D1-D8: 10 15 або еквівалентна ланка, описана в одному з прикладів. Конкретніше, L знаходиться в пара-положенні до ланки CR1. Спосіб одержання похідних криптофіцину Сполуку формули (II) одержують відповідно до Схеми 1 з похідного криптофіцину формули (III) і попередника лінкеру (PL): 13 UA 108473 C2 5 10 15 20 25 30 Схема 1 G означає групу -СН=СН2, -(СН2)nY або -(C1-C6)алкілен-Y, де n є цілим числом від 1 до 6, і Y означає -OH, -SH, -Cl, -OGP, де GP означає відхідну групу, таку як, наприклад, мезилатна (OMs) або тозилатна група, або Y означає -N3, -NH2, -COOH, -NR12-СН2-ССН, в якій R12 означає Н або (С1-С6)алкільну групу, конкретніше, метильну групу. Попередник лінкеру PL виконує роль, що полягає у введенні лінкеру L у похідне криптофіцину після взаємодії групи G з хімічною функціональною групою, що знаходиться на PL. G може також означати групу (тобто Y означає групу з 9 наступних груп (R12 і R12 означають Н або (С1-С6)алкільну групу): ), вибирану або -(CH2)n-SH. Відповідно до Схеми 1 для одержання похідного криптофіцину (II) з похідного криптофіцину (III) можуть бути необхідні декілька стадій і/або реакцій. Так, наприклад, у випадку, коли Z a=Н, віддають перевагу введенню лінкеру L, в якому Za=-S(C1-C6)алкіл, використовуючи відповідний попередник лінкеру, потім відновлюють дисульфідну функціональну групу -SS(C1-C6)алкіл до тіольної функціональної групи -SH. Для цього можна використати, наприклад, ТСЕР: у зв’язку з цим див. Burns J.A., et al., J.Org.Chem. 1991, 56(8), 2648-2650. Це перетворення -SS(C1-C6)алкіл -SH може застосовуватися, наприклад, до лінкеру L1-4 і L21-23 Таблиці II. Аналогічно, у випадку, коли ZbRb , можна вводити лінкер L, в якому ZbRb=-O-аліл, із використанням відповідного попередника лінкеру, потім видаляють захист із групи -СООН і вводять групу . Видалення захисту може бути здійснене обробкою паладієвим каталізатором, наприклад, Pd(PPh3)4, у присутності аміну-“поглинача”, наприклад, морфоліну; активацію можна здійснити N,N-дисукцинімідилкарбонатом у присутності основи, наприклад, DIPEA, або за допомогою NHS у присутності сполучального агента, наприклад, DCC. Це перетворення однієї групи ZbRb в іншу групу ZbRb (наприклад, -О-аліл ) може бути застосоване для одержання інших груп ZbRb, зокрема, груп, описаних вище. У випадку, коли R1 означає атом галогену і R2 – ацильну групу, переважно одержати спочатку сполуку формули (II), в якій R2 означає групу -ОН (після введення лінкеру) і потім ввести ацильну групу за допомогою відповідної сполуки, що ацилює. Схеми 1 і 1 ілюструють також одержання похідного криптофіцину, що включає лінкер, який містить відповідно групу малеімідо або галогенацетамідо (L* означає такий фрагмент лінкеру L, щоб L=-L*-малеімідо або L=-L*-галогенацетамідо). 14 UA 108473 C2 Схема 1 5 10 15 20 25 30 35 40 45 Схема 1 Ці похідні одержують взаємодією похідного криптофіцину, що включає лінкер L, що містить аміно- або тіольну групу, із модифікуючим агентом, що дозволяє ввести відповідно малеімідоабо галогенацетамідогрупу. Приклади реакцій між групою G і хімічною функціональною групою, що знаходиться на PL - реакція нуклеофільного заміщення між попередником лінкеру PL, що несе аміногрупу -NH(може бути використана також сіль аміну) і G=-(CH2)nCl або -(CH2)nOMs (див. наприклад, Таблицю II, PL1-4, PL7a, PL8-10, PL21-23): цю реакцію можна провести в полярному апротонному розчиннику в присутності основи, такої, як, наприклад, TEA або DIPEA. Див. приклад 1, сполука 7 або приклад 15, сполука 48; - реакція ацилування між попередником лінкеру PL, що несе функціональну карбамоїлгалогенідну групу, і G=-(CH2)nОН (див. наприклад, Таблицю II, PL5): цю реакцію можна вести в полярному апротонному розчиннику в присутності амінної основи, такої, як, наприклад, TEA. Відповідно до варіанту можна також здійснити реакцію між попередником лінкеру PL, що несе функціональну аміногрупу -NH-, і G=-(CH2)nО-C(=О)-О-(4-нітрофеніл), одержаним із G=(CH2)nОН і п-нітрофенілхлорформіату (активація спирту у формі карбонату) відповідно до схеми, представленої нижче: (R12=Н або (C1-C6)алкіл): -NHR12 + крипто-(СН2)nО-C(=О)-О-(4-нітрофеніл) крипто-(CH2)nО-C(=О)-NR12- активація спирту в формі карбонату може бути також використана для здійснення реакції між попередником лінкеру, що несе функціональну групу -ОН, і G=-(CH2)nNH2 або -(СН2)nОН для одержання, відповідно, карбаматної (-ОС(=О)-NH-) або карбонатної (-ОС(=О)-О-) функціональної групи відповідно до наступних схем: -О-С(=О)-О-(4-нітрофеніл) + крипто-(СН2)nNH2 крипто-(СН2)nNH-C(=О)-O-OH + крипто-(CH2)nО-С(=О)-О-(4-нітрофеніл) крипто-(СН2)nО-C(=О)-O(див. наприклад, Таблицю II, PL6a-6b, PL24-25) - реакція етерифікації між попередником лінкеру PL, що несе функціональну кислотну групу СООН, і G=-(СН2)nОН (див. наприклад, Таблицю II, PL14b): цю реакцію можна вести в полярному апротонному розчиннику в присутності амінної основи, такої як, наприклад, DMAP, і сполучного агента, наприклад, DCC; - реакція амідування між попередником лінкеру PL, що несе функціональну кислотну групу СООН, і G=-(СН2)nNН2 (див. наприклад, Таблицю II, PL14a): цю реакцію можна вести в полярному апротонному розчиннику в присутності сполучного агента, наприклад, EDCl або HOBt; - реакція амідування між попередником лінкеру PL, що несе функціональну групу -NН2, і G=(СН2)nCOOH (див. наприклад, Таблицю II, PL7c): цю реакцію можна вести в полярному апротонному розчиннику в присутності сполучного агента, наприклад, EDCl або HOBt; - 1,3-диполярна циклоприєднання (у хімії називають також “click" реакцією), реакція між попередником лінкеру PL, що несе термінальну алкінову функціональну групу, і G=-(СН2)nN3, або між попередником лінкеру PL, що несе азидну функціональну групу, і G=-(СН2)nNR12CH2CCH (див. наприклад, Таблицю II, PL 15-18): цю реакцію можна вести в полярному розчиннику в присутності Cu(I) як каталізатора (див. циклоприєднання за Хьюзгеном: Rostovtsev V.V., et al., Angew.Chem.Int.Ed. 2002, 41, 2596-2599; Tornoe C.W., et al., J.Org.Chem. 2002, 67, 15 UA 108473 C2 5 10 15 20 25 30 35 40 45 50 55 3057-3064); - метатезис, реакція між попередником лінкеру PL, що несе термінальну етиленненасичену функціональну групу, і G=-СН=СН2 (див. наприклад, Таблицю II, PL19, PL20): цю реакцію можна го вести в полярному апротонному розчиннику в присутності каталізатора Грубса 2 покоління (CAS №246047-72-3, див. про цю реакцію Poeylaut-Palena A.A. et al., J.Org.Chem. 2008, 73, 20242027). Про лінкер L Лінкер L може бути вибраний із наступних сполук: -GX(CR13R14)t(OCH2CH2)у(CR15R16)uQGCR1; -GX(CR13R14)t(OCH2CH2)yY-(CR15R16)uQGCR1; -GX(CR13R14)t(CR17=CR18)(CR15R16)u(OCH2CH2)yQGCR1; -GX(CR13R14)t(OCH2CH2)у(CR17=CR18)(CR15R16)uQGCR1; -GX(CR13R14)t-феніл-(CR15R16)uYQGCR1; -GX(CR13R14)t-фурил-(CR15R16)uYQGCR1; -GX(CR13R14)t-оксазоліл-(CR15R16)uYQGCR1; -GX(CR13R14)t-тіазоліл-(CR15R16)uYQGCR1; -GX(CR13R14)t-тієніл-(CR15R16)uYQGCR1; -GX(CR13R14)t-імідазоліл-(CR15R16)uYQGCR1; -GX(CR13R14)t-піперазиніл-СО(CR15R16)uYQGCR1; -GX(CR13R14)t-піперидинілметил-NH12-CO(CR15R16)uYQGCR1; -GX(CR13R14)t-піперидиніл-(CR15R16)uYQGCR1; -GX(CR13R14)t-піперидиніл-NR12-(CR15R16)uYQGCR1; -GX(CR13R14)t-триазоліл-(CR15R16)uYQGCR1; -GX(CR13R14)t-триазоліл-(CR15R16)uYQGCR1; -GX(CR13R14)t-феніл-(CR15R16)uQGCR1; -GX(CR13R14)t-фурил-(CR15R16)uQGCR1; -GX(CR13R14)t-оксазоліл-(CR15R16)uQGCR1; -GX(CR13R14)t-тіазоліл-(CR15R16)uQGCR1; -GX(CR13R14)t-тієніл-(CR15R16)uQGCR1; -GX(CR13R14)t-імідазоліл-(CR15R16)uQGCR1; -GX(CR13R14)t-піперазиніл-(CR15R16)uQGCR1; -GX(CR13R14)t-піперидиніл-(CR15R16)uQGCR1; -GX(CR13R14)t-піперидинілметил-NR12-(CR15R16)uQGCR1; -GX(CR13R14)t-піперидиніл-NR12-(CR15R16)uQGCR1; -GX(CR13R14)t-триазоліл-(CR15R16)uQGCR1; або -GY(CR13R14)t(OCH2CH2)у(CR15R16)uQGCR1; -GY(CR13R14)t(OCH2CH2)y-Y-(CR15R16)uQGCR1; -GY(CR13R14)t(CR17=CR18)(CR15R16)u(OCH2CH2)yQGCR1; -GY(CR13R14)t(OCH2CH2)у(CR17=CR18)(CR15R16)uQGCR1; -GY(CR13R14)t-феніл-(CR15R16)uYQGCR1; -GY(CR13R14)t-фурил-(CR15R16)uYQGCR1; -GY(CR13R14)t-оксазоліл-(CR15R16)uYQGCR1; -GY(CR13R14)t-тіазоліл-(CR15R16)uYQGCR1; -GY(CR13R14)t-тієніл-(CR15R16)uYQGCR1; -GY(CR13R14)t-імідазоліл-(CR15R16)uYQGCR1; -GY(CR13R14)t-піперазиніл-СО(CR15R16)uYQGCR1; -GY(CR13R14)t-піперидинілметил-NR12-СО(CR15R16)uYQGCR1; -GY(CR13R14)t-піперидиніл-(CR15R16)uYQGCR1; -GY(CR13R14)t-піперидиніл-NR12-(CR15R16)uYQGCR1; -GY(CR13R14)t-триазоліл-(CR15R16)uYQGCR1; -GY(CR13R14)t-феніл-(CR15R16)uQGCR1; -GY(CR13R14)t-фурил-(CR15R16)uQGCR1; -GY(CR13R14)t-оксазоліл-(CR15R16)uQGCR1; -GY(CR13R14)t-тіазоліл-(CR15R16)uQGCR1; -GY(CR13R14)t-тієніл-(CR15R16)uQGCR1; -GY(CR13R14)t-імідазоліл-(CR15R16)uQGCR1; 16 UA 108473 C2 5 10 15 20 25 30 -GY(CR13R14)t-піперазиніл-(CR15R16)uQGCR1; -GY(CR13R14)t-піперазиніл-(CR15R16)uQСCR1; -GY(CR13R14)t-піперидиніл-(CR15R16)uQGCR1; -GY(CR13R14)t-піперидинілметил-NR12-(CR15R16)uQGCR1; -GY(CR13R14)t-піперидиніл-NR12-(CR15R16)uQGCR1; -GY(CR13R14)t-тpиазоліл-(CR15R16)uQGCR1; G позначає групу -СН=СН- або -(СН2)n-; G позначає групу -(СН2)n-; n позначає ціле число від 1 до 6; Х позначає простий зв’язок або групу -СО-, -СОО- або -СОNR12-, причому група СО зв’язана з G; Y позначає групу -О-, -ОСО-, -ОСОО-, -ОСОNR12-, -NR12-, -NR12CO, -NR12CONR12-, NR12COO- або -S(О)q-, атом О або групу NR12, зв’язану з G; Y позначає групу -О-, -ОСО-, -ОСОО-, -ОСОNR12-, -NR12-, -NR12CO-, -NR12CONR12-, NR12COO-, -S(О)q-, -CO-, -COО- або -CONR12R12, R12, R13, R14, R15 і R16, R17 і R18 означають, незалежно один від одного, Н або (С1С6)алкільну групу; t, u і у позначають цілі числа від 0 (коли група відсутня) до 20, причому t+u+у повинна бути вищою або дорівнювати 1; q позначає ціле число, що означає 0, 1 або 2; Q позначає простий зв’язок або (С1-С10)алкіленову групу або (ОСН2СН2)i, де i позначає ціле число від 1 до 20, конкретніше, від 1 до 10, ще конкретніше, від 1 до 8 або від 1 до 6, і ще конкретніше, від 2 до 5. Символ i може приймати будь-яке зі значень у зазначених діапазонах, зокрема, 2, 3, 4 або 5. У випадку, коли використовують лінкер формули -GY(CR13R14)t(OCH2CH2)у -Y(CR15R16)uQGCR1 і якщо у означає 0 (відсутність ПЕГ-групи) і Q означає простий зв’язок, тоді u не може дорівнювати 0. Конкретніше, виключені лінкер, що включають кінцеву ланку -NR12C(=О)-О-(Y=NR12; u означає 0; Q означає простий зв’язок і GCR1=-C(=О)ZbRb). у позначає ціле число від 0 до 20, конкретніше, від 1 до 20, ще конкретніше, від 1 до 10, від 1 до 8 або від 1 до 6, і ще конкретніше, від 2 до 5. Символ у може приймати будь-які зі значень у зазначених діапазонах, зокрема, 2, 3, 4 або 5. Деякі з цих лінкерів описані в заявках WO 07085930 і WO 09016516. Лінкер L може бути вибраний із лінкеру формули (IV): 40 , в якій: - (AA)w означає послідовність із w амінокислот AA, сполучених між собою пептидними зв’язками; - w позначає ціле число від 1 до 12, переважно, від 1 до 6; - n позначає ціле число від 1 до 6; - D позначає одну з наступних ланок: 45 в яких: R12 позначає Н або (С1-С6)алкільну групу; R19, R20, R21, R22 позначають, незалежно один від одного, Н, атом галогену, -ОН, -CN або (С1С4)алкільну групу; 35 17 UA 108473 C2 5 10 15 20 25 Т, зв’язаний із (СН2)n, позначає NR12 або О; V1 позначає О, S, NR12; V2 позначає CR22 або N; V3, V4, V5 вибрані, незалежно один від одного, із CR22 або N. Прикладом D2 є наступна ланка: . АА позначає амінокислоту природного або не природного походження, конкретніше, вибрану з: аланіну (Ala), β-аланіну, 2-аміно-2-циклогексилоцтової кислоти, 2-аміно-2-фенілоцтової кислоти, аргініну (Arg), аспартамової кислоти (Asp), цистеїну (Cys), глутаміну (Gln), глутамінової кислоти (Glu), гліцину (Gly), гістидину (His), ізолейкіну (Ile), лейкіну (Leu), лізину (Lys), метіоніну (Met), фенілаланіну (Phe), проліну (Pro), серину (Ser), треоніну (Thr), триптофану (Trp), тирозину (Tyr), валіну (Val), γ-аміномасляної кислоти, α,α-диметил-γ-аміномасляної кислоти, β,β-диметилγ-аміномасляної кислоти, орнітину (Orn), цитруліну (Cit). Послідовність (AA)w має формулу: , в якій R23 означає залишок однієї з амінокислот, описаних вище. Прикладами послідовностей є наступні: Gly-Gly, Phe-Lys, Val-Lys, Val-Cit, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Ala-Lys, Val-Cit, Phe-Cit, Leu-Cit, Ile-Cit, Trp-Cit, Phe-Ala, Ala-Phe, Gly-Gly-Gly, Gly-Ala-Phe, Gly-Val-Cit, Gly-Phe-Leu-Cit, Gly-Phe-Leu-Gly, Ala-LeuAla-Leu. Попередниками лінкерів є такі, які містять відповідну ОН-вмісні ланцюги: . WO 2005/082023 (див., зокрема, с.61-64) описує способи одержання деяких попередників лінкерів. Способи одержання попередників лінкерів PL25 і PL26, описані нижче, можуть бути також використані для одержання інших аналогічних попередників лінкерів, що містять іншу послідовність (AA)w. Лінкер L може бути також вибраний із тих, які описані в Таблиці II або зі сполук, описаних у прикладах. У всіх формулах лінкерів група NR12 або NR12 означає, конкретніше, NH або NMe. Одержання сполук формули (III), коли G=-(CH2)nOH або -CH=CH2 18 UA 108473 C2 5 10 15 20 25 30 35 40 Схема 2 Р1 одержують згідно з відомостями, що містяться в заявках WO 98/08505, WO 00/23429 і WO 00/34252, а також в наступних публікаціях: Rej R., et al., J. Org. Chem. 1996, 61, 6289-6295; Salamonczyk G.M., et al., J. Org. Chem. 1996, 61, 6893-6900 або J. Med. Chem. 1999, 42(14), 25882603 (включені в опис як посилання). На сторінках 158-159 публікації “The isolation, characterization and development of а novel class of potent antimitotic macrocyclic depsipeptides: the cryptophycins”, Розділ 9, в “Anticancer agents from natural products”, Taylor&France, CRC press book, isbn=0-8493-1863-7, дані схеми синтезу, що дозволяє одержати різні фрагменти (А, В, С і D) криптофіцину та одержати в результаті Р1. Авторами Rej R., et al., J. Org. Chem. 1996, 61, 6289-6295 зображений на схемах 1-6 шлях одержання одного з похідних криптоміфіцину згідно з Фігурою 1, однак ці схеми можуть бути застосовні у разі одержання Р 1 з використанням йодинових початкових реагентів. Р1 дозволяє одержати інші похідні криптофіцину за допомогою стадій, детально описаних нижче; Стадія (i): розкриття епоксидного циклу Р1 у кислому середовищі з одержанням діольної функціональної групи. Можна використати, наприклад, концентровану перхлорну кислоту; Стадія (ii): окисне розщеплення діолу за допомогою, наприклад, періодату натрію; Стадія (iii): реакція Вітіга, що використовує відповідний галогенід фосфонію, наприклад, бромід, і сильну основу, таку, як, наприклад, BuLi; Стадія (iv): реакція епоксидування Корі-Чайковського з використанням хіральної солі сульфонію, наприклад, трифлату, у присутності основи, такої, як, наприклад, КОН; Стадія (v): зняття захисту з силілованого простого ефіру, використовуючи, наприклад, розчин тетрабутиламонійфториду. Бромід 4-(триізопропілсилоксиметил)бензилтрифенілфосфонію одержують з 1-(бромметил)4-(триізопропілсилоксиметил)бензолу (CAS№ 934667-38-6), одержання якого з 1,4бензолдиметанолу (CAS№ 589-29-7, ринковий продукт) описане Potter R.G., et al., Organic Letters 2007, 9(7), 1187-1190. Сполуки, в яких R11 означає (С1-С4)алкільну групу, одержують аналогічним способом, виходячи з відповідного діолу, який або є ринковим продуктом, або одержують С-алкілуванням за Фріделем-Крафтсом із 1,4-бензолдиметанолу. Виходячи з 1-(бромметил)-4-(триізопропілсилоксиметил)бензолу (CAS№ 135408-73-0), одержання якого описане на схемі 4а патенту ЕР 0496548, або на сторінці 83 статті Nevill C.R.Jr., et al., Bioorganic & Med. Chem. Lett. 1991, 1(1), 83-86, можна одержати відповідний бромід фосфонію. Сполуки, в яких R11 означає (С1-С4)алкільну групу, одержують аналогічним способом, виходячи зі сполуки, еквівалентної сполуці 1, описаній на сторінці 83 статті Nevill C.R.Jr., et al., Bioorganic & Med. Chem. Lett. 1991, 1(1), 83-86, яка або є ринковим продуктом, або одержують С-алкілуванням за Фріделем-Крафтсом з п-толуолоцтової кислоти. Трифторметансульфонат (1R,4R,5R,6R)-4,7,7-триметил-6-(4-вінілбензил)-6тіоніабіцикло[3.2.1]октану, що використовується на стадії (iv), одержують із (1R,4R,5R)ізотіоцинеолу (див. Aggarwal V. et al., JACS 2010, 132, 1828-1830), одержання якого з (R) 19 UA 108473 C2 5 10 15 20 25 30 лимонену (CAS № 95327-98-3), ринковий продукт) описано в цьому ж самому посиланні. Бромід трифеніл(п-вінілбензил)фосфонію (CAS № 118766-51-1) одержують з відповідного бромпохідного (див. Drefahl G., et al., Chem.Ber. 1961, 94(8), 2002-2010), одержання якого з 4винилбензилового спирту (CAS № 1074-61-9, ринковий продукт) описане в статті Shimomura Про., et al., Tetrahedron 2005, 61, 12160-12167. Виходячи з Р7 або Р8, які є сполуками формули (III), в яких G=-(CH2)n ОН, можна одержати інші сполуки формули (III), що мають інші групи G. випадок, коли G=-(CH2)nCl або -(CH2)nN3 Схема 3 Виходячи з групи G=-CH2OH, можна одержати групи G=-CH2Cl або -CH2N3: - введення -Cl може бути здійснене в присутності CMS: див. приклад 1, сполука 2; - азидування може бути здійснене в присутності дифенілфосфоразиду (PhO) 2P(=О)N3 і основи, наприклад, DBU. Схема 3 описує ці реакції для випадку, коли n=1, але спосіб може бути також застосований для випадку, коли n>1. випадок, коли G=-(CH2)nCООН Схема 4 Виходячи з групи G=-CH2OH, можна одержати групу G=-CH2CООН шляхом окислення. Схема 4 описує подвійне окислення: 1 окислення за допомогою реагенту Дес-Мартіна (див. “Encyclopedia of Reagents for Organic Synthesis”; Paquette L.A., Ed.; Wiley: Chichester, UK, 1995, т.7, 4982-4987 або Boeckman R.K.Jr., et al., J.J. “The Dess-Martin Periodinane” Org. Synth. 2004, 10, 696-702), і подальше 2 окислення по типу Pinnick у присутності 2-метил-2-бутену (Pinnick H.W., Tetrahedron 1981, 37, 2091-2096). Схема 4 описує ці реакції у разі використання вихідної сполуки, коли n=2, але цей спосіб застосовний також для n>2. випадок, коли G=-(CH2)nNН2 Схема 5 Виходячи з групи G=-CH2N3, одержання якої описане на Схемі 3, можна одержати групу G=CH2NН2 за допомогою реакції відновлення, використовуючи фосфін, такий як ТСЕР. Див. про цю реакцію: Faucher A.-M. еt al., Synthetic Comm 2003, 33, 3503-3511: 20 UA 108473 C2 5 10 15 20 Схема 5 Згідно з варіантом, виходячи з групи G=-CH2OH, можна одержати групу G=-CH2NН2 за допомогою реакції Міцунобу, використовуючи трифенілфосфін і DEAD. Про цю реакцію див. Mitsunobu ПРО., Synthesis 1981, 1-28; Hughes D.L., Org. Reactions 1992, 42, 335-656; Hughes D.L., Org. Prep. 1996, 28, 127-164. Схеми 5 і 5 описують випадок, коли n=1, але вони можуть бути застосовними також для n>1. випадок, коли G=-(CH2)nNR12-CH2CCH Виходячи з групи G=-(CH2)nCl, можна одержати групу G=-(CH2)n-NR12-CH2-CCH за допомогою нуклеофільного заміщення, використовуючи сполуку формули NHR 12-CH2-CCH (R12=Н: пропаргіламін; R12=(C1-C6)алкіл: одержано відповідно до Mock W.L., et al., J.Org.Chem. 1989, 54,(22), 5302-8). випадок, коли G=-(CH2)n-SН Схема 6 Виходячи з групи G=-(CH2)nCl, можна одержати групу G=-(CH2)nSН прямою функціоналізацією за допомогою триметилсилілтіолату тетрабутиламонію, що одержується in situ з тетрабутиламонійфториду і гексаметилдисилатіану згідно Hu J. et al., J. Org. Chem. 1999, 64, 4959-4961 (див. приклад 8). Схема 6 описує цю реакцію для випадку, коли n=1, але спосіб може бути застосованим також для n>1. У процесі цієї реакції може утворитися проміжний димер формули: випадок, коли G=-ALK-SН 25 30 Схема 7 Р3 дозволяє одержати інші похідні криптофіцину згідно зі Схемою 7: Стадія (i): реакція Вітіга з використанням придатного галогеніду фосфонію наприклад, броміду, і сильної основи, наприклад BuLi; Стадія (ii): поєднання Кумади з використанням придатного реактиву Гріньяра, наприклад, 21 UA 108473 C2 5 10 15 броміду алкоксимагнію, захищеного в формі силілованого простого ефіру, у присутності паладієвого або нікелевого каталізатора (див., наприклад, Organic Letters 2009, 11, 5686-5689 або Synthesis 2009, 141, 2408-2412). Стадії (iii)-(v) описані на Схемі 2, а стадія (vi) описана на Схемі 6. Бромід (4-бромбензил)трифенілфосфонію є ринковим продуктом (CAS № 51044-13-4). Броміди алкоксимагнію, захищені в формі силілованого простого ефіру, можуть бути одержані з відповідних бромспиртів шляхом захисту спиртової групи відповідним хлорсиланом із подальшим одержанням магнійорганічної сполуки в присутності магнію, в апротонному полярному безводному розчиннику, такому як ТГФ (див., наприклад, Organic Letters 2005, 7, 183-186). Бромспирти, лінійні або розгалужені, що містять 1-6 атомів вуглецю, є комерційно доступними, такі як 3-бром-1-пропанол (CAS №627-18-9) або 1-бром-2-пропанол (CAS № 1968673-8), або можуть бути одержані з відповідних складних бромефірів або бромкетонів згідно зі способами, описаними в літературі. Хлорсиланом може бути, наприклад, третбутилдиметилхлорсилан (CAS № 18162-48-6) або триізопропілхлорсилан (CAS № 13154-24-0). випадок, коли G=-(CH2)n-малеімідо Схема 8 У доповнення до Схеми 1, яка описує спосіб одержання похідних криптофіцину, що містить 20 25 малеімідну ланку, і виходячи з групи G=-CH2OH, можна одержати групу G= , здійснюючи реакцію Міцунобу в присутності трифенілфосфіну і DEAD згідно Matuszak N. et al., J. Med. Chem. 2009, 52, 7410-7420. Схема 8 описує цю реакцію для випадку, коли n=1, але вона застосовна і до випадку, коли n>1. На Схемах 1-8, представлених вище, лінкер знаходиться в пара-положенні, однак ці схеми однаково дійсні для лінкерів в орто- або мета-положеннях. Аналогічно до цього, хоч ці схеми наведені для похідного криптофіцину, вони застосовні для одержання інших похідних формули (II), зокрема, D1-D8. Зокрема, у випадку С-52 можна використати наступні сполуки, одержання яких описане в Alawar R.S., et al., J. Med. Chem. 2003, 46, 2985-3007 або в WO 9808505: G=-CH2OH: сполука 31b схеми 5 G=-CH2CH2OH: сполука 49 схеми 9 G=-CH2COOH: сполука 51 схеми 9 або приклад 81 у WO 9808505 G=-C(=О)Н: приклад 80 у WO 9808505 30 35 40 З іншого боку, виходячи зі сполуки 31b, в якій G=-CH2OH, можна одержати сполуки, в яких G=-CH2Cl або -CH2N3: - G=-CH2Cl: див. приклад 1, сполука 2; - G=-CH2N3: конверсія -CH2OH в -CH2N3 може бути здійснена в полярному апротонному розчиннику в присутності дифенілфосфоразиду та основи, такої як DBU, див. приклад 19, сполука 60. - G=-CH2малеімідо: конверсія -CH2OH у -CH2малеімідо може бути здійснена в полярному апротонному розчиннику в присутності малеіміду, трифенілфосфіну і DEAD. Відомості, викладені в J. Med. Chem. 2003, 46, 2985-3007, можуть бути застосовані для одержання інших похідних криптофіцину, що містять інші замісники R 6-R9. Одержання попередників лінкеру PL PL може бути одним з наступних попередників: 22 UA 108473 C2 PL1 5 10 15 20 25 30 35 40 45 , що одержують згідно з нижче описаною схемою: . Стадія (i): активація кислоти за допомогою NHS; активацію проводять при КТ у присутності сполучного агента, такого як, наприклад, гідрохлорид 1-(3-диметиламінопропіл)-3етилкарбодиіміду, розчиненого в безводному апротонному розчиннику, такому як DCM. Можна використати умови прикладу 1 одержання сполуки 4. Стадія (ii): амідування N-Boc-піперидином; пептидне поєднання здійснюють у полярному апротонному розчиннику при КТ у присутності основи, якою може бути третинний амін, такий як ТЕА або DIPEA. Розчинником може бути DMF. Можна використати умови прикладу 1 для одержання сполуки 5. Стадія (iii): реакція зняття захисту з аміну за допомогою розчину кислоти, наприклад, соляної кислоти (наприклад, розчиненої в діоксані). Можна використати умови прикладу 1 одержання сполуки 6. Вихідна кислота, наприклад, 4-метил-4-(метилдитіо)-пентанова кислота, може бути комерційно доступна або одержана з галогеновмісної карбонової кислоти шляхом послідовних обробок тіоацетатом калію і похідним типу метантіосульфонату. Див. також US 2719170. PL2, що одержується згідно з нижчеописаною схемою: Стадія (i): відновне амінування за допомогою альдегіду; реакцію здійснюють при КТ у безводному полярному апротонному розчиннику, такому як THF, у дві стадії: утворення проміжного комплексу в присутності ізопропоксиду титану, потім відновлення in situ відновним агентом, таким як, наприклад, ціанборгідрид натрію. Можна використати умови прикладу 5 одержання сполуки 17. Стадія (ii): реакція зняття захисту з аміну за допомогою розчину кислоти, наприклад, соляної кислоти (наприклад, розчиненої в діоксані). Можна використати умови прикладу 5 одержання сполуки 18. Вихідний альдегід, наприклад, 2-метил-2-(метилдитіо)пропаналь, може бути комерційно доступний або одержаний окисленням спирту, що несе дисульфідну ланку, що одержується з галогеновмісного спирту, захищеного належно (наприклад, у формі силілованого простого ефіру), внаслідок послідовних обробок тіоацетатом калію і похідним типу метантіосульфонату. PL3 ZaS-ALK-NHR12, що одержується згідно з нижчеописаною схемою: у випадку, коли R12=Н Стадія (i): утворення оксиму; описаний вище альдегід, розчиняють у полярному протонному розчиннику, такому як етанол, потім обробляють гідрохлоридом О-метилгідроксиаміну при нагріванні зі зворотним холодильником у присутності основи, такої як гідроксид натрію. Можна використати умови прикладу 3 одержання сполуки 11. Стадія (ii): відновлення оксиму; оксим відновлюють обробкою при нагріванні зі зворотним холодильником розчином диметилсульфідборану в безводному полярному апротонному розчиннику, такому як THF. Можна використати умови прикладу 3 одержання сполуки 12. у випадку, коли R12Н Стадія (i): відновне амінування за допомогою альдегіду; реакцію здійснюють при КТ у безводному полярному апротонному розчиннику, такому як THF, у присутності відновного агента, такого як, наприклад, триацетоксиборгідрид натрію. PL4, що одержується згідно з нижчеописаною схемою: 23 UA 108473 C2 5 10 15 20 25 30 35 40 45 50 Цей лінкер одержують аналогічно способу, описаному для PL2. Стадія (i): відновне амінування за допомогою альдегіду; реакцію здійснюють при КТ у безводному полярному апротонному розчиннику, такому як THF, у дві стадії: утворення проміжного комплексу в присутності ізопропоксиду титану, потім відновлення in situ відновним агентом, таким як, наприклад, ціанборгідрид натрію. Можна використати умови прикладу 5 одержання сполуки 17. Стадія (ii): реакція зняття захисту з аміну за допомогою розчину кислоти, наприклад, соляної кислоти (наприклад, розчиненої в діоксані). Можна використати умови прикладу 5 одержання сполуки 18. PL5 , що одержується згідно з нижчеописаною схемою: Стадія (i): зняття захисту з аміну; реакцію здійснюють при КТ у полярному апротонному розчиннику, такому як DCM, обробкою аміну дитрет-бутилдикарбонатом у присутності основи, такої як, наприклад, ТЕА. Стадія (ii): перетворення спирту в бромід; реакцію здійснюють при КТ в полярному апротонному розчиннику, такому як, THF, обробкою спиртової функціональної групи за допомогою CBr4 у присутності фосфіну, наприклад, трифенілфосфіну; див. про це Appel R. Angew. Chem. Int. Ed. Engl. 1975, 14, 801-811 або Desmaris N., et al., Tetrahedron Letters 2003, 44(41), 7589-7591. Стадія (iii): заміщення броміду тіоацетатом; реакцію здійснюють при КТ у безводному полярному апротонному розчиннику, такому як DMF, використовуючи як нуклеофілу тіоацетат калію. Стадія (iv): утворення дисульфідного зв’язку; реакцію здійснюють у полярному протонному безводному розчиннику, такому як метанол, у присутності основи, такої як, наприклад, метанолят натрію, і реагенту, що містить піридилдисульфідну ланку. Згідно з варіантом: Стадія (v): активація спирту у формі мезилату; реакцію здійснюють у полярному апротонному безводному розчиннику, такому як DCM, обробкою мезилхлоридом у присутності основи, такої як, наприклад, ТЕА. Стадія (vi): утворення вільного тіолу; реакцію здійснюють при нагріванні зі зворотним холодильником у полярному протонному розчиннику, такому як суміш етанолу/вода, у дві стадії, здійснювані послідовно: заміщення мезилату на тіосечовину, потім гідроліз in situ солі ізотіоуронію шляхом додавання основи, такої як NaOH. Стадія (vii): активація тіолу у формі піридилдисульфіду; реакцію здійснюють при КТ у полярному протонному розчиннику, такому як етанол, при обробці реагентом, що містить піридил-дисульфідну ланку, у присутності кислоти, такої як оцтова кислота. Стадія (viii): зняття захисту з аміну за допомогою розчину кислоти, наприклад, соляної кислоти (наприклад, розчиненої в діоксані). Стадія (ix): активація аміну в формі карбамоїлхлориду; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як DCM, шляхом обробки дифосгеном у присутності основи, такої як ТЕА. PL6 RbZb-OC-ALK-(OCH2CH2)i-OH, що одержують згідно з нижчеописаною схемою: у випадку, коли ALK=CH2CH2 шлях А: шлях В: Стадія (i): зняття захисту за допомогою розчину соляної кислоти (наприклад, розчину в діоксані) або трифтороцтової кислоти. Стадія (ii): захист карбонової кислоти в формі складного алілового ефіру; реакцію 24 UA 108473 C2 5 10 15 20 здійснюють при КТ у полярному апротонному розчиннику, такому як, DMF, у присутності алілброміду та основи, такої як карбонат калію. Стадія (iii): елонгація ПЕГ ланцюга; реакцію здійснюють у полярному апротонному безводному розчиннику, такому як THF, шляхом обробки ненасиченої кислоти, захищеної в формі складного ефіру, алкоголятом, що генерується під дією натрію в каталітичній кількості. у випадку, коли ALKCH2CH2 Стадія (iv): елонгація ПЕГ ланцюга; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як THF або DMF, шляхом обробки галогенованого складного ефіру алкоголятом ПЕГ діолу, монозахищеного у формі простого ефіру тетрагідропірану (ТНР). Одержання цього типу монозахищеного ПЕГ діолу описане в літературі, див., наприклад, Richard A. et al., Chem. Eur. J. 2005, 11, 7315-7321 або Sakellariou E.G., et al., Tetrahedron 2003, 59, 9083-9090. ПЕГ спирти, що містять кислотну функціональну групу, захищену в формі складного третбутилового ефіру, комерційно доступні (такий як трет-бутил-12-гідрокси-4,7,10триоксадодеканоат) або їх одержують із трет-бутилакрилату і ПЕГ діолу. Початкові ПЕГ діоли комерційно доступні для i=3-12. PL7 RbZb-OC-ALK-(OCH2CH2)i-NHR12, що одержується згідно з нижчеописаними схемами: у випадку, коли ALK=CH2CH2 випадок, коли R12=Н випадок, коли R12Н 25 у випадку, коли ALKCH2CH2 випадок, коли R12=Н випадок, коли R12Н 30 Стадія (i): захист карбонової кислоти у формі складного алілового ефіру; реакцію здійснюють при КТ у полярному апротонному розчиннику, такому як, DСM, у присутності алілового спирту, що поєднує агента, такого як EDCl, і основи, такої як DMAP. Можна використати умови прикладу 14 одержання сполуки 42. 25 UA 108473 C2 5 10 15 20 Стадія (ii): зняття захисту за допомогою розчину соляної кислоти (наприклад, розчину в діоксані) або трифтороцтової кислоти. Можна використати умови прикладу 14 одержання сполуки 43. Стадія (iii): алкілування атома азоту; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як THF, шляхом обробки основою, такою як NaH, у присутності реагенту, що несе відхідну групу (нуклеофуг), такого як алкілгалогенід. Можна використати умови прикладу 15 одержання сполуки 46. Стадія (iv): елонгація ПЕГ ланцюга; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як THF або DMF, шляхом обробки галогенованого складного ефіру алкоголятом бензофенонімін-ПЕГ-спирту, що генерується під дією NaH або нафталеніду калію, як описано у WO 2007/127440; Стадія (v): омилення складного ефіру; реакцію здійснюють шляхом взаємодії складного ефіру з гідроксидом літію в присутності води. Стадія (vi): захист аміну; реакцію здійснюють при КТ у полярному апротонному розчиннику, такому як DCM, шляхом обробки аміну дитрет-бутилдикарбонатом у присутності основи, такої як, наприклад, ТЕА. Амін-ПЕГ-кислоти є комерційно доступними при i=3, 5, 6, 10, або можуть бути одержані з трет-бутилакрилату і відповідного амін-ПЕГ-спирту. Амін-ПЕГ-спирти є комерційно доступними, наприклад, при i=3, 4, 7, 8, або можуть бути одержані з ПЕГ діолів, комерційно доступних при i=3-12, згідно з процедурою, описаною в US 7230101. Захист амінофункції бензофеноном може бути здійснений у процесі азеотропної дегідратації в присутності кислоти Льюїса, такої як ефірат BF 3. PL8 , що одержують згідно зі схемами, описаними нижче: у випадку, коли ALK=CH2CH2 25 35 Стадія (i): зняття захисту з вихідної сполуки за допомогою розчину соляної кислоти (наприклад, розчину в діоксані) або трифтороцтової кислоти. Можна використати умови прикладу 16 одержання сполуки 50. Стадія (ii): захист карбоксильної функціональної групи кислоти в формі складного алілового ефіру; реакцію здійснюють при КТ у полярному апротонному розчиннику, такому як DMF, у присутності алілброміду та основи, такої як карбонат калію. Можна використати умови прикладу 16 одержання сполуки 51. Стадія (iii): активація спирту в формі мезилату; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як DCM, обробкою мезилхлоридом у присутності основи, такої як ТЕА. 40 Стадія (iv): реакція між мезилатною та амінною функціональною групою сполуки (алкілування); реакцію здійснюють при КТ у безводному полярному апротонному розчиннику, такому як DCM, у присутності основи, такої як ТЕА. Можна використати умови прикладу 16 одержання сполуки 52. у випадку, коли ALK CH2CH2 30 45 Стадія (v): елонгація ПЕГ ланцюга; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як THF або DMF, шляхом обробки галогенованого складного ефіру алкоголятом ПЕГ діолу, монозахищеного в формі простого ефіру тетрагідропірану (ТНР). Одержання цього типу монозахищеного ПЕГ діолу описане в літературі, див., наприклад, Richard A. et al., Chem. Eur. J. 2005, 11, 7315-7321 або Sakellariou E.G., et al., Tetrahedron 2003, 59, 9083-9090. ПЕГ спирти, що містять кислотну функціональну групу, захищену в формі складного трет 26 UA 108473 C2 бутилового ефіру, комерційно доступні (такий як трет-бутил-12-гідрокси-4,7,10триоксадодеканоат) або їх одержують із трет-бутилакрилату і ПЕГ діолу. Початкові ПЕГ діоли комерційно доступні при i=3-12. PL9 5 10 15 , що одержується згідно з нижчеописаною схемою: Стадія (i): алкілування аміну; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як ацетонітрил, із використанням алілгалогеналкілкарбоксилату, такого як алілбромацетат, у присутності основи, такої як, наприклад, ТЕА. Можна використати умови прикладу 13 одержання сполуки 38. Стадія (ii): зняття захисту з аміну за допомогою розчину кислоти, наприклад, соляної кислоти (наприклад, розчиненої в діоксані). Можна використати умови прикладу 13 одержання сполуки 39. Алілгалогеналкілкарбоксилат може бути одержаний із алілового спирту і відповідного галогенацилгалогеніду і може бути комерційно доступним, коли ALK=-(CH2)1-6- (такий як бромацетилбромід або 4-бутаноїлхлорид). PL10 , що одержують згідно з нижчеописаними схемами: у випадку, коли ALK=CH2CH2 у випадку, коли ALKCH2CH2 20 25 30 35 Стадія (i): розкриття циклічного ангідриду; реакцію здійснюють при КТ у безводному полярному апротонному розчиннику, такому як DCM, у присутності основи, такої як ТЕА. Стадія (ii): захист карбонової кислоти у формі складного алілового ефіру; реакцію здійснюють при КТ у полярному апротонному розчиннику, такому як DСM, у присутності алілового спирту, що поєднує агента, такого як EDCl, і основу, таку як DMAP. Стадія (iii): зняття захисту за допомогою розчину соляної кислоти (наприклад, розчину в діоксані). Стадія (iv): пептидне поєднання; реакцію між карбоновою кислотою і аміном здійснюють при КТ у полярному апротонному розчиннику, такому як DСM, у присутності сполучного агента, такого як система DIC/HOBt. Стадія (v): омилення складного метилового ефіру; реакцію здійснюють при КТ у суміші полярних розчинників, такій як суміш THF/вода, у присутності гідроксиду літію. Двоосновні кислоти, монозахищені у формі складного метилового ефіру, є комерційно доступними при ALK=-(CH2)1-6- (такого як складний монометиловий ефір 1,6-гександіової кислоти). PL11 у випадку, коли ALK=CH2CH2 випадок, коли R12=Н , що одержується згідно з нижчеописаними схемами: 27 UA 108473 C2 5 10 15 20 25 30 35 . Стадія (i): утворення аміду та активація кислоти; здійснюють послідовно дві стадії в полярному апротонному розчиннику, такому як DCM: реакцію між амінофункцією і Nгідроксисукцинімідил-галогенацетатом, потім введення in situ сполучного агента, такого як DIC. Можна використати умови прикладу 17 одержання сполуки 56. випадок, коли R12Н Стадія (ii): захист карбонової кислоти у формі складного метилового ефіру та аміну у формі трифторацетаміду; реакцію здійснюють у дві послідовні стадії в полярному апротонному розчиннику, такому як, DСM: захист кислоти шляхом обробки триметилсилілдіазометаном у присутності метанолу, потім захист аміну додаванням трифтороцтового ангідриду та основи, такої як ТЕА. Стадія (iii): алкілування аміну та омилення складного ефіру; реакцію здійснюють у дві послідовні стадії в середовищі полярного апротонного безводного розчинника, такого як THF: алкілування аміну обробкою основою, такою як NaH, у присутності реагенту, що несе нуклеофуг, такого як алкілгалогенід R12Hal, потім введення гідроксиду літію і води. Стадія (i): продовження стадії (iii), повторюють реакції стадії (i), описані для випадку R 12=Н. у випадку, коли ALKCH2CH2 випадок, коли R12=Н випадок, коли R12Н Стадія (iv): елонгація ПЕГ ланцюга; реакцію здійснюють у безводному полярному апротонному розчиннику, такому як THF або DMF, шляхом обробки галогенованого складного ефіру алкоголятом бензофенонімін-ПЕГ-спирту, що генерується під дією NaH або нафталеніду калію (див. WO 2007/127440) Стадія (v): селективне розщеплення іміну шляхом гідрування в присутності паладію на вугіллі (див. Wessjohann, L. et al., Synthesis 1989, 5, 359-63); Стадія (vi): захист аміну введенням трифтороцтового ангідриду та основи, такої як ТЕА. Амін-ПЕГ-кислоти є комерційно доступними при i=3, 5, 6, 10, або можуть бути одержані з трет-бутилакрилату і відповідного амін-ПЕГ-спирту. Амін-ПЕГ-спирти є комерційно доступними, наприклад, при i=3, 4, 7, 8, або можуть бути одержані з ПЕГ діолів, комерційно доступних при i=3-12, згідно з процедурою, описаною в US 7230101. Захист амінофункції бензофеноном може бути здійснений у процесі азеотропної дегідратації в присутності кислоти Льюїса, такої як ефірат BF3. PL12 , де Z=Br або I, що одержується згідно з нижчеописаними схемами: у випадку, коли ALK=CH2CH2 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel conjugates, preparation thereor, and therapeutic use thereof
Автори англійськоюBouchard, Herve, Brun, Marie-Priscille, Commercon, Alain, Zhang, Jidong
Автори російськоюБушар Эрве, Брен Мари-Присцилл, Коммерсон Ален, Чжан Цзидун
МПК / Мітки
МПК: A61P 35/00, C07D 273/00, A61K 31/395
Мітки: кон'югати, одержання, застосування, терапії, їхнє
Код посилання
<a href="https://ua.patents.su/121-108473-konyugati-khneh-oderzhannya-i-zastosuvannya-v-terapi.html" target="_blank" rel="follow" title="База патентів України">Кон’югати, їхнє одержання і застосування в терапії</a>
Попередній патент: Спосіб одержання мішені плазмовим напиленням
Наступний патент: Синтетичний промотор, який індукується патогенами
Випадковий патент: Сигарета, забезпечена запалювальним пристроєм