Антитіло, яке зв’язується з cd38, для лікування захворювання, опосередкованого cd38
Номер патенту: 98756
Опубліковано: 25.06.2012
Автори: Вюгт Мартін ван, Граус Іво, Верс Мішель де, Опрінс Юдіт, Вінкел Ян ван де, Паррен Пауль Паррен
Формула / Реферат
1. Антитіло, що зв'язується з CD38 людини, кодоване
(1) нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно з SEQ ID NO: 11 та SEQ ID NO: 16, відповідно.
2. Антитіло, що зв'язується з CD38 людини, яке включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, де варіабельний район легкого ланцюга включає VL CDR1 з послідовністю згідно з SEQ ID NO: 13, VL CDR2 з послідовністю згідно з SEQ ID NO: 14 та VL CDR3 з послідовністю згідно з SEQ ID NO: 15, і варіабельний район важкого ланцюга включає VН CDR1 з послідовністю згідно з SEQ ID NO: 18, VН CDR2 з послідовністю згідно з SEQ ID NO: 19 та VН CDR3 з послідовністю згідно з SEQ ID NO: 20.
3. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VL район з амінокислотною послідовністю згідно з SEQ ID NO: 12.
4. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VL район, що має щонайменше приблизно 90 %, наприклад приблизно 95 %, ідентичності амінокислотної послідовності з послідовністю згідно з SEQ ID NO: 12.
5. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VН район з амінокислотною послідовністю згідно з SEQ ID NO: 17.
6. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VН район, що включає амінокислотну послідовність, яка охоплює район VН CDR1 - VН CDR3 в SEQ ID NO: 17.
7. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VН район, що має щонайменше приблизно 90 %, наприклад приблизно 95 %, ідентичності амінокислотної послідовності з послідовністю згідно з SEQ ID NO: 17 або з районом, що охоплює VН CDR1 - VН CDR3 в SEQ ID NO: 17.
8. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VН район, що має 1-5, наприклад 1-3, амінокислотні заміщення, делеції або добавки в порівнянні з послідовністю згідно з SEQ ID NO: 17 або з районом, що охоплює VН CDR1 - VН CDR3 в SEQ ID NO: 17.
9. Антитіло за п. 2, що зв'язується з CD38 людини, яке включає VL район, як визначено за п. 3, і VН район, як визначено за п. 5.
10. Антитіло за будь-яким з пп. 1-9, що зв'язується з CD38 людини, де антитіло має одну чи більше з таких характеристик зв'язування:
(1) діє як антагоніст CD38;
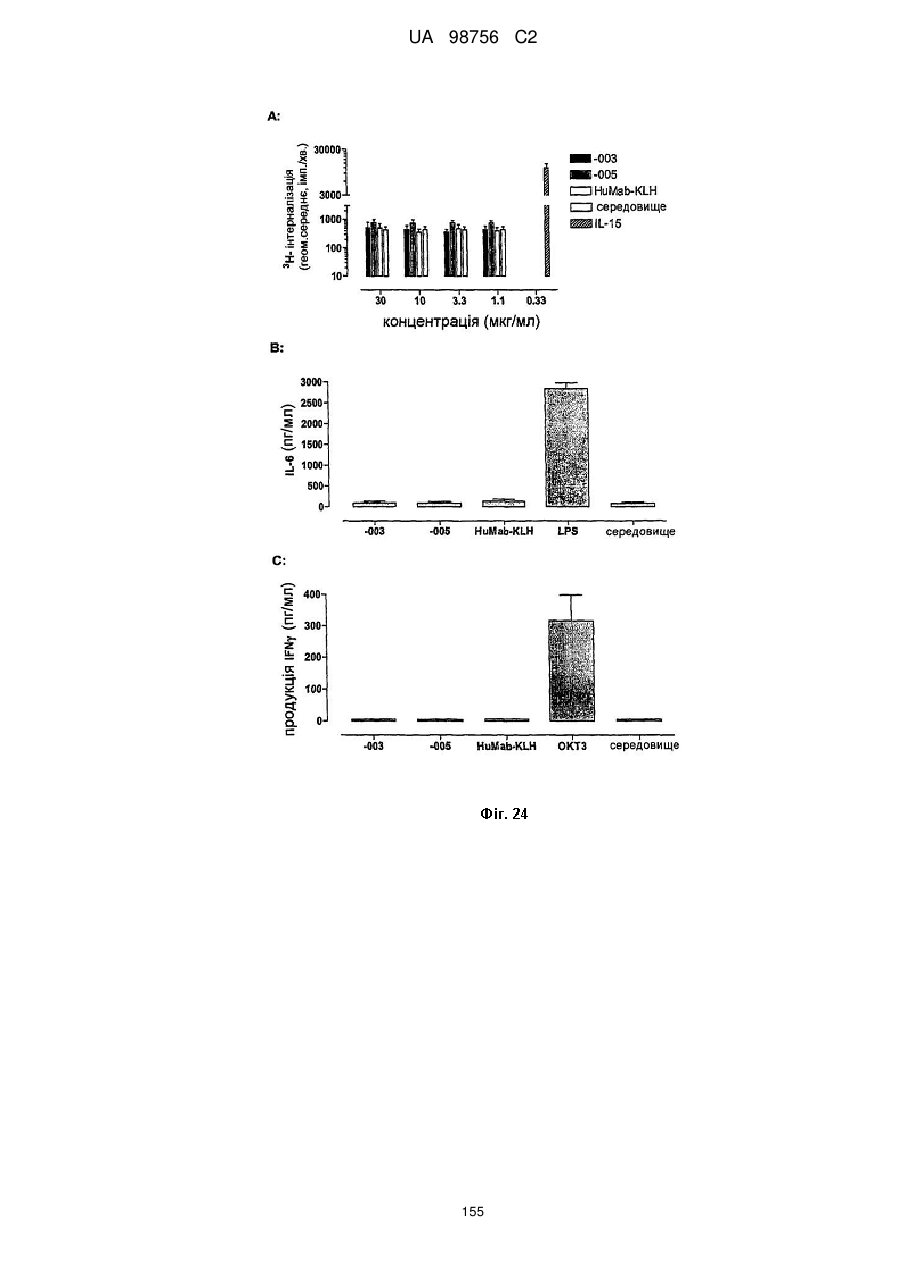
(2) не індукує значну проліферацію мононуклеарних клітин периферичної крові, яку визначають способом, описаним в прикладі 18 опису;
(3) не індукує вивільнення значної кількості IL-6 моноцитами людини або мононуклеарними клітинами периферичної крові, яке визначають способом, описаним в прикладі 19 опису;
(4) не індукує вивільнення детектованої кількості IFN-g Т-клітинами людини або мононуклеарними клітинами периферичної крові людини, яке визначають способом, описаним в прикладі 20 опису;
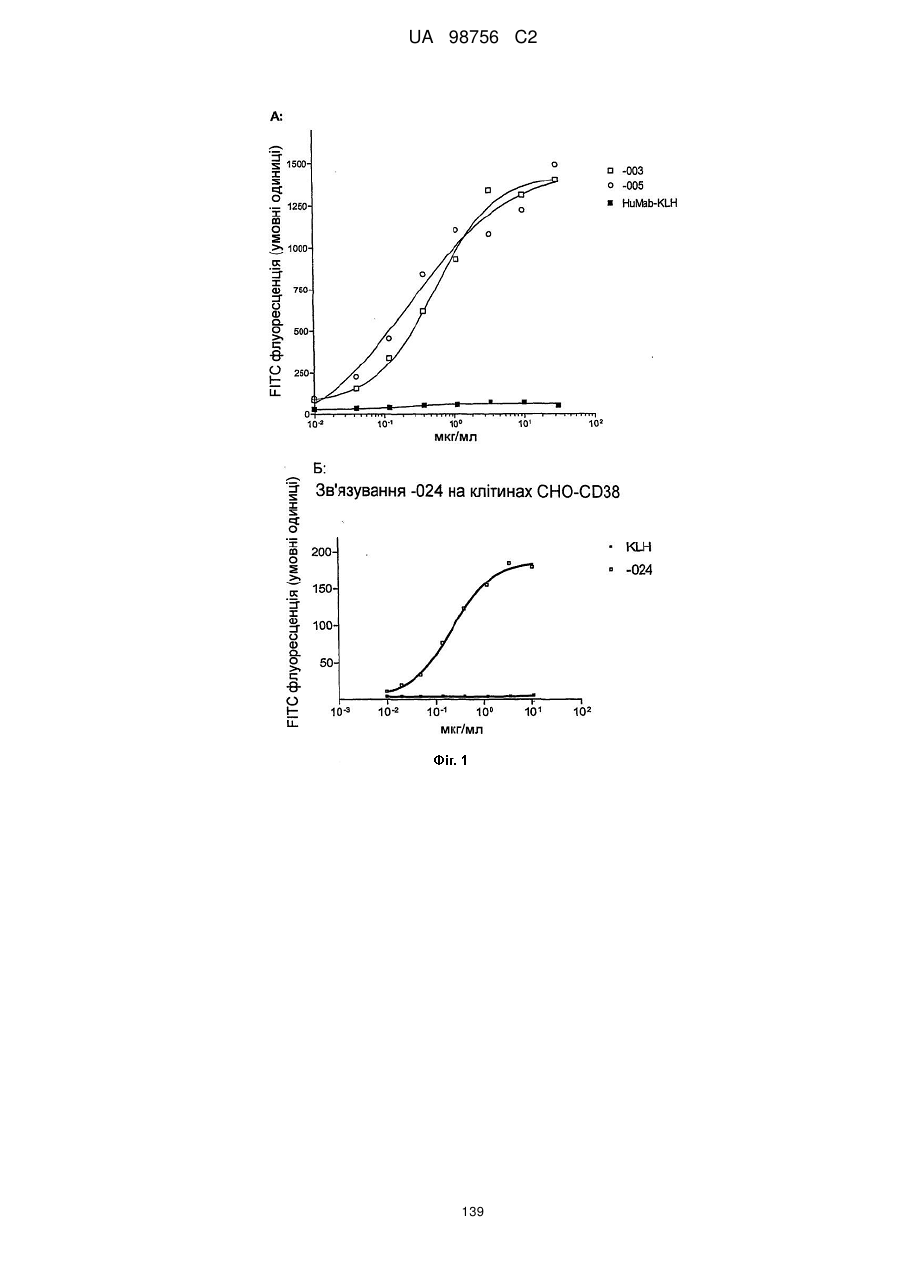
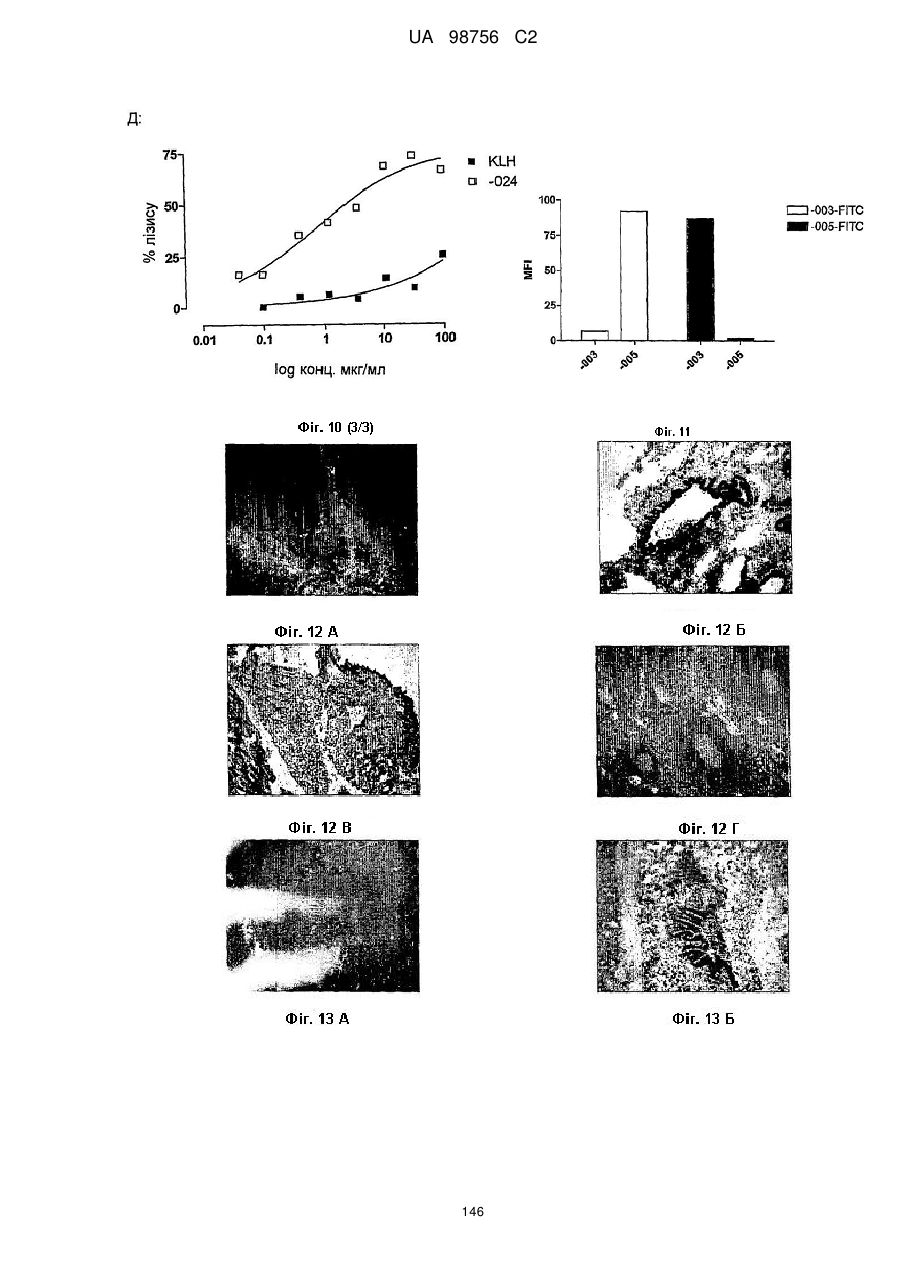
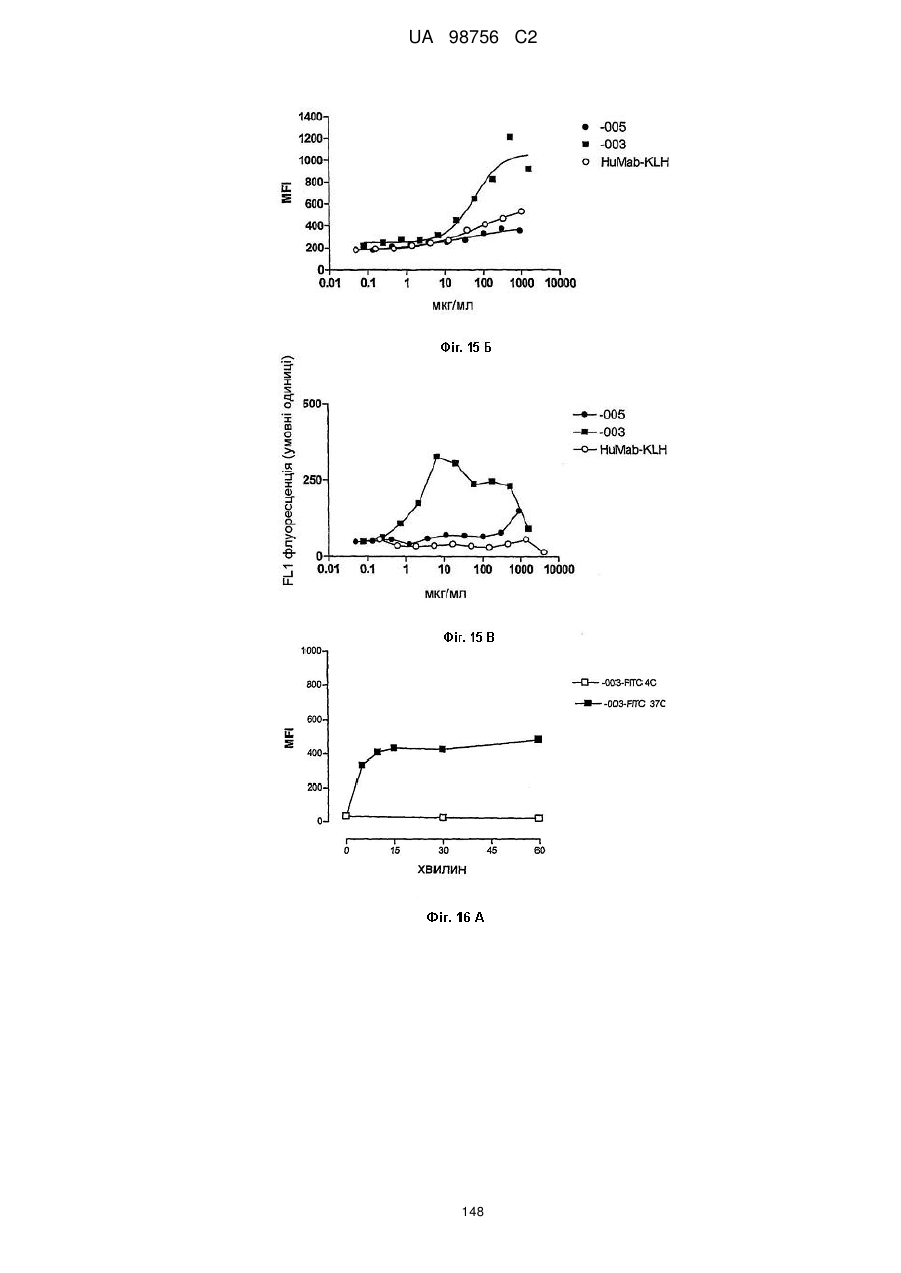
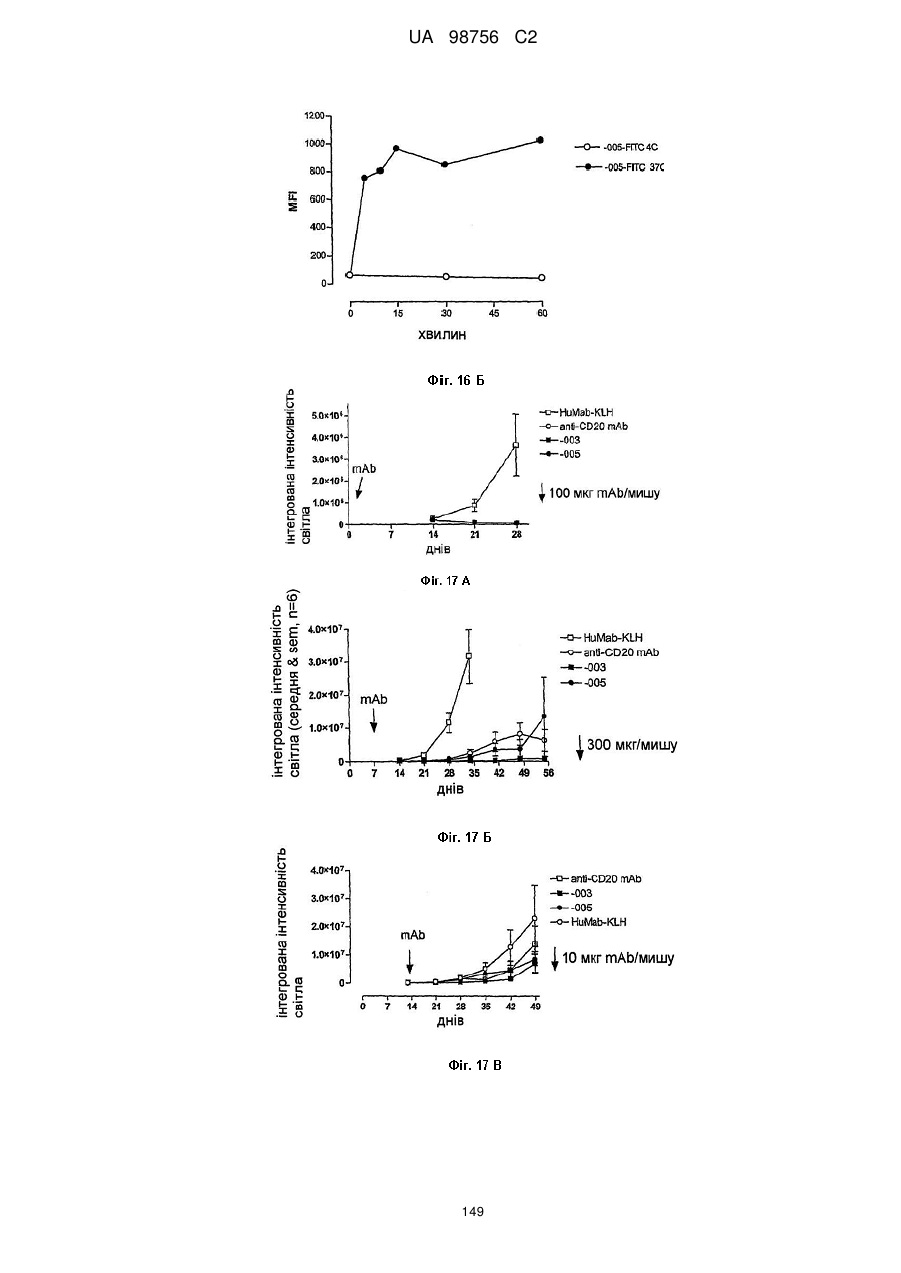
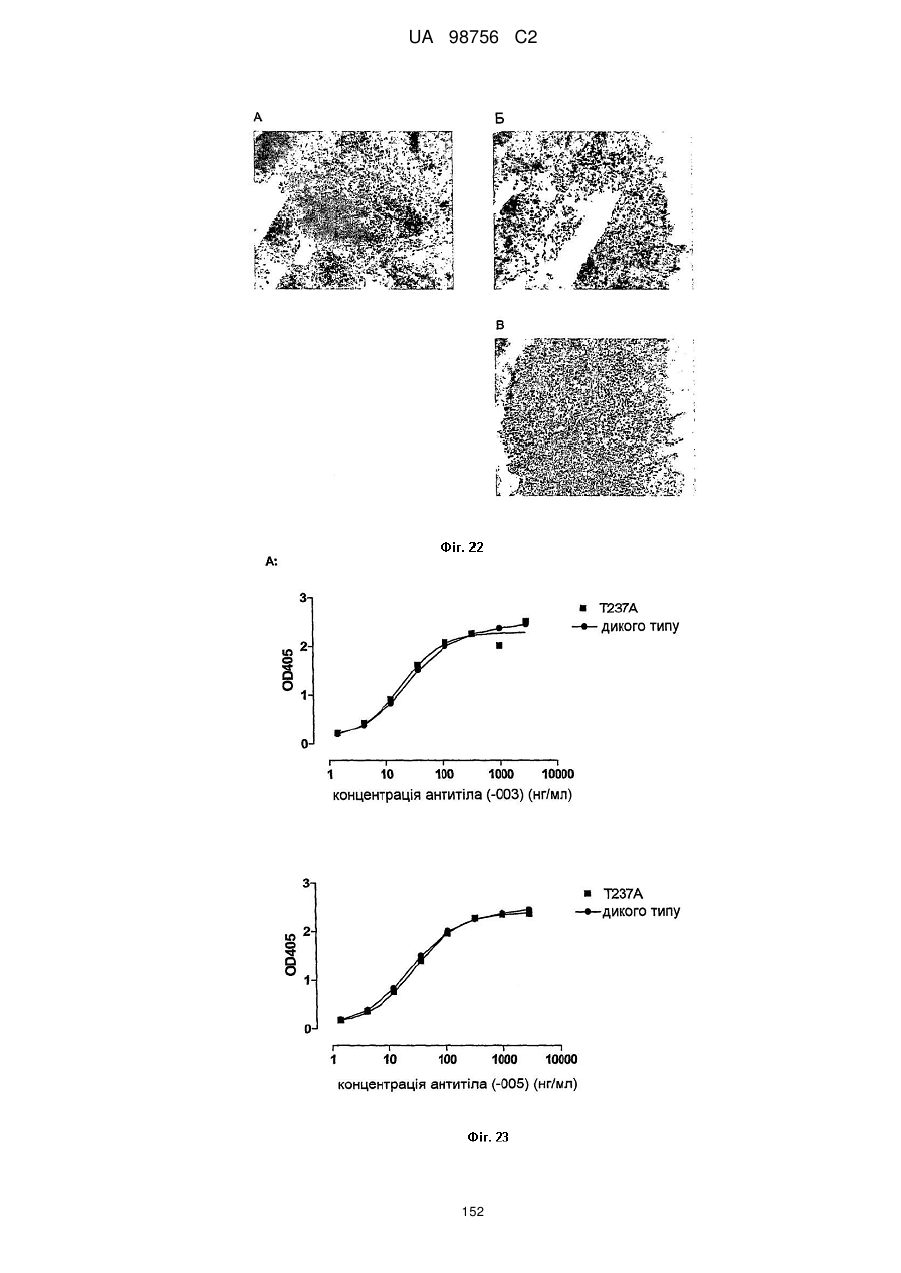
(5) інтерналізується клітинами, що експресують CD38; наприклад інтерналізується клітинами CHO-CD38 протягом 5-15 хв. при 37 °C, у спосіб, описаний в прикладі 12 опису;
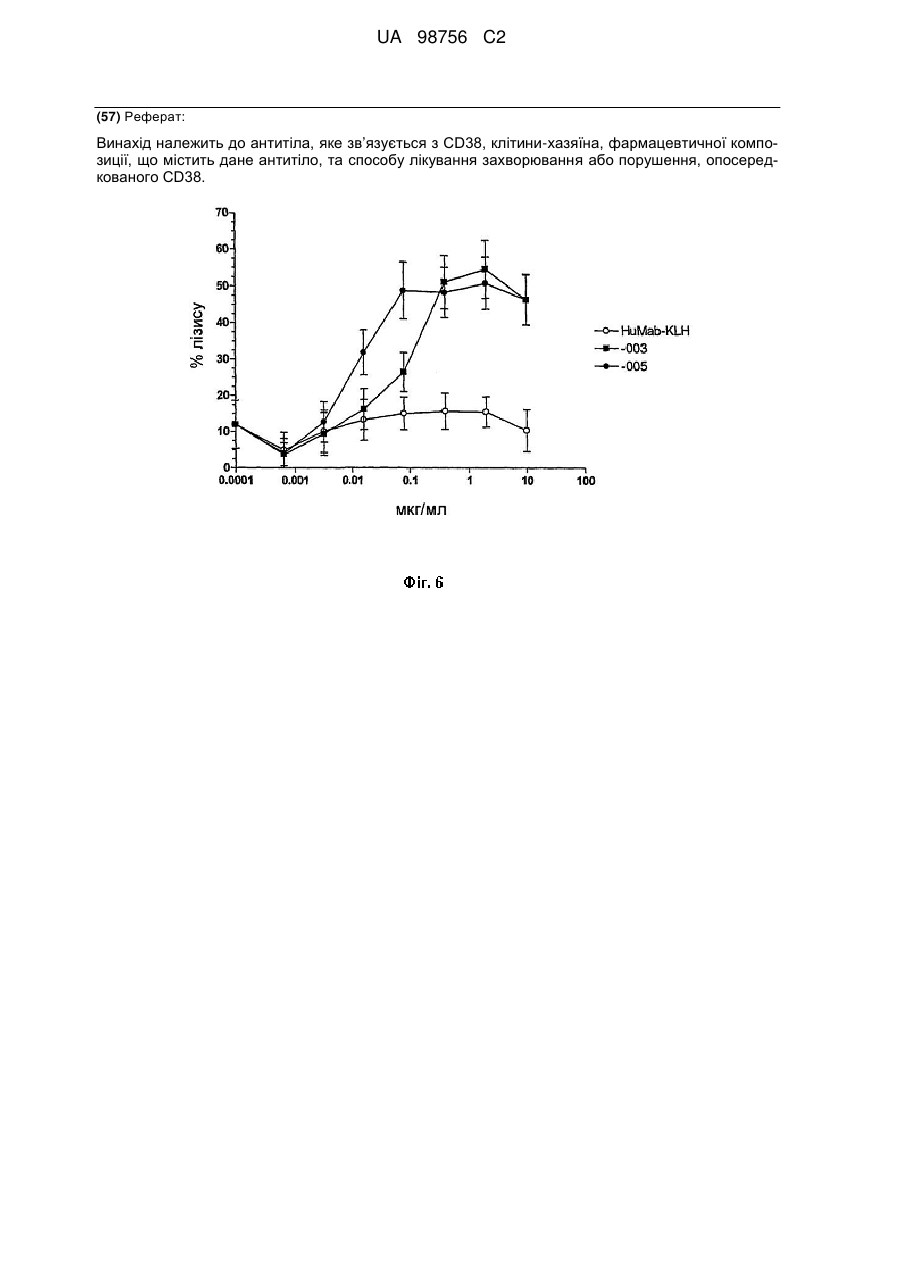
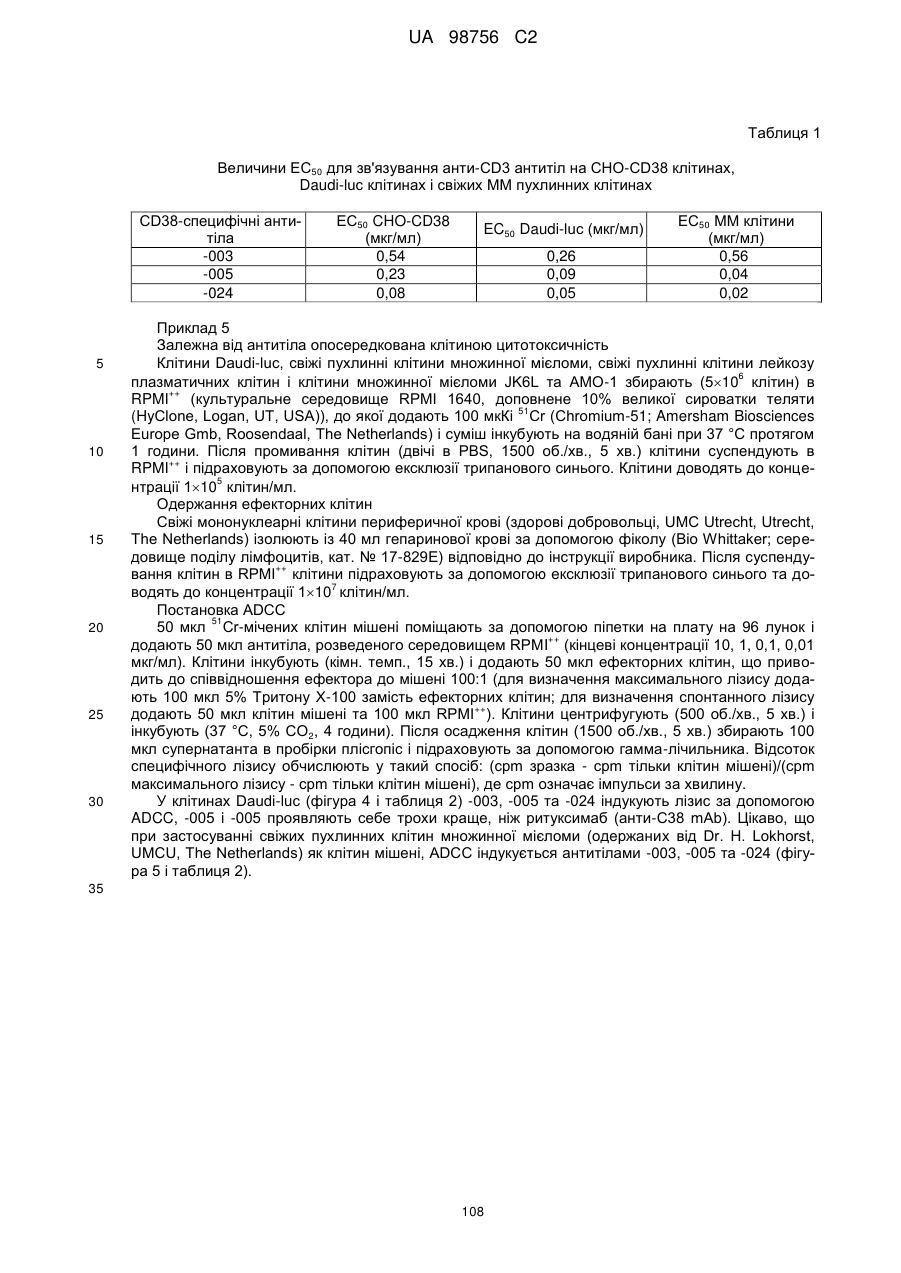
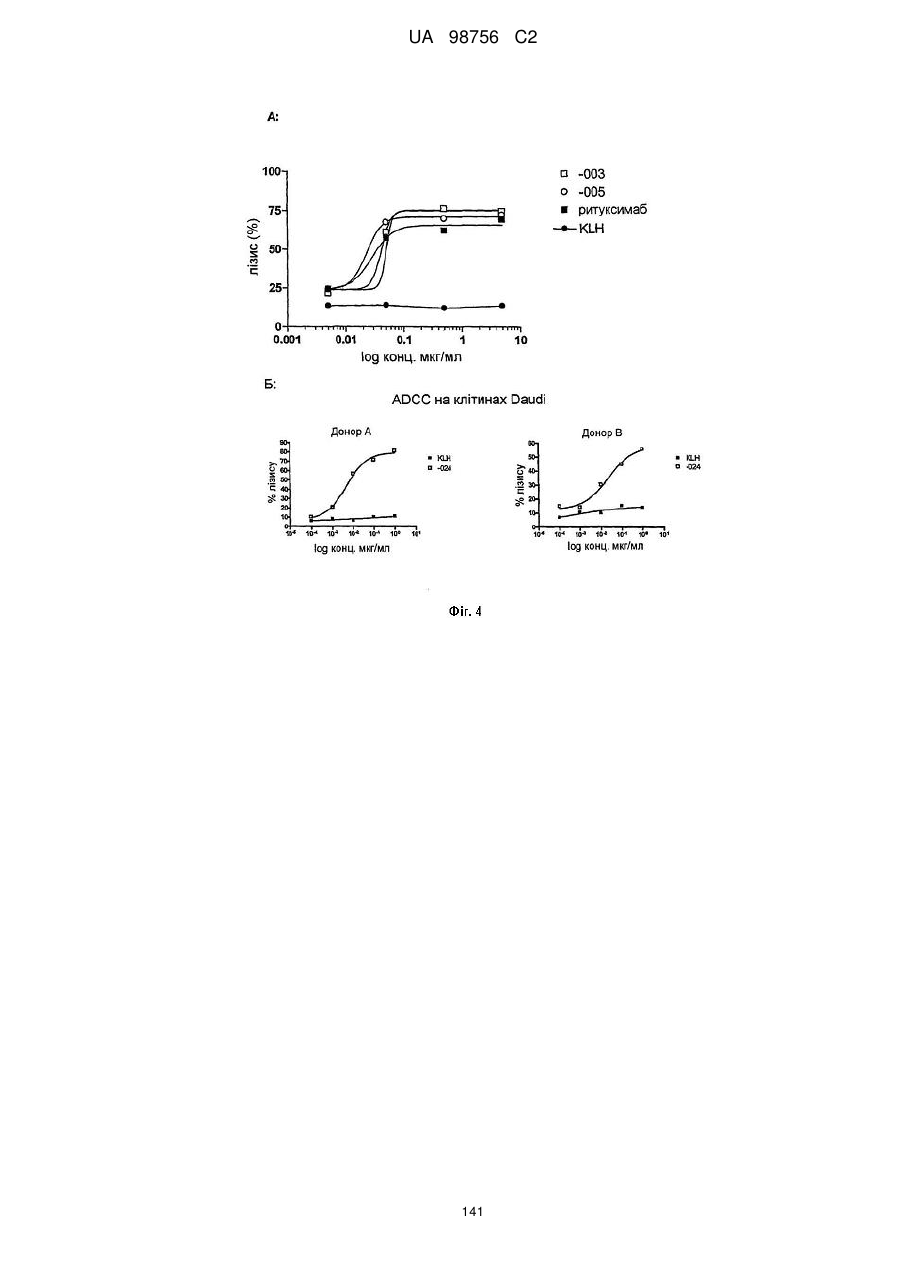
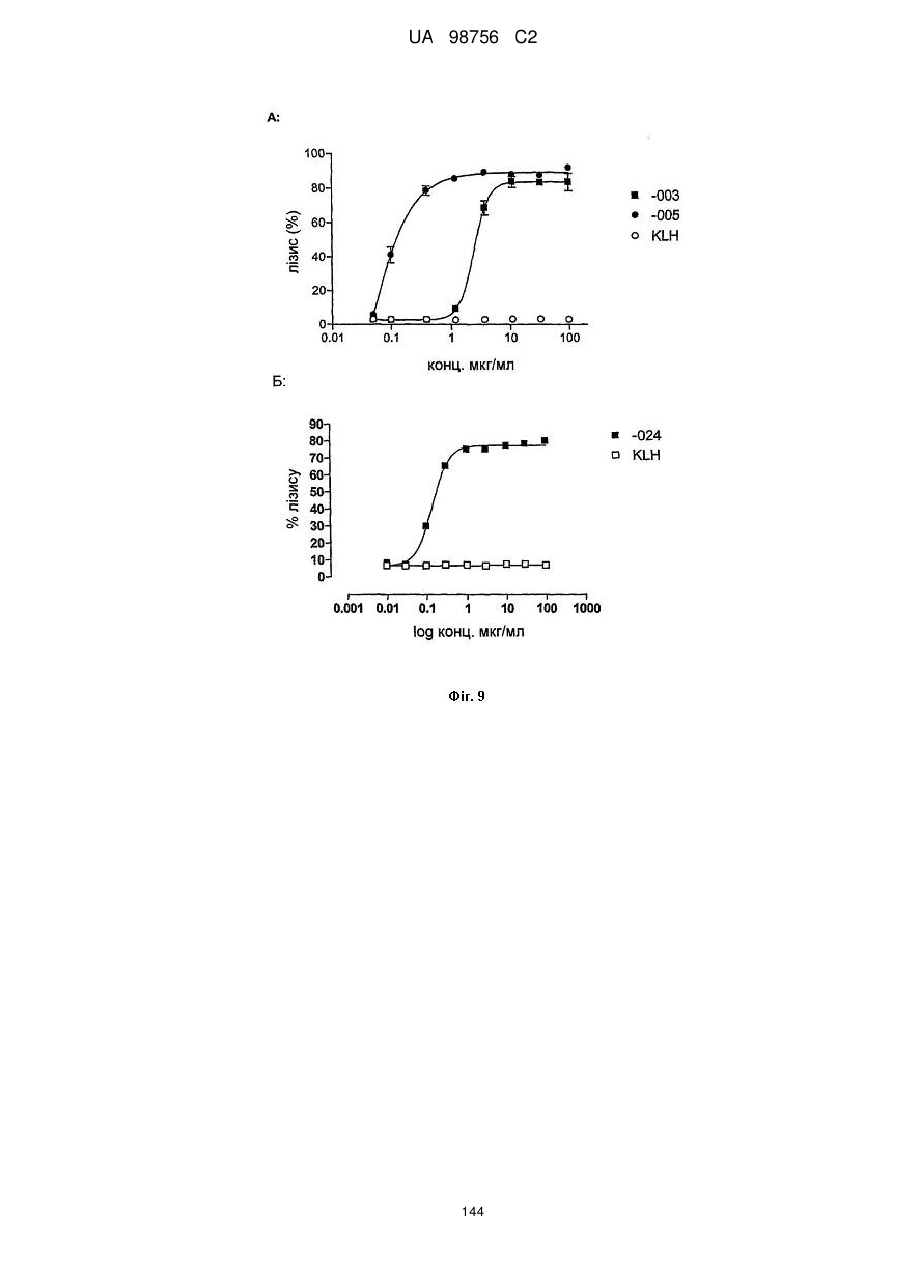
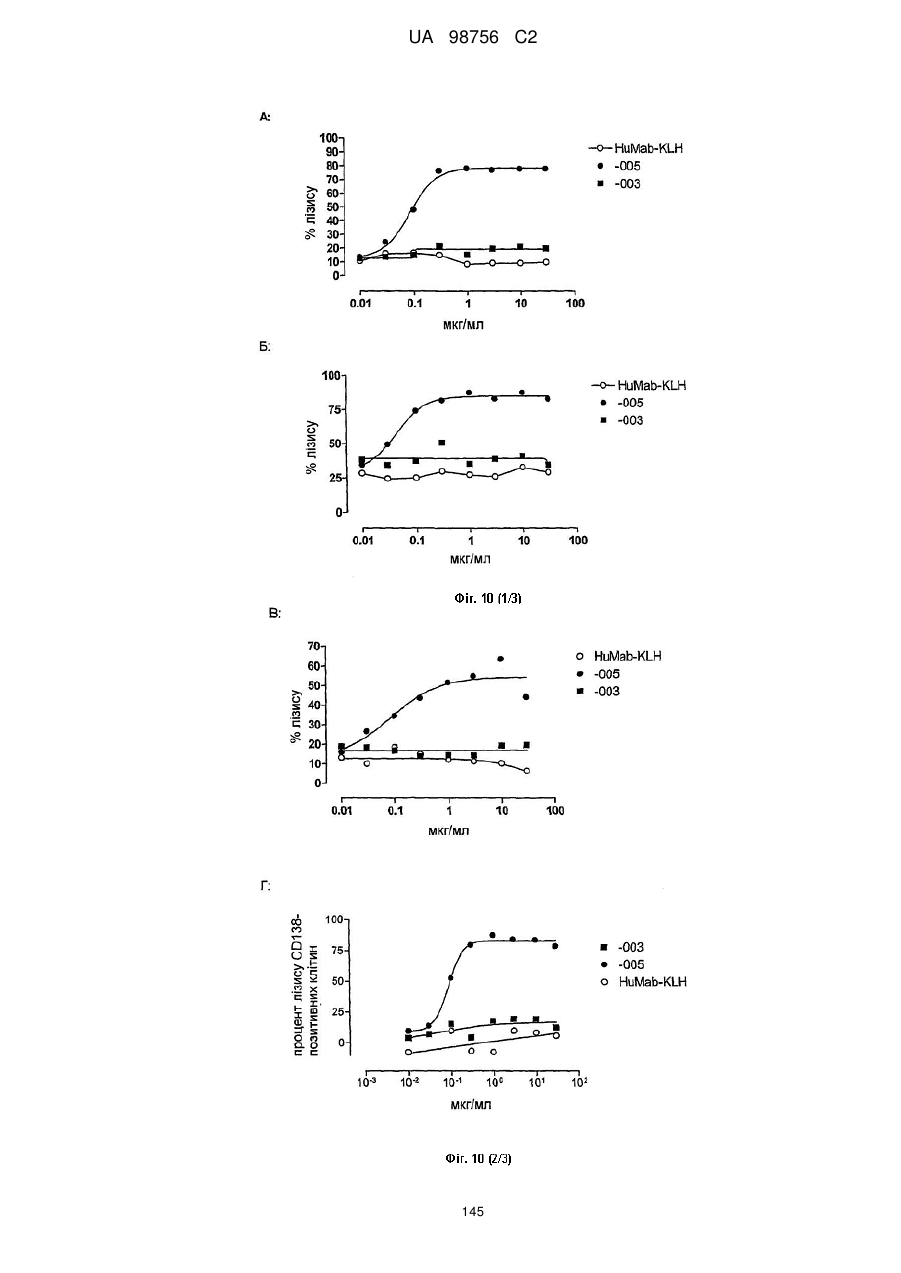
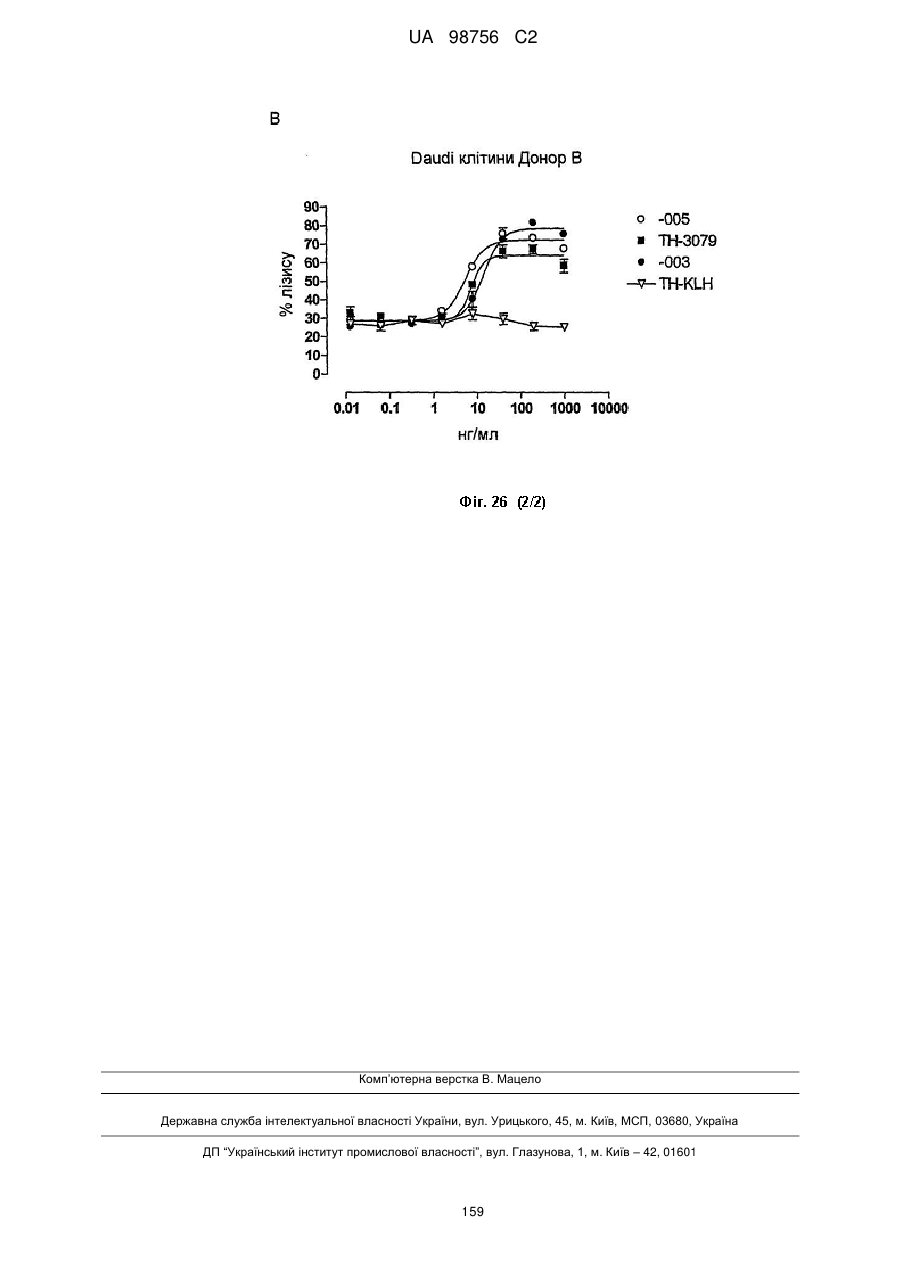
(6) індукує ADCC; наприклад, зі значенням EC50 нижче 15 нг/мл, наприклад нижче 10 нг/мл, у клітинах Daudi-luc, і зі значенням EC50 нижче 75 нг/мл, наприклад нижче 50 нг/мл, 30 нг/мл або 10 нг/мл, у клітинах ММ, як визначають способом, описаним в прикладі 5 опису;
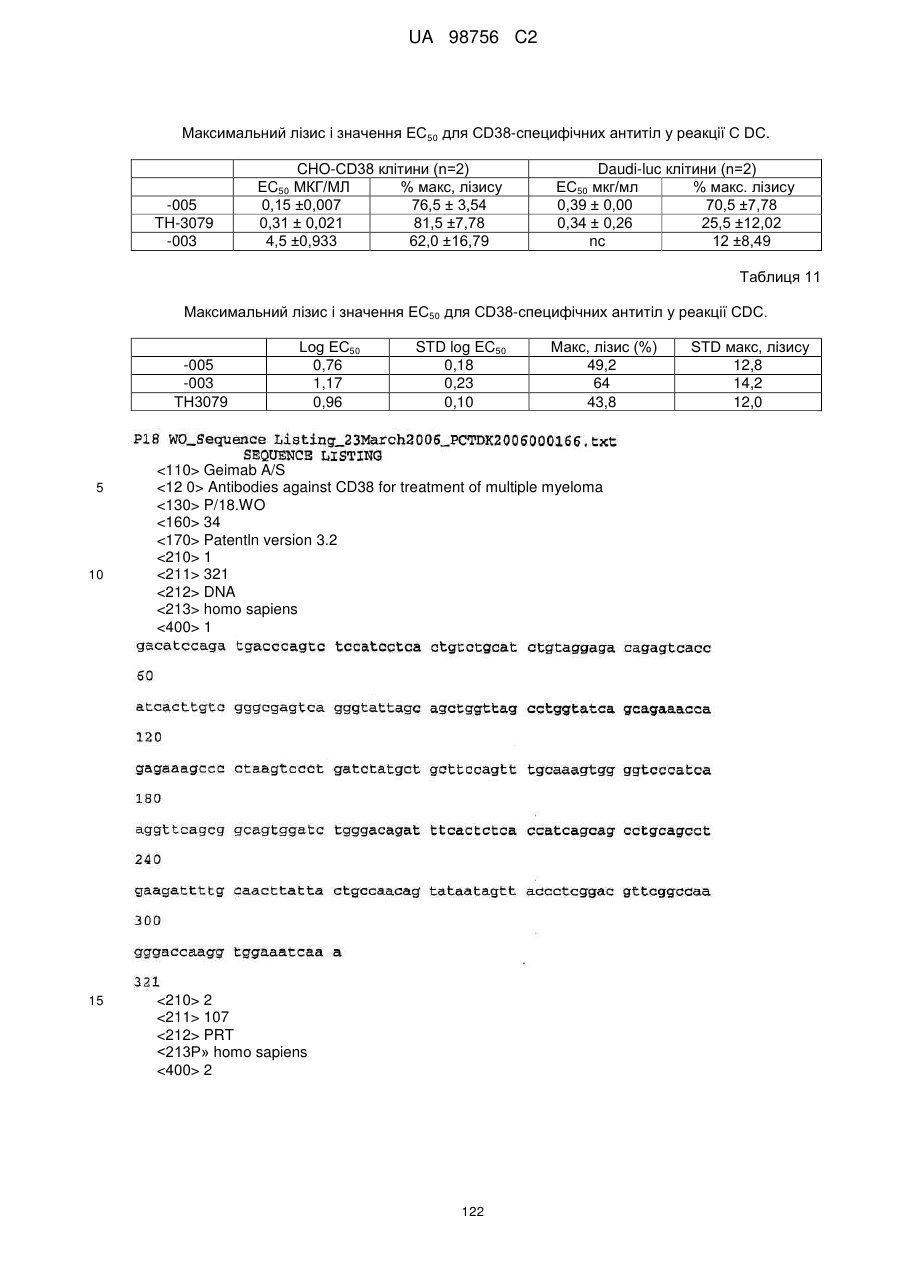
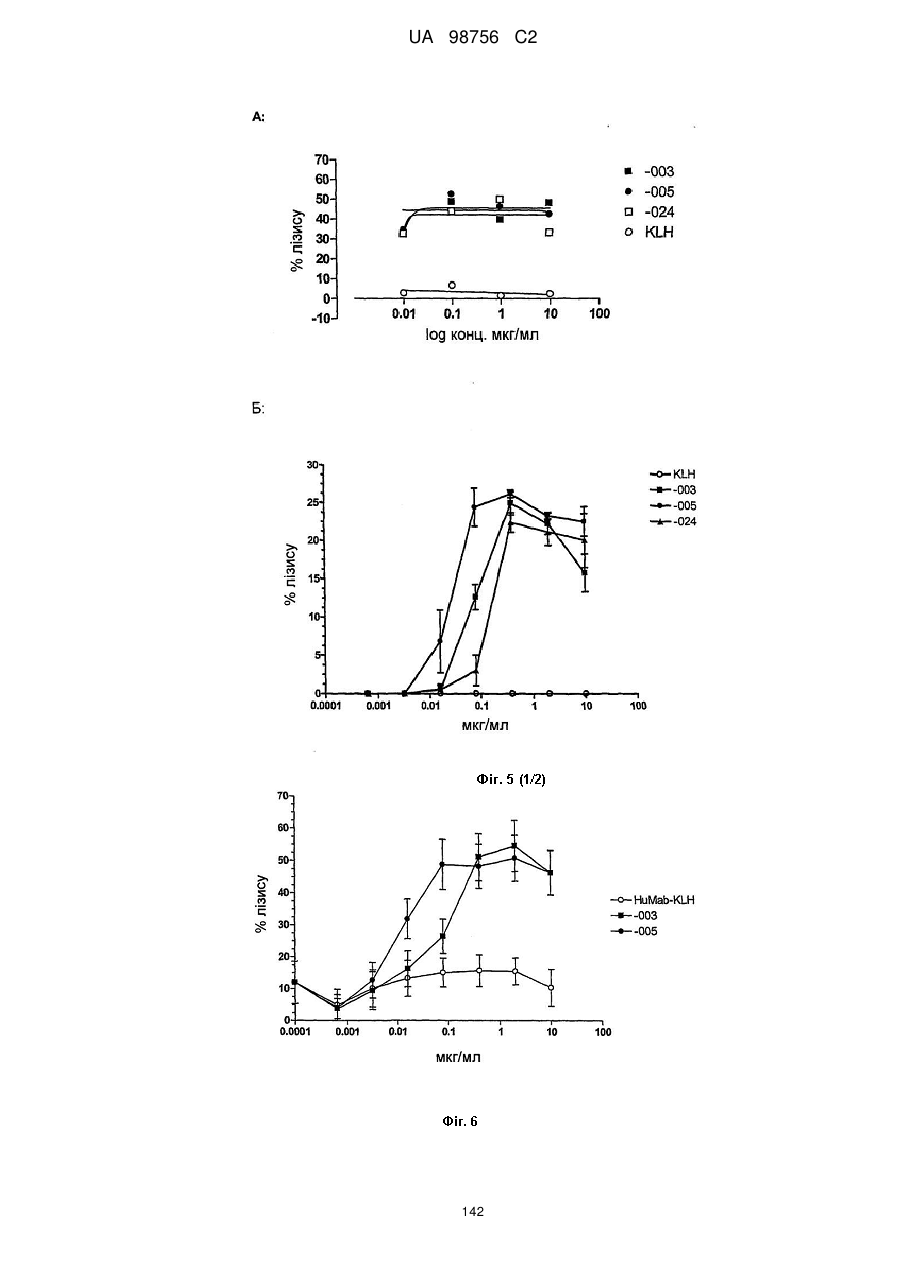
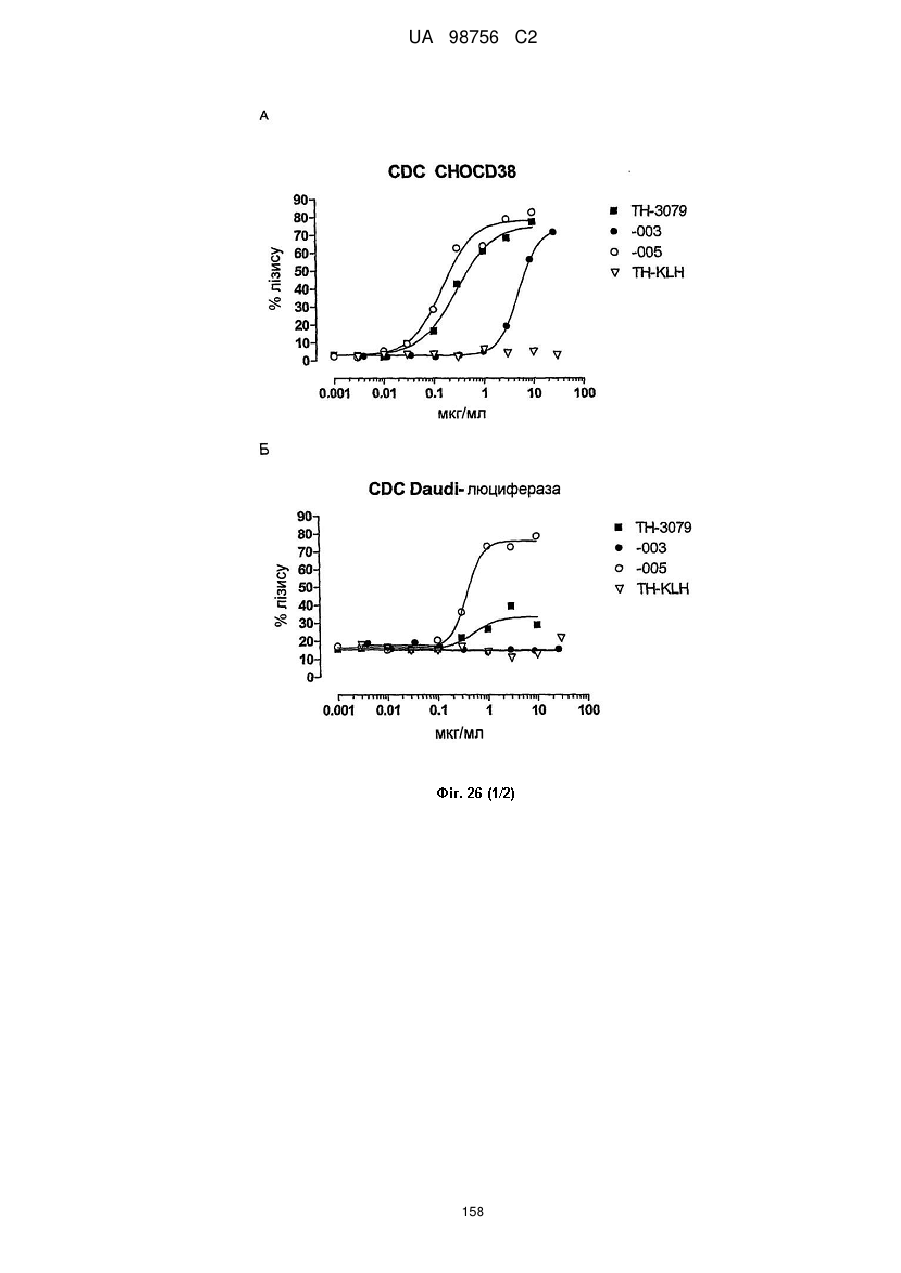
(7) індукує CDC у присутності комплементу, наприклад, зі значенням EC50 нижче 5 мкг/мл, наприклад нижче 1 мкг/мл, у клітинах Daudi-luc або CHO-CD38, у спосіб, описаний в прикладі 6 опису;
(8) інгібує синтез цГДФР;
(9) інгібує синтез цАДФР;
(10) зв'язується з CD38 людини зі спорідненістю (КD) нижче 10-8 М, наприклад в інтервалі від 10-8 М до 10-11 М, наприклад в інтервалі від 7´10-9 М до 10-10 М, як визначають за допомогою поверхневого плазмонного резонансу, як описано в прикладі 20 опису.
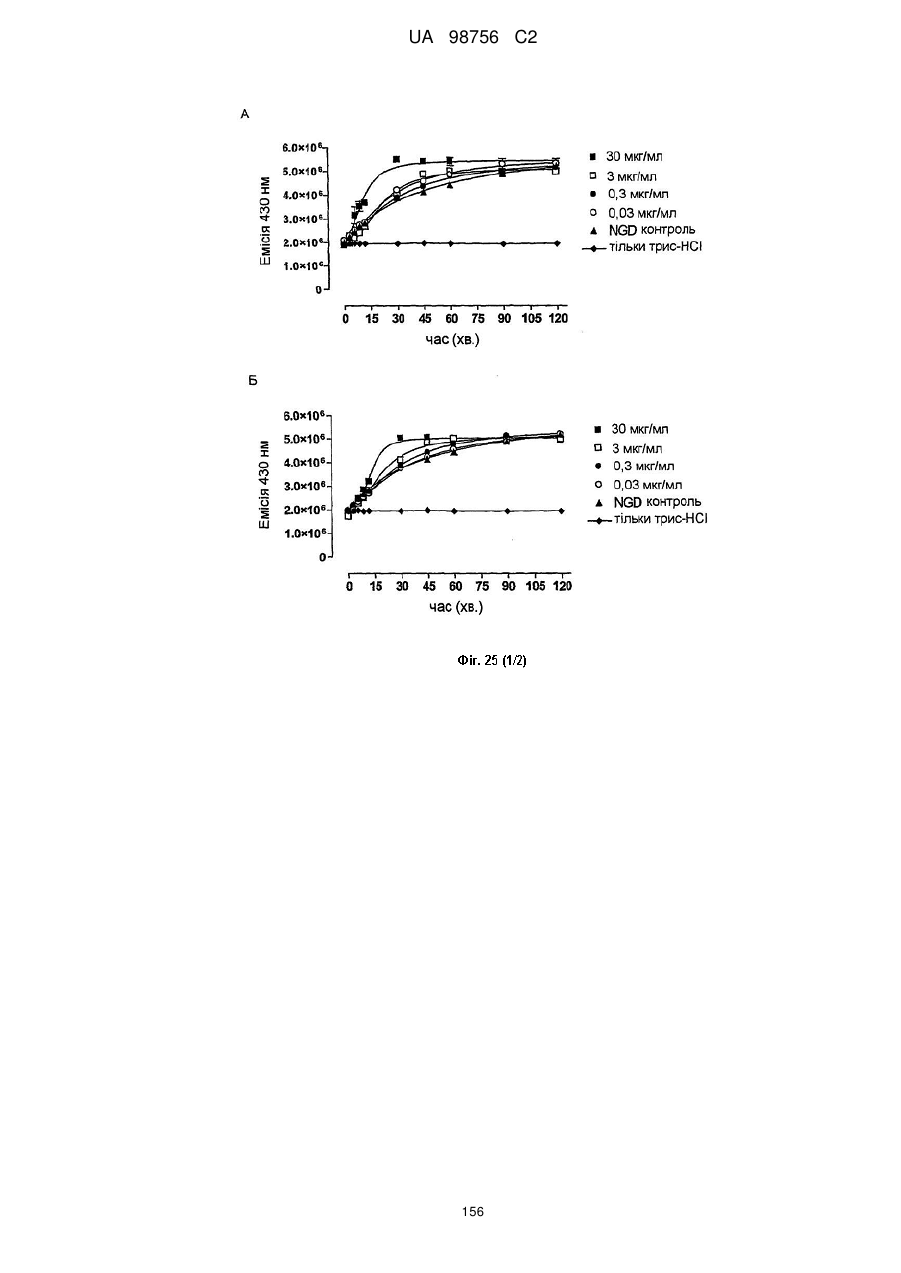
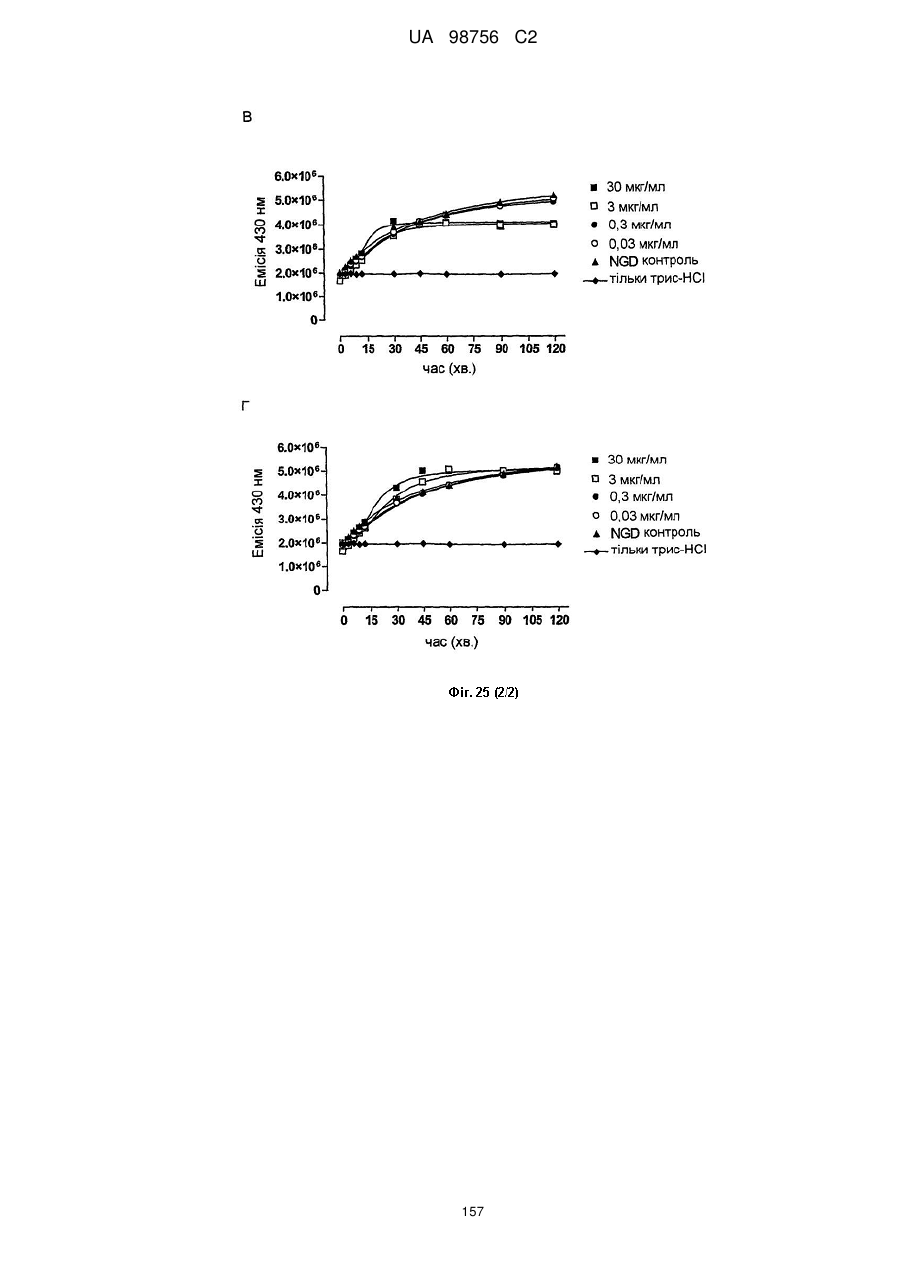
11. Антитіло за п. 10, що інгібує синтез цГДФР щонайменше на 25 %, наприклад на 30 %, через 90 хв. у концентрації 3 мкг/мл, як визначають за допомогою спектрофотометричного способу, описаного в прикладі 24 опису.
12. Антитіло за п. 10, що інгібує синтез цАДФР щонайменше на 25 %, наприклад на 30 %, через 90 хв. у концентрації 3 мкг/мл, як визначають за допомогою ВЕРХ способу, описаного в Munshi et al., J. Biol. Chem. 275, 21566-21571 (2000).
13. Антитіло за будь-яким з пп. 1-12, що є моноклональним антитілом людини.
14. Антитіло за будь-яким з пп. 1-13, яке характеризується тим, що воно є повнорозмірним антитілом IgG1, ІgG2, ІgG3, ІgG4, IgD, IgA, IgE або IgM, наприклад антитілом IgG1, краще антитілом IgG1,k, або антитілом IgM, краще антитілом IgM,k.
15. Антитіло за будь-яким з пп. 1-14, де антитіло є глікозильованим в еукаріотичній клітині.
16. Антитіло за будь-яким з пп. 1-15, що є фрагментом антитіла або одноланцюговим антитілом.
17. Антитіло за будь-яким з пп. 1-15, яке додатково включає хелатуючий лінкер для приєднання радіоізотопу.
18. Антитіло за будь-яким з пп. 1-17, що находиться, по суті, в ізольованій формі.
19. Антитіло, що специфічно зв'язується з епітопом CD38, де епітоп також специфічно зв'язується антитілом за п. 1.
20. Антитіло за п. 19, що специфічно зв'язується з районом SKRNIQFSCKNIYR і районом EKVQTLEAWVIHGG в CD38 людини (SEQ ID NO: 31).
21. Антитіло за п. 19, що має по суті такі ж характеристики специфічного зв'язування CD38 людини, як антитіло за п. 1.
22. Еукаріотична або прокаріотична клітина-хазяїн, що продукує антитіло за будь-яким з пп. 1-21.
23. Еукаріотична клітина-хазяїн за п. 22, що є трансфектомою, яка продукує моноклональне анти-CD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга та важкого ланцюга людини, які включають
(1) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:11 та SEQ ID NO:16, відповідно,
(2) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах, які є консервативними модифікаціями вищенаведених послідовностей.
24. Еукаріотична клітина-хазяїн за п. 22, що є трансфектомою, яка продукує моноклональне анти-CD38 антитіло людини, що має варіабельні райони важкого ланцюга та легкого ланцюга людини, які включають:
(1) амінокислотну послідовність варіабельної області легкого ланцюга людини згідно з SEQ ID NO: 12 та амінокислотну послідовність варіабельної області важкого ланцюга людини згідно з SEQ ID NO: 17;
(2) консервативні модифікації вищенаведених амінокислотних послідовностей варіабельних областей легкого ланцюга людини та важкого ланцюга людини.
25. Фармацевтична композиція, яка включає антитіло за будь-яким з пп. 1-21 і фармацевтично прийнятний носій.
26. Фармацевтична композиція за п. 25, яка включає один чи більше додаткових терапевтичних агентів.
27. Спосіб лікування захворювання або порушення, що залучає експресуючі CD38 клітини, у суб'єкта, де спосіб включає введення антитіла за будь-яким з пп. 1-21 або фармацевтичної композиції за п. 25 або 26 суб'єкту, що потребує цього.
28. Спосіб за п. 27, де інгібують ріст та/або проліферацію клітин, що експресують CD38, який включає введення антитіла за будь-яким з пп. 1-21 або фармацевтичної композиції за п. 25 або 26 так, що ріст та/або проліферація клітин інгібуються.
Текст
Реферат: Винахід належить до антитіла, яке зв’язується з CD38, клітини-хазяїна, фармацевтичної композиції, що містить дане антитіло, та способу лікування захворювання або порушення, опосередкованого СD38. UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Область техніки, до якої належить винахід Даний винахід стосується антитіл, що зв'язують CD38, які мають специфічні характеристики і які застосовуються для лікування inter alia множинної мієломи. Рівень техніки Множинна мієлома є злоякісним переродженням В-клітин, яке характеризується латентним накопиченням у кістковому мозку секреторних плазматичних клітин з низьким проліферативним індексом і збільшеною тривалістю життя. Це захворювання, в остаточному підсумку, атакує кості та кістковий мозок, що приводить до множинних пухлин і повсюдного ушкодження всієї кістякової системи. Приблизно 1% всіх ракових захворювань і трохи більше 10% всіх злоякісних гематологічних захворювань можна віднести до множинної мієломи (MM). Частота випадків MM зростає в старіючій популяції, де медіана віку встановлення цього діагнозу доводиться приблизно на 61 рік. Доступні зараз терапії множинної мієломи включають хіміотерапію, трансплантацію стовбурових клітин, Thalomid® (талідомід), Velcade® (ботремозид), Aredia® (памідронат) і Zometa® (золедронова кислота). На сьогодні, протоколи лікування, які включають сполучення хіміотерапевтических агентів, таких як вінкристин, BCNU, мельфалан, циклофосфамід, адріаміцин і преднізон або дексаметазон, приводять до частоти повної ремісії тільки близько 5% і медіана виживаності становить приблизно 36-48 місяців від моменту постановки діагнозу. Недавні досягнення при застосуванні хіміотерапії з високими дозами з наступною трансплантацією аутологічної тканини кісткового мозку або мононуклеарних клітин периферичної крові привели до збільшення відсотка повної ремісії та тривалості ремісії. Однак загальна виживаність збільшилася лише незначно і ніяких доказів лікування отримано не було. В остаточному підсумку, всі пацієнти із MM одержують рецидив хвороби навіть при підтримуючій терапії інтерферономальфа (IFN-) самим по собі або в сполученні зі стероїдами. Ефективність доступних режимів хіміотерапевтичного лікування при MM обмежена низькою швидкістю проліферації клітин і розвитком множинної стійкості до ліків. У більш ніж 90% хворих MM захворювання стає стійким до хіміотерапії. В результаті йде пошук альтернативних режимів лікування з метою розробки адоптивної імунотерапії, спрямованої на поверхневі антигени на плазматичних клітинах. CD38 є прикладом антигену, експресованого такими злоякісними плазматичними клітинами, він експресується при різних злоякісних захворюваннях крові, включаючи, без обмеження, хронічний лімфоцитарний лейкоз В-клітин, гострий лімфоцитарний лейкоз В-клітин, макроглобулінемію Валденстрема, первинний системний амілоїдоз, лімфому клітин мантії, пролімфоцитарний/мієлоцитарний лейкоз, гострий мієлоїдний лейкоз, хронічний мієлоїдний лейкоз, фолікулярну лімфому, лейкоз NK-клітин і лейкоз плазматичних клітин. Експресія CD38 описана для епітеліальних/ендотеліальних клітин різного походження, включаючи гранулярний епітелій простати, острівкові клітини підшлункової залози, епітелій проток у залозах, включаючи привушну залозу, клітини бронхіального епітелію, клітини яєчка та яєчників і клітини пухлини аденокарциноми ободової і прямої кишки. Захворювання, при яких може бути залучена експресія CD38, включають, без обмеження, бронхо-епітеліальні карциноми легенів, рак грудей (що розвився зі злоякісної проліферації епітеліальної вистілки проток і часток груди), пухлини підшлункової залози, пухлини, що розвилися з b-клітин, з епітелію кишечнику (наприклад, аденокарцинома та карцинома лускатих клітин). У ЦНС нейробластома експресує CD38. Інші захворювання включають карциному простати, семіноми яєчка та рак яєчника. У нормі, CD38 експресується гемопоетичними клітинами в щільних тканинах. Що стосується + гемопоетичних клітин, основна частина медулярних тимоцитів є CD38 , спочиваючі та цирку+ люючі Т- і В-клітини є CD38 , і активовані клітини є CD38 . CD38 також експресується в приблизно 80% спочиваючих NK клітин та моноцитів і лімфобластами центра розмноження лімфатичного вузла, плазматичними В-клітинами та деякими внутрішньофолікулярними клітинами. CD38 може також експресуватися деревоподібними клітинами. Значна частина нормальних клітин кісткового мозку, особливо клітини попередників, експресують CD38. До того ж, 50-80% кров'я+ них клітин пуповини є CD38 і залишається такими в крові людини протягом перших двох-трьох років життя. На додаток до лімфатичних клітин попередника, CD38 також експресується в еритроцитах і кров'яних пластинках. Що стосується твердих тканин, CD38 експресується в кишечнику інтраепітеліальними клітинами та лімфоцитами lamina propria, клітинами Пуркінье та нейрофібрилярними клубками мозку, епітеліальними клітинами простати, β-клітинами підшлункової залози, остеокластами костей, ретинальними клітинами ока, сарколемою гладкої та поперечно-смугастої мускулатури. Функції, приписувані CD38, включають як рецепторну роль в адгезії та передачі сигналу, так + і (екто)-ферментативну активність. Виступаючи в ролі ектоферменту, CD38 застосовує НАД як 1 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 субстрат для утворення циклічної АДФ-рибози (цАДФР) і АДФР, а також нікотинаміду та нікотинамідаденіндинуклеотидфосфату (НАДФ). Показано, що цАДФР є вторинним месенджером для 2+ вивільнення Са з ендоплазматичного ретикулума. На додаток до передачі сигналу за допомо2+ гою Са , опосередкована CD38 передача сигналу відбувається за допомогою взаємодії (crosstalk) з комплексами антиген-рецептор на Т- та В-клітинах або інших типах рецепторних комплексів, наприклад, молекулами МНС, і в такий спосіб включена в кілька клітинних відповідей, а також у перемикання та секрецію lgG1. AHTИ-CD38 антитіла описані в літературі, наприклад, в Lande R. et al., Cell Immunol. 220 (1), 30-8 (2002), Auciello CM et al., Tissue antigens 56(6), 539-547 (2000) та CotnerT. et al., Int. Immunopharmacol. 3(3), 255-268 (1981). У CD38 кілька функцій, які можуть активуватися або не активуватися молекулою, що зв'язалася з CD38. Наприклад, мишачі анти-СР38 антитіла ІВ4 мають агоністичними властивостями по відношенню до CD38. Показано, що ІВ4 індукують акти2+ вацію Т-клітин, на що вказує вивільнення (мобілізація) Са у клітинах Jurkat (Zubiaur V. et al., J. Immunol. 159(1), 193-205 (1997)), індукують значну проліферацію мононуклеарних клітин периферичної крові (РВМС), індукують вивільнення значних рівнів IL-6 та індукують вивільнення детектованих рівнів IFN- (Lande, Zubiaur Morra, Ansiello, supra). Розкриття винаходу Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке кодується (1) нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах, згідно SEQ ID NО:1 та SEQ ID NО:6, відповідно; (2) нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах, згідно SEQ ID NО:11 та SEQ ID NО:16, відповідно; (3) нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах, згідно SEQ ID NО:21 та SEQ ID NО:26, відповідно; або (4) нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах, які є консервативними модифікаціями послідовностей за пунктами (1), (2) або (3). Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH CDR3 з послідовністю згідно SEQ ID NО:10. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VL CDR3 з послідовністю згідно SEQ ID NO:5 та VH CDR3 з послідовністю згідно SEQ ID NO:10. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, де варіабельний район легкого ланцюга включає VL CDR1 з послідовністю згідно SEQ ID NO:3, VL CDR2 з послідовністю згідно SEQ ID NO:4 та VL CDR3 з послідовністю згідно SEQ ID NO:5, і варіабельний район важкого ланцюга включає VH CDR1 з послідовністю згідно SEQ ID NO:8, VH CDR2 з послідовністю згідно SEQ ID NO:9 таун CDR3 з послідовністю згідно SEQ ID NO:10. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VL район с амінокислотною послідовністю згідно SEQ ID NO:2. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VL район з амінокислотною послідовністю, яка має, щонайменше, 90%, наприклад, щонайменше, 95% ідентичності послідовності згідно SEQ ID NO:2. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район с амінокислотною послідовністю згідно SEQ ID NO:7. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район з амінокислотною послідовністю, що охоплює VH CDR1 - VH CDR3 район SEQ ID NO:7. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район з амінокислотною послідовністю, яка має, щонайменше, 90%, наприклад, щонайменше, 95% ідентичності послідовності згідно SEQ ID NO:7, або яка охоплює VH CDR3 -VH CDR3 район послідовності згідно SEQ ID NO:7. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район, що має 1-5, наприклад, 1-3 заміщення, делеції або додавання амінокислот у порівнянні з послідовністю згідно SEQ ID NO:7, або що охоплює VH CDR1 -VH CDR3 район SEQ ID NO:7. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L район, як визначено вище, i VH район, як визначено вище. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH CDR3 з послідовністю згідно SEQ ID NO:20. 2 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L CDR3 з послідовністю згідно SEQ ID NO:15 TaVH CDR3 з послідовністю згідно SEQ ID N0:20. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, де варіабельний район легкого ланцюга включає VL CDR1 з послідовністю згідно SEQ ID NO:13, VL CDR2 з послідовністю згідно SEQ ID NO:14 та VL CDR3 з послідовністю згідно SEQ ID NO:15, і варіабельний район важкого ланцюга включає VH CDR1 з послідовністю згідно SEQ ID NO:18, VH CDR2 з послідовністю згідно SEQ ID NO:19 тa VH CDR3 з послідовністю згідно SEQ ID NO:20. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VL район с амінокислотною послідовністю згідно SEQ ID NO:12. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L район з амінокислотною послідовністю, яка має, щонайменше, 90%, наприклад, щонайменше, 95% ідентичності послідовності згідно SEQ ID NO:12. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район с амінокислотною послідовністю згідно SEQ ID NO:17. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район, що включає амінокислотну послідовність, яка охоплює VH CDR1 -VH CDR3 район SEQ ID NO:17. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V H район з амінокислотною послідовністю, що має, щонайменше, 90%, наприклад, щонайменше, 95% ідентичності послідовності згідно SEQ ID NO:17, або що охоплює VH CDR1 -VH CDR3 район SEQ ID NO:17. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район, що має 1-5, наприклад, 1-3 заміщення, делеції або додавання амінокислот у порівнянні з послідовністю згідно SEQ ID NO:17, або що охоплює VH CDR1 -VH CDR3 район SEQ ID NO:17. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L район, як визначено вище, i VH район, як визначено вище. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH CDR3 з послідовністю згідно SEQ ID NO:30. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L CDR3 з послідовністю згідно SEQ ID NO:25 тa VH CDR3 з послідовністю згідно SEQ ID NO:30. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, де варіабельний район легкого ланцюга включає VL CDR1 з послідовністю згідно SEQ ID NO:23, VL CDR2 з послідовністю згідно SEQ ID NO:24 та VL CDR3 з послідовністю згідно SEQ ID NO:25, і варіабельний район важкого ланцюга включає VH CDR1 з послідовністю згідно SEQ ID NO:28, VH CDR2 з послідовністю згідно SEQ ID NO:29 та VH CDR3 з послідовністю згідно SEQ ID NO:30. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L район с амінокислотною послідовністю згідно SEQ ID NO:22. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V L район з амінокислотною послідовністю, що має, щонайменше, 90%, наприклад, щонайменше, 95% ідентичності послідовності згідно SEQ ID NO:22. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район с амінокислотною послідовністю згідно SEQ ID NO:27. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район с амінокислотною послідовністю, що охоплює VH CDR1 - VH CDR3 район SEQ ID NO:27. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає V H район з амінокислотною послідовністю, що має, щонайменше, 90%, наприклад, щонайменше, 95% ідентичності послідовності згідно SEQ ID N0:27 або що охоплює VH CDR1 -VH CDR3 район SEQ ID NO:27. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VH район, що має 1-5, наприклад, 1-3 заміщення, делеції або додавання амінокислот у порівнянні з послідовністю згідно SEQ ID NO:27, або що охоплює VH CDR1 -VH CDR3 район SEQ ID NO:27. Даний винахід пропонує антитіло, що зв'язується з CD38 людини, яке включає VL район, як визначено вище, і VH район, як визначено вище. Даний винахід пропонує пептид, який зв'язується з CD38 людини (SEQ ID NO:31) і який не зв'язується з мутантним CD38 людини, де залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, як визначено вище, де EC50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком феніла 3 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 ланіну (SEQ ID NO:34), становить менше 50%, наприклад, менше 10%, менше 5% або менше 1%, величини EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, що зв'язується з CD38 людини (SEQ ID NO:31) і не зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, як визначено вище, де ECso для зв'язування пептиду з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), становить менше 50%, наприклад, менше 10%, менше 5% або менше 1%, величини ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, як визначено вище, де згаданий пептид зв'язується з мутантним CD38 людини, у якому залишок треоніна в положенні 237 заміщений залишком аланіну (SEQ ID NO:32) в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, як визначено вище, де ЕС50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), відповідає 75%-125% величини EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, що зв'язується з CD38 людини (SEQ ID NO:31), де пептид має такі характеристики зв'язування: (1) зв'язується з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31), (2) зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31), і (3) зв'язується з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID N0:32), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, що зв'язується з CD38 людини (SEQ ID NO:31), де пептид має такі характеристики зв'язування: (1) не зв'язується з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31), (2) не зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31), і (3) зв'язується з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, де ЕС50 визначають за допомогою ELISA, як описано в прикладі 17 даного опису. Даний винахід пропонує пептид, що конкурує з антитілом відповідно до втілення (1) вище за зв'язування CD38. В одному втіленні конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу, де конкуренція визначена як сигнал, що становить, щонайменше, 90% при вимірюванні по поглинанню, або із застосуванням вимірів перехресного блокування, як описано в прикладі 7 винаходу, де конкуренція визначена як сигнал, що становить, щонайменше, 90% при вимірюванні по флуоресценції. Даний винахід пропонує пептид, який специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом, як визначено вище. Даний винахід пропонує пептид, що специфічно зв'язується з районом SKRNIQFSCKNIYR і районом EKVQTLEAWVIHGG CD38 людини (SEQ ID NO:31). Даний винахід пропонує пептид, який має, в основному, такі ж характеристики специфічного зв'язування з CD38 людини, як антитіло, що визначено вище. Даний винахід пропонує пептид, який зв'язується з CD38 людини, де антитіло має одну чи більше з таких характеристик: (1) діє як антагоніст CD38; (2) не індукує значну проліферацію мононуклеарних клітин периферичної крові, як визначають способом, описаним в прикладі 18 даного винаходу; (3) не індукує вивільнення значної кількості IL-6 моноцитами людини або мононуклеарними клітинами периферичної крові, як визначають способом, описаним в прикладі 19 даного винаходу; (4) не індукує вивільнення детектованої кількості IFN- Т-клітинами людини або мононуклеарними клітинами периферичної крові, як визначають способом, описаним в прикладі 20 даного винаходу; 4 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 (5) интерналізується клітинами, що експресують CD38, наприклад, інтерналізується клітинами CHO-CD38 протягом 5-15 хв. при 37 °С способом, описаним в прикладі 12 даного винаходу; (6) індукує ADCC, наприклад, зі значенням ЕС50 нижче 15 нг/мл, наприклад, нижче 10 нг/мл, у клітинах Daudi-luc і зі значенням ЕС50 нижче 75 нг/мл, наприклад, нижче 50 нг/мл, 30 нг/мл або 10 нг/мл, у клітинах MM, як визначають способом, описаним в прикладі 5 даного винаходу; (7) індукує CDC у присутності комплементу, наприклад, зі значенням ЕС 50 нижче 5 мкг/мл, наприклад, нижче 1 мкг/мл у клітинах Daudi-luc або CHO-CD38 відповідно до способу, описаному в прикладі 6 даного винаходу; (8) інгібує синтез цГДФР; (9) інгібує синтез цАДФР; -8 (10) зв'язується з CD38 людини зі спорідненістю (К D) нижче 10 М, наприклад, в інтервалі від -8 -11 -9 -10 10 Μ до 10 М, наприклад, в інтервалі від 710 М до 10 М, як визначають за допомогою поверхневого плазмонового резонансу, як описано в прикладі 20 даного винаходу. Даний винахід пропонує пептид, як описано вище, що інгібує синтез цГДФР не менш ніж на 25%, наприклад, не менш ніж на 30%, через 90 хв. у концентрації 3 мкг/мл, як визначають за допомогою спектроскопічного способу, описаного в прикладі 24 даного винаходу. Даний винахід пропонує пептид, як визначено вище, що інгібує синтез цАДФР не менш ніж на 25%, наприклад, не менш ніж на 30%, через 90 хв. у концентрації 3 мкг/мл, як визначають за допомогою ВЕРХ, як описано у Munshi et al., J. Biol. Chem. 275, 21566-21571 (2000). В одному втіленні пептид, як визначено вище, є моноклональним антитілом людини. Даний винахід пропонує антитіло, як визначено вище, яке відрізняється тим, що воно є повнорозмірним lgG1, lgG2, lgG3, lgG4, IgD, IgA, IgE або IgM антитілом, наприклад, lgG1 антитілом, краще, lgG1, антитілом або IgM антитілом, краще, IgM, антитілом. Даний винахід пропонує ізольоване моноклональне антитіло людини, яке включає (1) амінокислотну послідовність варіабельного району важкого ланцюга, вироблену з Hv1263/3M28(VHI) послідовності зародкової лінії людини і амінокислотну послідовність варіабельного району легкого ланцюга, вироблену з L15(VI) послідовності зародкової лінії людини, де антитіло людини зв'язується з CD38 людини, або (2) амінокислотну послідовність варіабельного району важкого ланцюга, вироблену з VH3DP-47/V3-23 (VHIII) ПОСЛІДОВНОСТІ зародкової лінії людини, і амінокислотну послідовність варіабельного району легкого ланцюга, одержану з L6 (VI) послідовності зародкової лінії людини, де антитіло людини зв'язується з CD38 людини. Даний винахід пропонує пептид, як визначено вище, де пептид глікозильований в еукаріотичній клітині. В одному втіленні, антитіло відповідно до винаходу є фрагментом антитіла або одиночним ланцюгом антитіла. Даний винахід пропонує пептид, як визначено вище, який далі включає лінкер хелатор для приєднання радіоізотопу. Даний винахід пропонує пептид, як визначено вище, що находиться, в основному, в ізольованому виді. Даний винахід пропонує ізольовану нуклеїнову кислоту, що кодує пептид, як визначено вище. Даний винахід пропонує експресуючий вектор, який включає послідовність нуклеїнової кислоти, що кодує пептид, як визначено вище. Даний винахід пропонує експресуючий вектор, що включає (1) VL нуклеотидну послідовність згідно SEQ ID NO:1, (2) VH нуклеотидну послідовність згідно SEQ ID NO:6, (3) VL нуклеотидну послідовність згідно SEQ ID NO:1 та VH нуклеотидну послідовність згідно SEQ ID NO:6, (4) VL нуклеотидну послідовність згідно SEQ ID NO:11, (5) VH нуклеотидну послідовність згідно SEQ ID NO:16, (6) VL нуклеотидну послідовність згідно SEQ ID NO:11 та VH нуклеотидну послідовність згідно SEQ ID NO:16, (7) VL нуклеотидну послідовність згідно SEQ ID NO:21, (8) VH нуклеотидну послідовність згідно SEQ ID NO:26, (9) VL нуклеотидну послідовність згідно SEQ ID NO:21 та VH нуклеотидну послідовність згідно SEQ ID NO:26. 5 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід пропонує експресуючий вектор, як визначено вище, який далі включає нуклеотидну послідовність, що кодує константний район легкого ланцюга, важкого ланцюга або обох легкого та важкого ланцюгів антитіла людини. Даний винахід пропонує експресуючий вектор, як визначено вище, де нуклеотидна послідовність, що кодує константний район легкого ланцюга, важкого ланцюга або обох легкого та важкого ланцюгів антитіла людини, кодує lgG1 антитіло. Даний винахід пропонує гібридому, що продукує моноклональне анти-СО38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають (1) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:1 та SEQ ID NO:6, відповідно; (2) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:11 та SEQ ID NO:16, відповідно; (3) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовностів їх варіабельних районах згідно SEQ ID NO:21 та SEQ ID NO:26, відповідно; або (4) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності в їх варіабельних районах, які є консервативними модифікаціями послідовностей відповідно до пунктів (1), (2) або (3). Даний винахід пропонує гібридому, яка продукує моноклональне анти-СО38 антитіло людини, що несе варіабельні райони важкого ланцюга та легкого ланцюга людини, які включають (1) варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:2 і варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:7, (2) варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:12 і варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:17, (3) варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:22 і варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:27, або (4) консервативні модифікації послідовностей у варіабельних районах амінокислотних послідовностей легкого ланцюга людини та важкого ланцюга людини відповідно до пунктів (1), (2) або (3). Даний винахід пропонує трансфектому, що продукує моноклональне анти-CD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають (1) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:1 та SEQ ID NO:6, відповідно; (2) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:11 та SEQ ID NO:16, відповідно; (3) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:21 та SEQ ID NO:26, відповідно; або (4) нуклеїнові кислоти легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах, що є консервативними модифікаціями послідовностей відповідно до пунктів (1), (2) або (3). Даний винахід пропонує трансфектому, яка продукує моноклональне анти-CD38 антитіло людини, що несе варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають (1) варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:2 і варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:7, (2) варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:12 і варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:17, (3) варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:22 і варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:27, або (4) консервативні модифікації послідовностей у варіабельних амінокислотних послідовностях легкого ланцюга людини та важкого ланцюга людини відповідно до пунктів (1), (2) або (3). Даний винахід пропонує еукаріотичну або прокаріотичну клітину хазяїна, що продукує пептид, як визначено вище. 6 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід пропонує еукаріотичну або прокаріотичну клітину хазяїна, що містить експресуючий вектор, як визначено вище. Даний винахід пропонує трансгенну тварину, що не є людиною, або рослину, які включають нуклеїнові кислоти, що кодують важкий ланцюг людини та легкий ланцюг людини, де тварина або рослина продукує детектовану кількість пептиду, як визначено вище. Даний винахід пропонує імунокон'югат, що включає пептид, як визначено вище, з'єднаний із цитотоксичним агентом, радіоізотопом або ліками. Даний винахід пропонує імунокон'югат, що включає пептид, як визначено вище, де пептид є мономерним ІgМ антитілом, з'єднаним із цитотоксичним агентом, радіоізотопом або ліками. Даний винахід пропонує біспецифічну чи мультиспецифічну молекулу, що включає пептид, як визначено вище, і специфічність зв'язування ефекторної клітини людини. Даний винахід пропонує біспецифічну чи мультиспецифічну молекулу, що включає пептид, як визначено вище, і специфічність зв'язування CD3, CD4, CD138, IL-15R, мембранно-зв'язаного або зв'язаного з рецептором TFN-, Fc рецептором людини або мембранно-зв'язаного чи зв'язаного з рецептором IL-15. Даний винахід пропонує фармацевтичну композицію, що включає пептид, як визначено вище, або імунокон'югат, як визначено вище, і фармацевтично прийнятний носій. Даний винахід пропонує фармацевтичну композицію, як визначено вище, що включає один чи більше додатковий терапевтичний агент. Даний винахід пропонує спосіб інгібування росту та/або проліферації клітин, експресуючих CD38, що включає введення пептиду, як визначено вище, імунокон'югата, як визначено вище, фармацевтичної композиції, як визначено вище, або експресуючого вектора, як визначено вище, так що ріст та/або проліферація клітин інгібується. Даний винахід пропонує спосіб лікування захворювання або порушення, що утягує клітини, які експресують CD38 у суб'єкта, де спосіб включає введення пептиду, як визначено вище, імунокон'югата, як визначено вище, фармацевтичної композиції, як визначено вище, або експресуючого вектора, як визначено вище, суб'єкту, який потребує цього. Даний винахід пропонує спосіб запобігання захворювання або порушення, що утягує клітини, які експресують CD38, де спосіб включає введення пептиду, як визначено вище, імунокон'югата, як визначено вище, фармацевтичної композиції, як визначено вище, або експресуючого вектора, як визначено вище, суб'єкту, який потребує цього. В одному втіленні захворювання або порушення є ревматоїдним артритом. В одному втіленні захворювання або порушення є множинною мієломою. В одному втіленні спосіб включає введення одного чи більше додаткового терапевтичного агента суб'єкту. В одному втіленні додаткові один чи більше терапевтичний агент вибирають із хіміотерапевтичного агента, протизапального агента, імуносупресивного та/або імуномодуляторного агента. В одному втіленні додаткові один чи більше терапевтичний агент вибирають із групи, що складається із цисплатину, гефітинібу, цетуксимабу, ритуксимабу, бевацизумабу, ерлотинібу, бортезомібу, талідоміду, памідронату, золедронової кислоти, клодронату, ризендронату, ібандронату, етидронату, алендронату, тилудронату, триокису миш'яку, леналідоміду, філграстиму, пегфілграстиму, зарграмостиму, суберройаніліду гідроксамової кислоти та SCIO-469. Даний винахід пропонує in vitro спосіб детектування наявності CD38 антигену або клітин, експресуючих CD38, у зразку, який включає: А) контактування зразка з пептидом, як визначено вище, в умовах, що дозволяють утворення комплексу між пептидом та CD38, і Б) детектування утворення цього комплексу. Даний винахід пропонує набір для детектування наявності CD38 антигену або клітин, експресуючих CD38, у зразку, що включає пептид, як визначено вище. Даний винахід пропонує in vivo спосіб детектування CD38 антигену або клітин, експресуючих CD38 у суб'єкта, який включає: А) введення пептиду, як визначено вище, в умовах, що дозволяють утворення комплексу між пептидом та CD38, і Б) детектування утвореного комплексу. Даний винахід пропонує антиідіотипове антитіло, що зв'язується з антитілом, як визначено вище. В одному втіленні антиідіотипове антитіло застосовують для детектування рівня антитіла, як визначено вище, у зразку. В одному втіленні антиідіотипове антитіло застосовують для детектування рівня моноклонального антитіла людини проти CD38 у зразку. 7 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 Короткий опис малюнків Фігура 1А показує зв'язування -003, -005 та антитіла контрольного ізотипу HuMab-KLH з СО38-трансфекованими СНО (CHO-CD38) клітинами при вимірюванні за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 4. Фігура 1Б показує зв'язування -024 та HuMab-KLH з СР38-трансфекованими СНО (CHOCD38) клітинами при вимірюванні за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 4. Фігура 2А показує зв'язування -003, -005 та HuMab-KLH з Daudi клітинами при вимірюванні за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 4. Фігура 2Б показує зв'язування -024 та HuMab-KLH з Daudi клітинами при вимірюванні за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 4. Фігура 3 показує зв'язування -003, -005, -024 та HuMab-KLH із клітинами множинної мієломи. Постановка експерименту описана в прикладі 4. Фігура 4А показує здатність -003 та -005 індукувати лізис клітин Daudi за допомогою ADCC у порівнянні з ритуксимабом та HuMab-KLH. Постановка експерименту описана в прикладі 5. Фігура 4Б показує здатність -024 індукувати лізис клітин Daudi за допомогою ADCC у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 5. Фігура 5А показує здатність -003, -005 та -024 індукувати лізис свіжих пухлинних клітин множинної мієломи за допомогою ADCC у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 5. Фігура 5Б показує здатність -003, -005 та -024 індукувати лізис свіжих пухлинних клітин лейкозу плазматичних клітин за допомогою ADCC у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 5. Фігура 6 показує здатність -003 та -005 індукувати лізис JK6L (клітин лінії множинної мієломи) за допомогою ADCC у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 5. Фігура 7 показує здатність -003 та -005 індукувати лізис АМО-1 (клітин лінії множинної мієломи) за допомогою ADCC у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 5. Фігура 8 показує СDС-опосередкований лізис Daudi-luc клітин, індукований -003 та -005, у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 9А показує CDC-опосередкований лізис CHO-CD38 клітин, індукований -003 та -005, у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 9Б показує CDC-опосередкований лізис CHO-CD38 клітин, індукований -024, у порівнянні з HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 10А показує CDC-опосередкований лізис 3% стійких до лікування пухлинних клітин у присутності -003, -005 та HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 10Б показує CDC-опосередкований лізис 9% стійких до лікування пухлинних клітин у присутності -003, -005 та HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 10В показує СDС-опосередкований лізис 30-40% стійких до лікування пухлинних клітин у присутності -003, -005 та HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 10Г показує CDC-опосередкований лізис 70% стійких до лікування пухлинних клітин у присутності -003, -005 та HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 10Д показує CDC-опосередкований лізис клітин множинної мієломи в присутності 024 та HuMab-KLH. Постановка експерименту описана в прикладі 6. Фігура 11 показує, що -003 та -005 не виявляють перехресного блокування зв'язування з CD38. Постановка експерименту описана в прикладі 7. Фігура 12А показує імуногістологічне фарбування макрофагів, лімфоцитів і плазматичних Вклітин за допомогою -003. Постановка експерименту описана в прикладі 10. Фігура 12Б показує імуногістологічне фарбування бронхіального епітелію за допомогою -003. Постановка експерименту описана в прикладі 10. Фігура 12У показує імуногістологічне фарбування міоцитів за допомогою -003. Постановка експерименту описана в прикладі 10. Фігура 12М показує імуногістологічне фарбування лімфоїдної тканини мавпи циномолгус за допомогою -003. Постановка експерименту описана в прикладі 10. Фігура 13А показує імуногістологічне фарбування макрофагів, лімфоцитів і плазматичних Вклітин за допомогою -005. Постановка експерименту описана в прикладі 10. Фігура 13Б показує імуногістологічне фарбування бронхіального епітелію за допомогою -005. Постановка експерименту описана в прикладі 10. 8 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 Фігура 13В показує імуногістологічне фарбування міоцитів за допомогою -005. Постановка експерименту описана в прикладі 10. Фігура 13Г показує імуногістологічне фарбування лімфоїдної тканини мавпи циномолгус за допомогою -005. Постановка експерименту описана в прикладі 10. Фігура 14А показує імуногістологічне фарбування ендотелія печінки за допомогою CD31. Постановка експерименту описана в прикладі 10. Фігура 14Б показує імуногістологічне фарбування ендотелія печінки за допомогою vWF. Постановка експерименту описана в прикладі 10. Фігура 14В показує імуногістологічне фарбування ендотелія печінки за допомогою анти-KLH. Постановка експерименту описана в прикладі 10. Фігура 14Г показує імуногістологічне фарбування ендотелія печінки за допомогою -003. Постановка експерименту описана в прикладі 10. Фігура 14Д показує імуногістологічне фарбування ендотелія печінки за допомогою -005. Постановка експерименту описана в прикладі 10. Фігура 15А показує перехресну реактивність -003 та -005 у порівнянні з HuMab-KLH на лімфоцитах мавпи циномолгус, вимірювану за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 11. Фігура 15Б показує перехресну реактивність -003 та -005 у порівнянні з HuMab-KLH на моноцитах мавпи циномолгус, вимірювану за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 11. Фігура 15В показує перехресну реактивність -003 та -005 у порівнянні з HuMab-KLH на РВМС мавп резус, вимірювану за допомогою проточної цитометрії. Постановка експерименту описана в прикладі 11. Фігура 16А показує інтерналізацію -003 при вимірюванні по гасінню флуоресценції етидій броміду. Постановка експерименту описана в прикладі 12. Фігура 16Б показує інтерналізацію -005 при вимірюванні по гасінню флуоресценції етидій броміду. Постановка експерименту описана в прикладі 12. Фігура 17А показує обумовлене -003 та -005 у порівнянні з анти-СD20 моноклональним антитілом (ритуксимаб) і HuMab-KLH інгібування росту пухлинних клітин у превентивній постановці при вимірюванні за допомогою in vivo SCID люциферазного одержання зображення. Постановка експерименту описана в прикладі 13. Фігура 17Б показує обумовлене -003 та -005 у порівнянні з анти-СD20 моноклональним антитілом (ритуксимаб) і HuMab-KLH інгібування росту пухлинних клітин у терапевтичній постановці І при вимірюванні за допомогою in vivo SCID люциферазного одержання зображення. Постановка експерименту описана в прикладі 13. Фігура 17В показує обумовлене -003 та -005 у порівнянні з анти-СD20 моноклональним антитілом (ритуксимаб) і HuMab-KLH інгібування росту пухлинних клітин у терапевтичній постановці II при вимірюванні за допомогою in vivo SCID люциферазного одержання зображення. Постановка експерименту описана в прикладі 13. Фігура 17Г показує обумовлене -003 та -024 у порівнянні з HuMab-KLH інгібування росту пухлинних клітин у терапевтичній постановці III при вимірюванні за допомогою in vivo SCID люциферазного одержання зображення. Постановка експерименту описана в прикладі 13. Фігура 18 показує індукцію апоптозу за допомогою -003 та -005 у порівнянні з анти-СD20 моноклональним антитілом (ритуксимаб) і HuMab-KLH зі зшивками та без них. Постановка експерименту описана в прикладі 14. Фігура 19 показує гістологічну оцінку СD38-позитивних клітин в імплантованих RA-SCID гетеротрансплантатах миші на 14 день після обробки анти-KLH (HuMab-KLH) або -005. Способи описані в прикладі 15. Фігура 20 показує гістологічну оцінку СD138-позитивних клітин в імплантованих RA-SCID гетеротрансплантатах миші на 14 день після обробки анти-KLH (HuMab-KLH) або -005. Способи описані в прикладі 15. Фігура 21 показує CD38 фарбування В-клітин у гетеротрансплантатах перед імплантацією (А) або після обробки анти-KLH (Б) або -005 (В). Способи описані в прикладі 15. Фігура 22 показує CD138 фарбування В-клітин у гетеротрансплантатах перед імплантацією (А) або після обробки анти-KLH (Б) або -005 (В). Способи описані в прикладі 15. Фігура 23 показує зв'язування -003 та -005 з диким типом і мутантним CD38 людини при вимірюванні за допомогою ELISA. 23A: зв'язування -003 та -005 з Т237А мутантом CD38 людини. 23Б: зв'язування -003 та -005 з Q272R мутантом CD38 людини. 23D: зв'язування -003 та -005 з S274F мутантом CD38 людини. Способи описані в прикладі 17. 9 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 Фігура 24 показує дію -003 та -005 у порівнянні з HuMab-KLH на проліферацію (А), продукцію IL-6 (Б) і продукцію IFN-γ (В) клітинами РВМС людини. Способи описані в прикладах 18, 19 та 20, відповідно. Фігура 25 показує ферментативну продукцію цГДФ-рибози в присутності різних концентрацій -003 (Б), -005 (В), -024 (Г) або анти-KLH (А). Способи описані в прикладі 23. Фігура 26 показує порівняння між -003 -005 та Morphosys антитілом ТН-3079 при CDC клітин CHO-CD38 (26А), CDC клітин Daudi (26Б) і ADCC клітин Daudi (26В). Послідовності відповідно до винаходу наведені в прикладеному списку послідовностей. SEQ ID NO:1 є нуклеотидною послідовністю VL району антитіла -003. SEQ ID NO:2 є амінокислотною послідовністю VL району антитіла -003. SEQ ID NO:3 є амінокислотною послідовністю VL CDR1 антитіла -003, що включає амінокислотні залишки 24-34 SEQ ID NO:2. SEQ ID NO:4 є амінокислотною послідовністю VL CDR2 антитіла -003, що включає амінокислотні залишки 50-56 SEQ ID NO:2. SEQ ID NO:5 є амінокислотною послідовністю VL CDR3 антитіла -003, що включає амінокислотні залишки 89-97 SEQ ID NO:2. SEQ ID NO:6 є нуклеотидною послідовністю VH району антитіла -003. SEQ ID NO:7 є амінокислотною послідовністю VH району антитіла -003. SEQ ID NO:8 є амінокислотною послідовністю VH CDR1 антитіла -003, що включає амінокислотні залишки 31-35 SEQ ID NO:7. SEQ ID NO:9 є амінокислотною послідовністю VH CDR2 антитіла -003, що включає амінокислотні залишки 50-66 SEQ ID NO:7. SEQ ID NO:10 є амінокислотною послідовністю VH CDR3 антитіла -003, що включає амінокислотні залишки 99-109 SEQ ID NO:7. SEQ ID NO:11 є нуклеотидною послідовністю VL району антитіла -005. SEQ ID NO:12 є амінокислотною послідовністю VL району антитіла -005. SEQ ID NO:13 є амінокислотною послідовністю V L CDR1 антитіла -005, що включає амінокислотні залишки 24-34 SEQ ID NO:12. SEQ ID NO:14 є амінокислотною послідовністю VLCDR2 антитіла -005, що включає амінокислотні залишки 50-56 SEQ ID NO:12. SEQ ID NO:15 є амінокислотною послідовністю V L CDR3 антитіла -005, що включає амінокислотні залишки 89-97 SEQ ID NO:12. SEQ ID NO:16 є нуклеотидною послідовністю VH району антитіла -005. SEQ ID NO:17 є амінокислотною послідовністю VH району антитіла -005. SEQ ID NO:18 є амінокислотною послідовністю VH CDR1 антитіла -005, що включає амінокислотні залишки 31-35 SEQ ID NO:17. SEQ ID NO:19 є амінокислотною послідовністю VH CDR2 антитіла -005, що включає амінокислотні залишки 50-66 SEQ ID NO:17. SEQ ID NO:20 є амінокислотною послідовністю VH CDR3 антитіла -005, що включає амінокислотні залишки 99-111 SEQ ID NO:17. SEQ ID NO:21 є нуклеотидною послідовністю VL району антитіла -024. SEQ ID NO:22 є амінокислотною послідовністю VL району антитіла -024. SEQ ID NO:23 є амінокислотною послідовністю V L CDR1 антитіла -024, що включає амінокислотні залишки 24-34 SEQ ID NO:22. SEQ ID NO:24 є амінокислотною послідовністю V L CDR2 антитіла -024, що включає амінокислотні залишки 50-56 SEQ ID NO:22. SEQ ID NO:25 є амінокислотною послідовністю V L CDR3 антитіла -024, що включає амінокислотні залишки 89-97 SEQ ID NO:22. SEQ ID NO:26 є нуклеотидною послідовністю VH району антитіла -024. SEQ ID NO:27 є амінокислотною послідовністю VH району антитіла -024. SEQ ID NO:28 є амінокислотною послідовністю VH CDR1 антитіла -024, що включає амінокислотні залишки 31-35 SEQ ID NO:27. SEQ ID NO:29 є амінокислотною послідовністю VH CDR2 антитіла -024, що включає амінокислотні залишки 50-66 SEQ ID NO:27. SEQ ID NO:30 є амінокислотною послідовністю VH CDR3 антитіла -024, що включає амінокислотні залишки 99-111 SEQ ID NO:27. SEQ ID NO:31 є послідовністю CD38 людини. SEQ ID NO:32 є послідовністю мутантного CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну. 10 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 SEQ ID NO:33 є послідовністю мутантного CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну. SEQ ID NO:34 є послідовністю мутантного CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну. Здійснення винаходу Даний винахід пропонує СО38-зв'язуючі пептиди («CD38BP»), які можна застосовувати для лікування, діагностики та запобігання різноманітних порушень, що втягують клітини, які експресують CD38, наприклад, множинної мієломи. В одному втіленні, CD38BP відповідно до винаходу є антитілом -003. -003 є моноклональним lgG1 антитілом людини, яке має VL район, що складається з послідовності згідно SEQ ID NO:2, та VH район, що складається з послідовності згідно SEQ ID NO:7. В одному втіленні, CD38BP відповідно до винаходу є антитілом -005. -005 є моноклональним lgG1 антитілом людини, яке має VL район, що складається з послідовності згідно SEQ ID NO:12, та VH район, що складається з послідовності згідно SEQ ID NO:17. В одному втіленні, CD38BP відповідно до винаходу є антитілом -024. -024 є моноклональним lgG1 антитілом людини, яке має VL район, що складається з послідовності згідно SEQ ID NO:22, та VH район, що складається з послідовності згідно SEQ ID NO:27. Антитіла взаємодіють із антигенами мішені первинно через амінокислотні залишки, які розташовані в шести районах важкого та легкого ланцюга (CDR), що визначають комплементарність. Через це амінокислотні послідовності усередині CDR більше розрізняються між індивідуальними антитілами, ніж послідовності за межами CDR. Оскільки CDR послідовності відповідають за більшу частину взаємодій антиген-антитіло, можливо експресувати рекомбинантні антитіла, які симулюють властивості специфічних антитіл, що зустрічаються в природі, за допомогою створення експресуючих векторів, які включають CDR послідовності зі специфічних антитіл, що зустрічаються в природі, вставлені серед каркасних послідовностей іншого антитіла з іншими властивостями (див., наприклад, Riechmann et al., Nature 332, 323-327 (1998), Jones et al., Nature 321, 522-525 (1986), Queen et al., PNAS USA 86, 10029-10033 (1989)). Оскільки в даній області техніки добре відомо, що CDR3 домени важкого ланцюга антитіла грають особливо важливу роль у специфічності/спорідненості зв'язування антитіла з антигеном (Ditzel H.J. et al., J. Immunol. 157(2), 739-49 (1996), Barbas S.M. et al., J. Am. Chem. Soc. 116, 2161-2162 (1994), Barbas S.M. et al., Proc. Natl. Acad. Sci. USA 92(7), 2529-33 (1995)), CD38BP за винаходом можуть включати CDR3 важкого ланцюга антитіл -003, -005 або -024. CD38BP за винаходом можуть також включати CDR3 важкого та легкого ланцюга антитіл -003, -005 або -024. CD38BP за винаходом можуть далі включати CDR2 антитіл -003, -005 та -024, відповідно. CD38BP за винаходом можуть далі включати CDR1 антитіл -003, -005 та -024, відповідно. Даний винахід пропонує CD38BP, які конкурують із -003 за зв'язування з CD38. Даний винахід пропонує CD38BP, які конкурують із -005 за зв'язування з CD38. Даний винахід пропонує CD38BP, які конкурують із -024 за зв'язування з CD38. В одному втіленні конкуренцію визначають за допомогою ELISA, як описано в розділі прикладів. В одному втіленні конкуренцію визначають за допомогою FACS, як описано в розділі прикладів. Даний винахід пропонує CD38BP, що специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілами -003 або -005 або -024. Даний винахід пропонує CD38BP, що має, в основному, такі ж характеристики специфічного зв'язування по відношенню до CD38 людини, як -003 або -005 або -024. Даний винахід пропонує CD38BP, який включає V L CDR1, що складається, в основному, з SEQ ID NO:3. Даний винахід пропонує CD38BP, який включає V L CDR2, що складається, в основному, з SEQ ID NO:4. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:5. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:5, та VL CDR1, що складається, в основному, з SEQ ID NO:3. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:5, та VL CDR2, що складається, в основному, з SEQ ID NO:4. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:5, та VL CDR2, що складається, в основному, з SEQ ID NO:4, та VL CDR1, що складається, в основному, з SEQ ID NO:3. 11 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід пропонує CD38BP, який включає VH CDR1, що складається, в основному, з SEQ ID NO:8. Даний винахід пропонує CD38BP, який включає VH CDR2, що складається, в основному, з SEQ ID NO:9. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:10. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:10, та VH CDR1, що складається, в основному, з SEQ ID NO:8. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:10, та VH CDR2, що складається, в основному, з SEQ ID NO:9. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:10, та VH CDR2, що складається, в основному, з SEQ ID NO:9, та VH CDR1, що складається, в основному, з SEQ ID NO:8. Даний винахід пропонує CD38BP, який включає V L CDR1, що складається, в основному, з SEQ ID NO:13. Даний винахід пропонує CD38BP, який включає V L CDR2, що складається, в основному, з SEQ ID NO:14. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:15. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:15, та VL CDR1, що складається, в основному, з SEQ ID NO:13. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:15, та VL CDR2, що складається, в основному, з SEQ ID NO:14. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:15, та VL CDR2, що складається, в основному, з SEQ ID N0:14, та VL CDR1, що складається, в основному, з SEQ ID NO:13. Даний винахід пропонує CD38BP, який включає VH CDR1, що складається, в основному, з SEQ ID NO:18. Даний винахід пропонує CD38BP, який включає VH CDR2, що складається, в основному, з SEQ ID NO:19. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:20. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:20, та VH CDR1, що складається, в основному, з SEQ ID NO:18. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:20, та VH CDR2, що складається, в основному, з SEQ ID NO:19. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:20, та VH CDR2, що складається, в основному, з SEQ ID NO:19, та VH CDR1, що складається, в основному, з SEQ ID NO:18. Даний винахід пропонує CD38BP, який включає V L CDR1, що складається, в основному, з SEQ ID NO:23. Даний винахід пропонує CD38BP, який включає V L CDR2, що складається, в основному, з SEQ ID NO:24. Даний винахід пропонує CD38BP, який включає VL CDR3, що складається, в основному, з SEQ ID NO:25. Даний винахід пропонує CD38BP, який включає VL CDR3, що складається, в основному, з SEQ ID NO:25, та VL CDR1, що складається, в основному, з SEQ ID NO:23. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:25, та VL CDR2, що складається, в основному, з SEQ ID NO:24. Даний винахід пропонує CD38BP, який включає V L CDR3, що складається, в основному, з SEQ ID NO:25, та VL CDR2, що складається, в основному, з SEQ ID NO:24, та VL CDR1, що складається, в основному, з SEQ ID NO:23. Даний винахід пропонує CD38BP, який включає VH CDR1, що складається, в основному, з SEQ ID NO:28. Даний винахід пропонує CD38BP, який включає VH CDR2, що складається, в основному, з SEQ ID NO:29. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:30. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:30, та VH CDR1, що складається, в основному, з SEQ ID NO:28. 12 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:30, та VH CDR2, що складається, в основному, з SEQ ID NO:29. Даний винахід пропонує CD38BP, який включає VH CDR3, що складається, в основному, з SEQ ID NO:30, та VH CDR2, що складається, в основному, з SEQ ID NO:29, та VH CDR1, що складається, в основному, з SEQ ID NO:28. Даний винахід пропонує CD38BP, який включає (а) перший VL район, що включає три VL CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:3, SEQ ID NO:4 та SEQ ID NO:5, і (б) перший VH район, що включає три VH CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:8, SEQ ID NO:9 та SEQ ID NO:10. Даний винахід пропонує CD38BP, який включає (а) перший VL район, що включає три VL CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:13, SEQ ID NO:14 та SEQ ID NO:15, і (б) перший VH район, що включає три VH CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:18, SEQ ID NO:19 та SEQ ID NO:20. Даний винахід пропонує CD38BP, який включає (а) перший VL район, що включає три VL CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:23, SEQ ID NO:24 та SEQ ID NO:25, і (б) перший VH район, що включає три VH CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:28, SEQ ID NO:29 та SEQ ID NO:30. В одному втіленні VL район та VH район обидва розташовані на одному ланцюзі пептиду. В наступному втіленні VL район та VH район розділені гнучким лінкером. В одному втіленні VL район та VH район розташовані на різних ланцюгах пептиду. В наступному втіленні VL район та VH район розташовані на різних ланцюгах пептиду скрученого білка імуноглобуліну. В одному втіленні перший VL район і перший VH район орієнтовані таким чином, що три CDR в VL районі та три CDR в VH районі кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. В наступному втіленні пептид включає другий VL район, ідентичний першому VL району, та другий VH район, ідентичний першому VH району, де другий VL район і другий VH район кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Даний винахід пропонує CD38BP, який включає VL район, що є функціональним варіантом VL району антитіла -003 або -005 або -024. В одному втіленні VL район CD38BP складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:2 або SEQ ID NO:12 або SEQ ID NO:22, відповідно. В одному втіленні, CD38BP має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 80%, щонайменше, приблизно 90% або, щонайменше, приблизно 95% епітоп-зв'язуючих характеристик антитіл -003 або -005 або 024, відповідно. Даний винахід пропонує CD38BP, який включає V H район, що є функціональним варіантом VH району антитіла -003 або -005 або -024. В одному втіленні VH район пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:7 або SEQ ID NO:17 або SEQ ID NO:27, відповідно. В одному втіленні, CD38BP має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 80%, щонайменше, приблизно 90% або, щонайменше, приблизно 95% епітоп-зв'язуючих характеристик антитіл -003 або -005 або 024, відповідно. Даний винахід пропонує CD38BP, який включає, щонайменше, один CDR, що є функціональним варіантом CDR антитіла -003 або -005 або -024. В одному втіленні, щонайменше, один з CDR пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності 13 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 послідовності амінокислот послідовності згідно SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:8, SEQ ID NO:9 чи SEQ ID NO:10, або згідно SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:18, SEQ ID NO:19 чи SEQ ID NO:20, або згідно SEQ ID NO:23, SEQ ID NO:24, SEQ ID NO:25, SEQ ID NO:28, SEQ ID NO:29 чи SEQ ID NO:30, відповідно. В одному втіленні, CD38BP має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 80%, щонайменше, приблизно 90% або, щонайменше, приблизно 95% епітоп-зв'язуючих характеристик антитіла -003 або -005 або -024, відповідно. В одному втіленні, CD38BP має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 80%, щонайменше, приблизно 90% або, щонайменше, приблизно 95% спорідненості, авідності чи специфічності антитіла -003 або -005 або -024. В одному втіленні CD38BP конкурує з -003 або -005 або -024 за зв'язування CD38. В наступному втіленні конкуренцію вимірюють за допомогою ELISA, як описано в розділі прикладів. В іншому подальшому втіленні конкуренцію вимірюють за допомогою FACS, як описано в розділі прикладів. В одному втіленні CD38BP специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом -003 або -005 або -024. В одному втіленні CD38BP зв'язується з CD38 людини з більшою спорідненістю, ніж -003 або -005 або -024. В одному втіленні CD38BP має, в основному, такі ж характеристики специфічного зв'язування CD38, як -003 або -005 або -024. В одному втіленні CD38BP, в основному, вільний від інших зв'язуючих CD38 пептидів. В одному втіленні CD38BP за даним винаходом є антитілом. В наступному втіленні CD38BP є антитілом людини. В іншому подальшому втіленні CD38BP є гуманізованим антитілом. В іншому подальшому втіленні CD38BP є хімерним антитілом. В іншому втіленні антитіло за даним винаходом є моноклональним антитілом. В одному втіленні антитіло згідно з даним винаходом є lgG1, lgG2, lgG3, lgG4, IgD, IgA, IgE або IgM антитілом. В наступному втіленні антитіло є lgG1 антитілом. В наступному втіленні антитіло є lgG1, антитілом. В іншому подальшому втіленні антитіло є IgM антитілом. В іншому подальшому втіленні антитіло є ІgМ, антитілом. В одному втіленні антитіло згідно з даним винаходом є фрагментом антитіла або одиночним ланцюгом антитілом. В одному втіленні CD38BP глікозильований в еукаріотичній клітині. В одному втіленні CD38BP далі включає лінкер хелатор для приєднання радіоізотопу. В одному втіленні CD38BP находиться, в основному, в ізольованій формі. Даний винахід пропонує ізольовану нуклеїнову кислоту, що кодує CD38BP за даним винаходом. Даний винахід пропонує експресуючий вектор, який включає послідовність нуклеїнової кислоти, що кодує CD38BP згідно з даним винаходом. В одному втіленні експресуючий вектор включає VL нуклеотидну послідовність згідно SEQ ID NO:1, VH нуклеотидну послідовність згідно SEQ ID NO:6 або VL нуклеотидну послідовність згідно SEQ ID NO:1 та VH нуклеотидну послідовність згідно SEQ ID NO:6. В одному втіленні експресуючий вектор включає VL нуклеотидну послідовність згідно SEQ ID NO:11, VH нуклеотидну послідовність згідно SEQ ID NO:16 або VL нуклеотидну послідовність згідно SEQ ID N0:11 та VH нуклеотидну послідовність згідно SEQ ID NO:16. В одному втіленні експресуючий вектор включає VL нуклеотидну послідовність згідно SEQ ID NO:21, VH нуклеотидну послідовність згідно SEQ ID NO:26 або VL нуклеотидну послідовність згідно SEQ ID NO:21 та VH нуклеотидну послідовність згідно SEQ ID NO:26. В наступному втіленні експресуючий вектор далі включає нуклеотидну послідовність, що кодує константний район легкого ланцюга, важкого ланцюга або обох легкого та важкого ланцюгів антитіла людини. В наступному втіленні нуклеотидна послідовність, що кодує константний район легкого ланцюга, важкого ланцюга або обох легкого та важкого ланцюгів антитіла людини, кодує lgG1 антитіло. Даний винахід пропонує гібридому, що продукує моноклональне анти-СО38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності у варіабельному районі легкого ланцюга згідно SEQ ID NO:1 або консервативні модифікації їхніх послідовностей і нуклеотидні послідовності у варіабельному районі важкого ланцюга згідно SEQ ID NO:6 або консервативні модифікації їх послідовностей. В одному втіленні, нуклеїнова кислота легкого ланцюга людини включає нуклеотидну 14 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 послідовність згідно SEQ ID NO:1, і нуклеїнова кислота важкого ланцюга людини включає нуклеотидну послідовність згідно SEQ ID NO:6. Даний винахід пропонує гібридому, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:2 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:7 або консервативні модифікації цієї послідовності. В одному втіленні варіабельний район легкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:2 і варіабельний район важкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:7. Даний винахід пропонує трансфектому, що продукує моноклональне анти-CD38 антитіло людини, кодоване нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:1 або консервативними модифікаціями цієї послідовності та нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:6 або консервативними модифікаціями цієї послідовності. В одному втіленні моноклональне анти-СО38 антитіло людини кодується нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:1 і нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:6. Даний винахід пропонує трансфектому, яка продукує моноклональне анти-CD38 антитіло людини, що включає варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:2 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:7 або консервативнімодифікації цієї послідовності. В одному втіленні легкий ланцюг людини включає варіабельну амінокислотну послідовність згідно SEQ ID NO:2 і важкий ланцюг людини включає варіабельну амінокислотну послідовність згідно SEQ ID NO:7. Даний винахід пропонує гібридому, яка продукує моноклональне анти-СD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності у варіабельному районі легкого ланцюга згідно SEQ ID NO:11 або консервативні модифікації цих послідовностей, і нуклеотидні послідовності у варіабельному районі важкого ланцюга згідно SEQ ID NO:16 або консервативні модифікації цих послідовностей. В одному втіленні, нуклеїнова кислота легкого ланцюга людини включає нуклеотидну послідовність згідно SEQ ID NO:11, і нуклеїнова кислота важкого ланцюга людини включає нуклеотидну послідовність згідно SEQ ID NO:16. Даний винахід пропонує гібридому, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають амінокислотну послідовність у варіабельному районі легкого ланцюга згідно SEQ ID NO:12 або консервативні модифікації цієї послідовності, та амінокислотну послідовність у варіабельному районі важкого ланцюга згідно SEQ ID NO:17 або консервативні модифікації цієї послідовності. В одному втіленні варіабельний район легкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:12, і варіабельний район важкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:17. Даний винахід пропонує трансфектому, яка продукує моноклональне анти-CD38 антитіло людини, кодоване нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:11 або консервативними модифікаціями цієї послідовності, та нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:16 або консервативними модифікаціями цієї послідовності. В одному втіленні моноклональне анти-СD38 антитіло людини кодується нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:11 і нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:16. Даний винахід пропонує трансфектому, яка продукує моноклональне анти-CD38 антитіло людини, що включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:12 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:17 або консервативні модифікації цієї послідовності. В одному втіленні легкий ланцюг людини включає варіабельну амінокислотну послідовність згідно SEQ ID NO:12 і важкий ланцюг людини включає варіабельну амінокислотну послідовність згідно SEQ ID NO:17. Даний винахід пропонує гібридому, яка продукує моноклональне анти-СD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидну послідовність у варіабельному районі легкого ланцюга згідно SEQ ID NO:21 або консервативні модифікації цієї послідовності, та нуклеотидну послідовність у варіа 15 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 бельному районі важкого ланцюга згідно SEQ ID NO:26 або консервативні модифікації цієї послідовності. В одному втіленні, нуклеїнова кислота легкого ланцюга людини включає нуклеотидну послідовність згідно SEQ ID NO:21, і нуклеїнова кислота важкого ланцюга людини включає нуклеотидну послідовність згідно SEQ ID NO:26. Даний винахід пропонує гібридому, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:22 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга згідно SEQ ID NO:27 або консервативні модифікації цієї послідовності. В одному втіленні варіабельний район легкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:22, і варіабельний район важкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:27. Даний винахід пропонує трансфектому, яка продукує моноклональне анти-CD38 антитіло людини, кодоване нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:21 або консервативними модифікаціями цієї послідовності, та нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:26 або консервативними модифікаціями цієї послідовності. В одному втіленні моноклональне анти-СО38 антитіло людини кодується нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:21 і нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:26. Даний винахід пропонує трансфектому, яка продукує моноклональне анти-CD38 антитіло людини, що включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:22 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:27 або консервативні модифікації цієї послідовності. В одному втіленні легкий ланцюг людини включає варіабельну амінокислотну послідовність згідно SEQ ID NO:22, і важкий ланцюг людини включає варіабельну амінокислотну послідовність згідно SEQ ID NO:27. Даний винахід пропонує еукаріотичну або прокаріотичну клітину хазяїна, що продукує CD38BP згідно з даним винаходом. Даний винахід пропонує еукаріотичну або прокаріотичну клітину хазяїна, що містить експресуючий вектор згідно з даним винаходом. Даний винахід пропонує трансгенну тварину, відмінну від людини, або рослину, які включають нуклеїнові кислоти, що кодують важкий ланцюг людини та легкий ланцюг людини, де тварина або рослина продукує детектовану кількість CD38BP згідно з даним винаходом. Даний винахід пропонує імунокон'югат, що включає CD38BP згідно з даним винаходом, з'єднаний із цитотоксичним агентом, радіоізотопом або ліками. В одному втіленні пептид є мономерним ІgМ антитілом, з'єднаним із цитотоксичним агентом, радіоізотопом або ліками. Даний винахід пропонує біспецифічну чи мультиспецифічну молекулу, що включає CD38BP згідно з даним винаходом і специфічність зв'язування ефекторної клітини людини. В одному втіленні специфічність зв'язування ефекторної клітини людини є специфічністю зв'язування CD3, CD4, CD138, IL-15R, мембранно-зв'язаного або зв'язаного з рецептором TFN-, Fc рецептором людини або мембранно-зв'язаного чи зв'язаного з рецептором IL-15. Даний винахід пропонує антиідіотипове антитіло, що зв'язується з CD38BP згідно з даним винаходом. Даний винахід пропонує застосування антиідіотипового антитіла згідно з даним винаходом для детектування рівня моноклонального антитіла людини проти CD38 у зразку. Далі йде список вибраних втілень даного винаходу. Втілення 1: антитіло, що зв'язується з CD38 людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:1 та SEQ ID NO:6, відповідно або консервативні модифікації їх послідовності. Втілення 2: антитіло, що зв'язується з CD38 людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:1 та SEQ ID NO:6, відповідно. Втілення 3: антитіло, що зв'язується з CD38 людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:11 та SEQ ID NO: 16, відповідно або консервативні модифікації їх послідовності. 16 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Втілення 4: антитіло, що зв'язується з CD38 людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:11 та SEQ ID NO:16, відповідно. Втілення 5: антитіло, що зв'язується з CD38 людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:21 та SEQ ID NO:26, відповідно або консервативні модифікації їх послідовності. Втілення 6: антитіло, що зв'язується з CD38 людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності в їх варіабельних районах згідно SEQ ID NO:21 та SEQ ID NO:26, відповідно. Втілення 7: пептид, що конкурує з антитілом відповідно до втілення 2 за зв'язування з CD38. Втілення 8: пептид за втіленням 7, де конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу. Втілення 9: пептид за втіленням 7, де конкуренцію визначають шляхом вимірювання перехресного блокування, як описано в прикладі 7 винаходу. Втілення 10: пептид, що специфічно зв'язується з епітопом CD38, де епітоп також специфічно зв'язується антитілом відповідно до втілення 2. Втілення 11: пептид, що має в основному такі ж характеристики специфічного зв'язування для зв'язування CD38 людини, як антитіло відповідно до втілення 2. Втілення 12: пептид, який включає VL CDR1, що складається, в основному, з SEQ ID NO:3. Втілення 13: пептид, який включає VL CDR2, що складається, в основному, з SEQ ID NO:4. Втілення 14: пептид, який включає VL CDR3, що складається, в основному, з SEQ ID NO:5. Втілення 15: пептид відповідно до втілення 14, де пептид включає також V L CDR1, що складається, в основному, з SEQ ID NO:3. Втілення 16: пептид відповідно до втілення 14, де пептид включає також V L CDR2, що складається, в основному, з SEQ ID NO:4. Втілення 17: пептид відповідно до втілення 16, де пептид включає також VL CDR1, що складається, в основному, з SEQ ID NO:3. Втілення 18: пептид, який включає VH CDR1, що складається, в основному, з SEQ ID NO:8. Втілення 19: пептид, який включає VH CDR2, що складається, в основному, з SEQ ID NO:9. Втілення 20: пептид, який включає VH CDR3, що складається, в основному, з SEQ ID NO:10. Втілення 21: пептид відповідно до втілення 20, де пептид включає також VH CDR1, що складається, в основному, з SEQ ID NO:8. Втілення 22: пептид відповідно до втілення 20, де пептид включає також V H CDR2, що складається, в основному, з SEQ ID NO:9. Втілення 23: пептид відповідно до втілення 22, де пептид включає також V H CDR1, що складається, в основному, з SEQ ID NO:8. Втілення 24: пептид, який включає (а) перший VL район, що включає три VL CDR, які незалежно один від одного складаються, в основному, з SEQ ID N0:3, SEQ ID NO:4 та SEQ ID NO:5, і (б) перший VH район, що включає три VH CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:8, SEQ ID NO:9 та SEQ ID NO:10. Втілення 25: пептид відповідно до втілення 24, де VL район та VH район обидва розташовані на одному ланцюзі пептиду. Втілення 26: пептид відповідно до втілення 24, де V L район та VH район розділені гнучким лінкером. Втілення 27: пептид відповідно до втілення 24, де VL район та VH район розташовані на різних ланцюгах пептиду. Втілення 28: пептид відповідно до втілення 24, де VL район та VH район розташовані на різних ланцюгах пептиду в скрученому білку імуноглобуліну. Втілення 29: пептид відповідно до втілень 24-28, де перший VL район і перший VH район орієнтовані таким чином, що три CDR в VL районі та три CDR в VH районі кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Втілення 30: пептид відповідно до втілення 29, де пептид включає другий V L район, ідентичний першому VL району, та другий VH район, ідентичний першому VH району, де другий VL район і другий VH район кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Втілення 31: пептид, який включає VL район, що є функціональним варіантом VL району антитіла відповідно до втілення 2. 17 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Втілення 32: пептид відповідно до втілення 31, де VL район пептиду складається, в основному, з послідовності, що має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:2. Втілення 33: пептид, який включає VH район, що є функціональним варіантом VH району антитіла відповідно до втілення 2. Втілення 34: пептид відповідно до втілення 33, де VH район пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:7. Втілення 35: пептид, який включає, щонайменше, один CDR, що є функціональним варіантом CDR антитіла відповідно до втілення 2. Втілення 36: пептид відповідно до втілення 35, де, щонайменше, один CDR пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:8, SEQ ID NO:9, SEQ ID ΝΟ:10. Втілення 37: пептид відповідно до будь-якого з втілень від 31 до 36, де пептид має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% епітоп-зв'язуючих характеристик антитіла відповідно до втілення 2. Втілення 38: пептид відповідно до будь-якого з втілень від 31 до 36, де пептид має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% спорідненості, авідності або специфічності антитіла відповідно до втілення 2. Втілення 39: пептид відповідно до будь-якого з втілень від 12 до 38, де пептид специфічно зв'язує CD38 людини. Втілення 40: пептид відповідно до будь-якого з втілень від 12 до 39, де пептид конкурує з антитілом відповідно до втілення 2 за зв'язування CD38. Втілення 41: пептид відповідно до втілення 40, де конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу. Втілення 42: пептид відповідно до втілення 7, де конкуренцію визначають шляхом визначення перехресного блокування, як описано в прикладі 7 винаходу. Втілення 43: пептид відповідно до втілення 39, де пептид специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом відповідно до втілення 2. Втілення 44: пептид відповідно до будь-якого з втілень від 39 до 43, де пептид зв'язується з CD38 людини з більшою спорідненістю, ніж антитіло відповідно до втілення 2. Втілення 45: пептид відповідно до будь-якого з втілень від 39 до 43, де пептид має, в основному, такі ж характеристики специфічного зв'язування CD38, як антитіло відповідно до втілення 2. Втілення 46: пептид відповідно до будь-якого з втілень від 39 до 45, де пептид, що зв'язує CD38, в основному, вільний від інших пептидів, що зв'язують CD38. Втілення 47: пептид, що зв'язується з CD38 людини (SEQ ID NO:31) і не зв'язується з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Втілення 48: пептид відповідно до втілення 47, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 50% величини ЕС 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 49: пептид відповідно до втілення 48, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 10% ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 50: пептид відповідно до втілення 49, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну 18 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 (SEQ ID NO:34), становить менше 5% ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 51: пептид відповідно до втілення 50, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 1% ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 52: пептид, що зв'язується з CD38 людини (SEQ ID NO:31) і не зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Втілення 53: пептид відповідно до втілення 52, де ЕС50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 50% величини ЕС 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 54: пептид відповідно до втілення 53, де ЕС50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 10% величини EC 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 55: пептид відповідно до будь-якого з втілень від 47 до 51, що не зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Втілення 56: пептид відповідно до втілення 55, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID N0:34), становить менше 50% величини ЕС5о для зв'язування пептиду з CD38 людини (SEQ ID N0:31). Втілення 57: пептид відповідно до втілення 55, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 10% величини EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 58: пептид відповідно до будь-якого з втілень від 47 до 57, де згаданий пептид зв'язується з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Втілення 59: пептид відповідно до втілення 58, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 75% величини EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 60: пептид відповідно до втілення 59, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 85% величини EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 61: пептид відповідно до втілення 60, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 90% величини ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 62: пептид відповідно до втілення 61, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 95% величини ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 63: пептид, що конкурує з антитілом відповідно до втілення 4 за зв'язування CD38. Втілення 64: пептид відповідно до втілення 63, де конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу. Втілення 65: пептид відповідно до втілення 63, де конкуренцію визначають шляхом вимірювання перехресного блокування, як описано в прикладі 7 винаходу. Втілення 66: пептид, що специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом відповідно до втілення 4. Втілення 67: пептид, що має, в основному, такі ж характеристики специфічного зв'язування CD38, як антитіло відповідно до втілення 4. Втілення 68: пептид, який включає VL CDR1, що складається, в основному, з SEQ ID NO:13. Втілення 69: пептид, який включає VL CDR2, що складається, в основному, з SEQ ID NO:14. Втілення 70: пептид, який включає VL CDR3, що складається, в основному, з SEQ ID NO:15. 19 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Втілення 71: пептид відповідно до втілення 70, де пептид включає також V L CDR1, що складається, в основному, з SEQ ID NO:13. Втілення 72: пептид відповідно до втілення 70, де пептид включає також VL CDR2, що складається, в основному, з SEQ ID NO:14. Втілення 73: пептид відповідно до втілення 72, де пептид включає також V L CDR1, що складається, в основному, з SEQ ID NO:13. Втілення 74: пептид, який включає VH CDR1, що складається, в основному, з SEQ ID NO:18. Втілення 75: пептид, який включає VH CDR2, що складається, в основному, з SEQ ID NO:19. Втілення 76: пептид, який включає VH CDR3, що складається, в основному, з SEQ ID NO:20. Втілення 77: пептид відповідно до втілення 76, де пептид включає також VH CDR1, що складається, в основному, з SEQ ID NO:18. Втілення 78: пептид відповідно до втілення 76, де пептид включає також VH CDR2, що складається, в основному, з SEQ ID NO:19. Втілення 79: пептид відповідно до втілення 78, де пептид включає також VH CDR1, що складається, в основному, з SEQ ID NO:18. Втілення 80: пептид, який включає (а) перший VL район, що включає три VL CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:13, SEQ ID NO:14 та SEQ ID NO:15, і (б) перший VH район, що включає три VH CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:18, SEQ ID NO:19 та SEQ ID NO:20. Втілення 81: пептид відповідно до втілення 80, де VL район та VH район обидва розташовані на одному ланцюзі пептиду. Втілення 82: пептид відповідно до втілення 81, де V L район та VH район розділені гнучким лінкером. Втілення 83: пептид відповідно до втілення 80, де VL район та VH район розташовані на різних ланцюгах пептиду. Втілення 84: пептид відповідно до втілення 83, де VL район та VH район розташовані на різних ланцюгах пептиду в скрученому білку імуноглобуліну. Втілення 85: пептид відповідно до втілень 80-84, де перший VL район і перший VH район орієнтовані таким чином, що три CDR в VL районі та три CDR в VH районі кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Втілення 86: пептид відповідно до втілення 85, де пептид включає другий V L район, ідентичний першому VL району, та другий VH район, ідентичний першому VH району, де другий VL район і другий VH район кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Втілення 87: пептид, який включає VL район, що є функціональним варіантом VL району антитіла відповідно до втілення 4. Втілення 88: пептид відповідно до втілення 87, де VL район пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:12. Втілення 89: пептид, який включає VH район, що є функціональним варіантом VH району антитіла відповідно до втілення 4. Втілення 90: пептид відповідно до втілення 89, де VH район пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:17. Втілення 91: пептид, який включає, щонайменше, один з CDR, що є функціональним варіантом CDR антитіла відповідно до втілення 4. Втілення 92: пептид відповідно до втілення 91, де, щонайменше, один з CDR пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:18, SEQ ID NO:19, SEQ ID NO:20. Втілення 93: пептид відповідно до будь-якого з втілень від 87 до 92, де пептид має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонай 20 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 менше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% епітоп-зв'язуючих характеристик антитіла відповідно до втілення 4. Втілення 94: пептид відповідно до будь-якого з втілень від 87 до 92, де пептид має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% спорідненості, авідності або специфічності антитіла відповідно до втілення 4. Втілення 95: пептид відповідно до будь-якого з втілень від 68 до 94, де пептид специфічно зв'язує CD38 людини. Втілення 96: пептид відповідно до будь-якого з втілень від 68 до 95, де пептид конкурує з антитілом відповідно до втілення 4 за зв'язування CD38. Втілення 97: пептид відповідно до втілення 96, де конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу. Втілення 98: пептид відповідно до втілення 96, де конкуренцію визначають шляхом визначення перехресного блокування, як описано в прикладі 7 винаходу. Втілення 99: пептид відповідно до втілення 95, де пептид специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом відповідно до втілення 4. Втілення 100: пептид відповідно до будь-якого з втілень від 95 до 99, де пептид зв'язується з CD38 людини з більшою спорідненістю, ніж антитіло відповідно до втілення 4. Втілення 101: пептид відповідно до будь-якого з втілень від 95 до 99, де пептид має, в основному, такі ж характеристики специфічного зв'язування CD38, як антитіло відповідно до втілення 4. Втілення 102: пептид відповідно до будь-якого з втілень від 95 до 101, де пептид, що зв'язує CD38, в основному вільний від інших пептидів, що зв'язують CD38. Втілення 103: пептид, відповідно до будь-якого з втілень від 63 до 102, що зв'язується з CD38 людини (SEQ ID NO:31) і не зв'язується з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Втілення 104: пептид відповідно до втілення 103, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 50% ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 105: пептид відповідно до втілення 104, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 10% EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 106: пептид відповідно до втілення 105, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 5% EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 107: пептид відповідно до втілення 106, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 1% ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 108: пептид, що зв'язується з CD38 людини (SEQ ID NO:31) і не зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID N0:31). Втілення 109: пептид відповідно до втілення 108, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 50% величини EC 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 110: пептид відповідно до втілення 109, де EC50 Для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 10% величини ЕС 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 111: пептид відповідно до будь-якого з втілень від 103 до 107, що не зв'язується з мутантним CD38 людини, у якому залишок глутаміну в положенні 272 заміщений залишком аргініну (SEQ ID NO:33), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). 21 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Втілення 112: пептид відповідно до втілення 111, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 50% величини ЕС 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 113: пептид відповідно до втілення 112, де ЕС50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок серину в положенні 274 заміщений залишком фенілаланіну (SEQ ID NO:34), становить менше 10% величини ЕС 50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 114: пептид відповідно до будь-якого з втілень від 103 до 113, де згаданий пептид зв'язується з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), в такому ж ступені, як він зв'язується з CD38 людини (SEQ ID NO:31). Втілення 115: пептид відповідно до втілення 114, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 75% величини ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 116: пептид відповідно до втілення 115, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 85% величини ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 117: пептид відповідно до втілення 116, де EC 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 90% величини EC50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 118: пептид відповідно до втілення 117, де ЕС 50 для зв'язування пептиду з мутантним CD38 людини, у якому залишок треоніну в положенні 237 заміщений залишком аланіну (SEQ ID NO:32), становить більше 95% величини ЕС50 для зв'язування пептиду з CD38 людини (SEQ ID NO:31). Втілення 119: пептид, що конкурує з антитілом відповідно до втілення 6 за зв'язування CD38. Втілення 120: пептид відповідно до втілення 119, де конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу. Втілення 121: пептид відповідно до втілення 119, де конкуренцію визначають шляхом визначення перехресного блокування, як описано в прикладі 7 винаходу. Втілення 122: пептид, який специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом відповідно до втілення 6. Втілення 123: пептид, який має, в основному, такі ж характеристики специфічного зв'язування CD38, як антитіло відповідно до втілення 6. Втілення 124: пептид, який включає VL CDR1, що складається, в основному, з SEQ ID NO:23. Втілення 125: пептид, який включає VL CDR2, що складається, в основному, з SEQ ID NO:24. Втілення 126: пептид, який включає VL CDR3, що складається, в основному, з SEQ ID NO:25. Втілення 127: пептид відповідно до втілення 126, де пептид включає також VL CDR1, що складається, в основному, з SEQ ID NO:23. Втілення 128: пептид відповідно до втілення 126, де пептид включає також V L CDR2, що складається, в основному, з SEQ ID NO:24. Втілення 129: пептид відповідно до втілення 128, де пептид включає також V L CDR1, що складається, в основному, з SEQ ID NO:23. Втілення 130: пептид, який включає VH CDR1, що складається, в основному, з SEQ ID NO:28. Втілення 131: пептид, який включає VH CDR2, що складається, в основному, з SEQ ID NO:29. Втілення 132: пептид, який включає VH CDR3, що складається, в основному, з SEQ ID NO:30. Втілення 133: пептид відповідно до втілення 132, де пептид включає також V H CDR1, що складається, в основному, з SEQ ID NO:28. Втілення 134: пептид відповідно до втілення 132, де пептид включає також V H CDR2, що складається, в основному, з SEQ ID NO:29. Втілення 135: пептид відповідно до втілення 134, де пептид включає також V H CDR1, що складається, в основному, з SEQ ID NO:28. Втілення 136: пептид, який включає 22 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 (а) перший VL район, що включає три VL CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:23, SEQ ID NO:24 та SEQ ID NO:25, і (б) перший VH район, що включає три VH CDR, які незалежно один від одного складаються, в основному, з SEQ ID NO:28, SEQ ID NO:29 та SEQ ID NO:30. Втілення 137: пептид відповідно до втілення 136, де VL район та VH район обидва розташовані на одному ланцюзі пептиду. Втілення 138: пептид відповідно до втілення 137, де V L район та VH район розділені гнучким лінкером. Втілення 139: пептид відповідно до втілення 136, де VL район та VH район розташовані на різних ланцюгах пептиду. Втілення 140: пептид відповідно до втілення 139, де VL район та VH район розташовані на різних ланцюгах пептиду в скрученому білку імуноглобуліну. Втілення 141: пептид відповідно до втілень 136-140, де перший VL район і перший VH район орієнтовані таким чином, що три CDR в VL районі та три CDR в VH районі кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Втілення 142: пептид відповідно до втілення 141, де пептид включає другий V L район, ідентичний першому VL району, та другий VH район, ідентичний першому VH району, де другий VL район і другий VH район кооперативно зв'язані так, щоб вносити вклад у вибіркове та/або специфічне зв'язування антигенної детермінанти CD38 людини. Втілення 143: пептид, який включає VL район, що є функціональним варіантом VL району антитіла відповідно до втілення 6. Втілення 144: пептид відповідно до втілення 143, де VL район пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:22. Втілення 145: пептид, який включає VH район, що є функціональним варіантом VH району антитіла відповідно до втілення 6. Втілення 146: пептид відповідно до втілення 145, де VH район пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, принаймні, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:27. Втілення 147: пептид, який включає, щонайменше, один CDR, що є функціональним варіантом CDR антитіла відповідно до втілення 6. Втілення 148: пептид відповідно до втілення 147, де, щонайменше, один CDR пептиду складається, в основному, з послідовності, яка має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% ідентичності послідовності амінокислот послідовності згідно SEQ ID NO:23, SEQ ID NO:24, SEQ ID NO:25, SEQ ID O28, SEQ ID NO:29, SEQ ID NO:30. Втілення 149: пептид відповідно до будь-якого з втілень від 143 до 148, де пептид має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% епітоп-зв'язуючих характеристик антитіла відповідно до втілення 6. Втілення 150: пептид відповідно до будь-якого з втілень від 143 до 148, де пептид має, щонайменше, приблизно 50%, щонайменше, приблизно 60%, щонайменше, приблизно 70%, щонайменше, приблизно 75%, щонайменше, приблизно 80%, щонайменше, приблизно 85%, щонайменше, приблизно 90%, щонайменше, приблизно 95% спорідненості, авідності або специфічності антитіла відповідно до втілення 6. Втілення 151: пептид відповідно до будь-якого з втілень від 124 до 150, де пептид специфічно зв'язує CD38 людини. Втілення 152: пептид відповідно до будь-якого з втілень від 124 до 151, де пептид конкурує з антитілом відповідно до втілення 6 за зв'язування CD38. Втілення 153: пептид відповідно до втілення 152, де конкуренцію визначають за допомогою ELISA, як описано в прикладі 8 або 9 винаходу. Втілення 154: пептид відповідно до втілення 152, де конкуренцію визначають шляхом визначення перехресного блокування, як описано в прикладі 7 винаходу. 23 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 Втілення 155: пептид відповідно до втілення 151, де пептид специфічно зв'язується з епітопом CD38, причому епітоп також специфічно зв'язується антитілом відповідно до втілення 6. Втілення 156: пептид відповідно до будь-якого з втілень від 151 до 155, де пептид зв'язується з CD38 людини з більшою спорідненістю, ніж антитіло відповідно до втілення 6. Втілення 157: пептид відповідно до будь-якого з втілень від 151 до 155, де пептид має, в основному, такі ж характеристики специфічного зв'язування CD38, як антитіло відповідно до втілення 6. Втілення 158: пептид відповідно до будь-якого з втілень від 151 до 157, де пептид, що зв'язує CD38, в основному вільний від інших пептидів, що зв'язують CD38. Втілення 159: пептид відповідно до будь-якого з втілень від 1 до 158, де пептид не є агоністом CD38. Втілення 160: пептид відповідно до будь-якого з втілень від 1 до 159, де пептид не індукує значної проліферації мононуклеарних клітин периферичної крові. Втілення 161: пептид відповідно до будь-якого з втілень від 1 до 160, де пептид не індукує вивільнення значних рівнів IL-6 моноцитами людини або мононуклеарними клітинами периферичної крові. Втілення 162: пептид відповідно до будь-якого з втілень від 1 до 161, де пептид не індукує вивільнення детектованих рівнів IFN- Т-клітинами людини або мононуклеарними клітинами периферичної крові. Втілення 163: пептид відповідно до будь-якого з втілень від 7 до 162, де пептид є антитілом. Втілення 164: антитіло відповідно до будь-якого з втілень від 1 до 6 або 163, де антитіло є антитілом людини. Втілення 165: антитіло відповідно до будь-якого з втілень від 1 до 6 або 163, де антитіло є гуманізованим антитілом. Втілення 166: антитіло відповідно до будь-якого з втілень від 1 до 6 або 163, де антитіло є хімерним антитілом. Втілення 167: антитіло відповідно до будь-якого з втілень від 1 до 6 або 163-166, де антитіло є моноклональним антитілом. Втілення 168: антитіло відповідно до будь-якого з втілень від 1 до 6 або 163-167, яке характеризується тим, що воно є lgG1, lgG2, lgG3, lgG4, IgD, IgA, IgE або IgM антитілом. Втілення 169: антитіло відповідно до втілення 168, що характеризується тим, що воно є lgG1 антитілом. Втілення 170: антитіло відповідно до втілення 169, що характеризується тим, що воно є lgG1, антитілом. Втілення 171: антитіло відповідно до втілення 168, що характеризується тим, що воно є IgM антитілом. Втілення 172: антитіло відповідно до втілення 171, що характеризується тим, що воно є ІдМ, антитілом. Втілення 173: пептид відповідно до будь-якого з втілень від 2 до 172, де пептид глікозильований в еукаріотичній клітині. Втілення 174: антитіло відповідно до будь-якого з втілень від 1 до 6 або від 163 до 173, що є фрагментом антитіла або одиночним ланцюгом антитіла. Втілення 175: пептид або антитіло відповідно до будь-якого з втілень від 1 до 174, які далі включають лінкер хелатор для приєднання радіоізотопу. Втілення 176: пептид відповідно до будь-якого з втілень від 1 до 175, що находиться, в основному, в ізольованому виді. Втілення 177: ізольована нуклеїнова кислота, що кодує пептид відповідно до будь-якого з втілень від 1 до 175. Втілення 178: експресуючий вектор, який включає послідовність нуклеїнової кислоти, що кодує пептид відповідно до будь-якого з втілень від 1 до 175. Втілення 179: експресуючий вектор, який включає VL нуклеотидну послідовність згідно SEQ ID NO:1, VH нуклеотидну послідовність згідно SEQ ID NO:6 або VL нуклеотидну послідовність згідно SEQ ID NO:1 та VH нуклеотидну послідовність згідно SEQ ID NO:6. Втілення 180: експресуючий вектор, який включає VL нуклеотидну послідовність згідно SEQ ID NO:11, VH нуклеотидну послідовність згідно SEQ ID NO:16 або VL нуклеотидну послідовність згідно SEQ ID NO:11 та VH нуклеотидну послідовність згідно SEQ ID NO:16. Втілення 181: експресуючий вектор відповідно до втілення 179 або 180, який далі включає нуклеотидну послідовність, що кодує константний район легкого ланцюга, важкого ланцюга або обох легкого та важкого ланцюгів антитіла людини. 24 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 Втілення 182: експресуючий вектор відповідно до втілення 181, де нуклеотидна послідовність, що кодує константний район легкого ланцюга, важкого ланцюга або обох легкого та важкого ланцюга антитіла людини, кодує lgG1 антитіло. Втілення 183: гібридома, яка продукує моноклональне анти-СD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, що включають нуклеотидні послідовності у варіабельному районі легкого ланцюга згідно SEQ ID NO:1 або консервативні модифікації цих послідовностей, і нуклеотидні послідовності у варіабельному районі важкого ланцюга згідно SEQ ID NO:6 або консервативні модифікації цих послідовностей. Втілення 184: гібридома, відповідно до втілення 183, де нуклеїнові кислоти легкого ланцюга людини включають нуклеотидну послідовність згідно SEQ ID NO:1 і нуклеїнові кислоти важкого ланцюга людини включають нуклеотидну послідовність згідно SEQ ID NO:6. Втілення 185: гібридома, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга згідно SEQ ID NO:2 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга згідно SEQ ID NO:7 або консервативні модифікації цієї послідовності. Втілення 186: гібридома, відповідно до втілення 185, де варіабельний район легкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:2 і варіабельний район важкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:7. Втілення 187: трансфектома, яка продукує моноклональне анти-СD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини SEQ ID NO:1 або консервативними модифікаціями цих послідовностей, і нуклеїновими кислотами важкого ланцюга згідно SEQ ID NO:6 або консервативними модифікаціями цих послідовностей. Втілення 188: трансфектома відповідно до втілення 187, де моноклональне анти-СD38 антитіло людини кодується нуклеїновою кислотою варіабельного району легкого ланцюга людини згідно SEQ ID NO:1 і нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:6. Втілення 189: трансфектома, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга згідно SEQ ID NO:2 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга згідно SEQ ID NO:7 або консервативні модифікації цієї послідовності. Втілення 190: трансфектома відповідно до втілення 189, де легкий ланцюг людини включає варіабельну амінокислотну послідовність легкого ланцюга згідно SEQ ID NO:2, і важкий ланцюг людини включає варіабельну амінокислотну послідовність важкого ланцюга згідно SEQ ID NO:7. Втілення 191: гібридома, яка продукує моноклональне анти-СD38 антитіло людини, кодоване нуклеїновими кислотами легкого ланцюга людини та важкого ланцюга людини, які включають нуклеотидні послідовності у варіабельному районі легкого ланцюга згідно SEQ ID NO:11 або консервативні модифікації цих послідовностей, і нуклеотидні послідовності у варіабельному районі важкого ланцюга згідно SEQ ID NO:16 або консервативні модифікації цих послідовностей. Втілення 192: гібридома відповідно до втілення 191, де нуклеїнові кислоти легкого ланцюга людини включають нуклеотидну послідовність згідно SEQ ID NO:11, нуклеїнові кислоти важкого ланцюга людини включають нуклеотидну послідовність згідно SEQ ID NO:16. Втілення 193: гібридома, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони важкого ланцюга людини та легкого ланцюга людини, які включають варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:12 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга згідно SEQ ID NO:17 або консервативні модифікації цієї послідовності. Втілення 194: гібридома відповідно до втілення 193, де варіабельний район легкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:12, і варіабельний район важкого ланцюга людини включає амінокислотну послідовність згідно SEQ ID NO:17. Втілення 195: трансфектома, яка продукує моноклональне анти-СD38 антитіло людини, кодоване нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:11 або консервативними модифікаціями цих послідовностей, і нуклеотидними послідовностями важкого ланцюга людини згідно SEQ ID NO:16 або консервативними модифікаціями цих послідовностей. Втілення 196: трансфектома відповідно до втілення 195, де моноклональне анти-СD38 антитіло людини кодується нуклеїновими кислотами варіабельного району легкого ланцюга людини згідно SEQ ID NO:11 і нуклеїновими кислотами важкого ланцюга людини згідно SEQ ID NO:16. Втілення 197: трансфектома, яка продукує моноклональне анти-СD38 антитіло людини, що включає варіабельні райони легкого ланцюга людини та важкого ланцюга людини, які включа 25 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 ють варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:12 або консервативні модифікації цієї послідовності, та варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:17 або консервативні модифікації цієї послідовності. Втілення 198: трансфектома відповідно до втілення 197, де легкий ланцюг людини включає варіабельну амінокислотну послідовність легкого ланцюга людини згідно SEQ ID NO:12, і важкий ланцюг людини включає варіабельну амінокислотну послідовність важкого ланцюга людини згідно SEQ ID NO:17. Втілення 199: еукаріотична або прокаріотична клітина хазяїна, що продукує пептид відповідно до будь-якого з втілень від 1 до 175. Втілення 200: еукаріотична або прокаріотична клітина хазяїна, що містить експресуючий вектор відповідно до втілення 178. Втілення 201: трансгенна тварина, відмінна від людини, або рослина, які включають нуклеїнові кислоти, що кодують важкий ланцюг людини та легкий ланцюг людини, де тварина або рослина продукує детектовану кількість пептиду відповідно до будь-якого з втілень від 1 до 175. Втілення 202: імунокон'югат, який включає пептид відповідно до будь-якого з втілень від 1 до 174, з'єднаний із цитотоксичним агентом, радіоізотопом або ліками. Втілення 203: імунокон'югат, який включає пептид відповідно до будь-якого з втілень від 1 до 168 або від 171 до 174, де пептид є мономерним ІgМ антитілом, з'єднаним із цитотоксичним агентом, радіоізотопом або ліками. Втілення 204: біспецифічна або мультиспецифічна молекула, яка включає пептид відповідно до будь-якого з втілень від 1 до 175, і специфічність зв'язування ефекторної клітини людини. Втілення 205: біспецифічна або мультиспецифічна молекула, яка включає пептид відповідно до будь-якого з втілень від 1 до 175, і специфічність зв'язування CD3, CD4, IL-15R, мембраннозв'язаного або зв'язаного з рецептором TFN-, Fc рецептором людини або мембраннозв'язаного чи зв'язаного з рецептором IL-15. Втілення 206: фармацевтична композиція, яка включає пептид відповідно до будь-якого з втілень від 1 до 176, або імунокон'югат відповідно до будь-якого з втілень від 202 до 205 і фармацевтично прийнятний носій. Втілення 207: фармацевтична композиція, відповідно до втілення 206, яка включає один чи більше додатковий терапевтичний агент. Втілення 208: спосіб інгібування росту та/або проліферації клітин, експресуючих CD38, який включає застосування пептиду відповідно до будь-якого з втілень від 1 до 176, імунокон'югата відповідно до будь-якого з втілень від 202 до 205, фармацевтичної композиції відповідно до втілення 206 або 207, або експресуючого вектора відповідно до будь-якого з втілень від 178 до 182, так що ріст та/або проліферація клітин інгібуються. Втілення 209: спосіб лікування захворювання або порушення, що утягує клітини, які експресують CD38, де цей спосіб включає застосування/введення пептиду відповідно до будь-якого з втілень від 1 до 176, імунокон'югата відповідно до будь-якого з втілень 202 до 205, фармацевтичної композиції відповідно до втілення 206 або 207, або експресуючого вектора відповідно до будь-якого з втілень від 178 до 182 суб'єкту, що потребує цього. Втілення 210: спосіб запобігання захворювання або порушення, що утягує клітини, які експресують CD38 у суб'єкта, де спосіб включає введення терапевтично ефективної кількості пептиду відповідно до будь-якого з втілень від 1 до 176, імунокон'югата відповідно до будь-якого з втілень від 202 до 205, фармацевтичної композиції відповідно до втілення 206 або 207, або експресуючого вектора відповідно до будь-якого з втілень від 178 до 182 суб'єкту, що потребує цього. Втілення 211: спосіб відповідно до втілення 209 або 210, де захворювання або порушення є ревматоїдним артритом. Втілення 212: спосіб відповідно до втілення 209 або 210, де захворювання або порушення є множинною мієломою. Втілення 213: спосіб відповідно до будь-якого з втілень від 209 до 212, де спосіб включає введення одного чи більше додаткового терапевтичного агента суб'єкту. Втілення 214: спосіб відповідно до втілення 213, де додаткові один чи більше терапевтичний агент вибирають із хіміотерапевтичного агента, протизапального агента, імуносупресивного та/або імуномодуляторного агента. Втілення 215: спосіб відповідно до втілення 213, де додаткові один чи більше терапевтичний агент вибирають із групи, що складається із цисплатину, гефітинібу, цетуксимабу, ритуксимабу, бевацизумабу, ерлотинібу, бортезомібу, талідоміду, памідронату, золедронової кислоти, клодронату, ризендронату, ібандронату, етидронату, алендронату, тилудронату, тріокисиду миш'яку, 26 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 60 леналідоміду, філграстиму, пегфілграстиму, зарграмостиму, субероїланіліду гідроксамової кислоти та SCIO-469. Втілення 216: in vitro спосіб детектування наявності CD38 антигену або клітин, експресуючих CD38, у зразку, який включає: А) контактування зразка з пептидом відповідно до будь-якого з втілень від 1 до 176, в умовах, що дозволяють утворення комплексу між пептидом та CD38, і Б) детектування утворення цього комплексу. Втілення 217: in vitro спосіб відповідно до втілення 216, де згаданий пептид є антитілом. Втілення 218: набір для детектування наявності CD38 антигену або клітин, експресуючих CD38, у зразку, який включає пептид відповідно до будь-якого з втілень від 1 до 176. Втілення 219: in vivo спосіб детектування CD38 антигену або клітин, експресуючих CD38 у суб'єкта, який включає: а) введення пептиду відповідно до будь-якого з втілень від 1 до 176, в умовах, що дозволяють утворення комплексу між пептидом та CD38, і б) детектування утвореного комплексу. Втілення 220: in vitro спосіб відповідно до втілення 219, де згаданий пептид є антитілом. Втілення 221: антиідіотипове антитіло, що зв'язується з пептидом відповідно до будь-якого з втілень 2, 4 або від 163 до 174. Втілення 222: застосування антиідіотипового антитіла відповідно до втілення 221 для детектування рівня пептиду відповідно до будь-якого з втілень 2, 4 або від 163 до 174, у зразку. Втілення 223: застосування антиідіотипового антитіла відповідно до втілення 221 для детектування рівня моноклонального антитіла людини проти CD38 у зразку. Терміни «CD38» та «антиген CD38» застосовуються тут взаємозамінно та включають будьякі варіанти, ізоформи та види гомологів CD38 людини, які природно експресуються клітинами, трансфекованими геном CD38. Синоніми CD38, як прийнято в даній області техніки, включають АДФ-рибозил-циклазу 1, цАДФР-гідролазу 1, CD38-rs1, гідролазу 1 циклічної АДФ-рибози, I-19, NIM-R5 антиген. Термін «пептид» по відношенню як до СD38-зв'язуючих пептидів, так і до не-CD38 пептидів, описаних тут, включає будь-який придатний пептид і може застосовуватися як синонім термінам «поліпептид» та «білок», якщо не зазначено інше або це не суперечить контексту; за умови, що читач розуміє, що кожен тип відповідної молекули, яка містить амінокислотний полімер, може бути зв'язаний з істотними розбіжностями і таким чином утворює окреме втілення даного винаходу (наприклад, такий пептид, як антитіло, що складається з декількох поліпептидних ланцюгів, значно відрізняється, наприклад, від одноланцюгового антитіла, пептидного імуноадгезину або одноланцюгового імуногенного пептиду). Тому термін «пептид» тут слід в основному розуміти як застосовний до будь-якого придатного пептиду будь-якого придатного розміру або складу (з погляду кількості амінокислот і числа об'єднаних ланцюгів у молекулі білка). Далі, пептиди в контексті способів і композицій винаходу, описаних тут, можуть включати залишки, що не зустрічаються в природі, та/або не-L-амінокислотні залишки, якщо не зазначено інше або це не суперечить контексту. Як буде обговорюватися далі, якщо не зазначено інше або це не суперечить контексту, термін пептид (і якщо обговорювати окремі втілення терміна, поліпептид та/або білок) також охоплює дериватизовані молекули пептиду. Стисло, у контексті даного винаходу, похідне (дериват) є пептидом, у якого один чи більше амінокислотний залишок хімічно модифікований (наприклад, за допомогою алкілування, ацилювання, утворення складного ефіру, утворення аміду) або зв'язаний з одним чи більше неамінокислотним органічним та/або неорганічним атомним або молекулярним замісником (наприклад, групою поліетиленгліколю (ПЕГ), ліпофільним замісником (який при необхідності може бути зв'язаний з амінокислотною послідовністю пептиду через роздільний залишок або групу, таку як β-аланін, -амінобутирову кислоту (ГАБК), L/D-глутамінову кислоту, бурштинову кислоту і т.п.) флуорофором, біотином, радіоізотопом і т.д., і може також або альтернативно включати неосновні, неприродного походження та/або не-L амінокислотні залишки, якщо не зазначено інше або це не суперечить контексту (однак, знову слід розуміти, що такі похідні можуть розглядатися як незалежні властивості даного винаходу і включення таких молекул в поняття пептиду зроблене скоріше заради зручності опису даного винаходу, ніж для введення якої би то не було рівності між голими пептидами та такими похідними). Необмежуючі приклади таких амінокислотних залишків включають, наприклад, 2-аміноадипінову кислоту, 3-аміноадипінову кислоту, β-аланін, β-амінопропіонову кислоту, 2-аміномасляну кислоту, 4аміномасляну кислоту, 6-амінокапронову кислоту, 2-аміногептанову кислоту, 2-аміноізомасляну кислоту, 3-аміноізомасляну кислоту, 2-амінопімелінову кислоту, 2,4-діаміномасляну кислоту, десмозин, 2,2'-діамінопімелінову кислоту, 2,3-діамінопропіонову кислоту, N-етилгліцин, N 27 UA 98756 C2 5 10 15 20 25 30 35 40 45 50 55 етиласпарагін, гідроксилізин, ало-гідроксилізин, 3-гідроксипролін, 4-гідрокпролін, ізодесмозин, алоізолейцин, N-метилгліцин, N-метилізолейцин, 6-N-метиллізин, N-метилвалін, норвалін, норлейцин, орнітин і статин, галогеновані амінокислоти. «Антиген-зв’язуючий пептид» стосується будь-якого пептиду, що специфічно зв'язується із частиною даного антигену в клітинних та/або фізіологічних умовах протягом часу, достатнього, щоб індукувати, прискорити, підсилити та/або іншим чином модулювати фізіологічну дію, зв'язану з антигеном; щоб дозволити детекцію за допомогою ELISA, блотингу (Western blot) або інших подібних застосовних технік дослідження зв'язування білків, описаних тут та/або відомих в даній області техніки, та/або бути зв'язаним з ним іншим детектованим способом протягом відповідного часу (наприклад, щонайменше, приблизно 15 хв., щонайменше, приблизно 30 хв., щонайменше, приблизно 45 хв., щонайменше приблизно 1 година, щонайменше, приблизно 2 години, щонайменше, приблизно 4 години, щонайменше, приблизно 6 годин, щонайменше, приблизно 12 годин, приблизно 1-12 годин, приблизно 1-36 годин, приблизно 1-48 годин, приблизно 1-72 годин, приблизно один тиждень або довше). СD38-зв'язуючий пептид, або CD38BP, є пептидом, що зв'язує антиген, який специфічно зв'язується з антигеном CD38. В одному втіленні, зв'язування CD38BP із CD38 вимірюють за допомогою способу, описаного в прикладі 4. Термін «імуноглобулін» стосується класу структурно споріднених глікопротеїдів, що складаються із двох пар поліпептидних ланцюгів, однієї пари легких (L) ланцюгів з низькою молекулярною вагою та однієї пари важких (Н) ланцюгів, де всі чотири зв'язані між собою дисульфідними зв'язками. Структура імуноглобулінів добре охарактеризована. Див., наприклад, Fundamental nd Immunology ch. 7 (Paul W. Ed. 2 ed., Raven Press, NY (1989)). Стисло, кожен важкий ланцюг звичайно складається з варіабельного району важкого ланцюга (скорочено позначеного тут як VH) і константного району важкого ланцюга. Константний район важкого ланцюга звичайно складається із трьох доменів, СH1, СH2 і СH3. Кожен легкий ланцюг звичайно складається з варіабельного району легкого ланцюга (скорочено позначеного тут як VL) і константного району легкого ланцюга. Константний район легкого ланцюга звичайно складається з одного домену CL. Райони VH та VL можна далі підрозділити на райони гіперваріабельності (або гіперваріабельні райони, які можуть бути гіперваріабельними по послідовності та/або формі петель, що задаються структурою), називані також районами, що визначають комплементарність (CDR), які перемежовуються більш консервативними районами, називаними каркасними районами (FR). Кожен VH та VL звичайно складається із трьох CDR і чотирьох FR, організованих від амінокінця до карбокси-кінця в такому порядку: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4 (див. також Chothia and Lesk, L Моl. ВіоІ. 196, 901-917 (1987)). Звичайно, нумерацію амінокислотних залишків у цьому районі проводять у спосіб, описаний в Kabat et al., Sequences of Proteins of th Immunological Interest, 5 ed., Public Health Service, National Institute of Health, Bethesda, MD (1991) (такі фрази, як нумерація залишків варіабельного району, як у Кабата або за Кабатом, стосуються тут такої системи нумерації варіабельних доменів важкого ланцюга або варіабельних доменів легкого ланцюга). При застосуванні цієї системи нумерації дійсна лінійна амінокислотна послідовність пептиду може містити менше амінокислот або додаткові амінокислоти відповідно до укорочення або вставок в FR або CDR варіабельного домену. Наприклад, варіабельний домен важкого ланцюга може включати вставку з одиничної амінокислоти (залишок 52а за Кабатом) після залишку 52 в VH CDR2 і вставлені залишки (наприклад, 82а, 82б та 82в і т.д., за Кабатом) після залишку 82 в FR важкого ланцюга. Нумерацію залишків за Кабатом можна визначити для даного антитіла за допомогою зіставлення (вирівнювання) районів гомології послідовності зі «стандартною» пронумерованою послідовністю Кабата. Термін антитіло (Аb) у контексті даного винаходу стосується молекули імуноглобуліну, фрагменту молекули імуноглобуліну або похідного будь-якого з них, що має здатність специфічно зв'язуватися з антигеном у типових фізіологічних умовах протягом значних періодів часу, таких як, щонайменше, приблизно 30 хв., щонайменше, приблизно 45 хв., щонайменше, приблизно 1 година, щонайменше, приблизно 2 години, щонайменше, приблизно 4 години, щонайменше, приблизно 8 годин, щонайменше, приблизно 12 годин, приблизно 24 годин чи більше, приблизно 48 годин чи більше, приблизно 3, 4, 5, 6, 7 або більше днів і т.д., або будь-якого іншого відповідного визначеного функціонально періоду (такого, як час, достатній для того, щоб індукувати, прискорити, підсилити та/або модулювати фізіологічну відповідь, викликану зв'язуванням антитіла з антигеном). Варіабельні райони важкого та легкого ланцюгів молекули імуноглобуліну містять зв'язуючі домени, які взаємодіють із антигеном. Константні райони антитіл (Abs) можуть опосередковувати зв'язування імуноглобуліну із тканинами хазяїна або факторами, що включають різні клітини 28
ДивитисяДодаткова інформація
Назва патенту англійськоюAntibody which binds to human cd38 for the treatment of cd38 mediated disease
Автори англійськоюWeers, Michel de, Graus, Yvo, Oprins, Judith, Parren, Paul, Parren, Winkel, Jan van de, Vugt, Martine van
Назва патенту російськоюАнтитело, которое связывается с cd38, для лечения заболевания, опосредованного cd38
Автори російськоюВерс Мишель де, Граус Иво, Опринс Юдит, Паррен Пауль Паррен, Винкел Ян ван де, Вюгт Мартин ван
МПК / Мітки
МПК: A61P 35/00, C12N 5/10, C07K 16/28, C12N 15/13, A61K 39/395
Мітки: опосередкованого, cd38, захворювання, антитіло, зв'язується, лікування, яке
Код посилання
<a href="https://ua.patents.su/161-98756-antitilo-yake-zvyazuehtsya-z-cd38-dlya-likuvannya-zakhvoryuvannya-oposeredkovanogo-cd38.html" target="_blank" rel="follow" title="База патентів України">Антитіло, яке зв’язується з cd38, для лікування захворювання, опосередкованого cd38</a>
Попередній патент: Пляшка скляна і спосіб використання цієї скляної пляшки після її опорожнення
Наступний патент: Бензамідні сполуки, корисні як інгібітори деацетилази гістонів
Випадковий патент: Спосіб захисту від землетрусів шляхом розв'язаного від коливань встановлення будівель і об'єктів на опори через віртуальні маятники з великим періодом коливання