Спосіб одержання органілтрифторосульфуранів
Номер патенту: 71020
Опубліковано: 15.11.2004
Автори: Мартинюк Євген Григорович, Ягупольський Лев Мусійович, Шермолович Юрій Григорович, Пашинник Валерій Юхимович, Табачук Максим Ростиславович
Формула / Реферат
Спосіб одержання органілтрифторосульфуранів загальної формули І
RSF3 , (I)
де
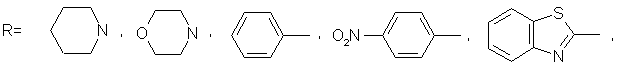
який включає взаємодію сполук формули R-S-S-R, де R має наведені вище значення, з хлором в присутності надлишку дрібнодисперсного фториду калію при температурі 10-20°С та молярному співвідношенні R-S-S-R: хлор: фторид калію, що складає 1,0 : 5,0 : 20,0.
Текст
Спосіб одержання органілтрифторосульфуранів загальної формули І RSF3 , (I) де Винахід відноситься до органічної хімії, зокрема органілтрифторосульфуранам, до нового, універсального способу одержання діалкіламінотрифторосульфуранів, арилтрифторосульфуранів і гетерилтрифторосульфуранів які широко використовуються в синтетичній органічній та біоорганічній хімії. Діалкіламінотрифторосульфурани знайшли широке використання в органічному синтезі для заміни різноманітних функціональних груп в молекулах на атоми фтору, а також як вихідні сполуки в синтезі різних типів сіркоорганічних сполук [1-3]. Відомо також використання арилтрифторосуль фуранів як фторуючи х реагентів [1]. Для синтезу діалкіламінотрифторосульфуранів широко використовується метод, який базується на взаємодії діалкіламінотриметилсиланів із чотири-фтористою сіркою в автоклаві [4-6] або в розчині діетилового ефіру при низькій температурі [7,8], а арилтрифторосульфурани можуть бути одержані реакцією елементного фтору або дифториду срібла з діарилдисульфідами [9-11]. Гетерилтрифторосульфурани, які містять трифторосульфуранову груп у біля вуглецевого атому гетероциклу, до теперішнього часу одержані не були. Наведені в хімічних та патентних виданнях методи одержання органілтрифторосульфуранів не є універсальними і можуть бути використані лише для синтезу окремих типів трифторосульфуранів, базуються на використанні високореакційноздатних, токсичних та тр уднодоступних реагентів (чотири-фториста сірка, фтор, дифторид срібла), що в значній мірі обмежує можливості застосування цих методів. Найбільш близьким по суті та одержаним результатам є спосіб синтезу арилтрифторосульфуранів, який вибрано нами за прототип, що базується на взаємодії елементного фтору з 2,4динітрофенілдисульфідом [9]. За цим методом цільовий продукт - 2,4-динітрофенілтрифторосульфуран, одержано з виходом, який не перевищує 51%. R= N , O N , , ON 2 S , , N (13) 71020 (11) UA (19) Недоліком цього методу є те, що він не може бути застосований для одержання діалкіламінотрифторосульфуранів, арилтрифторосульфуранів, які містять в ароматичному кільці замісники, до складу яких входить гетероатом (виняток нітрогрупа), а також гетерилтрифторосульфурани. Задача винаходу є розробка простого, універсального методу одержаним різних типів органілтрифторосульфуранів. Поставлена задача досягається реакцією ор C2 який включає взаємодію сполук формули R-S-S-R, де R має наведені вище значення, з хлором в присутності надлишку дрібнодисперсного фториду калію при температурі 10-20°С та молярному співвідношенні R-S-S-R: хлор: фторид калію, що складає 1,0 : 5,0 : 20,0. 3 71020 4 ганічних сполук, які містять зв'язок -S-S- (діаміди ЯМР19F (ефір): δ=56,74 (д, JFa-Fе=55Гц, 2Fa), 18,08 тіосульфінової кислоти, діарилдисульфіди, диге(т, JF е-Fа=55Гц, 1Fе). терил-дисульфіди) із хлором в присутності надлиПриклад 3. шку дрібнодисперсного фториду калію (spray Одержання фенілтрифторосульфурану (1в). dried). а) До суспензії 2,2г (0,01 моля) дифенілдисульфіду, 10,4г (0,18 моля) фториду калію (spray dried) в 30мл ацетонітрилу додають при інтенсивному перемішуванні і температурі реакційної суміші 20°С по краплям протягом 3,5год розчин 3,55г (0,05 моля) хлору в 40мл ацетонітрилу. Після припинення додавання хлору, перемішують при 20°С 1год. Осад відфільтровують, фільтрат випаровуРеакція проходить в ацетонітрилі при темпеють у вакуумі 10-20мм рт.ст., залишок фракціонуратурі 10-20°С при мольному співвідношенні реають. Вихід 2,71г (87,5%), т. кип. 70-71°С (12мм гентів R-S-S-R : хлор: фторид калію як 1,0:5,0:20,0. рт.ст.). Виходи діалкіламінотрифтросульфуранів в цій б) В суспензію 24г (0,11 моля) дифенілдисуреакції становлять 60-67%, арилтрифльфіду, 65г (1,12 моля) фториду калію (spray dried) торосульфуранів та гетерилтрифторосульфуранів в 150мл ацетонітрилу при 10°С пропускають при досягають 98% в розрахунку на взятий дисульфід. перемішуванні протягом 4год хлор (до знебарвЗагальна методика одержання органілтрифторолення червоного кольору). Осад відфільтровують, сульфуранів. фільтрат випаровують у вакуумі 10-20мм рт.ст., В реактор ємкістю 500мл, обладнаний магнітзалишок фракціонують. Вихід 33,2г (98%), т. кип. ною мішалкою, термометром, краплинною лійкою 70-71°С (12 мм рт.ст.). Знайдено %: С 44,10; Η (або трубкою для пропускання хлору) вміщують 3,12; S 19,60. C6H5F3S. Вирахувано %: С 43,37; Η 0,05моля тетраалкілдіаміду тіосульфінової кисло3,03; S 19,29. Спектр ЯМР19F (ефір): 19 F ЯМР ти, діарилдисульфіду або дигетерилдисульфіду (ефір): δ=57,24 (д, JFа-Fе=65Гц, 2Fа), -42,58 (τ, JF е0,5-1 моль фториду калію (spray dried) і 100мл суа е F =65Гц, 1F ). хого ацетонітрилу. При інтенсивному перемішуПриклад 4. ванні і температурі реакційної суміші 10-20°С доОдержання n-нітрофенілтрифторосульфурану дають по краплях протягом 2год. розчин 0,25 моля (1г). хлору в 170мл ацетонітрилу (або пропускають в До суспензії 11,0г (0,035 моля) ди(п-нітрофереакційну масу протягом ~ 4год розраховану кільніл)дисульфіду, 34,8г (0,6 моля) фториду калію кість хлору). Після закінчення додавання хлору, (spray dried) в 100мл ацетонітрилу додають при перемішують при температурі 20°С 1год. Осад інтенсивному перемішуванні і температурі реаквідфільтровують, фільтрат випаровують в вакуумі ційної суміші 20°С по краплям протягом 3,5год 10-20 мм рт.ст., залишок фракціонують або крисрозчин 12,0г (0,17 моля) хлору в 100мл ацетонітталізують. рилу. Після припинення додавання хлору, переміВинахід ілюструється наступними прикладами. шують при 20°С 1год. Осад відфільтровують, фіПриклад 1. льтрат випаровують у вакуумі 10-20мм рт.ст. В Одержання піперидинотрифторосульфурану залишку кристалічна речовина, вихід 12,7г (98%). (1а). До суспензії 18,6г (0,08 моля) піперидиду тіоПісля перекристалізації із чотирихлористого вугсульфінової кислоти, 58г (1,0 моль) фториду калію лецю, т. пл 57-58°С. Спектр ЯМР19F(CD3CN): (spray dried) в 100мл ацетонітрилу додають при δ=60,34 (д, JFа-Fе=70Гц, 2Fa), -45,60 (τ, JFе-Fа=70Гц, інтенсивному перемішуванні і температурі реак1Fе). ційної суміші 15°С по краплям протягом 3,5год. Приклад 5. розчин 28,4г (0.4 моля) хлору в 270мл ацетонітриОдержання бензтіазоліл-2-трифторосульфулу. Після припинення додавання хлору темперарану (Ід). туру реакційної суміші доводять до 20°С і переміДо суспензії 11,0г (0,033 моля) ди(2-бензтіазошують при цій температурі 2год. Осад відліл)дисульфіду, 34,8г (0,6 моля) фториду калію фільтровують, фільтрат випаровують в вакуумі 10(spray dried) в 100мл ацетонітрилу додають при 20 мм рт.ст., залишок фракціонують. Вихід 18,6г інтенсивному перемішуванні і температурі реак(67%), т. кип. 75-76°С (12 мм рт.ст.), n D20 1,4515 [7]. ційної суміші 20°С по краплям протягом 3,5год Спектр ЯМР 19F (е фір): δ = 57,97 (2Fa), 2077 (Fe). розчин 10,7г (0,15 моля) хлору в 100мл ацетонітПриклад 2. рилу. Після припинення додавання хлору, переміОдержання морфолінотрифторосульфурану шують при 20°С 1год. Осад відфільтровують, фі(16). До суспензії 11.8г (0.05 моля) морфоліду тіольтрат випаровують у вакуумі 10-20мм рт.ст. В сульфінової кислоти, 93г (1.6 моля) фториду калію залишку кристалічна речовина, вихід 14,1г (spray dried) в 100мл ацетонітрилу додають при (95,5%). Після перекристалізації із гексану, т. пл. інтенсивному перемішуванні і температурі реак76-77°С. Спектр ЯМР19F (CD3CN): δ=60,03 (д, JFаційної суміші 15°С по краплям протягом 2год розе a е а e F =50Гц, 2F ), -29.00 (τ, JF -F =50Гц, 1F ). Спектр чин 17,8г (0,25 моля) хлору в 170мл ацетонітрилу. ЯМР1H(CD3CN): δ=7,64-7,70 (м, 2Н); 8,04-8,07 (м, Після припинення додавання хлору, температуру 1H); 8,32-8,35 (м, 1Н). Знайдено, %: С 37,70; Η реакційної суміші доводять до 20°С і перемішують 1,82; S 28,55. C7H4F3NS 2. Вирахувано, %: С 37,66; при цій температурі 1год. Осад відфільтровують, Η 1,80; S 28,72. фільтрат випаровують в вакуумі 10-20мм рт.ст., Література залишок фракціонують. Вихід 10,5г (60%), т. кип. 1. Marko vsky L.; Pashinnik V. Fluorosulfuranes // 41-42°С (0,5мм рт.ст.), nD201.4540 [7]. Спектр 5 71020 6 Reviews on Heteroatom Chemistry. - 1989. - Vol.2. Aminoschwefel (IV) -monofluoridimiden // Chem. Ber. P.112-151. - 1971. - Vol.104. - P.1247-1255. 2. Hudlizky M. Fluorination with Diethylaminosul7. Markovskij L.N., Pashinnik V.E., Kirsanov A.V. fur Trifluoride and Related Aminofluoro-sulfuranes // Application of Dialkyl-aminosulfur Trifluorides in the Org. React. - 1988. - Vol.35. - P.513-637. Synthesis of Fluoroorganic Compounds // Synthesis. 3. Marko vsky L.N., Pashinnik V.E. Fluorination of 1973. - P.787-789. Organic Compounds with Fluorosulfuranes in Book: 8. A.c. 433136 СССР, МКИ С07С149/14. СпоNew Fluorination Agents in Organic Synthesis / Gerсоб получения диалкил(алкилman L.S.; Semskov S.V., Eds.; Springer Verlag: Berарил)аминотрифторидов серы / Л.Н. Марковский, lin:, 1989. - P.254-271. В.Е. Пашинник, А.В. Кирсанов (СССР). 4. Demitras G.C., Kent R.A., MacDiarmid A.G. Опубл.25.06.74,бюл. №23. Preparation of Ammo-Derivatives of Sulfur Tetra9. Chamberlain D.L., Kharash N. Synthesis of fluoride and Phosphorus Pentafluoride // Chem. and 2,4-Dinitrophenyl Sulfur Trifluo-.rid and Antimony (III) Ing. - 1964. - P. 1712. Halide // J. Am. Chem. Soc. - 1955. - Vol.77. 5. Halasz S.P., Glemser O. Darstellung neuer P.1041-1043. Aminoschwefelmonofluoridimide imd -oxid10. Sheppard W.A. Arylsulfur trifluorides and penmonofluoridimide sowie über die Structur der tafluorides // J. Am. Chem. Soc. - 1960. - Vol.82. Aminoschwefeloxid-trifluoride // Chem. Ber. - 1970. P.4751-4752. Vol.103. - P.594-602. 11. Sheppard W.A. Alkyl- and arylsulfur 6. Halasz S.P., Glemser O. Darstellung von trifluorides // J. Am. Chem. Soc. -1962.-Vol.84.Piperidinoschwefel (IV) trifluorid sowie neuen P.3058-3063. Комп’ютерна в ерстка Р. Ціхановський Підписне Тираж 38 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, Льв івська площа, 8, м. Київ , МСП, 04655, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for the preparation of organyltrifluorosulfuranes
Автори англійськоюShermolovych Yurii Hryhorovych, Yahupolskyi Lev Musiiovych
Назва патенту російськоюСпособ получения органилтрифторосульфуранов
Автори російськоюШермолович Юрий Григорьевич, Ягупольский Лев Мусийович
МПК / Мітки
МПК: C07C 321/00, C07C 313/00, C07B 39/00
Мітки: спосіб, органілтрифторосульфуранів, одержання
Код посилання
<a href="https://ua.patents.su/3-71020-sposib-oderzhannya-organiltriftorosulfuraniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання органілтрифторосульфуранів</a>
Попередній патент: Спосіб електрохімічної обробки катіоніту
Наступний патент: Тканина фільтрувальна
Випадковий патент: Теплообмінник для утилізації гарячих відхідних газів







