Протипухлинна комбінація, що містить антитіло, яке специфічно розпізнає cd38, і бортезоміб
Номер патенту: 112170
Опубліковано: 10.08.2016
Автори: Декерт Джутта, Лежен Паскаль, Парк Пітер Ю, Мейо Мішель Ф
Формула / Реферат
1. Фармацевтична комбінація, що містить антитіло, яке специфічно розпізнає CD38, і щонайменше бортезоміб, де вказане антитіло містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні гіперваріабельні ділянки, що містять амінокислотні послідовності SEQ ID NO: 13, 14 (або 81) і 15, і де вказаний легкий ланцюг містить три послідовні гіперваріабельні ділянки, що містять амінокислотні послідовності SEQ ID NO: 16, 17 і 18.
2. Комбінація за п. 1, де вказане антитіло являє собою химерне або гуманізоване антитіло.
3. Комбінація за будь-яким з пп. 1-2, де вказане антитіло містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить амінокислотну послідовність SEQ ID NO: 66, і де вказаний легкий ланцюг містить амінокислотну послідовність, вибрану з групи, яка складається з SEQ ID NO: 62 або 64.
4. Фармацевтична комбінація, що містить антитіло, яке специфічно розпізнає CD38, і щонайменше бортезоміб, де вказане антитіло складається з легкого ланцюга, який містить амінокислотну послідовність SEQ ID NO: 62, і важкого ланцюга, який містить амінокислотну послідовність SEQ ID NO: 66.
5. Комбінація за будь-яким одним з пп. 1-4 для застосування в лікуванні раку, де протипухлинна ефективність комбінації складає від приблизно 11 до приблизно 42 % Т/С.
6. Комбінація за будь-яким одним з пп. 1-4 для застосування в лікуванні раку, де протипухлинна ефективність комбінації складає від приблизно 0 до приблизно 10 % Т/С.
7. Фармацевтична комбінація за будь-яким одним з пп. 1-4 для застосування в лікуванні раку.
8. Комбінація за п. 7, де вказане антитіло являє собою химерне або гуманізоване антитіло.
9. Комбінація за пп. 7-8, де антитіло, що специфічно розпізнає CD38, і бортезоміб вводять окремо.
10. Комбінація за пп. 7-8, де антитіло, що специфічно розпізнає CD38, і бортезоміб вводять з невеликим інтервалом.
11. Комбінація за пп. 7-8, де введення антитіла, що специфічно розпізнає CD38, і бортезомібу є тривалим протягом певного періоду часу так, щоб отримувати максимальну ефективність комбінації.
12. Промисловий виріб, що містить:
a) пакувальний матеріал,
b) комбінацію антитіла, що специфічно розпізнає CD38, і щонайменше бортезомібу, де вказане антитіло містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні гіперваріабельні ділянки, що містять амінокислотні послідовності SEQ ID NO: 13, 14 (або 81) і 15, і де вказаний легкий ланцюг містить три послідовні гіперваріабельні ділянки, що містять амінокислотні послідовності SEQ ID NO: 16, 17 і 18; і
с) етикетку або вкладиш в упаковку, що міститься у вказаному пакувальному матеріалі, які вказують, що вказана їх комбінація є ефективною для лікування раку.
Текст
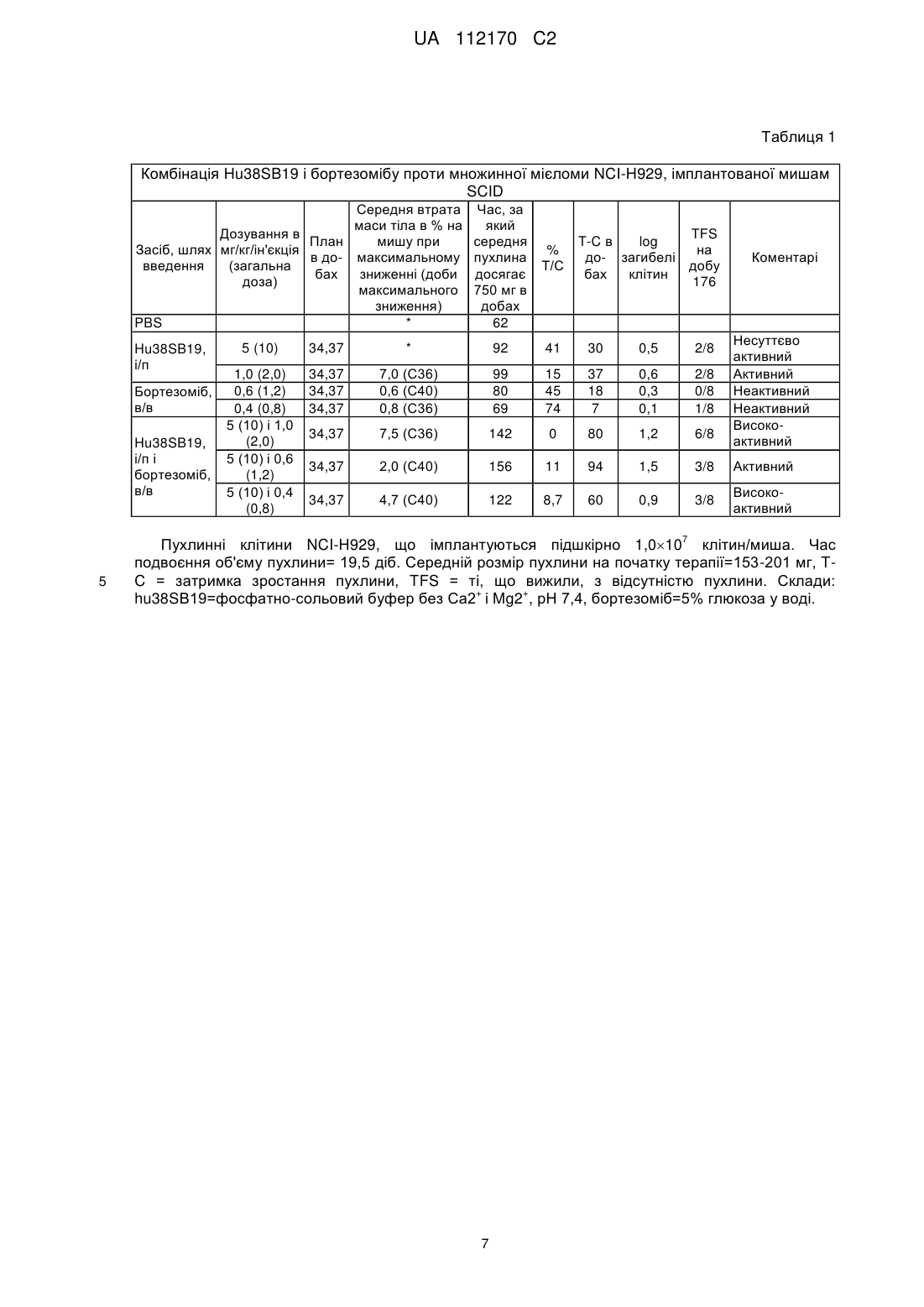
Реферат: Винахід стосується фармацевтичної композиції, що містить антитіло, яке специфічно розпізнає CD38, і бортезоміб. UA 112170 C2 (12) UA 112170 C2 UA 112170 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід стосується комбінацій моноклональних антитіл, направлених проти CD38, і бортезомібу, які є терапевтично придатними при лікуванні неопластичних захворювань. CD38 являє собою трансмембранний глікопротеїн II типу 45 кДа з довгим С-кінцевим позаклітинним доменом і коротким N-кінцевим цитоплазматичним доменом. Білок CD38 являє + собою біфункціональний екзофермент, який може каталізувати конверсію NAD в циклічну АДФрибозу (cADPR), а також гідролізувати cADPR до АДФ-рибози. Експресія CD38 підвищується, і він пов'язаний з багатьма гематопоетичними злоякісними новоутвореннями. Моноклональні антитіла 38SB13, 38SB18, 38SB19, 38SB30, 38SB31 і 38SB39, які специфічно розпізнають CD38, описані в заявці PCT WO2008/047242, повністю включеній в даний опис за + допомогою посилання. Вказані антитіла до CD38 здатні знищувати CD38 клітини за допомогою трьох різних цитотоксичних механізмів: індукція апоптозу, антитілозалежна клітинна цитотоксичність (ADCC) і комплементзалежна цитотоксичність (CDC). Крім того, ці антитіла + здатні безпосередньо індукувати апоптоз CD38 клітин, навіть за відсутності стромальних клітин або продукованих клітинами строми цитокінів. Термін "антитіло" використовують в даному описі в самому широкому значенні, і воно конкретно включає моноклональні антитіла (включаючи непроцесовані моноклональні антитіла) будь-якого ізотипу, такого як IgG, IgM, IgA, IgD і IgE, поліклональні антитіла, поліспецифічні антитіла, химерні антитіла і фрагменти антитіл. Характерне антитіло IgG складається з двох ідентичних важких ланцюгів і двох ідентичних легких ланцюгів, які сполучені дисульфідними зв'язками. Кожний важкий і легкий ланцюг містить константну ділянку і варіабельну ділянку. Кожна варіабельна ділянка містить три сегменти, які називаються "ділянками, що визначають комплементарність " ("CDR") або "гіперваріабельними ділянками", які переважно відповідальні за зв'язування епітопу антигену. Як правило, їх позначають як CDR1, CDR2 і CDR3, нумеруючи послідовно від N-кінця. Найбільш висококонсервативні ділянки варіабельних ділянок поза CDR називаються "каркасними ділянками". Як використовують в даному описі, "VH" або "VH" стосується варіабельної ділянки важкого ланцюга імуноглобуліну антитіла, включаючи важкий ланцюг Fv-, scFv-, dsFv-, Fab-, Fab'- або F(аb')2-фрагмента. Посилання на "VL" або "VL" стосується варіабельної ділянки легкого ланцюга імуноглобуліну антитіла, включаючи легкий ланцюг Fv-, scFv-, dsFv-, Fab-, Fab'- або F(ab')2фрагмента. Антитіло 38SB13 містить щонайменше один важкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:50, і щонайменше один легкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:38, де вказаний важкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:1, 2 і 3, і вказаний легкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:4, 5 і 6. Антитіло 38SB18 містить щонайменше один важкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:52, і щонайменше один легкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:40, де вказаний важкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:7, 8 і 9, і вказаний легкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:10,11 і 12. Антитіло 38SB19 містить щонайменше один важкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO 54, і щонайменше один легкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:42, де вказаний важкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:13, 14 (або 81) і 15, і вказаний легкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:16, 17 і 18. Антитіло 38SB30 містить щонайменше один важкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:56, і щонайменше один легкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:44, де вказаний важкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:19, 20 і 21, і вказаний легкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:22, 23 і 24. Антитіло 38SB31 містить щонайменше один важкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:58, і щонайменше один легкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:46, де вказаний важкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:25, 26 і 27, і вказаний легкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:28, 29 і 30. 1 UA 112170 C2 5 10 15 20 25 30 35 40 45 50 55 60 Антитіло 38SB39 містить щонайменше один важкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:60, і щонайменше один легкий ланцюг, що містить амінокислотну послідовність, яка складається з SEQ ID NO:48, де вказаний важкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:31, 32 і 33, і вказаний легкий ланцюг містить три послідовні CDR, що містять амінокислотні послідовності, які складаються з SEQ ID NO:34, 35 і 36. Гібридомні клітинні лінії, що продукують 38SB13, 38SB18, 38SB19, 38SB30, 38SB31 і 38SB39 антитіла миші до CD38 були депонованими в Американській колекції типових культур (10801 University Bid, Manassas, VA, 20110-2209, USA), 21 червня 2006 року, під реєстраційними номерами РТА-7667, РТА-7669, РТА-7670, РТА-7666, РТА-7668 і РТА-7671 відповідно (як описано в WO2008/047242, повністю включеній в даний опис за допомогою посилання). Термін "гуманізоване антитіло", як використовують в даному описі, стосується химерного антитіла, яке містить мінімальну послідовність, що виділяється з імуноглобуліну, що не належить людині. Метою гуманізації є зниження імуногенності ксеногенного антитіла, такого як антитіло миші, для введення людині, при цьому зберігаючи повну антигенну афінність зв'язування і специфічність антитіла. Гуманізовані антитіла або антитіла, адаптовані для невідторгнення іншими ссавцями, можна отримувати декількома способами, такими як зміна поверхні і трансплантація CDR. Як використовують в даному описі, спосіб зміни поверхні використовують в поєднанні з молекулярним моделюванням, статистичним аналізом і мутагенезом для зміни поверхонь не CDR варіабельних ділянок антитіла для доведення до схожості з поверхнями, відомих антитіл хазяїна-мішені. Спосіб трансплантації CDR включає заміщення ділянок, що визначають комплементарність, наприклад, антитіла миші, в каркасному домені людини, наприклад, див. WO 92/22653, повністю включену в даний опис за допомогою посилання. Гуманізовані химерні антитіла можуть містити константні ділянки і варіабельні ділянки, відмінні від ділянок, що визначають комплементарність (CDR), що виділяються по суті або виключно з відповідних ділянок антитіла людини, і CDR, що виділяються по суті або виключно у ссавця, що не є людиною. Стратегії і способи зміни поверхні антитіл і інші способи зниження імуногенності антитіл у різного хазяїна, описані в патенті США 5639641, який, таким чином, повністю включений за допомогою посилання. Антитіла можна гуманізувати різними іншими способами, включаючи трансплантацію CDR (EP 0239400, WO 91/09967, патенти США №№ 5530101 і 5585089), заміну поверхневих амінокислот або зміну поверхні (EP 0592106, EP 0519596, Padlan Е.А., 1991, Molecular Immunology 28(4/5):489-498, Studnicka G.M. et al, 1994, Protein Engineering, 7(6):805814, Roguska М.А. et al., 1994, PNAS, 91:969-973, повністю включені в даний опис за допомогою посилання), перестановку ланцюгів (патент США № 5565332, повністю включений в даний опис за допомогою посилання) і визначення залишків конформаційної рухливості (PCT/US2008/074381, повністю включений в даний опис за допомогою посилання). Антитіла людини можна отримувати різними відомими в даній галузі способами, включаючи способи фагового дисплея. Див. також патенти США №№ 4444887, 4716111, 5545806 і 5814318, і публікації міжнародних патентних заявок номера WO 98/46645, WO 98/50433, WO 98/24893, WO 98/16654, WO 96/34096, WO 96/33735 і WO 91/10741 (вказані посилання повністю включені за допомогою посилання). Антитіла до CD38 фармацевтичної комбінації за даним винаходом являють собою + гуманізовані антитіла, які розпізнають CD38 і знищують CD38 клітини шляхом апоптозу, ADCC і CDC. У додатковому варіанті здійснення гуманізовані антитіла за винаходом здатні знищувати + вказані CD38 клітини шляхом апоптозу навіть за відсутності стромальних клітин або продукованих клітинами строми цитокінів. Один з варіантів здійснення такого гуманізованого антитіла являє собою гуманізоване антитіло 38SB13, 38SB18, 38SB19, 38SB30, 38SB31 або 38SB39 або їх зв'язуючий епітоп фрагмент. CDR антитіл 38SB13, 38SB18, 38SB19, 38SB30, 38SB31 і 38SB39 визначають моделюванням і теоретично розраховують їх молекулярні структури. Таким чином, в одному з варіантів здійснення даний винахід стосується гуманізованих антитіл або їх зв'язуючого епітоп фрагмента, що містить одну або більше CDR, що містять амінокислотну послідовність, вибрану з групи, що складається з SEQ ID NO:1, 2, 3,4, 5, 6,7, 8, 9, 10,11, 12, 13,14, 15, 16,17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 і 81. В одному з варіантів здійснення наданий гуманізований варіант 38SB13, який містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:1, 2, і 3, і де вказаний легкий ланцюг містить три послідовні ділянки, що визначають 2 UA 112170 C2 5 10 15 20 25 30 35 40 45 50 55 60 комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:4, 5 і 6. В іншому варіанті здійснення наданий гуманізований варіант 38SB18, який містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:7, 8 і 9, і де вказаний легкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:10, 11 і 12. В іншому варіанті здійснення наданий гуманізований варіант 38SB19, який містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:13, 14 (або 81) і 15, і де вказаний легкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:16, 17 і 18. В іншому варіанті здійснення наданий гуманізований варіант 38SB30, який містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:19, 20 і 21, і де вказаний легкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:22, 23 і 24. В іншому варіанті здійснення наданий гуманізований варіант 38SB31, який містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:25, 26 і 27, і де вказаний легкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:28, 29 і 30. В іншому варіанті здійснення наданий гуманізований варіант 38SB39, який містить щонайменше один важкий ланцюг і щонайменше один легкий ланцюг, де вказаний важкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:31, 32 і 33, і де вказаний легкий ланцюг містить три послідовні ділянки, що визначають комплементарність, які містять амінокислотні послідовності, надані SEQ ID NO:34, 35 і 36. В одному з варіантів здійснення даний винахід стосується гуманізованих антитіл або їх фрагментів, які містять VH, що містить амінокислотну послідовність, вибрану з групи з SEQ ID NO:66 і 72. В одному з варіантів здійснення надане гуманізоване антитіло 38SB19, яке містить VH, що містить амінокислотну послідовність, надану SEQ ID NO:66. В іншому варіанті здійснення надане гуманізоване антитіло 38SB31, яке містить VH, що містить амінокислотну послідовність, надану SEQ ID NO:72. В іншому варіанті здійснення даний винахід стосується гуманізованих антитіл або їх фрагментів, які містять VL, що містить амінокислотну послідовність, вибрану з групи з SEQ ID NO:62, 64, 68 і 70. В одному з варіантів здійснення надане гуманізоване антитіло 38SB19, яке містить VL, що містить амінокислотну послідовність, вибрану з групи з SEQ ID NO:62 і 64. В іншому варіанті здійснення надане гуманізоване антитіло 38SB31, яке містить VL, що містить амінокислотну послідовність, вибрану з групи з SEQ ID NO: 68 і 70. Показано, що кожний з гуманізованих варіантів антитіл 38SB13, 38SB18, 38SB19, 38SB30, 38SB31 і 38SB39 є особливо ефективним як протиракові засоби, їх отримання, фізичні властивості і сприятливі фармакологічні властивості описані в WO 2008/047242, яка повністю включена в даний опис за допомогою посилання. В основному, дози, що застосовуються для лікування індивідуума, що є людиною, які залежать від чинників, характерних для індивідууму, що підлягає лікуванню, знаходяться в діапазоні від 1 до 150 мг/кг, від 10 до 100 мг/кг або від 50 до 100 мг/кг при пероральному введенні або від 1 до 150 мг/кг, від 10 до 100 мг/кг або від 50 до 100 мг/кг при внутрішньовенному введенні. Бортезоміб являє собою дипептид боронової кислоти ([(1R)-3-метил-1-({(2S)-3-феніл-2[(піразин-2-ілкарбоніл)аміно]пропаноїл}аміно)бутил]боронова кислота, торгове найменування: Velcade™) з протипухлинною дією (Richardson et al., N. Engl. J. Med., 352:2487-2498, 2005). Бортезоміб являє собою високоспецифічний зворотний інгібітор 26S-протеасоми. У нормальних клітинах протеасома регулює експресію і функцію білків за допомогою деградації убіквітинілованих білків, крім того, вона залучена в елімінацію неправильно згорнених білків. Механізм дії бортезомібу включає стабілізацію NF-kB, p21, р27, р53, Bid і Вах, інгібування активації кавеоліну-1 і активацію JNK, а також реакцію на стрес ендоплазматичного ретикулума (Boccadoro et al., Cancer Cell Int., 5(1): 18, 2005). Незважаючи на те, що найвірогідніше залучені багато які механізми, інгібування протеасоми, таким чином, може забезпечувати активацію загибелі клітин, що програмується в неопластичних клітинах в залежності від придушення проапоптотичних шляхів. Зокрема, засіб інгібує ядерний фактор (NF)-каппаB, таким чином, 3 UA 112170 C2 5 10 15 20 25 30 35 40 45 50 55 60 перешкоджаючи опосередкованій NF-каппаВ виживаності клітин, зростанню пухлини і ангіогенезу. Таким чином, бортезоміб застосовують для лікування множинної мієломи і лімфоми мантійних клітин. Бортезоміб, як правило, вводять внутрішньовенно. У цей час виявлено і для даного винаходу, що ефективність гуманізованих антитіл до CD38 можна значно поліпшувати при їх введенні в комбінації щонайменше з однією речовиною, яка є терапевтично придатною в лікуванні типів раку і має механізм, ідентичний або відмінний від механізму гуманізованих антитіл до CD38, і яка обмежена в даному винаході бортезомібом. Крім того, що активність залежить від використовуваної дози, можна використати більш низькі дози і збільшувати активність, в той же час знижуючи токсичність явищ. Поліпшену ефективність комбінації за винаходом можна продемонструвати визначенням терапевтичного синергізму. Комбінація виявляє терапевтичний синергізм, якщо вона терапевтично перевершує найкращий засіб дослідження, що застосовується окремо в його максимально переносимій дозі або в його найбільш високій дозі, що тестується, при якій не отримують токсичність у видів тварин. Цю ефективність можна кількісно оцінювати, наприклад, за допомогою log10 загибелі клітин, який визначають за наступною формулою: log10 загибелі клітин=Т-С (доба)/3,32Тd в якій T-C являє собою затримку росту пухлини, яка є середнім часом в добах для пухлин групи, що отримувала лікування, (T) і пухлин контрольної групи (C) до досягнення попередньо визначеного значення (1 г, наприклад), і Td являє собою час в добах, необхідний для подвоєння об'єму пухлини у контрольних тварин [Т.Н. Corbett et al., Cancer, 40:2660-2680 (1977), F.M. Schabel et al., Cancer Drug Development, Part В., Methods in Cancer Research, 17:3-51, New York, Academic Press Inc. (1979)]. Вважають, що продукт є активним, якщо log10 загибелі клітин є більшим або дорівнює 0,7. Вважають, що продукт є дуже активним, якщо log10 загибелі клітин є більшим або дорівнює 2,8. Комбінація виявляє терапевтичний синергізм, коли log10 загибелі клітин є більшим значення log10 загибелі клітин найкращого компонента, що вводиться окремо в його максимально переносимій дозі або в його найбільш високій дозі, що тестується. Ефективність комбінацій відносно солідних пухлин можна визначати експериментально наведеним нижче способом. Тваринам, як правило, мишам, що піддаються експерименту, підшкірно трансплантують з однієї сторони або з двох сторін пухлинні клітини або фрагмент на 0 добу. Тварин, що несуть пухлини, у випадковому порядку розподіляли по групах в залежності від розміру їх пухлини до піддавання різним видам лікування і контролям. Хіміотерапію починають, коли пухлини досягають попередньо визначеного розміру після трансплантації в залежності від типу пухлини, і спостерігають тварин кожну добу. Різні групи тварин зважують щодобово під час лікування доти, поки, не отримують максимальну втрату маси, і настає подальше повне відновлення маси. Потім групи зважують один раз або двічі на тиждень до закінчення випробування. Пухлини вимірюють від 1 до 5 разів на тиждень в залежності від часу подвоєння об'єму пухлини доти, поки пухлина не досягає приблизно 750 мг, або доти, поки тварина не гине (якщо це відбувається до того, як пухлина досягне 750 мг). Тваринам проводять розтин відразу після евтаназії або загибелі. Протипухлинну активність визначають відповідно до різних зареєстрованих параметрів. Результати, що отримуються з комбінаціями hu38SB19 і бортезомібом, які застосовуються вїх оптимальних дозах, наведені в даному описі як приклади. Таким чином, даний винахід також стосується фармацевтичних композицій, що містять комбінації за винаходом. Компоненти, з яких складається комбінація, можна вводити одночасно, з невеликим інтервалом, окремо або тривало протягом певного періоду часу так, щоб отримувати максимальну ефективність комбінації, де для кожного введення можна змінювати його тривалість від швидкого введення до безперервної перфузії. Інтервал між щонайменше одним введенням антитіла, що специфічно розпізнає CD38, і щонайменше одним введенням бортезомібу становить приблизно 1 місяць або менше, або приблизно 2 тижні або менше, або приблизно 1 добу або менше. Таким чином, з метою даного винаходу комбінації не обмежені тільки такими, які отримують фізичною асоціацією компонентів, а також такими, які дозволяють окреме введення, яке може бути одночасним або тривалим протягом певного періоду часу. Композиції за винаходом переважно являють собою композиції, які можна вводити парентерально. Однак ці композиції можна вводити перорально, підшкірно або інтраперитонеально у випадку локальних регіональних терапій. 4 UA 112170 C2 5 10 15 20 25 30 35 40 45 50 55 60 Композиції для парентерального введення, як правило, являють собою фармацевтично прийнятні стерильні розчини або суспензії, які необов'язково можна отримувати, як необхідно в момент використання. Для отримання неводних розчинів або суспензій можна використати природні рослинні олії, такі як оливкова олія, сезамова олія або рідкий вазелін, або ін'єктовані органічні складні ефіри, такі як етилолеат. Стерильні водні розчини можуть складатися з розчину продукту у воді. Водні розчини є придатними для внутрішньовенного введення, отриманий рН є відповідним чином підведеним, і розчин отримують ізотонічним, наприклад, з достатньою кількістю хлориду натрію або глюкози. Стерилізацію можна провести нагріванням або будь-яким іншим способом, який не надає негативної дії на композицію. Комбінації також можуть знаходитися в формі ліпосом або в формі асоціації з носіями, такими як циклодекстрини або поліетиленгліколі. Композиції для перорального, підшкірного або інтраперитонеального введення переважно можуть являти собою водні суспензії або розчини. У комбінаціях за винаходом, застосування компонентів яких може бути одночасним, окремим або тривалим протягом певного періоду часу, особливо переважно, щоб кількість гуманізованого антитіла до CD38 складала від 10 до 90% по масі комбінації, де можливо, що цей вміст варіює в залежності від природи асоційованої речовини, бажаної ефективності і від природи підлягаючого лікуванню раку. Комбінації за винаходом є особливо придатними при лікуванні деяких типів раку, включаючи (але, не обмежуючись ними) наступні: карциному і аденокарциному, включаючи карциному сечового міхура, молочної залози, товстої кишки, голови і шиї, передміхурової залози, нирки, печінки, легені, яєчника, підшлункової залози, шлунка, шийки матки, щитовидної залози і шкіри, і включаючи плоскоклітинну карциному; гемопоетичні пухлини лімфоїдного походження, включаючи множинні мієломи, лейкоз, гострий і хронічний лімфоцитарний (або лімфоїдний) лейкоз, гострий і хронічний лімфобластний лейкоз, В-клітинну лімфому, Т-клітинну лімфому, неходжкінську лімфому (наприклад, Беркіта); гемопоетичні пухлини мієлоїдного походження, включаючи гострий і хронічний мієлогенні (мієлоїдні або мієлоцитарні) лейкоз і промієлоцитарний лейкоз, пухлини мезенхімального походження, включаючи фібросаркому, остеосаркому і рабдоміосаркому, пухлини центральної і периферичної нервової системи, включаючи астроцитому, нейробластому, гліому і шваноми, і інші пухлини, включаючи меланому, тератокарциному, пігментну ксеродерму, кератоакантому і семиному і інші типи раку, які ще визначають, в яких експресується CD38. Вони в основному є придатними для лікування лейкозу, лімфоми і типів раку, стійких до протиракових засобів, що широко використовуються, оскільки антитіла до CD38 за винаходом мають унікальний механізм дії. В одному з варіантів здійснення протипухлинна ефективність комбінації становить приблизно 11-42% Т/С. Т/С(%) являє собою відношення середній об'єм пухлини тих, що отримували лікування/середній об'єм пухлини контролю100. В іншому варіанті здійснення протипухлинна ефективність комбінації становить приблизно 0-10% Т/С. Таким чином, один з аспектів винаходу являє собою вказані вище комбінації для застосування при лікуванні раку. В іншому аспекті винахід також стосується застосування вказаних вище комбінацій для отримання лікарського засобу для лікування раку. Інший варіант здійснення винаходу являє собою промисловий виріб, що містить: a) пакувальний матеріал; b) комбінацію антитіла, що специфічно розпізнає CD38, і щонайменше бортезомібу, де + вказане антитіло здатне знищувати CD38 клітини шляхом апоптозу, антитілозалежної клітинної цитотоксичності (ADCC) і комплементзалежної цитотоксичності (CDC) і c) етикетку або вкладиш в упаковку, що міститься у вказаному пакувальному матеріалі, який вказує, що вказана їх комбінація є ефективною для лікування раку. Приклад У цьому прикладі продемонстрована ефективність in vivo комбінації антитіла до CD38/бортезомібу за винаходом відносно інгібування зростання пухлини. Введення препарату, що тестується Лікування hu38SB19 і бортезомібом починали після закінчення тридцяти чотирьох діб після інокуляції клітин, і дози розраховували на основі маси тіла окремих тварин, що визначається з останнього вимірювання, яке проводиться до дозування. Введення PBS і антитіла hu38SB19 проводили шляхом інтраперитонеальної (і/п) ін'єкції і бортезоміб, за допомогою внутрішньовенної (в/в) ін'єкції в хвостову вену з використанням 1,0 мл шприца, оснащеного голкою 27 калібру, 1/2 дюйми. Конкретний план дослідження 5 UA 112170 C2 5 10 15 20 25 30 35 40 45 50 У самиць мишей CB. 17 SCID ініціювали модель підшкірного ксенотрансплантату множинної 7 мієломи NCI-H929 шляхом підшкірної ін'єкції 110 клітин на мишу, суспендованих в 0,1 мл середовища для культивування, яке не містить сироватки. Після закінчення тридцяти трьох діб після інокуляції пухлинних клітин шістдесят чотири миші у випадковому порядку розподіляли у 8 груп (n=8) по об'єму пухлини. Об'єми пухлин 3 знаходилися в діапазоні від 86,7 до 355,2 ((189,0±74,3), середнє значення±SD) мм . Маса тіла мишей знаходилася в діапазоні від 17,2 до 22,4 ((19,4±1,1), середнє значення±SD) грам. Мишей в кожній групі ідентифікували по отвору у вусі. Групи, що отримували лікування, включали контроль PBS (200 мкл/миша/обробка), антитіло hu38SB19 (5,0 мг/кг/обробка), бортезоміб (1,0, 0,6 і 0,4 мг/кг/обробка) і групи трьох комбінацій з hu38SB19 (5,0 мг/кг/обробка) і бортезомібом (1,0, 0,6 і 0,4 мг/кг/обробка). PBS, hu38SB19 і бортезоміб вводили двічі на тиждень протягом одного тижня (34 і 37 діб сукупно для 2 видів лікування). Лікування починали на 34 добу після інокуляції пухлинних клітин. Об'єми пухлин вимірювали від одного до двох разів на добу щотижня в трьох напрямах з 3 використанням циркуля. Об'єм пухлини виражали в мм (або мг) з використанням формули: V=довжинаширинависота1/2. Масу тіла вимірювали двічі на тиждень як приблизний показник токсичності засобу, що тестується. Об'єм пухлини і масу тіла визначали і реєстрували за допомогою програмного забезпечення Labcat. Результати Протипухлинну активність антитіла hu38SB19 і бортезомібу окремо і в комбінації оцінювали у самиць мишей SCID, які несуть підшкірні ксенотрансплантати пухлини NCI-H929, моделі множинної мієломи людини. Використали наступні кінцеві точки: Токсичність визнавали при дозуванні лікарського засобу, що включає 20% втрати маси тіла або 10% загибелі. Протипухлинну ефективність визначали, розраховуючи: Т/С(%)=середній об'єм пухлини що отримували лікування/середню об'єм пухлини контролюхЮО, де Т/С42% є мінімальним рівнем протипухлинної активності. Т/С
ДивитисяДодаткова інформація
Назва патенту англійськоюAntitumor combinations containing antibodies recognizing specifically cd38 and bortezomib
Автори англійськоюDeckert, Jutta, Lejeune, Pascale, Mayo, Michele F, Park, Peter U
Автори російськоюДекерт Джутта, Лежен Паскаль, Мейо Мишель Ф, Парк Питер Ю
МПК / Мітки
МПК: C07K 16/28, A61K 39/395, A61K 31/495, A61P 35/00
Мітки: яке, містить, комбінація, антитіло, протипухлинна, розпізнає, cd38, специфічно, бортезоміб
Код посилання
<a href="https://ua.patents.su/41-112170-protipukhlinna-kombinaciya-shho-mistit-antitilo-yake-specifichno-rozpiznaeh-cd38-i-bortezomib.html" target="_blank" rel="follow" title="База патентів України">Протипухлинна комбінація, що містить антитіло, яке специфічно розпізнає cd38, і бортезоміб</a>
Попередній патент: Відновлений керамічний нагрівальний елемент
Наступний патент: Інгенол-3-ацилати iii і інгенол-3-карбамати
Випадковий патент: Спосіб одержання магнітного сплаву