Біарилзаміщені похідні азабіциклічних алканів
Номер патенту: 99936
Опубліковано: 25.10.2012
Автори: Гопалакрішнан Муралі, Лі Чіх-Хунг, Лі Тао, Сіппі Кевін Б, Цзи Цзяньго
Формула / Реферат
1. Сполука формули (І)
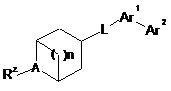 (I)
(I)
або її фармацевтично прийнятна сіль, або її проліки, де
n дорівнює 1, 2 або 3;
А являє собою N або Ν+-Ο;
Rz являє собою водень, алкіл, циклоалкіл або арилалкіл;
L вибраний із групи, що складається з О, S чи -N(Ra)-;
Аr1 являє собою 5-членну гетероарильну групу;
Аr2 являє собою арильну або гетероарильну групу, і
Ra вибраний із групи, що складається з водню, алкілу і алкілкарбонілу.
2. Сполука за п. 1, де Аr1 вибраний із групи, що складається з:
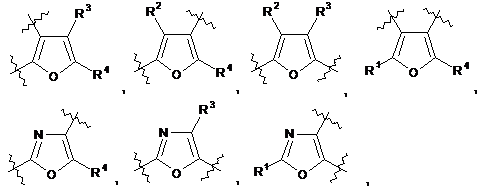

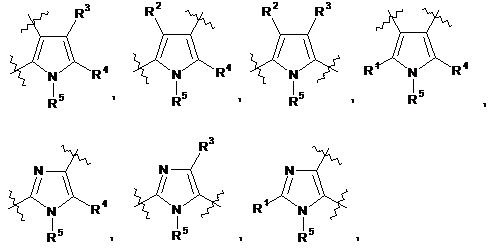
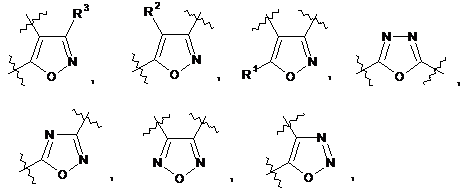
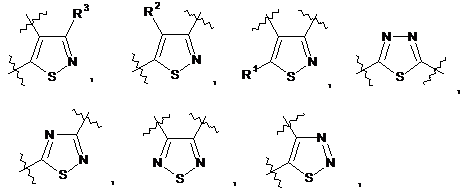

де
R1, R2, R3 і R4 незалежно являють собою водень, ацил, ацилокси, алкеніл, алкокси, алкоксіалкокси, алкоксіалкіл, алкоксикарбоніл, алкоксііміно, алкоксисульфоніл, алкіл, алкілсульфоніл, алкініл, аміно, карбокси, ціано, форміл, галогеналкокси, галогеналкіл, галоген, гідрокси, гідроксіалкіл, меркапто, нітро, тіоалкокси, -NRgRj, (NRgRj)алкіл, (NRgRj)aлкoкcи, (NRgRj)кapбoнiл або (NRgRj)сульфоніл;
R5 являє собою водень, ацил, алкіл або алкілсульфоніл; і кожний з Rg і Rj незалежно являє собою водень або алкіл, або алкілкарбоніл.
3. Сполука за п. 1, де Аr2 являє собою

де
кожний з Ζ1, Ζ2, Ζ3, Ζ4 і Z5 незалежно являє собою азот або є вуглецем, де атом вуглецю необов'язково заміщений замісником, вибраним із групи, що складається з водню, галогену, алкілу, -ORc, -алкіл-ORc, -NRdRe і -алкіл-NRdRe;
кожний з R6 і R7 незалежно вибирають із групи, що складається з водню, алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксііміно, алкоксисульфонілу, алкілу, алкілкарбонілу, алкілкарбонілокси, алкілсульфонілу, алкінілу, карбокси, ціано, формілу, галогеналкокси, галогеналкілу, галогену, водню, гідрокси, гідроксіалкілу, меркапто, нітро, тіоалкокси, -NRfRg, (NRfRg)алкілу, (NRfRg)алкокси, (NRfRg)кapбoнiлy і (NRfRg)cyльфoнiлy; кожний з Ra, Rb, Rc, Rd, Re, Rf і Rg незалежно являє собою водень, алкіл або алкілкарбоніл.
4. Сполука за п. 3, яка додатково включає таутомери сполуки, коли R6 або R7 являють собою гідрокси.
5. Сполука за п. 2, де
А являє собою N;
Rz являє собою Η або метил;
L являє собою О;
n дорівнює 2, і
Аr1 являє собою
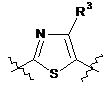 або
або  .
.
6. Сполука за п. 3, де
А являє собою N;
Rz являє собою Η або метил;
L являє собою О;
n дорівнює 2;
Аr2 являє собою
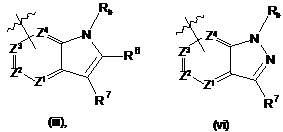 .
.
7. Сполука за п. 2, де
А являє собою N;
Rz являє собою Η або метил;
L являє собою О;
n дорівнює 2;
Аr1 являє собою
 і
і
Аr2 являє собою
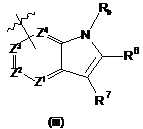 .
.
8. Сполука за п. 1, вибрана з групи, що складається з
2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілоксі]-5-(1H-індол-5-іл)тіазол;
2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол;
2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл)тіазол;
5-(1H-індол-6-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол;
5-(1H-індол-4-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол;
5-(бензофуран-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол;
5-(бензо[b]тіофен-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол;
5-(2-(трифторметил)-1Н-індол-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол;
5-(дибензо[b,d]тіофен-2-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол;
2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілоксі]-5-(1Н-індол-5-іл)тіазол;
2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілоксі]-5-(1Н-індол-6-іл)тіазол;
2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол;
2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл)тіазол;
2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-феніл-1,3,4-тіадіазол;
2-(1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(бензофуран-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(бензо[b]тіофен-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(3-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-13,4-тіадіазол;
2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-м-толіл-1,3,4-тіадіазол;
2-(4-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(3-хлорфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(1Н-індол-6-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(1Н-індол-4-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(3-ціанофеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(3-трифторметилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(4-хлорфеніл)-5-((1R,3R,5S)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси)-1,3,4-тіадіазол;
2-(2-(трифторметил)-1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(3-хлор-4-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(4-(трифторметил)феніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(4-метоксифеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(3-амінофеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(4-етилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол;
2-(4-ацетилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол
і
N-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-іл]-5-феніл-1,3,4-тіадіазол-2-амін.
9. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за п. 1 і фармацевтично прийнятний носій.
10. Спосіб селективного модулювання дії нікотинових ацетилхолінових рецепторів a7, нікотинових ацетилхолінових рецепторів a4b2 або обох нікотинових ацетилхолінових рецепторів a7 і a4b2 у ссавця, що включає введення ефективної кількості сполуки за п. 1.
11. Спосіб за п. 10, де сполука за п. 1 являє собою агоніст щонайменше одного з нікотинових ацетилхолінових рецепторів a7 або a4b2.
12. Спосіб лікування стану або порушення, опосередкованого нікотиновими ацетилхоліновими рецепторами a7 і a4b2, у суб'єкта, що включає введення суб'єкту сполуки за п. 1.
13. Спосіб за п. 12, де стан або порушення, опосередкований нікотиновими ацетилхоліновими рецепторами a7 і a4b2, вибирають із групи, що складається із синдрому дефіциту уваги, синдрому дефіциту уваги з гіперактивністю, хвороби Альцгеймера, легких когнітивних порушень, старечого слабоумства, слабоумства при СНІД, хвороби Піка, слабоумства, пов'язаного з тільцями Леві, слабоумства, пов'язаного із синдромом Дауна, аміотрофічного латерального склерозу, хвороби Хантінгтона, зниженої функції ЦНС внаслідок черепно-мозкової травми, гострого болю, післяопераційного болю, хронічного болю, запалення, запального болю, невропатичного болю, безплідності, необхідності нового росту кровоносних судин, пов'язаної з загоєнням ран, необхідності нового росту кровоносних судин, пов'язаної з васкуляризацією при пересадженні шкіри і відсутністю кровообігу, ревматоїдного артриту, хвороби Крона, виразкового коліту, запального захворювання кишечнику, відторгнення трансплантованих органів, гострого імунного захворювання, пов'язаного з трансплантацією органів, хронічного імунного захворювання, пов'язаного з трансплантацією органів, септичного шоку, синдрому токсичного шоку, синдрому сепсису, депресії, ревматичного спондиліту і токсикоманії.
14. Спосіб за п. 13, де стан або порушення, опосередкований нікотиновими ацетилхоліновими рецепторами a7 і a4b2, являє собою стан або порушення, опосередкований нікотиновими ацетилхоліновими рецепторами a7, і вибраний з групи, що складається з когнітивних розладів, нейродегенерації і шизофренії.
15. Спосіб за п. 14, де сполука за п. 1 являє собою агоніст щонайменше одного нікотинового ацетилхолінового рецептора a7, і де спосіб додатково включає введення атипового нейролептика.
16. Спосіб за п. 15, де атиповий нейролептик, являє собою щонайменше один, вибраний із групи, що складається з клозапіну, рисперидону, оланзапіну, кветапіну, зипразидону, зотепіну і ілоперидону.
17. Спосіб за п. 10, що додатково включає введення сполуки за п. 1 разом із другою композицією, використовуваною для лікування когнітивних порушень.
18. Спосіб за п. 17, де когнітивне порушення являє собою синдром дефіциту уваги і друга композиція включає щонайменше одну з вибраних із групи, що складається з декстроамфетаміну, левоамфетаміну, декстротреометилфенідату, левотреометилфенідату, амантадину, амінептину, бензфетаміну, бупропіону, клонідину, модафінілу, пемоліну, селегіліну і мілнаципрану.
19. Спосіб за п. 17, де когнітивне порушення являє собою хворобу Альцгеймера і друга композиція включає щонайменше одну, вибрану з групи, що складається з інгібітора ацетилхолінестерази, антагоніста NMDA, вітаміну С і вітаміну Е.
Текст
Реферат: Винахід стосується біарилзаміщених похідних азабіциклічних алканів, композицій, що включають такі сполуки, і способів лікування станів і порушень з використанням таких сполук і композицій. UA 99936 C2 (12) UA 99936 C2 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 ПЕРЕХРЕСНЕ ПОСИЛАННЯ НА СПОРІДНЕНУ ЗАЯВКУ За даною заявкою запитується пріоритет на підставі попередньої заявки сер. № 60/989538, поданої 21 листопада 2007 р. ГАЛУЗЬ ВИНАХОДУ Даний винахід належить до біарилзаміщених похідних азабіциклічних алканів, зокрема, до похідних азабіциклічних алканів, заміщених 5-членним гетероарильним кільцем, до композицій, що включають такі сполуки, а також до способів лікування станів і порушень з використанням таких сполук і композицій. ОПИС ВІДПОВІДНОЇ ГАЛУЗІ ТЕХНІКИ Нікотинові ацетилхолінові рецептори (nAChRs) широко поширені в центральній (ЦНС) і периферичній (ПНС) нервовій системі. Такі рецептори відіграють важливу роль у регулюванні функції ЦНС, зокрема, за рахунок модулювання вивільнення широкого спектра нейротрансмітерів, таких як ацетилхолін, норепінефрин, дофамін, серотонін і ГАМК. Отже, нікотинові рецептори опосередковують дуже широкий діапазон фізіологічних функцій і стали об'єктом для терапевтичного лікування розладів, пов'язаних з когнітивною діяльністю, навчанням і пам'яттю, нейродегенерацією, болем і запаленням, психозами і сенсорними шляхами, настроєм і емоціями, поряд з іншими. Рослинний алкалоїд нікотин взаємодіє з усіма підтипами nAChRs. Незважаючи на те, що нікотин, як було продемонстровано, має різну біологічну активність, не всі дії, опосередковувані нікотином, є бажаними. Наприклад, нікотин у терапевтичних дозах викликає побічні дії на шлунково-кишковий тракт і серцево-судинну систему, і він викликає звикання і залежність. Ліганди, що селективно взаємодіють тільки з визначеними підтипами nAChRs, надають можливість досягнення сприятливої лікувальної дії з підвищеним коефіцієнтом безпеки. Множина підтипів nAChRs була виявлена в центральній нервовій системі і периферичній нервовій системі. Кожен підтип по-різному впливає на регулювання загальних фізіологічних функцій. Зазвичай nAChRs являють собою іонні канали, що складаються з пентамерів. У нейронній тканини було виявлено щонайменше 12 субодиниць білків, 2-10 і 2-4. Ці субодиниці забезпечують велику різноманітність гомомерних і гетеромерних комбінацій, що є причиною різноманітних підтипів рецепторів. Наприклад, переважаючий рецептор, що відповідає за високу афінність зв'язування нікотину в тканині головного мозку, має склад (4)2(2)3 (підтип 42), тоді як інша основна популяція рецепторів являє собою гомопентамери (7)5 (підтип 7). 7 і 42 nAChRs: Рецептори з багатьма ролями 7 і 42 nAChRs грають ролі в різноманітних процесах, включаючи когнітивні функції, захист від дегенерацій нейронів, послаблення болю і шизофренії; а також виконують інші функції, що здаються менш пов'язаними з нейронною активністю, наприклад, ангіогенез і акросомна реакція сперми при заплідненні яйцеклітини. Було показано, що nAChRs 7 і 42 відіграють значну роль у підвищенні когнітивних функцій, включаючи аспекти навчання, пам'яті й уваги (Levin E D., J. Neurobiol. 53: 633-640, 2002). Так, наприклад, nAChRs 7 були пов'язані зі станами і порушеннями, що належать до синдрому дефіциту уваги (ADD), синдрому дефіциту уваги при гіперактивності (ADHD), хвороби Альцгеймера (ХА), помірних когнітивних порушень, старечого слабоумства, слабоумства, пов'язаного з тільцями Леві, слабоумства, пов'язаного із синдромом Дауна, слабоумства при СНІД, хвороби Піка, а також дефіциту когнітивних функцій, пов'язаного із шизофренією, поряд з іншою системною діяльністю. Підтип рецепторів 42 причетний до уваги, сприйняття, шизофренії, епілепсії і контролю болю (Paterson and Norberg, Progress in Neurobiology 61 75-111, 2000). На додаток до їхньої ролі в підвищенні когнітивних функцій було показано, що 7-вмісні nAChRs задіяні в нейропротекторну дію нікотину, як in vitro (Jonnala, R.B. and Buccafusco, J.J., J. Neurosci. Res. 66: 565-572, 2001), так і in vivo (Shimohama, S. et al., Brain Res. 779: 359-363, 1998). Більш конкретно, нейродегенеративні розлади лежать в основі цілого ряду прогресуючих захворювань ЦНС, таких як хвороба Альцгеймера, хвороба Паркінсона, латеральний аміотрофічний склероз, хвороба Хантінгтона, слабоумство з тільцями Леві, а також знижена функція ЦНС у результаті черепно-мозкової травми. Наприклад, порушення функції nAChRs 7 за рахунок -амілоїдних пептидів, пов'язаних із хворобою Альцгеймера, спричинило як ключовий фактор до розвитку когнітивного дефіциту, пов'язаного з захворюванням (Liu, Q.-S., Kawai, H. Berg, D.K., PNAS 98: 4734-4739, 2001). Було показано, що активація nAChRs 7 блокує таку нейротоксичність (Kihara, T. et al., J. Biol. Chem. 276: 13541-13546, 2001). Таким чином, селективні ліганди, що підвищують активність 7, можуть протистояти недолікам хвороби Альцгеймера й інших нейродегенеративних захворювань. 1 UA 99936 C2 5 10 15 20 25 30 35 40 45 Шизофренія являє собою комплексне захворювання, що характеризується порушеннями сприйняття, пізнання й емоцій. Є значущі по задіяності nAChRs 7 у дане захворювання, включаючи вимірюваний дефіцит цих рецепторів у пацієнтів після смерті (Leonard, S. Eur. J. Pharmacol. 393: 237-242, 2000). Дефіцит сенсорної обробки (гейтинг) є одним з ознак шизофренії. Цей дефіцит може бути приведений у норму за допомогою нікотинових лігандів, що працюють за допомогою nAChRs 7 (Adler L. E. et al., Schizophrenia Bull. 24: 189-202, 1998, Stevens, K. E. et al., Psychopharmacology 136: 320-327, 1998). Когнітивні порушення, пов'язані із шизофренією, часто обмежують можливості пацієнта нормально функціонувати, симптом, що виліковується неадекватно за допомогою загальнодоступних методів лікування, наприклад, при лікуванні атипічними нейролептиками. (Rowley, М. et al., J. Med. Chem. 44: 477-501, 2001). Такий когнітивний дефіцит був пов'язаний з дисфункцією нікотинової холінергічної системи, зокрема, зі зниженою активністю рецепторів. (Friedman, J.I. et al., Biol Psychiatry, 51: 349-357, 2002). Ангіогенез, процес задіяний у ріст нових кровоносних судин, має важливе значення в ряді корисних системних функцій, таких як загоєння раней, васкуляризація шкірних трансплантатів і посилення кровообігу, наприклад, збільшення циркуляції навколо оклюзії судини. Було показано, що неселективні агоністи nAChRs, такі як нікотин, стимулюють ангіогенез (Heeschen, К. et al., Nature Medicine 7: 833-839, 2001). Було показано, що активація nAChRs 7 задіяна в поліпшення ангіогенезу (Heeschen, К. et al., J. Clin. Invest. 110: 527-536, 2002). Популяція nAChRs 7 у спинному мозку модулює серотонергічну трансмісію, що пов'язана зі знеболювальною дією нікотинових сполук (Cordero-Erausquin М., and Changeux, J.-P. PNAS 98:2803-2807, 2001). Ліганди nAChRs 7 демонструють терапевтичний потенціал для лікування хворобливих станів, у тому числі гострого болю, післяопераційних болів, а також станів хронічного болю, включаючи запальний біль і нейропатичний біль. Крім того, nAChRs 7 експресуються на поверхні первинних макрофагів, що беруть участь у запальній відповідній реакції. Активація рецептора 7 інгібує вивільнення TNF і інших цитокінів, що включають запальну відповідну реакцію (Wang, H. et al., Nature 421: 384-388, 2003). TNF-опосередковані захворювання включають, наприклад, ревматоїдний артрит, хворобу Крона, виразковий коліт, запальне захворювання кишечнику, відторгнення трансплантованого органа, гостре імунне захворювання, пов'язане з трансплантацією органів, хронічне імунне захворювання, пов'язане з трансплантацією органів, септичний шок, синдром токсичного шоку, синдром сепсису, депресію і ревматичний спондиліт. Акросомна реакція сперми ссавців являє собою екзоцитозний процес, важливий для запліднення яйцеклітини спермою. Показано, що активація nACh 7 на клітинах сперми необхідна для акросомної реакції (Son, J.-H. and Meizel S. Biol. Reproduct. 68: 1348-1353 2003). Активність nAChRs як 7, так і 42 можна модулювати або регулювати за допомогою введення лігандів, селективних у відношенні підтипу nACh. Ліганди можуть виявляти властивості антагоніста, агоніста або часткового агоніста. Також відомі сполуки, що функціонують як позитивні алостеричні модулятори. Хоча відомі сполуки, такі як нікотин, які неселективно модулюють підтипи нікотинових рецепторів, у тому числі nAChRs 42 і 7, бажаними є сполуки, що селективно взаємодіють з 7-вмісними нейронними nAChRs, nAChRs 42, або обома nAChRs 7 і 42 через множину ролей даних рецепторів у болю, пізнанні, порушеннях і захворюваннях. КОРОТКИЙ ВИКЛАД СУТІ ВИНАХОДУ Даний винахід належить до біарилзаміщених азабіциклічних сполук, а також композицій, що включають такі сполуки, і способів їх застосування. Один з аспектів даного винаходу належить до сполуки формули (I) , 50 або її фармацевтично прийнятної солі, або її проліків, де n дорівнює 1, 2 або 3; + А являє собою -N- або -N -O -; z R являє собою водень, алкіл, циклоалкіл і арилалкіл; 2 UA 99936 C2 а 5 10 15 20 25 30 35 40 45 50 55 a L вибраний із групи, що складається з O, S і -N(R )-, де R вибраний із групи, що складається з водню, алкілу й алкілкарбонілу; 1 Ar являє собою 5-членну гетероарильну групу; 2 Ar являє собою арильну або гетероарильну групи. Інший аспект винаходу належить до фармацевтичної композиції, що включає сполуки за винаходом. Такі композиції можна застосовувати згідно зі способом винаходу, як правило, у вигляді частини терапевтичного режиму для лікування або попередження станів і порушень, пов'язаних з активністю nACh і, більш конкретно, з активністю nACh 7, активністю nACh 42, або як активністю nACh 7, так і активністю nACh 42. Ще один аспект винаходу належить до способу модулювання активності nACh як 7, так і 42. Спосіб можна використовувати для лікування, попередження або як для лікування, так і для попередження станів і порушень, пов'язаних з активністю обох підтипів nACh 7 і 42, особливо у ссавців. Наступний аспект винаходу належить до способу селективного модулювання активності nACh, наприклад, активності nACh 7. Спосіб можна використовувати для лікування, попередження або як для лікування, так і для попередження станів і порушень, пов'язаних з активністю nACh 7 у ссавців. Більш конкретно, даний спосіб можна використовувати при станах і розладах, пов'язаних із синдромом дефіциту уваги, синдромом дефіциту уваги з гіперактивністю (ADHD), хворобою Альцгеймера (ХА), шизофренією, помірними когнітивними порушеннями, віковими порушеннями пам'яті (AAMI), старечим слабоумством, слабоумством при СНІД, хворобою Піка, слабоумством, пов'язаним з тільцями Леві, слабоумством, пов'язаним із синдромом Дауна, шизофренією, аміотрофічним латеральним склерозом, хворобою Хантінгтона, зниженою функцією ЦНС внаслідок черепно-мозкової травми, гострим болем, післяопераційними болями, хронічним болем, запальним болем, невропатичним болем, безплідністю, недоліком кровообігу, необхідністю росту нових кровоносних судин, пов'язаною з загоєнням раней, особливо кровообігу навколо оклюзії судини, необхідністю росту нових кровоносних судин, пов'язаною з васкуляризацією шкірних трансплантатів, ішемією, запаленням, сепсисом, загоєнням ран і інших ускладнень, пов'язаних з діабетом, поряд з іншою системною і нейроімуномодуляторною активністю. Також даний винахід стосується способу селективного модулювання активності nACh, наприклад, активності nACh 42. Далі в даному описі більш докладно описані сполуки, композиції, що включають дані сполуки, способи застосування сполук і способи одержання сполук, а також проміжних сполук, одержуваних у таких способах. ДОКЛАДНИЙ ОПИС По-перше, визначені терміни. По-друге, сполуки за винаходом описані і показано, як вони отримані, включаючи множину прикладів їхнього синтезу. Нарешті, далі обговорюється й ілюструється застосування даних сполук. Визначення термінів Як використовується в даному описі і прикладеній формулі винаходу, наступні терміни мають наступні значення: Термін "алкеніл" означає лінійний або розгалужений вуглеводневий ланцюг, що містить від 2 до 10 вуглеців і містить щонайменше один подвійний вуглець-вуглецевий зв'язок, утворений за рахунок видалення двох воднів. Ілюстративні приклади алкенілів включають, але не обмежуючись вказаним, етеніл, 2-пропеніл, 2-метил-2-пропеніл, 3-бутеніл, 4-пентеніл, 5гексеніл, 2-гептеніл, 2-метил-1-гептеніл і 3-деценіл. Термін "алкенілен" означає двовалентну групу, отриману з лінійного або розгалуженого вуглеводневого ланцюга, що складається з 2-10 атомів вуглецю й містить щонайменше один подвійний зв'язок. Ілюстративні приклади алкенілену включають, але не обмежуючись вказаним, -CH=CH-, -CH=CH2CH2- і -CH=C(СН3)СН2-. Термін "алкенілокси" означає алкенільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади алкенілокси включають, але не обмежуючись вказаним, алілокси, 2-бутенілокси і 3-бутенілокси. Термін "алкокси" означає алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади алкенілокси включають, але не обмежуючись вказаним, метокси, етокси, пропокси, 2-пропокси, бутокси, трет-бутокси, пентилокси і гексилокси. Термін "алкоксіалкокси" означає алкоксильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через іншу алкоксильну групу, як визначено в даному описі. 3 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 Ілюстративні приклади алкоксіалкокси включають, але не обмежуючись вказаним, третбутоксиметокси, 2-етоксіетокси, 2-метоксіетокси і метоксиметокси. Термін "алкоксіалкоксіалкіл" означає алкоксіалкоксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкоксіалкоксіалкілу включають, але не обмежуючись вказаним, третбутоксиметоксиметил, етоксиметоксиметил, (2-метоксіетокси)метил і 2-(2-метоксіетоксі)етил. Термін "алкоксіалкіл" означає алкоксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкоксіалкілу включають, але не обмежуючись вказаним, третбутоксиметил, 2-етоксіетил, 2-метоксіетил і метоксиметил. Термін "алкоксикарбоніл" означає алкоксильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади алкоксикарбонілу включають, але не обмежуючись вказаним, метоксикарбоніл, етоксикарбоніл і трет-бутоксикарбоніл. Термін "алкоксикарбонілалкіл" означає алкоксикарбонільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкоксикарбонілалкілу включають, але не обмежуючись вказаним, 3-метоксикарбонілпропіл, 4-етоксикарбонілбутил і 2-трет-бутоксикарбонілетил. Термін "алкоксисульфоніл" означає алкоксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через сульфонільну групу, як визначено в даному описі. Ілюстративні приклади алкоксисульфонілу включають, але не обмежуючись вказаним, метоксисульфоніл, етоксисульфоніл і пропоксисульфоніл. Термін "алкіл" означає лінійний або розгалужений вуглеводневий ланцюг, що містить від 1 до 10 атомів вуглецю. Ілюстративні приклади алкілів включають, але не обмежуючись вказаним, метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил, ізобутил, трет-бутил, н-пентил, ізопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-ноніл, н-децил. Термін "алкілкарбоніл" означає алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади алкілкарбонілу включають, але не обмежуючись вказаним, ацетил, 1оксопропіл, 2,2-диметил-1-оксопропіл, 1-оксобутил, і 1-оксопентил. Термін "алкілкарбонілалкіл" означає алкілкарбонільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкілкарбонілалкілу включають, але не обмежуючись вказаним, 2оксопропіл, 3,3-диметил-2-оксопропіл, 3-оксобутил і 3-оксопентил. Термін "алкілкарбонілокси" означає алкілкарбонілгрупи, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади алкілкарбонілокси включають, але не обмежуючись вказаним, ацетилокси, етилкарбонілокси і трет-бутилкарбонілокси. Термін "алкілен" означає двовалентну групу, отриману з лінійного або розгалуженого вуглеводневого ланцюга, що містить від 1 до 10 атомів вуглецю. Ілюстративні приклади алкілену включають, але не обмежуючись вказаним, -СН2-, -СН(СН3)-, -C(СН3)2-, -CH2CH2-, CH2CH2CH2-, -CH2CH2CH2CH2- і -CH2CH(СН3)СН2-. Термін "алкілсульфініл" означає алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через сульфінільну групу, як визначено в даному описі. Ілюстративні приклади алкілсульфінілу включають, але не обмежуючись вказаним, метилсульфініл і етилсульфініл. Термін "алкілсульфінілалкіл" означає алкілсульфінільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкілсульфінілалкілу включають, але не обмежуючись вказаним, метилсульфінілметил і етилсульфінілметил. Термін "алкілсульфоніл" означає алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через сульфонільну групу, як визначено в даному описі. Ілюстративні приклади алкілсульфонілу включають, але не обмежуючись вказаним, метилсульфоніл і етилсульфоніл. Термін "алкілсульфонілалкіл" означає алкілсульфонільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкілсульфонілалкілу включають, але не обмежуючись вказаним, метилсульфонілметил і етилсульфонілметил. 4 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін "алкілтіо" означає алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади алкілтіо включають, але не обмежуючись вказаним, метилтіо, етилтіо, трет-бутилтіо і гексилтіо. Термін "алкілтіоалкіл" означає алкілтіогрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади алкілтіоалкілу включають, але не обмежуючись вказаним, метилтіометил і 2-(етилтіо)етил. Термін "алкініл" означає лінійну або розгалужену вуглеводневу групу, що містить від 2 до 10 атомів вуглецю і містить щонайменше один вуглець-вуглецевий потрійний зв'язок. Ілюстративні приклади алкінілу включають, але не обмежуючись вказаним, ацетиленіл, 1-пропініл, 2-пропініл, 3-бутиніл, 2-пентиніл і 1-бутиніл. Термін "алкінілен" означає двовалентну групу, отриману з лінійного або розгалуженого вуглеводневого ланцюга, що містить від 2 до 10 атомів вуглецю й містить не менше одного потрійного зв'язка. Ілюстративні приклади алкінілену включають, але не обмежуючись вказаним, -CC-, -CH2CC-, -СН(СН3)CH2CC-, -CCCH2- і -CС-ССН(СН3)СН2-. Термін "алкінілокси" означає алкінільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади алкінілокси включають, але не обмежуючись вказаним, 2-пропінілокси і 2-бутинілокси. Термін "арил, " означає феніл, біциклічний арил або трициклічний арил. Біциклічний арил являє собою нафтил, феніл, конденсований з циклоалкілом, або феніл, конденсований з циклоалкенілом. Ілюстративні приклади біциклічного арилу включають, але не обмежуючись вказаним, дигідроінденіл, інденіл, нафтил, дигідронафталеніл і тетрагідронафталеніл. Трициклічний арил являє собою антрацен або фенантрен, або біциклічний арил, конденсований з циклоалкілом, або біциклічний арил, конденсований з циклоалкенілом, або біциклічний арил, конденсований з фенілом. Ілюстративні приклади трициклічного арильного кільця включають, але не обмежуючись вказаним, азуленіл, дигідроантраценіл, флуореніл і тетрагідрофенантреніл. Арильні групи за даним винаходом можуть бути заміщеними 1, 2, 3, 4 або 5 замісниками, незалежно вибраними з алкенілу, алкокси, алкоксіалкокси, алкоксіалкоксіалкілу, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілсульфінілу, алкілсульфінілалкілу, алкілсульфонілу, алкілсульфонілалкілу, алкілтіо, алкілтіоалкілу, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, формілалкілу, галогену, галогеналкілу, гідрокси, гідроксіалкілу, меркапто, нітро, -NZ1Z2 і (NZ3Z4)карбонілу. Термін "арилалкокси" означає арильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкоксигрупу, як визначено в даному описі. Ілюстративні приклади арилалкокси включають, але не обмежуючись вказаним, 2-фенілетокси, 3-нафт-2илпропокси і 5-фенілпентилокси. Термін "арилалкоксикарбоніл" означає арилалкоксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади арилалкоксикарбонілу включають, але не обмежуючись вказаним, бензилоксикарбоніл і нафт-2-илметоксикарбоніл. Термін "арилалкіл" означає арильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади арилалкілу включають, але не обмежуючись вказаним, бензил, 2-фенілетил, 3фенілпропіл і 2-нафт-2-илетил. Термін "арилалкілтіо" означає арилалкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади арилалкілтіо включають, але не обмежуючись вказаним, 2-фенілетилтіо, 3-нафт-2-илпропілтіо і 5фенілпентилтіо. Термін "арилкарбоніл" означає арильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як визначено в даному описі. Ілюстративні приклади арилкарбонілу включають, але не обмежуючись вказаним, бензоїл і нафтоїл. Термін "арилокси" означає арильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади арилокси включають, але не обмежуючись вказаним, фенокси, нафтилокси, 3-бромфенокси, 4-хлорфенокси, 4метилфенокси і 3,5-диметоксифенокси. Термін "арилоксіалкіл" означає арилоксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. 5 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 Ілюстративні приклади арилоксіалкілу включають, але не обмежуючись вказаним, 2феноксіетил, 3-нафт-2-илоксипропіл і 3-бромфеноксиметил. Термін "арилтіо" означає арильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади арилтіо включають, але не обмежуючись вказаним, фенілтіо і 2-нафтилтіо. Термін "арилтіоалкіл" означає арилтіогрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади арилтіоалкілу включають, але не обмежуючись вказаним, фенілтіометил, 2-нафт-2-илтіоетил і 5-фенілтіометил. Термін "азидо" означає групу -N3. Термін "карбоніл" означає групу -C(=O)-. Термін "карбокси" означає групу -CO2H. Термін "карбоксіалкіл" означає карбоксильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади карбоксіалкілу включають, але не обмежуючись вказаним, карбоксиметил, 2-карбоксіетил і 3-карбоксипропіл. Термін "ціано" означає групу -CN. Термін "ціаноалкіл" означає ціаногрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади ціаноалкілу включають, але не обмежуючись вказаним, ціанометил, 2-ціаноетил і 3ціанопропіл. Термін "циклоалкеніл" означає циклічний вуглеводень, що містить від 3 до 8 вуглеців і містить щонайменше один вуглець-вуглецевий подвійний зв'язок, утворений шляхом видалення двох атомів водню. Ілюстративні приклади циклоалкенілу включають, але не обмежуючись вказаним, 2-циклогексен-1-іл, 3-циклогексен-1-іл, 2,4-циклогексадієн-1-іл і 3-циклопентен-1-іл. Термін "циклоалкіл" означає моноциклічну, біциклічну або трициклічну кільцеву систему. Моноциклічні кільцеві системи ілюструються насиченою циклічною вуглеводневою групою, що містить від 3 до 8 атомів вуглецю. Приклади моноциклічних кільцевих систем включає циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. Біциклічні кільцеві системи ілюструються місточковою моноциклічною кільцевою системою, в якій два суміжні або несуміжні атоми вуглецю моноциклічного кільця зв'язані алкіленовим містком між одним-трьома додатковими атомами вуглецю. Ілюстративні приклади біциклічних кільцевих систем включають, але не обмежуючись вказаним, біцикло[3.1.1]гептан, біцикло[2.2.1]гептан, біцикло[2.2.2]октан, біцикло[3.2.2]нонан, біцикло[3.3.1]нонан і біцикло[4.2.1]нонан. Циклоалкільна група за винаходом необов'язково є заміщеною 1, 2, 3, 4 або 5 замісниками, вибраними з групи, що складається з алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксисульфонілу, алкілу, алкілкарбонілу, алкілкарбонілокси, алкілсульфонілу, алкілтіо, алкілтіоалкілу, алкінілу, карбокси, ціано, формілу, галогеналкокси, галогеналкілу, галогену, гідрокси, гідроксіалкілу, меркапто, оксо, NZ1Z2 і (NZ3Z4)карбонілу. Термін "циклоалкілалкіл" означає циклоалкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади циклоалкілалкілу включають, але не обмежуючись вказаним, циклопропілметил, 2-циклобутилетил, циклопентилметил, циклогексилметил і 4циклогептилбутил. Термін "циклоалкілкарбоніл" означає циклоалкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади циклоалкілкарбонілу включають, але не обмежуючись вказаним, циклопропілкарбоніл, 2-циклобутилкарбоніл і циклогексилкарбоніл. Термін "циклоалкілокси" означає циклоалкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню, як це визначено в даному описі. Ілюстративні приклади циклоалкілокси включають, але не обмежуючись вказаним, циклопропілокси, циклобутилокси, циклопентилокси, циклогексилокси, циклогептилокси і циклооктилокси. Термін "циклоалкілтіо" означає циклоалкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки, як визначено в даному описі. Ілюстративні приклади циклоалкілтіо включають, але не обмежуючись вказаним, циклопропілтіо, циклобутилтіо, циклопентилтіо, циклогексилтіо, циклогептилтіо і циклооктилтіо. Термін "етилендіокси" означає -О(СН2)2О-групу, в якій атоми кисню етилендіоксигрупи приєднані до вихідного фрагмента молекули через один атом вуглецю, утворюючи 5-членне 6 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 кільце, або атоми кисню етилендіоксигрупи приєднані до вихідного фрагмента молекули через два суміжні атоми вуглецю, утворюючи 6-членне кільце. Термін "форміл" означає групу -C(=O)H. Термін "формілалкіл" означає формільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади формілалкілу включають, але не обмежуючись вказаним, формілметил і 2-формілетил. Термін "галоген" означає -Cl, -Br, -I або -F. Термін "галогеналкокси" означає щонайменше один галоген, як він визначений у даному описі, з'єднаний з вихідним фрагментом молекули через алкоксигрупу, як визначено в даному описі. Ілюстративні приклади галогеналкокси включають, але не обмежуючись вказаним, хлорметокси, 2-фторетокси, трифторметокси і пентафторетокси. Термін "галогеналкіл" означає щонайменше один галоген, як він визначений у даному описі, з'єднаний з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади галогеналкілу включають, але не обмежуючись вказаним, хлорметил, 2фторетил, трифторметил, пентафторетил і 2-хлор-3-фторпентил. Термін "гетероарил" означає моноциклічний гетероарил або біциклічний гетероарил. Моноциклічний гетероарил являє собою 5- або 6-членне кільце, що містить щонайменше один гетероатом, вибраний із групи, що складається з азоту, кисню і сірки. 5-членне кільце містить два подвійні зв'язки, і 6-членне кільце містить три подвійні зв'язки. 5- або 6-членний гетероарил зв'язаний з вихідним фрагментом молекули через будь-який атом вуглецю або будь-який здатний до заміщення атом азоту, що містяться в гетероарилі, за умови, що належна валентність зберігається. Ілюстративні приклади моноциклічних гетероарилів включають, але не обмежуючись вказаним, фурил, імідазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, оксазоліл, піридиніл, піридазиніл, піримідиніл, піразиніл, піразоліл, піроліл, тетразоліл, тіадіазоліл, тіазоліл, тієніл, триазоліл і триазиніл. Біциклічний гетероарил складається з моноциклічного гетероарилу, конденсованого з фенілом, або моноциклічного гетероарилу, конденсованого з циклоалкілом, або моноциклічного гетероарилу, конденсованого з циклоалкенілом, або моноциклічного гетероарилу, конденсованого з моноциклічним гетероарилом. Біциклічний гетероарил зв'язаний з вихідним фрагментом молекули через будь-який атом вуглецю або будь-який здатний до заміщення атом азоту, що містяться в біциклічному гетероарилі за умови, що зберігається належна валентність. Ілюстративні приклади біциклічного гетероарилу включають, але не обмежуючись вказаним, азаіндоліл, бензімідазоліл, бензофураніл, бензоксадіазоліл, бензоізоксазол, бензоізотіазол, бензооксазол, 1,3-бензотіазоліл, бензотіофеніл, цинолініл, фуропіридин, індоліл, індазоліл, ізобензофуран, ізоіндоліл, ізохінолініл, нафтиридиніл, оксазолопіридин, хінолініл, хіноксалініл і тієнопіридиніл. Гетероарильна група за винаходом необов'язково є заміщеною 1, 2, 3 або 4 замісниками, незалежно вибраними з групи, що складається з алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкоксисульфонілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкілтіоалкілу, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, галогеналкокси, галогеналкілу, галогену, гідрокси, гідроксіалкілу, меркапто, нітро, -NZ1Z2 і (NZ3Z4)карбонілу. Гетероарильні групи за винаходом, що заміщені гідроксильною групою, можуть бути присутніми у вигляді таутомерів. Гетероарильні групи за винаходом охоплюють всі таутомери, включаючи неароматичні таутомери. Термін "гетероарилалкокси" означає гетероарильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкоксильну групу, як визначено в даному описі. Ілюстративні приклади гетероарилалкокси включають, але не обмежуючись вказаним, фур-3-илметокси, 1Н-імідазол-2-ілметокси, 1H-імідазол-4-ілметокси, 1-(піридин-4-іл)етокси, піридин-3-ілметокси, 6-хлорпіридин-3-ілметокси, піридин-4-ілметокси, (6(трифторметил)піридин-3-іл)метокси, (6-(ціано)піридин-3-іл)метокси, (2-(ціано)піридин-4іл)метокси, (5-(ціано)піридин-2-іл)метокси, (2-(хлор)піридин-4-іл)метокси, піримідин-5-ілметокси, 2-(піримідин-2-іл)пропокси, тієн-2-ілметокси і тієн-3-ілметокси. Термін "гетероарилалкіл" означає гетероарил, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади гетероарилалкілу включають, але не обмежуючись вказаним, фур-3илметил, 1H-імідазол-2-ілметил, 1H-імідазол-4-ілметил, 1-(піридин-4-іл)етил, піридин-3-ілметил, 6-хлорпіридин-3-ілметил, піридин-4-ілметил, (6-(трифторметил)піридин-3-іл)метил, (6(ціано)піридин-3-іл)метил, (2-(ціано)піридин-4-іл)метил, (5-(ціано)піридин-2-іл)метил, (2 7 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 (хлор)піридин-4-іл)метил, піримідин-5-ілметил, 2-(піримідин-2-іл)пропіл, тієн-2-іметил і тієн-3ілметил. Термін "гетероарилалкілкарбоніл" означає гетероарилалкіл, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Термін "гетероарилалкілтіо" означає гетероарилалкільну групу, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади гетероарилалкілтіо включають, але не обмежуючись вказаним, фур-3-илметилтіо, 1H-імідазол2-ілметилтіо, 1H-імідазол-4-ілметилтіо, піридин-3-ілметилтіо, 6-хлорпіридин-3-ілметилтіо, піридин-4-ілметилтіо, (6-(трифторметил)піридин-3-іл)метилтіо, (6-(ціано)піридин-3-іл)метилтіо, (2-(ціано)піридин-4-іл)метилтіо, (5-(ціано)піридин-2-іл)метилтіо, (2-(хлор)піридин-4-іл)метилтіо, піримідин-5-ілметилтіо, 2-(піримідин-2-іл)пропілтіо, тієн-2-ілметилтіо і тієн-3-ілметилтіо. Термін "гетероарилкарбоніл" означає гетероарильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади гетероарилкарбонілу включають, але не обмежуючись вказаним, фур-3-илкарбоніл, 1H-імідазол-2-ілкарбоніл, 1H-імідазол-4-ілкарбоніл, піридин-3-ілкарбоніл, 6хлорпіридин-3-ілкарбоніл, піридин-4-ілкарбоніл, (6-(трифторметил)піридин-3-іл)карбоніл, (6(ціано)піридин-3-іл)карбоніл, (2-(ціано)піридин-4-іл)карбоніл, (5-(ціано)піридин-2-іл)карбоніл, (2(хлор)піридин-4-іл)карбоніл, піримідин-5-ілкарбоніл, піримідин-2-ілкарбоніл, тієн-2-ілкарбоніл і тієн-3-ілкарбоніл. Термін "гетероарилокси" означає гетероарильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади гетероарилокси включають, але не обмежуючись вказаним, фур-3-илокси, 1H-імідазол-2-ілокси, 1H-імідазол-4-ілокси, піридин-3-ілокси, 6-хлорпіридин-3-ілокси, піридин-4-ілокси, (6(трифторметил)піридин-3-іл)окси, (6-(ціано)піридин-3-іл)окси, (2-(ціано)піридин-4-іл)окси, (5(ціано)піридин-2-іл)окси, (2-(хлор)піридин-4-іл)окси, піримідин-5-ілокси, піримідин-2-ілокси, тієн2-ілокси і тієн-3-ілокси. Термін "гетероарилоксіалкіл" означає гетероарилоксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади гетероарилоксіалкілу включають, але не обмежуючись вказаним, піридин-3-ілоксиметил і 2-хінолін-3-ілоксіетил. Термін "гетероарилтіо" означає гетероарильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади гетероарилтіо включають, але не обмежуючись вказаним, піридин-3-ілтіо і хінолін-3-ілтіо. Термін "гетероарилтіоалкіл" означає гетероарилтіогрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади гетероарилтіоалкілу включають, але не обмежуючись вказаним, піридин3-ілтіометил і 2-хінолін-3-ілтіоетил. Термін "гетероцикл" або "гетероциклічний" належить до моноциклічного гетероциклу, біциклічного гетероциклу або трициклічного гетероциклу. Моноциклічний гетероцикл являє собою 3-, 4-, 5-, 6- або 7-членне кільце, що містить щонайменше один гетероатом, незалежно вибраний із групи, що складається з O, N, і S. 3- або 4-членне кільце містить 1 гетероатом, вибраний із групи, що складається з O, N і S. 5-членне кільце містить нуль або один подвійний зв'язок і один, два або три гетероатоми, вибрані із групи, що складається з O, N і S. 6- або 7членне кільце містить нуль, один або два подвійні зв'язки й один, два або три гетероатоми, вибрані із групи, що складається з O, N і S. Моноциклічний гетероцикл з'єднаний з вихідним фрагментом молекули через будь-який атом вуглецю або азоту, що містяться в моноциклічному гетероциклі. Ілюстративні приклади моноциклічного гетероциклу включають, але не обмежуючись вказаним, азетидиніл, азепаніл, азиридиніл, діазепаніл, 1,3-діоксаніл, 1,3діоксоланіл, 1,3-дитіоланіл, 1,3-дитіаніл, імідазолініл, імідазолідиніл, ізотіазолініл, ізотіазолідиніл, ізоксазолініл, ізоксазолідиніл, морфолініл, оксадіазолініл, оксадіазолідиніл, оксазолініл, оксазолідиніл, піперазиніл, піперидиніл, піраніл, піразолініл, піразолідиніл, піролініл, піролідиніл, тетрагідрофураніл, тетрагідротієніл, тіадіазолініл, тіадіазолідиніл, тіазолініл, тіазолідиніл, тіоморфолініл, 1,1-діоксидотіоморфолініл (сульфон тіоморфоліну), тіопіраніл і тритіаніл. Біциклічний гетероцикл являє собою 5- або 6-членний моноциклічний гетероцикл, конденсований з фенільною групою, або 5- або 6-членний моноциклічний гетероцикл, конденсований з циклоалкілом, або 5- або 6-членний моноциклічний гетероцикл, конденсований з циклоалкенілом, або 5- або 6-членний моноциклічний гетероцикл, конденсований з моноциклічним гетероциклом. Біциклічний гетероцикл з'єднаний з вихідним фрагментом молекули через будь-який атом вуглецю або азоту, що містяться в біциклічному гетероциклі. 8 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 Ілюстративні приклади біциклічного гетероциклу включають, але не обмежуючись вказаним, 1,3-бензодіоксоліл, 1,3-бензодитіоліл, 2,3-дигідро-1,4-бензодіоксиніл, бензодіоксоліл, 2,3дигідро-1-бензофураніл, 2,3-дигідро-1-бензотієніл, хроменіл і 1,2,3,4-тетрагідрохінолініл. Трициклічний гетероцикл являє собою біциклічний гетероцикл, конденсований з фенілом, або біциклічний гетероцикл, конденсований з циклоалкілом, або біциклічний гетероцикл, конденсований з циклоалкенілом, або біциклічний гетероцикл, конденсований з моноциклічним гетероциклом. Трициклічний гетероцикл з'єднаний з вихідним фрагментом молекули через будь-який атом вуглецю або азоту, що містяться в трициклічному гетероциклі. Ілюстративні приклади трициклічного гетероциклу включають, але не обмежуючись вказаним, 2,3,4,4а, 9,9агексагідро-1H-карбазоліл, 5а, 6,7,8,9,9а-гексагідродибензо[b, d]фураніл і 5а, 6,7,8,9,9агексагідродибензо[b, d]тієніл. Гетероцикли за даним винаходом необов'язково є заміщеними 1, 2, 3 або 4 замісниками, незалежно вибраними з групи, що складається з алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкоксисульфонілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкілтіоалкілу, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, галогеналкокси, галогеналкілу, галогену, гідрокси, гідроксіалкілу, меркапто, оксо, -NZ1Z2 і (NZ3Z4)карбонілу. Термін "гетероциклоалкокси" означає гетероциклічну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкоксигрупу, як визначено в даному описі. Ілюстративні приклади гетероциклоалкокси включають, але не обмежуючись вказаним, 2піридин-3-ілетокси, 3-хінолін-3-ілпропокси і 5-піридин-4-ілпентокси. Термін "гетероциклоалкіл" означає гетероцикл, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Термін "гетероциклоалкілкарбоніл" означає гетероциклоалкіл, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади гетероциклоалкілкарбонілу включають, але не обмежуючись вказаним, піперидин-4-ілметилкарбоніл, піперазин-1-ілметилкарбоніл, 3-метил-1-піролідин-1ілбутилкарбоніл, (1R)-3-метил-1-піролідин-1-ілбутилкарбоніл, (1S)-3-метил-1-піролідин-1ілбутилкарбоніл. Термін "гетероциклоалкілтіо" означає гетероциклоалкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади гетероциклоалкілтіо включають, але не обмежуючись вказаним, 2-піридин-3-ілетилтіо, 3-хінолін3-ілпропілтіо і 5-піридин-4-ілпентилтіо. Термін "гетероциклокарбоніл" означає гетероцикл, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Термін "гетероциклокарбонілалкіл" означає гетероциклокарбоніл, як визначено в даному описі, з'єднаний з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Термін "гетероциклоокси" означає гетероциклічну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню. Ілюстративні приклади гетероциклоокси включають, але не обмежуючись вказаним, піридин-3-ілокси і хінолін-3-ілокси. Термін "гетероциклооксіалкіл" означає гетероциклооксигрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади гетероциклооксіалкілу включають, але не обмежуючись вказаним, піридин-3-ілоксиметил і 2-хінолін-3-ілоксіетил. Термін "гетероциклотіо" означає гетероциклічну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади гетероциклотіо включають, але не обмежуючись вказаним, піридин-3-ілтіо і хінолін-3-ілтіо. Термін "гетероциклотіоалкіл" означає гетероциклотіогрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади гетероциклотіоалкілу включають, але не обмежуючись вказаним, піридин-3-ілтіометил і 2-хінолін-3-ілтіоетил. Термін "гідрокси" означає -OH-групу. Термін "гідроксіалкіл" означає щонайменше одну гідроксильну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади гідроксіалкілу включають, але не обмежуючись вказаним, гідроксиметил, 2-гідроксіетил, 3-гідроксипропіл, 2,3-дигідроксипентил і 2-етил-4-гідроксигептил. Термін "захисна група гідрокси" або "O-захисна група" означає замісник, що захищає гідроксильні групи від небажаних реакцій при проведенні синтезів. Приклади захисних груп гідрокси включають, але не обмежуючись вказаним, заміщені метилові прості ефіри, наприклад, 9 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 метоксиметиловий, бензилоксиметиловий, 2-метоксіетоксиметиловий, 2(триметилсиліл)етоксиметиловий, бензиловий і трифенілметиловий; тетрагідропіранілові прості ефіри; заміщені етилові прості ефіри, наприклад, 2,2,2-трихлоретиловий і трет-бутиловий; силілові прості ефіри, наприклад, триметилсиліловий, трет-бутилдиметилсиліловий і третбутилдифенілсиліловий; циклічні ацетали і кеталі, наприклад, метиленацеталь, ацетонід і бензиліденацеталь; циклічні складні орто-ефіри, наприклад, метоксиметиленовий; циклічні карбонати і циклічні боронати. Зазвичай використовувані захисні групи гідрокси представлені в T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 3rd edition, John Wiley & Sons, New York (1999). Термін "нижчий алкеніл" належить до підгрупи алкенілу, як він визначений у даному описі, і означає алкенільну групу, що містить від 2 до 4 атомів вуглецю. Прикладами нижчого алкенілу є етеніл, пропеніл і бутеніл. Термін "нижчий алкокси" належить до підгрупи алкокси, як він визначений у даному описі, і означає нижчу алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом кисню, як це визначено в даному описі. Ілюстративні приклади нижчого алкокси включають, але не обмежуючись вказаним, метокси, етокси, пропокси, 2-пропокси, бутокси і трет-бутокси. Термін "нижчий алкіл" належить до підгрупи алкілу, як визначено в даному описі й означає групу з лінійним чи розгалуженим вуглеводневим ланцюгом, що містить від 1 до 4 атомів вуглецю. Прикладами нижчого алкілу є метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, вторбутил і трет-бутил. Термін "нижчий алкілтіо" належить до підгрупи алкілтіо, означає нижчу алкільну групу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через атом сірки. Ілюстративні приклади нижчого алкілтіо включають, але не обмежуючись вказаним, метилтіо, етилтіо і трет-бутилтіо. Термін "нижчий алкініл" належить до підгрупи алкінілу, як він визначений у даному описі, і означає алкінільну групу, що містить від 2 до 4 атомів вуглецю. Прикладами нижчого алкінілу є етиніл, пропініл і бутиніл. Термін "нижчий галогеналкокси" належить до підгрупи галогеналкокси, як визначено в даному описі, і означає лінійну або розгалужену галогеналкоксигрупу, що містить від 1 до 4 атомів вуглецю. Ілюстративні приклади нижчого галогеналкокси включають, але не обмежуючись вказаним, трифторметокси, трихлорметокси, дихлорметокси, фторметокси і пентафторетокси. Термін "нижчий галогеналкіл" належить до підгрупи галогеналкілу, як визначено в даному описі, і означає лінійну або розгалужену галогеналкільну групу, що містить від 1 до 4 атомів вуглецю. Ілюстративні приклади нижчого галогеналкілу включають, але не обмежуючись вказаним, трифторметил, трихлорметил, дихлорметил, фторметил і пентафторетил. Термін "меркапто" означає -SH групу. Термін "меркаптоалкіл" означає меркаптогрупу, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через алкільну групу, як визначено в даному описі. Ілюстративні приклади меркаптоалкілу включають, але не обмежуючись вказаним, 2меркаптоетил і 3-меркаптопропіл. Термін "метилендіокси" означає групу -OCH2O-, в якій атоми кисню метилендіокси з'єднані з вихідним фрагментом молекули через два суміжні атоми вуглецю. Термін "захисна група азоту" означає групи, призначені для захисту аміногрупи від небажаних реакцій під час процесу синтезу. Переважні захисні групи азоту представляють ацетил, бензоил, бензил, бензилоксикарбоніл (Cbz), форміл, фенілсульфоніл, третбутоксикарбоніл (Вос), трет-бутилацетил, трифторацетил і трифенілметил (тритил). Зазвичай використовувані захисні групи азоту представлені в T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 3rd edition, John Wiley & Sons, New York (1999). Термін "нітро" означає групу -NO2. Термін "NZ1Z2" означає двох груп, Z1 і Z2, що з'єднані з вихідним фрагментом молекули через атомазоту. Кожну групу Z1 і Z2 незалежно вибирають із групи, що складається з водню, алкілу, алкілкарбонілу, алкоксикарбонілу, арилу, арилалкілу, формілу і (NZ5Z6)карбонілу. У деяких випадках у даному винаході, Z1 і Z2 разом з атомом азоту, з яким вони зв'язані, утворюють гетероциклічне кільце. Ілюстративні приклади NZ 1Z2 включають, але не обмежуючись вказаним, аміно, метиламіно, ацетиламіно, ацетилметиламіно, феніламіно, бензиламіно, азетидиніл, піролідиніл і піперидиніл. Термін "NZ3Z4" означає двох груп, Z3 і Z4, що з'єднані з вихідним фрагментом молекули через атом азоту. Кожну групу Z3 і Z4 незалежно вибирають із групи, що складається з водню, 10 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 алкілу, арилу та арилалкілу. Типові приклади NZ 3Z4 включають, але не обмежуючись вказаним, аміно, метиламіно, феніламіно і бензиламіно. Термін "NZ5Z6" означає двох груп, Z5 і Z6, що з'єднані з вихідним фрагментом молекули через атом азоту. Кожну групу Z5 і Z6 незалежно вибирають із групи, що складається з водню, алкілу, арилу й арилалкілу. Типові приклади NZ 5Z6 включають, але не обмежуючись вказаним, аміно, метиламіно, феніламіно і бензиламіно. Термін "(NZ3Z4)карбоніл" означає групу NZ3Z4, як визначено в даному описі, з'єднану з вихідним фрагментом молекули через карбонільну групу, як це визначено в даному описі. Ілюстративні приклади (NZ3Z4)карбонілу включають, але не обмежуючись вказаним, амінокарбоніл, (метиламіно)карбоніл, (диметиламіно)карбоніл і (етилметиламіно)карбоніл. Термін "оксо" означає фрагмент =O. Термін "сульфініл" означає групу -S(=O)-. Термін "сульфоніл" означає групу -SO2-. Термін "таутомер" означає протонний зсув від одного атома сполуки до іншого атому тієї ж сполуки, де дві або більше структурно різні сполуки знаходяться в рівновазі одна з одною. Хоча зазвичай може бути визнано, що зірочка використовується для того, щоб вказати, що точний склад субодиниці рецептора є невизначеним, наприклад, 34* означає рецептор, що містить білки 3 і 4 у поєднанні з іншими субодиницями, передбачається, що термін "7", як він використовується в даному описі, включає рецептори, точний склад субодиниць яких є як визначеним, так і невизначеним. Наприклад, як використано в даному описі, 7 включає гомомерні рецептори (7)5 і рецептори 7*, які позначають nACh, що містить щонайменше одну субодиницю 7. Сполуки за винаходом можна використовувати у вигляді фармацевтично прийнятних солей, складних ефірів або амідів, отриманих з неорганічних і органічних кислот. "Фармацевтично прийнятні солі, складні ефіри й аміди", включають солі, цвітеріони, складні ефіри й аміди сполук формули (I), що, у межах відомого медичного судження, є придатними для використання в контакті з тканинами людини і нижчих тварин, які без надмірної токсичності, подразнення, алергійної реакції, і т.п., відповідають розумному співвідношенню користь/ризик і є ефективними для їх передбачуваного застосування. Вираження "фармацевтично прийнятна сіль" належить до тих солей, що, у межах відомого медичного судження, є придатними для використання в контакті з тканинами людини і нижчих тварин, що без надмірної токсичності, подразнення, алергійної реакції, і т.п., відповідають розумному співвідношенню користь/ризик. Солі можуть бути отримані in situ під час остаточного виділення й очищення сполук за винаходом або окремо, шляхом взаємодії вільної основної функціональної групи з придатною органічною кислотою. Ілюстративні кислотно-адитивні солі включають, але не обмежуючись вказаним, ацетат, адипат, альгінат, цитрат, аспартат, бензоат, бензолсульфонат, бісульфат, бутират, камфорат, камфорсульфонат, диглюконат, фумарат, гліцерофосфат, гемісульфат, гептаноат, гексаноат, фумарат, гідрохлорид, гідробромід, гідройодид, 2-гідроксіетансульфонат (ізетіонат), лактат, малеат, метансульфонат, нікотинат, 2-нафталінсульфонат, оксалат, памоат, пектинат, персульфат, 3-фенілпропіонат, пікрат, пивалат, пропіонат, сукцинат, тартрат, тіоціанат, фосфат, глутамат, бікарбонат, п-толуолсульфонат і ундеканоат. Основні азотвмісні групи можуть бути кватернізовані з використанням таких агентів, як нижчі алкілгалогеніди, такі, як метил-, етил-, пропіл- і бутил-хлориди, броміди і йодиди; діалкілсульфати, такі як диметил-, діетил-, дибутил- і діаміл-сульфати, довголанцюжкові галогеніди, такі як децил-, лаурил-, міристил- і стеарил-хлориди, броміди і йодиди; арилалкілгалогеніди, такі як бензил- і фенетил-броміди та інші. У такий спосіб одержують продукти, розчинні або дисперговані в воді або олії. Приклади кислот, які можна використовувати для утворення фармацевтично прийнятних кислотно-адитивних солей, включають такі неорганічні кислоти, як хлористоводнева кислота, бромистоводнева кислота, сірчана кислота і фосфорна кислота і такі органічні кислоти, як щавлева кислота, малеїнова кислота, бурштинова кислота і лимонна кислота. Основно-адитивні солі можуть бути отримані in situ під час остаточного виділення й очищення сполук за винаходом або окремо, шляхом взаємодії наявного фрагмента карбонової кислоти з пидатною основою, такою як гідроксид, карбонат або бікарбонат фармацевтично прийнятного катіона металу або аміак, або органічний первинний, вторинний або третинний амін. Фармацевтично прийнятні солі включають, але не обмежуючись вказаним, солі на основі катіонів лужних металів або лужноземельних металів, такі як солі літію, натрію, калію, кальцію, магнію й алюмінію, і тому подібні, і на основі нетоксичних катіонів четвертинного амонію й амінів, включаючи амоній, тетраметиламоній, тетраетиламоній, метиламін, диметиламін, 11 UA 99936 C2 5 10 15 20 25 30 35 40 45 триметиламін, триетиламін, діетиламін, етиламін і тому подібні. Інші ілюстративні органічні аміни, використовувані для утворення основно-адитивних солей включають етилендіамін, етаноламін, діетаноламін, піперидин і піперазин. Термін "фармацевтично прийнятний складний ефір" належить до складних ефірів сполук за винаходом, що гідролізуються in vivo і включають ті, які легко розщеплюються в організмі людини, залишаючи вихідну сполуку або її сіль. Приклади фармацевтично прийнятних, нетоксичних складних ефірів за винаходом включають С1-С6 алкілові складні ефіри і С5-C7 циклоалкілові складні ефіри, хоча C1-C4 алкілові складні ефіри є переважними. Складні ефіри сполук формули (I) можуть бути отримані відповідно до загальноприйнятих способів. Фармацевтично прийнятні складні ефіри можуть бути приєднані до гідроксильних груп за допомогою взаємодії сполуки, що містить гідроксильну групу з кислотою й алкілкарбоновою кислотою, такою як оцтова кислота, або з кислотою й арилкарбоновою кислотою, такою як бензойна кислота. У випадку сполук, що містять карбоксильні кислотні групи, фармацевтично прийнятні складні ефіри одержують зі сполук, що містять карбоксильні кислотні групи, при взаємодії сполуки з основою, такою як триетиламін, і алкілгалогенідом, алкілтрифлатом, наприклад, йодистим метилом, бензилйодидом, циклопентилйодидом. Вони також можуть бути отримані шляхом взаємодії сполуки з кислотою, наприклад, соляною кислотою, і алкілкарбоновою кислотою, такою як оцтова кислота, або з кислотою й арилкарбоновою кислотою, такою як бензойна кислота. Термін "фармацевтично прийнятний амід", як він використовується в даному описі, належить до нетоксичних амідів за винаходом, отриманих з аміаку, первинних C 1-C6 алкіламінів і вторинних C1-C6 діалкіламінів. У випадку вторинних амінів, амін також може бути у вигляді 5або 6-членного гетероциклу, що містить один атом азоту. Аміди, отримані з аміаку, C 1-C3-алкіл первинні аміди і С1-С2-діалкіл вторинні аміди є переважними. Аміди сполук формули (I) можуть бути отримані відповідно до загальноприйнятих способів. Фармацевтично прийнятні аміди можуть бути отримані зі сполук, що містять первинні або вторинні аміногрупи, шляхом взаємодії сполуки, що містить аміногрупу з алкілангідридом, арилангідридом, ацилгалогенідом або ароїлгалогенідом. У випадку сполук, що містять карбоксильні кислотні групи, фармацевтично прийнятні складні ефіри одержують зі сполук, що містять карбоксильні кислотні групи, шляхом взаємодії сполуки з основою, такою як триетиламін, дегідратуючим агентом, таким як дициклогексилкарбодіімід або карбонілдіімідазол, і алкіламіном, діалкіламіном наприклад, з метиламіном, діетиламіном, піперидином. Вони також можуть бути отримані при взаємодії сполуки з кислотою, такою як сірчана кислота, і алкілкарбонової кислоти, такої як оцтова кислота, або з кислотою й арилкарбоновою кислотою, такою як бензойна кислота, в умовах дегідратації з додаванням молекулярних сит. Композиція може містити сполуку за винаходом у вигляді фармацевтично прийнятних проліків. Термін "фармацевтично прийнятні проліки" або "проліки", як він використовується в даному описі, належить до тих проліків сполук за винаходом, що, у межах відомого медичного судження, є придатними для використання в контакті з тканинами людини і нижчих тварин, які без надмірної токсичності, подразнення, алергійної реакції, і т.п., відповідають розумному співвідношенню користь/ризик і є ефективними для їх передбачуваного застосування. Проліки за винаходом легко можуть бути перетворені in vivo на вихідну сполуку формули (I), наприклад, шляхом гідролізу в крові. Докладне обговорення наводиться в T. Higuchi and V. Stella, Pro-drugs as Novel Delivery Systems, т. 14, серія A.C.S. Symposium Series, і в Edward B. Roche (ред.), Bioreversible Carriers in Drug Design, American Pharmaceutical Association and Pergamon Press (1987). Винахід передбачає фармакологічно активні речовини або хімічно синтезовані або утворені в природних умовах біотрансформації сполук формули (I). Сполуки за винаходом Сполуки за винаходом мають формулу (I): 50 55 Зокрема, сполуки формули (I) можуть включати, але не обмежуючись вказаним, сполуки, в z яких R являє собою H або алкіл, А являє собою N, і n дорівнює 1 або 2. Є деякі переважні z сполуки, в яких R являє собою Н або метил, А являє собою N; L являє собою О, і n дорівнює 2. 12 UA 99936 C2 1 Зокрема, у сполуках формули (I), Ar вибирають з: 5 10 1 2 3 4 де R , R , R і R незалежно вибирають з водню, ацилу, ацилокси, алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксііміно, алкоксисульфонілу, алкілу, алкілсульфонілу, алкінілу, аміно, карбокси, ціано, формілу, галогеналкокси, галогеналкілу, галогену, гідрокси, гідроксіалкілу, меркапто, нітро, тіоалкокси, -NRgRj, (NRgRj)алкілу, (NRgRj)алкокси, (NRgRj)карбонілу і (NRgRj)сульфонілу; 5 R незалежно вибирають з водню, ацилу, алкілу й алкілсульфонілу; і кожен Rg і Rj незалежно являє собою водень або алкіл, або алкілкарбоніл. 1 Зокрема, Ar являє собою 15 Більш конкретно, винахід включає, але не обмежуючись вказаним, сполуки формули (I), де А 1 являє собою N; R являє собою Н або метил; L являє собою O; n дорівнює 2, і Ar являє собою 20 2 Сполуки формули (I) містять Ar , що являє собою 13 UA 99936 C2 , 1 5 10 15 2 3 4 5 де X вибирають із групи, що складається з O, S, і -N(Rа)-; кожний з Z , Z , Z , Z і Z незалежно являє собою азот або вуглець, де атом вуглецю необов'язково заміщений замісником вибраним із групи, що складається з водню, галогену, алкілу, -ORс, -алкіл-ORc, NRdRe і -алкіл-NRdRe. 6 7 Кожний з R і R незалежно вибирають із групи, що складається з водню, алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксііміно, алкоксисульфонілу, алкілу, алкілкарбонілу, алкілкарбонілокси, алкілсульфонілу, алкінілу, карбокси, ціано, формілу, галогеналкокси, галогеналкілу, галогену, водню, гідрокси, гідроксіалкілу, меркапто, нітро, тіоалкокси, -NRfRg, (NRfRg)алкілу, (NRfRg)алкокси, (NRfRg)карбонілу і (NRfRg)сульфонілу, за 6 7 умови, що коли R або R являє собою гідрокси, припустимі відповідні таутомери. Кожний з R a, Rb, Rc, Rd, Re, Rf і Rg незалежно вибирають із групи, що складається з водню й алкілу, z алкілкарбонілу. R вибирають з водню, алкілу, циклоалкілалкілу й арилалкілу. Розкрито z z переважні сполуки, де R являє собою водень або алкіл. Переважно R являє собою H або метил. 2 Розкрито переважні сполуки, де Ar являє собою 20 1 2 3 4 6 7 2 де Z , Z , Z , Z , Rb, R і R є такими, як визначено раніше. Більш переважно Ar являє собою молекулу формули (iii) Найбільш переважно, даний винахід належить до сполук формули (I), де А являє собою N; z 1 R являє собою метил; L являє собою O; n дорівнює 2, і Ar являє собою 25 і 2 Ar являє собою 30 Сполуки для способу за винаходом, включаючи, але не обмежуючи тими, які вказані в прикладах або конкретно названі іншим чином, можуть модулювати, і часто мають афінність відносно nAChRs і, зокрема, nAChRs 7. У якості лігандів nAChRs 7, сполуки за винаходом 14 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 можуть використовуватися для лікування або попередження nACh-7 опосередкованих захворювань або станів. Конкретні приклади сполук, які можна використовувати для лікування або попередження опосередкованих nACh 7 захворювань або станів, включають, але не обмежуючись вказаними: 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазол; 2-[(ендо))-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол; 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси)-5-(піридин-3-іл]тіазол; 5-(1Н-індол-6-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол; 5-(1Н-індол-4-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол; 5-(бензофуран-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол; 5-(бензо[b]тіофен-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол; 5-(2-(трифторметил)-1Н-індол-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3ілокси]тіазол; 5-(дибензо[b, d]тіофен-2-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол; 2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазол; 2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-6-іл)тіазол; 2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол; 2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл)тіазол; 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-феніл-1,3,4-тіадіазол; 2-(1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(бензофуран-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(бензо[b]тіофен-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4 тіадіазол; 2-(3-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-м-толіл-1,3,4-тіадіазол; 2-(4-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(3-хлорфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(1Н-індол-6-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(1H-індол-4-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(3-ціанофеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(3-трифторметилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазол; 2-(4-хлорфеніл)-5-((1R, 3R, 5S)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(2-(трифторметил)-1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]1,3,4-тіадіазол; 2-(3-хлор-4-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(4-(трифторметил)феніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазол; 2-(4-метоксифеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(3-амінофеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(4-етилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол; 2-(4-ацетилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол і N-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-іл]-5-феніл-1,3,4-тіадіазол-2-амін; або їх фармацевтично прийнятні солі, складні ефіри, аміди, і проліки. Сполукам привласнені назви з використанням програмного забезпечення AutoNom, що розроблене компанією MLD Information Systems Gmb (раніше відомої як інформаційна система Бейльштейн, Beilstein Informationssysteme) Франкфурт, Німеччина, і є частиною програмного пакета CHEMDRAW® Ultra версія 6.0.2 (Cambridge Soft. Кембридж, MA). Сполуки за винаходом можуть існувати у виді стереоізомерів, в яких присутні асиметричний або хіральний центри. Дані стереоізомери є "R" або "S", залежно від конфігурації замісників навколо хірального елемента. Терміни "R" і "S", використані в даному описі, належать до конфігурацій, як вони визначені в ІЮПАК 1974, Рекомендації з розділу E, Фундаментальна стереохімія, Pure Appl. Chem., 1976, 45: 13-30. Приєднання L до азабіциклічного алкану можна розглядати як охоплює як ендо-, так і і екзогеометрії. Винахід передбачає різні стереоізомери і їх суміші, і вони спеціально включені в обсяг даного винаходу. Стереоізомери включають енантіомери і діастереомери, і суміші енантіомерів або діастереомерів. Індивідуальні стереоізомери сполук за винаходом можуть бути отримані синтетично з комерційно доступних вихідних матеріалів, що містять асиметричний або хіральний центри або шляхом одержання рацемічних сумішей з наступним оптичним розділенням, добре відомим звичайним фахівцям у даній галузі. Дані способи оптичного розділення ілюструються на прикладі (1) з'єднання суміші енантіомерів з хіральним допоміжним агентом, розділення отриманої суміші діастереомерів або 15 UA 99936 C2 5 10 15 перекристалізацією хроматографічно і необов'язкового вивільнення оптично чистого продукту від допоміжної добавки, як описано в довіднику Furniss, Hannaford, Smith, and Tatchell, "Vogel's Textbook of Practical Organic Chemistry", 5-і видання (1989), Longman Scientific & Technical, Essex CM20 2JE, Англія, або (2) прямого розділення суміші оптичних енантіомерів на хіральних хроматографічних колонках або (3) методами дробової перекристалізації. Способи одержання сполук за винаходом Реакції, проілюстровані на схемах, проводять у розчиннику, що придатний для використовуваних реагентів і матеріалів, і придатному для перетворень, що проводяться. Описані перетворення можуть потребувати зміни порядку синтетичних стадій або вибору однієї конкретної схеми способу перед іншою, для того, щоб одержати бажану сполука за винаходом, залежно від функціональної групи, що присутня у молекулі. Описані нижче способи, можуть викликати застосування різних енантіомерів. Там де стереохімія показана на схемі, вона призначена тільки для ілюстрації. Схема 1 2 20 25 30 35 Сполуки формули (8), де Ar є такими, як визначено для формули (I), можуть бути отримані як описано на схемі 1. Сполуки формули (1) при обробці сполукою формули (2), де X являє собою кисень, сірку або азот; Y являє собою бромід, хлорид або йодид, в присутності Cu, 1,10фенантроліну і Cs2CO3 у розчиннику, такому як, але не обмежуючись вказаним, толуол, при 110ºC, як описано в Org. Lett., 2002, 4, 973, призводять до сполук формули (3). Сполуки формули (3) при обробці гексаметилдіоловою або органо-борановою сполукою формули (4), m такою як біс(пінаколато)дибор або біс(катехолато)дибор, де R являє собою водень, алкіл або арил, у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc)2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, призводять до відповідних похідних олова або боронової кислоти/складних ефірів формули (5), де М являє собою -Sn-(Me)3 або m 2 B(OR )2. Сполуки формули (5) при обробці сполуками формули (6), де Ar являє собою арильне чи гетероарильне кільце і галоген являє собою бромід, хлорид або йодид, у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc) 2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, буде призводити до сполук формули (8). Альтернативно, сполуки формули (6) при обробці гексаметилдіоловом або сполукою формули (4), що містить диборан, такою як біс(пінаколато)дибор і біс(катехолато)дибор, у присутності паладієвого каталізатора, будуть призводити до сполук, що містять оловоорганічне похідне або 2 борорганічну кислоту/складний ефір формули (7), де Аr являє собою біциклічний гетероарил і m де М являє собою -Sn-(Me)3 або -B(OR )2. Сполуки формули (7) при обробці сполукою формули (3) у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc) 2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, призводять до сполуки формули (8). 40 16 UA 99936 C2 Схема 2 1 5 10 15 20 25 30 35 Сполуки формули (13), де Ar являє собою азотовмісний гетероарил, наприклад, імідазоли, 2 оксазоли, тіазоли, оксадіазоли, тіадіазоли і триазоли, і Ar є таким, як визначено для формули z (I), можуть бути отримані, як показано на схемі 2. Сполуки формули (9), де R є таким, як визначено раніше, і К являє собою калій, отримані при обробці гідроксил-вмісних гетероциклів аналогічної формули трет-бутоксидом калію в розчинниках, таких як, але не обмежуючись вказаним, TГФ, ДМЕ або ДМФ для одержання калій-оксид вмісних сполук формули (9). Сполуки 1 2 формули (9) при обробці сполуками формули (10), де Y являє собою бром, хлор і йод, Y являє 2 1 2 3 собою бром, хлор, йод, або Ar , і J , J і J незалежно являють собою будь-який з вуглецю або азоту, сірки і кисню, такі як, але не обмежуючись вказаним, 2,5-дибромтіазол і 2,5-дибром-1,3,42 2 тіадіазол, призводять до сполук формули (11). Коли Y являє собою Ar , сполуки формули (11) 2 являють собою переважні варіанти здійснення. Коли Y являє собою галоген, сполуки формули (11) при обробці гексаметилдіоловом або диборвмісною сполукою формули (4) у присутності паладієвого каталізатора згідно зі способом, представленим на схемі 1, призводять до сполук формули (12). Сполуки формули (12), при обробці сполуками формули (6) у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc)2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, призводять до сполук формули (13). Альтернативно, сполуки формули (11) при обробці органостанановими сполуками або сполуками формули (7), що містять органоборну кислоту, як описано на схемі 1, у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc)2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, призводять до сполук формули (13). Схема 3 Альтернативно, сполуки формули (8) можуть бути отримані, як вказано на схемі 3. Сполуки 1 формули (1) при обробці сполукою формули (14), де X являє собою кисень, сірку або азот; Z , 3 4 2 Z і Z являють собою азот або вуглець, Y являє собою бром, хлор, йод або Ar , у присутності, але не обмежуючись вказаним, діетилазодикарбоксилату або діізопропілазодикарбоксилату і фосфіну, такого, як трифенілфосфин, утворюють сполуки формули (15). Коли Y являє собою 2 Ar , сполуки формули (15) являють собою переважні варіанти здійснення. Коли Y являє собою галоген, подальша обробка сполуки відповідно до умов, викладених для схем 1-2, призводить до сполук формули (8), що являють собою переважні варіанти здійснення. 17 UA 99936 C2 Схема 4 5 10 15 20 Інший спосіб одержання сполук формули (8) описаний на схемі 4. Сполуки формули (7), що містять олово або боронову кислоту/складний ефір можуть бути сконденсовані з різними гетероарилгалогенідами, що забезпечує спосіб одержання біарильних сполук формули (17) і сполук формули (20). Наприклад, сполуки формули (7) при обробці сполуками формули (16) у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc) 2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, призводять до сполук формули (17). Сполуки формули (17) при обробці сполуками формули (1) у присутності йодиду міді (I) і карбонату цезію і 1,10-фенантроліну, як описано на схемі 1, призводять до сполук формули (8). Альтернативно, а сполуки формули (7) при обробці сполукою формули (18), де R являє собою бензил або іншу придатну захисну групу спирту, як відомо фахівцю в даній галузі, у присутності паладієвого каталізатора призводять до сполук формули (19). Видалення захисної групи спирту, наприклад, а коли R являє собою бензил, зазвичай досягається за допомогою палладію-на-вугіллі в атмосфері водню, призводячи до сполук формули (20). Сполуки формули (20) при обробці сполуками формули (1) у присутності трифенілфосфіну і діетилдіазокарбоксилату або аналогічного реагенту призводять до одержання сполук формули (8). Схема 5 18 UA 99936 C2 5 10 15 20 Сполуки формули (25), що є ілюстративними сполуками формули (I), де L являє собою -NH-, можуть бути отримані, як показано на схемі 5. Сполуки формули (21) при обробці сполуками 2 2 формули (22), де Y являє собою бромід, хлорид, йодид або Ar ; разом із триацетоксиборгідридом натрію і Na2SO4 в оцтовій кислоті призводять до сполук формули (23). Альтернативно, сполуки формули (23) можуть бути отримані шляхом обробки сполук формули 1 2 (24) сполукою формули (2), де Y являє собою хлор, бром або йод, і Y являє собою бромід, 2 хлорид, йодид або Ar ; у присутності паладієвого каталізатора, такого як, але не обмежуючись вказаним, Pd(OAc)2, PdCl2(PPh3)2, Pd(PPh3)4, PdCl2(dppf), Pd2(dba)3, переважно в толуолі. Коли 2 2 Y являє собою Ar , сполуки формули (23) є ілюстративними сполуками даного винаходу. Коли 2 Y являє собою галоген, подальша обробка сполуки формули (23) олов'яною або диборною сполукою формули (4), такою як біс(пінаколато)дибор і біс(катехолато)дибор, в умовах, описаних для схеми 2, призводять до відповідних сполук формули (26), що представляють собою похідні олова або боронову кислоту/складний ефір. Сполуки формули (26) при обробці сполукою формули (6) у присутності паладієвого каталізатора, призводять до сполук формули (25). Альтернативно, сполуки формули (23) при обробці сполукою формули (7), що містить олово або боронову кислоту/складний ефір, у присутності паладієвого каталізатора також призводять до сполук формули (25). Схема 6 1 25 30 35 40 45 2 Сполуки формули (30), де L являє собою S, і Ar і Ar є такими, як визначено відповідно до формули (I), можуть бути отримані, як показано на схемі 6. Сполуки формули (27), де Y являє 2 собою бромід, хлорид, йодид або Ar , будучи попередньо обробленими гідридом натрію в розчиннику, такому як, але не обмежуючись вказаним, ДМФ, з наступною обробкою сполукою 2 формули (1) призводять до сполук формули (28). Коли Y являє собою Ar , сполуки формули (28) є репрезентативними для даного винаходу. Коли Y являє собою галоген, додаткова обробка сполук формули (28) сполукою формули (7), як описано на схемі 1, призводить до сполук формули (30), що є ілюстративними сполуками формули (I), де L являє собою S. Крім того, сполуки формули (28) при обробці гексаметилдіоловом або диборним реагентом формули (4), таким як біс(пінаколато)дибор і біс(катехолато)дибор, у присутності паладієвого каталізатора призводять до сполуки формули (29). Сполуки формули (29) при обробці сполуками формули (6), де галоген являє собою бром, хлор або йод, у присутності паладієвого каталізатора призводять до сполук формули (30). Крім того, сполуки формули (I), де А являє собою N, можуть бути перетворені на сполуки + формули (I), де А являє собою N -O при обробці окисником. Приклади окисника, включають, але не обмежуючись вказаним, водний перекис водню і м-хлорпербензойну кислоту. Реакцію, як правило, здійснюють у розчиннику, такому як, але не обмежуючись вказаним, ацетонітрил, вода, дихлорметан, ацетон або їх суміш, переважно в суміші ацетонітрилу і води, при температурі від приблизно 0ºC до приблизно 80ºC, протягом приблизно від 1 години до приблизно 4 днів. Сполуки і проміжні сполуки за винаходом можуть бути виділені й очищені способами, добре відомими фахівцям у даній галузі органічного синтезу. Приклади традиційних методів виділення й очищення сполук можуть включати, але не обмежуючись вказаним, хроматографію на твердих носіях, таких як силікагель, оксид алюмінію або похідні діоксиду кремнію з щепленими алкілсилановими групами; перекристалізацію при високій або низькій температурі з необов'язковою попередньою обробкою активованим вугіллям; тонкошарову хроматографію, перегонку при різних тисках, сублімацію у вакуумі і розтирання, як це описано, наприклад, у 19 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 "Vоgеl's Textbook of Practical Organic Chemistry", п'яте видання (1989), автори Furniss, Hannaford, Smith, і Tatchell, видавництво Longman Scientific & Technical, Essex CM20 2JE, Англія. Сполуки за винаходом містять щонайменше один основний азот, відповідно до чого сполуки можна обробити кислотою з утворенням бажаної солі. Наприклад, сполука може бути піддана взаємодії з кислотою, при кімнатній температурі або вище для одержання бажаної солі, що випадає в осад, і яку збирають за допомогою фільтрування після охолодження. Приклади кислот, що підходять для реакції, включають, але не обмежуючись вказаним, винну, молочну, бурштинову, а також мигдальну, атромолочну, метансульфонову, етансульфонову, толуолсульфонову, нафталінсульфонову, вугільну, фумарову, глюконову, оцтову, пропіонову, саліцилову, хлористоводневу, бромистоводневу, фосфорну, сірчану, лимонну або оксимасляну кислоту, камфорсульфонову, яблучну, фенілоцтову, аспарагінову, глутамінову, і тому подібні. Для захисту аміногруп, що є присутніми в описаних сполуках, можна використовувати захисні групи азоту. Такі методи і деякі придатні захисні групи азоту описані в Greene and Wuts, (Protective Groups in Organic Synthesis, John Wiley and Sons (1999)). Наприклад, придатні захисні групи азоту включають, але не обмежуючись вказаним, трет-бутоксикарбоніл (Boc), бензилоксикарбоніл (Cbz), бензил (Вn), ацетил і трифторацетил. Зокрема, Boc-захисна група може бути вилучена шляхом обробки кислотою, такою як трифтороцтова кислота або хлористоводнева кислота. Захисні групи Cbz і Вn можуть бути вилучені за допомогою каталітичного гідрування. Ацетильна і трифторацетильна захисні групи можуть бути вилучені за допомогою гідроксид-іонів. Сполуки і способи за винаходом можуть бути краще зрозумілі шляхом посилання на наступні приклади, що призначені як ілюстрація, але не обмеження, обсягу винаходу. Приклад 1 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазол біс(хлористоводнева кислота) Приклад 1А 5-бром-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол Тропін (Aldrich, 420 мг, 3,0 ммоль) у ТГФ (безводний, Aldrich, 20 мл) обробляли третбутоксидом калію (Aldrich, 350 мг, 3,50 ммоль) при температурі навколишнього середовища протягом 1,0 години. До вищевказаного розчину при 10-20ºЗ додавали розчин 2,5дибромтіазолу (Aldrich, 969 мг, 4,0 ммоль) у ТГФ (безводний, Aldrich, 10 мл). Потім суміш перемішували при температурі навколишнього середовища протягом 3 годин. Суміш гасили водою (1 мл) і концентрували при зниженому тиску. Залишок розбавляли CHCl3 (100 мл) і промивали насиченим розчином солі (2×10 мл). Органічний розчин концентрували при зниженому тиску і залишок очищували методом хроматографії (Si 2, CH2Cl2/MeOH/NH3• H2O, об. 1 90/10/2, Rf = 0,15), одержуючи вказану в заголовку сполуку. H ЯМР (300 MГц, CD3OD) δ м.ч. 2,00-2,12 (м, 8H), 2,36 (с, 3H), 3,17-3,29 (м, 2H), 5,10 (т, J = 5,09 Гц, 1H), 7,12 (с, 1H); МС + + (DCI/NH3) m/z = 303 (M+1) . 305 (M+1) . Приклад 1B 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазол Розчин продукту прикладу 1А (200 мг, 0,66 ммоль), 5-індолілборонової кислоти (Frontier, 160 мг, 1,0 ммоль) і водного розчину К2СО3 (2M, 1 мл) у присутності Pd(PPh3)4 (15,3 мг, 0,013 ммоль) у діоксані (4 мл) нагрівали при 80-90ºC протягом 10 годин. Суміш охолоджували до температури навколишнього середовища й очищували методом хроматографії (Si 2, 1 CH2Cl2/MeOH/NH3• Н2О, об. 90/10/2, Rf = 0,10), одержуючи вказану в заголовку сполуку. H ЯМР (300 MГц, CDCl3) δ м.ч. 1,99-2,16 (м, 6H), 2,18-2,30 (м, 2H), 2,33 (с, 3H), 3,12-3,18 (м, 2H), 5,16 (т, J = 4,92 Гц, 1H), 6,58 (т, J = 2,60 Гц, 1H), 7,23 (т, J = 3,00 Гц, 1H), 7,31 (дд, J = 8,40, 1,70 Гц, 1H), + 7,39 (д, J = 8,50 Гц, 1H), 7,69 (с, 1H), 8,22 [с (ушир.), 1H]; МС (DCI/NH 3) m/z = 340 (M+1) . Приклад 1С 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазол біс(хлористоводнева кислота) Продукт прикладу 1B (210 мг, 0,62 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,5 мл, 2,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин. Тверду речовину, що випала, відфільтрували і сушили, одержуючи вказану в заголовку сполуку 1 у вигляді білої твердої речовини. H ЯМР (300 мгц, піридин-D5) δ м.ч. 2,03-2,38 (м, 8H), 2,79 (с, 3H), 3,74-3,93 (м, 2H), 5,39 (т, J = 4,45 Гц, 1H), 6,77 (с, 1H), 7,55 (дд, J = 8,44, 1,38 Гц, 1H), 7,577,62 (м, 1H), 7,64 (с, 1H), 7,70 (д, J = 8,29 Гц, 1H), 8,05 (с, 1H), 12,37 [с, (ушир.), 1H]; МС + (DCI/NH3) m/z = 340 (M+1) . Аналіз, обчислено для C14H18Cl3·2,00HCl·1,40H2O: C, 52,15; H, 5,94; N, 9,60. Знайдено: C, 51,89; H, 5,56; N, 9,22. Приклад 2 20 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол хлористоводнева кислота Приклад 2А 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол Продукт прикладу 1А (200 мг, 0,66 ммоль) конденсували з фенілбороновою кислотою (Aldrich, 122 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3• Н2О, об. 90/10/2, Rf = 0,20). 1 H ЯМР (300 мгц, CDCl3) δ м.ч. 2,13-2,44 (м, 8H), 2,63 (с, 3H), 3,40-3,71 (м, 2H), 5,28 (т, J = 4,58 + Гц, 1H), 7,28-7,59 (м, 6H); МС (DCI/NH3) m/z = 301 (M+1) . Приклад 2B 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол хлористоводнева кислота Продукт прикладу 2А (140 мг, 0,47 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,5 мл, 2,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, 1 одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,03-2,38 (м, 8H), 2,79 (с, 3H), 3,74-3,93 (м, 2H), 5,39 (т, 2,23-2,37 (м, 4H), 2,41-2,57 (м, 4H), 2,84 (с, 3H), 3,87-4,07 (м, 2H), 5,26 (т, J = 3,45 Гц, 1H), 7,25-7,35 (м, 1H), 7,35-7,43 (м, + 2H), 7,45-7,55 (м, 3H) МС (DCI/NH3) m/z = 301 (M+1) . Приклад 3 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл]тіазол хлористоводнева кислота Приклад 3A 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл]тіазол Продукт прикладу 1А (200 мг, 0,66 ммоль) конденсували 3-піридинілбороновою кислотою (Aldrich, 123 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3• Н2О, об. 90/10/2, Rf = 0,10). 1 H ЯМР (300 мгц, CDCl3) δ м.ч. 2,14-2,50 (м, 6H), 2,66 (с, 3H), 2,80-3,10 (м, 2H), 3,54-3,78 (м, 2H), 5,32 (т, J = 5,80 Гц, 1H), 7,31 (ддд, J = 4,75, 1H), 7,37 (с, 1H), 7,72 (ддд, J = 4,75, 8,20, 2,30, 1,70 Гц, 1H), 8,53 (дд, J = 8,20, 4,70, 0,70 Гц, 1H), 8,70 (д, J = 1,70 Гц, 1H); МС (DCI/NH3) m/z = 302 + (M+1) . Приклад 3B 2-[(ендо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл)тіазол хлористоводнева кислота Продукт прикладу 3A (140 мг, 0,47 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,5 мл, 2,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, 1 одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,23-2,65 (м, 8H), 2,85 (с, 3H), 3,87-4,04 (м, 2H), 5,39 (т, J = 4,24 Гц, 1H), 7,92 (с, 1H), 8,11 (дд, J = 8,14, 5,76 Гц, 1H), 8,72-8,82 (м, 2H), 9,13 (д, J = 2,03 Гц, 1H); МС (DCI/NH 3) m/z + = 301 (M+1) . Приклад 4 Трифторацетат 5-(1Н-індол-6-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазолу Суміш продукту прикладу 1А (150 мг, 0,497 ммоль), 6-індолілборонової кислоти (Frontier, 158 мг, 0,981 ммоль), хлориду біс(трифенілфосфон)паладію(II) (Aldrich 7,0 мг, 0,01 ммоль) і біфеніл-2-ілдициклогексилфосфіну (Strem Chemicals, 10,5 мг, 0,03 ммоль) у суміші діоксан/EtOH/Na2CO3 (водний, 1M) (об. 1/1/1, 3 мл) нагрівали до 130ºC і піддавали TM мікрохвильовому опроміненню при 300 Вт протягом 15 хвилин у мікрохвильовій печі Emry Creator. Тверду речовину відфільтровували за допомогою шприцевого фільтра й органічний розчин безпосередньо очищували за допомогою препаративної ВЕРХ (Gilson, стовпчик Xterra® 5 мкм, 40×100 мм, елюювальні розчинники, MeCN/H2O, що містить 0,1 % об. ТФОК (від 90 % до 10 % протягом 25 хвилин, швидкість потоку 40 мл/хв, УФ, 254 нм). Фракції, що містять цільовий продукт, збирали і концентрували при зниженому тиску. Залишок перемішували в суміші простий ефір/етанол (об. 10/1, 5 мл) при температурі навколишнього середовища протягом 16 1 годин, одержуючи вказану в заголовку сполуку. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,33-2,57 (м, 8H), 2,84 (с, 3H), 3,85-3,98 (м, 2H), 5,25 (т, J = 4,24 Гц, 1H), 6,45 (дд, J = 2,4, 0,7 Гц, 1H), 7,18 (дд, J = 8,1, 1,7 Гц, 1H), 7,27 (тд, J = 2,2, 1,0 Гц, 1H), 7,36 (с, 1H), 7,48-7,51 (м, 1H), 7,55 (д, J = 8,1 Гц, + 1H); МС (DCI/NH3) m/z = 340 (М+Н) . Аналіз, обчислений для C19H21N3OS·1,12 CF3CO2H: C, 54 61; H, 4,77; N, 8,99; знайдено C, 54,54; H, 4,65; N, 8,86. Приклад 5 Трифторацетат 5-(1H-індол-4-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазолу Продукт прикладу 1А (150 мг, 0,497 ммоль) конденсували з 4-індолілбороновою кислотою (Frontier, 160 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 4, одержуючи вказану в 1 заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,31-2,58 21 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 (м, 8H), 2,85 (с, 3H), 3,90-3,98 (м, 2H), 5,28 (т, J = 4,2 Гц, 1H), 6,71 (дд, J = 3,2, 0,8 Гц, 1H), 7,13 (д, J = 2,7 Гц, 1H), 7,14 (с, 1H), 7,34 (д, J = 3,4 Гц, 1H), 7,39 (ддд, J = 6,0, 3,1, 1,0 Гц, 1H), 7,48 (с, + 1H); МС (DCI/NH3) m/z = 340 (M+H) . Аналіз, обчислений для C19H21N3OS·CF3CO2H·0,35H2O: C, 54,86; H, 4,98; N, 9,14; Знайдено C, 55,21; H, 4,97; N, 8,75. Приклад 6 Трифторацетат 5-(бензофуран-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3ілокси]тіазолу Продукт прикладу 1А (150 мг, 0,497 ммоль) конденсували з бензофуран-5-бороновою кислотою (Maybridge, 240 мг, 1,5 ммоль) згідно зі способом, описаним у прикладі 4. Вказану в 1 заголовку сполуку одержували у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,30-2,55 (м, 8H), 2,85 (с, 3H), 3,90-3,98 (м, 2H), 5,26 (т, J = 4,3 Гц, 1H), 6,87 (дд, J = 2,2, 0,8 Гц, 1H), 7,41 (с, 1H), 7,46 (дд, J = 8,5, 1,7 Гц, 1H), 7,53 (д, J = 8,8 Гц, 1H), 7,75 (д, J = 1,7 Гц, 1H), 7,79 + (д, J = 2,4 Гц, 1H); МС (DCI/NH3) m/z = 341 (M+H) . Аналіз, обчислено для C19H20N2O2S·1,10 CF3CO2H: C, 54,66; H, 4,57; N, 6,01. Знайдено C, 54,95; H, 4,53; N, 6,01. Приклад 7 Фумарат 5-(бензо[b]тіофен-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазолу Продукт прикладу 1А (150 мг, 0,497 ммоль) конденсували з 2-бензо[b]тіофен-5-іл)-4,4,5,5тетраметил-1,3,2-діоксабороланом (Maybridge, 260 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 4. Суміш очищували методом препаративної ВЕРХ (Gilson, Xterra® колонка, 7 мкм, 40×100 мм, елююючий розчинник, MeCN/H2O (з 0,1 M NH4HCO3/NH4OH, PH = 10) (об. від 90/10 до 10/90 протягом 25 хвилин), швидкість потоку 40 мл/хв, УФ, 254 нм), для одержання вільної основи вказаної в заголовку сполуки. Вільну основу потім обробляли фумаровою кислотою в суміші EtOAc/EtOH (про., 10:1, 5 мл) при температурі навколишнього середовища протягом 16 1 годин, одержуючи вказану в заголовку сполуку. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,29-2,55 (м, 8H), 2,84 (с, 3H), 3,88-3,95 (м, 2H), 5,26 (т, J = 4,30 Гц, 1H), 6,69 (с, 2H), 7,39 (д, J = 5,4 Гц, 1H), 7,49-7,55 (м, 2H), 7,63 (д, J = 5,8 Гц, 1H), 7,92 (д, J = 8,5 Гц, 1H), 7,97 (д, J = 1,7 Гц, 1H); МС + (DCI/NH3) m/z = 357 (M+H) . Аналіз, обчислено для C19H20N2OS2·1,10 C4H4O4: C, 58,05; H, 5,08; N, 5,79. Знайдено C, 58,07; H, 4,98; N, 5 73. Приклад 8 Геміфумарат 5-(2-(трифторметил)-1Н-індол-5-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан3-ілокси]тіазолу Продукт прикладу 1А (150 мг, 0,497 ммоль) конденсували з 5-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)-2-(трифторметил)-1Н-індолом (посилання на патент США 2005043347, 300 мг, 0,965 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи вказану в заголовку 1 сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,26-2,53 (м, 8H), 2,76 (с, 3H), 3,75-3,83 (м, 2H), 5,21 (т, J = 4,1 Гц, 1H), 6,68 (с, 1H), 6,91 (д, J = 1,4 Гц, 1H), 7,38 (с, 1H), + 7,47 (с, 1H), 7,48 (с, 1H), 7,77 (с, 1H); МС (DCI/NH3) m/z = 408 (M+H) . Аналіз, обчислено для C20H20F3N3OS·0,90 C4H4O4: C, 55,37; H, 4,65; N, 8,21; Знайдено C, 55,47; H, 4,69; N, 8,32. Приклад 9 Фумарат 5-(дибензо[b, d]тіофен-2-іл)-2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3ілокси]тіазолу Продукт прикладу 1А (150 мг, 0,497 ммоль) і дибензо[b, d]тіофен-2-боронову кислоту (Acros, 137 мг, 0,60 ммоль) обробляли згідно зі способом, описаним у прикладі 7, одержуючи вказану в 1 заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,30-2,57 (м, 8H), 2,84 (с, 3H), 3,90-3,96 (м, 2H), 5,28 (т, J = 4,1 Гц, 1H), 6,69 (с, 1H), 7,47-7,54 (м, 2H), 7,61 (с, 1H), 7,64 (дд, J = 8,5, 1,7 Гц, 1H), 7,87-7,94 (м, 2H), 8,28-8,35 (м, 1H), 8,37 (д, J = 1,7 Гц, 1Н); + МС (DCI/NH3) m/z = 407 (M+H) . Аналіз, обчислено для C23H22N2OS2·1,40C4H4O4: C, 60,36; H, 4,89; N, 4,92; Знайдено C, 60,23; H, 4,94; N, 4,59. Приклад 10 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазолу три(хлористоводнева кислота) Приклад 10A (екзо)-8-Метил-8-азабіцикло[3.2.1]окт-3-ил-4-нітробензоат До розчину (ендо)тропіну (2,82 г, 20,0 ммоль), 4-нітробензойної кислоти (3,34 г, 20,0 ммоль) і трифенілфосфіну (5,24 г, 20,0 ммоль) у сухому ТГФ (100 мл) додавали до діізопропілазодикарбоксилату (4,04 г, 20,0 ммоль) при кімнатній температурі. Отриману суміш перемішували при температурі навколишнього середовища протягом 40 годин і потім концентрували при зниженому тиску. Залишок очищували методом хроматографії (140 г Si2, 1 EtOAc:MeOH:NH3·H2O, 90:10:1, Rf = 0,30), одержуючи вказану в заголовку сполуку. H ЯМР 22 UA 99936 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 (300 мгц, CD3OD) H ЯМР (300 мгц, CD3OD) δ 1,74-2,23 (м, 8H), 2,38 (с, 3H), 3,32-3,38 (м, 2H), + 5,23-5,38 (м, 1H), 8,21 (д, J = 8,82 Гц, 2H), 8,32 (д, J = 8,82 Гц, 2H) м.ч. МС (DCI/NH3): 291 (M+H) . Приклад 10B (екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ол Продукт прикладу 10А (5,0 г, 0,017 моль) в етанолі (10 мл) обробляли NaOH (1н, 200 мл) при кімнатній температурі протягом 40 годин. Суміш екстрагували CHCl 3/iPrOH (об. 90/10, 3×100 мл). Об'єднані екстракти концентрували при зниженому тиску, одержуючи вказану в 1 заголовку сполуку. H ЯМР (300 мгц, CD3OD) δ 1,55-1,69 (м, 4H), 1,80 (м, 2H), 1,99-2,09 (м, 2H), + 2,28 (с, 3H), 3,14-3,21 (м, 2H), 3,79-3,93 (м, 1H) м.ч. МС (DCI/NH3): 142 (M+H) . Приклад 10С 5-бром-2-[(екзо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]тіазол Продукт прикладу 10В (420 мг, 3,0 ммоль) конденсували з 2,5-дибромтіазолом (Aldrich, 969 мг, 40 ммоль) згідно зі способом, описаним у прикладі 1А. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·Н2О, об. 90/10/2, Rf = 0,40), 1 одержуючи вказану в заголовку сполуку. H ЯМР (300 мгц, CD3OD) δ м.ч. 1,82-2,12 (м, 4H), 2,192,33 (м, 2H), 2,33-2,46 (м, 2H), 2,64 (с, 3H), 3,57-3,83 (м, 2H), 5,15-5,51 (м, 1H), 7,12 (с, 1H); МС + + (DCI/NH3) m/z = 303 (M+1) , 305 (M+1) . Приклад 10D 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазол Продукт прикладу 10С (200 мг, 0,66 ммоль) конденсували з 5-індолілбороновою кислотою (Frontier, 160 мг, 1,0 ммоль) згідно зі способом прикладу 1B. Вказану в заголовку сполуку 1 очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,10). H ЯМР (300 мгц, CD3OD) δ м.ч. 1,89-2,11 (м, 4H), 2,21-2,32 (м, 2H), 2,34-2,46 (м, 2H), 2,60 (с, 3H), 3,583,85 (м, 2H), 5,14-5,41 (м, 1H), 6,45 (д, J = 4,07 Гц, 1H), 7,22-7,30 (м, 3H), 7,39 (д, J = 8,48 Гц, 1H), + 7,64 (с, 1H); МС (DCI/NH3) m/z = 340 (M+1) . Приклад 10E 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(1Н-індол-5-іл)тіазолу три(хлористоводнева кислота) Продукт прикладу 10D (210 мг, 0,62 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,5 мл, 2,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, 1 одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, піридин-D5) δ м.ч. 1,84-1,94 (м, 2H), 2,16-2,29 (м, 2H), 2,40-2,51 (м, J = 3,07 Гц, 2H), 2,80 (с, 3H), 2,90-3,14 (м, 2H), 3,87-4,00 (м, 2H), 5,40-5,56 (м, 1H), 6,75 (с, 1H), 7,45-7,53 (м, 2H), 7,59-7,66 (м, + 2H), 8,01 (с, 1H), 12,28 (с, 1H); МС (DCI/NH3) m/z = 340 (M+1) . Аналіз, обчислено для C14H18Cl3·3,52HCl·0,10EtOAc: C, 48,89; H, 5,35; N, 8,82. Знайдено: C, 49,22; H, 4,86; N, 8,42. Приклад 11 2-[(екзо)-8-Метил-8-aзaбіцикло[3.2.1]октан-3-ілокси]-5-(1H-індол-6-іл)тіазол три(хлористоводнева кислота) Приклад 11A 2-[(екзо)-8-Метил-8-aзaбіцикло[3.2.1]октан-3-ілокси]-5-(1H-індол-5-іл)тіазол Продукт прикладу 10С (200 мг, 0,66 ммоль) конденсували з 6-індолілбороновою кислотою (Frontier, 160 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,10). 1 H ЯМР (300 мгц, CDCl3) δ м.ч. 1,95-2,30 (м, 3H), 2,31-2,56 (м, 5H), 2,74 (с, 3H), 3,62-3,90 (м, 2H), 5,24-5,56 (м, 1H), 6,51-6,63 (м, 1H), 7,20-7,25 (м, 2H), 7,44 (с, 1H), 7,62 (д, J = 8,14 Гц, 1H), 8,22 + (с, 1H); МС (DCI/NH3) m/z = 340 (M+1) . Приклад 11B 2-[(екзо)-8-Метил-8-aзaбіцикло[3.2.1]октан-3-ілокси]-5-(1H-індол-5-іл)тіазол три(хлористоводнева кислота) Продукт прикладу 11A (140 мг, 0,41 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,5 мл, 2,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, 1 одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 MГц, піридин-D5) δ м.ч. 1,83-1,94 (м, 2H), 2,17-2,33 (м, 2H), 2,37-2,55 (м, 2H), 2,85 (с, 3H), 2,93-3,19 (м, 2H), 3,91-4,03 (м, 2H), 5,33-5,61 (м, 1H), 6,71-6,75 (м, 1H), 7,44 (дд, J = 8,00, 1,60 Гц, 1H), 7,56+ 7,59 (м, 1H), 7,60 (с, 1H), 7,75-7,86 (м, 2H), 12,23 (с, 1H); МС (DCI/NH 3) m/z = 340 (M+1) . Аналіз, обчислено для C14H18Cl3·3,70HCl·1,30H2O: C, 45,84; H, 5,53; N, 8,44. Знайдено: C, 45,80; H, 5,13; N, 8,06. Приклад 12 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол хлористоводнева кислота Приклад 12A 23 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол Продукт прикладу 10С (100 мг, 0,33 ммоль) конденсували з фенілбороновою кислотою (Aldrich, 61 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,40). 1 H ЯМР (300 мгц, CDCl3) δ м.ч. 2,01-2,23 (м, 2H), 2,28-2,50 (м, 4H), 2,48-2,71 (м, 2H), 2,76 (с, 3H), + 3,63-3,98 (м, 2H), 5,09-5,64 (м, 1H), 7,27-7,55 (м, 6H); МС (DCI/NH3) m/z = 301 (M+1) . Приклад 12B 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-фенілтіазол хлористоводнева кислота Продукт прикладу 12A (90 мг, 0,30 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,25 мл, 1,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, 1 одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 MГц, піридин-D5) δ м.ч. 1,91-2,34 (м, 4H), 2,34-2,49 (м, 2H), 2,53-2,67 (м, 2H), 2,83 (с, 3H), 3,91-4,19 (м, + 2H), 5,29-5,61 (м, 1H), 7,17-7,63 (м, 6H); МС (DCI/NH3) m/z = 301 (M+1) . Приклад 13 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл)тіазола три(хлористоводнева кислота) Приклад 13A Продукт прикладу 10С (100 мг, 0,33 ммоль) конденсували з 3-піридинілбороновою кислотою (Aldrich, 62 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,40). 1 H ЯМР (300 мгц, CDCl3) δ м.ч. 1,88-2,05 (м, 2H), 2,19-2,51 (м, 6H), 2,64 (с, 3H), 3,56-3,76 (м, 2H), 5,19-5,46 (м, 1H), 7,28 (ддд, J = 7,80, 3,00, 0,60 Гц, 1H), 7,32 (с, 1H), 7,66-7,74 (м, 1H), 8,52 (дд, J + = 4,92, 1,53 Гц, 1H), 8,71 (д, J = 1,70 Гц, 1H); МС (DCI/NH3) m/z = 302 (M+1) . Приклад 13B 2-[(екзо)-8-Метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-(піридин-3-іл)тіазолу три(хлористоводнева кислота) Продукт прикладу 13A (100 мг, 0,33 ммоль) обробляли HCl (Aldrich, 4M у діоксані, 0,25 мл, 1,0 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, 1 одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,05-2,31 (м, 4H), 2,33-2,49 (м, 2H), 2,54-2,69 (м, 2H), 2,84 (с, 3H), 3,95-4,15 (м, 2H), 5,33-5,73 (м, 1H), 7,90 (с, 1H), 8,10 (дд, J = 8,14, 5,76 Гц, 1H), 8,62-8,83 (м, 2H), 9,12 (д, J = + 2,03 Гц, 1H); МС (DCI/NH3) m/z = 301 (M+1) . Аналіз. Обчислено для C16H19N3OS·3,78HCl·1,78H2O: C, 40,68; H, 5,63; N, 8,90. Знайдено: C, 40,34; H, 5,24; N, 8,70. Приклад 14 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-феніл-1,3,4-тіадіазол Приклад 14A 2-бром-5-феніл-1,3,4-тіадіазол Переміщуваний розчин 2-аміно-5-феніл-[1,3,4]тіадіазолу (Aldrich, 0,885 г, 5,0 ммоль) у MeCN (безводний, Aldrich, 20 мл) обробляли бромідом міді(II) (Acros, 2,23 г, 10,0 ммоль) і ізоамілнітритом (Aldrich, 1,17 г, 10,0 ммоль) при кімнатній температурі протягом 10 годин. Суміш гасили насиченим розчином хлористого амонію (5 мл) і екстрагували ефіром (3×40 мл). Об'єднані екстракти концентрували й очищували за допомогою флеш-хроматографії 1 [EtOAc/гексани = 20/80 (об.), Rf = 0,6], одержуючи вказану в заголовку сполуку. H ЯМР (300 мгц, + + CDCl3) δ м.ч. 7,44-7,55 (м, 3H), 7,85-7,94 (м, 2H). MS (DCI/NH3) m/e 241 (M+H) , 243 (M+H) . Приклад 14B 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-феніл-1,3,4-тіадіазол Розчин тропіну (Aldrich, 140 мг, 1,0 ммоль) у ТГФ (безводний, Aldrich, 10 мл) перемішували з трет-бутоксидом калію (Aldrich, 114 мг, 1,0 ммоль) при температурі навколишнього середовища протягом 1,0 години. Потім додавали продукт прикладу 14A (241 мг, 1,0 ммоль) при 10-20ºC, і суміш перемішували при 60ºC протягом 10 годин, а потім гасили водою (1 мл) і концентрували. Залишок розбавляли CHCl3 (30 мл) і промивали насиченим розчином солі (2×5 мл). Органічний розчин концентрували і залишок очищували з використанням хроматографії (Si 2, 1 CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,15), одержуючи вказану в заголовку сполуку. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,31-2,44 (м, 4H), 2,46-2,59 (м, 4H), 2,84 (с, 3H), 3,78-4,11 (м, 2H), 5,36 (т, + J = 3,05 Гц, 1H), 7,43-7,61 (м, 3H), 7,77-7,93 (м, 2H); МС (DCI/NH3) m/z = 302 (M+1) . Приклад 15 2-(1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол біс(пара-толуолсульфонова кислота) Приклад 15A 2,5-дибром-1,3,4-тіадіазол 24 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 До переміщуваного розчину 2,5-діаміно-[1,3,4]тіадіазолу (Aldrich, 13,0 г, 72,2 ммоль) у MeCN (безводний, Aldrich, 250 мл) додавали бромід міді(II) (Acros, 18,80 г, 83,7 ммоль) і ізо-амілнітрит (Aldrich, 17,0 г, 145,0 ммоль) при 0-10ºC. Потім суміш перемішували при температурі навколишнього середовища протягом 10 годин. Суміш гасили насиченим розчином хлористого амонію (100 мл) і екстрагували ефіром (3×200 мл). Об'єднані екстракти концентрували й очищували за допомогою флеш-хроматографії [EtOAc/гексани = 20/80 (об.), Rf = 0,6], + + одержуючи вказану в заголовку сполуку. Мас-спектр (DCI/NH3) m/е 243 (M+H) , 245 (M+H) , 247 + (M+H) . Приклад 15B 2-бром-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол Продукт прикладу 15A (2,44 г, 10 ммоль) конденсували з тропіном (Aldrich, 1,40 г, 10,0 ммоль) відповідно до способу, описаного у прикладі 14А. Вказану в заголовку сполуку 1 очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,10). H ЯМР (300 мгц, CDCl3) δ м.ч. 1,83-1,96 (м, 2H), 1,98-2,12 (м, 4H), 2,15-2,28 (м, 2H), 2,30 (с, 3H), 3,08+ + 3,30 (м, 2H), 5,27 (т, J = 5,09 Гц, 1H); МС (DCI/NH3) m/z = 304 (M+1) , 306 (M+1) . Приклад 15C 2-(1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол Продукт прикладу 15B (150 мг, 0,49 ммоль) конденсували з 5-індолілбороновою кислотою (Frontier, 160 мг, 1,0 ммоль) і обробляли згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, 1 Rf = 0,10). H ЯМР (300 мгц, CD3OD) δ м.ч. 1,97-2,27 (м, 8H), 2,34 (с, 3H), 3,17-3,26 (м, 2H), 5,18 (т, J = 4,92 Гц, 1H), 6,55 (д, J = 2,37 Гц, 1H), 7,33 (д, J = 3,39 Гц, 1H), 7,47 (д, J = 8,48 Гц, 1H), 7,62 + (дд, J = 8,65, 1,87 Гц, 1H), 8,02 (с, 1H); МС (DCI/NH3) m/z = 341 (M+1) . Приклад 15D 2-(1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол біс(пара-толуолсульфонова кислота) Продукт прикладу 15C (100 мг, 0,29 ммоль) обробляли п-TsOH·H2O (57 мг, 0,3 ммоль) у EtOAc (5 мл) при температурі навколишнього середовища протягом 10 годин, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,32-2,58 (м, 14H), 2,85 (с, 3H), 3,85-4,10 (м, 2H), 5,33 (т, J = 4,07 Гц, 1H), 6,56 (д, J = 3,39 Гц, 1H), 7,23 (д, J = 8,14 Гц, 4H), 7,34 (д, J = 3,05 Гц, 1H), 7,47-7,51 (м, 1H), 7,63 (дд, J = 8,65, 1,53 + Гц, 1H), 8,04 (д, J = 1,36 Гц, 1H); МС (DCI/NH3) m/z = 341 (M+1) . Аналіз. Обчислено для C18H20N4OS·1,90TsOH·1,50H2O: C, 54,12; H, 5,54; N, 8,07. Знайдено: C, 53,83; H, 5,25; N, 8,38. Приклад 16 Фумарат 2-(бензофуран-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з бензофуран-5-бороновою кислотою (Maybridge, 240 мг, 1,5 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,28-2,58 (м, 8H), 2,79 (с, 3H), 3,80-3,88 (м, 2H), 5,35 (т, J = 4,1 Гц, 1H), 6,68 (с, 2H), 6,96 (дд, J = 2,4, 1,0 Гц, 1H), 7,63 (д, J = 8,5 Гц, 1H), 7,83 (дд, J = 8,6, 1,9 Гц, 1H), 7,87 (д, J = 2,4 Гц, 1H), 8,12 + (д, J = 1,7 Гц, 1H); МС (DCI/NH3) m/z = 342 (M+H) . Аналіз. Обчислено для C18H19N3O2S·1,00·C4H4O4: C, 57,76; H, 5,07; N, 9,18, Знайдено C, 57,56; H, 4,97; N, 9,45. Приклад 17 Фумарат 2-(бензо[b]тіофен-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (303 мг, 1,0 ммоль) конденсували з 2-(бензо[b]тіофен-5-іл)-4,4,5,5тетраметил-1,3,2-діоксабороланом (Maybridge, 520 мг, 2,0 ммоль) згідно зі способом, описаним 1 у прикладі 7, одержуючи вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,33-2,45 (м, 4H), 2,49-2,58 (м, 4H), 2,83 (с, 3H) 3,90-3,97 (м, 2H), 5,37 (т, J = 4,20 Гц, 1H), 6,69 (с, 2H), 7,49 (дд, J = 5,4, 0,7 Гц, 1H), 7,72 (д, J = 5,4 Гц, 1H), 7,85 (дд, J = + 8,5, 2,4 Гц, 1H), 8,05 (д, J = 8,5 Гц, 1H), 8,32 (д, J = 1,0 Гц, 1H); МС (DCI/NH 3) m/e = 358 (M+H) . Аналіз. Обчислено для C18H19N3OS2·1,1C4H4O4: C, 55,45; H, 4,86; N, 8,66; Знайдено C, 55,27; H, 4,89; N, 8,54. Приклад 18 Фумарат 2-(3-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 3-фторфенілбороновою кислотою (Aldrich, 168 мг, 1,2 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,32-2,42 (м, 4H), 2,48-2,56 (м, 4H), 25 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 2,83 (с, 3H), 3,90-3,95 (м, 2H), 5,36 (т, J = 4,2 Гц, 1H), 6,69 (с, 2H), 7,24-7,32 (м, 1H), 7,53 (тд, J = + 8,2, 5,6 Гц, 1H), 7,62-7,68 (м, 2H); МС (DCI/NH3) m/z = 320 (M+H) . Аналіз. Обчислено для C16H18FN3OS·1,15C4H4O4: C, 54,63; H, 5,03; N, 9,28; Знайдено C, 54,50; H, 5,29; N, 9,20. Приклад 19 Фумарат 2-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-5-м-толіл-1,3,4-тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з м-толілбороновою кислотою (Aldrich, 180 мг, 1,32 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи вказану в 1 заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,29-2,44 (м, 8H), 2,52 (с, 3H), 2,83 (с, 3H), 3,85-2,96 (м, 2H), 5,35 (т, J = 4,1 Гц, 1H), 6,69 (с, 2H), 7,30-7,43 + (м, 2H), 7,59-7,76 (м, 2H); МС (DCI/NH3) m/z = 316 (M+H) ; Аналіз. Обчислено для C17H21N3OS·1,05C4H4O4: C, 58,23; H, 5,81; N, 9,61; Знайдено C, 58,16; H, 5,85; N, 9,57. Приклад 20 Фумарат 2-(4-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 4-фторфенілбороновою кислотою (Aldrich, 130 мг, 0,93 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,31-2,42 (м, 4H), 2,49-2,55 (м, 4H), 2,83 (с, 3H), 3,88-3,95 (м, 2H), 5,34 (т, J = 4,2 Гц, 1H), 6,69 (с, + 2H), 7,21-7,30 (м, 2H), 7,85-7,93 (м, 2H); МС (DCI/NH3) m/z = 320 (M+H) . Аналіз. Обчислено для C16H18FN3OS·1,10C4H4O4: C, 54,81; H, 5,05, N, 9,40; Знайдено C, 54,82; H, 4,85; N, 9,52. Приклад 21 Фумарат 2-(3-хлорфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 3-хлорфенілбороновою кислотою (Aldrich, 187 мг, 1,2 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,33-2,40 (м, 4H), 2,48-2,55 (м, 4H), 2,84 (с, 3H), 3,88-3,96 (м, 2H), 5,38 (т, J = 4,2 Гц, 1H), 6,69 (с, 2H), 7,46-7,57 (м, 2H), 7,76 (дт, J = 7,1, 1,7 Гц, 1H), 7,89-7,92 (м, 1H); МС (DCI/NH3) m/z = 336 + (M+H) ; Аналіз. Обчислено для C16H18Cl3OS·1,30 C4H4O4: C, 52,31; H, 4,80; N, 8,63; Знайдено С 52,18; H, 4,85; N, 8,73. Приклад 22 2-(1Н-індол-6-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол паратолуолсульфонова кислота Приклад 22А 2-(1Н-індол-6-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол Продукт прикладу 15B (150 мг, 0,49 ммоль) конденсували з 6-індолілбороновою кислотою (Frontier, 160 мг, 1,0 ммоль) і обробляли згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, 1 Rf = 0,10). H ЯМР (300 мгц, CD3OD) δ м.ч. 2,08-2,42 (м, 8H), 2,50 (с, 3H), 3,39-3,52 (м, 2H), 5,23 (т, J = 4,58 Гц, 1H), 6,52 (д, J = 3,05 Гц, 1H), 7,39 (д, J = 3,39 Гц, 1H), 7,47 (дд, J = 8,20, 1,50 Гц, + 1H), 7,62-7,66 (м, 1H), 7,90 (с, 1H), 8,54 (с, 1H); МС (DCI/NH3) m/z = 341 (M+1) . Приклад 22B 2-(1Н-індол-6-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол паратолуолсульфонова кислота Продукт прикладу 22А (130 мг, 0,38 ммоль) обробляли п-TsOH·H2O (144 мг, 0,76 ммоль) у EtOAc (10 мл) при температурі навколишнього середовища протягом 10 годин, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,18-2,70 (м, 11H), 2,85 (с, 3H) 3,88-4,03 (м, 2H), 5,35 (т, J = 4,41 Гц, 1H), 6,53 (д, J = 3,05 Гц, 1H), 7,23 (д, J = 7,80 Гц, 2H), 7,40 (д, 1H), 7,47 (дд, J = 8,31, 1,53 Гц, 1H), 7,65 (д, J = 8,48 Гц, 1H), 7,71 + (д, J = 8,14 Гц, 2H), 7,91 (с, 1H); МС (DCI/NH3) m/z = 341 (M+1) . Аналіз. Обчислено для C18H20N4OS·1,10TsOH·0,20H2O: C, 57,86; H, 5,52; N, 10,50. Знайдено: C, 57,90; H, 5,18; N, 10,19. Приклад 23 2-(1Н-індол-4-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол паратолуолсульфонова кислота Приклад 23A 2-(1Н-індол-4-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол Продукт прикладу 15B (150 мг, 0,49 ммоль) конденсували з 6-індолілбороновою кислотою (Frontier, 160 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 1B. Вказану в заголовку сполуку очищували методом хроматографії (Si2, CH2Cl2/MeOH/NH3·H2O, об. 90/10/2, Rf = 0,10). 1 H ЯМР (300 мгц, CD3OD) δ м.ч. 1,98-2,32 (м, 8H), 2,34 (с, 3H), 3,17-3,27 (м, 2H), 5,22 (т, J = 4,92 26 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 Гц, 1H), 7,05 (д, J = 2,37 Гц, 1H), 7,20 (т, J = 7,60 Гц, 1H), 7,41 (д, J = 3,39 Гц, 1H), 7,48 (д, J = 7,46 + Гц, 1H), 7,56 (д, J = 8,14 Гц, 1H); МС (DCI/NH3) m/z = 341 (M+1) . Приклад 23B 2-(1Н-індол-4-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4-тіадіазол паратолуолсульфонова кислота . Продукт прикладу 22А (150 мг, 0,44 ммоль) обробляли п-TsOH H2O (168 мг, 0,88 ммоль) у EtOAc (10 мл) при температурі навколишнього середовища протягом 10 годин, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,36-2,63 (м, 11H), 2,85 (с, 3H), 3,84-4,11 (м, 2H), 5,38 (т, J = 4,75 Гц, 1H), 7,05 (д, J = 4,07 Гц, 1H), 7,16-7,27 (м, 3H), 7,43 (д, J = 3,05 Гц, 1H), 7,49 (д, J = 7,46 Гц, 1H), 7,57 (д, J = 8,14 Гц, 1H), + 7,70 (д, J = 8,10 Гц, 2H); МС (DCI/NH 3) m/z = 341 (M+1) . Аналіз. Обчислено для C18H20N4OS·1,00TsOH·0,40H2O: C, 57,76; H, 5,58; N, 10,78. Знайдено: C, 57,33; H, 5,25; N, 10,49. Приклад 24 Трифторацетат 2-(3-ціанофеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 3-ціанофенілбороновою кислотою (Aldrich, 185 мг, 1,2 ммоль) згідно зі способом, описаним у прикладі 4, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,32-2,71 (м, 8H), 2,85 (с, 3H), 3,92-3,99 (м, 2H), 5,40 (т, J = 4,4 Гц, 1H), 7,70 (т, J = 7,8 Гц, 1H), 7,88 (дт, J = 7,8, 1,4 Гц, 1H), 8,16 (ддд, J = 8,1, 1,8, 1,0 Гц, 1H), 8,24 (т, J = 1,7 Гц, 1H); МС + (DCI/NH3) m/z = 327 (M+H) . Аналіз. Обчислено для C17H18N4OS·1,40CF3CO2H·0,60H2O: C, 47,86; H, 4,18, N, 11,28; Знайдено C, 47,63; H, 3,88; N, 11,56. Приклад 25 Фумарат 2-(3-трифторметилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]1,3,4-тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 3трифторметилфенілбороновою кислотою (Aldrich, 228 мг, 1,2 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи вказану в заголовку сполуку у вигляді білої твердої 1 речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,31-2,57 (м, 8H), 2,85 (с, 3H), 3,92-3,98 (м, 2H), 5,305,42 (м, 1H), 6,70 (с, 2,80H), 7,72 (т, J = 7,8 Гц, 1H), 7,83 (д, J = 7,8 Гц, 1H), 8,09 (д, J = 7,8 Гц, + 1H), 8,17 (с, 1H); МС (DCI/NH3) m/z = 370 (M+H) . Аналіз. Обчислено для C17H18F3N3OS·1,40C4H4O4: C, 51,03; H, 4,47; N, 7,90; Знайдено C, 51,17; H, 4,55; N, 7,75. Приклад 26 Фумарат 2-(4-хлорфеніл)-5-((1R, 3R, 5S)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси)-1,3,4тіадіазол Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 4-хлорфенілбороновою кислотою (Aldrich, 187 мг, 1,2 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,32-2,39(м, 4H), 2,46-2,55 (м, 4H), 2,84 (с, 3H), 3,85-2,96 (м, 2H), 5,33-5,39 (м, 1H), 6,69 (с, 2H), + 7,53 (д, J = 8,5 Гц, 2H), 7,85 (д, J = 8,5 Гц, 2H); МС (DCI/NH3) m/z = 336 (M+H) . Аналіз. Обчислено для C16H18Cl3OS·1,15C4H4O4: C, 52,72; H, 4,85, N, 8,95; Знайдено C, 52,76; H, 4,77; N, 9,12. Приклад 27 Біс(фумарат) 2-(2-(трифторметил)-1Н-індол-5-іл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан3-ілокси]-1,3,4-тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 5-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)-2-(трифторметил)-1Н-індолом (посилання: опублікована патентна заявка США № 2005043347, 380 мг, 1,22 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,30-2,64 (м, 8H), 2,86 (с, 3H), 3,93-2,98 (м, 2H), 5,32-5,39 (м, 1H), 6,72 (с, 5H), 7,03 (с, 1H), 7,57 (д, J = 8,5 Гц, 1H), 7,83 (дд, J = 8,6, 1,9 Гц, 1H), 8,15 (д, J = 1,7 Гц, 1H); МС (DCI/NH3) m/z = 409 + (M+H) . Аналіз. Обчислено для C19H19F3N4OS·2,5C4H4O4·0,7H2O: C, 48,97; H, 4,31; N, 7,88; Знайдено C, 48,99; H, 4,30; N, 7,62. Приклад 28 Фумарат 2-(3-хлор-4-фторфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 3-хлор-4-фторфенілбороновою кислотою (Aldrich, 190 мг, 1,09 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,32-2,42 (м, 4H), 2,44-2,56 (м, 4H), 2,83 (с, 3H), 3,88-2,96 (м, 2H), 5,32-5,39 (м, 1H), 6,69 (с, 2,2H), 27 UA 99936 C2 5 10 15 20 25 30 35 40 45 50 55 60 7,41 (т, J = 8,6 Гц, 1H), 7,82 (ддд, J = 8,7, 4,5, 2,4 Гц, 1H), 8,03 (дд, J = 7,0, 2,2 Гц, 1H); МС + (DCI/NH3) m/z = 354 (M+H) . Аналіз. Обчислено для C16H17ClFN3OS·1,10C4H4O4: C, 50,88; H, 4,48; N, 8,73; Знайдено C, 50,93; H, 4,53; N, 8,67. Приклад 29 Фумарат 2-(4-(трифторметил)феніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]1,3,4-тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 4(трифторметил)фенілбороновою кислотою (Aldrich, 190 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи вказану в заголовку сполуку у вигляді білої твердої 1 речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,32-2,43 (м, 4H), 2,50-2,57 (м, 4H), 2,83 (с, 3H), 3,863,95 (м, 2H), 5,32-5,43 (м, 1H), 6,69 (с, 2,30H), 7,82 (д, J = 8,5 Гц, 2H), 8,06 (д, J = 8,1 Гц, 2H). MS + (DCI/NH3) m/e = 370 (M+H) . Аналіз. Обчислено для C17H18F3N3OS·1,15C4H4O4: C, 51,59; H, 4,53; N, 8,36; Знайдено C, 51,38; H, 4,48; N, 8,36. Приклад 30 Фумарат 2-(4-метоксифеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 4-метоксифенілбороновою кислотою (Aldrich, 152 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,29-2,42 (м, 4H), 2,44-2,56 (м, 4H), 2,83 (с, 3H), 3,86 (с, 3H), 3,88-3,94 (м, 2H), 5,29-5,36 (м, 1H), + 6,69 (с, 2,30H), 7,04 (д, J = 8,8 Гц, 2H), 7,78 (д, J = 8,8 Гц, 2H); МС (DCI/NH3) m/z = 332 (M+H) . Аналіз. Обчислено для C17H21N3O2S·1,15C4H4O4: C, 55,80; H, 5,55; N, 9,04; Знайдено C, 55,91; H, 5,34; N, 9,20. Приклад 31 Геміфумарат 2-(3-амінофеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (152 мг, 0,50 ммоль) конденсували з 3-амінофенілбороновою кислотою (Aldrich, 137 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,31-2,38 (м, 4H), 2,45-2,51 (м, 4H), 2,81 (с, 3H), 3,82-3,92 (м, 2H), 5,30-5,38 (м, 1H), 6,68 (с, 1,30H), 6,83 (ддд, J = 8,0, 2,2, 1,0 Гц, 1H), 7,05-7,09 (м, 1H), 7,14-7,22 (м, 2H); МС (DCI/NH3) + m/z = 317 (M+H) . Аналіз. Обчислено для C16H20N4OS·0,65C4H4O4: C, 57,01, H, 5,81; N, 14,30; Знайдено C, 56,85; H, 5,88; N, 14,37. Приклад 32 Фумарат 2-(4-етилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 4-етилфенілбороновою кислотою (Aldrich, 150 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 7, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 1,27 (т, J = 7,5 Гц, 5H), 2,31-2,43 (м, 4H), 2,48-2,56 (м, 4H), 2,71 (кв., J = 7,8 Гц, 2H), 2,83 (с, 3H), 3,87-3,95 (м, 2H), 5,31-5,38 (м, 1H), 6,69 (с, 2,30H), 7,35 (д, J = 8,5 Гц, 2H), 7,75 (д, J = 8,5 Гц, 2H); + МС (DCI/NH3) m/z = 330 (M+H) . Аналіз. Обчислено для C17H21N3O2S·1,15C4H4O4: C, 58,85; H, 6,04; N, 9,19, Знайдено C, 58,94; H, 6,08; N, 9,34. Приклад 33 Трифторацетат 2-(4-ацетилфеніл)-5-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-ілокси]-1,3,4тіадіазолу Продукт прикладу 15B (150 мг, 0,495 ммоль) конденсували з 4-ацетилфенілбороновою кислотою (Aldrich, 164 мг, 1,0 ммоль) згідно зі способом, описаним у прикладі 4, одержуючи 1 вказану в заголовку сполуку у вигляді білої твердої речовини. H ЯМР (300 мгц, CD3OD) δ м.ч. 2,34-2,45 (м, 4H), 2,48-2,56 (м, 4H), 2,64 (с, 3H), 2,86 (с, 3H), 3,90-3,98 (м, 2H), 5,38-5,44 (м, 1H), + 7,99 (д, J = 8,5 Гц, 2H), 8,12 (д, J = 8,8 Гц, 2H); МС (DCI/NH3) m/z = 344 (M+H) . Аналіз. Обчислено для C18H21N3O2S·1,20 CF3CO2H: C, 51,02; H, 4,66; N, 8,75; Знайдено C, 51,23; H, 4,48; N, 8,70. Приклад 34 N-[(ендо)-8-метил-8-азабіцикло[3.2.1]октан-3-іл]-5-феніл-1,3,4-тіадіазол-2-амін Розчин продукту прикладу 14A (0,17 г, 0,71 ммоль) і дигідрохлориду (ендо)-8-метил-8азабіцикло[3.2.1]октан-3-аміну (Apollo, 0,10 г, 0,7 ммоль) у N, N-діізопропілетиламіні (2 мл) і диметилсульфоксиді (2 мл) перемішували в запаяній ампулі при 130ºC протягом ночі. Суміш охолоджували до кімнатної температури і розбавляли водою (5 мл), екстрагували CHCl3 (4×10 мл). Об'єднані екстракти промивали насиченим розчином солі (2×5 мл) і концентрували 28
ДивитисяДодаткова інформація
Назва патенту англійськоюBiaryl substituted azabicyclic alkane derivatives
Автори англійськоюJi Jianguo, Li Tao, Sippy, Kevin B, Lee, Chih-Hung, Gopalakrishnan Murali
Назва патенту російськоюБиарилзамещенные производные азабициклических алканов
Автори російськоюЦзи Цзяньго, Ли Тао, Сиппи Кевин Б, Ли Чих-Хунг, Гопалакришнан Мурали
МПК / Мітки
МПК: A61K 31/46, C07D 451/06, A61P 25/00, C07D 451/04
Мітки: похідні, азабіциклічних, біарилзаміщені, алканів
Код посилання
<a href="https://ua.patents.su/42-99936-biarilzamishheni-pokhidni-azabiciklichnikh-alkaniv.html" target="_blank" rel="follow" title="База патентів України">Біарилзаміщені похідні азабіциклічних алканів</a>
Попередній патент: Класифікація точок доступу з використанням пілот-ідентифікаторів
Наступний патент: Спосіб і пристрій для грубого відокремлення твердих частинок із газів, обтяжених твердими частинками
Випадковий патент: Спосіб лікування нікотинової залежності












