Застосування ретигабіну для лікування невропатичних болів
Номер патенту: 72550
Опубліковано: 15.03.2005
Автори: Дост Ріта, Бартш Рені, Рундфельдт Кріс, Тобер Крістін, Росток Ангеліка
Формула / Реферат
1. Застосування сполуки формули І
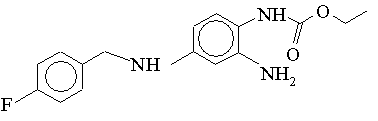
або її фармацевтично прийнятних солей для профілактики й лікування невропатичних болів.
2. Застосування сполуки формули І за п. 1 для лікування алодинії.
3. Застосування сполуки формули І за п. 1 для лікування болів, обумовлених гіпералгезією.
4. Застосування сполуки формули І за п. 1 для лікування фантомних болів.
5. Застосування сполуки формули І за п. 1 для лікування невропатичного болю при діабетичній невропатії.
6. Застосування сполуки формули І за п. 1 для лікування невропатичного болю при мігрені.
Текст
Даний винахід стосується застосування 2-аміно-4-(4-фторбензиламіно)-1-етоксикарбоніламінобензену формули І (за INN: ретигабін) або його застосовних у фармацевтиці солей для профілактики й лікування невропатичних болів. Поняття ''невропатичний біль", такий як алодинія та гіпералгезія, означає особливий вид чутли вості до болю, яка відрізняється від звичайного сприйняття больових подразнень. Пацієнти, які страждають на гіпералгезію, сприймають больові подразнення набагато важче у порівнянні зі здоровими людьми. Поняттям "алодинія" називають феномен сприйняття болю, який виникає при контакті з певним об'єктом або під впливом тепла чи холоду, тобто обумовленого факторами, що як такі не є больовими подразниками. Такі відчуття виявляються іноді в дуже значній мірі і переносяться людиною важко. Це неадекватне сприйняття болю в різних мовах інтерпретується по-різному з використанням термінів, які в їхньому значенні частково перекривають один одний, але далеко не у всіх випадках є синонімами. Так, зокрема, у німецькій мові загальноприйнятими є поняття "Allodynia", (алодинія), "Paraesthesie" (парестезія), "Hyperesthesie" (гіперестезія), "Hyperalgesie" (гіпералгезія) і "Phantomschmerz" (фантомний біль), тоді як в англійській мові поряд із поняттями "allodynia", "hyperalgesia" і "phantom limb pain" використовуються також поняття "reflex sympathetic distrophy" (RSD) (Rogers and Valley, 1994) і "sympathetically maintained pain" (SMP) (J.N. Rogers, MA. Valley, Reflex sympathetic distrophy; Clin. Pediatr. Med. Surg. 11(1), стор. 73-83 (січень 1994)). Під алодинією мається на увазі наднеприємне, аж до прояву больових відчуттів, сприйняття теплових або викликуваних зіткненням з відповідними об'єктами подразнень, обумовлене зниженням порогу больової чутливості тільки у випадку таких стимуляторів. Під гіпералгезією мається на увазі вкрай підвищене сприйняття больових подразнень найрізноманітнішого типу, які є самі по собі такими, що також обумовлено зниженням порогу больової чутливості. Під фантомним болем маються на увазі больові відчуття, джерело яких відсутнє, наприклад, після ампутації кінцівки, тобто біль, який локалізується людиною у відсутній кінцівці. У науковій літературі для цього типу больових відчуттів часто використовують узагальнене поняття "опосередкований невропатичний біль". Характерним при цьому є той факт, що власне больові відчуття обумовлені не наявністю подразника, який викликає звичайний біль, а генеруються периферичною або центральною нервовою системою, оскільки механізм системи, що сприймає та проводить біль, працює в цих умовах інакше. На відміну від інших форм болю, невропатичний біль у більшості випадків носить хронічний характер і зазвичай не піддається або погано піддається лікуванню класичними анальгетиками, такими як опіоїди. До захворюзань, при яких спостерігається змінений механізм системи, що сприймає та проводить біль, належать серед інших такі: 1. Класичні наслідки при інфекційному захворюванні Herpes zoster (оперізувальний лишай) описано як тривалу, стійку алодинію (H.L. Fields, Μ. Rowbotham, R. Baron, Postherpetic neuralgia: irritable nociceptors and diafferentation, Neurobiol. Dis. 5(4) стор. 209-227 (жовтень 1998)). 2. В уражених ВІЛ пацієнтів на різних стадіях захворювання з'являються больові відчуття, які належать до різновидів гіпералгезії і які необхідно чітко відрізняти від ноцицептивного болю (тобто болю, викликуваного больовими подразниками) (М. Lefkowitz, Pain management for the AIDS patient, J. Fla. Med. Assoc. 83(10), стор. 701-704 (грудень 1996)). 3. Опікові рани призводять до виникнення в уражених частинах тіла невропатичної гіпералгезії, і хоча причину, яка викликала біль (висока температура), вже усунено, опікові рани часто є вкрай болючими. 4. Після терапії високими дозами цитостатиків, застосовуваних при лікуванні раку, від пацієнтів часто також приходиться чути скарги на больові відчуття (J.M. Brant, Cancer-related neuropathic pain, матеріали Nurse Pract. Forum 9(3), стор. 154-162 (вересень 1998)). К.Д. Таннеру та іншим (K.D. Tanner, D.B. Reichling, J.D. Levine, Nociceptor hyper-responsiveness during vincristine-induced painful peripheral neuropathy in the rat. J. Neurosci 18(16), стор. 6480-6491 (15 серпня 1998)) вдалося довести, що причина болів, які виникають у зв'язку з лікуванням вінкристином, обумовлена підвищеною збудливістю периферичних больових рецепторів, або, іншими словами, має місце гіпералгезія. 5. Пухлинне захворювання як таке може також викликати (наприклад, у результаті хронічного стиснення нервів пухлиною) невропатичні болі, що належать до різновидів гіпералгезії (J.M. Brant, Cancer-related neuropathic pain, матеріали Nurse Pract. Forum 9(3), стор. 154-162 (вересень 1998)). 6. Невралгія трійчастого нерва є однією з широко розповсюджених форм гіпералгезії, яка часто виявляється без видимого ушкодження нервів (K.J. Burchiel, Trigeminal neuropathic pain, матеріали Acta Neurochir. Suppl. 58, стор. 145-149, Відень (1993). 7. У хворих на діабет під час хвороби часто у формі пізнього ушкодження з'являється гіпералгезія. Хворі скаржаться на сильні болі кінцівок при одночасному зниженні тактильності шкіри (D.S. Bell, Lower limb problems in diabetic patients. What are the causes? What are the remedies? Postgrad. Med. 89(8), стор. 237-240, 243-244 (червень 1991)). 8. Дифузійний біль, який виникає при фіброміалгії, також відносять до форм алодинії (I.J. Russel, Advances in fibromyalgia: possible role for central neurochemicals, Am. J. Med. Sci. 315(6), стор. 377-384 (червень 1998)). 9. Ще одним захворюванням, при якому спостерігаються симптоми гіпералгезії та алодинії, є вульводинія. Це захворювання характеризується хронічними помилковими відчуттями (печінням, поколюванням, сверблячкою) в ділянці вульви при відсутності збудників інфекції, що могли бути причиною таких явищ (T.G. Bohl та ін., Vulvodymia and its differential diagnoses, Semin. Cutan. Med. Surg. 17(3), стор. 189-195 (вересень 1998)). 10. У пацієнтів із хронічними болями в спині часто можна спостерігати компресію (стиснення, защемлення) нервових корінців спинного мозку. Крім хронічних болів, це компресійне ушкодження нервових корінців виявляється також у неприємних, спонтанно виникаючих сенсорних відчуття х (парестезія). Навіть після усунення стиснення хірургічним шляхом багато пацієнтів продовжують проте скаржитися на больові відчуття. Такі повторювані відчуття відносять до невропатичних болів і, поставивши відповідний діагноз, можна чітко визначити їхню відмінність від інших (запальних) форм болю (J. Sorensen, Μ. Bengtsson, Intravenous phentolamine test - an aid in the evaluation of patients with persistent pain after low-back surgery? матеріали Acta Anaesthesiol. Scand. 41(5), стор. 581-585 (травень 1997)). 11. У 10-20% пацієнтів з ушкодженнями спинного мозку в ряді випадків з'являються дуже сильні больові відчуття, які через нестачу неушкодженого спинного мозку генеруються у головному мозку і не можуть бути співвіднесені з больовим стимулом. Такий біль вважається головним невропатичним болем (Р.К. Eide, Pathophysiological mechanismum of central neuropathic pain after spinal cord injury, Spinal Cord. 36(9), стор. 601612 (вересень 1998)), 12. Біль, що виникає після ампутації, за своїми характерними ознаками є невропатичним болем (A. Hill, Phantom limb pain: a review of the literature on attributes and potential mechanismus, J. Pain Symptom Manage 17(2), стор. 125-142 (лютий 1999)). 13. Внутрішні органи також можуть бути джерелом гіпералгезії (Е.А. Ma yer, G.F. Gabhart, Basic and -clinical aspects of visceral hyperalgesia [див. коментар у Gastroenterology 180(2), стор. 618 (лютий 1995)], Gastroenterology 107(1), стор. 271-293 (липень 1994 p.)). Пацієнти з такою формою гіпералгезії страждають від неадекватних відчуттів фізіологічних реакцій у різних ділянках шлунково-кишкового тракту, таких, наприклад, як відчуття переповнення шлунка, болі у шлунку або здуття, хоча відповідні патологічні причини подібних відчуттів відсутні. Як уже зазначалося вище, підвищена або неадекватна реакція на біль є симптомом найрізноманітніших захворювань, і неможливо дати однозначну відповідь на питання, чи має місце будь-який єдиний для усіх випадків патогенез. Така розмаїтість больових відчуттів підтверджується й тим, що неадекватна реакція на біль може виявлятися зовсім по-різному. Загальним, однак, для всіх цих реакцій на біль є те, що морфін або зовсім не дає ніякого ефекту, або досягти позитивного ефекту можна лише при використанні таких дозувань, які викликають небажані побічні дії. Фактори, що обумовлюють реакцію на біль, можуть бути найрізноманітнішими. Так, зокрема, для пацієнтів з алодинією, індукованою герпесом, достатньо протягу, щоб викликати в них пекучі болі. При лікуванні цих пацієнтів варто виходити з того, що збудники якимсь чином ушкоджують нейрони, у результаті чого знижується поріг больової чутли вості. У випадку діабету припускається, що недостатнє живлення нервів киснем і живильними речовинами внаслідок мікроангіопатії призводить до хронічного ушкодження нервів. Це ушкодження викликає, у свою чергу, процес регенерації, який виявляється у брунькуванні нервових волокон. Процеси перебудови в спинному мозку, так само як і в периферичній нервовій системі, розглядаються багатьма авторами як можлива причина гіпералгезії (див., наприклад, A.I. Basbaum, Spinal mechanismus of acute and persistent pain, Reg. Anesth. Pain Med. 24(1), стор. 59-67 (січень-лютий 1999)). У результаті хронічної компресії (стиснення) нервів останні ушкоджуються, однак цілком не руйнуються. У гострих випадках компресії збуджується локальний больовий сигнал, тоді як при хронічній компресії індукуються фактори транскрипції в тілі клітини (а тим самим поза ділянкою компресії в спинному мозку), і така індукція продовжується протягом декількох тижнів. Нейропептиди, такі як субстанція Р, активують брунькування нервових волокон, а також не уражені сусідні нейрони. Крім того, було встановлено, що тіла нервових клітин експресують із підвищеним рівнем норадреналінові рецептори У результаті цього нейрони можуть спонтанно, без зовнішнього імпульсу активуватися і спонтанно викликати больові відчуття. Після зовнішнього стимулювання до головного мозку направляються не окремі імпульсні розряди, а безперервні розряди (Т. Herdegen, Μ. Zimmermann, Immediate erali genes (IEGs) incoding inducible transcription factors (ITFs) and neuropeptides in the nervous system: functional networks for long-term plasticity, опубліковано в Neuropeptides in the spinal cord (за ред. F. Nyberg, H.S. Sharma, Z. Wiesenfeld-Hallin), Progress in Brain Research, том 104, стор. 299-321, вид-во Elsevier Piblishers, Amsterdam (1995)). Участь норадреналінових рецепторів, речовини-переносника симпатичної нервової системи, дає основу говорити про "підтримку" цією системою болю, оскільки в результаті фізіологічного активування симпатичної нервової системи активуються й ці нейрони. Тому в англійській мові широке поширення одержало поняття "reflex sympathetic distrophy" (RSD) (IN. Rogers, M.A. Valley, Reflex sympathetic distrophy, Clin. Pediatr. Med. Surg. 11(1), стор. 73-83 (січень 1994)) або "sympathetically maintained pain" (SMP). Цитостатики, такі як вінкристин, безпосередньо підвищують збудливість больових рецепторів периферичної нервової системи і, можливо, викликають у такий спосіб гіпералгезію (K.D. Tanner, D.B. Reichling, J,D. Levine, Nociceptor hyper-responsiveness during vincristine-induces painful peripheral neuropathy in the rat, J. Neurosci. 18(16), стор. 6480-6491 (серпень 1998)). В експериментах на тваринах фа хівці намагалися з'ясувати основні загальні механізми гіпералгезії. Коли в пацюків частковою лігатурою одного з нервів, що відходять від спинного мозку, викликалася сильна гіпералгезія, що виявляється периферично, у спинному мозку вдавалося виявити групи надактивних нейронів у вигляді аномально (ектопічно) спонтанно активних осередків (H.L. Pan, J.C. Eisenach, S.R. Chen, Gabapentin suppresses ectopic nerve discharges and reverses allodynia in neuropathic rats, J. Pharmacol. Exp. Ther. 288(3), стор. 1026-1030 (березень 1999)). Введенням у відповідних дозах габапентину, медикаменту з вираженою дією при невропатичному болі, можна придушити спонтанну активність цих вогнищ нервових клітин (ектопічні вогнища). При такому ж діапазоні доз удається придушити периферичну гіпералгезію. Аналогічні досліди проводилися також на іншій моделі (HJ, Haebler, X.G. Liu, S. Eschenfelder, W. Jaenig, Is sympathetic-sensory coupling in L5 spinal nerve-injured rats direct? Soc. Neurosci. Abstr. 24, стор. 2084 (1998)). При розтині спинномозкового нерва L5, починаючи з 4-го дня, протягом декількох тижнів спостерігалася несподівано спонтанна активність окремих нервових волокон із залишку зазначеного нерва. Цей феномен з певною часткою імовірності можна співвіднести з фантомним болем. Спонтанну активність цих нервових волокон після ампутації можна пояснити розгальмовуванням NMDA-субтипу глутаматового рецептора (М. Zhuo, NMDA receptor-dependent long term hyperalgesia after tail amputation in mice, Eur. J. Pharmacol. 349(2-3), стор. 211-220 (22 травня 1998)). Можливу участь NMD A-рецептора підтверджують також дослідження, при проведенні яких удалося встановити, що завдяки інтратекальному введенню антагоністів NM.D A можна послабити біль. Підсумовуючи вищесказане, можна констатувати, що стан підвищеного збудження відповідних нервів може відігравати певну роль як причина гіпералгезії, відповідно неадекватного сприйняття болю, але разом із тим не можна виключити й вплив інших факторів. При терапії зазначених захворювань необхідно проводити чітку різницю між симптоматичним лікуванням больових відчуттів і лікуванням причин захворювання з урахуванням захисту нервових клітин (R. Moerz, Schmerzbehandlung bei diabetischen Neuropathien, Fortschritte der Medizin 13, стор. 29-30 (1999)). Для пацієнтів, які зазнають невропатичного болю, обумовленого діабетом, з метою уникнення подальшого прогресування хвороби і попередження можливих ускладнень, таких як ураження нижніх кінцівок, основною програмою є оптимізація обміну речовин, однак таке лікування не чинить впливу на симптоми болю. Причину захворювання, тобто нейродегенеративне ушкодження нервів і мікроангіопатію, яка лежить в основі захворювання, можна лікувати, застосовуючи субстанції, що захищають нервові клітини (нейропротективні), такі як альфа-ліпонова кислота, або інші антиоксиданти, такі як вітамін Е, релевантні (важливі) для нервової системи вітаміни, такі як вітамін В1, В6 або В12, або ж заходами, що поліпшують кровообіг, такими як фізичні тренування. Такий вид лікування не чинить швидкого впливу на біль, однак, якщо при цьому вдається поліпшити функціональну повноцінність нервової системи, то цілком можливо досягти й ослаблення на тривалий час больових відчуттів. На відміну від цього, власне симптоматична терапія болю змушена удатися до інших медикаментів. Причина в тім, що ні анальгетики, такі як похідні морфіну, що впливають на центральну нервову систему, ні звичайні анальгетики, такі як парацетамол або ацетилсаліцилова кислота, що впливають на периферичну нервову систему, у цих випадках не дають потрібного ефекту. Тому приходиться застосовувати антидепресанти, такі як амітриптилін, іміпрамін чи пароксетин, або протисудомні засоби, такі як карбамазепін або габапентин. Трамадол як опіоїдний анальгетик завдяки його здатності впливати й на інші рецептори адренергічної системи також є ефективним. У патентній літературі описується використання топірамату (патент US 5760007) і мокгонідину (заявка ЕР 901790) для лікування невропатичних болів. Ціль такого підходу полягає в лікуванні симптомів болю як таких, а не причин, що їх з умовлюють. Усі зазначені медикаменти при цьому дозволяють послабити больові симптоми лише в частини пацієнтів. Виникнення невропатичного болю, індукованого герпесом, можна попередити за рахунок застосування віростатиків на ранній стадії захворювання, захистивши у такий спосіб нервові клітини від шкідливого впливу вірусу і знизивши тим самим прояв невропатичних болів, однак по завершенні гострої стадії цього інфекційного захворювання ефективність названих медикаментів стосовно симптоматичних болів практично дорівнює нулю. Послабити ці болі в пацієнтів з таким захворюванням можна за рахунок прийому антидепресантів, карбамазепіну або габапентину. При обумовлених компресією невропатичних болях, наприклад, при синдромі карпального тунелю або при стисненні (защемленні) корінців спинномозкових нервів, первинну причину захворювання можна усун ути хірургічним шляхом, розширивши "вузькі місця" (місця стиснення). При завчасному призначенні медикаментів, які мають нейропротективну (захисну) дію, подальший процес ушкодження нервів можна сповільнити або призупинити. Проте, незважаючи на хірургічне втручання, значна частина пацієнтів ще тривалий час і після операції страждає від болів, які не піддаються задовільному лікуванню класичними анальгетиками. У цих випадках доцільно застосовувати антидепресанти й такі медикаменти, як карбамазепін або габапентин. При фантомному болі лікувати його першопричину, ампутацію, звісно, неможливо і, таким чином, для усунення невропатичних болів застосовне лише симптоматичне лікування з використанням вищезгаданих гр уп медикаментів. Проте останнім часом здійснюються спроби при планових ампутаціях шляхом блокади провідності нервів, які розсікаються, протягом декількох днів до проведення операції протидіяти розвитку невропатичних болів. Хоча перші позитивні результати й отримано, проте однозначного підтвердження ефективності такого підходу, заснованого на контрольованих клінічних дослідженнях, дотепер ще немає. Підсумовуючи ви щесказане, можна констатувати, що для симптоматичного лікування невропатичних болів класичні анальгетики є малоефективними. З урахуванням цього застосовують такі медикаменти, як антидепресанти, карбамазепін або валпроат, які взагалі не мають анальгетичної дії щодо не невропатичних болів. Однак, і при такому лікуванні часто не вдається досягти задовільних результатів. Таким чином, існує нагальна потреба в розробленні нових субстанцій для вибіркового лікування невропатичних болів. Метою даного винаходу згідно з цим є одержання субстанції, за допомогою якої можна було б лікувати больові симптоми невропатичних болів. Несподівано було встановлено, що ретигабін формули І має високоефективну дію проти невропатичних болів. Тим самим відкриваються зовсім нові можливості для профілактики й лікування невропатичних болів. Ретигабін і спосіб його одержання відомі (заявка DE 4200259). Ретигабін являє собою похідне неопіоїдного анальгетика флупіртину, який, як було встановлено, поряд із анальгетичною ефективністю має також протисудомну дію. За рахунок оптимізації структури для чіткішого розмежування потрібних (протисудомних) властивостей і небажаних (анальгетичних) ефектів шляхом моделювання з використанням фармакофора вдалося визначити межу між протисудомною і анальгетичною дією субстанцій цього класу. У порівнянні з флупіртином ретигабін має більш сильну протисудомну дію, тоді як ніякого анальгетичного ефекту, що було встановлено на моделях гострого болю, він не виявляє (A. Rostock, С. Tober, С. Rundtfeldt, R. Bartsch, J. Engel, E.E. Polymeropoulos, B. Kutscher, W. Loescher, D. Honack, H.S. White, H.H. Wolf, D-23129: a new anticonvulsant with a broad spectrum activity in animal models of epileptic seizures, Epilepsy Res. 23(3), стор. 211-223 (квітень 1996)). Ретигабін має, як було встановлено на експериментальних моделях нападів епілепсії, широкий спектр дії (С. Tober, A. Rostock, С. Rundfeldt, R. Bartsch, D-23129: a potent anticonvulsant in the amygdala kindling model of complex partial seizures, Eur. J. Pharmacol 303(3), στορ. 163-169 (15 травня 1996)) і проходить у даний час клінічні випробування при лікуванні епілепсії. У деяких публікаціях (наприклад, у заявці ЕР 857065) описано, крім того, застосування ретигабіну для лікування нейродегенеративних захворювань. Авторам даного винаходу вдалося несподіваним чином установити, що ефективна дія ретигабіну проти невропатичних болів залежить від його дозування. Анальгетична ж дія, як і очікувалося і як було встановлено в цій моделі в ранній фазі, виявлялася лише в найменшій мірі, і її можна зіставити з порівняльною субстанцією габапентином. Фармакологічні дослідження Дослідження придушення * гіпералгезії на пацюках на моделі з використанням формаліну У цій моделі тваринам в задню кінцівку з боку підошви підшкірно ін'єкували низькопроцентний розчин формаліну, ви вчаючи при цьому дві фази їхньої поведінкової реакції на викликаний біль (MJ. Field, R.J. Oles, A.S. Lewis, S. McCleary, J. Hughes, L. Singh, Gabapentin (neurontin) and S-(+)-3-isobutylgaba represent a novel class of selective antihyperalgesic agents, Br. J. Pharmacol. 121(8), стор. 1513-1522 (серпень 1997)). Рання фаза, яка продовжувалася максимум до 10-ої хвилини, характеризувалася тим, що тварини безперервно облизували й покусували уражену кінцівку. Пізню тонічну фазу, що настає через 20-60 хв. після ін'єкції, можна охарактеризувати як стадію прояву гіпералгезії. Ця індукована формаліном гіпералгезія включає центральні механізми, ініційовані сенситивністю нейронів у дорсальному розі спинного мозку, яка виникає внаслідок ушкодження тканини або зростаючим активуванням С-аферентних волокон. Field та ін. (1997) установили, що опіоїди в цій моделі неефективні в зазначеній пізній фазі поведінкових реакцій, які виявляються в гіпералгезії. Протисудомний засіб габапентин, на відміну від цього, знижував у залежності від введених доз больові реакції в пацюків. Дослідження з використанням ретигабіну Методика Самців пацюків Sprague Dawley вагою 70-90 г поодинці піддавали відповідній адаптації і спостерігали їх принаймні за 15 хв. до початку досліду. Підшкірна ін'єкція 0,05 мл 2,5% формальдегіду в ізотонічному розчині повареної солі в задню кінцівку з боку підошви викликала сильну негайну реакцію, яка виявлялася в покусуванні й облизуванні протягом декількох хвилин, із наступним переходом у пізню гіпералгезичну фазу, що продовжувалася аж до 60 хв. після ін'єкції формаліну. Реакції, що виявлялися в пізній фазі (починаючи з 10-ої хвилини) (покусування й облизування) є мірою визначення гіпералгезичних реакцій. Ці реакції фіксували протягом 40 хв. через кожні 5 хвилин. Тестовані субстанції вводили перорально за 60 хв. до ін'єкції формаліну. Функцію порівняльної субстанції виконував габапентин. Дослід проводили в групах по 15 тварин. Результати У залежності від доз у 5, 10 і 20 мг/кг, які вводяться перорально, ретигабін придушував відповідно пізню фазу больових реакцій, що позначається як гіпералгезія або невропатичний біль. Дія 10 мг/кг ретигабіну відповідала приблизно ефекту, який досягається при пероральному введенні габапентину в дозуванні 60 мг/кг (див. таблицю). Як і при використанні габапентину, ефективність дії в ранній фазі болю, тобто анальгетична дія, виявлялася лише в незначній мірі. Так, зокрема, число больових реакцій у ранній фазі в контрольної групи досягало в цілому 35, а в пізній фазі 30. При використанні ж ретигабіну число больових реакцій у ранній фазі в залежності від введених доз знижувалося до 32, 25 і 18 відповідно, тоді як у пізній фазі цей показник становив максимум 5, а в деяких випадках больові реакції практично взагалі не спостерігалися. При використанні габапентину число больових реакцій у ранній фазі також знижувалося лише до 27, тоді як у пізній фазі цей показник становив менше 6. Таблиця Е фект дії ретига біну на гіпералгезію пацюків після перорального вв едення Оброблення 1 2 3 4 5 Час Розчинник без актив ної су бстанції Ретигабін Ретигабін Ретигабін Габапентин Д оза мг/кг Су ма пов едінков их реакцій у середньому через кожні 5 хв ., починаючи з моменту вв едення формаліну (середній показн ик ±станда ртне в ідхилення) 5 10 15 20 25 30 35 40 35,3±2,76 14,9±7,00 5,0 10,0 20,0 60,0 31,9±5,46 25,1**±6,42 17,6**±8,52 ++ 26,5 ±6,12 5,33**±6,43 2,5**±2,78 0,9**±1,81 ++ 4,6 ±4,53 24,0±7,78 30,1±3,91 28,9±7,08 23,9±7,90 23,8±7,61 17,5±11,40 9,9**±8,51 26,4±6,63 21,1±6,15 20,6±7,85 14,5*±7,80 10,9±8,98 5,6**±3,46 12,9**±8,49 16,5**±10,49 8,8**±8,91 8,4**±8,47 8,3*±7,29 5,4**±8,47 12,5**±8,83 9,3**±9,18 9,0**±8,70 7,9**±5.91 2,9**±3,36 ++ ++ ++ ++ + 4,5 ±5,76 12,4 ±7,11 11,5''±7,27 8,4 ±7,76 6,8 ±8,76 5,6 ±9,21 Статистично значимі розбіжності при використанні ретигабіну в порівнянні з групою, обробленою розчинником без активної субстанції, визначали дисперсійним аналізом за нижченаведеним критерієм Уїльямса (*р
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of retigabin for treatment of neuropathic pain
Автори англійськоюDost Rita
Назва патенту російськоюПрименение ретигабина для лечения невропатических болей
Автори російськоюДост Рита
МПК / Мітки
МПК: A61K 31/27, A61P 25/00
Мітки: застосування, болів, лікування, ретигабіну, невропатичних
Код посилання
<a href="https://ua.patents.su/5-72550-zastosuvannya-retigabinu-dlya-likuvannya-nevropatichnikh-boliv.html" target="_blank" rel="follow" title="База патентів України">Застосування ретигабіну для лікування невропатичних болів</a>
Попередній патент: Зцентрований подвійний карданний шарнір
Наступний патент: Пристрій для зберігання радіоактивних матеріалів
Випадковий патент: Спосіб механізованого скошування комишу









