Спосіб обробки води
Номер патенту: 76675
Опубліковано: 15.08.2006
Автори: Шевченко Валерій Васильович, Клименко Ніна Сергіївна, Синівський Володимир Георгієвич, Шевчук Олександр Володимирович, Вортман Марина Яківна
Формула / Реферат
Спосіб обробки води видаленням та розділенням іонів полівалентних металів шляхом обробки води комплексоутворювачем, ультрафільтрацією та одержанням суміші іонів металів, розділенням їх зміною рН з подальшою ультрафільтрацією для переходу окремих металів в пермеат, який відрізняється тим, що як комплексоутворювач використовують олігоуретанбіссаліцилат структурної формули:
R’-NH-CO-NH-R-NH-CO-(-CH2-CH2-O-)x-CO-NH-R-NH-CO-NH-R’,
де
R означає 2,4-2,6 С6Н3СН3,
R’ означає
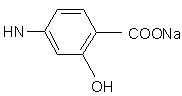 або
або 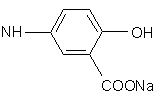 ,
,
або
R’-O-CO-NH-R-NH-CO-(-CH2-CH2-O-)x-CO-NH-R-NH-CO-O-R’,
де
R означає 2,4-2,6 С6Н3СН3,
R’ означає
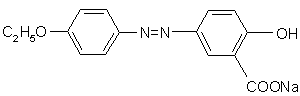 ,
,
Х = 13, 32, 90,
ММ = 1240-4710.
Текст
Спосіб обробки води видаленням та розділенням іонів полівалентних металів шляхом обробки води комплексоутворювачем, ультрафільтра цією та одержанням суміші іонів металів, розділенням їх зміною рН з подальшою ультрафільтрацією для переходу окремих металів в пермеат, який відрізняється тим, що як комплексоутворювач використовують олігоуретанбіссаліцилат структурної формули: R’-NH-CO-NH-R-NH-CO-(-CH2-CH2-O-)x-CO-NH-RNH-CO-NH-R’, де R означає 2,4-2,6 С6Н3СН3, R’ означає Винахід належить до способу обробки води шляхом видалення та розділення іонів полівалентних металів та може бути використаний у гідрометалургійній промисловості при очищенні стічних вод гальванічних виробництв, а також в аналітичній хімії для концентрування, розділення та визначення вмісту іонів металів. При очищенні стічних вод різних виробництв, переробці морської води та інших водних розчинів існує проблема селективного видалення цінних компонентів, до яких належать і полівалентні метали. Відомий метод обробки води для її очищення, заснований на використанні осаджуючих неорганічних та деяких органічних реагентів [1]. Для розділення іонів металів у вигляді гідроксидів широко використовують зміну рН розчину. В залежності від добутку розчинності гідроксид ме NH COONa , OH або або R’-O-CO-NH-R-NH-CO-(-CH2-CH2-O-)x-CO-NH-RNH-CO-O-R’, де R означає 2,4-2,6 С6Н3СН3, R’ означає C2H5O N=N C2 OH (13) COONa OH COONa , (19) UA (11) Х=13, 32, 90, ММ=1240-4710. 76675 HN 3 76675 4 талу буде осаджуватися при вищому або нижчому на другий ультрафільтраційний апарат, де мемзначенні рН. Однак, гідроксиди багатьох металів браною затримується тільки полімер, а суміш катіосаджуються при одних і тих же або перекриваюонів проходить у пермеат, який являє собою кончих значеннях рН, наприклад, гідроксиди таких центрат, збагачений іонами полівалентних металів як: Co, Ni, Cu, Pb та Fe. При осадженні металів. До недоліків запропонованого методу металів у вигляді хелатних сполук часто не вдаслід віднести: ється досягти задовільних результатів, оскільки рН 1 - малу ефективність таких полімерних агенвипадання в осад комплексів багатьох металів тів як полівінілпіролідон, поліакриламід, флокулянт перекриваються. В таблиці 1 приведені умови ВА-2 та ВА-212 внаслідок малого ступеня комплеосадження гідроксихінолінатів металів (А) та комксоутворення з іонами полівалентних металів; плексів з N-бензоілфенілгідроксиламіном (Б) [2]. 2 - використовуємий поліетиленполіімін не має селективності щодо окремих полівалентних метаТаблиця 1 лів, що не дозволяє здійснювати їх розділення; 3 - необхідність введення 10-20 - кратного Умови осадження надлишку полімеру в розчин пояснюється неможгідроксихінолінатів металів (рН середовища) ливістю повної участі функціональних груп полімеру в комплексоутворенні внаслідок стеричних труднощів у молекулах полімеру. Метали A, pH Б, рН Завданням цього винаходу є створення ефекFe3+ 2,5-10,0 3,0-5,2 тивного способу обробки води із забезпеченням Co2+, Ni2+ 4,0-13,5 5,2-6,5 видалення та селективного розділення поліваленCu2+ 5,5-13,5 3,5-6,3 тних металів із водних середовищ. Cd2+ 5,0-13,0 5,5-6,5 Вирішення поставленого завдання здійснюMn2+ 6,0-9,0 6,5-7,8 2+ ється тим, що спосіб обробки води видаленням та Pb 8,5-12,5 3,0-6,0 розділенням ионів полівалентних металів з водних розчинів, включаючий обробку вихідного розчину Відомий спосіб обробки води видаленням іонів комплексоутворювачем, ультрафільтрацію з отриметалів з многокомпонентних розчинів, який поєдманням суміші комплексів металів, розділення їх нує в собі комплексоутворення та ультрафільтразміною рН концентрату суміші комплексів з подацію (КОУФ) [3, 4]. льшою ультрафільтрацією для переходу окремих Принцип методу КОУФ полягає в тому, що в металів у пермеат, згідно із запропонованим винарозчин, який містить іони полівалентних металів, ходом, як комплексоутворювачі використовують вводиться високомолекулярний компонент, який олігоуретанбіссаліцилати структурної формули: утворює з ними стійкі комплексні сполуки, що приR’-NH-CO-NH-R-NH-CO-(-CH2-CH2-O-)x-CO-NHводить, як правило, до утворення полімерних комR-NH-CO-NH-R' плексів більших стеричних розмірів, що дозволяє де здійснювати їх виділення (концентрування) з розR=2,4-2,6 С6Н3СН3 чинів на великопористих ультрафільтраційних мембранах з великою продуктивністю. У фільтраті залишаються низькомолекулярні компоненти, які не утворюють комплекси і тому не затримуються ультрафільтраційними мембранами. При цьому відбувається розділення суміші низькомолекулярних сполук, які містять мікрокількості цінних, але важковиділяємих іонів полівалентних металів (перехідних, рідких і рідкоземельних), які необхідно відділити від макрокількості іонів лужних та лужноземельних елементів а також концентрування високомолекулярних комплексів полівалентних металів [4]. Найбільш близьким за технічною суттю до заявляємого винаходу є спосіб обробки води із застосуванням як реагентів водорозчинних полімерів-полівінілпіролідону, поліакриламіду, промислових флокулянтів ВА-2 і ВА-212 та поліетиленполіміну з молекулярною масою 30000 [3]. У вказаному способі обробки води, який містить іони полівалентних металів та інші іони, змішується в реакторі з полімерним водорозчинним реагентом, який утворює комплексні сполуки з полівалентними металами. Підготовлений таким чином розчин подається в ультрафільтраціний апарат, де напівпроникла мембрана затримує тільки полімерний комплекс, вільно пропускаючи в пермеат воду та солі металів, які залишились незв'язаними. Потім комплекс руйнують у регенераторі зміною рН середовища, і потік направляють R'=NH COONa NH OH OH COONa , , R'-O-CO-NH-R-NH-CO-O-(-CH2-CH2-O-)x-CONH-R-NH-CO-O-R' де R= 2,4-2,6 С6Н3СН3 R'=C2H5O N=N OH COONa X=13, 32, 90 MM=1240-4710 Вказані олігоуретанбіссаліцилати, їх властивості та спосіб одержання в літературі не описані. Синтез олігоуретанбіссаліцилатів здійснювали за передполімерним способом. На першій стадії в розплаві реакцією олігооксіетиленгліколю (ОЕГ) молекулярних мас (MM) 500-4000 з подвійним мольним надлишком толуілендіізоціанату (ТДІ) отримували ізоціанатний форполімер (ІФП) з вмістом ізоціанатних груп, близьким до теоретично розрахованого. Потім ІФП обробляють подвійним мольним надлишком 4-аміноабо 5-аміносаліциловими кислотами (АСК), або оксиетилфеніленазосаліциловою кислотою (ОФАСК). Синтез проводять у середовищі органічного розчинника (ДМФА, діоксан) при концентрації розчину 70%. Цільовий продукт виділяли шляхом видалення 5 76675 6 розчинника у вакуумі при 70°С до постійної маси Приклад 2 кінцевого продукту. Використовували олігоуретанбіссаліцилат MM Олігоуретанбіссаліцилати в конденсованому 1296. В 1дм3 суміші, яка містить в 1м3 водного ростані представляють собою тверді речовини або зчину 0,128кг титану, 0,126кг міді, 20,0кг NaCL, в'язкі рідини, розчинні у воді, ДМФА, діоксані та 50,0кг CaCL2, 10,0кг КСl, 10,0кг MgCL2 з рН=6, донерозчинні в ефірі, гексані. дають 7,44кг олігоуретанбіссаліцилату, яка утвоБудову отриманих сполук підтверджували за рює в водному розчині комплекс з іонами міді та допомогою 14-спектрів та функціонального аналізу титану. Потім розчин підлягають ультрафільтрації на кінцеві групи, вміст яких був у всіх випадках на мембрані УАМ-500 при тиску 0,5МПа. Високоміблизьким до теоретично розрахованого. В ІЧнералізований розчин, який містить іони лужних та спектрах присутні смуги валентних коливань СО лужно-земельних металів, на 100% проходить чеуретанової групи при 1680см-1, широка смуга варез мембрану, а концентрат олігоуретабіссаліцилентних коливань NH та ОН груп з максимумом латних комплексів металів затримується в надме3400см-1. мбранному просторі. При цьому коефіцієнт В таблиці 2 подані деякі характеристики викоконцентрування міді становить 19,2, а титану ристаних олігоуретанбіссаліцилатів. 19,6, рН утворення комплексів становить 6,0, рН руйнування комплексу з міддю становить 3,5, а рН, Таблиця 2 необхідне для руйнування комплексу з титаном 0. Характеристики олігоуретанбіссаліцилатів Приклад 3 Використовували олігоуретанбіссаліцилат MM № MM вихід- Тип саліци- MM кінце- Вміст 2196. В умовах прикладу 1 підлягають ультрафіп/п ного оліго- лової кисло- вого про- іонних льтрації 12,66кг олігомеру 3 в суміші, яка містить в етеру ти дукту груп, % 1дм3 водного розчину 0,12кг заліза. 0,542кг урану, 1 500 АСК 1296 11,2 20,0кг NaCL, 50,0кг CaCL2, 10,0кг КС1, 10,0кг 2 1500 АСК 2196 6,10 MgCL2 на мембрані УАМ -200. При цьому коефіці3 1500 ОФАСК 2464 5,43 єнт концентрування заліза становить 19,4, а урану 4 4000 АСК 4680 2,86 -19,2. рН утворення комплексів становить 5,0, рН руйнування комплексу з ураном становить 2,5, рН Для експериментальної перевірки заявляеморуйнування комплексу з залізом - 0,2. го способу було вивчено дію олігоуретанбіссаліПриклад 4. цилатів та їх комплексів на мембранах типу УАМ Використовували олігоуретанбіссаліцилат MM (50, 100, 200, 500) у діапазоні тиску 0,1-0,5МПа. 2464. В умовах прикладу 1 підлягають ультрафіЗаявляємий спосіб підтверджується такими льтрації 7,56кг олігомеру в суміші , яка містить в прикладами, які ні в якому разі не обмежують об1дм3 водного розчину 0,16кг нікелю. 0,126кг титану 20,0кг NaCL, 50,0кг CaCL2, 10,0кг КСl, 10,0кг MgCL2 сяг патентних домагань. Приклад 1 на мембрані УАМ-200. При цьому рН середовища Молекулярна маса використаної олігоуретандорівнює 6,0 концентрація соляної кислоти, яка біссаліцилату MM- 4680. По заявляємому способу необхідна для руйнування комплексу становить обробки води в 1дм3 суміші, яка містить в 1м3 вод0,6моль/дм3, рН руйнування комплексу з міддю ного розчину 0,120кг заліза, 0,126кг міді, 20,0кг 3,5. Коефіцієнт концентрування нікелю - 2,2, титаNaCL, 50,0кг СаСL2, 10,0кг КСl, 10,0кг MgCL2 з ну - 19,8. pH=6, додають 28,1кг олігоуретанбіссаліцилату, Приклад 5 (за прототипом). яка утворює в водному розчині комплекс з іонами 1дм3 суміші відходів калійного виробництва, міді та заліза. Потім розчин підлягають ультрафіяка містить в 1м3 0,00036кг Сu, 0,00033 кг Ni і 174кг льтрації на мембрані УАМ-500 при тиску 0,5МПа. NaCl обробляли 0,5кг поліетиленполііміном при Високомінералізований розчин, який містить іони рН=7,2. Вказаний розчин підлягав ультрафільтралужних та лужноземельних металів, на 100% проції на мембрані УАМ-300 при тиску 0,15Мпа. Конходить через мембрану, а концентрат олігоуретацентрат поліетиленімінних комплексів полівалентбіссаліцилатних комплексів металів затримується них металів затримується в надмембранному в надмембранному просторі, вода залишається просторі, а розчин лужних металів на 100% прохоочищенною. Потім концентрат комплексів міді та дить через мембрану. Потім концентрат комплекзаліза підкисляли ЇМ розчином соляної кислоти у сів міді та нікелю підкислювали 1М розчином сорегенераторі до рН=3,5, при цьому руйнується ляної кислоти до рН=3, що сприяє руйнуванню комплекс міді та безперешкодно фільтрується чеобох комплексів та переходу нікелю та міді в перрез мембрану, потім підкисляли водний розчин меат. Коефіцієнт розділення міді - 17,5, а нікелю соляною кислотою до рН=0,2, при цьому руйнуєть- 17,0. ся комплекс заліза та безперешкодно фільтруєтьЦільові метали вводились у розчин баластних ся через мембрану, суміш катіонів металів пересолей у вигляді хлоридних та нітратних солей. 3 ходить в пермеат, який являє собою концентрат, Концентрація баластних солей в дослідах, кг/м : збагачений іонами полівалентних металів, коефіNaCI - 20,0, CaCl2 - 50,0, KCl - 10,0, MgCl2 - 10,0. У цієнт концентрування заліза становить 19,4, а таблиці 3 наведені ступені видалення іонів поліваміді 19,2. лентних металів із водних розчинів. 7 76675 8 Таблиця 3 Ступені видалення ионів полівалентних металів із водних розчинів № п/п 1 2 3 4 5 Склад вихідної води, г/л Fe3+=0,12 Сu2+=0,176 Сu2+=0,176 ТiO2+=0,128 Fe3+=0,12 UO22+=0,542 Ni2+=0,16 ТіО2+=0,176 Fe3+=0,00012 Cu2+=0,000176 Вміст іонів металів, % Cu2+ ТіО2+ UO22+ Олігоуретан біссаліцилат рН зразка Fe3+ 1 6,0 95-98 94-97 2 6,0 95-97 96-98 3 5,0 95-98 93-96 4 6,0 97-98 Поліетиленполіїмін 6,0 96-99 Як видно з даних таблиці, ступінь видалення іонів полівалентних металів Fe3+, Cu2+, TiO2+, UC22+ за допомогою синтезованих олігоуретанбіссаліцилатів становить 93-99%. Ni2+ 96-97 У таблиці 4 наведені дані по затримці ионів полівалентних металів на ультрафільтраційних мембранах, їх вміст в концентраті після руйнування комплексів, рН руйнування комплексів, а також коефіцієнт концентрування. Таблиця 4 Дані по затримці іонів полівалентних металів № п/п 1 2 3 4 5 6 Тип та вміст Вміст іонів, кг/м3 РН руйнуолігоуретан- Тип мем- рН вихідКк, коефіцієнт Метал вання комв концентрабіссаліцилату, брани ної суміші вихідне концентрування плексу ті кг/м3 Fe, 0,120 2,33 19,4 0,2 28,1 УАМ-500 6,0 Сu 0,126 2,42 19,2 3,5 Ті, 0,128 2,51 19,6 0,0 7,44 УАМ-100 6,0 Сu 0,126 2,46 19,5 3,5 Fe, 0,120 2,31 19,3 0,2 12,6 УАМ-200 5,0 U 0,542 10,5 19,2 2,5 Ni, 0,120 2,34 19,5 0,2 7,56 УАМ-100 5,0 Ті 0,542 10,5 10,4 2,5 Fe, 0,128 2,33 19,1 3,0 14,25 УАМз-200 6,0 U 0,128 2,48 19,4 0,0 Прототип. - калійні виробництва ( P=0,15Мпа; Kv=18) Си , 0,0036 0,063 17,5 3,0 ПоліетиленNi , УАМ-300 7,2 0,0033 0,056 17,5 поліімін 0,5 3,0 Na 177 177 1,0 Тиск при проведеному експерименті Р=0,5МПа, Кv=20. Кк - коефіцієнт концентрування, співвідношення вмісту металу в концентраті і у вихідному розчині. Кv - коефіцієнт зменшення об'єму, співвідношення об'єму, вихідного розчину і концентрату. Вміст металів у пробах визначали абсорбційним методом на спектрофотометрі "Сатурн" з приставкою "Графік". Порівнювальний аналіз із прототипом показує, що завдяки реалізації вищенаведеної структурної формули дані олігоуретанбіссаліцилати утворюють комплекси із іонами полівалентних металів, константи стійкості яких відрізняються один від одного. Це дозволяє послідовно змінюючи кислотність концентрату, селективне виділяти цільові йони полівалентних металів. Таким чином, з наведених прикладів та даних таблиць 3 та 4 слід зробити висновок, що олігоу ретанбіссаліцилати утворюють стійкі комплекси з Fe2+, Cu2+, UO22+, ТiO2+, Ni2+ та інш. За даними спектроскопії комплекси з залізом мають максимум поглинання у видимій області спектру 490нм, а дослідження спектрів ЕПР показує, що залізо у комплексі має координаційне число 6 та до складу координаційної сфери входять атоми О та N. При ультрафільтрації розчинів комплексів олігоуретанбіссаліцилатів з іонами полівалентних металів, спостерігається незначне збільшення затримки комплексів з підвищенням тиску. Параметри ультрафільтрації, рН утворення та руйнування комплексів подані в таблиці 4. Слід зазначити, що, представлені полімери показують, що даний спосіб легко здійснюється на сучасному обладнанні та може бути використаний в гідрометалургійній промисловості, при очищенні стічних вод гальванічних виробництв, а також у 9 76675 10 аналітичній хімії для концентрування, розділення 3. Дытнерский Ю.И. Баромембранные процеста визначення вмісту іонів металів. сы. М.. «Химия», 1986, 272С. Література: 4. Дытнерский Ю.И., Жилин Ю.Н., Волчек К.Ф. 1. Темкина В.Я, Дятлова Н.М., Колпакова И.Д. Концентрирование переходных металлов в многоКомплексоны. М. «Химия» 1970, 415С. компонентных растворах. комплексообразованием 2. Брык М.Т, Цапюк Е.А. Ультрафильтрация. К. и ультрафильтрацией // Химия и технология воды. «Наукова думка», 1989, 320С. - 1984. - 6.- №5.- С.401-408. Комп’ютерна верстка Н. Лисенко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for water treatment
Автори англійськоюVortman Maryna Yakivna, Klymenko Nina Serhiivna, Shevchenko Valerii Vasyliovych, Shevchuk Oleksandr Volodymyrovych
Назва патенту російськоюСпособ обработки воды
Автори російськоюВортман Марина Яковлевна, Клименко Нина Сергеевна, Шевченко Валерий Васильевич, Шевчук Александр Владимирович
МПК / Мітки
МПК: C02F 1/64, C02F 1/62, C02F 1/58
Код посилання
<a href="https://ua.patents.su/5-76675-sposib-obrobki-vodi.html" target="_blank" rel="follow" title="База патентів України">Спосіб обробки води</a>
Попередній патент: Олігоуретанбіссаліцилати як комплексоутворювачі іонів полівалентних металів
Наступний патент: Стенд для очищення центрових для сифонного розливу сталі
Випадковий патент: Склад для обробки рулонних скловолокнистих матеріалів









