Спосіб одержання похідних циклогексанолу
Номер патенту: 78511
Опубліковано: 10.04.2007
Автори: Кім Кеун-Сік, Лі Сунг-Воо, Парк Дзін-Соо, Чай Кі-Байунг, Кім Кванг-іл
Формула / Реферат
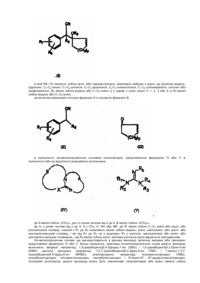
1. Спосіб одержання похідних циклогексанолу формули І
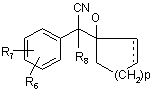 ,(I)
,(I)
в якій R6 і R7 являють собою орто- або паразамісники, незалежно вибрані з групи, що складається з водню, гідроксилу, С1-С6 алкілу, С1-С6 алкокси, С7-С9 аралкокси, С2-С7 алканоїлокси, С1-С6 алкілмеркапто, галогену або трифторметилу; R8 являє собою водень або С1-С6 алкіл; р є одним з цілих чисел 0, 1, 2, 3 або 4; a R9 являє собою водень або С1-С6 алкіл;
що включає взаємодію сполуки формули II із сполукою формули III
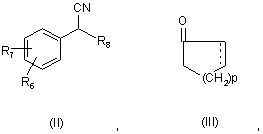
у присутності неметалоорганічних основних каталізаторів, представлених формулою IV або V
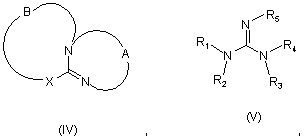
в якій А являє собою -(СH2)n-, де n є цілим числом від 2 до 4; В являє собою -(CH2)m-, де m є цілим числом від 2 до 5; Х являє собою СН2, О, NH або NR', де R' являє собою С1-С4 алкіл або ацил, або алкілнесучий полімер; кожний з R1-R4 незалежно являє собою водень, алкіл, циклоалкіл, або алкіл- або циклоалкілнесучий полімер, і всі від R1 до R4 не є воднем, a R5 є алкілом, циклоалкілом або алкіл- або циклоалкілнесучим полімером, і де R9 являє собою алкіл, причому алкільну групу вводять алкілуванням.
2. Спосіб за п. 1, в якому сполука формули II являє собою п-метоксифенілацетонітрил.
3. Спосіб за п. 1, в якому сполука формули III являє собою циклогексанон.
4. Спосіб за будь-яким з пп. 1-3, в якому неметалоорганічний основний каталізатор є сумішшю каталізаторів, вибраних з одного або більше амідинів або гуанідинів формули (IV) або (V).
5. Спосіб за будь-яким з пп. 1-4, в якому основний каталізатор є або гомогенним, або іммобілізованим на полімерному носії.
6. Спосіб за будь-яким з пп. 1-5, в якому неметалоорганічну основу вибирають з групи, що складається з 1,8-діазабіцикло[5.4.0]ундец-7-ену (DBU), 1,5-діазабіцикло[4.3.0]нон-5-ену (DBN), 1,5,7-триазабіцикло[4.4.0]дец-5-ену (TBD), 7-метил-1,5,7-триазабіцикло[4.4.0]дец-5-ену (MTBD), тетраметилгуанідину (TMG) і N'-бутил-N'',N''-дициклогексилгуанідину.
7. Спосіб за будь-яким з пп. 1-6, в якому кількість неметалоорганічної основи, що використовують, знаходиться в інтервалі від близько 0,005 до близько 0,5 еквівалентів відносно одного еквівалента сполуки формули II.
8. Спосіб за будь-яким з пп. 1-7, в якому не використовують розчинник.
9. Спосіб за будь-яким з пп. 1-7, в якому взаємодію сполуки формули ІІ з сполукою формули ІІІ проводять в присутності розчинника.
10. Спосіб за будь-яким з пп.1-9, в якому температура реакції знаходиться в інтервалі від близько -20°С до 80°С.
11. Спосіб за п. 10, в якому температура реакції знаходиться в інтервалі від близько 10°С до 30°С.
12. Спосіб за будь-яким з пп. 1-11, в якому сполуки формул II і III і основні каталізатори використовують в еквівалентних співвідношеннях 1:1~1,5:0,05~0,5.
Текст
Даний винахід відноситься до способу одержання похідних циклогексанолу таких, як 1-[ціано(4метоксифеніл)метил]циклогексанол. Стан області техніки, що відноситься до проблеми Похідні циклогексанолу такі, як 1-[ціано(4-метоксифеніл)метил]циклогексанол, являють собою корисні проміжні сполуки для одержання сполук типу венлафаксину, які володіють антидепресантним ефектом за рахунок інгібування повторного поглинання нейромедіаторів, норепінефріну і серотоніну. Як описано в патенті США № 4535186, похідні циклогексанолу можна одержати шляхом взаємодії циклоалканону або циклоалкенону з аніоном відповідним чином заміщеного (орто або пара) фенілацетонітрилу. Спосіб одержання, описаний в патенті США № 4535186, включає використання металоорганічної основи такої, як н-бутиллітій, для утворення в даній реакції аніону фенілацетонітрилу. Металоорганічна основа є дорогою, повинна використовуватися в кількості, щонайменше, одного еквівалента реагенту при низькій температурі нижче за -50°С, звичайно чутлива до вологи повітря з ризиком займання або вибуху, і дає низький вихід продукту, менше за 50 процентів. Тому металоорганічні основи вважаються незручними для синтезу в промисловому масштабі. У патенті США № 5043466 описаний спосіб одержання похідних циклогексанолу, в якому використовують металоорганічну основу таку, як діізопропіламід літію, що показано наступним механізмом реакції. У патенті США № 5043466 змінюють пропорцію змішування вуглеводневих розчинників, намагаючись поліпшити температуру і ви хід реакції, але проблема, пов'язана з основою все ж залишається, причому діізопропіламід літію незручний для синтезу в промисловому масштабі, оскільки він є дуже дорогим, складним в поводженні і може стати причиною виникнення пожежі або вибуху. У китайській патентній публікації № 1225356 (CNO1225356A) описано використання таких основ, як метилат натрію, етилат натрію, гідрид натрію і амід натрію для одержання похідних циклогексанолу, щоб підвищити температуру реакції до інтервалу від 0 до 5°С. Однак, описані основи використали в кількостях, щонайменше, одного еквівалента реагенту і, крім того, вони небезпечні, оскільки також схильні до зайнмання або вибуху. Приведені вище відомі способи складаються з двох стадій, тобто взаємодії фенілацетонітрилу з основою для утворення аніону і приєднання даного аніону до кетонної сполуки. Зокрема, реакція на стадії утворення аніону включає деякі складності відносно кінцевої точки даної стадії і кількісного аналізу одержаного аніону. Подібні проблеми приводять до коливань виходу на стадії приєднання і, таким чином, з цієї причини вони також складні для промислового використання. Відповідно, даний винахід спрямований на спосіб одержання похідних циклогексанолу, який значною мірою долає труднощі і недоліки звичайної області техніки. Метою даного винаходу є надання способу одержання похідних циклогексанолу шля хом взаємодії фенілацетонітрилу з циклогексанолом, щоб зробити можливим економічне і розумне промислове масове виробництво. Наступна мета даного винаходу полягає в наданні способу одержання похідних циклогексанолу, який є безпечним і сприятливим по відношенню до навколишнього середовища без ризику пожежі або вибуху, і більш простим, ніж звичайні синтези, оскільки всі реагенти змішують в одній реакції. Одним з аспектів даного винаходу є спосіб одержання похідних циклогексанолу формули І, в якій R6 і R7 являють собою орто- або паразаступники, незалежно вибрані з групи, що включає водень, гідроксил, С1-С6 алкил, С1-С6 алкокси, С7-С9 аралкокси, С2-С7 алканоїлокси, С1-С6 алкілмеркапто, галоген або трифторметил; R8 являє собою водень або С 1-С6 алкіл; ρ є одним з цілих чисел 0, 1, 2, 3 або 4; a R9 являє собою водень або С1-С6 алкіл; що включає взаємодію сполуки формули II із сполукою формули III, в присутності не-металоорганічних основних каталізаторів, представлених формулою IV або V, в присутності або за відсутності реакційного розчинника, де А являє собою -(СН2)n-, де n є цілим числом від 2 до 4; В являє собою -(СН2)m-, де m є цілим числом від 2 до 5; X є СН2, О, NH або NR', де R' являє собою С1-С4 алкіл або ацил, або алкілнесучий полімер; кожний з R1 до R4 незалежно являє собою водень, алкіл, циклоалкіл, або алкіл- або циклоалкілнесучий полімер, і всі від R1 до R4 не є воднями, R5 є алкілом, циклоалкілом або алкіл- або циклоалкіл-несучим полімером, і де R9 являє собою алкіл, причому алкільна група вводиться алкілуванням. He-металоорганічна основа, що використовується в даному винаході, включає амідини або гуанідини, представлені формулою IV або V. Більш конкретно, приклади не-металоорганічних основ даного винаходу включають амідини, наприклад, 1,8-діазабіцикло[5.4.0]ундец-7-ен (DBU) і 1,5-діазабіцикло[4.3.0]нон-5-ен (DBN); циклічні гуанідини, наприклад, 1,5,7-триазабіцикло[4.4.0]дец-5-ен (TBD) і 7-метил-1,5,7триазабіцикло[4.4.0]дец-5-ен (MTBD); алкілгуанідини, наприклад, тетраметилгуанідин (TMG), тетрабутилгуанідин, пентаметилгуанідин, пентабутилгуанідин і N'-6yraii-N", N"-дициклогексилгуанідин. Основний каталізатор даного винаходу може бути гомогенним каталізатором або може являти собою каталізатор, що містить органічну амінну основу на основі амідину або гуанідину, іммобілізовану на полімерному носії (наприклад, полістиролі), або неорганічному носії (наприклад, оксиді кремнію). Heметалоорганічна основа даного винаходу являє собою, щонайменше, одну основу, вибрану з групи, що складається із згаданих ви ще основ. Кількість не-металоорганічної основи, що використовується спеціально не обмежена і може знаходитися в інтервалі від близько 0,0001 до близько 2 еквівалентів, а більш переважно, від близько 0,005 до близько 0,5 еквівалентів відносно одного еквівалента сполук формули II. Реакцію даного винаходу можна успішно здійснити при використанні основних каталізаторів лише в каталітичній кількості, що є переважним. У даному винаході можна за вибором не використовувати органічний розчинник, що включає вуглеводні або прості ефіри, які потрібні при звичайному синтезі. Використовувати органічний розчинник чи ні, оптимально вирішується фахівцем в даній області, але звичайно вважають за краще не використовувати органічний розчинник. При одержанні похідних циклогексанолу таких, як 1-[ціано(4-метоксифеніл)метил]циклогексанол, представлених формулою І, відповідно до даного винаходу, температура реакції переважно знаходиться в інтервалі від близько -20 до 80°С, більш переважно, від близько 10 до 30°С. Спосіб даного винаходу можна здійснювати навіть при кімнатній температурі, що є переважним. Даний винахід являє собою спосіб одержання похідних циклогексанолу шляхом взаємодії відповідним чином заміщеного парафенілацетонітрилу і циклогексанону в присутності не-металоорганічної амінної основи (наприклад, DBU, DBN, TBN, MTBD, TMG або N'-6yTmi-N", N''-дициклогексилгуанідину) відповідно до механізму реакції І. У приведеній вище реакції R6-R9 і ρ такі, як визначено вище, а де R9 є алкілом, його вводять алкілуванням. При одержанні похідних циклогексанолу таких, як 1-[ціано(4-метоксифеніл)метил]циклогексанол, представлених формулою І, для утворення аніону фенілацетонітрилу використовують не-металоорганічну основу таку, як DBU, DBN, TBD, MTBD, TMG або N'-6yrmi-N", N''-дициклогексилгуанідин, що являє собою амінну основу, замість металоорганічної основи такої, як н-бутиллітий або діізопропіламід літію, що використовуються в звичайних способах. Використання не-металоорганічної основи у відносно невеликій кількості, яка порівняно недорога, менш чутлива до гідратації, з якою можна працювати при кімнатній температурі, без ризику пожежі або вибуху, дає можливість здійснювати виробництво в промисловому масштабі за допомогою безпечного і відносно простого промислового способу. Лише каталітичні кількості неметалоорганічної основи потрібні в даному винаході, згідно з яким одержують похідні циклогексанолу високої чистоти, з високим виходом. Крім того, даний винахід є більш простим і сприятливим по відношенню до навколишнього середовища, не приводить до металоорганічних побічних продуктів, оскільки в ньому уникають використання органічних розчинників. Тепер даний винахід буде детально описаний з посиланням на наступні приклади, які не призначені для обмеження об'єму даного винаходу. Приклад 1 У колбу вміщували 100г (0,68 моль) п-метоксифенілацетонітрилу, 100г (1,02 моль) циклогексанону і 32г (0,21 моль) 1,8-діазабіцикло[5.4.0]ундец-7-ену (DBU) і витримували при 15-20°С при перемішуванні протягом 48 годин. Потім до одержаного розчину додавали 1н НС1 для доведення рН до кислого рівня. Після однієї години перемішування при кімнатній температурі осад, що утворювався, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 140г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 84%, температура плавлення 123,7°С). Аналіз 1Н ЯМР (ДМС О-сіб): δ 7,27-6,93 (4Н, кв, ароматичні), 4,85 (1Н, с, ОН), 4,05 (3Н, с, ОСН3), 3,76 (1Н, с, CHCN), 1,69-1,08 (10Н, м, циклогексил) Аналіз 1ЯМР (CDC13): δ 7,23-6,89 (4Н, кв, ароматичні), 3,82 (ЗН, с, ОСН3), 3,73 (1Н, с, CHCN), 1,72-1,16 (10Н, м, циклогексил) Аналіз 13СЯМР (ДМСО-ёб): δ 159,4, 131,3, 125,8, 121,4, 114,1, 72,2, 55,8, 48,8,36,0,34,7,25,9,22,0,21,9 Mac-спектральний аналіз: молекулярна маса 245 [М^за C.I.M.S.] ІЧ (таблетка КВг): 3408 см -1 (-ОН), 2249 см -1 (- CN) Приклад 2 У колбу вміщували 52,7г (0,36 моль) п-метоксифенілацетонітрилу, 35,8г (0,36 моль) циклогексанону і 28,6г (0,19 моль) 1,8-діазабіцикло[5.4.0]ундец-7-ену і витримували при 15-20°С при перемішуванні протягом 90 годин. Потім до одержаного розчину додавали 1н НС1 для доведення рН до кислого рівня. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 62 г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 70%). Приклад 3 Дії здійснювали аналогічно тим, як описано в прикладі 1, за винятком того, що використали 0,5 еквіваленту 1,8-діазабіцикло[5.4.0]ундец-7-ену в 6-денній реакції, одержуючи 67 г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 80%). Приклад 4 У колбу вміщували 100г (0,68 моль) п-метоксифенілацетонітрилу, 167г (1,70 моль) циклогексанону і 52г (0,34 моль) 1,8-діазабіцикло[5.4.0]ундец-7-ену і витримували при 0°С при перемішуванні протягом 60 годин. Потім до одержаного розчину додавали 1н НС1 для доведення рН до кислого рівня. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 147г білої твердої речовини як цільової сполуки, 1-[щано(4-метоксифеніл)метил]циклогексанолу (вихід 88%). Приклад 5 Дії здійснювали аналогічно тим, як описано в прикладі 1, за винятком того, що використали 0,5 еквіваленту 1,8-діазабіцикло[5.4.0]ундец-7-ену в 8-годинній реакції, одержуючи 116г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 70%). Приклад 6 У колбу вміщували 25,4г (0,17 моль) п-метоксифенілацетонітрилу, 41,8г (0,42 моль) циклогексанону і 13,2г (0,087 моль) 1,8-діазабіцикло[5.4.0]ундец-7-ену і витримували при 25°С при перемішуванні протягом 24 годин. Потім до одержаного розчину додавали 1н НС1 для доведення рН до кислого рівня. Після додання 50 мл метилового спирту і однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 23,7 г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 56,1%). Приклад 7 У колбу вміщували 50,3г (0,34 моль) п-метоксифенілацетонітрилу, 34,8г (0,35 моль) циклогексанону і 43,3г (0,35 моль) 1,5-діазабіцикло[4.3.0]нон-5-ену (DBN) і витримували при 20-25°С при перемішуванні протягом 90 годин. До одержаного розчину додавали 50мл метилового спирту і 200мл очищеної води. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 116г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (вихід 70%). Приклад 8 У колбу вміщували 20г (0,14 моль) п-метоксифенілацетонітрилу, 13,7г (0,14 моль) циклогексанону і 21,2г (0,14 моль) 1,8-діазабіцикло[5.4.0]ундец-7-ену, розбавляли 100 мл метилового спирту і витримували при 1520°С при перемішуванні протягом 20 годин. До одержаного розчину додавали 20 мл метилового спирту і 150 мл очищеної води. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 17,4г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (вихід 52%). Приклад 9 Дії здійснювали аналогічно тим, як описано в прикладі 1, за винятком того, що використали 0,1 еквіваленту 1,8-діазабщикло[5.4.0]ундец-7-ену в 6-денній реакції, одержуючи 76,1 г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 90,5%). Приклад 10 У колбу вміщували 25,4г (0,17 моль) п-метоксифенілацетонітрилу, 83,6г (0,85 моль) циклогексанону і 26,7г (0,17 моль) 1,8-діазабіцикло[5.4.0]ундец-7-ену і витримували при 20-25°С при перемішуванні протягом 24 годин. До одержаного розчину додавали 50мл метилового спирту і 200мл очищеної води. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 18,0г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 42,6%). Приклад 11 Дії здійснювали аналогічно тим, як описано в прикладі 1, за винятком того, що температур у реакції підтримували в інтервалі від 35 до 40°С, одержуючи 30,6г білої твердої речовини як цільової сполуки, 1[ціано(4-метоксифеніл)метил]циклогексанолу (вихід 36,8%). Приклад 12 У колбу вміщували 100 г (0,68 моль) п-метоксифенілацетонігрилу, 100 г (1,02 моль) циклогексанону і 0,47 г (0,0034 моль) 1,5,7-триазабіцикло[4.4.0]дец-5-ену (TBD) і витримували при 20-25°С при перемішуванні протягом від 10 до 12 годин. До одержаного розчину додавали 1н НС1 для доведення рН до кислого рівня. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 128 г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (ви хід 77%). Приклад 13 Дії здійснювали аналогічно тим, як описано в прикладі 1, за винятком того, що використали 0,03 еквіваленту 7-метил-1,5,7-триазабіцикло[4.4.0]дец-5-ену (MTBD) в 20-22-годинній реакції, одержуючи 128 г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил]циклогексанолу (вихід 77%). Приклад 14 У колбу вміщували 50г (0,34 моль) п-метоксифенілацетонітрилу, 50г (0,51 моль) циклогексанону і 0,24г (0,0017 моль) 1,5,7-триазабіцикло[4.4.0]дец-5-ену (TBD) і витримували при 20-25°С при перемішуванні протягом 19 годин. Реакційну суміш розчиняли в 500мл етилацетату і, після додання 200мл очищеної води, нейтралізовували 6н НС1. Після розділення фаз при 30-35°С, органічний розчинник видаляли у вакуумі, а до фільтрату додавали 500мл етилацетату і 200мл очищеної води. Після однієї години перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 74г білої твердої речовини як цільової сполуки, 1-[ціано(4метоксифеніл)метил]циклогексанолу (ви хід 89%). Приклад 15 У колбу вміщували 25г (0,17 моль) п-метоксифенілацетонітрилу, 25г (0,25 моль) циклогексанону і 2,5г (0,0090 моль) N'-6yTmi-N", N"-дициклогексилгуанідину і витримували при 20-25°С при перемішуванні протягом 24 годин. До одержаного розчину додавали 1н НС1 для доведення рН до кислого рівня. Після одного часу перемішування при кімнатній температурі осад, що утворився, відділяли фільтруванням і промивали очищеною водою, потім етилацетатом і н-гексаном, одержуючи 30г білої твердої речовини як цільової сполуки, 1-[ціано(4-метоксифеніл)метил] циклoгeксанолу (вихід 72%). Порівняльний приклад 1 50г (0,34 моль) п-метоксифенілацетонітрилу розбавляли 250 мл сухо го тетрагідрофурану (ТГФ) і охолоджували до -70°С в атмосфері азоту. До одержаного розчину додавали по краплях 210 мл (0,34 моль) нбутиллітію (п-BuLi), підтримуючи температуру розчину нижче за -50°С. Після цього розчин перемішували протягом 30 хвилин і, після додання 50г (0,51 моль) циклогексанону, перемішували ще 45 хвилин, в той час як температуру розчину підтримували нижче за -50°С. Після цього температуру реакційного розчину підняли до 0°С і додали насичений розчин хлориду амонію, щоб спричинити розділення фаз. Водний шар екстрагували діетиловим ефіром і об'єднували з органічним шаром. Потім органічний розчинник видаляли при зниженому тиску, одержуючи 25,2г цільової сполуки, 1-[щано(4-метоксифеніл)метил]циклогексанолу (ви хід 34,2%). Температура плавлення: від 123 до 126°С. Mac-спектральний аналіз: молекулярна маса 245 [М+за C.I.M.S] Аналіз:1ЯМР (ДМСО-сіб): δ 7,32, 6,95 (4Н, кв, п-заміщена ароматика), 3,8 (ЗН, с, ОСНз), 3,76 (Ш, C.CHCN), 1,56 (10Н, м, аліфатичний циклогексил) Порівняльний приклад 2 Підтримуючи вн утрішню температуру нижче за 10°С, 76,5г п-метоксифенілацетонітрилу, розбавленого 75мл толуолу, повільно додавали до розчину діізопропіламіду літію, одержаного при доданні 73мл діізопропіламіну до 325мл 6М BuLi і 300мл толуолу в атмосфері азоту. Після 30 хвилин перемішування повільно додавали 46,0 г циклогексанону, розбавленого 50 мл толуолу, підтримуючи вн утрішню температуру нижче за 10°С, і перемішували ще близько 30 хвилин. Після цього одержаний розчин додавали до 100мл водного розчину 12н НС1 і 1 л холодної очищеної води. Після фільтрування фільтрат розбавляли хлористим метиленом і промивали очищеною водою. Замінивши хлористий метилен на діізопропіловий ефір, розчинник видаляли при зниженому тиску, фільтрат охолоджували і фільтрували, одержуючи 91,0 г білої твердої речовини як цільової сполуки, 1-[ціано(4метоксифеніл)метил]циклогексанолу (ви хід 79%). Посилальний приклад 12г (0,05 моль) 1-[ціано(4-метоксифеніл)метил]циклогексанолу, одержаного в прикладі 1, розчиняли в 250мл суміші аміаку і етанолу при співвідношенні змішування 2:8 (об./об.) і додавали 2,8г 5%-ного родію на оксиді алюмінію, щоб викликати реакцію гідрування. Каталізатор відфільтровували і промивали етанолом, фільтрат концентрували при зниженому тиску, одержуючи сполуку у вигляді масла, яке потім розбавляли 100мл толуолу і підкислювали до рН 2. Після фільтрування одержували 9г білої твердої речовини як цільової сполуки, 1-[2-аміно-1-(4-метоксифеніл)етил]циклогексанолу (вихід 57%). Температура плавлення: від 168 до 172°С. Mac-спектральний аналіз: молекулярна маса 250 [М+за C.I.M.S] Аналіз 1НЯМР (ДМСО-сіб): δ 7,85 (ЗН, с, ΝΗ3+), 3,75 (ЗН, с, ОСН3), 3,20 (ЗН, м, СНСН2), 1,35 (10Н, м, аліфатичний циклогексил) Як описано вище, в даному винаході наданий безпечний і відносно простий спосіб виробництва в промисловому масштабі похідних циклогексанолу таких, як 1-[ціано(4-метоксифеніл)метил]циклогексанол, згідно з формулою І. Даний винахід застосовує дійсно недорогу, не-металоорганічну основу в невеликих кількостях, яка є сприятливою по відношенню до навколишнього середовища і дозволяє уникнути використання органічних розчинників, для одержання 1-[ціано(4-метоксифеніл)метил]циклогексанолу високої чистоти з високим виходом .
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for the preparation of cyclohexanol derivatives
Назва патенту російськоюСпособ получения производных циклогексанола
МПК / Мітки
МПК: C07C 253/30, C07B 61/00, C07C 255/37
Мітки: одержання, циклогексанолу, спосіб, похідних
Код посилання
<a href="https://ua.patents.su/5-78511-sposib-oderzhannya-pokhidnikh-ciklogeksanolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних циклогексанолу</a>
Попередній патент: Будівельний модуль і спосіб зведення стін споруди із застосуванням цих модулів
Наступний патент: Шпала ш-1-1-prs
Випадковий патент: Структурний металокерамічний композиційний матеріал (варіанти) та спосіб виготовлення цього матеріалу (варіанти)