Спосіб одержання акриламідного полімеру
Текст
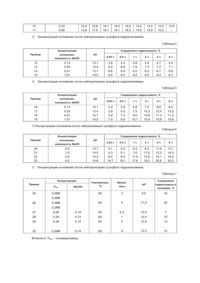
Изобретение относится к синтезу с гидроксамовыми группами, применяемыми при образовании комплексов железа, они оказывают благоприятное влияние на буровые растворы. Указанные полимеры применяют также в качестве флокулянтов. Известен способ получения этих полимеров путем взаимодействия гидроксиламина с полиакриламидом в водном растворе при температуре 50-80°С и значении рН 6,2-6,8 (Патент США 4587306, кл.525-354, опубл. 1986г.). Отмечено, что этот температурный интервал является оптимальным для минимизации разложения гидроксиламина при сохранении скорости реакции в разумных пределах. Утверждается, что указанный интервал значений рН соответствует высокой скорости реакции. Использованные примеры имеют молекулярный вес в пределах 1000-20000. Известен способ получения гидроксаматных полимеров взаимодействием гидроксиламина с полиакриламидом при температуре 90°С с использованием ацетата натрия в качестве буфера (заявка Франции 2476113, кл. С09К7/02, опубл. 1981г.). В известных способах по мере уменьшения концентрации гидроксиламина пропорционально снижаются скорость реакции и эффективность конверсии гидроксиламина в гидроксаматную группу. Таким образом, при низких концентрациях гидроксиламина, которые испытывались при гидроксамации полимеров, особенно в случае высокомолекулярных соединений, скорость реакции и эффективность использования гидроксиламина являются критическими параметрами, определяющими коммерческий успех процесса. В литературе имеются многочисленные публикации, касающиеся исследования кинетики реакции гидроксиламина с мономерными амидами такими, как ацетамид, формамид, ацетанилид (W.P. Jenks & Магу Gifchrist, "J.Am.Chem.Soc. 86, 5616 (1964); S.O. Eriksson G.B.Ariander-ohlson, Acta Chem. Scand 26, 2759 (1972), Г.Б. Сергеев, В.А. Батюк и Б.М. Сергеев "Кинетика и катализ", 15, 326 (1974). Во всех случаях в качестве оптимальных значений рН указывались величины в пределах 6-7, Дженкс и Гилкрист (Jencs & Gilchrist) упоминает более высокую константу скорости реакции при рН 9. Эти кинетические исследования обычно проводились в условиях разбавления при значительном избытке гидроксиламина для обеспечения кинетики первого порядка. Дженкс и Гилкрист также утверждают, что реакция катализируется буфферами, такими, как имидазол, пиридин, ацетат или карбонат. Ф.Бергманн ("Anat. Chem. 24, 1367 (1952) аналитического метода определения амидов. А.Мейстер и др. ("J.Boii. Chem." 215, 441,1955) также показали, что максимальное образование гидроксиламиновой кислоты при использовании различных природных аминов происходит при рН 6. Все вышеупомянутые статьи, в которых рассматриваются, главным образом, процессы гидроксимации мономолярных групп, касается в основном кинетики псевдопервого порядка. При взаимодействии мономерных частиц с солями гидроксиламина реакцию проводят при очень высокой концентрации гидроксиламина, а, следовательно, имеет место кинетика другого типа, которую трудно сравнивать с кинетикой полимерной системы во время гидроксамации при малой концентрации гидроксиламина. При высоких концентрациях гидроксиламина скорость реакции всегда будет очень высокой. По мере уменьшения концентрации гидроксиламина пропорционально снижаются скорость реакции и эффективность конверсии гидроксиламина в гидроксаматную группу. Таким образом при низких концентрациях гидроксиламина, которые испытывались при гидроксамации полимеров, особенно в случае высокомолекулярных соединений, скорость реакции и эффективность использования гидроксиламина являются критическими параметрами, определяющими коммерческий успех процесса. Если бы удалось создать процесс, в котором скорость реакции и эффективность использования гидроксиламина также увеличивалась, то была бы удовлетворена одна из насущных потребностей в данной области. В соответствии с известными способами оптимальным для взаимодействия акриламидных полимеров с гидроксиламином является значение рН, близкое к рКа последнего. Это обусловлено тем, что при значении рН, равном рКа, концентрации гидроксиламина и соли гидроксиламина, служащей катализатором реакции, одинаковы. За прототип заявляемого изобретения принят способ получения акриламидного полимера, содержащего гидроксамовые группы, обработкой водного раствора акриламидного полимера солью гидросиламина в присутствии гидроксида натрия при мольном соотношении соли гидроксиламина и амидных групп в исходном полимере, равном 0, 1-2:1 (заявка Франции 2498200, МКИ6 С09К7/02, опубл. 1982г.). Согласно этому способу получен полиакриламид с гидроксамовыми группами взаимодействием полиакриламида (ПАА), с солянокислым гидроксиламином в водной среде в присутствии гидроксида натрия в количестве, обеспечивающем степень нейтрализации гидроксиламина (ГА) на 80% (мольное соотношение щелочи и ГА 0,4:0,5-0,7). Способ позволяет получать ПАА с содержанием гидроксаматных групп до 31%. Недостатком способа является недостаточная скорость реакции и малая эффективность использования гидроксиламина. Для увеличения скорости реакции в известном способе требуется существенно увеличивать количество гидроксиламина, что делает процесс экономически невыгодным. В основу изобретения поставлена задача повышения эффективности использования гидроксиламина в способе получения акриламидного полимера, содержащего гидроксамовые группы, путем оптимизации технологических условий и режимов обработки акриламидного полимера с молекулярной массой 5 × 104 – 15 × 106 что позволяет достичь максимальной степени нейтрализации кислой соли и оптимального значения рН при минимальных количествах гидроксиламина , и тем самым увеличить скорость реакции и степень гидроксимации. Поставленная задача достигается за счет того, что в способе получения акриламидного полимера, содержащего гидроксамовые группы, обработкой водного раствора акриламидного полимера солью гидросиламина в присутствии гидроксида натрия при мольном соотношении соли гидроксиламина и амидных групп в исходном полимере, равном 0,1-2 : 1, согласно изобретения, используют акриламидный полимер с молекулярной массой 5 × 104 –15 × 106 и обработку проводят при рН, по меньшей мере 11, при температуре 40-80°С в течение 1-4 ч и концентрации раствора полимера, по меньшей мере, 2 мас.%. При этом в качестве акриламидного полимера используют полиакриламид. В данном процессе в качестве исходного сырья может быть использован любой водорастворимый или вододиспергируемый акриламидный полимер. Предпочтительными являются такие соединения, как полиакриламид, полиметакриламид, и т.п., но возможно применение сополимеров, тройных полимеров и т.д. акриламида, метакриламида и т.п. по содержанию сополимера, тройного полимера и т.п. до 90%, предпочтительно - 50%, включающего моноэтиленовый ненасыщенный сомономер, способный сополимеризоваться с указанным акриламидом. К подходящим для этих целей сомономером относятся акриловая кислота, метакриловая кислота, 2-акриломидо-2-метилпропансульфоновая кислота, алкиловые эфиры акриловой и метакриловой кислот такие, как метилакрилат, этилакрилат, метилметакрилат, бутилакрилат, этилеметакрилат и т.п.; акрилат натрия, винилацетат, винилинролидон, стирол, акрилонитрило и т.д. В связи с тем, что эти полимеры используют в водном растворе, то с увеличением молекулярного веса полимера требуется и большее разбавление раствора. К числу подходящих гидроксиламиновых солей относятся фосфат, перхлорат, сульфат, сульфит, гидрохлорид, ацетат, пропионат, и т. Предпочтительным является сульфат. Заявители обнаружили, что в случае полимеров скорость реакции неожиданно возрастает при повышении рН и, более того, происходит оптимизация эффективности использования гидроксиламина. В соответствии с предложенным заявителями новым способом, достигается увеличение гидроксамации на единицу используемого гидроксиламина. При малом времени реакции степень гидроксамации в полимере относительно низка. Увеличение времени взаимодействия приводит к незначительному ее увеличению. Эффективность взаимодействия с точки зрения степени гидроксамации увеличивается при более низких температурах, однако, скорость реакции снижается. Предпочтительный температурный интервал, таким образом, соответствует достижению оптимального сочетания степени гидроксамации и скорости реакции. Как упоминались выше, наиболее значимым условием ведения данного процесса является величина рН. Избыток аммиака, образующийся во время реакции, может быть устранен за счет нагревания, создания вакуума или прокачки системы инертным газом. Ниже представлены примеры, иллюстрирующие изобретение. Примеры 1 и 2. Проведен ряд реакций с целью определения влияния величины рН на взаимодействие гидроксиламина с полиакриламидом. Использованный полиакриламид имеет молекулярный вес 50000-60000. Он был получен путем полимеризации акриламида в водном растворе в присутствии сульфата аммония или метабисульфата натрия в качестве катализаторов. Реакцию с гидроксиламином: проводят при концентрации полиакрилов амида 2,8 моль/л, гидроаксиламина - 1,27 моль/л (добавляемого в виде сульфата гидроаксиламина при температуре 80°С). Сульфат гидроксиламина растворяют в воде и обрабатывают соответствующим основанием при охлаждении Образующийся раствор добавляют к раствору полиакриламида при перемешивании и соответствующей температуре. Через равные промежутки времени отбирают кратные количества смеси и анализируют с целью установления не прореагировавшего гидроксиламина, а также содержание гидроксомата определяют путем осаждения полимера в метаноле и гидролиза в концентрированной кислоте с последующим ионным хроматографическим анализом на освобожденный гидроксиламин или 13С ЯМР. Содержание карбоксилата определяют методом 13С ЯМР. Непрореагированный гидроксиламин определяют посредством йодометрического титрования. В таблице 1 показано, что наибольшие скорости достигаются при высоком начальном значении рН (примеры 1 и 2). Величина гидроксамации в таких опытах также выше. Примеры 3-6. Полиакриламид из примера 1 и 2 концентрации 1,41 моль/л (10 мас.%) подвергают взаимодействию с NH2OH (в виде сульфата гидроксиламина в концентрации 0,63 моль/л при температуре 80°С). Добавляют достаточное количество NaOH для нейтрализации H2SО4 в сульфате гидроксиламина и дополнительно избыток NaOH, как указано в табл.2, где представлены результаты кинетических исследований. Несмотря на то, что даже низшее значение рН (или концентрация основания уже оказываются достаточно значительными, тем не менее все еще наблюдается быстрое увеличение скорости при возрастании концентрации. Примеры 7-11. Полиакриламид из примеров 1 и 2 подвергают взаимодействию аналогично описанному в примерах 3-6, за исключением того, что концентрация полимера составляет 0,70 моль/л (5 мас.%), a NH2OH - 0,32 моль/л. Результаты показаны в таблице 3. В этом случае конечный уровень гидроксамата явно зависит от концентрации основания, возрастая с увеличением концентрации. Уровни гидроксамата обычно ниже, чем в примерах 3-6, где концентрация полимера была выше. Примеры 12-15. Для получения результатов, приведенных в таблице 4, полиакриламид из примеров 1 и 2 подвергают взаимодействию аналогично примерам 3-6, за исключением того, что концентрация полимера составляет 0,28 моль/л (2 мас.%). NH2OH - 0,13 моль/л. Примеры 16-19. Следуют процедуре из примеров 12-15 с той особенностью, что концентрация полиакриламида составляет 2 мас.%, а реакцию проводят при температуре 60°С. Результаты приведены в таблице 5. Примеры 20-23. Повторяют процедуру из примеров 12-15 с той особенностью, что реакцию проводят при температуре 40°С. Результаты показаны в таблице 6. Возрастает скорость реакции и уровень конечной гидроксамации при повышении концентрации NaOH с 2,0 моль/л до 4,0 моль/л. Таким образом, при температуре 40°С скорость гидроксамации велика при достаточно больших значениях рН. Примеры 24-30. Следуют процедуре, описанной в примерах 1 и 2, с той особенностью, что полиакриламид имеет молекулярную массу около 15 млн., используют различные концентрации полимера и гидроксиламина в исходном сырье, а реакцию проводят при разных значениях рН и соответствующих температурах и времени взаимодействия. Результаты показаны в таблице 7. В примерах 24-26 при таком же соотношении полимер-гидроксиламин наблюдается возрастающее внедрение гидроксамата при увеличении значения рН. Сравнение данных для примеров 27-30 с тем, что показаны в табл.5 для полимера с меньшим молекулярным весом свидетельствует о том, что при ведении реакции в практически аналогичных условиях наблюдается почти одинаковая чувствительность к гидроксамации. Пример 31. Следуют процедуре, описанной в примерах 1, 2, однако использует соль гидрохлорида. Получены аналогичные результаты. Пример 32. Следует процедуре из примеров 1 и 2 с той особенностью, что полимер представляет собой сополимер (молекулярная масса 72000) акриламида и акриловой кислоты (90:10), при этом получены аналогичные результаты. Примеры 33-37. Следует процедуре, описанной в примере 32, но вместо сополимера используют следующие полимеры: Пример 33 - акриламид (акрилат натрия) (60:40), молекулярная масса 120000. Пример 34 - полиметакриламит, молекулярная масса 2000000. Пример 35 - акриламид/акрилонитрил (70:30), молекулярная масса 8000. Пример 36 - акриламид (этилакрилат) (80:20), молекулярная масса 8000000. Пример 37 - акриламид акриловая кислота/стирол (80:10:10) молекулярная масса 800000. В каждом случае получены почти эквивалентные результаты. Примеры 38-40. Замены в примере 28 гидроксидамина из примера 31 на 0-метил-гидроксидамин, в примере 39 - на N-этилгидроксидамин и в примере 40 - на 0-фенилгидроксидамин привели к достижению аналогичной гидроксамации полимера во всех случаях. Таблица 1 Пример Нейтрализация, % 1 2 100 100 Значение рН Основание Началь- Конечное ное NaOH NaOH 8,5 10,8 10,2 10,5 Содержание гидроксамата в полимере, % 0,5 ч 1ч 2ч 3ч 4ч 5ч 6ч 7ч K x 10 4,2 16,7 8,7 23,3 17,1 27,2 20,5 26,0 21,9 21,8 26,7 21,7 21,5 25,2 11,9 31,1 Нейтрализация сульфата гидроксиламина. Таблица 2 Содержание гидроксамата, % Пример Концентрация основания, мoлярность NaOH pH 3 4 5 6 0,07 0,19 0,38 0,63 12,8 13,0 13,6 13,8 1) 0,5 ч 1ч 2ч 3ч 4ч 5ч 6ч 7ч 7,1 13,0 21,0 21,3 10,4 15,7 22,1 21,7 15,1 17,6 21,9 19,7 15,6 17,9 20,8 18,7 16,5 17,9 20,4 17,7 16,9 17,6 20,0 17,2 17,0 17,5 19,4 16,7 17,2 19,2 Концентрация основания после нейтрализации сульфата гидроксиламина. Таблица 3 Пример Концентрация основания, мoлярность NaOH pH Содержание гидроксамата, % 7 8 9 0,02 0,1 0,2 12,3 13,0 13,3 0,5 ч 1ч 2ч 3ч 4ч 5ч 6ч 7ч 3,0 7,5 11,6 4,7 9,5 12,4 6,6 10,7 12,4 7,3 11,2 12,1 8,0 11,1 12,0 8,5 10,8 11,5 8,9 10,9 11,2 8,9 10,9 11,0 10 11 1) 0,33 0,65 13,5 13,8 15,8 17,9 16,1 18,7 15,0 18,1 14,6 16,5 14,0 15,8 13,5 15,9 13,5 15,2 13,5 Концентрация основания после нейтрализации сульфата гидроксиламина. Таблица 4 Содержание гидроксамата, % Пример Концентрация основания, мoлярность NaOH pH 12 13 14 15 0,13 0,25 0,51 1,01 13,1 13,4 13,7 14,0 1) 0,25 ч 0,5 ч 1ч 2ч 4ч 6ч 3,8 6,4 8,6 9,4 4,4 6,8 8,8 9,0 4,8 7,9 9,2 8,5 4,9 7,3 9,2 8,6 4,7 7,2 8,7 8,4 4,4 7,1 8,6 8,3 Концентрация основания после нейтрализации сульфата гидроксиламина. Таблица 5 Пример Концентрация основания, мoлярность NaOH pH Содержание гидроксамата, % 16 17 18 19 0,13 0,25 0,51 1,01 13,1 13,4 13,7 14,0 0,25 ч 0,5 ч 1ч 2ч 4ч 6ч 2,0 3,6 4,8 7,4 2,9 5,0 7,4 9,0 4,9 7,5 9,6 10,1 7,0 10,3 10,9 10,5 8,6 12,0 11,3 10,8 8,4 12,2 11,3 10,6 1) Концентрация основания после нейтрализации сульфата гидроксиламина. Таблица 6 Содержание гидроксамата, % Пример Концентрация основания, мoлярность NaOH pH 20 21 22 23 0,5 1,0 2,0 4,0 13,7 14,0 14,3 14,6 1) 0,25 ч 0,5 ч 1ч 2ч 4ч 6ч 3,1 4,3 8,0 14,7 4,0 5,1 8,9 16,1 5,4 7,6 11,0 17,6 8,3 11,0 12,9 19,2 11,6 13,2 14,1 20,6 13,1 14,3 14,4 20,5 Концентрация основания после нейтрализации сульфата гидроксиламина. Таблица 7 Концентрация Пример 25 Pam рН Содержание гидроксамата в полимере, % 3 9,5 16 60 0,28M Время, часы 80 NH2 OH Температура, о С 4 11,0 25 0,28M 26 0,28M 0,28M 27 0,28 0,14 60 0,5 12,0 7 28 0,28 0,14 60 1 12,0 10 29 0,28 0,14 60 2 12,0 13 30 0,28M 0,14 60 4 12,0 13 М=моль/л, Pam – полиакриламид. Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03
ДивитисяДодаткова інформація
Назва патенту англійськоюThe method for acrylamide polymer obtaining
Автори англійськоюLevellin Morris Eugene, Spizer Donald Pole
Назва патенту російськоюСпособ получения акриламидного полимера
Автори російськоюЛевеллин Моррис Юджин, Спицер Дональд Пол
МПК / Мітки
МПК: C08F 220/00, C08F 8/00
Мітки: акриламідного, одержання, полімеру, спосіб
Код посилання
<a href="https://ua.patents.su/6-27266-sposib-oderzhannya-akrilamidnogo-polimeru.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання акриламідного полімеру</a>
Попередній патент: Жаростійка сталь
Наступний патент: Каталізатор полімерізації пропілену
Випадковий патент: Внутрішньоорбітальний імплантат