Спосіб одержання амінофенілперфторалкілсульфідів
Номер патенту: 6205
Опубліковано: 29.12.1994
Автори: Щупак Галина Михайлівна, Бойко Володимир Миколайович, Кірій Наталія Владленівна
Формула / Реферат
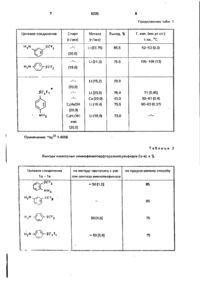
(57) Способ получения аминофенилперфторалкил сульфидов формулы I
где RF-CF3 или C3F7,
с использованием реакции перфторалкилирования соответствующими перфторалкилиодидами при УФ облучении в среде жидкого аммиака, отличающийся тем, что симм,-динитродифенилдисульфид подвергают обработке щелочным или щелочноземельным металлом в жидком аммиаке и в присутствии алифатического спирта с последующим непосредственным перфторалкилированием.
Текст
Способ получения аминофенилперфтоем - Ж., органической химии (1977), т. 13, рал кил сульфидов формулы I вып. 5, с. 1057-1061. 2. Зубаровский В.М. веб. Синтезы гетероциклических соединений (1964), вып. 6, с. NH о ел О 6205 2-меркэптобензтиэзола с выходом 67-72% гоп Для синтеза последних применяется [2], общий выход целевого продукта составтакже и п аминофенилгептафторпропилляет~50% сульфид(1в, Rr-CiFy) м-Аминофен ил трифторметил сульфид В литературе описаны способы получения этих соединений Синтезировались они 5 (16, Rr~=CF3) получали хлорированием и фторированием м-нитротиоэнизола с последуразличными путями. Так, о-аминофенмлт= ющим восстановлением образовавшегося рифторметилсульфид (1а, Rp CF3) получают, м~нитрофенилтрифторметилсульфида [3]. например, трифторметилированием о-амиИсходный м-нитротиоанизол синтезированотиофенола при УФ облучении в растворе жидкого аммиака[1]. Учитываято, что исход- 10 ли, исходя из м-нитророданбензола через ный о-зминотиофенол обычно получают из ипомежуточный м-нитротиофенолят натрия; SCH SCN SCCI, А N0 95% NO, •""* 76% N0, 85% Итоговый общий выход 56% дов связаны с получением, выделением и Описан также синтез п-зминофенилочисткой промежуточных эминотиофенотрифторметилсульфида (!в, RF=CF3) анало- 20 лов, с необходимостью работать с этими не гично орто-кзомеру фотохимическим только легко окисляющимися, но и мерзко перфторалкилированием п-аминотиофенопахнущими и токсичными веществами. С ла в растворе жидкого аммиака [4]. Несмотря целью устранения вышеуказанных недостатна то, что эта стадия обеспечивает высокую ков прототипа в задачу настоящего изобретестепень превращения, с учетом синтеза ис- 25 ния входит разработка такого способа ходного п-аминотиофенола[5]общий выход получения изомерных аминофенилперфтоцелевого продукта не превышает 60%. ралкилсульфидов (fa-їв), при котором генерируемые in situ аминотиофенолы По такому методу получен также п-амииспользовались бы для синтеза целевых нофенилгептафторпропилсульфид (1в, RF= =СзР7) с общим выходом ~ 50% [6]. 30 продуктов без выделения путем непосредстНедостатками известных способов яввенного их перфторалкилирования в перляются: вичной реакционной среде. 1) сравнительно низкая производительПоскольку процесс фотохимического ность метода. Для получения целевых проперфторалкилирования тиофенолов должен дуктов (Ja-Ів) по известным способам 35 протекать в щелочной среде, в частности, в необходимо заранее синтезировать, выдерастворе жидкого аммиака, для достижения лятьиочищатьпромежуточныеаминотиофепоставленной цели синтез аминотиофенолов необходимо осуществлять тоже в раснолы, и хотя методы для некоторых из них творе жидкого аммиака. имеются, выходы в среднем составляют По нашему мнению наиболее простым и 70% Поэтому несмотря на то, что непосред- 40 универсальным методом получения всех ственный процесс перфторалкилирования изомерных аминотиофенолов могло бы довольно результативен (выхода 70-90%), с оказаться восстановление промышленно учетом синтеза аминотиофенолов продукдоступных и легко синтезируемых в лаборативность метода в целом, составляет 5045 ториидинитродифен ил дисульфидов. Вообще 60% такие методы известны, однако, они осуще2) Необходимость работать с чрезвычайствляются не в жидком аммиаке. Например, но зловонными, вредными для организма человека и токсичными эминотиофенолаиспользуется действие цинка или олова в ми соляной и уксусной кислотах, амальгамы на3) Недоступность ряда мета-аминофе- 50 трия в спирте, а также каталитическое гидринилперфторалкилсульфидоа (16) вследствие рование в диоксане при повышенной отсутствия эффективного и простого метода температуре и давлении. Ясно, что ни один из них не может быть использован для решесинтеза м-аминотиофенола. В то время как ния поставленной задачи, т.к. асе они тредля синтеза орто- и пара-аминотиофенолов имеются достаточно хорошо разработанные 55 буют выделения и очистки получаемых методики, получение мета-аминотиофенола аминотиофенолов. остается мало доступным. Целью настоящего изобретения являТаким образом, из всего приведенного ется разработка нового универсального, выше следует, что основные трудности при метода синтеза аминафениллерфторалкилсинтезе аминофенилперфторалкилсульфисульфидов, упрощающего технологический 6205 процесс за счет устранения стадии выделения и очистки промежуточных аминотиофенолов, исключающего контакт человека и окружающей среды с токсичными и зловонными аминотиофенолами, что создает 5 основу для организации экологически безопасного производства, а также повышающего выхода целевых продуктов. Поставленная цель достигается заявляемым способом: постепенное прибавление 10 металлического лигия, натрия или кальция к суспензии симм.-динитродифенилдисульфида в жидком аммиаке в присутствии алифатического спирта и последующее УФ облучение образовавшего раствора вместе 15 с добавленным в него перфторалкилиодидом приводит к получению целевых соединений (Іа-Ів) с высоким выходом. Новизна заявляемого изобретения выражена, во-первых, в новом методе синтеза 20 промежуточных аминотиофенолов, заключающемся в восстановительном расщеплении соответствующих динитродифенилдисульфидов активными металлами в среде жидкого аммиака, а во-вторых, в совмещении в 25 одном технологическом процессе двух различных стадий: синтез аминотиофенолов и их перфторалкилирование. Предлагаемый способ имеет два существенных отличия: 1) объединение в одной 30 реакционной среде двух ранее раздельных и не связанных стадий: синтез промежуточных аминотиофенолов и их перфторалкилирование и 2) использование в качестве исходных соединений не зловонных и ток- 35 сичных аминотиофенолов, а изготовляемых в промышленности и экологически безопасных динитродифенилдисульфидов. Именно эти отличия позволили устранить все описанные выше недостатки. 40 Примеры конкретного исполнения. П р и м е р . м-Аминофенилтрифторметилсульфид. В четырехгорлый реактор из стекла пирекс, снабженный механической мешалкой, холодильником глубокого ох; 45 лаждения, термометром и охлаждаемый низкотемпературной баней, помещают 10 г (0,032 моль) 3,3'-динитродифенилдисульфида, 26 мл (0,64 моль) метанола, конденсируют 100-120 мл жидкого аммиака и при температуре от -50°С и до кипения аммиака малыми порциями прибавляют 5,3 г (0,76 моль) металлического лития, следя за тем, что реакционная смесь не слишком бурно вскипала. Полученную смесь выдерживают при этой температуре 20-30 мин до обесцвечивания раствора, конденсируют в нее 19-25 г(0,1-0,13 моль)трифториодметана и освещают лампой ПРК-4 в течение 1 часа. После удаления аммиака оставшуюся массу разбавляют водой, продукт извлекают бензолом, бензольный раствор промывают водой до рН 7 и сушат над К2СО3. Бензол отгоняют с дефлегматором, продукт перегоняют в вакууме. Аналогично получают все изомерные аминофенилперфторал кил сульфиды (Іа-Ів). Выходы, т.кип., т.пл. приведены в табл. 1, п-Аминофенилтрифторметилсульфид (ів, RF=CF3) И п-аминофенилгептафторпропилсульфид (Ів, CF3=C3F7) идентифицированы методом ГЖХ сравнением с заведомыми образцами (носитель Хроматон N-AW-DMCS с 5% силикона SE-30; длина колонки 2,4 м, температура 175°С, газ-носитель гелий, расход 15 мл.мин). Таким образом, предлагаемый способ является универсальным, позволяющим получать все изомеры целевых продуктов. Весь процесс может быть реализован в одном реакторе. Способ не требует значительных технологических проработок, позволяет значительно снизить материальные затраты, обеспечивает безопасность и экологическую чистоту процесса за счет устранения стадии выделения и очистки зловонных и токсичных аминотиофенолов. Предлагаемый способ позволяет значительно повысить выходы целевых соединений (таблица 2). Та бл и ца 1 Аминофенилперфторалкилсульфиды Іа-Ів Целевое соединение сх Н г Спирт (г/экв) Металл (г/экв) Выход, % Т. кип, (мм.рт.ст.): т.пл., °С СНзОН (20,0) Li(25,0) 85,4 83-84(11); 30-31 (19,9) Na (20,0) 51.8 82-83 (II); 29-30 6205 Продолжение габл 1 Спирт Металл (г/экв) (г/экв) _"_ Целевое соединение LI (23,75) 85.5 52-53 (0.3) LI (21,3) 75.6 105-106(13) Li (15.2) 20,0 (20,0) _'•_ LI (23,0) 75,4 71 (0,45) -" Са (20,0) 43,0 60-61 (0,4) С2Н5ОН LI (19,4) 75,5 60-63 (0,37) Li (18,0) 73,0 и ХУ Выход, % Т. кип. (мм рт ст.); т.пл.,°С (20,0) -'• (19.8) SC 3 F 7 н * Q (20,0) СзНтОНизо (20,0) Примечание: *гю 2 2 1.4656 Таблица Выходы изомерных аминофенилперфторалкилсульфидов(Із-в), а % Целевое соединение по методу-прототип у с уче по предлагаемому способу том синтеза аминотиофенола SCF, - 5 0 [1.2] 85 60 [4,5] 75 NH. 5СГ„ »гы 50 [5,6] 75 2 6205 Упорядник В. Бойко Замовлення 625 Техред М.Моргентал Коректор Я. Филь Тираж Підписне Державне патентне відомство України, 254655, ГСП, КиТв-53, Львівська пл., 8 Виробничо-видавничий комбінат "Патент", м. Ужгород, вул.Гзгаріна, 101
ДивитисяДодаткова інформація
Автори англійськоюBoiko Volodymyr Mykolaiovych
Автори російськоюБойко Владимир Николаевич
МПК / Мітки
МПК: C07C 323/37
Мітки: амінофенілперфторалкілсульфідів, спосіб, одержання
Код посилання
<a href="https://ua.patents.su/6-6205-sposib-oderzhannya-aminofenilperftoralkilsulfidiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання амінофенілперфторалкілсульфідів</a>
Попередній патент: Мікропрограмний автомат
Наступний патент: Спосіб комплексного лікування пародонтиту
Випадковий патент: Спосіб утилізації відходів у вигляді опалого листя