Пристрій для магнітної нанотерапії
Номер патенту: 79982
Опубліковано: 13.05.2013
Формула / Реферат
Пристрій для магнітної нанотерапії злоякісних пухлин, що містить штатив, блок живлення, охолоджувач, постійний електромагніт, електромагнітний аплікатор, зв'язаний з високочастотним генератором, позиційний стіл, який відрізняється тим, що має тримач з діамагнітного матеріалу, усередину якого вставлено локалізатор в формі диполів, які виконані з магніточутливих ін'єкційних голок, до яких підводиться з дозатора ліків протипухлинний магніточутливий нанокомплекс, вони знаходяться у магнітному полі постійного електромагніту, а з зовнішньої сторони тримача у напрямній скривленої еліпсоїдної форми розміщено електромагнітний аплікатор.
Текст
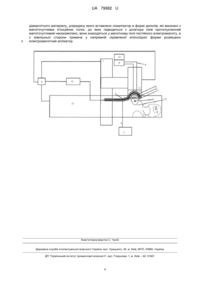
Реферат: UA 79982 U UA 79982 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель належить до медицини, а саме до онкології, і може бути використана як пристрій при проведенні комбінованої магнітної нанотерапії онкологічних хворих, крім того може використовуватися при лікуванні ряду неонкологічних захворювань в інших сферах медицини та ветеринарії. Відомий пристрій для магнітної нанотерапії злоякісних пухлин при локалізації магніточутливих наночастинок в злоякісній пухлині [1], що включає постійний електромагніт, який має просторове неоднорідне розподілення ізоліній постійного магнітного поля. Однак використання цього пристрою при лікуванні злоякісних пухлин у онкологічних хворих має певні обмеження обумовлені по-перше тим, що внаслідок малої величини градієнта постійного магнітного поля в пухлину потрапляє лише 10 % від всього об'єму внутрішньовенно введеного протипухлинного нанокомплексу, а по-друге - внаслідок додаткового зовнішнього намагнічування постійним магнітним полем з наночастинок утворюються великі конгломерати, в результаті чого через обмеження здатності інтегруватися наночастинками з речовинами пухлини за рахунок високої їх питомої поверхні втрачаються терапевтичні переваги використання наночастинок у комплексі з протипухлинним препаратом в порівнянні з традиційним офіціальними протипухлинними препаратами. Найбільш близьким аналогом пристрою, що заявляється, та вибраним як прототип, є пристрій для магнітної нанотерапії злоякісних пухлин, який містить штатив, блок живлення, охолоджувач, постійний електромагніт, електромагнітний аплікатор, зв'язаний з високочастотним генератором, позиційний стіл [2]. При роботі відомого пристрою застосовують неоднорідне постійне поле для локалізації наночастинок у пухлині та змінне електромагнітне поле радіочастотного діапазону, в наслідок чого ініціюється локорегіональна гіпертермія як результат трансформації електромагнітного опромінення в тепло попередньо введеними в злоякісну пухлину нанокомплексу з магніточутливих наночастинок, синтезованих з протипухлинним препаратом. Внаслідок цього в пухлину потрапляє також лише 10 % від всього об'єму внутрішньовенно введеного протипухлинного нанокомплексу та багато магніточутливих наночастинок накопичуються в нормальних тканинах печінки, нирок та селезінки. При цьому в пухлині виникає підвищення швидкості кровотоку при температурах 38-43 °C але суттєво вище в нормальних тканинах в діапазоні 38-50 °C. Ініціювання високотемпературного локального ефекту абляції (вапоризації) пухлини при температурах 42-46 °C досить обтяжливо для серцево-судинної системи хворих й можуть ініціювати побічні ефекти. Внаслідок цього, ефективність комбінованої протипухлинної терапії з застосуванням такого пристрою достатньо обмежена. В основу корисної моделі поставлена задача вдосконалення конструкції пристрою для магнітної нанотерапії злоякісних пухлин, в якому шляхом модифікації конструкційних матеріалів, застосування диполів, виконаних з магніточутливих інжекційних голок, до яких підводиться з дозатора ліків протипухлинний магніточутливий нанокомплекс, що знаходиться у неоднорідному магнітному полі постійного електромагніту, а з зовнішньої сторони тримача у напрямній скривленої еліпсоїдної форми розміщено електромагнітний аплікатор для забезпечення підвищення локалізації у пухлині магніточутливих наночастинок та суттєвого збільшення градієнтів неоднорідних постійного магнітного й змінного електромагнітного полів та відповідно підвищена асиметрія розподілу вихрових струмів. Це підвищує ефективність локорегіонального протипухлинного ефекту магнітної нанотерапії. Поставлена задача вирішується тим, що в пристрої для магнітної нанотерапії злоякісних пухлин, який містить блок живлення, охолоджувач, постійний електромагніт, електромагнітний аплікатор, зв'язаний з високочастотним генератором, використовується тримач з діамагнітного матеріалу, усередину якого вставлено локалізатор в формі диполів, які виконані з магніточутливих інжекційних голок, до яких підводиться з дозатора ліків протипухлинний магніточутливий нанокомплекс, вони знаходяться у магнітному полі постійного електромагніту, а з зовнішньої сторони розміщено електромагнітний аплікатор змінної форми. Відповідно до корисної моделі, диполі, які виконані з магніточутливих інжекційних голок, до яких підводиться з дозатора ліків протипухлинний магніточутливий нанокомплекс, знаходячись у неоднорідному магнітному полі постійного електромагніту, та розміщений електромагнітний аплікатор змінної форми з зовнішньої сторони забезпечують підвищення локалізації магніточутливого нанокомплексу в пухлині, внаслідок підвищення градієнта постійного магнітного поля в пухлині, що збільшує дію сили Лоренца, яка діє на заряд, що рухається, з боку магнітного поля F q v B c , (1) 1 UA 79982 U 5 10 15 20 25 30 35 40 45 50 55 де: q - величина заряду; v - швидкість руху заряду, B - вектор магнітної індукції, c коефіцієнт. Також ініціюється ефект розмагнічування магніточутливих наночастинок при їх опроміненні змінним електромагнітним полем. При цьому суттєво зменшується накопичування наночастинок в нормальних тканинах печінки, нирок та селезінці. Внаслідок того, що при цьому ініціюються помірні температури в пухлинні не більше 39-40 °C, що суттєво обмежує появу побічних ефектів, з боку серцево-судинної системи при лікуванні. Ініціація протипухлинного ефекту при застосуванні пристрою для магнітної нанотерапії злоякісних пухлин заснована на реакції Фентона, згідно з якою, іони заліза (II) окислюються пероксидом водню до іонів заліза (III), а потім знову під дією пероксиду перетворюються на залізо (II): 2+ 3+ Fe +Н2О2→ Fe +ОН·+ОН 3+ 2+ + Fe +Н2О2→Fe +ООН·+Н (2) Механізм цитотоксичної дії нанокомплексу за участю іонів заліза та протипухлинного препарату, наприклад доксорубіцину (С27Н29NO11НСl) та радіочастотному опромінені заснований на активації гідроксильних радикалів, які руйнують ліпіди, білки, ДНК та інші компоненти та структури пухлинних клітин [3]. Це ініціює процеси апоптозу та некрозу пухлинних клітин, гальмуючи їх ріст. Суть запропонованої корисної моделі пояснюється кресленням, на якому зображено пристрій для магнітної нанотерапії злоякісних пухлин. Пристрій містить штатив 1, блок живлення 2, охолоджувач 3, зв'язаний з холодопроводом 4, який підключено до постачальника холодоагенту 5, тримач 6 з діамагнітного матеріалу, у середину якого вставлено локалізатор 7 в формі диполів, які виконані з магніточутливих ін'єкційних голок, до яких підводиться з дозатора ліків 8 за допомогою трубок 9 з резервуара 10 протипухлинний магніточутливий нанокомплекс, локалізатор 7 знаходиться у неоднорідному магнітному полі постійного електромагніту 11, а з зовнішньої сторони тримача 6 розміщено електромагнітний аплікатор 12, зв'язаний з високочастотним генератором 13, просторова форма і розміри аплікатор 12 задаються за допомогою розміру та форми напрямної скривленої еліпсоїдної форми 14, яку вираховано з використанням компьютерного планування на основі цифрового зображення просторової форми та розміру пухлини 15 пацієнта 16, розміщеного на позиційному столі 17. Пристрій працює таким, чином. Заздалегідь до початку комбінованої терапії: на основі цифрових зображень пухлини та оточуючих її тканин отриманих одиничним або з'єднаними методами променевої терапії за допомогою ультразвукового апарату, комп'ютерного томографа, магніторезонансного томографа або позитрон-емісійного томографа індивідуально для кожного хворого за допомогою компьютерного планування проводять виготовлення ливарної моделі тримача 6 з напрямною скривленої еліпсоїдної форми 14, у яку вставляють локалізатори 7 в формі диполів, які виконані з магніточутливих ін'єкційних голок. Після цього ливарним методом з епоксидної смоли виготовляють тримач 6. У напрямну скривленої еліпсоїдної форми 14 тримача 6, згинаючи по її формі, вставляють охолоджувач 3 з електромагнітним аплікатором 12, зв'язаний з високочастотним генератором 13. Далі пацієнта 16 розташовують на позиційному столі 17. За допомогою штативу 1 виставляють, згідно із результатами комп'ютерного планування, відстань та кут аплікатора 12 й постійного електромагніту 11 для оптимального опромінення постійним магнітним та змінним електромагнітним полем пухлину 15 пацієнта 16. При лікуванні хворих з злоякісними пухлинами на поверхні тіла або безпосередньо під час операції, тобто під час інтраопераційного опромінення використовують трансдермальний варіант доставки ліків. Голки в тримачі 6 виставляють на відстані над нижньою основою таким чином, щоб вони проникали в тканини людини трохи більше, ніж на 10-15 мкм. При проведенні передопераційного комбінованого лікування, в випадках, коли злоякісні пухлини розташовані в глибині тіла хворого, препарат вводять внутрішньовенно в живлячі пухлину судини. Магніточутливий нанокомплекс 10 попередньо отримують внаслідок магнітомеханохімічного синтезу оксиду заліза Fe3O4 та протипухлинного антибіотика антрациклінового ряду - доксорубіцину [2]. Проводять ін'єкцію протипухлинного магніточутливого нанокомплексу 10, використовуючи голки локалізатора 7 та дозатора ліків 8 й трубки 9. Одночасно з хіміотерапією проводять неоднорідне опромінення постійним магнітним полем електромагніта 11 та змінним електромагнітним полем аплікатора 12, який одночасно охолоджують за допомогою охолоджувача 3, зв'язаного з холодопроводом 4, який підключено до постачальника холодоагенту 5. При електромагнітному опроміненні пухлини просторово неоднорідним постійним полем і змінним електромагнітним полем пристрою утворюються енергетичні рівні, пов'язані з дозволеними орієнтаціями елементарних магнітних моментів. Тобто поле знімає заборону на 2 UA 79982 U 5 10 15 20 25 30 35 40 45 50 певні електронні переходи в наночастинках заліза. Для реалізації робочих режимів пристрою розподіл електронів по орбіталях можливо розділити на два стани. Перший збуджений, виникає при опроміненні неоднорідним постійним магнітним і змінним електромагнітним полями 2 2 6 2 6 6 1 1 1s 2s 2p 3s 3p 3d 4s 4p . Він має взагалі шість неспарених електронів - чотири на внутрішній 3d оболонці й два на зовнішньому енергетичному рівні. Другий стабільний стан без зовнішнього 2 2 6 2 6 6 2 опромінення - 1s 2s 2p 3s 3p 3d 4s немає неспарених електронів на зовнішньому енергетичному рівні. Наявність неспарених електронів на зовнішній орбіті у наночастинках оксиду заліза підвищує вірогідність перетворення внаслідок окисно-відновних реакцій нейтральної форми протипухлинного препарату доксорубіцину в семихінонний аніон-радикал. При цьому в комплексі між наночастинками магнетиту і доксорубіцину під впливом електромагнітного поля виникають процеси переносу електронів. Одним з механізмів переносу електронів є виникнення циркуляційних (вихрових) струмів при електромагнітному опроміненні за рахунок нерівномірного намагнічування матеріалу нанокомплексу. Матеріал нанокомплексу є сильно неоднорідним за магнітними властивостями, оскільки магнетит Fe3O4 (FeO·Fe2O3) є феромагнетиком, магнітна проникність якого значно перевищує магнітну проникність доксорубіцину. Всередині рівномірно намагніченої наночастинки струмів не виникає, але по її поверхні при наявності вільних електронів весь час буде протікати струм. Інший механізм переносу електронів, так званий спінтронний механізм, пов'язаний з виникненням явищ гігантського магнеторезистивного ефекту в тонких шарах магнетиту та доксорубіцин, при якому опір залежить від магнітного поля і спінів. Внаслідок переносу електронів на бензольних кільцях доксорубіцину виникають кільцеві струми, які ініціюють довгоіснуючі вільні радикали, оскільки електрони π-орбіталі делокалізовані по бензольному кільцю. Механізм протипухлинної дії доксорубіцину заснований на активації гідроксильних радикалів, які руйнують компоненти та структури злоякісних пухлин та підвищують ефективність цілеспрямованої дії доксорубіцину. Без електромагнітного опромінювання, тобто при відсутності неспарених електронів на 2+ зовнішній орбіті у наночастинки іонів перехідних металів у відновленій формі, зокрема іони Fe володіють антиоксидантними властивостями [2]. Тобто після проведеного локорегіонарного електромагнітного опромінення пухлини нанокомплекс, перебуваючи в тілі пацієнта, захоплює вільні радикали і знижує токсичність, що знижує побічні ефекти лікування. Також, в залежності від величини енергії поглиненого зовнішнього постійного магнітного та перемінного електромагнітного опромінення ініційованого пристроєм, можливо регулювання кількості неспарених електронів внаслідок переходу їх з внутрішньої оболонки 3d іонів Fe, які обумовлюють магнітні властивості магнетиту на зовнішній орбіті у наночастинках оксиду заліза у Fe3O4. Таким чином дистанційним керуванням енергії поглинутого постійного магнітного та перемінного електромагнітного поля змінюються ступені окиснювання іонів заліза та реалізуються різні режими магнітної протипухлинної нанотерапії злоякісних пухлин. Проведені пілотні дослідження на експериментальній моделі пухлинного процесу карциносаркоми Уоркер з використанням пристрою та магніточутливого нанокомплексу з оксиду заліза та доксорубіцину засвідчили, що після проведення електромагнітного опромінення тварин за допомогою апарату “Магнітерм”, спостерігався максимальний протипухлинний ефект з коефіцієнтом гальмування пухлини тварин κ=3,87, в той же час при використанні офіцінального доксорубіцину та електромагнітного опромінення пухлини κ=1,30, тобто був суттєво менший. Під час сеансу електромагнітного опромінення температура в центрі пухлини не перевищувала 38 °C. Джерела інформації: 1. Alexioua Ch., Schmidtb A., Kleinb R., Hulinb P., Bergemannc Ch., Arnoldb W. Magnetic drug targeting: biodistribution and dependency on magnetic field strength Journal of Magnetism and Magnetic Materials 252, 2002. p. 363-366. 2. Орел В.Э., Щепотин И.Б., Смоланка И.И. и др. Радиочастотная гипертермия злокачественных новообразований, нанотехнологии и динамический хаос. - Тернополь: ТПМУ, Укрмедкнига, 2012. - 448 с. 3. Minotti G., Menna P., Salvatorelli E. et al. Anthracyclines: Molecular Advances and Pharmacologic Developments in Antitumor Activity and Cardiotoxicity // Luca Gianni. Pharmacol Rev. - 2004. - 56, №. 2. - P. 185-229. 55 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 60 Пристрій для магнітної нанотерапії злоякісних пухлин, що містить штатив, блок живлення, охолоджувач, постійний електромагніт, електромагнітний аплікатор, зв'язаний з високочастотним генератором, позиційний стіл, який відрізняється тим, що має тримач з 3 UA 79982 U 5 діамагнітного матеріалу, усередину якого вставлено локалізатор в формі диполів, які виконані з магніточутливих ін'єкційних голок, до яких підводиться з дозатора ліків протипухлинний магніточутливий нанокомплекс, вони знаходяться у магнітному полі постійного електромагніту, а з зовнішньої сторони тримача у напрямній скривленої еліпсоїдної форми розміщено електромагнітний аплікатор. Комп’ютерна верстка С. Чулій Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Назва патенту англійськоюDevice for magnetic nanotherapy
Автори англійськоюOrel Valerii Emmanuilovych, Orel Valerii Binhovych
Назва патенту російськоюУстройство для магнитной нанотерапии
Автори російськоюОрел Валерий Эммануилович, Орел Валерий Бингович
МПК / Мітки
МПК: A61N 2/08
Мітки: пристрій, магнітної, нанотерапії
Код посилання
<a href="https://ua.patents.su/6-79982-pristrijj-dlya-magnitno-nanoterapi.html" target="_blank" rel="follow" title="База патентів України">Пристрій для магнітної нанотерапії</a>
Попередній патент: Спосіб індукції калюсогенезу у міскантусу
Наступний патент: Спосіб лікування хворих з травматичним ураженням поперекового відділу спинного мозку при хребетно-спинномозковій травмі
Випадковий патент: Кормова добавка