Спосіб кореляційно-оптичного вимірювання часу тромбоутворення
Номер патенту: 97620
Опубліковано: 25.03.2015
Автори: Максимяк Петро Петрович, Гавриляк Михайло Степанович, Григоришин Петро Михайлович, Бойчук Тарас Миколайович
Формула / Реферат
Спосіб кореляційно-оптичного вимірювання часу тромбоутворення шляхом оцінки максимального показника Ляпунова з вейвлет-перетворенням вхідного сигналу розсіяного когерентного поля, який відрізняється тим, що візуалізують зображення поля розсіяного лазерного випромінювання, визначають коефіцієнт кореляції цих зображень у близькі моменти часу (запис зображень проводять з частотою 4 Гц) та час тромбоутворення крові у нормі та при бронхіальній астмі відповідно: група 0 - 16±0,1 с та 25±0,1 с; група А - 17±0,1 с та 22±0,1 с; група В - 12±0,1 с та 18+0,1 с; група АВ - 15±0,1 с та 24±0,1 с.
Текст
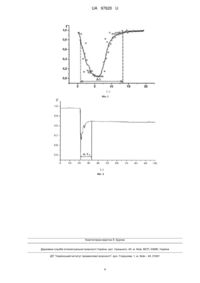
Реферат: UA 97620 U UA 97620 U 5 10 15 20 25 30 35 40 Корисна модель належить до галузі медицини, а саме до гематології, і може бути використана для проведення наукових досліджень та у клінічній практиці в гематології для аналізу динаміки дисперсності компонентів згортання крові, визначення рівня хаотичності системи та часу тромбоутворення. Відомо, що для вивчення компонентів системи гемостазу знаходять все більш широке застосування оптичні методи, які реєструють зміни інтенсивності світла в інкубаційному середовищі при утворенні фібринового згустка. Фібриноген є у складі, як плазми крові, так і в цільній крові. Дослідження процесу коагуляції і фібринолізу в плазмі і цільній крові представляє великий інтерес для клінічної практики, оскільки дає можливість оцінити концентрацію фібриногену в умовах, максимально наближених до фізіологічних норм. На даний час концентрація фібриногену визначається за коагуляційною методикою, за часом утворення згустка в розведеній безтромбоцитній плазмі при додаванні надлишку високоактивного тромбіну (тромбіновий час по Клаусу). Аналогом корисної моделі є спосіб вимірювання часу згортання крові в процесі тромбоутворення (Кудряшов Б.А. Биологические проблемы регуляции жидкого состояния крови и ее свертывания. - М., 1975. - 233 с), в якому на 1 мл тромбоцитарної плазми крові вносять 0,1 мл розчину тромбіну (1000 д. NiH), фіксують час утворення згустка, який у нормі становить 9-15 с. Недоліком аналога-способу є те, що він не дозволяє точно визначити час згортання крові, не дає можливості автоматизувати вимірювання часу тромбоутворення та дослідити динаміку протікання тромбінової реакції. Найближчим аналогом до корисної моделі, що пропонується, є спосіб аналізу тромбоутворення за показником Ляпунова з вейвлет-перетворенням вхідного сигналу розсіяного когерентного поля (Патент України № 31130; МПК G01N 33/48. Спосіб аналізу тромбоутворення за показником Ляпунова з вейвлет-перетворенням вхідного сигналу розсіяного когерентного поля), який виконується шляхом вимірювання часу тромбоутворення за графіком протікання тромбінової реакції після лазерного опромінювання кювети з плазмою крові та реєстрації когерентного опромінення фотодіодом, записом часової залежності інтенсивності розсіяного лазерного світла у комп'ютері з обчисленням максимального коефіцієнта Ляпунова, додатково проводять попереднє вейвлет-перетворення вхідного сигналу світлорозсіювання. Недоліком найближчого аналога є те, що не візуалізують зображення поля розсіяного лазерного випромінювання плазми крові, не визначають часову залежність коефіцієнта кореляції зображень плазми крові при тромбоутворенні. В основу корисної моделі поставлена задача, що полягає у вдосконаленні способу вимірювання часу тромбоутворення шляхом візуалізації зображень поля розсіяного лазерного випромінювання, визначення коефіцієнта кореляції цих зображень та часу тромбоутворення крові у нормі та при бронхіальній астмі. Ознаки корисної моделі: коефіцієнт пропускання, зображення тромбоутворення, коефіцієнт кореляції, час тромбоутворення. Спільними ознаками найближчого аналога та корисної моделі є коефіцієнт пропускання, час тромбоутворення. Відмінності корисної моделі від найближчого аналога наведено в таблиці 1. Таблиця 1 Порівняння корисної моделі та найближчого аналога за ознаками Ознаки коефіцієнт пропускання час тромбоутворення зображення тромбоутворення коефіцієнт кореляції 45 50 Корисна модель визначається визначається візуалізується визначається Найближчий аналог визначається визначається не візуалізується не визначається Визначення термінів, які використовуються при описі корисної моделі: когерентне розсіяне лазерне випромінювання, коефіцієнт пропускання, коефіцієнт кореляції. Теоретичні передумови здійснення способу, що заявляється. У процесі згортання крові проходить декілька десятків біохімічних реакцій, які призводять до утворення фібрину - основи гемостатичного тромбу. Каскадно-комплексна будова системи згортання і позитивні зворотні зв'язки призводять до швидкого, автокатолітичного утворення останнього ферменту каскаду тромбіну, який і здійснює перетворення фібриногену у фібрин, і тим самим здійснює згортання 1 UA 97620 U 5 10 15 крові. Фібриноген є глікопротеїном і присутній в плазмі та в α-гранулах тромбоцитів. Утворення фібрину в крові і в плазмі починається з першого моменту появи тромбіну. Перетворення фібриногену в фібрин протікає в три етапи. На першому етапі тромбін впливає на кінцеві ділянки ланцюгів фібриногену, що призводить до перетворення фібриногену в фібрин-мономер, в центрі якого утворюється реакційна поверхня зі зміненим зарядом. Реакційна поверхня фібрин-мономеру взаємодіє з комплементарними поверхнями на кінцях інших молекул фібринмономеру. Таким чином, відбувається спонтанна агрегація фібрин мономерів - їх полімеризація (другий етап). При цьому, фібрин-мономери з'єднані між собою за допомогою гідрофобних, іонних і водневих зв'язків. На третьому етапі внаслідок утворення пептидного зв'язку між глютаміном і лізином розчинний фібрин-полімер перетворюється на нерозчинний, підвищується стійкість згустка до дії хімічних розчинників і системи фібринолізу, також багаторазово збільшується в'язкість згустка. В результаті збільшення в'язкості згустка спостерігається зменшення динамічних параметрів розсіяного плазмою крові поля випромінювання, які можна експериментально якісно оцінити визначивши кореляцію між розподілами інтенсивності для близьких моментів часу. Отже аналіз поведінки кореляції в часі інтенсивності розсіяного поля дає можливість частково вирішити обернену задачу і може бути використаний для оцінки часу згортання крові. Для оцінки кореляції поля розсіяного когерентного випромінювання обчислюється коефіцієнт кореляції r для зображень А і В за формулою: ( A mn A )(Bmn B) r 20 25 30 35 40 45 50 55 m n ( A mn A )2 (Bmn B)2 m n m n , де m , n - розміри зображення в пікселях, A , B - середні значення інтенсивності для двох зображень. Якщо коефіцієнт кореляції r близький до нуля, то це свідчить про відсутність кореляції між зображеннями, і відповідно, якщо коефіцієнт кореляції близький до одиниці, то зображення корелюють між собою. Спосіб здійснюють наступним чином. На Фіг. 1 представлена оптична схема. Пучок He-Ne лазера 1 розширюється за допомогою телескопічної системи, що складається з мікрооб'єктива 2, діафрагми 3 та об'єктива 4. За допомогою лінзи 5 лазерне випромінювання фокусують на кюветі з досліджуваним зразком 6. Кювету 6 розміщують на предметному столику гоніометра. Розсіяне випромінювання плазмою крові фокусують за допомогою лінзи 7, направляють на діафрагму 8, що потрапляє на CCDкамеру 9, далі сигнал з камери записується на жорсткий диск комп'ютера 10. Об'єктом дослідження є плазма крові здорових і хворих на астму. Флуктуації інтенсивності поля оптичного випромінювання розсіяного плазмою крові вимірюють наступним чином: розміщують кювету зі зразком (плазма крові об'ємом 0,2 мл) згідно зі схемою експерименту, і додають до крові 0,2 мл розчину тромбіну. Тромбін викликає перетворення фібриногену у фібрин, тобто спричинює згортання плазми крові. Очевидно, що такі структурні перетворення відображаються на динаміці зображення плазми крові. Запис зображень (Фіг. 2) проводять з частотою 4 Гц, визначають кореляцію між сусідніми кадрами (Фіг. 3). Частота запису вибрана експериментально. Збільшення частоти запису з одного боку призводить до збільшення кількості експериментальних точок, з іншого - до зростання кореляції між сусідніми кадрами, що ускладнює визначення точного часу утворення тромбу. З часової залежності коефіцієнта кореляції визначають час тромбоутворення (Фіг. 3) t1 різниця у часі між положенням насичення залежності коефіцієнта кореляції і часом початку тромбоутворення. Приклад 1. У результаті експерименту отримано розподіли інтенсивності розсіяного лазерного випромінювання з частотою 4 Гц. На Фіг. 2 зображені фрагменти поля розсіяного випромінювання, а - через 5 с після початку запису; b - через 10 с після початку запису; с - через 15 с після початку запису. Додавання тромбіну до плазми крові на третій секунді від початку запису даних призвело до різкого зменшення коефіцієнту кореляції між сусідніми отриманими зображеннями плазми крові, що показано на Фіг. 3. Це пов'язано з турбулентним перемішуванням тромбіну з плазмою крові. Після цього в результаті реакції тромбіну з фібриногеном утворюються фібринові нитки, які призводять до зростання в'язкості крові і, як наслідок, зменшення динамічних параметрів плазми крові. Отже, під дією тромбіну кореляція між сусідніми отриманими зображеннями 2 UA 97620 U 5 10 збільшується, що дає можливість оцінити власний час утворення тромба t1 =12,4 с, який корелює з часом тромбоутворення визначеним турбідиметричним методом t1 =12 с. Для оцінки достовірності отриманих результатів проведено вимірювання часу тромбоутворення для зразків плазми цієї ж крові турбідиметричним методом. Метод базується на визначенні величини коефіцієнта пропускання плазми крові на довжині хвилі лазерного випромінювання =633 нм протягом певного часу при додаванні до неї тромбіну. В результаті отримана часова залежність коефіцієнта пропускання т плазми в процесі тромбоутворення Фіг. 4. Для турбідиметричного методу: t1 - різниця в часі між розміщенням максимуму на часовій залежності коефіцієнта пропускання і часом початку тромбоутворення. Приклад 2. Для оцінки часу тромбоутворення взята контрольна група крові у нормі та з бронхіальною астмою (табл. 2). Точність вимірювання 0,1с. Таблиця 2 Час тромбоутворення (с) Групи крові норма бронхіальна астма 15 20 25 Кров групи 0 16±0,1 Кров групи А 17±0,1 Кров групи В 12±0,1 Кров групи АВ 15+0,1 25±0,1 22±0,1 18±0,1 24±0,1 Технічний результат: спосіб кореляційно-оптичного вимірювання часу тромбоутворення дозволяє візуалізувати зображення поля розсіяного лазерного випромінювання, визначити коефіцієнт кореляції цих зображень та час тромбоутворення крові у нормі та при бронхіальній астмі відповідно: група 0-160,1 с та 250,1 с; група А - 170,1 с та 220,1 с; група В - 120,1 с та180,1 с;група АВ - 150,1 с та 240,1 с. ФОРМУЛА КОРИСНОЇ МОДЕЛІ Спосіб кореляційно-оптичного вимірювання часу тромбоутворення шляхом оцінки максимального показника Ляпунова з вейвлет-перетворенням вхідного сигналу розсіяного когерентного поля, який відрізняється тим, що візуалізують зображення поля розсіяного лазерного випромінювання, визначають коефіцієнт кореляції цих зображень у близькі моменти часу (запис зображень проводять з частотою 4 Гц) та час тромбоутворення крові у нормі та при бронхіальній астмі відповідно: група 0 - 16±0,1 с та 25±0,1 с; група А - 17±0,1 с та 22±0,1 с; група В - 12±0,1 с та 18+0,1 с; група АВ - 15±0,1 с та 24±0,1 с. 3 UA 97620 U Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Автори англійськоюMaksymiak Petro Petrovych, Boichuk Taras Mykolaiovych, Havryliak Mykhailo Stepanovych, Hryhoryshyn Petro Mykhailovych
Автори російськоюМаксимяк Петр Петрович, Бойчук Тарас Николаевич, Гавриляк Михаил Степанович, Григоришин Петр Михайлович
МПК / Мітки
МПК: G01N 33/00
Мітки: вимірювання, спосіб, кореляційно-оптичного, тромбоутворення, часу
Код посилання
<a href="https://ua.patents.su/6-97620-sposib-korelyacijjno-optichnogo-vimiryuvannya-chasu-tromboutvorennya.html" target="_blank" rel="follow" title="База патентів України">Спосіб кореляційно-оптичного вимірювання часу тромбоутворення</a>
Попередній патент: Спосіб моделювання інфікованого жовчного перитоніту
Наступний патент: Спосіб підготовки та збирання трансплантату для вільної аутодермопластики опікової рани
Випадковий патент: Ентеросорбент "фібросил"