Спосіб отримання хітозану гемостатичного
Номер патенту: 112716
Опубліковано: 10.10.2016
Автори: Луцик Максим Максимович, Луцик Максим Дмитрович, Білий Ростислав Олександрович, Стойка Ростислав Степанович
Формула / Реферат
1. Спосіб отримання хітозану гемостатичного, який відрізняється тим, що проводять деацетилювання хітину панцирів крабів або креветок шляхом гідролізу 40 % NaOH при температурі 110 °C протягом 5 годин, хітозан очищують розчиненням у 3 % оцтовій кислоті і осадженням його із розчину пропусканням газу аміаку, отриманий осад розчиняють підкисленням оцтовою кислотою, осаджують хітозан при концентрації етанолу 55-60 % в інтервалі рН 6-7, отриманий осад висушують.
2. Спосіб отримання хітозану гемостатичного за п. 1, який відрізняється тим, що осад хітозану висушують на плоскій поверхні шляхом вільного випаровування розчинника з наступним подрібненням отриманого матеріалу до частинок розміром 0,25 мм і менше шляхом просіювання через сито з розміром вічок 0,25 мм (60 меш).
3. Спосіб отримання хітозану гемостатичного за п. 1, який відрізняється тим, що препарат хітозану характеризується насипною щільністю менше 0,4 г/см3.
Текст
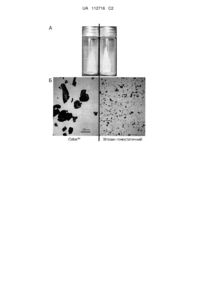
Реферат: Винахід належить до способу отримання хітозану гемостатичного, згідно з яким проводять деацетилювання хітину панцирів крабів або креветок шляхом гідролізу 40 % NaOH при температурі 110 °C протягом 5 годин, хітозан очищують розчиненням у 3 % оцтовій кислоті і осадженням його із розчину пропусканням газу аміаку, отриманий осад розчиняють підкисленням оцтовою кислотою, осаджують хітозан при концентрації етанолу 55-60 % в інтервалі рН 6-7, отриманий осад хітозану висушують на плоскій поверхні шляхом вільного випаровування розчинника з наступним подрібненням отриманого матеріалу до частинок розміром 0,25 мм і менше шляхом просіювання через сито з розміром вічок 0,25 мм (60 меш). UA 112716 C2 (12) UA 112716 C2 UA 112716 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід належить до медицини і стосується отримання засобу для швидкої зупинки кровотечі при наданні невідкладної медичної допомоги при травмах, отриманих в умовах бойових дій, нещасних випадків, катастроф, а також у гематології для лікування кровоточивості (гемофілії), у хірургії, і може використовуватись шляхом аплікації до місця ушкодження тканин (рани) у формі порошку або тампонів і бандажів із закріпленим шаром хітозанового композиту. Гемостатичні агенти, що застосовуються в медичній практиці, поділяються на такі основні групи [Achneck, Sileshi, Jamiolkowski, Albala, Shapiro and Lawson, A Comprehensive Review of Topical Hemostatic Agents: Efficacy and Recommendations for Use. Annals of Surgery, 2010. 251. 217-228]: фізичні агенти (кістковий віск, Ostene™); абсорбуючі агенти (желатинові плівки, окиснена целюлоза, мікрофібрилярний колаген); біологічні агенти (рекомбінантний тромбін, гемостатики на основі фібрину, екстрактів тромбоцитів тощо); синтетичні агенти (ціаноакрилати, гідрогель поліетиленгліколю, зшитий глутаровим альдегідом альбумін); гемостатичні пов'язки (фібринові пов'язки, хітинові/хітозанові пов'язки, пов'язки на основі мінералів цеоліту (QuickClot™) і каоліну [Trabattoni, Montorsi, Fabbiocchi, Lualdi, Gatto and Bartorelli, A new kaolin-based haemostatic bandage compared with manual compression for bleeding control after percutaneous coronary procedures. European Radiology, 2011. 21.1687-1691]. За ефективністю гемостатичної дії, вартістю, здатністю до зберігання та аплікації в екстремальних умовах гемостатичні пов'язки посідають головне місце. Кожному з їх представників притаманні певні переваги і недоліки. Так фібринові пов'язки здатні ефективно зупиняти кровотечу із великих поверхневих ушкоджень, проте їх крихкість (потреба у міцній упаковці) та висока вартість (500-1000 $/аплікацію) обмежують їх використання як компонентів похідних аптечок; мінерали цеоліту та каоліну є ефективні при зупинці кровотечі низького тиску (не артеріальної), проте їх дія пов'язана із екзотермічною реакцією, що супроводжується утворенням великої кількості тепла та термічного опіку рани [Achneck, Sileshi, Jamiolkowski, Albala, Shapiro and Lawson, A Comprehensive Review of Topical Hemostatic Agents: Efficacy and Recommendations for Use. Annals of Surgery, 2010. 251. 217-228]. Препарати на основі хітозану, прототипом яких є відомий засіб "Сеіох™", позбавлені наведених вище недоліків, що призвело до їх широкого застосування як компонентів польових аптечок, придатних для зупинки кровотечі як з обширних відкритих ран, так і глибоких проникаючих ран. Гемостатична дія хітозану не пов'язана із фізіологічною системою зсідання крові хребетних, а здійснюється альтернативним шляхом. Фізіологічна система крові має певні часові обмеження (від кількох до кількох десятків хвилин), які необхідні для уникнення спонтанного тромбоутворення, проте не дозволяє забезпечити гемостаз при екстремальних ушкодженнях. При контакті крові з хітозаном першочергове значення має поглинання частинками хітозану плазми крові, різке зростання в'язкості середовища, адсорбція клітин крові (еритроцитів) на частинках хітозану, активація тромбоцитів із вивільненням їх коагуляційних факторів, що призводить до утворення первинного псевдотромба, який подалі стабілізується факторами фізіологічного шляху зсідання крові. Роль тромбоцитів, однак, менш важлива, про що свідчить коагуляція хітозаном дефібринованої крові, у якій тромбоцити практично відсутні [Okamoto, Yano, Miyatake, Tomohiro, Shigemasa and Minami, Effects of chitin and chitosan on blood coagulation. Carbohydrate Polymers, 2003. 53. 337-342]. Незалежність дії хітозану від фізіологічної системи зсідання крові дозволяє застосовувати його як ефективний кровоспинний засіб при вроджених і набутих порушеннях гемокоагуляції (гемофілії, захворювання печінки). Крім того, хітозан має ряд інших переваг, до яких можна віднести відсутність екзотермічного ефекту при гідратації і набуханні (що є недоліком засобів з неорганічними сорбентами - цеолітів, каоліну, ферратів), біосумісність і біодеградабельність, слабка, однак достовірна, протибактерійна дія. Методи одержання хітозану описані у численних публікаціях і патентах [UA 33765, UA 61373, UA 62138, RU 2065447, RU 2067588, RU 2116314, RU 2117673, RU 2073017]. Принципово процес включає наступні етапи: деацетилювання хітину шляхом його гідролізу концентрованим розчином (40-52 %) їдкого натру або калію при температурі 95-160 °C, промивання нерозчинного матеріалу водою, очистки хітозану розчиненням у розведеній оцтовій кислоті, дегідратації і висушування продукту органічними розчинниками (етанолом, ацетоном). Відмінності між способами стосуються походження хітину як вихідної речовини (краби, креветки, рачки [UA 61373, RU 2065447], гриби чи їх міцелій [UA 33765, RU 2117673], комах [UA 62138, Немцев, Зуева, Хисматуллин, Албулов, Варламов, Получение хитина и хитозана из медоносных пчел. Прикладная биохимия и микроб., 2004, 40 (1). 46-50] та інші), умов гідролізу (температура і тривалість), а також застосування додаткових чинників (ультразвуку, рідкого 1 UA 112716 C2 5 10 15 20 25 30 35 40 45 50 55 60 аміаку, гідразину, відбілюючих агентів тощо). Отримуваний хітозан повільно розчиняється у 15 % оцтовій кислоті з утворенням в'язких розчинів, і нерозчинний у воді і сольових розчинах при нейтральному або лужному рН (7-8). Частинки хітозану мають високу насипну щільність і дуже слабо набухають у воді. Препарати хітозану цього типу, як комерційні (наприклад, компанії Sigma-Aldrich), так і отримані у лабораторних умовах, не проявляють гемостатичної дії. Для надання їм такої властивості необхідна додаткова спеціальна обробка. Найбільш близький до заявлюваного спосіб отримання гемостатичного матеріалу на основі хітозану описано у патенті [US 7981872]. У ньому для підвищення розчинності хітозану у нейтральній області рН, збільшення площі поверхні частинок та надання їм гемостатичних властивостей використовують сіль хітозану із янтарною кислотою (хітозан сукцинат) і добавку щонайменше одного із медичних сурфактантів. При цьому отримання янтарнокислої солі хітозану здійснюють у 77 % водному етанолі. Розчинник видаляють випаровуванням при 60 °C, висушений продукт подрібнюють і змішують з інертним наповнювачем і сурфактантом. Отриманий препарат містить частинки хітозан-сукцинату розміром від 0,297 мм (50 меш) до 0,84 мм (20 меш), або від 0,177 мм (80 меш) до 4 мм (5 меш), та значенням рН від 3,5 до 6. Недоліком даного способу отримання гемостатичного хітозану є висока кислотність похідних хітозану, що спричиняє ушкодження ділянки аплікації; або: яка при застосуванні на відкритій рані хоч і чинить антибактерійний вплив [Rabea, Badawy, Stevens, Smagghe and Steurbaut, Chitosan as Antimicrobial Agent: Applications and Mode of Action. Biomacromolecules, 2003. 4. 1457-1465], проте низьке значення рН інактивує фактори зсідання крові, такі як тромбін, викликає некротичні зміни поверхневих тканин рани і значно збільшує запалення оточуючої тканини і подовжує час загоєння рани [Tomizawa, Clinical benefits and risk analysis of topical hemostats: a review. Journal of Artificial Organs, 2005. 8. 137-142]; обробка хітозану у водноетанольній суміші з високою концентрацією алкоголю (77 %) призводить до ущільнення частинок і утворення препарату з високою насипною щільністю, що значно збільшує масу порошку, необхідну для покриття площі рани. Зниження насипної щільності гемостатичного препарату призвело б до економії матеріалу. Іншим недоліком запропонованого методу отримання хітозану є широкий діапазон розмірів частинок у порошку, з переважанням крупнодисперсних, що зменшує площу поверхні контакту з елементами крові. Нами встановлено, що розмір частинок порошкового хітозану прямо пропорційний до часу коагуляції і утворення згустку гепаринізованої крові (див. Приклад 2Б). Відомий спосіб отримання гемостатичних пов'язок [US 20150011503 А1], що включає 2550 % за вагою кислих хітозанових волокон та 75-50 % за вагою перехресно зшитого хітозанового матриксу. Метод забезпечує отримання гемостатичного хітозану та пов'язок на його основі, що характеризуються рН 2-6. Недоліком даного способу отримання гемостатичного хітозану є те, що похідні хітозану мають високу кислотність, що спричиняє ушкодження ділянки аплікації. Задачею винаходу є розробка способу отримання хітозану з високою гемостатичною/гемокоагуляційною активністю у формі порошку з високою пористістю частинок, відповідно низькою насипною щільністю, високою водопоглинаючою здатністю і швидкістю набухання у водному середовищі, близьким до нейтрального значенням рН водного розчину (у межах 5,5-6), розміром частинок 250 мкм і менше. Розроблений спосіб отримання хітозану гемостатичного включає деацетилювання хітину із панцирів ракоподібних (крабів або креветок) шляхом гідролізу 40 % NaOH при 110 °C на протязі 5 годин, очистку хітозану розчиненням його у 3 % оцтовій кислоті і осадженням із розчину пропусканням газу аміаку до рН 9,0±0,2, розчинення осаду підкисленням оцтовою кислотою, осадження хітозану етанолом, висушування і подрібнення осаду, що відрізняється тим, що з метою досягнення високої гемокоагуляційної активності хітозан осаджують у формі гелю при концентрації етанолу не вище 55-60 % у нейтральному значенні рН (в інтервалі рН 6-7). Осад гелю хітозану висушують на плоскій поверхні шляхом вільного випаровування розчинника при температурі не вище 40 °C з наступним подрібненням отриманого матеріалу до частинок розміром 0,25 мм і менше шляхом просіювання через сито 60 меш (0,25 мм). Запропонований спосіб відрізняється від раніше описаних тим, що: забезпечує отримання препарату хітозану гемостатичного, водний розчин якого має рН 5,56,8; забезпечує отримання препарату хітозану гемостатичного з розмірами частинок від 5 до 250 мкм (0,005 до 0,25 мм), що забезпечує високу площу поверхні частинок і високу швидкість зсідання крові; 3 отриманий препарат має низьку насипну щільність в межах від 0,17 до 0,4 г/см , що зменшує масу препарату, необхідну для покриття поверхні рани. 2 UA 112716 C2 5 10 15 20 25 30 35 40 45 50 55 60 На кресленні зображено: розмірний розподіл мікрочастинок хітозану гемостатичного отриманого запропонованим способом та із комерційного препарату Celox. A - фотографія препаратів у скляних ампулах дозволяє судити про гранулярність та поверхневий заряд (прилипання до скла) мікрочастинок препаратів. Б - мікрофотографія препаратів у гемоцитометричній камері. Шкала мікрометричної камери дозволяє оцінити розмір мікрочастинок препарату Celox та гемостатичного хітозану, отриманого запропонованим способом. Можливість реалізації способу показано на наступних прикладах: Приклад 1. Спосіб отримання хітозану гемостатичного Вихідною речовиною для отримання хітозану служить хітин із панцирів крабів або креветок. Очищений хітин подрібнюють до пудри із розміром частинок 0,1 мм з допомогою електричних подрібнювачів (напр. кавомолок) і просіювання через сито 100 меш. Деацетилювання хітину проводиться шляхом гідролізу 40 % NaOH при температурі 110 °C. Порцію хітину (напр. 10 г) суспендують у 7-8 об'ємах (напр. 70-80 мл) 40 % розчину NaOH (в/в), поступово додаючи хітин до потрібного об'єму лугу. Змішування проводять у фарфоровій ступці, щоб уникнути утворення згустків хітину, до набуття суспензією густої консистенції, здатної до перетікання. Обмеження об'єму лугу необхідне для запобігання осіданню частинок хітину і розшарування суспензії в процесі гідролізу. Суспензію переносять із ступки у колбу, яку заповнюють майже повністю, залишивши тільки невеликий об'єм повітря. Колбу закривають тефлоновим корком, поміщають у посудину типу автоклава, яка може витримувати тривалий нагрів (автоклав-стерилізатор, кастрюля-скороварка) і нагрівають протягом 5 годин при 110 °C (тиску посудині 160 кРа). Після остигання реакційної суміші її розбавляють двома об'ємами дистильованої води і центрифугують 15 хв при 2700 g. Осад промивають водою ще два рази, збираючи його центрифугуванням, після чого суспендують у 2 об'ємах води і доводять рН до 10-11 з допомогою концентрованої оцтової кислоти. Осад збирають центрифугуванням 15 хв при 1500 g або фільтрують через синтетичну тканину із штучного волокна із відповідною щільністю. Осад хітозану розмішують у 3 % розчині оцтової кислоти. Розчинений хітозан зумовлює високу в'язкість суспензії, тому об'єм оцтової кислоти повинен бути достатнім для забезпечення належної в'язкості суспензії. Суспензію перемішують механічною мішалкою протягом 12 годин, центрифугують при 2700 g протягом 20-25 хв і збирають в'язкий прозорий супернатант. Осад розмішують у 3 % оцтовій кислоті і перемішують механічною мішалкою 6 годин, центрифугують і відбирають супернатант. Осад знову суспендують у 3 % оцтовій кислоті, перемішують 3-4 години, центрифугують і відбирають супернатант. Нерозчинний у 3 % оцтовій кислоті осад зберігають для подальшої обробки і повторного гідролізу. Об'єднані супернатанти нейтралізують до рН 9 шляхом пропускання аміаку (газу) через розчин. Хітозан осаджується у формі крупних пластівців, який збирають центрифугуванням при 1500 g протягом 10 хв або фільтруванням через синтетичну тканину із штучного волокна. Осад промивають рівним об'ємом води і проводять обробку для отримання хітозану із гемостатичною активністю. Для цього до гелеподібного осаду додають 20 % оцтову кислоту при перемішуванні до розчинення речовини, яке починається при рН 5,0 і нижче. Розчинення здійснюється протягом кількох годин, для його прискорення суспензію пропускають через гомогенізатор Поттера-Ельвейема. До в'язкої суспензії додають при перемішуванні 25 % гідроокис амонію до рН 5,5, згустки утвореного осаду гомогенізують за допомогою шприца, пропускаючи суспензію через канюлю з малим отвором. Суспензію центрифугують при 2700 g і збирають в'язкий прозорий супернатант. Осад зберігають для подальшої обробки. Супернатант доводять до рН 6,1-6,3 за допомогою 25 % гідроокису амонію, який додають по краплях при інтенсивному перемішуванні. До отриманого розчину додають етанол при постійному перемішуванні до кінцевої концентрації 25 %. Желеподібний осад відділяють центрифугуванням при 1500 g, і означають як "фракція 1". До прозорого супернатанту додають етанол до концентрації 55-60 % і підлужнюють 10 % розчином гідроокису амонію до рН 6,7-6,8. Суміш витримують кілька годин або протягом ночі у холодильнику, після чого осад збирають центрифугуванням при 1500 g протягом 10 хв або фільтруванням через зазначену вище тканину ("фракція 2"). Обидва осади (фракція 1 і фракція 2) наносять тонким шаром на скляні пластини і залишають при температурі навколишнього середовища до повного висихання. Для прискорення висихання можна застосувати слабкий струмінь теплого повітря. Сухий матеріал збирають зі скла, подрібнюють до порошку, просівають через сито 60 меш (розмір частинок 0,25 мм і менше) і зберігають у ексикаторі над СаСl2. Приклад 2. Властивості препарату хітозану гемостатичного і тестування його активності Аналізовані зразки повинні бути подрібнені до частинок 0,2 мм і менше. Тести in vitro 3 включають: а) визначення насипної щільності препарату (г/см ), який відображає ступінь 3 UA 112716 C2 5 10 15 20 25 30 пористості речовини, б) набухання у воді і у сольовому фізіологічному розчині TBS (tris buffer saline), забуференому 10 мМ трис-оксиметил амінометаном, в) час коагуляції гепаринізованої або стабілізованої іншим антикоагулянтом крові. A. Насипну щільність визначають шляхом внесення у градуйовану по 0,1 мл пробірку (діаметром 5 мм) певної маси порошку досліджуваного зразка (30-100 мг, зважування на аналітичній вазі пробірки до і після заповнення) і постукуванням дна пробірки по твердій поверхні (стола, дерев'яної або пластикової пластини) добиваються постійного рівня стовпчика 3 порошку у пробірці. Вираховують масу 1 см порошку. Насипна щільність отримуваних нами 3 зразків активного хітозану-гемокоагулянту знаходилась в межах від, 0,17 до 0,4 г/см (таблиця). Менший показник насипної щільності дозволяє покрити однакову площу рани за допомогою меншої маси препарату. Водночас менша насипна щільність свідчить про високу пористість частинок хітозану і, відповідно, більшу площу їх поверхні, що покращує гемостатичні властивості. Б. Для визначення степеня набухання 5 мг порошку зразка вносять у градуйовану по 0,1 мл пробірку (діаметр 4-5 мм), у яку попередньо внесено 0,5 мл води. Спостерігають за осіданням частинок хітозану. У препаратах із задовільною гемокоагуляційною активністю частинки не опадають на дно пробірки, а залишаються на поверхні водяного стовпчика. При перемішуванні скляним гачком частинки зразу набухають і зумовлюють різке зростання в'язкості суспензії, яка стає гелеподібною. Частинки малоактивних препаратів займають об'єм 0,15-0,25 мл, частинки неактивних препаратів практично не набухають і займають об'єм 0,03-0,05 мл (таблиця). B. Визначення гемокоагуляційної здатності хітозану на гепаринізованій крові Кров людини стабілізували гепарином (0,2 мг/мл крові, гепарин фірми "Спофа"). У скляні пробірки розміром 35×7 мм із плоским дном вносили 0,2 мл гепаринізованої крові, після чого засипали 7 мг порошку хітозану, перемішували гачком, виготовленим із скляного капіляра, і визначали час утворення кров'яного згустку, що проявляється втратою крові до перетікання при нахилянні пробірки, в кінцевому результаті при перевертанні пробірки вверх дном. Хітозан, отриманий за розробленою методикою, зумовлював коагуляцію крові протягом 45-90 сек при співвідношенні 35 мг порошку на 1 мл гепаринізованої крові. Комерційні препарати хітозану не викликали гемокоагуляції протягом 30 хвилин в аналогічних умовах (таблиця). Коагуляція крові, стабілізованої іншими антикоагулянтами (ЕДТА, цитратом або оксалатом) відбувається аналогічно як із гепаринізованою кров'ю. Таблиця Характеристичні властивості різних зразків хітозану Показник Розмір частинок, мкм 3 Насипна щільність, г/см Набухання у воді, мл* рН водної суспензії Набухання у фізіологічному розчині TBS*, рН7, 4 Час коагуляції гепаринізованої крові, сек** Хітозан гемостатичний (патентований) 5250 0,17-0,40 0,50 5,5-6,5 0,50, висока в'язкість суспензії 45-90 Хітозан SigmaAldrich Cat. No. 448869 250500 0,59 0,04 нерозчинний 0,02 Відсутність коагуляції Сеlох (Meditrade Products Ltd., UK) 1201000 0,56 0,50 4,7 0,50, висока в'язкість суспензії 90 Примітки. * - 5 мг препарату вносили до 0,5 мл води або 0,5 мл TBS. ** 7 мг препарату вносили до 0,2 мл гепаринізованої крові 35 40 Приклад 3. Визначення гемостатичної дії препаратів хітозану на тваринах (мишах). Кровотечу у мишей викликали відрізанням 10 мм кінчика хвоста. Для зупинки кровотечі на рану накладали підготовлену заздалегідь марлеву пов'язку, яка являє собою квадратний 2 клаптик 8 шарів марлі, площею 1 см , що містить 12 мг порошку хітозану, рівномірно нанесеного на кожний шар. Клаптик складали у формі лійки і зберігали у пробірці Еппендорф. Перед застосуванням у лійку вносили ще 2-3 мг порошку хітозану. Мишу іммобілізують у спеціальній камері ("хатці"), так щоб хвіст вільно звисав. Гострим лезом відрізають 10 мм кінчика хвоста, на культю накладають пов'язку і притримують 5 хвилин, після чого її фіксують на хвості смужкою лейкопластиру. Через 5-10 хвилин мишу випускають у 4 UA 112716 C2 5 клітку і спостерігають протягом 30 хвилин. При добрій фіксації пов'язка тримається і миша її не зриває. При використанні хітозану гемостатичного просочування кров'ю пов'язки обмежене і не прогресує, в той час як при використанні комерційного препарату хітозану (без описаної обробки) пов'язка просочується кров'ю повністю. При ранньому знятті пов'язки (через 30 хв) кровотеча відновлюється, хоч із значно меншою інтенсивністю, внаслідок відриву згустку, тому рекомендовано залишати пов'язку на кілька годин або добу до самовільного відпадання. ФОРМУЛА ВИНАХОДУ 10 15 20 1. Спосіб отримання хітозану гемостатичного, який відрізняється тим, що проводять деацетилювання хітину панцирів крабів або креветок шляхом гідролізу 40 % NaOH при температурі 110 °C протягом 5 годин, хітозан очищують розчиненням у 3 % оцтовій кислоті і осадженням його із розчину пропусканням газу аміаку, отриманий осад розчиняють підкисленням оцтовою кислотою, осаджують хітозан при концентрації етанолу 55-60 % в інтервалі рН 6-7, отриманий осад висушують. 2. Спосіб отримання хітозану гемостатичного за п. 1, який відрізняється тим, що осад хітозану висушують на плоскій поверхні шляхом вільного випаровування розчинника з наступним подрібненням отриманого матеріалу до частинок розміром 0,25 мм і менше шляхом просіювання через сито з розміром вічок 0,25 мм (60 меш). 3. Спосіб отримання хітозану гемостатичного за п. 1, який відрізняється тим, що препарат 3 хітозану характеризується насипною щільністю менше 0,4 г/см . Комп’ютерна верстка Т. Вахричева Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП "Український інститут інтелектуальної власності", вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C08B 37/08, A61K 31/722
Мітки: хітозану, гемостатичного, спосіб, отримання
Код посилання
<a href="https://ua.patents.su/7-112716-sposib-otrimannya-khitozanu-gemostatichnogo.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання хітозану гемостатичного</a>
Попередній патент: Сальникове ущільнення
Наступний патент: Планарне джерело фотонного випромінення
Випадковий патент: Спосіб термоконтактного крекінгу нафтових залишків