Засіб “феррофол” для лікування залізодефіцитної анемії
Номер патенту: 40656
Опубліковано: 15.08.2001
Автори: Попова Ніна Олексіївна, Суховецька Людмила Федорівна, Толмачова Неоніла Вікторівна, Мирошніков Володимир Олександрович, Павлова Ганна Пилипівна, Шоно Ніна Андріївна, Діхтярьов Сергій Іванович, Тимченко Микола Михайлович, Мдгварелі Вадим Анатолійович, Губін Анатолій Дмитрович, Васильченко Євгенія Олексіївна, Георгієвський Віктор Петрович, Казарінов Микола Олександрович, Рибаченко Анатолій Іванович, Бобкова Людмила Миколаївна
Формула / Реферат
Средство для лечения железодефицитной анемии, включающее железа закисного сульфат, кислоту аскорбиновую и вспомогательные вещества, отличающееся тем, что дополнительно содержит кислоту фолиевую, а в качестве вспомогательных веществ - молочный сахар, крахмал, кислоту стеариновую и воду очищенную при следующем соотношении компонентов, мас.%:
Железа закисного сульфат
35,60-39,40
Кислота аскорбиновая
23,10-26,90
Кислота фолиевая
0,10-0,15
Молочный сахар
11,50-13,50
Крахмал
13,00-15,00
Кислота стеариновая
0,70-1,00
Вода очищенная
остальное
Текст
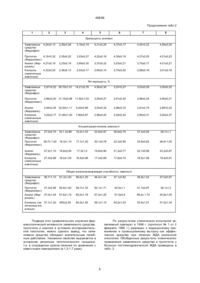
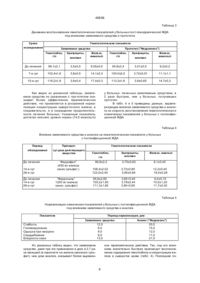
Средство для лечения железодефицитной анемии, включающее железа закисного сульфат, кислоту аскорбиновую и вспомогательные вещества, отличающееся тем, что дополнительно содержит кислоту фолиевую, а в качестве вспомогательных веществ - молочный сахар, крахмал, кислоту стеариновую и воду очи щенную при следующем соотношении компонентов, мас.%: Железа закисного сульфат 35,60-39,40 Кислота аскорбиновая 23,10-26,90 Кислота фолиевая 0,10-0,15 Молочный сахар 11,50-13,50 Крахмал 13,00-15,00 Кислота стеариновая 0,70-1,00 Вода очищенная остальное. Ю (13) 40656 (11) UA К причинам, препятствующим в прототипе и аналогах получе нию технического результата, достигаемого в заявляемом изобретении, следует отнести то, что качественный состав и количественное соотношение компонентов этих лекарственных средств не позволяют достичь высокого уровня биодоступ ности железа и хорошего противоанемического действия с одновременным сокращением сроков лечения и снижением частоты нежелательных побочных эффектов, обеспечиваемых заявляемым средством. В основу изобретения поставлена задача создания лекарственного средства для ле чения железодефицитной анемии путем качественного и количественного подбора компонентов, которые бы обеспечили более высокое специфическое действие при одновременном снижении дозы активно действующих веществ, приводящее к сокращению сроков лечения и снижению побочных отрицательных эффектов. Поставленная задача ре шается тем, что средство для лечения железодефицитной анемии (ЖДА), включающее железа закисного сульфат, кислоту аскорбиновую и вспомогательные вещества, в соо тветствии с изобретением дополнительно содержит кислоту фо лиевую, а в ка (19) Изобретение относится к медицине и химико-фармацевтической промышленности, а именно к созданию и производству лекарственных средств, используемых в те рапии железодефицитной анемии. Известно противоанемическое средство "Тардиферон" в виде драже, содержащее в качестве действующего вещества 0,257 г железа закисного сульфата (о коло 80 мг элементарного железа) и вспомогательные вещества [1]. Известно противоанемическое средство "Феррокаль" в ви де таблеток, содержащее в качестве действующих ве ществ 0,2 г железа закисного сульфата, 0,1 г кальция фруктозодифосфа та, 0,02 г церебролецитина [2]. Известно противоанемическое средство "Феромед" в виде капсул, содержащее в качестве активных ингредиентов железа закисного сульфат и фо лиевую кислоту [3]. Наиболее близким к заявляемому является противоанемическое средство "Ферроплекс" в виде драже белого цвета, содержащее 0,05 г железа закисного сульфата и 0,03 г аскорбиновой кислоты, а также вспомогательные вещества. Препарат предназначен для лечения железодефицитной анемии различной этиологии [4]. C2 ______________________________ 40656 честве вспомогательных веществ - молочный сахар, кра хмал, кислоту стеариновую и во ду очищен ную при следующем соотношении компонентов, мас.%: Железа закисного сульфат 35,60-39,40 Кислота аскорбиновая 23,10-26,90 Кислота фолиевая 0,10 - 0,15 Мо лочный сахар 11,50 - 13,50 Крахмал 13,00 - 15,00 Кислота стеа риновая 0,70 - 1,00 Вода очищенная Остальное Технический результат, получаемый при осуществлении изобретения, выражается в повышении специфической активности лекарственного средства, снижении частоты побочных отрицательных эффектов, сокращении сроков лечения. Приводим конкретные примеры осуществления изобретения. Для получения заявляемого лекарственного средства приготавливают 5 соста вов, содержащих следующие компоненты: железа закисного сульфат, кислоту аскорбиновую, кислоту фолиевую, молочный сахар, крахмал, кислоту стеариновую и воду очищен ную, которые отличаются друг от друга количественным содержанием ингредиентов (минимальный, оптимальный, максимальный и два запредельных значения). Пример 1. Для получения заявляемого средства приготавливают состав, со держащий следующее соотношение компонентов, мас.%: Железа закисного сульфат 35,60 Кислота аскорбиновая 23,10 Кислота фолиевая 0,10 Мо лочный сахар 11,50 Крахмал 13,00 Кислота стеа риновая 0,70 Вода очищенная Oстальное К высушенному железа закисного сульфа ту прибавляют смешанные с молочным сахаром и крахмалом картофельным фолиевую и аскорбиновую кислоты, перемешивают. Смесь увлажняют крахмальным клейстером, сушат до определенной влажности. Приготовленный состав опудривают смесью кислоты стеариновой и крахмала картофельного, после чего проводят сухое гранулирование и таблетируют ядра средней массой 0,4 г. Пример 2. Для получения заявляемого лекарственного средства приготавливают следующий состав, мас.%: Железа закисного сульфат 37,50 Кислота аскорбиновая 25,00 Кислота фолиевая 0,12 Мо лочный сахар 12,50 Крахмал 14,00 Кислота стеа риновая 0,85 Вода очищенная Oстальное Заявляемое лекарственное средство получают аналогично примеру 1. Пример 3. Для получения заявляемого лекарственного средства приготавливают следующий состав, мас.%: Железа закисного сульфат 39,40 Кислота аскорбиновая 26,90 Кислота фолиевая 0,15 Мо лочный сахар 13,50 Крахмал 15,00 Кислота стеа риновая 1,00 Вода очищенная Oстальное Заявляемое лекарственное средство получают аналогично примеру 1. При приготовлении лекарственного средства с недоста точным количеством вспомогательных ве ществ (менее, чем в примере 1) получают таблетки с повышенной распадаемостью. При изготовлении лекарственного средства с большим содержанием вспомогательных веществ, чем в примере 3, получают таблетки со сниженной прочностью и малой распадаемостью. Следовательно, запредельные количества крахмала, кислоты стеариновой и воды очищенной, использованные при приготовлении данной лекарственной формы, не позволяют получить лекарственное средство, соответствующее требованиям, предъявляемым к лекарственной форме "Таблетки" по структур но-механическим и др. характеристикам. Разработку соста ва заявляемого средства осуществляли, исхо дя из имеющихся в ли тературе данных по изучению зависимости часто ты побочных эффектов от дозы железа в препарате, влияния различных веществ на биодоступность железа, а также результатов собственных исследований, характеризующи х влияние некоторых биологически активных компонентов на его усвояемость. Как известно, нарушения функции желудочно-кишечного тракта (ЖКТ)* минимальны, если суточное количество элементарного железа не превышает 180 мг. Для повыше ния биодоступ ности препаратов железа и уменьшения побочных эффектов в их состав включают ве щества, способствующие вса сыванию железа в ЖКТ и акти вирующие его внутриклеточный метаболизм. Такими свойствами обладают некоторые углеводы, витамины, органические кислоты и аминокислоты. Наиболее часто применяется аскорбиновая кислота, которая не только способствуе т всасыванию железа в ЖКТ и участвуе т в его внутриклеточном обмене, но и необходима для коррекции ряда биохимических наруше ний, возникающих при ЖДА. Однако, значительное усиление абсорбции железа наблюдали при применении аскорбиновой кислоты в разовой дозе от 200 мг и выше на 30-50 мг элементарного железа. В то же время установлено, что ее длительное применение в суточных дозах, превышающих 500-700 мг, приводит к серьезным функциональным и биохимическим наруше ниям в организме. Поэтому, в состав таких препаратов необходимо дополнительное включение компонентов, усиливающи х действие аскорбиновой кислоты. Одним из таких веществ является фолиевая кислота, которая оказывает влияние на скорость утили зации железа гемопоэтическими тканями, а также необхо дима для синтеза нуклеи 2 40656 новых кислот и нормального образования клеток крови, включая процессы их созревания. При выборе оптимального соста ва заявляемого средства бы ло изуче но влияние различных доз аскорбиновой кислоты (50, 100, 150 и 200 мг на 48 мг элементарного железа), а также сочетанного применения аскорбиновой и фолиевой кислот на скорость всасыва ния железа в ЖКТ и интенсивность поглощения его гемопоэтическими тканями. При этом основное действующее ве щество (железа закисного суль фат) применяли в дозе 150 мг (около 48 мг элементарного железа) в одной таблетке исхо дя из то го, что при применении препаратов, со держащи х железа закисного сульфат в до зах 50 и 100 мг (около 16 и 32 мг элементар ного железа) в одной таблетке, для достижения выраженного про тивоа немического эффекта необхо димо назначать 2-3 таблетки на прием 3 раза в день, что создает определенные неудобства для пациентов. Применение же препаратов, со держащи х 200 мг железа закисного сульфа та (о коло 64 мг элементарного железа) в одной таблетке, может вызывать доста точно сильные диспептические побочные аффек ты в резуль тате высоких локальных концентраций ферроионов на сли зистой ЖКТ. К то му же, увели чение дозы железа закисного сульфа та от 150 мг до 200 мг не приводит к усиле нию те рапевти ческого эффек та. Исходя из указанного (см. табл.1), были приготовлены 5 составов, 4 из которых отличались друг от друга соотношением железа закисного сульфа та и аскорбиновой кислоты, а 5-й - дополнительным включением фолиевой кислоты. Таблица 1 Влияние различных доз аскорбиновой кислоты и со четанного применения аскорбиновой и фо лиевой кислот на биодоступность железа Состав лекарственного средства Исходная концентрация железа, мкмоль/л Концентрация железа через 2 ч, мкмоль/л Повышение концентрации железа, % Концентрация железа через 5 ч, мкмоль/л Поглощение железа тканя ми, % Железа закисного сульфат 12,0±1,01 31,8±1,2 165,0 25,7+0,94 19,2 Железа закисного сульфат + 50 мг аскорбиновой 11,4±0,85 31,2+1,6 174,20 24,9±0,87 20,2 11,7±0,91 37,3±1,09 218,7 22,9+0,76 38,6 11,5+0,76 41,1±1,5 257,2 16,4+0,82 60,1 12,2+0,84 43,8±1,1 266,9 12,1+0,80 70,1 11,8±0,93 40,9±1,1 246,6 12,6±0,72 69,1 кислоты Железа закисного сульфат + 100 мг аскорбиновой кислоты Железа закисного сульфат+ 150 мг аскорбиновой кислоты Железа закисного сульфат + 200 мг аскорбиновой кислоты Железа закисного сульфат + 100 мг аскорбиновой + 0,5 мг фо лиевой кислот Усвояемость железа из указанных составов оцени вали по ди намике изменения его концентрации в сыворо тке крови анемизированных живо тных. Оп ределение концентрации железа проводили че рез 2 ч после вве дения ле карственного средства (быстрая фа за резорбции, во вре мя которой вса сывае тся около 80% железа) и через 5 ч, и схо дя из того, что ско рость сни жения концентрации железа в сыворо тке является одним из показателей по глощения его ге мопоэтиче скими тканями, поскольку вы деление железа из орга низма лимитирова но и является пассивным процессом. Получен ные в резуль та те проведенных исследова ний данные (табл. 1), сви дете льствуют, что при менение аскорби новой кислоты в 3 40656 минимальной дозе (50 мг) практи чески не влияет на усвояе мость железа; применение в до зе 100 мг оказывает нез начитель ное влия ние; применение в до зах 150 и 200 мг оказывае т выраженное и практи чески одинаковое влияние на скорость вса сывания железа (увели чивае т в 1,51,6 раза по сравнению с применением одного железа закисного суль фа та) и несколько отличается по интен сивности поглощения его гемопоэтическими тканями (на 10% больше при применении аскорбиновой кислоты в до зе 200 мг). Со четан ное применение 100 мг аскорбиновой и 0,5 мг фо лие вой кислот при води ло к такой же скорости вса сывания железа, как применение 150 мг аскорбиновой кислоты и скорости поглощения его тканями - как применение 200 мг аскорбиновой кислоты. Та ким образом, подобранное соотношение биологи чески активных компоненто в (150 м г железа закисного сульфа та, 100 мг аскорбиновой и 0,5 мг фолие вой кислот) обеспечивае т вы сокую биодоступность железа, что поз воляет применять препарат в доста точно низких до зах и, тем са мым, предотвраща ть раз витие диспептических и др уги х побочных эффекто в. Кро ме того, при вве дении в состав пре парата фо лиевой кислоты до за аскорбиновой кислоты снижается до ве личины, в ко торой она не оказывае т отрицатель ного влияния на ор ганизм че ловека. Получае мое средство было испытано в лаборатор ных и кли нических усло виях. Противоа немическую активность заявляемого средства изуча ли в сравнении с прототи пом ("Ферроплексом") и аналогом ("Феррокалем") на модели постгеморрагической (железодефи цитной) анемии у крыс, адекватно моделирующей железодефи цитное состояние. О фармакотерапевтическом действии препаратов де лали заключение по скорости восстановления содержа ния гемоглобина, числа эритроцитов и ретикулоцитов, концентрации железа в сыворотке и общей железосвязывающей способности сыворотки крови у анемизированных животных. Указанные показатели определяли у интактных животных, на высоте разви тия анемии, а также в период регрессии патологического процесса. Ре зультаты, получен ные при сравнительном изуче нии эффективности препаратов, приведены в табл. 2, из которой видно, что по скорости восстановления содержания гемоглобина и числа эритроцитов лечебное действие заявляемого средства примерно соответствует эффекту прототи па и значительно превосхо дит эффект анало га (в 1,4 и 1,7 раза соответственно), а по скорости нормализации концентрации железа и общей железосвязывающей способности сыворотки значительно превосхо дит эффект и прототи па, и аналога, Так, указанные показатели восстанавливались до уровня нормы под влиянием заявляемого средства че рез 25 дн от начала его применения, под влиянием прототи па - через 35 дн, а под влиянием аналога даже к концу срока наблюдения эти показатели оста вались ниже исходного уро вня. Следует о тметить, что от скорости нормализации концентрации сывороточного железа и общей железосвязывающей способности сыворотки крови зависит дли тельность лечения ЖДА, так как только при восстановлении запасов железа в организме исчезают симпто мы тканевой ги поксии. Из указанной таблицы также видно, что снижение числа ре тикулоци тов о тноситель но состоя ния анемии у животных, ле чен ных заявляемым средством, происхо дило медленнее, чем у животных, по лучавши х прото тип (в 1,3 раза) и аналог (в 1,55 раза), что сви дете льствуе т о более вы раженном сти мули рующем действии заявляемого средства на костномозговое кроветво рение. Таблица 2 Противоанемическая активность заявляемого средства, прототипа и аналога Условия опыта Исходный уровень Состояние анемии 10 Лек. средство 1 Восстановительный период, дни 2 3 20 25 30 35 4 5 6 7 8 Заявляемое средство (Феррофол) 142,1±6,0 60,7±2,3 Гемоглобин, г/л 91,2±4,0 138,4±5,3 141,5±4,7 146,7±5,0 152,2±6,1 Прототип (Ферроплекс) Ав алог (Феррокаль) Контроль (нелеченные жив отные) 140,8±8,2 61,4±1,9 88,7±3,1 133,7±7,0 137,1±5,2 140,4±4,4 145,5±5,7 141,3±5,7 60,1±2,7 74,3±2,8 97,2±5,8 106,6±4,5 118,3±5,0 130,0±6,2 139,8±4,6 62,0±2,2 68,1±5,5 86,0±3,1 90,7±4,4 94,2±4,7 97,5±5,3 4 40656 Продолжение табл.2 1 2 3 4 5 6 7 8 Эритроциты, млн/мкл Заявляемое средство (Феррофол) 4,24±0 12 2,29±0,26 3,16±0,19 4,31±0,25 4,37±0,17 4,40+0,22 4,56±0,20 Прототип 4,19+0,32 (Ферроплекс) Аналог (Фер- 4,27±0,19 рокаль) Контроль 4,32±0,25 (нелеченные жив отные) 2,35±0,22 3,03±0,27 4,22±0,16 4,30±0,19 4,37±0,25 4,51±0,23 2,23±0,19 2,69±0,30 3,37±0,22 3,53±0,21 3,70±0,17 4,01±0,21 2,36±0,13 2,53±0,17 2,60±0,14 2,70±0,20 2,88±0,16 3,01±0,18 Ретикулоциты, % Заявляемое средство (Феррофол) 2,97+0,22 30,70±1,01 14,21±0,76 4,90±0,30 3,20+0,27 3,03±0,29 3,00±0,22 Прототип 2,86±0,20 31,10±0,98 (Ферроплекс) 11,82±1,03 3,50±0,27 2,91±0,30 2,88±0,24 2,90±0,31 Аналог (Феррокаль) Контроль (нелеченные жив отные) 2,94±0,26 32,00±1,11 9,20±0,89 3,04±0,32 2,96±0,33 2,91±0,19 2,89+0,23 3,02±0,17 31,60±1,20 7,80±0,67 2,96±0,43 2,93±0,24 2,90±0,31 2,92±0,37 Концентрация железа, мкмоль/л Заявляемое 27,0±0,75 16,1 ±0,86 средство (Феррофол) Прототип 26,7± 1,02 16,3±1,14 (Ферроплекс) 19,4±1,03 23,9±0,97 26,8±0,70 27,4±0,84 28,7±1,1 17,1±1,20 20,1±0,78 22,3±0,90 23,6±0,82 26,8+1,05 Аналог (Феррокаль) Контроль (нелеченные жив отные) 27,2±1,10 16,8±0,94 17,3±1,0 19,6±0,90 21,2±0,77 22,7±0,96 23,2±0,87 27,3±0,89 16,0±1,05 16,5±0,98 17,3±0,69 17,8±0,74 18,5±1,06 19,4±0,91 Общая железосв языв ающая способность, мкмоль/л Заявляемое средство (Феррофол) 36,7+1,13 61,3±1,50 56,6±1,20 46,4±1,44 37,1±0,82 36,9±1,02 37,0±0,97 Прототип 37,3±0,89 (Ферроплекс) Аналог (Фер- 37,0±1,04 рокаль) 60,8±1,62 58,7±1,33 50,1±1,71 44,5±1,1 41,7±0,87 38,1±1,2 61,6±1,74 60,0±1,16 57,3±1,20 51,5±0,9 48,2± 1,74 44,9±1,05 Контроль (не- 37,1±1,20 леченные жив отные) 605±2,05 60,2±1,50 58,1±1,10 54,2±1,03 53,0±1,51 51,5±1,34 Подводя итог сравнительного изучения фармакологической активности заявляемого средства, прототипа и аналога в условиях экспериментальной патологии, можно сделать вывод, что заявляемое средство обладает значительным лечебным действием. Указанное свойство выражается в ускорении регрессии патологического процесса, т.е. в сокращении сроков лечения по сравнению с известными препаратами (в 1,3-1,7 раза). По результатам клинических испытаний заявляемый препарат в 1996 г. (протокол № 1 от 2 февраля 1996 г.) разрешен к медицинскому применению и промышленному вы пуску как эффективное средство при лечении ЖДА различной этиологии. Обобщенные результаты клинического применения заявляемого средства и прототи па у больных постгеморрагической ЖДА приведены в табл. 3. 5 40656 Таблица 3 Динамика восста новления гематологических показателей у больных пост-геморрагической ЖДА под влиянием заявляемого средства и прототи па Сроки Гематологические показатели исследования Заявляемое средство Гемоглобин, г/л Эритроциты, До лечения 98,1±2,1 7-е сут 15-е сут Прототип ("Ферроплекс") Железо, мкмоль/л Гемоглобин, г/л Эритроциты, 3,5±0,5 9,05±0,5 94,8±2,4 3,51±0,5 9,2±0,2 102,4±1,6 3,8±0,5 14,1±0,3 100,0±2,0 3,72±0,51 11,1±1,1 116,2±1,8 3,9±0,4 17,4±0,3 113,3±1,6 3,8±0,65 14,7±0,3 млн/мкл Как видно из указанной табли цы, заявляемое средство по сра внению с: про тоти пом оказывает бо лее эффекти вное терапевтическое действие, что проявляется в ускоренной нормализации концентрации сыворо точного железа, а следова тель но, и в сокращении продолжительности ле чения больных, Указанный показатель дости гал ниж него уровня нормы (14,0 мкмоль/л) Железо, мкмоль/л млн/мкл у больных, лечен ных заявляемым средством, в 2 раза быстрее, чем у бо льных, по лучавши х прототип. В табл. 4 и 5 приведены данные, характеризующие влияние заявляемого средства и аналога на скорость восстановления гематологических и клинических показателей у больных с постинфекционной ЖДА. Таблица 4 Влияние заявляемого средства и аналога на гематологические показатели у больных с постинфекционной ЖДА Период Препарат, обследования сут.доза действующего вещества Гематологические показатели Гемоглобин, г/л До лечения “Феррофол" (450 мг железа закис.сульфат.) 14-е сут 28-е сут До лечения 14-е сут 28-е сут "Феррокаль" 1200 мг железа закис. сульфат) Эритроциты, млн/мкл Железо, ммоль/л 96,8±2,2 3,75±0,62 9,1±0,40 108,4±2,02 122,0±2,40 3,72±0,80 3,90±0,84 12,2±0,44 18,4±0,28 95,6±2,60 105,2±1,90 111,3±1,80 3,60+0,40 3,78±0,44 3,80+0,60 9,4±0,10 10,0±1,20 11,7±0,30 Таблица 5 Нормализация клинических показателей у больных с постинфекционной ЖДА под влиянием заявляемого средства и аналога Показатели Период нормализации, дни Заявляемое средство Аналог ("Феррокаль") 12,0 8,0 9,0 8,0 13,0 20,0 15,0 12,0 11,0 21,0 Слабость Головокружение Одышка при нагрузке Сердцебиение Бледность кожи Из указанных таблиц видно, что заявляемое средство, даже при его применении в дозе в 2,7 раза меньшей (в пересчете на железа закисного сульфат), чем доза аналога, оказывает более выражен ное терапевтическое действие. Так, под его влиянием значительно быстрее происхо дит восстановление содержания гемоглобина и концентрации железа в сыворотке крови (табл. 4). Последний по 6 40656 казатель восстанавливался в 2 раза интенсивнее, чем под влиянием аналога. Также быстрее (в 1,31,7 раза) нормализовались у больных клинические показатели течения патологии (табл. 5). Кроме того, как показали клинические исследования, заявляемое средство, в отличие от известных лекарственных средств, не оказывает побочных эффектов. Следуе т отметить, что ре зультаты клинического изучения заявляемого средства, прототипа ("Ферроплекса") и аналога ("Феррокаля") полностью подтверждают, а в некоторых случаях и превосхо дят данные, получен ные в условиях эксперимента. Обобщая результа ты проведенных исследований можно заключить, что заявляемое средство обладает по сравнению с прототипом и аналогом несомненными преимуществами: подобранное соотношение биологически активных компо нентов обеспечивает его высокую биодоступность, что приводит к быстрому насыщению организма железом, а, следовательно, и к сокращению сроков лечения больных. Кро ме того, указанные свойства позволяют применять препарат в достаточно низких дозах и, тем самым, предотвращать развитие диспептических побочных эффектов, характерных для железосодержащи х препаратов. Литература 1. Машковский М.Д. //Лекарственные средства. – М.: Медицина, 1993. - Ч. II. - С. 149. 2. Машковский М.Д. //Лекарственные средства. - М.: Ме дицина, 1993. - Ч. II. - С. 148. 3. Справочник ВИДАЛЬ. Лекарственные препараты в России. - Астра Фарм Сервис, 1995. - С. 925. 4. Машковский М.Д. //Лекарственные средства. - М.: Ме дицина, 1993. - Ч. II. - С. 148. Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03 7
ДивитисяДодаткова інформація
Назва патенту англійськоюDrug “ferrofol” for treatment of iron-deficiency anemia
Автори англійськоюKazarinov Mykola Oleksandrovych, Popova Nina Oleksiivna, Tolmachova Neonila Viktorivna, Pavlova Hanna Pylypivna, Rybachenko Anatolii Ivanovych, Hubin Anatolii Dmytrovych, Bobkova Liudmyla Mykolaivna, Vasylchenko Yevheniia Oleksiivna, Sukhovetska Liudmyla Fedorivna, Shono Nina Andriivna, Heorhiievskyi Viktor Petrovych, Dihtiariov Serhii Ivanovych, Tymchenko Mykola Mykhailovych, Mdhvareli Vadym Anatoliiovych, Myroshnikov Volodymyr Oleksandrovych
Назва патенту російськоюСредство "феррофол" для лечения железодефицитной анемии
Автори російськоюКазаринов Николай Александрович, Попова Нина Алексеевна, Толмачова Неонила Викторовна, Павлова Анна Филипповна, Рыбаченко Анатолий Иванович, Губин Анатолий Дмитриевич, Бобкова Людмила Николаевна, Васильченко Евгения Алексеевна, Суховецкая Людмила Федоровна, Шоно Нина Андреевна, Георгиевский Виктор Петрович, Дихтярев Сергей Иванович, Тимченко Николай Михайлович, Мдгварели Вадим Анатолиевич, Мирошников Владимир Александрович
МПК / Мітки
МПК: A61P 7/00, A61K 31/01, A61K 33/26
Мітки: залізодефіцитної, лікування, анемії, засіб, феррофол
Код посилання
<a href="https://ua.patents.su/7-40656-zasib-ferrofol-dlya-likuvannya-zalizodeficitno-anemi.html" target="_blank" rel="follow" title="База патентів України">Засіб “феррофол” для лікування залізодефіцитної анемії</a>
Попередній патент: Засіб для лікування гнійно-некротичних процесів
Наступний патент: Спосіб глушення шуму двигуна внутрішнього згорання і пристрій для його здійснення
Випадковий патент: Нелінійний радіолокатор