Спосіб кількісного визначення формальдегіду в організмі тварин при умовах, наближених до in vivo
Номер патенту: 93589
Опубліковано: 10.10.2014
Автори: Шандренко Сергій Григорович, Савчук Марина Миколаївна, Токарчук Катерина Олександрівна, Крисюк Ірина Павлівна
Формула / Реферат
1. Спосіб кількісного визначення вмісту ендогенного формальдегіду в організмі тварин, шляхом введення тваринам димедону, з подальшим визначенням в зразках крові комплексу формалдимедону, який відрізняється тим, що спочатку тваринам вводять димедон нормального складу, потім отримують зразки крові й тканин органів та визначають концентрацію утвореного формалдимедону флуоресцентним методом.
2. Спосіб за п. 1, який відрізняється тим, що вміст формалдимедону в біологічних зразках визначають будь-яким іншим методом.
3. Спосіб за п. 1, який відрізняється тим, що разом з димедоном вводять будь-який інший додатковий компонент або їх суміш, що не впливають на обмін альдегідів в організмі тварин.
Текст
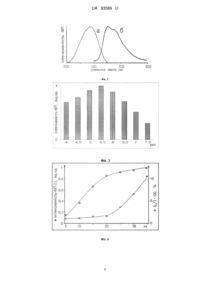
Реферат: Спосіб кількісного визначення вмісту ендогенного формальдегіду в організмі тварин, шляхом введення тваринам димедону, з подальшим визначенням в зразках крові комплексу формалдимедону, при якому спочатку тваринам вводять димедон нормального складу, потім отримують зразки крові й тканин органів та визначають концентрацію утвореного формалдимедону флуоресцентним методом. UA 93589 U (54) СПОСІБ КІЛЬКІСНОГО ВИЗНАЧЕННЯ ФОРМАЛЬДЕГІДУ В ОРГАНІЗМІ ТВАРИН ПРИ УМОВАХ, НАБЛИЖЕНИХ ДО IN VIVO UA 93589 U UA 93589 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель належить до експериментальної біології для кількісного визначення вмісту ендогенних альдегідів, що може бути використано для виявлення їх впливу на біологічні процеси, небажаних побічних ефектів, що виникають при оксидативному та карбонільному стресах, спричинених різноманітними захворюваннями (діабет, хвороба Альцгеймера, серцевосудинні захворювання і т. ін.). В організмі людини формальдегід (ФА) утворюється ендогенно в процесі метаболізму амінокислот і ксенобіотиків та може надходити з екзогенних джерел. Формальдегід проявляє мутагенну, генотоксичну, імуногенну та канцерогенну дії, є одним із чинників розвитку злоякісних новоутворень дихальної системи та лейкемії у людини, здатний утворювати інтрамолекулярні зшивки в білках і нуклеїнових кислотах та міжмолекулярні зв'язки між цими сполуками. Серед ендогенних альдегідів ФА відрізняється особливостями метаболізму, а також здатністю легко алкілювати аміногрупи амінокислот і основ нуклеїнових кислот, утворюючи гідроксиметильні аддукти і поперечні зшивки у вигляді метиленових містків в макромолекулах і між ними, включаючи і такі небезпечні в генотоксичному відношенні як ДНК-гістонові. Метаболізм ФА тісно пов'язаний з метаболізмом оксиду азоту (NO), наприклад, через залежний від глутатіону формальдегіддегідрогеназний шлях відновлення S-нітрозоглутатіону, перетворення тіопроліну і металотіонеїнів, включаючи реакції нітрозування, NO-синтазну, семікарбазидчутливу аміноксидазну (SSAO) системи [1]. Одним із шляхів регуляції ФА є ферментативна реакція за участі семікарбазидчутливої амінооксидази, яка утворює ФА із метиламіну-інтермедіату катаболізму креатину, фосфатидилхоліну, адреналіну та деяких ксенобіотиків. Інший шлях реалізується через здатність семікарбазиду напряму зв'язувати ФА у комплекс, утворюючи семікарбазон: Н2СО + H3NNHC(=O)NH2 → Н2С = NNHC(=O)NH2, та ефективно зменшувати його рівень в організмі [2]. Відомо, що найбільш поширеним способом визначення ФА є спосіб, який базується на реакції ФА з 2,4-динітрофенілгідразином із утворенням гідразону, кількісний аналіз якого проводять за допомогою HPLC- або газової хроматографії [3]. Відомо, що вміст ФА визначають в лужному середовищі, де ФА в реакції з реактивом пурпалд (4-аміно-3-гідразин-5-меркапто-1,2,4-триазол) утворює забарвлений продукт фіолетового кольору, кількісний вміст якого визначають фотометрично при довжині хвилі поглинання 550 [4]. Відомо, що вміст ФА визначають в кислому середовищі при підвищеній температурі, де ФА в реакції з хромотропною кислотою (4,5-дигідроксинафталін-2,7-дисульфокислота) утворює забарвлений комплекс малинового кольору, кількісний вміст якого визначають фотометрично при довжині хвилі поглинання 570 нм [5]. Відомо, що ФА визначають в реакції взаємодії ФА з реактивом Nash та ацетилацетоном, в результаті чого в присутності іонів амонію утворюється 3,5-диоктил-1,4-дигідролутидин, кількісний аналіз якого проводять флуоресцентним (при λ збудж. 370 нм, λпогл. 470 нм) або фотометричним (при λпогл. 412 нм) методами [6]. Відомо, що в сучасній модифікації кількість продуктів реакції ФА визначають за допомогою проточної флуоресцентної системи [7]. + Відомо, що у ферментативному методі визначення ФА використовують глутатіон- та NAD залежну формальдегіддегідрогеназу, яка трансформує ФА до S-формілглутатіону, який потім визначають шляхом збільшення флуоресценції при 460 нм [8]. Відомо про імуноферментне визначення антитіл IgE та IgG до формальдегіду, кон'югованого з альбуміном [9]. Відомо, що для визначення концентрації ФА у біологічних зразках використовують димедон (5,5-диметилциклогексан-1,3-діон), який є комплексоном до альдегідів. Останній утворює з ФА стабільний комплекс - формалдимедон (ФД), концентрацію якого визначають методом HPLC [10] або флуоресцентним методом в проточній системі [11]. Основним недоліком визначення ФА в організмі тварин за наведеними вище способами [311] є те, що концентрацію ФА в біологічних зразках (кров, тканини органів, сеча, слина) визначають в умовах in vitro, тобто після забору біологічного матеріалу. ФА - відносно стабільна сполука, однак, в біологічному середовищі є хімічно активною. ФА активно реагує з аміногрупами амінокислот, із азотистими основами нуклеїнових кислот, із глутатіоном і цистеїном, а також катаболізується формальдегіддегідрогеназою. Зміни в метаболізмі, що відбуваються при забої тварин і підготовці проб біоматеріалу можуть суттєво впливати на вміст у ньому ФА. Недоліком визначення концентрації ФА в біологічних зразках в умовах in vitro є те, що визначена за таких умов його концентрація може відрізнятися від справжнього рівня ФА, що призводить до некоректної оцінки стану обміну ФА в організмі. На користь такого твердження 1 UA 93589 U 5 10 15 20 25 30 35 40 45 50 55 свідчать експериментальні роботи [12-15]. Так, при інгаляційній експозиції тварин (щурів, мавп) у збагаченому ФА (14,4 ppm) газовому середовищі протягом 2-х годин визначена в умовах in vitro концентрація ФА у зразках крові та тканинах органів не відрізнялася від цього показника в контрольній групі тварин. Аналогічні результати були отримані в дослідженнях з добровольцями, які протягом 40 хв вдихали повітря, яке містило 1,8 ppm ФА [14]. Для коректної оцінки обміну ФА в організмі необхідно використовувати методи, що наближені до умов in vivo. Найближчим аналогом способу, що заявляється, є спосіб, де для визначення рівня ФА 14 тваринам вводять ізотоп - мічений С димедон, а потім в зразках крові радіометричним методом визначають комплекс ФД [16]. Недоліком такого визначення є те, що для даного способу використовуються радіоактивні ізотопи та високовартісне обладнання. Суть корисної моделі, що заявляється, полягає в розробці способу кількісного визначення ФА в організмі тварин при умовах, наближених до in vivo. Поставлену задачу вирішують шляхом зв'язування ФА в організмі експериментальних тварин димедоном нормального складу (далі - димедоном) в умовах in vivo, з подальшим визначенням у зразках тканин органів та(або) крові кількісного вмісту утвореного стабільного комплексу формалдимедону (ФД) флуоресцентним методом. Технічним рішенням способу, що заявляється, є кількісне визначення ФА при умовах, наближених до in vivo, що є коректною оцінкою рівня ФА в організмі тварин порівняно з визначенням цього показника in vitro. ФА в організмі тварини спочатку зв'язується в умовах in vivo димедоном з утворенням ФД, що дає можливість в подальшому кількісно визначити концентрацію утвореного комплексу в тканинах органів в умовах in vitro флуоресцентним методом [17] (фіг. 1, 2). Фіг.1. Хімічна схема способу визначення концентрації формальдегіду в організмі тварин. Фіг.2. Спектр флуоресценції формалдимедону (а: спектр збудження при λem = 460 нм; б: спектр збудження при λех = 380 нм) Фіг.3 Залежність інтенсивності флуоресценції формальдимедону від рН буферу оцтовокислий амоній/оцтова кислота. Фіг.4 Залежність інтенсивності флуоресценції формалдмедону I (O) та частки фонової флуоресценції І0/І (Δ) від часу прогрівання 100 Сº за концентрацій димедону – 2мМ, ФА 0,2мМ(pH 5,5). Фіг.5. Залежність інтенсивності флуоресценції формалдимедону від концентрації формальдегіду. Водорозчинний димедон при перитоніальному введенні тварині швидко розподіляється по тканинах різних органів; в реакції з ФА утворює ФД (фіг. 1), що є стабільною за фізіологічних умов сполукою з гідрофобними властивостями, за рахунок чого накопичується в клітинах і тканинах організму, та інтенсивність утворення його характеризує рівень ФА. При обробці зразків біологічного матеріалу за високої температури ФД в присутності джерела азоту утворює комплекс, що має в хімічній структурі піридинове кільце з флуоресцентними властивостями (фіг. 1). В якості азотвмісної сполуки використовують розчин оцтовокислого амонію. Оптимальними умовами утворення кінцевого флуоресцентного продукту ФД, визначеними за залежністю інтенсивності флуоресценції від рН розчину оцтовокислого амонію, підведеного до необхідного значення рН оцтовою кислотою, є діапазон рН: 5-6 (фіг. 3). Оптимальний час витримування модельних зразків при температурі 100 ºC, визначений за графіком залежності їх інтенсивності флуоресценції від часу прогрівання, складає 20 хв (фіг. 4). При більш тривалому прогріванні зразків суттєво зменшувався приріст інтенсивності флуоресценції (ΔI/Δt) та збільшувався приріст частки фонової флуоресценції (Δ(І 0/І)/Δt). Чутливість методу визначення концентрації ФА у воді сягає одиниць нМ, але, враховуючи інтенсивність «фонової» флуоресценції біологічних зразків, реальна чутливість методу зменшується майже на три порядки та становить одиниці мкМ. Залежність інтенсивності флуоресценції кінцевого продукту від концентрації ФА має лінійний характер у широкому діапазоні (фіг. 5). Приклад У способі, що заявляється, використовують самців щурів лінії Wistar масою 220-240 г, раціон харчування яких складається з концентрованого гранульованого комбікорму. Тварин розподіляють на 4 групи по 6 тварин в кожній: група № 1 - контрольна; щурам інших груп вводять разово перорально наступні ефектори: група № 2 - водний розчин ФА в дозі 10 мг/кг за 40 хвилин до забою; група № 3 - водний розчин метиламіну в дозі 250 мг/кг за 2 години до забою; група № 4 - водний розчин семікарбазиду в дозі 200 мг/кг за 2 години до забою. За 30 2 UA 93589 U 5 10 15 хв до завершення експерименту всім тваринам вводять перитоніально 1 %-й розчин димедону на фізіологічному розчині в дозі 100 мг/кг. [17] Кількість утвореного ФД, який є флуоресцентним продуктом, визначають у відповідно підготовлених зразках тканини печінки на флуориметрі FL800 (Biotek, США) при λех = 360 нм, λem = 420 нм. Розрахунки проводять за калібрувальною кривою стандартних розчинів ФД. Статистичну обробку проводять в програмі Statistica, достовірність змін оцінюють за tкритерієм Стьюдента. Ефективність розробленого методу перевіряють на декількох моделях модифікації рівня ФА у щурів [17]. Апробацію розробленого методу проводять на моделі модифікації обміну ФА в організмі за рахунок введення субстрату або інгібітору SSAO. Так, при разовому пероральному введенні метиламіну рівень ФА у зразках тканини печінки підвищується на 28 %. При разовому пероральному введенні семікарбазиду - інгібітору SSAO, цей параметр зменшується на 57 % (таблиця 1). Таке значне зменшення кількості ФА в організмі може бути обумовлено наявністю двох шляхів впливу семікарбазиду на обмін ФА, які описані вище. Таблиця 1 Вміст формальдегіду в зразках тканини печінки при введенні щурам формальдегіду, метиламіну, та семікарбазиду Групи тварин № 1 - контроль № 2 - формальдегід № 3 - метиламін № 4 - семікарбазид Зміна Концентрація ФА, концентрації ФА, мкг/г % 4,2±1,4 0 7,5±1,5* +78 5,4±0,9* +28 2,4±0,7* -57 Примітка: * - статистично достовірна різниця (р
ДивитисяДодаткова інформація
Автори англійськоюShandrenko Serhii Hryhorovych
Автори російськоюШандренко Сергий Григорьевич
МПК / Мітки
МПК: C07C 45/75
Мітки: визначення, тварин, умовах, формальдегіду, організмі, наближених, спосіб, кількісного
Код посилання
<a href="https://ua.patents.su/8-93589-sposib-kilkisnogo-viznachennya-formaldegidu-v-organizmi-tvarin-pri-umovakh-nablizhenikh-do-in-vivo.html" target="_blank" rel="follow" title="База патентів України">Спосіб кількісного визначення формальдегіду в організмі тварин при умовах, наближених до in vivo</a>
Попередній патент: Вузол з’єднання стержнів сітчастого купола
Наступний патент: Очисний комбайн
Випадковий патент: Новорічна штучна ялинка "люм'єр-03"