Спосіб визначення інфаркту та пристрій для його здійснення.
Номер патенту: 20935
Опубліковано: 07.10.1997
Автори: Морозкін Володимир Васильович, Костюшова Лілія Антонівна, Макулькин Руслан Федорович, Тимчишин Олег Львович, Запорожан Валерій Миколаєвич, Костюшов Володимир Васильович, Юрлов Владислав Михайлович, Мандрієвська Наталья Михайлівна, Костюшов Євгеній Васильович, Карповський Юхим Якович
Формула / Реферат
1. Способ определения инфаркта путем исследования сыворотки крови, отличающийся тем, что осуществляют амперометрическое титрование депротеинизированной сыворотки крови на наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, и по их появлению судят о наличии инфаркта.
2. Устройство для амперометрического титрования, включающее индикаторный платиновый электрод, электрод сравнения, ячейку для титрования, магнитную мешалку, П-образный солевой мостик, микроамперметр и бюретку с титрантом, отличающееся тем, что дополнительно содержит термостат, связанный с дозатором подачи промывающей жидкости и буфера в ячейку, устройство удаления отработанных реагентов из нее, электронный стабилизатор ЭДС электрода сравнения, расположенный между микроамперметром и левой ветвью U-образного электрода сравнения, который заполнен металлической ртутью, причем в правой ветви электрода сравнения, над металлической ртутью находится раствор электролита, в который опущено колено солевого мостика, а в левую ветвь опущен медный проводник непосредственно в металлическую ртуть.
3. Устройство для амперометрического титрования по п. 2, отличающееся тем, что дополнительно содержит блок автоматизированного управления и обработки информации (БАУОИ), непосредственно связанный с электронным стабилизатором ЭДС и микроамперметром а также с дозатором подачи промывающей жидкости и буфера для титрования, устройством удаления отработанных реагентов из ячейки для титрования, магнитной мешалкой, бюреткой с титрантом и термостатом.
Текст
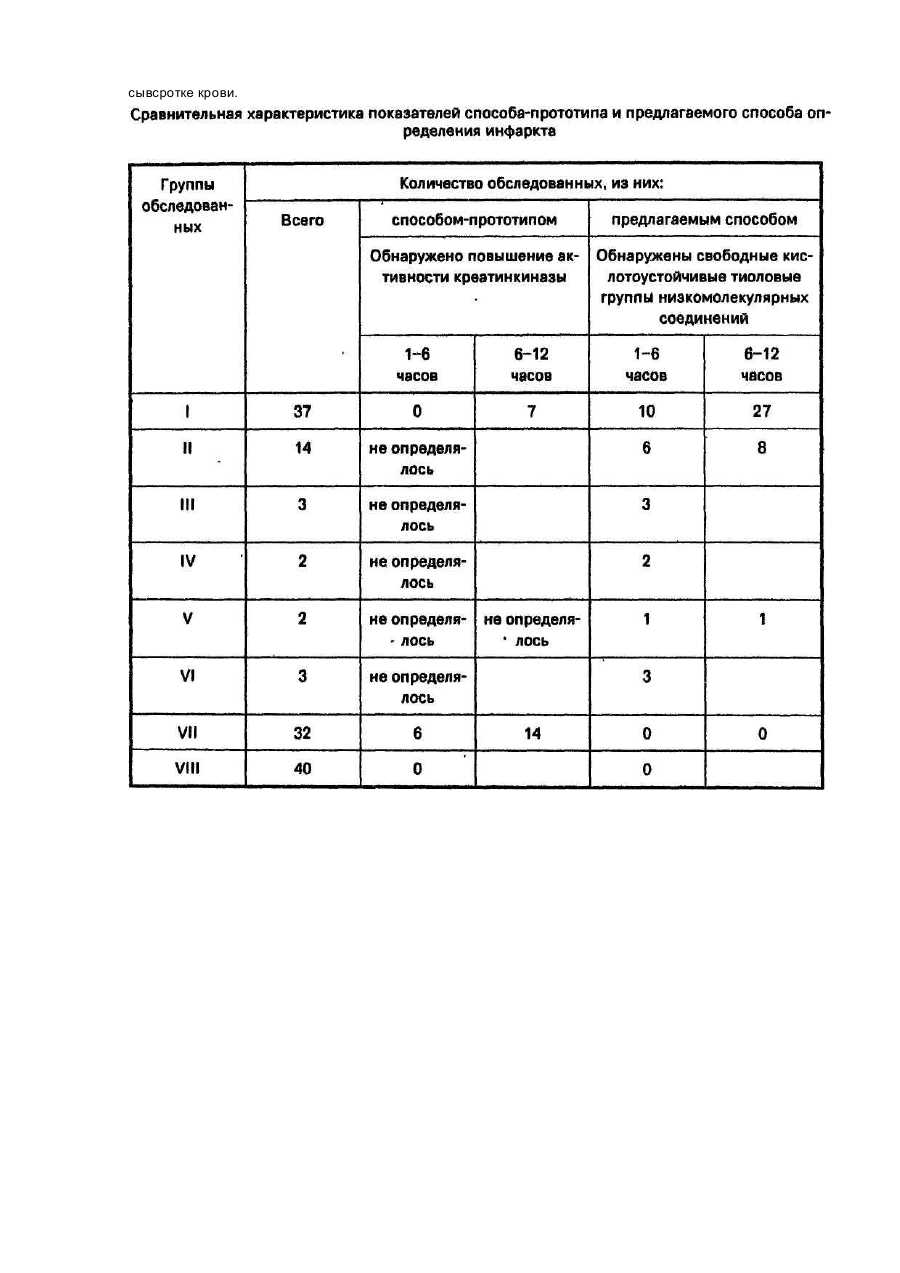
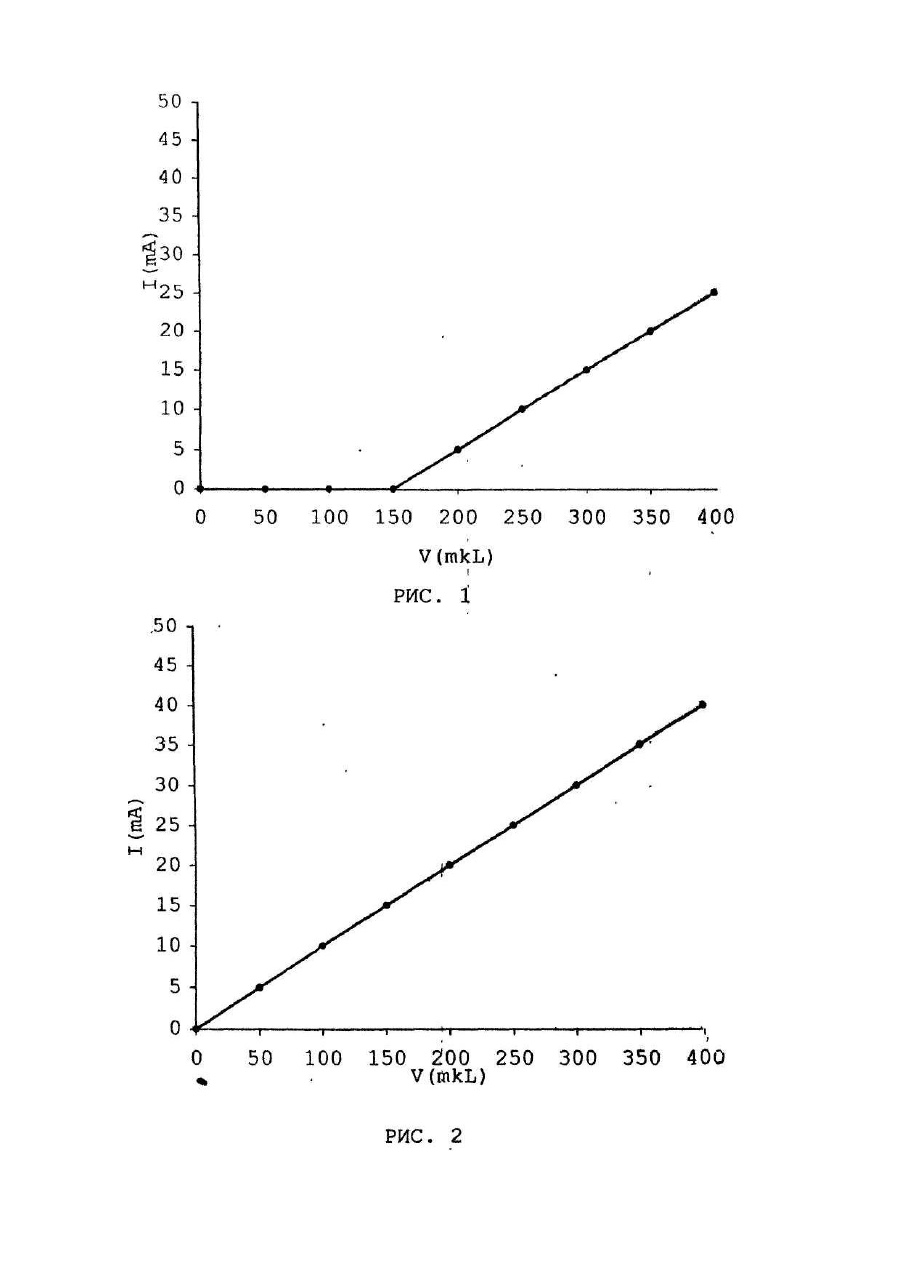
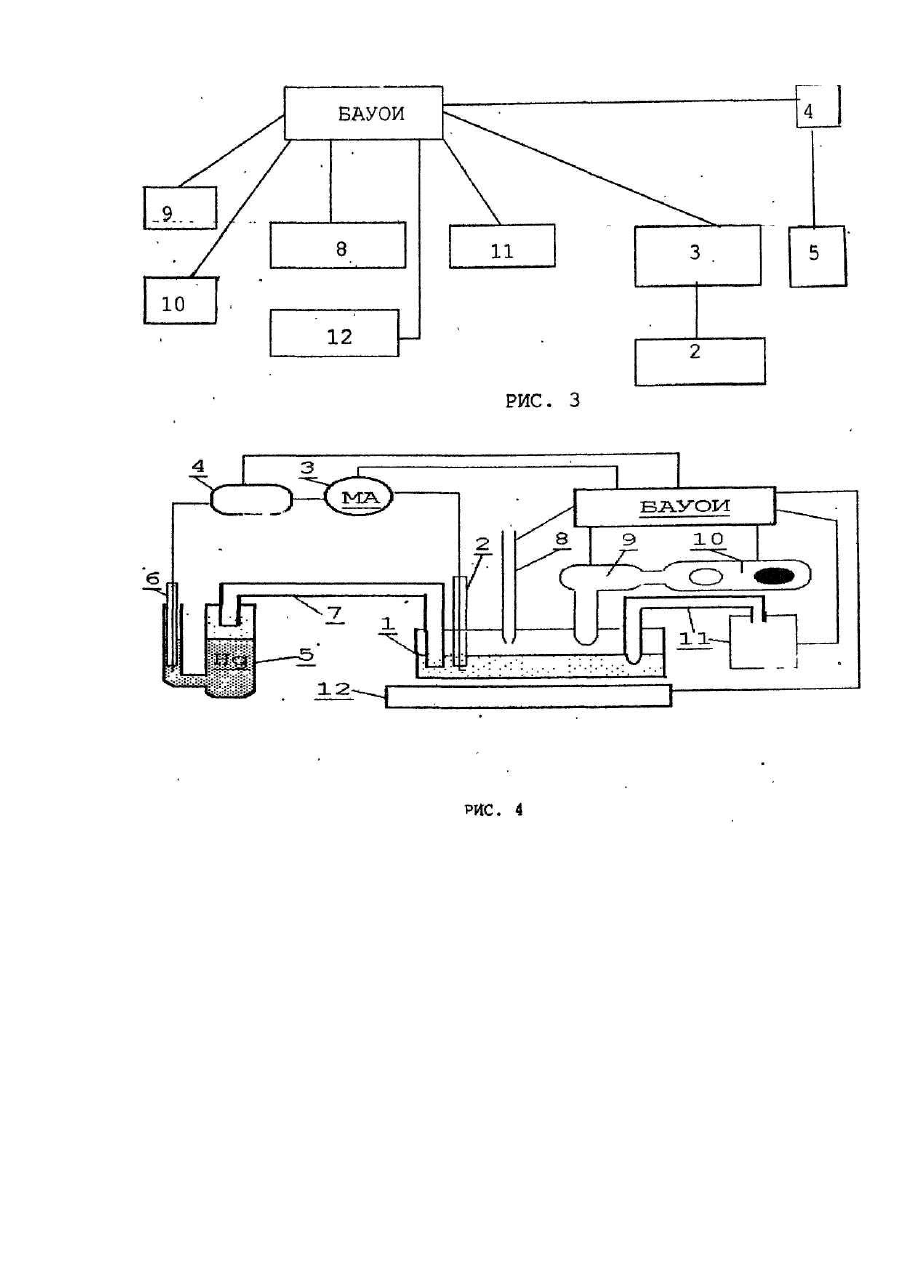
Изобретение относится к медицине и касается клинической биохимии и медицинского лабораторного оборудования, может быть использовано в терапии и хирургии. Согласно классификации и номенклатуры болезней, травм и причин смерти выделяют: инфаркт миокарда, инфаркт легкого, инфаркт мозга, инфаркт брызжейки, инфаркт кишечника, инфаркт печени, инфаркт почки ["Статистическая классификация болезней, травм и причин смерти" МКБ 9 -Адаптация I. М., 1984]. Как видно, характерное повреждение указанных выше внутренних органов объединено общим клиническим термином "инфаркт". Это стало возможным, вследствие общности патогенетических механизмов и патоморфологических изменений при формировании инфаркта внутренних органов [БМЭ. Изд. 3-е, 1978, Т.8. с. 309]. Все это явилось основанием для разработки заявляемого способа определения инфаркта, независимо от его локализации и поврежденного органа. Имеются различные способы определения инфаркта, например, инфаркта миокарда, путем исследования миоглобина в сыворотке крови. По повышению содержания миоглобина в сыворотке крови судят о наличии инфаркта миокарда [Староверов И., Масенко В., Филиппов И. и др. Значение серийного определения содержания миоглобина, ферментов и изоферментов для ранней диагностики инфаркта миокарда.Кардиология, t982, 22, № 5, с. 96-102]. Однако данный способ применяется в основном для диагностики инфаркта миокарда. Это связано с тем, что повышение содержания миоглобина при инфарктах головного мозга, печени, почек, селезенки, кишечника и пр. не происходит. Известный способ не специфичен, в связи с тем, что повышение содержания миоглобина в сыворотке крови отмечается не только при инфаркте, но и при воспалении, например, мышечной ткани (миокардиты, миозиты). Кроме того, способ не информативен в первые часы от момента возникновения инфаркта миокарда, так как повышение содержания миоглобина в сыворотке крови происходит только через 6-10 часов от момента возникновения повреждения миокарда. Известно устройство для амперометри-ческого титрования [Торчинский Ю.М. Суль-фгидрильные и дисульфидные группы белков. М., Наука, 1971, с. 92], которое представляет собой вращающийся индикаторный платиновый электрод, опущенный ячейку для титрования и соединенный через микроамперметр с электродом сравнения. Устройство снабжено солевым мостиком, заполненным гелем из агара с хлоридом калия, который с одной стороны опущен в ячейку для титрования, а с другой - в электрод сравнения. За прототип принят способ определения инфаркта миокарда путем исследования сыворотки крови, в которой определяют активность ферментов, например, креатинкиназы (КК). По повышению активности этого фермента в сыворотке крови судят о наличии у больного инфаркта миокарда [Диагностика и лечение внутренних болезней/Под общей ред. акад. РАМН Ф.И. Комарова. Т. 1. М., Медицина, 1996, с. 172-174]. Однако способ-прототип имеет следующие недостатки: он не применяется для определения инфаркта мозга (ишемический и геморрагический инсульт), инфаркта легкого, инфаркта селезенки, инфаркта почки и пр., в связи с тем, что при этих заболеваниях активность КК в сыворотке крови практически не изменяется. Способ-прототип не специфичен, так как повышение активности КК в сыворотке крови отмечается не только при инфаркте миокарда, но и при воспалительных процессах, например, гепатиты, миокардиты, циррозы печени и пр, Кроме того, он не информативен в первые часы от момента возникновения инфаркта миокарда, т.к. повышение активности КК в сыворотке крови происходит только через 6-12 часов от момента возникновения инфаркта миокарда. За прототип устройства принято устройство для амперометрического титрования [Соколовский В.В. Тиолдисульфидное соотношение крови как показатель состояния неспецифической резистентности организма // Учебное пособие. Санкт-Петербург, 1996, с. 15]. Устройство представляет собой ячейку для титрования, индикаторный платиновый электрод, электрод сравнения, П-об-разный солевой мостик, микроамперметр, бюретку с титрантом, магнитную мешалку. В ячейку для титрования опущены индикаторный платиновый электрод и бюретка с титрантом. Через микроамперметр индикаторный платиновый электрод связан с электродом сравнения. Солевой мостик связывает ячейку для титрования с электродом сравнения, причем электрод сравнения представляет собой конструкцию в виде небольшого стеклянного сосуда, заполненного металлической ртутью, над которой залит электролит. Сообщение микроамперметра с электродом сравнения осуществляется медным проводником через электролит, залитый над ртутью. Недостатками указанного выше известного устройства и устройства, принятого за прототип, с точки зрения возможности реализации предлагаемого способа, являются: нестабильная' величина ЭДС электрода сравнения; быстрое окисление медных проводников и выпадение солей меди в осадок, из-за их контакта с электролитом, нестабильные показания микроамперметра; низкое качество очистки ячейки для титрования от реагентов, осуществляемое ручным способом. Эти недостатки значительно снижают чувствительность устройства. Недостаточная чувствительность устройства не позволяет методом амперометрического титрования определять в депротеинизированной сыворотке крови наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. В основу изобретения по способу поставлена задача усовершенствования способа определения инфаркта, в котором, за счет амперометрического титрования свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, обеспечивается их выявление, что позволит определить инфаркт независимо от его локализации и поврежденного органа на ранней стадии его возникновения, а также повысить точность способа. Для реализации предлагаемого нами способа определения инфаркта, необходимо устройство с высокой чувствительностью, которое позволит методом амперометрического титрования определять в депротеинизированной сыворотке крови наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений.. В основу изобретения по устройству поставлена задача усовершенствования устройства для амперометрического титрования, в котором, за счет выполнения электрода сравнения в виде ІІ-образной формы, дополнительного введения электронного стабилизатора ЭДС электрода сравнения, дозатора подачи промывающей жидкости и буфера для титрования, устройства удаления отработанных реагентов, термостата, блока автоматизированного управления и обработки информации (БАУОИ), обеспечивается повышение чувствительности устройства, что позволит определять свободные кислотоустойчивые тиоловые группы низкомолекулярных соединений в депротеинизированной сыворотке крови с достаточной точностью. Поставленная задача по способу решается тем, что в способе определения инфаркта, путем исследования сыворотки крови, согласно изобретению, осуществляют амперометрическое титрование депротеинизированной сыворотки на наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, и по их появлению судят о наличии инфаркта, независимо от его локализации и поврежденного органе. Поставленная задача по устройству решается тем, что устройство для амперомет-рического титрования, включающее индикаторный платиновый электрод, электрод сравнения, ячейку для титрования, магнитную мешалку, П-образный солевой мостик, микроамперметр и бюретку с тит-рантом, согласно изобретению, дополнительно содержит термостат, связанный с дозатором подачи промывающей жидкости и буфера в ячейку для титрования, устройство удаления отработанных реагентов из нее и электронный сі абилизатор ЭДС электрода сравнения, расположенный между микроамперметром и левой ветвью и-образного электрода сравнения, который заполнен металлической ртутью, причем в правой ветви электрода сравнения, над металлической ртутью находится раствор электролита, в который опущено колесо П-образного солевого мостика, а в левую ветвь опущен медный проводник. Кроме того, дополнительно установлен БАУОИ, непосредственно связанный с электронным стабилизатором ЭДС и микроамперметром, а также с дозатором подачи промывающей жидкости и буфера для титрования, устройством удаления отработанных реагентов из ячейки для титрования, магнитной мешалкой, бюреткой с титрантом и термостатом. Заявляемый нами способ достаточно общий и высокоинформативный, так как позволяет выявлять изменения, характерные только для инфаркта, в аиде феномена появления свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, причем в первые часы от момента появления инфаркта и независимо от его локализации и поврежденного органа. Это подтверждается полученными нами данными о роли тиолопривных механизмов в формировании инфаркта. Так, при инфаркте, независимо от его локализации и поврежденного органа, мы впервые обнаружили феномен появления свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, о которые нами были определены при помощи заявляемого устройства. Этот феномен не определяется при других патологических процессах, например, при повреждении тканей обменнодистрофического характера, а также при воспалении, опухолевом росте и пр., но без формирования инфаркта. Известен способ определения тиоловых групп небелковой фракции, но в эритроцитах, лейкоцитах и других клетках, например, для определения интоксикации. Определение в сыворотке крови свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений методом амперометрического титрования неизвестно. Известны способы определения, например, инфаркта миокарда по повышению в сыворотке крови активности ферментов лактатдегидрогеназы (ЛДГ), креатинкиназы (КК), аспартатаминотрансферазы (АсАТ), а также миоглобина, но не известен способ определения инфаркта независимо от его локализации и поврежденного органа, путем исследования сыворотки крови, в которой методом амперометрического титрования определяют свободные кислотоустойчивые тиоловые группы низкомолекулярных соединений при помощи заявляемого устройства. В заявляемом устройстве выполнение электрода сравнения в виде U-образной формы позволит исключить контакт медных проводников с раствором электролита и окисление медных проводников, что предотвратит выпадение солей меди в осадок и стабилизирует электрохимические реакции. Это существенно повысит стабильность работы и чувствительность устройства для амперометрического титрования. Дополнительная установка электронного стабилизатора ЭДС электрода сравнения позволит регулировать электрохимические реакции в электроде сравнения, в результате чего обеспечивается стабильная величина ЭДС электрода сравнения. Дозатор подачи промывающей жидкости и буфера в ячейку для титрования позволит автоматизировать и стандартизовать дозирование реактивов. Устройство удаления отработанных реагентов из ячейки для титрования позволит автоматизировать удаление отработанных р, агентов и повысить качество очистки ячейки для титрования. Термостат предназначен для поддержания постоянного температурного режима реактивов и исследуемой сыворотки, который является обязательным условием. БАУОИ позволит автоматизировать процесс амперометрического титрования, учета и обработки информации. Таким образом, заявляемая совокупность признаков позволит повысить чувствительность устройства для амперометрического тит-рования, т.е. обеспечит возможность проведения амперометрического титрования свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови и, следовательно, реализацию заявляемого способа. На рис. 1 изображен график амперометрического титрования депротеинизмрованной сыворотки крови, на наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, свидетельствующий о их появлении, например у больных с диагнозом инфаркт миокарда. На рис, 2 показан график амперометрического титрования делротеинизированной сыворотки крови на наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, свидетельствующий об их отсутствии у практически здоровых лиц, а также у больных, у которых заболевание* возникло остро или протекало хронически в виде обострения, как результат инфекционных и неинфекционных поражений внутренних органов с признаками воспалительных, дистрофических, диспластических нарушений и пр., но без наличия патоморфологиче-ских изменений внутренних органов, характерных для инфаркта. На рис. 1 и рис. 2 по оси ординат откладывалась сила тока, а по оси абсцисс - количество раствора азотнокислого серебра, пошедшего на титрование. На рис. 3 показана блок-схема; на рис. 4 - общий вид устройства для осуществления заявляемого способа. Способ заключается в том, что производят забор венозной крови в количестве 5-7 мл в сухую стерильную пробирку, которую затем центрифугируют (3000 д, 5 минут). Сыворотку в количестве 2 мл отбирают в биохимическую пробирку для определения в ней содержания свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, а также в количестве 2,0 мл в биохимическую пробирку для исследования ее по способу-прототипу. В дальнейшем, согласно предлагаемого нами способа, осуществляют депротеинизацию, т.е. осаждение белков сыворотки крови, после чего в 1,0 мл депротеинизированной сыворотки крови определяют свободные кислотоустойчивые тиоловые группы низкомолекуляриых соединений методом амперометрического титрования на разработанном нами устройстве для амперометрического титрования, изображенном на рис. 4. Предлагаемое устройство для амперометрического титрования представляет собой ячейку для титрования (1), в которую з щен индикаторный платиновый электрод (2„ связанный через микроамперметр (3) и электронный стабилизатор ЭДС электрода сравнения (4) с электродом сравнения (5). Электрод сравнения (Б) представляет собой Іі-образнои Формы стеклянную трубку, заполненную ртутью. В левую ветвь элек-тоода сравнения (5), опущен медный проводник (8) непосредственно в ртуть. В правой ветви электрода сравнения, над ртутью находится раствор электролита, в который опущено левое колено Побразного солевого мостика (7). Правое колено П-образного солевого мостика (7) погружено в ячейку для титрования (1). Бюретка с титрантом (8) и дозатор подачи промывающей жидкости и буфера для титрования (9) опущены в ячейку для титрования (1). Термостат (10) связан с дозатором (9), Устройство удаления отработанных реагентов (11) непосредственно связано с ячейкой для титрования (1). Ячейка для титрования (1) установлена на магнитной мешалке (12). БАУОИ непосредственно связан с микроамперметром (3) и электронным стабилизатором ЭДС электрода сравнения (4), а также с дозатором подачи промывающей жидкости и буфера для титрования (9), термостатом (10), устройством удаления реагентов (11), магнитной мешалкой (12) и бюреткой с титрантом (8). Устройство для амперометрического титрования работает следующим образом: после включения в электрическую сеть происходит загрузка компьютерных программ БАУОИ, затем в автоматизированном режиме проводится подготовка устройства для• амперометрического титрования к работе: включается магнитная мешалка (12), термостат (10), который поддерживает постоянной температуру 37°С для аммиачного буфера и промывающей жидкости; промывается ячейка для титрования (1) при помощи устройства удаления отработанных реагентов (11), после чего ячейка для титрования (1) заполняется из дозатора подачи промывающей жидкости и буфера для титрования (9) аммиачным буфером в количестве 24,5 мл. Автоматически включается микроамперметр (3) и стабилизируется ЭДС электрода сравнения (5) при помощи электронного стабилизатора ЭДС (4). О готовности устройства для амперометрического титрования сообщается на мониторе БАУОИ. В автоматизированном режиме, в соответствующую "базу" БАУОИ вводятся паспортные данные пациента, которому будет проводиться определение свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. По команде с монитора БАУОИ в ячейку для титрования (1) вносят ручным способом дозирующей пипеткой депротеинизированную сыворотку крови в количестве 500 мкл и управляющей клавишей клавиатуры БАУОИ подают команду для начала амперометрического титрования. После этого, в автоматизированном режиме, из бюретки с титрантом (8) подается по 50 мкл раствора азотнокислого серебра. В ходе амперометрического титрования, содержащиеся в делротеинизированной сыворотке крови свободные кислотоустойчивые тиоло-. вые группы низкомолекулярных соединений, связывают ионы серебра с образованием меркаптида по уравнению реакции: По мере связывания ионов серебра со свободными кислотоустойчивыми тиоловыми группами низкомолекулярных соединений, стрелка микроамперметра (3) находится в стабильном положении равном "0". По достижении конечной точки титрования, когда ионы азотнокислого серебра прореагировали со всеми свободными кислотоустойчивыми тиоловыми группами низкомолекулярных соединений, в растворе появляется избыток ионов серебра, которые восстанавливаются на индикаторном платиновом электроде (2), что вызывает появление диффузного тока и стрелка микроамперметра (3) отклоняется от "0". После этого в ячейку для титрования дополнительно, 5 раз подается по 50 мкл раствор азотнокислого серебра и регистрируется диффузный ток (рис. 1). БАУОИ в автоматизированном режиме регистрирует показания микроамперметра (3) и рассчитывает количество азотнокислого серебра, затраченное на титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. В случае отсутствия в депротеинизирован-ной сыворотке крови свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, ионы серебра не связываются, и в растворе появляется их избыток, они восстанавливаются на индикаторном платиновом электроде (2), что вызывает появление диффузного тока сразу после добавления первой же порции азотнокислого серебра, в результате чего стрелка микроамперметра (3) отклоняется от "0" (рис. 2). Алгоритм расчета основан на графическом методе, представленном на рис. 1 и 2, где в прямоугольной системе координат автоматически наносятся точки, характеризующие величину тока (ось ординат) при соответствующем объеме азотнокислого серебра (ось абсцисс). Соединяя между собой точки, нанесенные на оси ординат и точки, нанесенные на оси абсцисс прямыми линиями, определяется точка их пересечения, которая и является конечной точкой титрования. Перпендикуляр, опущенный из конечной точки титрования на ось абсцисс, указывает на искомое количество азотнокислого серебра, пошедшего на титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. На рис. 1 - это количество составляет 150 мкл раствора азотнокислого серебра; а на рис. 2 -это количество составляет 0 мкл раствора азотнокислого серебра, так как, из-за отсутствия свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови при добавлении раствора азотнокислого серебра, сразу появляется диффузный ток. Учитывая, что 1 мкл раствора азотнокислого серебра эквивалентен 1 микромолю SH-групп (тиаловых групп), наличие содержания свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови согласно рис. 1 рассчитывается по известной формуле где C(SH) содержание свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений мкмоль/л); V(AgNO3) - объем раствора азотнокислого серебра, пошедшего на титрование (мкл); V - объем депротеинизированной сыворотки крови взятый на титрование (мкл); К - коэффициент разведения сыворотки крови. В дальнейшем БАУОИ, по специально разработанной программе, алгоритм которой основан на указанном выше графическом методе, в автоматизированном режиме рассчитывает содержание свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. Кроме того, учитывает и выдает результаты, а также формирует соответствующие "базы" данных, после чего на мониторе БАУОИ появляется сообщение об окончании амперометрического титрования. Управляющими клавишами клавиатуры БАУОИ подается команда на автоматизированное выключение микроамперметра (3), на промывку ячейки для титрования (1) и заполнение ее аммиачным буфером для дальнейшего проведения исследования следующему пациенту если это требуется. При необходимости, если исследования закончены, управляющей клавишей клавиатуры БАУОИ подается команда об окончании работы и установка для амперометрического титрования выключается из электрической с ти. Нами проведены исследования депротеинизированой сыворотки крови в следующих группах обследуемых: I группа - 37 больных с диагнозом инфаркт миокарда, обследованы в период от 1 до 6 часов с момента от начала заболевания - 10 больных, с 6 до 18 часов - 27 больных; II группа - 14 больных с диагнозом инфаркт мозга (ишемический и геморрагический инсульт), обследованы в период от 1 до б часов с момента от начала заболевания -6 больных, с 6 до 18 часов - 8 больных; III группа - 3 больных с диагнозом инфаркт почки, обследованы в период от 6 до 18 часов с момента от начала заболевания; IV - группа 2 - больных с диагнозом инфаркт селезенки, обследованы в период от 1 до 6 часов с момента от начала заболевания; V группа - 2 больных с диагнозом инфаркт легкого, обследованы в период от 1 до 6 часов с момента от начала заболевания -1 больной, с 6 до 18 часов - 1 больной; VI группа - 3 больных с диагнозом инфаркт кишечника, обследованы в период от 1 до 6 часов с момента от начала заболевания; VII группа (группа сравнения)- 32 больных, у которых заболевание возникло остро или протекало хронически в виде обострения, как результат инфекционных и неинфекционных поражений внутренних органов с признаками воспалительных, дистрофических, диспластических^ нарушений и пр., но без наличия патоморфологических изменений внутренних органов, характерных для инфаркта (острые респираторные инфекции, гипертоническая болезнь, ише-мическая болезнь сердца, острые панкреатиты, хронические гепатиты в стадии обострения и пр.), обследованы в период от 1 до 6 часов с момента от начала обострения заболевания - 11 человек, с б до 18 часов -21 человек; VIII - контрольная группа - 40 человек -практически здоровые лица. Получены следующие результаты: В I группе больных, в указанные часы от момента возникновения инфаркта миокарда, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низко-молекулярных соединений в количестве от 1 d до 52 мкмоль/л, у всех больных, что свидетельствует о наличии инфаркта. При параллельном исследовании сыворотки крови этих же больных способом-прототипом установлено, что повышение активности КК в первые 1-6 часов от момента возникновения инфаркта не обнаружено ни у одного обследованного, а в период от 6 до 18 часов повышение активности КК отмечено всего у 7 из 37 больных. У остальных больных этой группы (30 обследованных) не отмечено повышение активности КК и показатели практически не отличались от нормы. Во II группе больных, в указанные часы от момента возникновения инфаркта мозга, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в количестве от 10 до 57 мкмоль/л у всех больных, что свидетельствует о наличии инфаркта. В III группе больных, в указанные часы от момента возникновения инфаркта почки, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в де-протеинизированной сыворотке крови, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в количестве от 15 до 65 мкмоль/л у всех больных, что свидетельствует о наличии инфаркта. В IV группе больных, в указанные часы от момента возникновения инфаркта селезенки, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в количестве от 17 до 43 мкмоль/л у всех больных, что свидетельствует о наличии инфаркта. В V группе больных, в указанные часы от момента возникновения инфаркта легкого, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в количестве от 21 до 49 мкмоль/л у всех больных, что свидетельствует о наличии инфаркта. В VI группе больных, в указанные часы от момента возникновения инфаркта кишечника, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низко-молекулярных соединений в количестве от 28 до 50 мкмоль/л у всех больных, что свидетельствует о наличии инфаркта. В VII группе (группе сравнения) больных, в указанные часы от момента обострения заболевания, проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и ни у одного больного не было обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, т.е. их содержание составляло 0 мкмоль/л, что свидетельствует об отсутствии у этой группы больных инфаркта. Такие данные свидетельствуют, что при заболеваниях, не связанных с повреждением в виде инфаркта, свободные кислотоустойчивые тиоловые группы низкомолекулярных соединений в депротеинизированной сыворотке крови не появляются. При параллельном исследовании этой же сыворотки у больных VII группы способом-прототипом установлено, что активность КК у 12 больных не отличалась от нормальных показателей, а у 20 больных активность КК была повышена, из них у 7 больных с диагнозом хронический гепатит в стадии обострения; у 5 больных - ишемическая болезнь сердца, нестабильная форма стенокардии; у 8 больных - острый панкреатит. Такие данные свидетельствовали, что способ-прототип выявляет изменение активности КК не только при инфаркте миокарда, но и при других заболеваниях. В VIII контрольной группе (практически здоровых лиц) проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, и ни у одного из обследуемых не было обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. Это свидетельствует о том, что в сыворотке крови практически здоровых лиц отсутствуют свободные кислотоустойчивые тиоловые группы низкомолекулярных соединений, т.е. их количество составляет 0 мкмоль/л. При исследовании сыворотки крови способомпрототипом у лиц контрольной группы не было также выявлено повышение активности КК. Указанные выше диагнозы у больных I-VII групп были подтверждены клиническими данными, при помощи инструментальных, эндоскопических, функциональных, рентгенологических и клинико-лабораторных методов исследования. Кроме того, у 21 больного І- І групп заболевание закончилось летальным исходом, и у этих больных диагноз инфаркт был дополнительно подтвержден результатами патологоанатомического исследования. В связи с тем, что способ-прототип в основном используется для диагностики инфаркта миокарда, поэтому при инфарктах других внутренних органов, указанных во Н- І группах этот способ мы не применяли для сравнения с заявляемым способом. Однако сопоставление результатов исследований способом-прототипом с предлагаемым нами способом проводились, как указано выше, в I группе больных, у которых был диагноз инфаркт миокарда, а также в VII группе больных - группа сравнения и в VIII контрольной группе. Сравнительная характеристика показателей способа-прототипа и предлагаемого нами способа представлена в таблице. Данные таблицы свидетельствуют, что предлагаемый способ, в отличие от способапрототипа, позволяет в первые часы от момента возникновения инфаркта обнаружить характерные изменения в виде появления в депротеинизированной сыворотке крови свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений. Указанный показатель не был обнаружен при других заболеваниях (группа сравнения), а также у здоровых лиц (контрольная группа). Пример 1. Больной О-в, 1927 года рождения, доставлен в кардиореанимационное отделение 411 ОВГ 29.08.96 г., в 10 часов 25 минут с диагнозом: Ишемическая болезнь сердца; крупноочаговый заднеперегородочный инфаркт миокарда; диффузный мелкоочаговый кардиосклероз с нарушением ритма и проводимости. Заболел остро, 29,08.96 г., в 6 часов. Забор венозной крови был произведен в 10 часов 40 минут, т.е. спустя 4 часа 40 минут от начала заболевания. Проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови больного, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, содержание которых составило 52 мкмоль/л. Такие результаты подтверждали клинические данные и свидетельствовали о наличии у больного инфаркта. При параллельном исследовании сыворотки крови способом-прототипом активность КК составляла 70 U/L при норме до 240 U/L 23.09.96 г. больной 0-в умер. Патологоанатомический диагноз; Повторный трансмуральный инфаркт миокарда в заднеперегородочной области левого желудочка; крупноочаговый постинфарктный кардиосклероз; стенозирующий атеросклероз коронарной артерии (протокол вскрытия №157 от 23.09.96 г.). Пример 2. Больной Р-к., 1940 года рождения, доставлен в неврологическое отделение 411 ОВГ 27.03.96 г., в 13 часов 05 минут с диагнозом: Острое нарушение мозгового кровообращения по ишемическому типу в бассейне правой средней мозговой артерии; мозговая кома ІІ-ІІІ ст. Заболел остро 27.03.96 г., в 10 часов. Забор венозной крови осуществлен в 13 часов 40 минут, т.е. спустя 3 часа 40 минут от начала заболевания. Проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в делротеинизированной сыворотке крови больного, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений," содержание которых составило 49 мкмоль/л. Такие результаты подтверждали клинические данные и свидетельствовали о наличии у больного инфаркта. 09.04.96 г. больной Р-к умер. Патологоанатомический диагноз: Ишемический инфаркт левого полушария мозжечка на фоне церебрального атеросклероза; отек ткани головного мозга (протокол вскрытия № 53 от 10.04.96 г.). Пример 3. Больной К-в, 1957 года рождения, доставлен в реанимационное отделение 411 ОВГ 10.03.96 г. в 9 часов 20 минут с диагнозом: Сочетанная травма органов брюшной полости, острая почечная недостаточность. Заболел остро, 09.03.96 г., в 21 час. Забор венозной крови осуществлен в 9 часов 30 минут, т.е. спустя 12 часов 30 минут от начала заболевания. Проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови больного, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, содержание которых составило 25 мкмоль/л. Такие данные свидетельствовали о наличии у больного инфаркта. 14.03.96 г. на фоне нарастающей почечной недостаточности больной умер. Патоло-гоанатомический диагноз: Ушиб обеих почек; тромбоз почечной артерии левой почки, инфаркт левой почки (протокол вскрытия № 43 от 15.03.96 г.). Пример 4. Больной К-а. 1977 года рождения, доставлен в кардиологическое отделение 411 ОВГ 25.09.96 г. по поводу острого бактериального эндокардита неясной этиологии. 27.09.96 г. в 10 часов 20 минут на фоне удовлетворительного состояния появились резкие боли в левом подреберье, иррадиирующие е спину и усиливающиеся при вдохе, появился выраженный френикуссимптом слева, симптомы раздражения брюшины, выраженная спленомегалия. 27.09.96 г. в 12 часов 20 минут произведен забор венозной крови, т.е. спустя 2 часа от начала заболевания. Проводилось амперометрическое титрование свободных кислотоустойчивых тиоло-вых групп низкомолекулярных соединений в депротеинизированной сыворотке крови больного, и обнаружено наличие свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений, содержание которых составило 34 мкмоль/л. Такие данные свидетельствовали о наличии у больного инфаркта. 16.10.96 г. больной К-а умер. Патолого-анатомический диагноз: Бактериальный бородавчатый эндокардит митрального клапана; тромбоэмболические осложнения: организующийся инфаркт селезенки (протокол вскрытия № 201 от 17.10.96 г.). Пример 5. Больной Ф-ц, 1932 года рождения, доставлен в кардиореанимационное отделение 411 ОВГ 17.05.96 г., в 17 часов 35 минут с диагнозом: Инфекционный эндокардит, инфекционно-токсическая фаза, умеренная активность, острое течение. Заболел остро, 17.05.96 г., в 14 часов. Забор венозной крови был произведен 17.05.96 г., в 17 часов 40 минут, т.е. спустя 3 часа 20 минут от начала заболевания. Проводилось амперометрическое титрование свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови больного, которые не были обнаружены. Такие результаты подтверждали клинические данные и свидетельствовали об отсутствии у больного инфаркта. Пример 6. Донор П-в, 1958 года рождения, практически здоров, сдавал кровь как резервный донор. Забор венозной крови был произведен 12 июня 1996 в 10 часов 20 минут. Проводилось амперометрическое титрование свободных кислотоустойчивых иоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, которые не были обнаружены. Такие данные свидетельствовали, что в норме, у практически здоровых лиц свободные кислотоустойчивые тиоловые группы низкомолекулярных соединений в сыворотке крови отсутствуют. Полученные нами результаты свидетельствуют о том, что предлагаемый нами способ является: - универсальным для инфаркта, т.к. при амперометрическом титровании на предлагаемом нами устройстве в депротеинизированной сыворотке крови определяются характерные изменения для инфаркта, независимо от его локализации и поврежденного органа, в виде появления свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений; - специфичным для инфаркта, т.к. нами обнаружены изменения характерные только при формировании инфаркта, независимо от его локализации и поврежденного органа, в виде появления свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений в депротеинизированной сыворотке крови, которые определялись на предлагаемом нами устройстве; такие изменения не характерны для практически здоровых лиц и для больных, заболевания которых не связаны с инфарктом; - чувствительным, т.к. характерные изменения в виде появления в депротеинизированной сыворотке крови свободных кислотоустойчивых тиоловых групп низкомолекулярных соединений обнаруживаются в первые часы от момента возникновения инфаркта, независимо от его локализации и поврежденного органа. В отличие от известных, заявляемое нами устройство является более точным, за счет повышения чувствительности устройства, поэтому позволяет методом ам-перометрического титрования выявлять свободные кислотоустойчивые тиоловые группы низкомолекулярных соединений в депротеинизированной сывсротке крови.
ДивитисяДодаткова інформація
Автори англійськоюKostiushov Volodymyr Vasyliovych, Zaporozhan Valerii Mykolaiovych, Yurlov Vladyslav Mykhailovych, Karpovskyi Yukhym Yakovych, Makulkin Ruslan Fedorovych, Kostiushov Yevhenii Vasyliovych, Tymchyshyn Oleh Lvovych, Kostiushova Lilia Antonivna, Morozkin Volodymyr Vasyliovych
Автори російськоюКостюшов Владимир Васильевич, Запорожан Валерий Николаевич, Юрлов Владислав Михайлович, Карповский Ефим Яковлевич, Макулькин Руслан Федорович, Костюшов Евгений Васильевич, Тимчишин Олег Львович, Костюшова Лилия Антоновна, Морозкин Владимир Васильевич
МПК / Мітки
МПК: A61B 10/00, G01N 27/26, A61B 5/05, G01N 33/50
Мітки: визначення, здійснення, спосіб, пристрій, інфаркту
Код посилання
<a href="https://ua.patents.su/9-20935-sposib-viznachennya-infarktu-ta-pristrijj-dlya-jjogo-zdijjsnennya.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення інфаркту та пристрій для його здійснення.</a>
Попередній патент: Система теплопостачання
Наступний патент: Спосіб визначення біологічної сумісності тканин
Випадковий патент: Пневматичний диференціатор