Одностадійний спосіб одержання 4-амінодифеніламіну
Формула / Реферат
1. Одностадійний спосіб одержання 4-амінодифеніламіну що включає завантаження нітробензолу в реакційну зону під тиском водню в присутності основи і каталізатора гідрування.
2. Спосіб за п. 1, в якому анілін також завантажують в реакційну зону.
3. Спосіб за п. 1 або п. 2, в якому нітробензол поступово додають в реакційну зону протягом періоду часу від 0,1 години до 10 годин.
4. Спосіб за будь-яким з пп. 1-3, в якому каталізатор гідрування являє собою каталізатор на основі благородного металу.
5. Спосіб за будь-яким з пп. 1-4, в якому основу вибирають з групи, що включає лужні метали, гідриди лужних металів, гідроксиди лужних металів, алкоксиди лужних металів, каталізатори фазового перенесення в поєднанні з основою, вибраною з гідроксиду тетразаміщеного амонію, де кожний заступник незалежно вибраний з алкілу, арилу або арилалкілу, гідроксиду алкілзаміщеного діамонію, солей ариламонію в поєднанні з основою і краун-ефірів в поєднанні з основою, амінних основ, і їх суміші.
6. Спосіб за будь-яким з пп. 1-4, в якому основу вибирають з (С1-С6)алкоксидів, і гідроксидів четвертинного амонію.
7. Спосіб за п. 6, в якому основа являє собою гідроксид тетраметиламонію.
8. Спосіб за п. 7, в якому молярне відношення нітробензолу до гідроксиду тетраметиламонію менше, ніж приблизно 1,0.
9. Спосіб за будь-яким з пп. 1-8, в якому молярне відношення аніліну до нітробензолу становить приблизно 4 до 1.
10. Спосіб за п. 1, в якому вказаний 4-амінодифеніламін далі гідрують для одержання алкілованого 4-амінодифеніламіну.
11 Спосіб за п. 1, в якому вказаний 4-амінодифеніламін додатково піддають реакції відновного алкілування для одержання алкілованого 4-амінодифеніламіну.
Текст
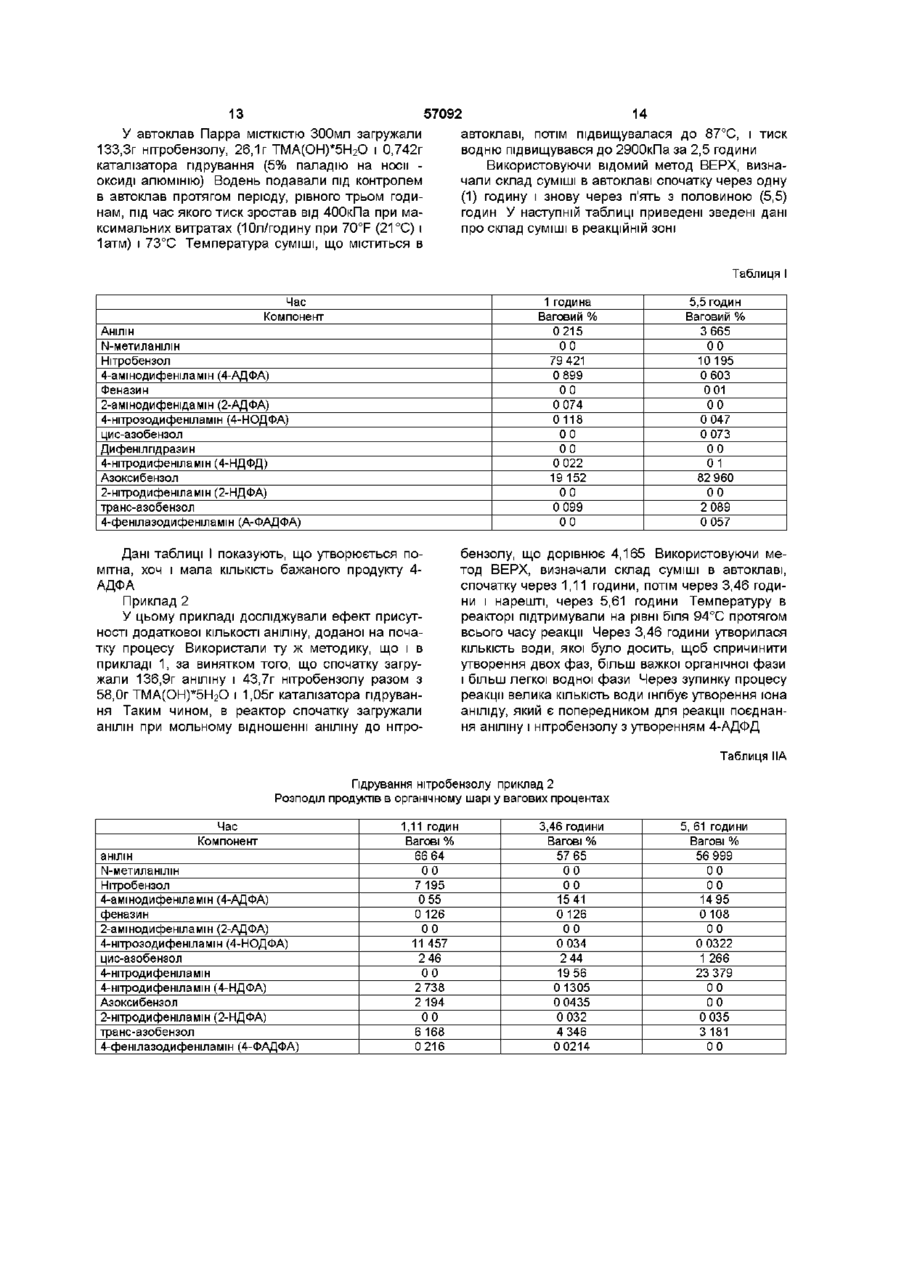
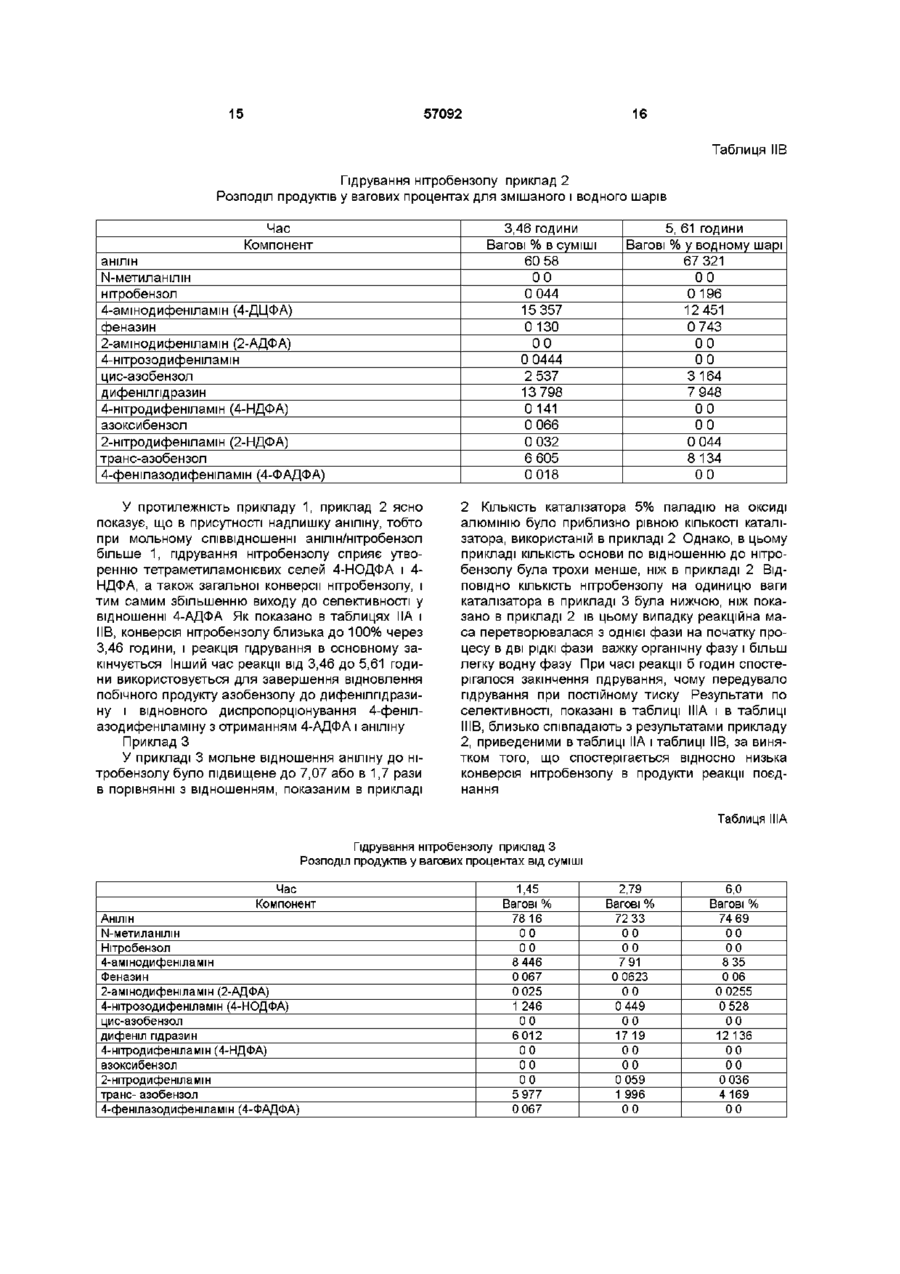
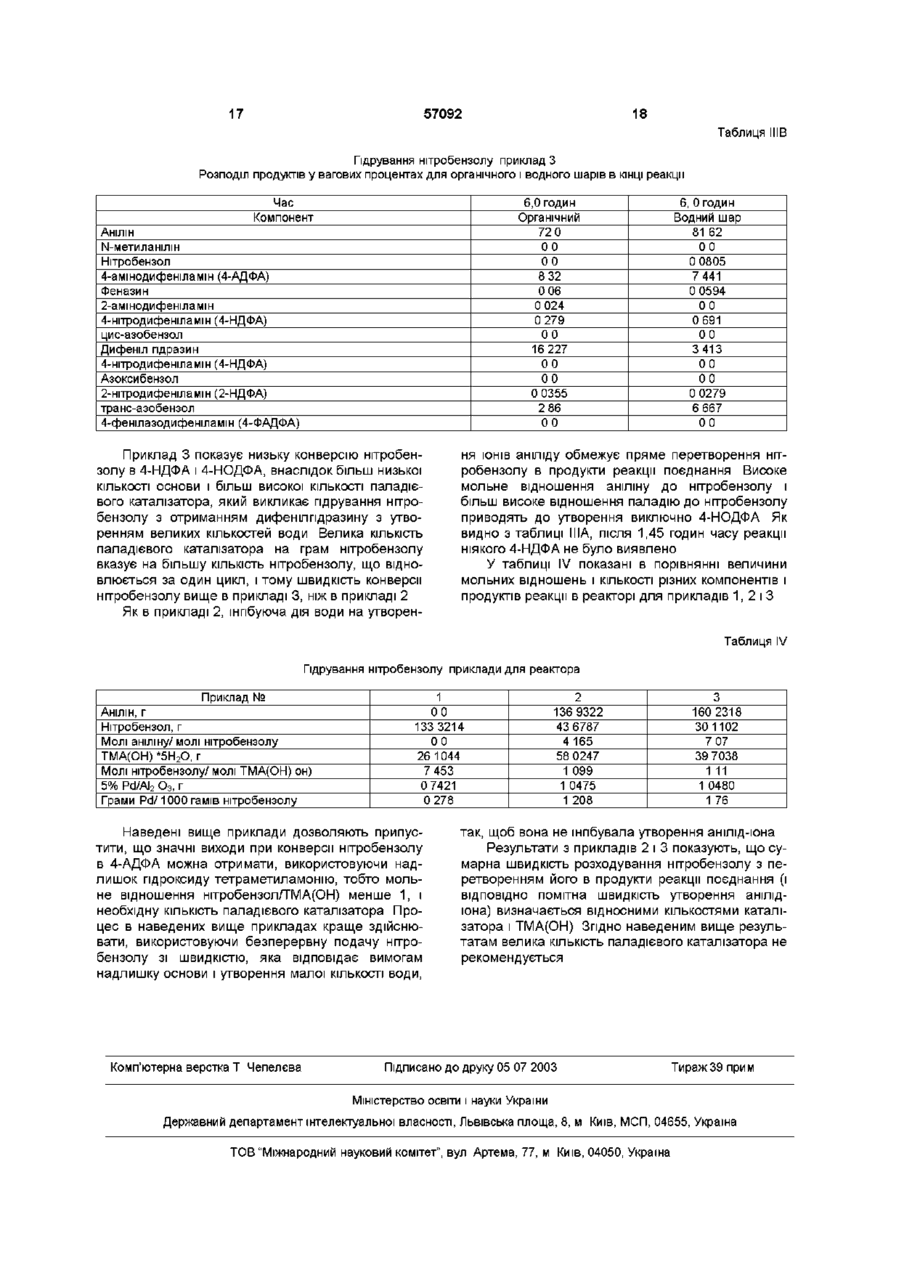
1 Одностадійний спосіб одержання 4амінодифеніламшу що включає завантаження нітробензолу в реакційну зону під тиском водню в присутності основи і каталізатора гідрування 2 Спосіб за п 1, в якому анілін також завантажують в реакційну зону 3 Спосіб за п 1 або п 2, в якому нітробензол поступово додають в реакційну зону протягом періоду часу від 0,1 години до 10 годин 4 Спосіб за будь-яким з пп 1-3, в якому каталізатор гідрування являє собою каталізатор на основі благородного металу Даний винахід відноситься до способу отримання 4-амінодифеніламшу (4-АДФА), важливого проміжного продукту для отримання заміщених парафенілендіамшів (ПФД), які є протистарителями для полімерів, особливо для каучуку Відомо, ЩО 4-АДФА отримують за механізмом нуклеофільного заміщення ароматичного кільця, при якому ПОХІДНІ аніліну заміняють галоген Цей спосіб включає отримання проміжного сполучення для 4-АДФА, а саме 4-нітродифеніламіну (4НДФА), і подальше відновлення нітрогрупи 4НДФА отримують реакцією п-хлорнітробензолу з похідним аніліну, таким як форманілід або його сіллю з лужним металом, в присутності акцептора кислоти або нейтралізуючого агента, такого як карбонат калію і, необов'язково, з використанням 5 Спосіб за будь-яким з пп 1-4, в якому основу вибирають з групи, що включає лужні метали, гідриди лужних металів, гідроксиди лужних металів, алкоксиди лужних металів, каталізатори фазового перенесення в поєднанні з основою, вибраною з гідроксиду тетразаміщеного амонію, де кожний заступник незалежно вибраний з алкілу, арилу або арилалкілу, гідроксиду алкілзаміщеного діамонію, солей ариламонію в поєднанні з основою і краун-ефірів в поєднанні з основою, змінних основ, і їх суміші 6 Спосіб за будь-яким з пп 1-4, в якому основу вибирають з (Сі-Сб)алкоксидів, і гідроксидів четвертинного амонію 7 Спосіб за п 6, в якому основа являє собою гідроксид тетраметиламонію 8 Спосіб за п 7, в якому молярне відношення нітробензолу до гідроксиду тетраметиламонію менше, ніж приблизно 1,0 9 Спосіб за будь-яким з пп 1-8, в якому молярне відношення аніліну до нітробензолу становить приблизно 4 до 1 10 Спосіб за п 1, в якому вказаний 4амінодифеніламш далі гідрують для одержання алкілованого 4-амінодифеніламшу 11 Спосіб за п 1, в якому вказаний 4амінодифеніламш додатково піддають реакції відновного алкілування для одержання алкілованого 4-амінодифеніламшу каталізатора Наприклад, патенти США №№ 4187248, 4683332, 4155936, 4670595, 412118, 4614817, 4209463, 4196146, 4187249, 4140716 Недолік цього способу полягає в тому, що галогенід, який замінюється, викликає корозію реакторів і забруднює стоки, і тому його необхідно видаляти, що вимагає значних витрат Крім того, використання похідних аніліну, таких як форманілід, і використання п-хлорнітробензолу вимагає додаткового виробничого обладнання і потужностей для отримання цих вихідних речовин з аніліну і нітробензолу ВІДПОВІДНО Відомо також, що 4-АДФА отримують шляхом реакції поєднання (конденсації) аніліну "голова до хвоста" Наприклад, патент Великобританії 1440767 і патент США № 4760186, Недоліком цьо О о> о ю 57092 го способу є те, що вихід 4-АДФА неприйнятний для промислового процесу Відомо також, що 4НДФА отримують декарбоксилюванням уретану Патент США № 3847990 Однак, такий спосіб, виходячи з його вартості і виходу, що отримується, непридатний для практичного застосування в промисловості Відомий спосіб отримання 4-АДФА гідруванням п-нітрозодифенілпдроксиламіну, який можна отримати каталітичною димерізацією нітрозобензолу, використовуючи в якості відновника аліфатичні сполуки, бензол, нафталін або етиленненасичені сполуки Наприклад, патенти США №№ 4178315 і 4404401 Відоме також отримання пнітрозодифеніламіну з дифеніламіну і алкілнітрату в присутності надлишку хлористого водню Наприклад, патенти США №№ 4518803 і 4479008 Також відоме отримання 4нітрозодифеніламіну реакцією ацетаніліду і нітробензолу в ДМСО в присутності гідроксиду натрію і карбонату калію при 80°С протягом 5 годин Див Ayyangar et al , Tetrahedron Letters, Vol 31, No 22, pp 3217-3220 (1990), також Wohl Chemishe Benchte, 36, p4135 (1903) і Chemishe Benchte, 34, p 2442 (1901) Однак, вихід нітрозодифеніламшу низький, і тому цей спосіб не підходить для практичного застосування в промисловості Крім того, при такому способі потрібне використання похідного аніліну, а саме ацетаніліду, що збільшує вартість вихідних речовин Відомий спосіб отримання 4-АДФА, що складається з послідовних стадій а) реакції аніліну з нітробензолом в присутності основи в умовах, що контролюються, з отриманням суміші, що містить солі 4-нітродифеніламшу і 4-нітрозодифеніламшу, і потім б) гідрування цих солей Такий спосіб описаний в патенті США № 5117063 У патенті США № 5420354 показаний інший спосіб отримання п-амшодифеніламіну взаємодією нітробензолу з воднем і аніліном в присутності каталізатора гідрування, шпбітора гідрування і кислотного каталізатора Хоч цей останній спосіб описаний як одностадійний, селективність відносно цільового продукту є відносно низькою За способом даного винаходу отримують 4АДФА в одностадійному процесі, в якому нітробензол загружають в реакційну зону під тиском водню в присутності сильної органічної основи і каталізатора гідрування РІЗНІ реакції проходять в одному і тому ж реакторі, переважно над нерухомим шаром каталізатора, внаслідок чого отримують 4-АДФА однією безперервною стадією технологічного процесу Крім того, спосіб даного винаходу набагато дешевше з точки зору виробничих витрат, а також витрат на сировині, що зумовлено зручністю проведення одностадійного процесу І, нарешті, цей спосіб має поліпшені показники виходу і селективності Короткий опис винаходу Даний винахід відноситься до способу отримання 4-АДФА, що включає загрузку нітробензолу в реакційну зону під тиском водню в присутності сильної органічної основи і каталізатора гідрування Цей спосіб забезпечує зручність і економічність одностадійного процесу і в той же час дає поліпшені показники виходу і селективності Крім того винахід відноситься до способу, в якому 4-АДФА, отриманий під тиском водню в згаданому вище процесі, далі гідрують з отриманням алкілованих парафенілендіамшів (ПФД), які є протистарителями і/або антиозонантами для полімерів, особливо для каучуку Ще одним способом даного винаходу є спосіб, в якому 4-АДФА пдроалкілують з отриманням алкілованого ПФД Більш конкретно, даний винахід відноситься до способу отримання 4-АДФА, проміжного продукту для отримання ПФД, в якому нітробензол в присутності сильної органічної основи загружають в реакційну зону під тиском водню Каталізатор гідрування загружають в реакційну зону на початку реакції, що протилежно способу, описаному в патенті США № 5453541, тих же заявників і включений сюди як посилання У цьому новому способі, реакція являє собою одностадійний процес, в якому нітробензол перетворюється в анілін, та ІНІЦІЮЄТЬСЯ реакція поєднання аніліну і нітробензолу по типу "голова до хвоста" в присутності сильної органічної основи Протікаючі внаслідок цього реакції дають суміш з високим вмістом проміжних продуктів для отримання 4-АДФА або його заміщених похідних, включаючи солі 4-нітродифеніламшу і/або 4-нітрозодифеніламшу, і потім 4-АДФА в якості продукту гідрування цієї суміші Ключовим моментом для отримання в даному процесі високого виходу і селективності у відношенні 4-АДФА є підбір таких умов проведення реакції, щоб отримати більше аніліну В противному разі вихід нітробензолу знижується внаслідок утворення азоксибензолу, і для виділення аніліну з азоксибензолу, що утворюється, потрібна ще одна стадія реакції, така як каталітичне гідрування азоксибензолу У способі даного винаходу 4-АДФА, що отримується, можна використати для отримання продуктів алкілування п-фенілендіамшу, які можна використати в якості антиоксидантів до антиозонантів Альтернативно, проміжні продукти для отримання 4-АДФА можна відновлювати, і відновлені продукти алкілувати в тому ж реакторі, використовуючи кетон в якості розчинника В одному варіанті здійснення винаходу, особлива увага звернена на молярне відношення нітробензолу до гідроксиду тетраметиламонію (ТМА(ОН)) У тому випадку, коли це відношення підтримується на рівні менше 1,0, підвищується селективність реакції гідрування, за допомогою якої нітробензол гідрується з отриманням 4-АДФА в одностадійному процесі, під тиском водню і в присутності сильної органічної основи, тобто ТМА(ОН), і каталізатора гідрування У іншому варіанті здійснення винаходу одностадійне гідрування нітробензолу з отриманням 4АДФА в присутності сильної органічної основи і каталізатора гідрування під тиском водню збільшується шляхом застосування в якості каталізатора благородного металу на відповідному носи, переважно паладію або платини, найбільш переважно паладію на вугіллі або оксиді алюмінію в якості носія Ще в одному варіанті здійснення винаходу вміст паладію, що використовується, контролюється, щоб оптимізувати вихід і селективність у відношенні 4-АДФА 57092 Ще в одному варіанті здійснення винаходу молярне відношення аніліну до нітробензолу контролюється таким чином, щоб оптимізувати вихід і селективність у відношенні 4-АДФА для одностадійного процесу перетворення, в якому нітробензол підлягає гідруванню з отриманням 4-АДФА під тиском водню і в присутності сильної органічної основи і каталізатора гідрування Альтернативно, анілін, хоч він утворюється в ході процесу гідрування, можна додатково вводити в реактор для того, щоб досягнути бажаного молярного співвідношення анілін/ нітробензол Докладний опис винаходу Спосіб отримання 4-АДФА, що є об'єктом винаходу, включає загрузку нітробензолу в обмежену зону під тиском водню і в присутності відповідної основи і каталізатора гідрування, і гідрування нітробензолу з отриманням 4-амінодифеніламшу (4-АДФА) Більш конкретно, винахід, що розглядається, включає загрузку нітробензолу в обмежену зону, що являє собою або реактор або реакційну зону, під тиском водню і в присутності сильної органічної основи і каталізатора гідрування В міру того як нітробензол гідрується, з нього утворюється анілін in situ, який реагує з частиною нітробензолу, утворюючи проміжні продукти для отримання 4-АДФА, особливо солі 4-нітродифеніламіну (4-НДФА) і 4нітрозодифеніламіну (4-НОДФА), нарівні з іншими продуктами реакції Далі в результаті гідрування ці проміжні продукти, 4-НДФА і 4-НОДФА, перетворюються в 4-АДФА по мірі протікання реакції Однією з переваг згаданого вище способу є можливість отримати 4-АДФА в одностадійному або проходячому в одному апараті процесі реакції Ключовим для отримання високого виходу і селективності у відношенні 4-амінодифеніламшу є такий вплив на реакцію, який дає збільшення утворення в реакції аніліну, в іншому випадку вихід знизиться внаслідок перетворення нітробензолу в азоксибензол, або буде потрібна ще одна стадія для отримання аніліну з азоксибензолу, така як каталітичне гідрування азоксибензолу Альтернативно, для отримання 4-АДФА можна збільшити утворення проміжних продуктів (4-НДФА і 4-НОДФА) шляхом введення окремої порції аніліну в зону реакції одночасно з нітробензолом Для отримання алкілованого ПФД, для якого 4АДФА є проміжним продуктом, спосіб, що розглядається, включає додаткову стадію гідрування 4АДФА, для здійснення перетворення в алкілований ПФД, що є протистарителем і антиозонантом для полімерів, особливо для каучуку Крім того, для отримання алкілованих п-фенілендіамінів спосіб, що розглядається, включає стадію відновного алкілування 4-АДФА, отриманого вище, з отриманням алкілованого ПФД Визначені декілька чинників, які мають важливе значення для оптимізацм одностадійного процесу, який запропонований тут для перетворення нітробензолу в 4-АДФА Одним з таких чинників є регулювання молярного відношення нітробензолу до основи ТМА(ОН) Це відношення повинне бути не більше, ніж 1,0 і переважно менш, ніж 1,0 При молярному відношенні нітробензолу до ТМА(ОН) більше 1,0 має місце негативний вплив на реакцію гідрування з отриманням 4-АДФА, який полягає в тому, що селективність зсувається у бік утворення азоксибензолу, аніліну і дифенілпдразину, а селективність по 4-амінодифеніламшу знижується Інший параметр одностадійного процесу цього винаходу заснований на підборі каталізатора гідрування, а також КІЛЬКОСТІ каталізатора і вмісту каталізатора на носи Ще одним чинником, який можна контролювати, щоб впливати на оптимізацію виходу і селективності у відношенні 4-АДФА, є молярне відношення аніліну до нітробензолу, що знаходиться в зоні реакції Молярне відношення аніліну до нітробензолу може змінюватися від великого надлишку нітробензолу до великого надлишку аніліну Переважно, реакцію проводять, використовуючи надлишок аніліну Співвідношення між 4-НДФА і 4НОДФА, що утворюються в ході реакції даного винаходу, можна регулювати шляхом зміни відношення аніліну до нітробензолу Наприклад, чим вище відношення аніліну до нітробензолу, тим вище відношення 4-НОДФА до 4-НДФА Переважною в цьому одностадійному процесі є така завантажування нітробензолу і аніліну, якщо він загружається, при якій досягається молярне відношення аніліну до нітробензолу, рівне 4 1 Це переважне тому, що можна легко здійснити регулювання селективності для отримання більш високої селективності у відношенні 4-АДФА Однак, при надмірній КІЛЬКОСТІ нітробензолу і при даній концентрації каталізатора гідрування деяка КІЛЬКІСТЬ нітробензолу буде втрачена внаслідок його перетворення в продукти відновлення нітробензолу, тобто в азоксибензол, азобензол і дифенілпдразин Крім вказаних вище чинників, істотним для одностадійного процесу є проведення процесу під тиском водню Тиск водню в реакційній зоні, згаданій тут, дає рушійну силу для здійснення гідрування в способі цього винаходу Для дуже активних каталізаторів гідрування, таких як каталізатори, що відносяться до класу благородних металів, манометричний тиск переважно знаходиться в інтервалі між 0 і 7000кПа, або при регулюванні витрат водню, або при регулюванні тиску Швидкість поглинання водню при регулюванні витрат однаково важлива для впливу на селективність у відношенні 4-нітрозодифеніламіну та ІНОДІ на селективність у відношенні 4амінодифеніламшу Використані витрати водню будуть залежати від типу і концентрації каталізатора Наприклад, активний каталізатор гідрування, такий як паладій на вугіллі, при високих концентраціях буде забезпечувати більше поглинання водню, що, ВІДПОВІДНО, буде сприяти відновленню нітробензолу з отриманням небажаних побічних продуктів, таких як азоксибензол, який знижує селективність у відношенні 4-АДФА У такій каталітичній системі витрати можуть бути відрегульовані для більш низьких тисків (таких як тиски нижче 700кПа) і більш високих концентрацій гідроксиду тетраметиламонію, ТМА(ОН), внаслідок чого збільшиться вихід 4-АДФА з нітробензолу Іншим аспектом даного винаходу є застосування основи, в присутності якої завантажений в 57092 реактор нітробензол гідрується ВІДПОВІДНІ ОСНОВИ включають, але не обмежуються ними, неорганічні основи, такі як, наприклад, лужні метали, такі як металевий натрій, гідриди, гідроксиди і алкоксиди лужних металів, такі як гідрид натрію, гідроксид ЛІТІЮ, гідроксид натрію, гідроксид цезію, гідроксид калію, трет-бутоксид калію і т п , включаючи їх суміші Переважними є сильні органічні основи, такі як алкоксиди лужних металів, такі як алкоксиди натрію або калію Інші прийнятні основи включають, але не обмежуються ними, каталізатори фазового перенесення в поєднанні з ВІДПОВІДНИМ джерелом основи, таким як гідроксиди тетраалкілзаміщеного амонію, в яких кожний замісник незалежно вибраний з алкільних, арильних або аралкільних груп, включаючи гідроксиди тетраалкіламонію, наприклад, гідроксид тетраметиламонію, гідроксиди арилтриалкіламонію, наприклад гідроксид фенілтриметиламонію, гідроксиди арилалкілтриалкіламонію, наприклад, гідроксид бензилтриметиламонію, алкілзаміщені гідроксиди діамонію, наприклад, гідроксид бісдибутилетилгексаметилендіамонію та ІНШІ поєднання каталізаторів фазового перенесення і ВІДПОВІДНИХ основ, такі як ВІДПОВІДНІ ОСНОВИ В поєднанні з солями ариламонію, краун-ефіром і т п і аміноутримуючі основи, такі як амід біс(триметилсиліл)літію і т п , включаючи їх суміші Переважними сполуками для використання в якості основи є гідроксиди тетраалкіламонію, такі як гідроксид тетраметиламонію (ТМА(ОН)) КІЛЬКІСТЬ основи, що використовується в даному процесі, може змінюватися в широких межах і залежить, наприклад, нарівні з іншими чинниками, від міри, до якої бажано збільшити або зменшити КІЛЬКІСТЬ певного продукту реакції Наприклад, реакція може бути проведена таким способом, при якому обмежується КІЛЬКІСТЬ основи, або реакція може бути проведена таким чином, коли обмежується КІЛЬКІСТЬ нітробензолу або аніліну Як було згадано раніше, основу необхідно використати в КІЛЬКОСТІ, достатній для того, щоб молярне відношення нітробензолу до ТМА(ОН) було меншим одиниці (1,0) Наприклад, при напівбезперервному способі проведення процесу основу додають в реакційну зону або вище, або нижче поверхні реакційної зони У цьому випадку основа переважно знаходиться в пдратованій формі, такій як дипдрат Крім того, в спосіб цього винаходу включене використання каталізатора гідрування Каталізатори гідрування добре ВІДОМІ В техніці Є цілий ряд типів каталізаторів, які придатні як каталізатори відновлення для даного винаходу Серед них наступні каталізатори, а також каталізатори аналогічної природи, мідь на оксиді алюмінію або на пемзі, оксид срібла-магнію на пемзі, оксид міді-церію на пемзі, оксид міді-марганцю або оксид залізамарганцю на пемзі, мідь на оксиді кремнію, платина на активованому вугіллі або на сажі, нікель на оксиді кремнію або кізельгурі, молібден або паладій на вугіллі або оксиді алюмінію з використанням інгібіторів каталізатора, таких як тюфен, тюмочевина, трифенілфосфіт, поліаміни, оксил магнію, морфолін і тюефіри, і каталізатори на основі сірчастих сполук благородних металів, з використанням реагентів для утворення сірчастих сполук, 8 таких як сірководень, сульфід натрію, сульфід амонію і д и мети л сульфоксид Потрібно вибирати такий каталізатор, щоб сповільнювати або інгібувати пряме гідрування нітробензолу до кінцевого продукту, такого як азоксибензол і замість цього давати можливість протікання реакції поєднання аніліну і нітробензолу Наприклад, використовуючи хроміт МІДІ, можна обмежити гідрування нітробензолу до азоксибензолу і спочатку збільшити швидкість реакції поєднання "голова до хвоста" аніліну і нітробензолу з отриманням солей 4-НОДФА і 4НДФА, які можна буде, при належному тиску, гідрувати безпосередньо з отриманням 4-АДФА Цей винахід, як описано тут вище, дає можливість отримувати 4-АДФА, використовуючи як ВИХІДНІ речовини тільки нітробензол, водень, органічну основу і каталізатор гідрування Окремі реакції, такі як поєднання "голова до хвоста" аніліну і нітробензолу і гідрування солей 4-НОДФА і 4-НДФА до 4-АДФА, не розділяються Крім того, при правильному підборі молярних відносин аніліну до нітробензолу і нітробензолу до органічної основи і при правильному ваговому відношенні органічної основи до каталізатора гідрування можна досягнути оптимальної селективності у відношенні 4АДФА без безперервного видалення протонної сполуки, такої як вода Однак, видалення протонної сполуки може збільшити селективність в деяких реакціях Ці ЧИННИКИ дають перевагу над винаходом, описаним в патенті США № 5453541, згаданим вище У даному винаході видалення протонної сполуки не є необхідним, поки виконуються вимоги збільшення селективності у відношенні 4-АДФА, які включають вибір належних молярних відносин аніліну до нітробензолу, нітробензолу до органічної основи і вагових відносин органічної основи до каталізатора гідрування, У даному винаході видалення води можна здійснювати для подальшого поліпшення селективності з використанням інших типів реакторів, таких як реактор безперервної дії з нерухомим шаром каталізатора гідрування, де для видалення води не потрібно вакуумних умов Крім того, отримання 4АДФА в даному винаході вимагає підвищеного тиску, значною мірою незалежно від видалення протонної сполуки, такої як вода В способі даного винаходу нітробензол переважно загружають в реакційну зону поступово, протягом деякого періоду часу, звичайно від 0,1 до 10 годин Температура в реакційній зоні переважно становить 90°С і підтримується постійною Манометричний тиск водню при регулюванні як по витратах, так і по тиску складає від 0 до приблизно ЗОООкПа При постійному тиску водню, незадовго до закінчення процесу, тиск складає від 2,757кПа доЗ,102кПа Оскільки нітробензол загружається протягом деякого проміжку часу, він спочатку підлягає реакції поєднання аніліну і нітробензолу по типу "голова до хвоста" з отриманням солей тетраметиламонію (ТМА) з 4-нітрозодифеніламшом і 4нітродифеніламіном У залежності від відношення аніліну до нітробензолу і концентрації каталізатора утворюються наступні продукти азоксибензол, азобензол, дифенілпдразин і 4-АДФА Наприклад, в присутності великого надлишку нітробензолу 57092 10 тримується між 20°С і 200°С, більш переважно від 80°СдоЮ0°С Хоч в якості реагентів вказуються нітробензол і анілін (якщо він використовується), в цьому способі також застосовні нітробензол або анілін, що містять один або більше замісників в ядрі, які не заважають реакції У способі цього винаходу може бути використаний розчинник або розріджувач, при умові, що він не заважає протікаючим в ньому реакціям ВІДПОВІДНІ системи розчинників включають, але не обмежуються ними, такі розчинники, як наприклад диметилсудьфоксид, N-метилпіролідон диметилформамід, анілін, піридин, нітробензол, неполярні вуглеводневі розчинники, такі як толуол і гексан, диметиловий ефір етиленгліколю, дизопропілетиламін, і подібні, а також їх суміші Крім того, в реакційну зону може бути загружена КІЛЬКІСТЬ аніліну в надлишку в порівнянні з тим, що необхідно для визначається КІЛЬКІСТЮ ВОДИ, ЩО утворилася в реареакції, і в цьому випадку такий надлишок аніліну кції відновлення, тому що при високому ВМІСТІ води буде служити розчинником (наприклад, порядку 4% по об'єму) реакція поєднання аніліну і нітробензолу "голова до хвоста" Термін "заміщені ПОХІДНІ аніліну", що викориссповільнюється, і реакція зсувається у бік утвотовується тут, означає анілін, що містить один або рення азоксибензолу більше електроноакцепторних або електронодонорних замісників в ароматичному КІЛЬЦІ ЗамісниСелективність у відношенні 4-АДФА можна таки, що застосовуються, включають, але не обмекож збільшити шляхом регулювання витрат водню жуються ними, галогеніди, NO2, Nbb, алкільні так, щоб поєднання "голова до хвоста" аніліну і групи, алкоксігрупи, -SO3, -СООН і арильні, аралкінітробензолу здійснювалося проти прямого гідрульні або алкарильні групи, що містять принаймні вання нітробензолу до кінцевого продукту, такого одну -NH2-rpyny Галоген іди вибрані з групи, що як азоксибензол Ці витрати водню при гідруванні складається з хлориду, броміду і фториду Перерегулюється так, щоб величина тиску знаходилася важні алькільні і алкоксигрупи містять від 1 до в нижній частині діапазону тиску приблизно 6 атомів вуглецю Переважні арильні, Інший альтернативний напівбезперевному аралкільні і алкарильні групи містять від приблизспособу є безперервний процес, в якому в неруно 6 до приблизно 18 атомів вуглецю Приклади хомий шар каталізатора гідрування безперервно заміщених похідних аніліну включають, але не подають анілін, нітробензол, водень і органічну обмежуються ними, 2-метоксианілш, 4основу, таку як пентапдрат гідроксиду тетраметиметоксианілін, 4-хлоранілін, п-толуїдин, 4ламонію, який заздалегідь розчинений в аніліні нітроанілін, 3-броманілш, З-бром-4-амшотолуол, пВеличини швидкості подачі цих потоків вихідних амінобензойну кислоту, 2, 4-діамшотолуол, 2,5речовин повинні відповідати величинам, які будуть дихлоранілін, 1,4-фенідендіамін, 4,4'давати максимальну селективність у відношенні 4АДФА, тобто молярне відношення аніліну до нітметилендіанілін, 1,3,5-триамшобензол та їх суміші робензолу переважно повинно становити 4 до 1 Азобензол також утворюється в цій реакції в або більше, і молярне відношення нітробензолу до різних кількостях в залежності від умов реакції органічної основи переважно близьке або менше Однак, азобензол є небажаним продуктом, оскіль1 КІЛЬКІСТЬ каталізатора гідрування, який повинен ки його утворення означає зниження виходу і севикористовуватися, є низькою при вході в реактор лективності у відношенні 4-АДФА Один з шляхів і поступово зростає до такої міри, щоб солі 4регулювання утворення азобензолу полягає в ЗМІНІ НОДФА і 4-НДФА перетворювалися в 4-АДФА відношення аніліну до нітробензолу Так, коли це Крім того, при застосуванні цього способу провевідношення збільшується, КІЛЬКІСТЬ азобензолу дення процесу полегшується безперервне видазвичайно зменшується Як обговорюється нижче і лення води, що сприяє підвищенню селективності як показано в прикладах, приведених нижче, ІНШІ у відношенні 4-ДЦФА ЗМІННІ, такі як КІЛЬКІСТЬ основи і кисню, можуть також впливати на КІЛЬКІСТЬ азобензолу, що утворюУ альтернативному періодичному способі проється Таким чином, використовуючи вказівки даведення процесу нітробензол можна загружати в ного винаходу, фахівець в даній області може реакційну зону весь відразу в такому співвіднопровести реакцію даного винаходу так, щоб контшенні, щоб число молей нітробензолу було менролювати КІЛЬКІСТЬ азобензолу, що утворюється шим числа молей органічної основи При цьому способі додавання необхідна певна КІЛЬКІСТЬ катаРеакція, що являє собою одностадійний пролізатора гідрування, так щоб частина нітробензолу цес, проводиться при ВІДПОВІДНІЙ температурі, яка не втрачалася при утворенні кінцевих продуктів, може змінюватися в широких межах Наприклад, таких як азоксибензол Однак, при завантажені температура може знаходитися в межах від приспочатку в реакційну зону аніліну, поступове додаблизно 80°С до приблизно 150°С, наприклад від вання нітробензолу є переважним для досягнення приблизно 80°С до приблизно 100°С, переважно більш високої селективності у відношенні 4-АДФА від приблизно 80°С до приблизно 90°С Найбільш переважною температурою для проведення реакТемпература реакційної зони переважно під(молярне відношення аніліну до нітробензолу значно менше одиниці або близько до нуля), основним побічним продуктом є азоксибензол 3 іншого боку, при надлишку аніліну (або коли молярне відношення аніліну до нітробензолу значно більше одиниці) ОСНОВНИМИ побічними продуктами є дифенілпдразин і азобензол Солі тетраметиламонію з 4-НОДФА і 4-НДФА каталітично відновлюються, даючи 4-АДФА і гідроксид тетраметиламонію Переважно при напівбезперевному способі проведення процесу нітробензол можна загружати протягом деякого часу, щоб досягнути максимально можливої селективності у відношенні 4-АДФА У цьому способі, КІЛЬКІСТЬ органічної основи, такої як ТМА(ОН), по відношенню до нітробензолу більше, і в присутності відповідної КІЛЬКОСТІ каталізатора гідрування можна отримати більш високу селективність у відношенні 4-АДФА Кінцева точка реакції 12 11 57092 ції даного винаходу є температура від приблизно Наприклад, патент США № 4900868 Перева80°С до приблизно 90°С, така як 85°С жно 4-АДФА і ВІДПОВІДНИЙ кетон або альдегід реагують в присутності водню і платини на вугіллі в Контроль КІЛЬКОСТІ води, що виділяється в якості каталізатора ВІДПОВІДНІ кетони включають процесі реакції, має важливе значення Вода утвометилізобутилкетон (МІБК), ацетон, метилізоамилрюється при відновленні нітробензолу в азоксибекетон і 2-октанон Потрібно зазначити, що відновнзол, при реакції поєднання "голова до хвоста" лення проміжних продуктів синтезу 4-АДФА і алкіаніліну і нітробензолу з утворенням ВІДПОВІДНИХ лування відновленої сполуки можна провести в солей 4-НОДФА і 4-НДФА і при відновленні солі 4тому ж самому реакційному апараті, використовуНДФА з отриманням 4-АДФА, Вода в реакційній ючи кетон в якості розчинника Наприклад, патент зоні інгібує реакцію аніліну з нітробензолом до США № 4463191 і статтю Banerjee et al , J Chem такої міри, коли реакція вже втрачає своє значенSoc Chem Comm 18,1275-76(1988) ня, тобто вихід 4-АДФА стає меншим бажаного Регулювання реакції таким чином, щоб КІЛЬКІСТЬ Передбачувані еквіваленти реагуючих речоводи, що утворюється, знизилася приблизно до вин і реагентів, описаних вище, являють собою концентрації 4%, приводить до того, що реакція реагуючі речовини і реагенти, в основному ВІДПОпротікає прийнятним образом У переважному ваВІДНІ описаним реагентам і маючи ті ж самі загальріанті здійснення винаходу, коли в якості основи ні властивості, в яких одна або більш ВІДМІННИХ використовується гідроксид тетраметиламонію, і в груп, наприклад NO2, є простими варіантами Крім якості розчинника використовується анілін, якщо того, коли замісник визначається як водень або КІЛЬКІСТЬ води зменшується ще більше, наприклад може бути воднем, точна хімічна природа заміснидо приблизно 0,5% від об'єму реакційної суміші, ка в цьому положенні, ВІДМІННОГО від водню, не є загальна КІЛЬКІСТЬ 4-НДФА І 4-НОДФА і/або їх сокритичною, поки вона не впливає негативним чилей зростає Таким чином, дана реакція може проном на загальну активність і/або на проведення водитися в безводних умовах "Контролюєма КІЛЬсинтезу КІСТЬ" води, що утворюється, - це КІЛЬКІСТЬ аж до ХІМІЧНІ реакції, описані вище, звичайно описутієї, яка інгібує реакцію аніліну з нітробензолом, ються, виходячи з самого широкого додатку до наприклад аж до приблизно 4% Ь^О від об'єму способу цього винаходу Іноді умови реакції мореакційної суміші, коли анілін використовується як жуть бути непридатні в тому конкретному вигляді, розчинник Верхня межа КІЛЬКОСТІ ВОДИ, прийнятної як вони описані, до кожної реагуючої речовини і для реакції, змінюється в залежності від розчинниреагенту в межах вказаного обсягу винаходу Нака Наприклад, коли в якості розчинника викорисприклад, деякі ВІДПОВІДНІ основи можливо не бутовується ДМСО, і в якості основи використовудуть так само розчинні в одному розчиннику, як ється гідроксид тетраметиламонію, верхня межа вони розчинні в інших розчинниках Реагуючі реКІЛЬКОСТІ води, що утворюється в реакції, складає човини і реагенти, для яких це має місце, можуть біля 8% НгО з розрахунку на об'єм реакційної субути легко визначені фахівцями в даній області У міші Однак, коли в якості розчинника використовсіх таких випадках можна або успішно здійснити вується анілін з тією ж самою основою, верхня реакції за допомогою звичайних видозмін, відомих межа становить 4% Ь^О з розрахунку на об'єм фахівцям, наприклад, шляхом ВІДПОВІДНОГО вибору реакційної суміші Крім того, допустима КІЛЬКІСТЬ температури, тиску і т п , шляхом заміни реагентів, води, що утворюється, буде змінюватися в залежщо звичайно застосовуються, на ІНШІ, наприклад, ності від типу основи, КІЛЬКОСТІ основи і від катіона основи, що використовується в різних системах розчинників Однак, фахівець в даній області, використовуючи вказівки, дані в даному винаході, зможе визначити конкретну верхню межу КІЛЬКОСТІ води, що утворюється, для конкретного розчинника, типу і КІЛЬКОСТІ основи, катіона основи і т п Мінімальна КІЛЬКІСТЬ ВОДИ, необхідна для під тримки селективності відносно бажаних продуктів, також буде залежати від розчинника, що використовується, типу і КІЛЬКОСТІ основи, катіона основи, і т п , і також може бути визначена фахівцем в даній області В одному варіанті здійснення винаходу КІЛЬКІСТЬ води, що утворюється, присутньої в реакційній зоні процесу, регулюється шляхом безперервного видалення води, що утворилася, з використанням проточного реактора безперервної дії з нерухомим шаром каталізатора, як описано вище Безперервне видалення води, що утворилася, буде збільшувати утворення солей 4-НОДФД і 4-НДФА, і тим самим збільшувати селективність у відношенні 4-АДФА Відновне алкілування 4-АДФА для отримання антиозонантів можна провести будь-ким з декількох добре відомих способів на ІНШІ розчинники або ІНШІ ОСНОВИ, ШЛЯХОМ зви чайної видозміни умов реакції і т п , або можна застосувати до способу цього винаходу ІНШІ реакції, описані тут або загальновідомі з інших джерел У всіх препаративних методиках всі ВИХІДНІ речовини ВІДОМІ або легко виходять з відомий вихідних речовин Можна вважати, що без додаткової лабораторної розробки, фахівець в даній області, користуючись попереднім описом, може використати даний винахід в повній мірі Тому подальші переважні конкретні варіанти здійснення винаходу потрібно тлумачити просто як приклади, що ілюструють, а що не обмежують ніяким чином обсяг винаходу Всі реагенти використовуються втому вигляді, як вони отримані, якщо це не обумовлене особливо, і все виходи були визначені методом ВЕРХ, як викладено нижче Спосіб цього винаходу можна повністю зрозуміти з наступних прикладів, в яких всі температури дані в градусах Цель сію, весь тиск є манометричним тиском, і всі співвідношення є ваговими, якщо це не обумовлене особливо 4-НДФА і 4-НОДФА присутні у вигляді їх солей Приклад 1 13 57092 У автоклав Парра МІСТКІСТЮ 3 0 0 М Л загружали 133,3г нітробензолу, 26,1г ТМА(ОН)*5Н 2 О і 0,742г каталізатора гідрування (5% паладію на носи оксиді алюмінію) Водень подавали під контролем в автоклав протягом періоду, рівного трьом годинам, під час якого тиск зростав від 400кПа при максимальних витратах (10л/годину при 70°F (21 °С) і 1атм) і 73°С Температура суміші, що міститься в 14 автоклаві, потім підвищувалася до 87°С, і тиск водню підвищувався до 2900кПа за 2,5 години Використовуючи відомий метод ВЕРХ, визначали склад суміші в автоклаві спочатку через одну (1) годину і знову через п'ять з половиною (5,5) годин У наступній таблиці приведені зведені дані про склад суміші в реакційній зоні Таблиця І Час Компонент 1 година Ваговий % 0 215 00 79 421 0 899 00 0 074 0118 00 00 0 022 19 152 00 0 099 00 АНІЛІН N-метиланшш Нітробензол 4-амінодифеніламш (4-АДФА) Феназин 2-амінодифенідамш (2-АДФА) 4-нітрозодифеніламш (4-НОДФА) цис-азобензол Дифеншпдразин 4-нітродифеніламш (4-НДФД) Азоксибензол 2-нітродифеніламш (2-НДФА) транс-азобензол 4-фенілазодифеніламш (А-ФАДФА) Дані таблиці І показують, що утворюється помітна, хоч і мала КІЛЬКІСТЬ бажаного продукту 4АДФА Приклад 2 У цьому прикладі досліджували ефект присутності додаткової КІЛЬКОСТІ аніліну, доданої на початку процесу Використали ту ж методику, що і в прикладі 1, за винятком того, що спочатку загружали 136,9г аніліну і 43,7г нітробензолу разом з 58,0г ТМА(ОН)*5Н 2 О і 1,05г каталізатора гідрування Таким чином, в реактор спочатку загружали анілін при мольному відношенні аніліну до нітро 5,5 годин Ваговий % 3 665 00 10 195 0 603 0 01 00 0 047 0 073 00 01 82 960 00 2 089 0 057 бензолу, що дорівнює 4,165 Використовуючи метод ВЕРХ, визначали склад суміші в автоклаві, спочатку через 1,11 години, потім через 3,46 години і нарешті, через 5,61 години Температуру в реакторі підтримували на рівні біля 94°С протягом всього часу реакції Через 3,46 години утворилася КІЛЬКІСТЬ води, якої було досить, щоб спричинити утворення двох фаз, більш важкої органічної фази і більш легкої водної фази Через зупинку процесу реакції велика КІЛЬКІСТЬ ВОДИ інгібує утворення юна аніліду, який є попередником для реакції поєднання аніліну і нітробензолу з утворенням 4-АДФД Таблиця НА Гідрування нітробензолу приклад 2 Розподіл продуктів в органічному шарі у вагових процентах Час Компонент анілін N-метиланшш Нітробензол 4-амінодифеніламш (4-АДФА) феназин 2-амінодифеніламш (2-АДФА) 4-нітрозодифеніламш (4-НОДФА) цис-азобензол 4-нітродифеніламш 4-нітродифеніламш (4-НДФА) Азоксибензол 2-нітродифеніламш (2-НДФА) транс-азобензол 4-фенілазодифеніламш (4-ФАДФА) 1,11 годин Вагові % 66 64 00 7 195 0 55 0 126 00 11 457 2 46 00 2 738 2 194 00 6 168 0 216 3,46 години Вагові % 57 65 00 00 1541 0 126 00 0 034 2 44 19 56 0 1305 0 0435 0 032 4 346 0 0214 5, 61 години Вагові % 56 999 00 00 14 95 0 108 00 0 0322 1 266 23 379 00 00 0 035 3 181 00 15 16 57092 Таблиця ІІВ Гідрування нітробензолу приклад 2 Розподіл продуктів у вагових процентах для змішаного і водного шарів Час Компонент анілін N-метиланілш нітробензол 4-амінодифеніламш (4-ДЦФА) феназин 2-амінодифеніламш (2-АДФА) 4-нітрозодифеніламш цис-азобензол дифеніл гідразин 4-нітродифеніламш (4-НДФА) азоксибензол 2-нітродифеніламш (2-НДФА) транс-азобензол 4-фенілазодифеніламш (4-ФАДФА) У протилежність прикладу 1, приклад 2 ясно показує, що в присутності надлишку аніліну, тобто при мольному співвідношенні анілін/нітробензол більше 1, гідрування нітробензолу сприяє утворенню тетраметиламонієвих селей 4-НОДФА і 4НДФА, а також загальної конверсії нітробензолу, і тим самим збільшенню виходу до селективності у відношенні 4-АДФА Як показано в таблицях НА і ІІВ, конверсія нітробензолу близька до 100% через 3,46 години, і реакція гідрування в основному закінчується Інший час реакції від 3,46 до 5,61 години використовується для завершення відновлення побічного продукту азобензолу до дифенілпдразину і відновного диспропорцюнування 4-фенілазодифеніламшу з отриманням 4-АДФА і аніліну Приклад З У прикладі 3 мольне відношення аніліну до нітробензолу було підвищене до 7,07 або в 1,7 рази в порівнянні з відношенням, показаним в прикладі 3,46 години Вагові % в суміші 60 58 00 0 044 15 357 0 130 00 0 0444 2 537 13 798 0 141 0 066 0 032 6 605 0 018 5, 61 години Вагові % у водному шарі 67 321 00 0 196 12 451 0 743 00 00 3 164 7 948 00 00 0 044 8 134 00 2 КІЛЬКІСТЬ каталізатора 5% паладію на оксиді алюмінію було приблизно рівною КІЛЬКОСТІ каталізатора, використаній в прикладі 2 Однако, в цьому прикладі КІЛЬКІСТЬ основи по відношенню до нітробензолу була трохи менше, ніж в прикладі 2 В І Д ПОВІДНО КІЛЬКІСТЬ нітробензолу на одиницю ваги каталізатора в прикладі 3 була нижчою, ніж показано в прикладі 2 їв цьому випадку реакційна маса перетворювалася з однієї фази на початку процесу в дві рідкі фази важку органічну фазу і більш легку водну фазу При часі реакції б годин спостерігалося закінчення гідрування, чому передувало гідрування при постійному тиску Результати по селективності, показані в таблиці ІІІА і в таблиці ІІІВ, близько співпадають з результатами прикладу 2, приведеними в таблиці ПА і таблиці ІІВ, за винятком того, що спостерігається відносно низька конверсія нітробензолу в продукти реакції поєднання Таблиця ІІІА Гідрування нітробензолу приклад З Розподіл продуктів у вагових процентах від суміші Час Компонент АНІЛІН N-метиланшш Нітробензол 4-амінодифеніламш Феназин 2-амінодифеніламш (2-АДФА) 4-нітрозодифеніламш (4-НОДФА) цис-азобензол дифеніл гідразин 4-нітродифеніламш (4-НДФА) азоксибензол 2-нітродифеніламш транс- азобензол 4-фенілазодифеніламш (4-ФАДФА) 1,45 Вагові % 78 16 00 00 8 446 0 067 0 025 1 246 00 6 012 00 00 00 5 977 0 067 2,79 Вагові % 72 33 00 00 7 91 0 0623 00 0 449 00 1719 00 00 0 059 1 996 00 6,0 Вагові % 74 69 00 00 8 35 0 06 0 0255 0 528 00 12 136 00 00 0 036 4 169 00 17 57092 18 Таблиця NIB Гідрування нітробензолу приклад З Розподіл продуктів у вагових процентах для органічного і водного шарів в КІНЦІ реакції Час Компонент 6,0 годин Органічний 72 0 00 00 8 32 0 06 0 024 0 279 00 16 227 00 00 0 0355 2 86 00 АНІЛІН N-метиланшш Нітробензол 4-амінодифеніламш (4-АДФА) Феназин 2-амінодифеніламш 4-нітродифеніламш (4-НДФА) цис-азобензол Дифеніл гідразин 4-нітродифеніламш (4-НДФА) Азоксибензол 2-нітродифеніламш (2-НДФА) транс-азобензол 4-фенілазодифеніламш (4-ФАДФА) Приклад 3 показує низьку конверсію нітробензолу в 4-НДФА і 4-НОДФА, внаслідок більш низької КІЛЬКОСТІ основи і більш високої КІЛЬКОСТІ паладієвого каталізатора, який викликає гідрування нітробензолу з отриманням дифенілпдразину з утворенням великих кількостей води Велика КІЛЬКІСТЬ паладієвого каталізатора на грам нітробензолу вказує на більшу КІЛЬКІСТЬ нітробензолу, що відновлюється за один цикл, і тому швидкість конверсії нітробензолу вище в прикладі 3, ніж в прикладі 2 6, 0 годин Водний шар 81 62 00 0 0805 7 441 0 0594 00 0 691 00 3 413 00 00 0 0279 6 667 00 ня ІОНІВ аніліду обмежує пряме перетворення нітробензолу в продукти реакції поєднання Високе мольне відношення аніліну до нітробензолу і більш високе відношення паладію до нітробензолу приводять до утворення виключно 4-НОДФА Як видно з таблиці ІІІА, після 1,45 годин часу реакції ніякого 4-НДФА не було виявлено У таблиці IV показані в порівнянні величини мольних відношень і КІЛЬКОСТІ різних компонентів і продуктів реакції в реакторі для прикладів 1, 2 і З Як в прикладі 2, інгібуюча дія води на утворенТаблиця IV Гідрування нітробензолу приклади для реактора Приклад № АНІЛІН, Г Нітробензол, г Молі аніліну/МОЛІ нітробензолу ТМА(ОН) *5Н2О, г Молі нітробензолу/ молі ТМА(ОН) он) 5% Pd/AI2 Оз, г Грами Pd/1000 гамів нітробензолу 1 00 133 3214 00 26 1044 7 453 0 7421 0 278 Наведені вище приклади дозволяють припустити, що значні виходи при конверсії нітробензолу в 4-АДФА можна отримати, використовуючи надлишок гідроксиду тетраметиламонію, тобто мольне відношення нітробензол/ТМА(ОН) менше 1, і необхідну КІЛЬКІСТЬ паладієвого каталізатора Процес в наведених вище прикладах краще здійснювати, використовуючи безперервну подачу нітробензолу зі швидкістю, яка відповідає вимогам надлишку основи і утворення малої КІЛЬКОСТІ ВОДИ, Комп'ютерна верстка Т Чепелєва 2 136 9322 43 6787 4 165 58 0247 1 099 1 0475 1 208 3 160 2318 30 1102 7 07 39 7038 1 11 1 0480 1 76 так, щоб вона не інгібувала утворення анілід-юна Результати з прикладів 2 і 3 показують, що сумарна швидкість розходування нітробензолу з перетворенням його в продукти реакції поєднання (і ВІДПОВІДНО помітна швидкість утворення анілідюна) визначається відносними кількостями каталізатора і ТМА(ОН) Згідно наведеним вище результатам велика КІЛЬКІСТЬ паладієвого каталізатора не рекомендується Підписано до друку 05 07 2003 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюA catalytic nitrobenzene hydration with formation of 4-aminodiphenylamine in the presence of hydroxylholding compound and solvent
Назва патенту російськоюКаталитическое гидрирование нитробензола с образованием 4-аминодифениламина в присутствии гидроксилудерживающего соедиения и растворителя
МПК / Мітки
МПК: C07B 61/00, C07C 209/36, C07C 211/54, C07C 209/02
Мітки: одержання, одностадійний, 4-амінодифеніламіну, спосіб
Код посилання
<a href="https://ua.patents.su/9-57092-odnostadijjnijj-sposib-oderzhannya-4-aminodifenilaminu.html" target="_blank" rel="follow" title="База патентів України">Одностадійний спосіб одержання 4-амінодифеніламіну</a>
Попередній патент: Спосіб одержання бензолсульфонату амлодипіну
Наступний патент: Інструментальна сталь
Випадковий патент: Котел-утилізатор