Спосіб перетворювання активності іонів речовини у водному розчині
Формула / Реферат
1. Спосіб перетворювання активності іонів речовини у водному розчині у вихідний сигнал шляхом керування струмом поляризації робочого електрода, який полягає в тому, що струмом поляризації підтримують потенціал робочого електрода відносно потенціалу електрода порівняння рівним опорній напрузі, перетворюючи різницю між потенціалом робочого електрода і опорною напругою в струм поляризації із заданим коефіцієнтом перетворювання, який відрізняється тим, що здійснюють модуляцію швидкості потенціалотвірної реакції шляхом модуляції опорної напруги з постійними амплітудою і частотою за високочастотним діапазоном зміни активності іонів, подають додатковий струм поляризації робочого електрода, струм поляризації робочого електрода підсумовують з додатковим струмом поляризації робочого електрода, перетворюють сумарний струм поляризації робочого електрода в проміжний сигнал і фільтрують його, виділяючи модульовану та немодульовану складові, демодулюють модульовану складову і перетворюють у вихідний сигнал із заданим коефіцієнтом перетворювання, причому як робочий електрод використовують електрод з іон-селективними властивостями, подають додатковий опорний сигнал з постійною амплітудою і нульовою частотою, керують додатковим струмом поляризації робочого електрода так, щоб виділена немодульована складова проміжного сигналу наближалася до заданого значення додаткового опорного сигналу.
2. Спосіб перетворювання за п. 1, який відрізняється тим, що здійснюють переривання сумарного струму поляризації робочого електрода з частотою не менше подвійної частоти модуляції швидкості потенціалотвірної реакції.
Текст
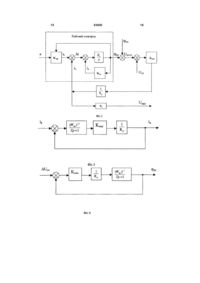
1. Спосіб перетворювання активності іонів речовини у водному розчині у вихідний сигнал шляхом керування струмом поляризації робочого електрода, який полягає в тому, що стр умом поляризації підтримують потенціал робочого електрода відносно потенціалу електрода порівняння рівним опорній напрузі, перетворюючи різницю між потенціалом робочого електрода і опорною напругою в струм поляризації із заданим коефіцієнтом перетворювання, який відрізняється тим, що здійснюють модуляцію швидкості потенціалотвірної реакції шляхом модуляції опорної напруги з постійними амплітудою і частотою за високочастот C2 2 (19) 1 3 83693 При дослідженні мікроструктури аналізованого середовища необхідно визначати розміри градієнтних прошарків до сантиметрів і зондувальні системи повинні мати метрологічні характеристики, що дозволяють реєструвати зазначені відхилення [5, с.211]. У [6] відзначено, що при використанні вимірювального каналу сульфідів у сульфідселективного електрода несиметрична інерційність: при зростанні - (3 ¸ 5)с і спаданні активності сульфідів - (3 ¸ 5)хв. У зображеній там же ілюстрації зондування (приблизно до 1000м) чітко видний гістерезис при опусканні і підйомі приладу в зонах зі ступінчастою структурою профілю активності сульфідів. Видно, що тонка структура профілю сульфідів сильно відфільтрована, а гістерезис свідчить про розбіжність профілів активності сульфідів при опусканні і підйомі приладу. Тому в електрохімічних перетворювачах керують електрохімічною реакцією в процесі перетворювання активності іонів речовини у вихідний сигнал, форсуючи швидкість електрохімічної реакції і підвищуючи швидкодію перетворювання. Відомий спосіб перетворювання активності іонів, який називають «фіксацією напруги» [7,с.362], що полягає в неперервному наближенні спаду напруги Upe-eп на ланцюзі «робочий електрод електрод порівняння» до еталонної напруги Ueт шляхом неперервної поляризації робочого електрода керованим струмом, що при заданому коефіцієнті перетворювання різниці напруги між Upe-eп і Ueт у керований струм є інформативним. Перетворюють цей струм у ви хідну напругу Uвих через масштабуючий резистор R0. По вихідній напрузі роблять висновок про активність іонів. Недоліком цього способу є неперервність поляризації робочого електрода, який вносить похибку від спаду напруги на омічному опорі «робочий електрод-електрод порівняння». Відомий спосіб перетворювання активності іонів [8] з використанням переривання керованого струму для виміру омічної напруги, у якому на мить зупиняють проходження струму через електродну систему, вимірюють потенціал робочого електрода перед перериванням струму, обчислюють різницю між цими потенціалами, що по суті є омічним спадом напруги, записують в елементи активного ЗП, значення яких використовують для обчислення поправок, після чого передають на вхід стабілізатора напруги як iR - компенсацію. Однак дії, зв'язані з обчисленням поправок, приводять до громіздких технічних рішень - застосуванням ряду аналогових запам'ятовувань, а також втраті інформації через утрату вимірюваного заряду в ранній стадії експерименту, що приводить до невизначеної точності перетворювання, позначеної в [8] як «достатньої». Відомий спосіб перетворювання активності іонів [9] з використанням переривання керованого струму на час перетворювання різниці між заданим рівнем і різницею потенціалів між робочим електродом і електродом порівняння. При цьому під час імпульсу керованого струму здійснюють поляризацію робочого електрода. Імпульси поляризації подають доти, поки різниця потенціалів між зазначеними електродами не встановиться рівною 4 заданому рівню. По кількості накопичених імпульсів роблять висновок про активність іонів речовини. Недоліком способу є керування електрохімічною реакцією імпульсом незмінного по амплітуді керованого струму. Виникає протиріччя: якщо для досягнення необхідного розрізнення застосовувати імпульси струму з малою амплітудою, то можна не ввійти в коридор заданої похибки. У [9] так і зазначене - поліпшення сталої часу в 10 разів можливо за рахунок 10- кратного погіршення розрізнення. Відомий спосіб вивчення кінетики електродних процесів, за допомогою якого можна одержати залежність струму поляризації, як вихідного сигналу, не тільки від потенціалу робочого електрода, але й активності іонів речовини в розчині, підтримуючи потенціал електрода постійним [10, с.405]. Цей спосіб дозволяє конструктивним шляхом зменшити вплив омічного спаду напруги в розчині електроліту. Однак йому властивий недолік вищезгаданих аналогів - залежність струму поляризації від потенціалу електрода порівняння, стосовно якого здійснюють потенціометрію. Найбільш близьким до запропонованого по сукупності ознак є спосіб перетворювання активності іонів речовини, реалізований в схемі[7,с.362], тому він обраний як прототип. Прототип і спосіб, що заявляється, мають наступні загальні істотні ознаки: підтримують потенціал робочого електрода щодо потенціалу електрода порівняння рівним опорній напрузі шляхом поляризації робочого електрода керованим струмом, перетворюють різницю між потенціалом робочого електрода й опорною напругою в струм поляризації із заданим коефіцієнтом перетворювання, а керований струм поляризації перетворюють у ви хідний сигнал. Сутність способу-прототипу полягає в наступному. Керують струмом поляризації робочого електрода, цим струмом підтримують потенціал робочого електрода за допомогою електрода порівняння рівним опорній напрузі, перетворюючи різницю між потенціалом робочого електрода на фоні потенціалу електрода порівняння й опорною напругою в цей струм із заданим коефіцієнтом перетворювання, рівень струму поляризації перетворюють у напругу, що є ви хідним сигналом. Для оцінки цього способу скористаємося формою математичного опису елементів [11, с.36], що відображує різні фізичні процеси в електрохімічному перетворювачі [7,с.362], де реалізований спосіб - прототип. Уявимо іон-селективний електрод, занурений у розчин речовини, аналізованої цим електродом, як електрохімічну систему електрод-середовище, елементи якоі є з'єднані між собою направлені ланки, що перетворюють сигнал в одному напрямку, а кожна окрема ланка описується своїм коефіцієнтом перетворювання, що відображує перетворення вхідного сигналу у ви хідний [11,с.110]. При висновку використовуємо основні рівняння електрохімічної кінетики в спрощеному вигляді [10,с.394]: 5 æ ajzE ö i a = K 1 exp ç + ÷, è RT ø æ bjzE ö i k = K 2 a exp ç ÷, è RT ø де 83693 (1) (2) æ W ö æ W ö K 1 = k 1 expç - 0 ÷, a K 2 = k 2 expç - 0 ÷; ç ÷ ç ÷ RT ø è è RT ø іа - струм, що характеризує швидкість прямої реакції [10,с.401] (перехід іонів чуттєвої частини вимірювального електрода в розчин) [10,с.389] ; ik- струм, що характеризує швидкість зворотної реакції (перехід іонів розчиненої речовини, концентрація якої виміряється, до чуттєвої частини вимірювального електрода - у даному випадку це потенціалотвірні іони). W0- постійна частина енергії активації реакційно-здатних (активних) часток; a i b - постійні частки від різниці рівнів енергії між іонами на поверхні електрода й у розчині, сума яких дорівнює одиниці [10,с.392,398]; j - електродний потенціал; R - газова стала; Т - абсолютна температура; z - заряд (валентність іона); F - стала Фарадея. Позначки струмів, що відображають напрямки електродної реакції, але не збігаються з її абревіатурою в індексах - а і k, уведені з тією метою, щоб виключити фактор впливу, з якого матеріалу виконана чуттєва частина електрода -металу, неметалу, 1го роду, 2го роду і т.д. З ура хуванням електродної ємності, що істотно впливає на динаміку перетворювання, структурна схема, яка відображає перетворення активності іонів в електродний потенціал, зображена на фіг. 1. На структурній схемі зображені чотири ланки електрохімічної системи: a ® ik ; елемент порівняння; Di ® j i j ® ia . a ® ik ; - ланка, що перетворює активність вимірюваних іонів у струм зворотної реакції. Коефіцієнт перетворювання, що характеризує перетворення а в ік , має вигляд: æ bjzE ö (3) Wзв р = K 2 exp ç ÷, è RT ø Ланка, яка зображена у вигляді кола, розділеного на чотири сектори, відображає перетворення струмів і а та ік у їхню різницю Dі . Dі ® j - ланка, що перетворює різницевий струм в електродний потенціал, відображає ємнісну модель електрода, у якому ця ланка зображена у вигляді інтегратора зі статичним коефіцієнтом передачі Кі, який залежить не тільки від ємності подвійного електричного шару, діелектричної проникності середовища, що заповнює простір між обкладками конденсатора подвійного електричного шару - e , відстані між ними - d 0 , яка обумовле на розмірами іонів, але і властивостей селектив 6 ності електрода, що визначають тільки наявних у розчині іонів, яки заряджають цю ємність. Незалежно від цього коефіцієнта при настанні рівноваги Dі = 0 і потенціал j на виході інтегратора більше j не змінюється, стаючи рівним рів н. З урахуванням вищевикладеного коефіцієнт перетворювання ланки Dі ® j в операторній формі набуває вигляду: K (4) W (p) = i , p де р - параметр перетворювання Лапласа. j ® ia - ланка, яка перетворює електродний потенціал у струм прямої електрохімічної реакції, що, згідно [12, с. 81], визначає витік конденсатора подвійного електричного шару. Коефіцієнт перетворювання, який характеризує перетворення j в іа, має розмірність [Ом] і має вигляд: æ ajzE ö (5) Wпр = K 1 exp ç + ÷, è RT ø З огляду на те, що спосіб-прототип фіксує потенціал робочого електрода та він мало відхиляється від фіксованого схемою значення коефіцієнти Wзвр і Wпp стають лінеаризовані [14,с.136], та що a + b = 1 й a = b = 0,5 а = Р = 0,5 [10,с.с.392,408], зі структурної схеми можна визначити коефіцієнт перетворювання робочого електрода в операторної формі: W (p)pe = j(p) K 2 zF = exp( j(p))j(p) ´ C(p) K 1 RT 1 (6) , 1 p+1 a zF a zF K i K 1 exp( j(p)) RT RT який дуже ілюстративний. Дробовий вираз, що стоїть після статичного коефіцієнта відображає динаміку перетворювальної ланки ik ® j , яка є ´ аперіодичною ланкою першого порядку, що підтверджено в [13]. Причому його стала часу T = 1 / K i K 1 exp( a zj / RT)a z / RT змінюється при зміні j , що обумовлює несиметричну інерційність при зростанні та спаданні активності іонів, як згадувалося ви ще - [6]. Визначивши математичний опис фізичних процесів у робочому електроді, з урахуванням вищевикладеного зображено структурну схему, що відображає спосіб-прототип, на фіг.2. У зображеній структурній схемі використані наступні позначення: iп - керований струм поляризації робочого електрода; j ре - потенціал робочого електрода; Upe-еп - е.р.с. електродної системи «робочий електрод - електрод порівняння»; Uoп - опорна напруга, з якою порівнюють напругу Upe- еп; Rp - опір розчину струму поляризації і п; R0 - масштабуючий резистор; Uвих - ви хідна напруга. 7 83693 Через те, що за допомогою способу - прототипу система «електрод-середовище» стає лінійною до зображеної структурної схеми можна застосувати правила перетворювання - поміняти місцями елементи порівняння [14, с. 179]. Звідси випливає, що при досить великому коефіцієнті перетворювання електродного потенціалу в струм поляризації іп по ньому можна судити про інформаційний струм і k З ура хуванням виразу (2) і масштабуючого резистора R0 вихідний сигнал при застосуванні способу - прототипу має вигляд: (7) Uв их = R0 K 2 exp p( -b zF j / RT )a Для аналізу швидкодії беремо деякі припущення. Беремо потенціал електрода порівняння рівним нулю, наприклад, як у водневого електрода. Опір розчину між робочим електродом і електродом порівняння настільки малий, що спадом напруги на ньому можна зневажити [10, с.405]. UОП = 0. Визначимо, у скільки разів зменшує сталу часу цей спосіб перетворювання. З урахуванням припущень і правил перетворювання структурних схем [14, с.179], зображено структурну схему ланки ik ® iп на фіг.3. У зображеній структурній схемі використані наступні позначення: (Wпp)-1 - статичний коефіцієнт передачі ланки ik ® j , рівний 1 / K 1 exp( a zj / RT ); Т - стала часу ланки ik ® j ; КПІДС - коефіцієнт перетворювання підсилювача; Iп - керований струм поляризації. Зі структурної схеми, зображеної на фіг.3, можна визначити коефіцієнт передачі ланки ik ® iп : (Wпр )-1 i(p)n W (p)i k ® i п = = i(p)k = K ПІДС ®¥ K × K ПІД С 1 + K × K ПІД С × Tp + 1 × K ПІД С × ( Wпр )-1 1 Rp 1 1+ × K ПІД С × Tp + 1 Rp 1 , T з+1 1 + K × K ПІД С = K ПІДС ® ¥ (8) де К=(Wпp)-1/Rp. 3 отриманого коефіцієнта передачі видно, що приведений спосіб перетворювання іонів в інформаційний сигнал зменшує сталу часу електрода в 1+ККПІДС разів. Нехай К=1, тоді, установивши підсилювач з реальним коефіцієнтом передачі, рівним 105, сталу часу (3 ¸ 5хв) при вимірі сульфідів можна зменшити в 105 разів, тобто до (1,8 ¸ 3)мс, що вже цілком прийнятне в умовах зондування. В аналогу [9] показано, що сталу часу електрода при керуванні електрохімічною реакцією вдалося зменшити до 10мкс, що не межа, однак задача подальшого зменшення сталої часу не ставилася. Це говорить про те, що ланки, описувані коефіцієнтами передачі Wзвр і Wпp, практично безінерційні, тому оператор р у їхні х позначеннях опущений. Зі способу-прототипу видно, що стабільність підтримки електродного потенціалу залежить в основному від стабільності потенціалу електрода 8 порівняння. На стандартній гідрологічній станції прилад можуть опускати до 2000 -6000м [15], тому для дослідження гідрохімічних параметрів до електрода порівняння ставлять такі вимоги, щоб його потенціал не залежав від гідростатичного та механічного тиску і щоб він був простий в експлуатації в морських умовах [16]. Цей електрод являє собою конструктивно дуже складний пристрій, тому що при високому тиску слід забезпечувати примусове протікання внутрішнього розчину назовні через сольовий місток у досліджуване середовище. Застосування непротічного електрода порівняння полегшує його експлуатацію, однак дифузійні потенціали можуть досягати значної величини - до 30мВ. Занадто мала витрата внутрішнього електроліту електрода порівняння приводить до дуже відчутних ди фузійних потенціалів, а збільшена - до надмірно великої витрати електроліту і сольовому впливу при вимірах у порівняно малих обсягах [16,с.24,25]. В основу винаходу поставлена задача створення способу перетворювання активності іонів речовини, у якому за рахунок частотного рознесення сигналів робочого електрода та електрода порівняння і стабілізації неінформаційної частини сигналу, одержуваного від електродної системи «робочий електрод-електрод порівняння», забезпечується технічний результат - усунення фактора впливу зміни потенціалу електрода порівняння на результат перетворювання. Вказаний технічний результат підвищує точність перетворювання. Поставлена задача вирішується тим, що в способі перетворювання активності іонів речовини у водному розчині у вихідний сигнал шляхом керування струмом поляризації робочого електрода, який полягає в тому, що цим струмом підтримують потенціал робочого електрода щодо потенціалу електрода порівняння рівним опорній напрузі, перетворюючи різницю між потенціалом робочого електрода й опорною напругою в цей струм із заданим коефіцієнтом перетворювання, новим є те, що здійснюють модуляцію швидкості потенціалотвірної реакції шляхом модуляції опорної напруги з постійними амплітудою і частотою за високочастотним діапазоном зміни активності іонів, подають додатковий струм поляризації робочого електрода, стр ум поляризації робочого електрода підсумовують з додатковим струмом поляризації робочого електрода, перетворюють сумарний струм поляризації робочого електрода в проміжний сигнал і фільтрують його, виділяючи модульовану та не модульовану складові, демодулюють модульовану складову і перетворюють у вихідний сигнал із заданим коефіцієнтом перетворювання, причому як робочий електрод використовують електрод з іон-селективними властивостями, подають додатковий опорний сигнал з постійною амплітудою і нульовою частотою, керують додатковим струмом поляризації робочого електрода так, щоб виділена не модульована складова проміжного сигналу наближалася до заданого значення додаткового опорного сигналу. Залежність коефіцієнта перетворювання активності іонів речовини від потенціалу робочого еле 9 83693 ктрода (вираз (2)) надала можливість модулювати швидкість потенціалотвірної реакції, а зменшення сталої часу робочого електрода за рахунок керування поляризуючим струмом із заданим коефіцієнтом перетворювання - модулювати коефіцієнт перетворювання ланки a ® ik з високою частотою. Пояснимо запропонований спосіб перетворювання активності іонів речовини у вихідний сигнал, використовуючи структурну схему можливої реалізації запропонованого способу, зображену на фиг. 5, за умові, коли електродна система «робочий електрод - електрод порівняння» знаходиться в досліджуваному розчині. Для зручності міркувань скористаємося правилами перетворювання структурних схем [14,с.179], згідно з якими суматори переставлені місцями, внаслідок чого контур із струмом поляризації іп став зовнішнім контуром, а контур із струмом прямої реакції і а - внутрішнім. Перетворюють різницю е.р.с. електродної системи «робочий електрод - електрод порівняння» та опорною напругою в струм поляризації робочого електрода - іп. Нехай електронний пристрій, що реалізує цю операцію, так само, як і в прототипі, складається з операційного підсилювача з коефіцієнтом передачі Кпідс і опору розчину Rp між допоміжним електродом (електродом для інжекції струму) і робочим електродом. Знаючи частотний діапазон перетворюваного сигналу - активності іонів речовини, визначають частоту генератора опорної напруги D Uoп, яка, відповідно до запропонованого способу, повинна бути ви щою за максимальну частоту зміни перетворюваного сигналу, і з постійною амплітудою подають на порівнюючий вхід операційного підсилювача (замість опорної Uoп в прототипі). Як було показане вище - в прототипі зворотний зв'язок з високим коефіцієнтом перетворювання, що о хоплює робочий електрод, істотно збільшує його швидкодію. Структурна схема DU оп ® j ре перетворювальної ланки зображена на фіг.4, звідки видно, що потенціал робочого електрода j ре при впливі змінної напруги D Uoп прагне за нею з тією ж швидкодією, що й ік до іп. Від j ре, відповідно до виразу (2), залежить коефіцієнт передачі Wзвр, що характеризує потенціалотвірну реакцію. З огляду на те, що між робочим електродом і підсилювачем напруги стоять суматори, будь-яке значення потенціалу електрода порівняння, відмінне від нуля, приводить до появи додаткового струму і на вході ланки ik ® j , який поляризує еп робочий електрод так, щоб е.р.с. електродної системи залишалася рівною опорній напрузі. При модуляції опорної напруги в запропонованому способі перетворювання з'явиться ще один струм Diп , який моделює потенціал робочого електрода і залежить тільки від опорної напруги та коефіцієнтів передачі Кпідс і 1/Rp. Модуляція потенціалу робочого електрода приводить до модуляції потенціалотвірної реакції 10 на частоті зміни опорної напруги D Uoп, оскільки, згідно (2), від зміни j ре змінюється коефіцієнт передачі Wзвр, що стоїть перед активністю іонів речовини. Таким чином, на вході ланки ik ® j з'являється ще один струм Dik , який несе інформацію про активність іонів речовини в модульованому вигляді через приріст коефіцієнта передачі D Wзвр. Після обліку всіх дій вираз для струму поляризації набуває наступного вигляду: (9) iп = ik + i еп + D ik + Diп де іеп - складова струму поляризації, що формується потенціалом електрода порівняння. Формують додатковий струм поляризації робочого електрода і п дод та підсумовують його зі струмом поляризації іп. Перетворюють сумарний струм поляризаії å iп робочого електрода за допомогою масштабуючого резистора R0 в проміжний сигнал – Uпр. Фільтрують цей сигнал, виділяючи модульовану Uм і не модульовану Uнм складові проміжного сигналу, демодулюють модульовану складову, перетворюючи її у ви хідний сигнал із заданим коефіцієнтом перетворювання. Немодульовану складову проміжного сигналу порівнюють з додатковим опорним сигналом Uоп дод постійної амплітуди. За результатами порівняння сигналів Uнм і Uoп дод керують додатковим струмом поляризації робочого електрода так, щоб виділена немодульована складова проміжного сигналу Uнм прагнула заданого значення додаткового опорного сигналу Uoп дод. Нехай сумарний струм поляризації å iп перетворюють у проміжний сигнал Uпр за допомогою операційного підсилювача із струмовим входом і резистором R0 в ланцюзі зворотного зв'язку, як і в прототипі. Тоді модульовану частину проміжного сигналу Uм можна отримати, наприклад, за допомогою звичайного фільтра, який перепускає сигнали на частоті вище за високочастотний діапазон зміни активності іонів речовини, як в [17,с.58]. Демодуляцію модульованої частини проміжного сигналу Uм можна здійснити, наприклад, шляхом детектування і фільтрації в смузі частот зміни активності іонів речовини [17,с.108]. Нехай коефіцієнти передачі фільтра, що виділяє модульовану складову проміжного сигналу та демодулятора є такими, що дорівнюють одиниці, тоді вираз для демодульованого сигналу Uвих, з урахуванням виразів (2) і (9), набуває вигляду: é b zF ù Uв их = R 0K 2 exp ê (jpe + Djpe )úa + R 0Diп = ë RT û = R 0Wзв ра + R0 Diп. (10) З виразу (10) видно, що якщо складова R0 D іп залежить лише від коефіцієнта перетворювання різниці е.р.с. електродної системи й опорної напруги в стр ум і від резистора R0, що можна врахувати, то демодульований сигнал залежить не тільки від активності іонів речовини, але і від множника Wзвр, який завжди змінюється від немо 11 83693 дульованої частини потенціалу робочого електрода, куди входить потенціал електрода порівняння. Нехай для перетворювання різниці е.р.с. і опорного сигналу в керований струм поляризації робочого електрода, як і в прототипі, застосований підсилювач напруги з високим коефіцієнтом передачі КПІДС а струм визначається напругою з виходу цього підсилювача і опором розчину між допоміжним електродом і робочим електродом Rр1. Хай додатковий струм поляризації робочого електрода іп дод визначається вихідною напругою електронного керованого пристрою з коефіцієнтом передачі Ккер і опором розчину між додатковим допоміжним електродом і робочим електродом Rp2 такої ж конструкції, як і основний, щоб опір розчину між кожним з цих електродів і робочим електродом був однаковим Rp1 = Rp2. У принципі підсумовування сигналів можна проводити, використовуючи лише один допоміжний електрод, тоді умова рівності опорів Rp1 і Rp2 стане ідеальною. Другий допоміжний електрод уводиться для наочності, підкреслюючи, що уводиться додатковий струм поляризації робочого електрода. Виділяють не модульовану частину проміжного сигналу за допомогою фільтра нижніх частот, який перепускає сигнали тільки в смузі частот зміни активності іонів речовини [17, с.108], і порівнюють з додатковою опорною напругою з постійною амплітудою Uoп дод. Нехай коефіцієнт передачі цього фільтра у вказаному діапазоні частот дорівнюєодиниці, тоді вираз для не модульованого сигналу з урахуванням виразу (9) набуває вигляду: Uнм =R0ik+R0iеп (11) За умові виконання, наприклад, коефіцієнта K передачі Ккер дуже великим ( kep® ¥ ), або керування додатковим струмом поляризації за астатичним законом, наприклад, наділюючи коефіцієнт Ккер інтегрувальними властивостями, сигнал Uнм завжди прагнутиме Uoп дод. Хай Uoп дод = 0, тоді і не модульована складова прагнутиме нуля. А це значить, що множник Wзвр, який завжди змінюється від не модульованої частини потенціалу робочого електрода, куди входить і потенціал електрода порівняння, завжди прагне одиниці. (12) Wзв р = exp [(- b zF / RT )jнм ] ® 1 Таким чином, вихідний сигнал стає рівним: b zF (13) Uв их = R0 K 2 exp( D jpe )a = R 0K 2D Wзв ра RT З виразу (13) виходить, що в запропонованому способі перетворювання активності іонів речовини у ви хідний сигнал виключаються впливи не тільки від потенціалу електрода порівняння, але і не модульованого струму зворотної реакції ik у виразі (9), тобто і від інших факторів, що поляризують робочий електрод в частотному діапазоні зміни активності іонів, бо в j нм входять і інші складові, наприклад, адитивна складова електронних пристроїв, які також поляризують робочий електрод. Усунення впливу вказаних факторів на результат перетворення є додатковим технічним результатом винаходу. 12 Забезпечена винаходом незалежність вихідного сигналу від потенціалу електрода порівняння дозволяє при проектуванні вимірювальних перетворювачів активності іонів речовини відмовитися від застосування конструктивно і технологічно складних електродів порівняння, а застосувати, наприклад, будь-який, зручний для конкретних умов, провідник. Порівняння не модульованої складової Uнм з додатковим опорним сигналом Uoп дод в запропонованому способі перетворювання активності іонів речовини у вихідний сигнал дозволяє вибрати самий оптимальний режим на кривій поляризації електрода установкою значення Uoп дод, наприклад, відносно крутизни цієї кривої, або вибрати таке значення Uoп дод, при якому електродна ємність мінімальна, а значить і інерційність електродної системи - мінімальна. Ця можливість є іншим додатковим технічним результатом винаходу. У разі, коли спадом напруги на розчині між робочим електродом і електродом порівняння нехтувати не можна, наприклад, при вимірюванні активності речовин в прісних водах, спосіб дозволяє розв'язати вищезгадану суперечність в пристроях з перериванням струму поляризації - підвищити швидкодію без погіршення роздільної здатності, оскільки амплітуда керованого струму не залишається незмінною, як це виконане в [9], а залежить від потенціалу робочого електрода. Необхідно лише виконати умову - переривання сумарного струму поляризації проводити з частотою згідно теоремі Котельникова, тобто не менш подвійної частоти модуляції швидкості потенціалотвірної реакції. Запропонований спосіб перетворювання активності іонів у ви хідний сигнал дозволяє досягти вказані технічні результати і у разі здійснення потенціометрії робочими електродами без селективних властивостей, оскільки у будь-якому випадку виміряють їх потенціал щодо електрода порівняння. Проте відсутність властивостей селективності робочого електрода вимагає додаткових умов, наприклад, забезпечення швидкодії і стійкості під час швидкої зміні активності відразу декількох видів іонів, тощо. Використані джерела: 1. Linear Products, 1C Data Book / Burr - Brown (www.burr-brown.com/), 1996 / 1997.- С.4.109. 2. Сульфид-селективный электрод XC-S-001. Паспорт и инструкция по эксплуатации. Научновнедренческапя фирма «Аналитические системы» - С Петербург. 3. Савенко B.C. Введение в ионометрию природных вод (применение ионо-селективных электродов в гидрохимии) - Л.: Гидрометеоиздат, 1986. 4. Камман К. Работа с ионселективными электродами / Пер.с нем., под ред. док. хим. наук О.М.Петрухина - М.: Мир, 1980. 5. Парамонов А.Н., Кушнир В.М., Забурдаев В.И. Современные методы и средства измерения гидрологических параметров океана - Киев.: Наукова думка, 1979. 6. Забурдаев В.И., Кирющенко И.Г., Иванов А.Ф., Клидзио А.Н., Нечесин Е.Г., Присекин В.А. К вопросу методики выполнения высокоточных из 13 83693 мерений гидрологических и гидрохимических элементов морской воды СТД - зондом «Исток-7»/ Морское и экологическое приборостроение: Сб. тр. международного НТС МГИ НАН Украины - Севастополь, 1995. 7. Хоровиц П., Хилл У. Искусство схемотехники - Под ред. канд. тех. наук М.В.Гальперина-М.: Мир, 1984. - Т.2 - 590 с. - прототип. 8. Richard Bezman. Sampled-Data Approach to the Reduction of Uncompensated Resistance Effects in Potentiostatic Experiments. // Analytical Chmistry, Vol.44, No.11, September 1972. 9. William W. Goldsworthy and Ray G. Clem. Bipolar Digipotentiogrator for Electroanalytical Uses. Direct Conversion of Charge to a Digital Number.// Analytical Chmistry, Vol.44, No.8, July 1972. Ю.Скорчелетти В.В. Теоретическая электрохимия. 3-е изд., переработанное - Ленинградское отд.: Химия, 1970. - 608с. 11. Теория автоматического управления - 2-е изд., перераб. и доп. - Под ред. д.т.н. проф. А.В.Нетушила- М.:Высшая школа, 1976. - 400с. 12. Лопатин Б.А. Кондуктометрия. - Новосибирск.: Редакционно - издательский отдел Сибирского отделения АН СССР, 1964. - 280с. 14 13. Забурдаев В.Н., Кирющенко И.Г., Гайский П.В., Никитин А.В., Даниленко М.А., Овсяный Е.И. Результаты испытаний измерителей рН, концентрации сульфид-ионов и ионов свинца гидрохимического зонда / Системы контроля окружающей среды: Сб.научн.тр. МГИ НАН Украины - Севастополь, 2003, -С.34-43. 14. Воронов А.А., Титов В.К., Новогранов Б.Н. Основы теории автоматического регулирования и управления. - М.: Высшая школа, 1977. - 519с. 15. Гайский В.А., Гайский П.В. Оценка динамических погрешностей измерения профилей гидрологических параметров зондирующим прибором / Диагноз состояния экосистемы Черного моря и зоны сопряжения суши и моря: Сб. тр. науч. конференции МГИ НАН Украины под редакцией чл. корр. НАНУ В.Н.Еремеева - Севастополь, 1997, С.185-187. 16. Рабинович М.Е., Вн уков Ю.Л. Методы измерения гидрохимических параметров и их применение в зондирующи х комплексах МГИ НАН Украины / Препринт МГИ НАН Украины - Севастополь.: СО «ЭКОСИ -Гидрофизика», 1995, - 76с. 17. Щербаков В.И., Грездов Г.И. Электронные схемы на операционных усилителях. - Киев: «Техніка», 1983.- 213с. 15 83693 16 17 Комп’ютерна в ерстка Т. Чепелев а 83693 Підписне 18 Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for transformation of activity of substance in water solution
Автори англійськоюKiriuschenko Ihor Heorhiiovych
Назва патенту російськоюСпособ преобразования активности ионов вещества в водном растворе
Автори російськоюКирющенко Игорь Георгиевич
МПК / Мітки
МПК: G01N 27/333
Мітки: водному, речовини, розчині, іонів, активності, спосіб, перетворювання
Код посилання
<a href="https://ua.patents.su/9-83693-sposib-peretvoryuvannya-aktivnosti-ioniv-rechovini-u-vodnomu-rozchini.html" target="_blank" rel="follow" title="База патентів України">Спосіб перетворювання активності іонів речовини у водному розчині</a>
Попередній патент: Карданний вал
Наступний патент: Запобіжний пристрій для водонагрівальної системи
Випадковий патент: Пристрій для зниження ударного шуму при перевантаженні кускового матеріалу