Спосіб лікування склеродермії із застосуванням фрагментів колагену
Формула / Реферат
1. Спосіб лікування склеродермії (SSc) у хворого, що включає пероральне введення хворому одного або більше фрагментів колагену, причому вказані фрагменти колагену вибрані з групи, що складається з: α1(І) СВ2, СВ3, СВ4, СВ5, СВ6, СВ8 і СВ7, та α 2(І) СВ0, СВ1, СВ2, СВ3, СВ4 і СВ3-5.
2. Спосіб за п. 1, де вказаний хворий страждає на вказану склеродермію протягом щонайменше 3 років.
3. Спосіб за п. 1, де вказаний колаген отримують від людини або від видів тварин, відмінних від людний.
4. Спосіб за п. 1, де вказаний фрагмент колагену перорально вводять вказаному хворому у дозі приблизно 500 мкг/день.
5. Спосіб за п. 4, де хворого лікують протягом приблизно 12 місяців.
6. Спосіб за п. 1, де пероральне введення вказаного фрагмента коллагену індукує толерантність у вказаного хворого.
7. Лікарська форма для перорального введення для лікування склеродермії у хворого, що включає один або більше фрагментів колагену, причому вказані фрагменти колагену вибрані з групи, що складається з: α1(І) СВ2, СВ3, СВ4, СВ5, СВ6, СВ8 і СВ7, та α2(І) СВ0, СВ1, СВ2, СВ3, СВ4 і СВ3-5.
8. Лікарська форма за п. 7, що пристосована для щоденного введення.
9. Лікарська форма за п. 7, де вказаний один або більше фрагментів колагену пристосовується до індукованої толерантності у вказаного хворого під час перорального введення.
10. Застосування лікарської форми за будь-яким з пунктів 7-9, де застосування здійснюється протягом близько 12 місяців.
11. Лікарська форма для перорального введення щонайменше один раз щодня для лікування склеродермії у хворого, який страждає від вказаної склеродермії протягом близько 3 років, що включає щонайменше 500 мкг одного або більше фрагментів колагену, вибраних з групи, що складається з: α1(І) СВ2, СВ3, СВ4, СВ5, СВ6, СВ8 і СВ7, та α2(І) СВ0, СВ1, СВ2, СВ3, СВ4 і СВ3-5.
12. Застосування лікарської форми за п. 11 протягом щонайменше 12 місяців.
13. Застосування лікарської форми за п. 11 протягом щонайменше 15 місяців.
14. Лікарська форма для перорального введення щонайменше один раз щодня для лікування склеродермії у хворого, який страждає від склеродермії протягом щонайменше 3 років, причому вказана лікарська форма включає щонайменше 500 мкг пептиду α1(І) СВ або пептиду α1(1) СВ7.
15. Застосування лікарської форми за п. 14 протягом щонайменше 12 місяців.
Текст
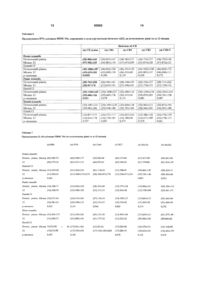
1. Спосіб лікування склеродермії (SSc) у хворого, що включає пероральне введення хворому одного або більше фрагментів колагену, причому вказані фрагменти колагену вибрані з групи, що складається з: α1(І) СВ2, СВ3, СВ4, СВ5, СВ6, СВ8 і СВ7, та α 2(І) СВ0, СВ1, СВ2, СВ3, СВ4 і СВ3-5. 2. Спосіб за п. 1, де вказаний хворий страждає на вказану склеродермію протягом щонайменше 3 років. 3. Спосіб за п. 1, де вказаний колаген отримують від людини або від видів тварин, відмінних від людини. 4. Спосіб за п. 1, де вказаний фрагмент колагену перорально вводять вказаному хворому у дозі приблизно 500 мкг/день. 5. Спосіб за п. 4, де хворого лікують протягом приблизно 12 місяців. 6. Спосіб за п. 1, де пероральне введення вказаного фрагмента колагену індукує толерантність у вказаного хворого. C2 2 UA 1 3 ральний імунітет типів І, III та IV у хворих на SSc. Найбільш характерним симптомом цієї хвороби є потовщення шкіри й щільне облягання нею тіла. Ураження внутрішніх органів, звичайно, включає шлунково-кишковий тракт, легені, нирки та серце. Можлива модуляція функцій фібробластів та моноцитів/макрофагів, а також ряду інших клітинмішеней Т-лімфоцитами через синтез цитокінів інших типів. Стосовно фіброзу, продукування фіброгенних цитокінів Т-клітинами на зразок IL-4, TGF-β1 та β2 може безпосередньо стимулювати синтез колагену фібробластами в культурі. Тклітини, через секрецію інтерферону (IFN) гама, можуть активувати макрофаги, що, в свою чергу, може призводити до синтезу певних фіброгенних цитокінів включно з фактором росту, похідним від еритроцитів TGF-β1 та β2, що, знову ж таки, може стимулювати фібробласти до синтезу колагену. Даний винахід стосується спосібів лікування фіброзної хвороби шляхом перорального введення тканинного білка, отриманого з тканини, ураженої фіброзом. Фіброзні хвороби, що можуть лікуватися відповідно до даного винаходу, включають склеродермію (SSc), фіброз шкіри, цироз печінки, фіброз нирок, фіброз легенів, фіброз серця, фіброз шлунково-кишкового тракту, фіброз судин тощо. В одному варіанті втілення, дані способи використовуються для лікування хворих на фіброзну хворобу, що триває щонайменше 3 роки, краще - 5 років. В іншому варіанті втілення, фіброзна хвороба лікується пероральним введенням колагену, отриманого з тканин, уражених фіброзом. Залежно від типу тканини, для лікування може застосовуватися колаген різноманітних типів. Колаген можна готувати з людської тканини, ураженої фіброзом, або з відповідної тканини тварин - наприклад, птахів або ссавців. В іншому разі можна використовувати колаген, синтезований хімічно або продукований методом рекомбінації. Крім того, відповідно до даного винаходу, можна використовувати фрагмент або суміш фрагментів колагену. В найкращому варіанті втілення, хворому вводяться колаген або фрагменти колагену перорально в дозі близько 500мкг/день приблизно протягом 12 місяців. Фіг.1: коробкові діаграми змін у MRSS (модифікованого показника стану шкіри Роднана (Rodnan)) у різні моменти часу та в хворих різних підгруп SSc. Фіг.2: кореляція відносної частки хворих SSc з процентом покращення MRSS за 12 місяців. Фіг.3: кореляція відносної частки хворих SSc з процентом покращення MRSS за 15 місяців. Фіг.4: показано розщеплення а1(І) та α2(І) під дією CNBr. Даний винахід вперше показав, що пероральне введення колагену типу І (СІ) індукує толерантність до СІ хворим на системний склероз (SSc) та покращує клінічні вияви хвороби. SSc - це прототип системної фіброзної хвороби, пов'язаної з підвищеним накопиченням позаклітинної білкової матриці на зразок колагену. Не 93063 4 віддаючи перевагу будь-якій конкретній теорії, можна вважати, що пероральне введення тканинного білка (на зразок колагену), що міститься в зоні тканини, враженої фіброзом, де Т-клітини активуються різноманітними стимулами, може знижувати кількість Т-клітин. Звідси випливає, що пригнічується секреція Т-клітинами фіброгенних цитокінів та цитокінів, що активують моноцити/макрофаги. В іншому разі, ці цитокіни стимулювали б фібробласти в цій зоні тканини, продукуючи позаклітинну білкову матрицю на зразок колагену. Відповідно, даний винахід пропонує способи лікування фіброзної хвороби шляхом перорального введення тканинного білка, отриманого з тканини, ураженої фіброзом. Фіброзні хвороби, що можуть лікуватися даними способами, включають, але не тільки, SSc, фіброз шкіри, цироз печінки, фіброз нирок, фіброз легенів, фіброз серця (що виникає, наприклад, в умовах застійної серцевої недостатності), фіброз шлунково-кишкового тракту, фіброз судин, що виникає в умовах атеросклерозу. Способи, що пропонуються даним винаходом, придатні для лікування цих фіброзних хвороб незалежно від того, чим вони спричинені. В певному втіленні, дані способи використовуються для лікування хворих на фіброзну хворобу протягом останніх 3 років, краще - останні 5 років. Відповідно до даного винаходу, фіброзну хворобу можна лікувати шляхом перорального введення колагену, отриманого з тканин, уражених фіброзом. Наприклад, відомо, що SSc пов'язаний з надмірним накопиченням колагену типу І, тому саме колаген типу І призначається хворим на SSc для перорального введення. Цироз печінки, фіброз легенів та колагенова хвороба пов'язані з підвищеним накопиченням колагену, відповідно, типів І, III та V. Тому хворим на цироз печінки, фіброз легенів та колагенову хворобу призначається перорально колаген, відповідно, типів І, III та V або його фрагменти. Надати толерантності може також назальне введення малих синтетичних пептидів, наприклад, у формі носових крапель або носових чи інгаляційних аерозолів. Колаген можна готувати та видобувати з уражених фіброзом тканин людини або тварин, наприклад, птахів (як то домашніх курчат) або ссавців (биків чи свиней). Альтернативно, можна використовувати синтетичний колаген, синтезований хімічно або продукований методом рекомбінації. Більше того, за даним винаходом можна використовувати фрагмент або суміш фрагментів колагену. Наприклад, для лікування хворих на SSc можна використовувати пептиди отримані розщепленням колагену типу І під дією CNBr. Колаген або його фрагменти можна призначати хворому перорально, в дозі приблизно 2001000мкг/день, краще - приблизно 400-600мкг/день, найкраще - приблизно 500мкг/день. Лікування може тривати щонайменше шість місяців, краще - 12 або більше місяців, або ж до зменшення чи поліпшення клінічних проявів хвороби. Даний винахід додатково ілюструється наступними прикладами. 5 Приклад 1 Щоб визначити, чи пероральне введення бичачого колагену типу І (СІ) у дозах 500мкг/день поліпшує клінічні прояви системного склерозу (SSc), було проведено багатоцентрове дослідження подвійним сліпим методом з контрольною групою плацебо. Хворих для дослідження відбирали за наступними критеріями: - Чоловіки або жінки віком щонайменше 18 років. - Наявність клінічно діагностованого дифузного SSc (за критеріями ACR 1980) протягом не більше 3 років (рання фаза) та від 4 до 10 років (пізня фаза). - Стійке враження шкіри за історією хвороби або з медичного огляду. - Стійкий модифікований показник стану шкіри Роднана (MRSS) протягом 1 місяця до включення в групу дослідження: стійкий MRSS≥16 в момент відбору та стійкий MRSS під час рандомізації (початковий рівень) відповідно до наступної таблиці: MRSS під час Допустимий MRSS під час рандовідбору мізації (початковий рівень) 16 до 20 17-20 16-24 21-25 ±4 26-30 ±5 ≥31 ±7 168 хворих, що відповідали зазначеним критеріям, було стратифіковано й рандомізовано на щоденне введення плацебо [2мл 0,1Μ оцтової кислоти (НАс)] або 500мкг бичачого СІ протягом 12 місяців. Вимірювали MRSS як первинну відмінність клінічного результату на початковому рівні та за 4, 8, 12 і 15 місяців. Опитування за формами Scleroderma Health Assessment Questionnaire (SHAQ), Short Form 36 (SF-36), оцінки за програмами Physician's Global Assessment, Patient's Global Assessment, вимірювання кров'яного тиску, ваги та вмісту креатиніну в сироватці визначалися як вторинні клінічні результати на початковому рівні та за 4, 8, 12 і 15 місяців. Вимірювання FVC (Forced Vital Capacity - Форсована життєва ємність легень) та DLCO (Diffusing Capacity of the Lung for Carbon Monoxide - Дифузна ємність легень стосовно оксиду вуглецю) проводилися не раніше, ніж за 5 тижнів до початкового рівня та через 12 місяців як параметри вторинних клінічних результатів. Потрібен був також попередній (до відбору) візит для призначення хворим виключних ліків чи лікування. Фіг.1 ілюструє підсумок відмінностей в MRSS на 4-й (синій колір), 8-й (червоний), 12-й (зелений) 15-й (оранжевий) місяці від початкового рівня з розбиттям на 4 підгрупи. Кожна коробка описує розподіл відмінностей в MRSS у кожній групі та в кожний момент часу; верхній край відповідає процентилю в 75%, нижній - в 25%; лінія всередині коробки позначає середню відмінність в MRSS. Значення поза інтервалом показано лініями, що виходять з коробок. 93063 6 Результати вказують на відсутність, на 12-му місяці, будь-якої статистичної різниці в середній відмінності між групою, що приймала СІ, та групою плацебо. Такі ж результати дали й інші клінічні та лабораторні параметри (див. Таблицю 1 та Таблицю 2). Однак на 15-му місяці в MRSS з'явилася дуже помітна відмінність: 7,9 у хворих пізньої фази, що приймали СІ (група "пізнього колагену") проти 2,9 у хворих пізньої фази групи плацебо ("пізнє плацебо"). Як показано на Фіг.1, середнє значення в оранжевій коробці на 15-му місяці, для групи хворих пізньої фази, що приймали колаген, є, без сумніву, значно нижчим порівняно з середніми значенням в інших оранжевих ящиках, і навіть взагалі найнижчим. Це означає, що хворі підгрупи пізньої фази, що приймали СІ, досягали найбільшого покращення MRSS. р-значення середньої відмінності MRSS між групам лікування пізньої фази дорівнює 0,0063; решта тестів не є значущими на рівні 0,05. Помічено, що змінна MRSS, сама по собі, не дає нормального розподілу, але розподіл відмінностей в MRSS на 12-му або 15-му місяцях є нормальним. Звідси випливає, що рзначення було отримано з t-тесту (перевірка за критерієм Ст'юдента). Щоб пересвідчитися в наявності відмінностей в MRSS між лікувальною групою та групою плацебо, використовували непараметричне тестування - а саме, за критерієм суми рангів, - що дало таке ж р-значення. Після дихотомізації відмінностей в MRSS та визначення процентної частки хворих, в яких спостерігалося покращення MRSS, отримали два графіки (Фіг.2 та Фіг.3). На графіках показано процентну частку хворих в кожній з чотирьох підгруп, в яких відбулося різної міри покращення MRSS. Наприклад, на першому графіку майже в 50% хворих групи пізнього колагену спостерігалося 20процентне зниження MRSS на 12-му місяці. На відміну від цього, в групі раннього колагену аналогічне покращення спостерігалося лише приблизно в 19% хворих. З обох графіків з очевидністю випливає, що хворим пізньої фази лікування колагеном принесло найпомітніші результати порівняно з іншими підгрупами. Перевірка колагенової групи за критерієм хі-квадрат підтвердила, що на 15-му місяці в значно більшої частки хворих пізньої фази спостерігалося покращення MRSS щонайменше на 25% порівняно з хворими ранньої фази. В сумі, дане дослідження показало, що пероральне введення бичачого СІ в дозі 500мкг/день протягом 12 місяців дає суттєве зниження MRSS на 15 місяці дослідження в хворих, хвороба яких триває від ≥4 до 10 років, що свідчить про уповільнений ефект перорального введення колагену для лікування фіброзу шкіри. Протягом дослідження не спостерігалося жодного помітного впливу перорального введення СІ на результати PFT (Pulmonary Function Test - Легенева функціональна проба) HAQ (Health Assessment Questionnaire - Оцінка стану здоров'я опитуванням), і не відбувалося жодних подій, котрі можна було би пов'язати з лікуванням СІ. Уповільнений ефект перорального лікування колагеном узгоджується з відомою властивістю фібробластів, котрим потрібен певний час для того, щоб "включитися" після нейтралізації 7 Т-клітин. Ці ж результати дають підстави для припущення, що Т-клітини видають більшу частину фіброгенних сигналів лише в хворих пізньої фази. Приклад 2 В цьому прикладі описано дослід, що проводився для визначення, чи лікування пероральним введенням СІ в дозі 500мкг/день мало наслідком виникнення толерантності до СІ в хворих, включених у дослідження, описане в Прикладі 1. До та після 12-місячного курсу лікування природним бичачим СІ, а також у разі виключення з дослідження на період від 3 до 11 місяців, в хворих брали проби сироватки та РВМС (Peripheral Blood Mononuclear Cell - Одноядерні клітини в периферійній крові). РВМС вирощувалися в культурі з ланцюжками бичачого α1(І), бичачого α2(І), з природним бичачим СІ або пептидами СВ (CNBr) з α1(І) або α2(І). Пептиди СВ виділяли розщепленням бичачих або людських α1(І) та α2(І) під дією CNBr (див. Фіг.4 та Таблицю 3) та очищенням методом іонно-обмінної хроматографії. Очищені пептиди СВ з α1(І) та α2(І), як і невиділені пептиди з α1(І) та α2(І), використовувалися в культурі РВМС, взятої з хворих на SSc на початковому рівні та перед прийманням СІ чи плацебо, а також на 12му місяці. Супернатанти РВМС піддавали аналізу ELISA (імуноферментний твердофазний аналіз) на вміст IFN та IL-10 на 0-му та 12-му місяцях. Зниження вмісту IFN або підвищення продукування IL-10 клітинами РВМС, стимульованими ланцюжками, після лікування пероральним введенням СІ визначали як первинну змінну імунологічного результату. Результати підсумовано в Таблицях 4-9. Як можна бачити з Таблиць 5-6, досягнуто значне зниження продукування IFN клітинами РВМС в суміш пептидів α1(І) СВ та в α1(І) СВ7 в групах хворих повної та пізньої фаз хвороби, що проходили лікування пероральним введенням СІ протягом 12 місяців. Крім того, спостерігається значне підвищення продукування IL-10 клітинами РВМС, вирощеним в культурах людських α2(І) та α1(І) СВ7 в групах хворих повної та пізньої фаз (Таблиці 7-8). Ці результати дають підстави припускати, що пероральне введення бичачого СІ є потенційно ефективним в лікуванні хворих на дифузну форму SSc, що триває >4 років, і це відбувається, без сумніву, завдяки модуляції продукування ТН1/ТН2. Підвищення продукування антиген-специфічного IL-10 дає підстави сподіватися на набуття толерантності до СІ хворими, що досягли летальної концентрації. Стосовно всього контингенту хворих на SSc, спостерігалися зворотні кореляції між тривалістю хвороби та продукуванням IL-10: α1(І) CB3 (р=0,0059, N=153); α1(І) СВ7 (р=-0.0335, N=150); людський α1(І) (р=-0,0166, N=152); суміш α2(І) СВ (р=0,0032, N=154). 93063 8 Стосовно ранніх хворих, спостерігалася зворотна кореляція між MRSS та продукуванням IFN в α2(І) СВ2 (р=-0,026, N=94). Стосовно всього контингенту хворих на SSc, спостерігалася зворотна кореляція між SF-36 та продукуванням IFN в α1(І) CB4 (р=-0,0448, N=143). Стосовно пізніх хворих, спостерігалася зворотна кореляція між SF-36 та продукуванням IFN в α1(І) СВ4 та РНА (фітогемагглютинін) (відповідно р=-0,0364, N=57; р=-0,028, N=58). Стосовно всього контингенту хворих на дифузний SSc, спостерігалася пряма кореляція між FVC та продукуванням IL-10 клітинами РВМС, вирощеними в культурі α1(І) CB4 та людській α2(І) (відповідно р=0,0122, N=152; р=0,0072, N=94). Стосовно ранніх хворих, спостерігалася пряма кореляція між FVC та продукуванням IL-10 в людську α2(І) (р=0,0062, N=94). Стосовно ранніх хворих, спостерігалася зворотна кореляція між FEV1 та продукуванням IL-10 в α2(І) СВ4 та суміш α1(І) СВ (відповідно р=0,0067, N=92; р=-0,0041, N=94). Стосовно всього контингенту хворих на SSc, спостерігалася зворотна кореляція між FEV1 та продукуванням IL-10 в суміш α1(І) CB (р=0,0241, N=154). Стосовно ранніх хворих, спостерігалася пряма кореляція між DLCO та продукуванням IFN в α1(І) CB7 (р=0,0367, N=90). Стосовно ранніх хворих, спостерігалася пряма кореляція між DLCO та продукуванням IFN в α2(І) СВ2 (р=0,0383, N=59). В сумі, вивчення імунної реакції на основі культури РВМС, взятої в хворих з СІ, та пептидів, отриманих з СІ, показало, що більше продукування IFN and IL-10 культурою РВМС відбувалося у хворих на ранній стадії хвороби (тривалість
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for treatment of sclerodermia using collagen fragments
Автори англійськоюPOSTLETHWAITE ARNOLD E, KANG ANDREW H
Назва патенту російськоюСпособ лечения склеродермии с применением фрагментов коллагена
Автори російськоюПаслтвейт Арнольд Е., Канг Ендрю Г.
МПК / Мітки
МПК: A61K 38/39, A61P 43/00
Мітки: спосіб, склеродермії, лікування, застосуванням, колагену, фрагментів
Код посилання
<a href="https://ua.patents.su/10-93063-sposib-likuvannya-sklerodermi-iz-zastosuvannyam-fragmentiv-kolagenu.html" target="_blank" rel="follow" title="База патентів України">Спосіб лікування склеродермії із застосуванням фрагментів колагену</a>
Попередній патент: Первинна кисла фосфатна сіль антагоніста рецептора простагландину d2
Наступний патент: Штучний шаруватий матеріал для резонансних дек музичних інструментів
Випадковий патент: Установка для одержання метилового ефіру жирних кислот