Застосування ротиготину для лікування або попередження втрати допамінергічних нейронів
Формула / Реферат
1. Застосування ротиготину, його солей або проліків для виробництва медикаменту для лікування або профілактики захворювань, пов'язаних зі збільшеною деструкцією допамінергічних клітин,
де лікування або профілактику здійснюють на індивідах, яких вибрано з групи:
(a) індивіди без симптомів хвороби Паркінсона, але зі збільшеним ризиком розвитку хвороби Паркінсона, які проявляють мутацію в ПАРК-гені та/або піддаються дії сильних інсектицидів; та/або
(b) індивіди з ранніми симптомами хвороби Паркінсона, у яких ще не присутні принаймні три з чотирьох кардинальних симптомів хвороби Паркінсона (ригідність, тремор в спокійному стані, брадикінезія, нестабільність осанки),
де проліками ротиготину є естери, карбонати, карбамати, ацеталі, кеталі, ацилоксіалкілові етери, фосфати, фосфонати, сульфати, сульфонати, тіокарбонільні естери,окситіокарбонільні естери, тіокарбамати, етери та силілові етери фенольної гідроксильної групи ротиготину.
2. Застосування за п. 1, де медикамент призначений для профілактики хвороби Паркінсона.
3. Застосування за п. 1, де хворобу, яка асоційована із збільшеною деструкцією допамінергічних клітин, вибрано з альфа-синуклеопатій, хвороби Гентингтона, REM-порушення швидкого сну та розладів нюху.
4. Застосування за будь-яким з попередніх пунктів, де індивіди виявляють один чи більше з наступних ранніх клінічних симптомів: розлади нюху, депресія, розлади швидкого сну типу "REM-поведінковий розлад", обстипація та короткотермінові аномалії руху.
5. Застосування за будь-яким з попередніх пунктів, де індивіди виявляють мутацію у ПАРК-гені та/або модифікації у альфа-синуклеїновій або нейромеланіновій системі.
6. Застосування за будь-яким з попередніх пунктів, де індивіди перед початком застосування медикаменту виявляють втрату допамінергічних клітин у чорній субстанції менше 60 %.
7. Застосування за будь-яким з попередніх пунктів, де індивіди перед початком застосування медикаменту мають показник за шкалою UPDRS менше 9.
8. Застосування за будь-яким з попередніх пунктів, де індивіди мають моторний показник за Hoehn-Yahr, що складає 0.
9. Застосування за будь-яким з попередніх пунктів, де медикамент призначений для парентерального, трансдермального застосування або застосування до слизової.
10. Застосування за будь-яким з попередніх пунктів, де ротиготин вводять у дозах 0,05-50 мг на добу.
11. Застосування за будь-яким з попередніх пунктів, де проліки вибрано з групи: естери, карбамати, ацеталі, кеталі, фосфати, фосфонати, сульфати, сульфонати та силілові етери.
12. Застосування за будь-яким з пп. 1-10, де проліки вибрано з групи: карбонати, ацилоксіалкілові етери, тіокарбонілові естери, окситіокарбонілові естери, тіокарбамати та етери.
13. Застосування за будь-яким з попередніх пунктів, де медикамент містить на додаток до ротиготину одну речовину з антиапоптотичною дією, таку як Міноциклін, FK-506, Циклоспорин А або zVAD та/або нейротрофіни.
14. Медикамент, який містить ротиготин, його солі або проліки та фармацевтично прийнятні ад'юванти, для лікування або профілактики захворювань, пов'язаних зі збільшеною деструкцією допамінергічних клітин,
де лікування або профілактику здійснюють на індивідах, яких вибрано з групи:
(a) індивіди без симптомів хвороби Паркінсона, але зі збільшеним ризиком розвитку хвороби Паркінсона, які проявляють мутацію в ПАРК-гені та/або піддаються дії сильних інсектицидів; та/або
(b) індивіди з ранніми симптомами хвороби Паркінсона, у яких ще не присутні принаймні три з чотирьох кардинальних симптомів хвороби Паркінсона (ригідність, тремор в спокійному стані, брадикінезія, нестабільність осанки),
де проліками ротиготину є естери, карбонати, карбамати, ацеталі, кеталі, ацилоксіалкілові етери, фосфати, фосфонати, сульфати, сульфонати, тіокарбонільні естери, окситіокарбонільні естери, тіокарбамати, етери та силілові етери фенольної гідроксильної групи ротиготину.
15. Комплект для діагностування та профілактичного лікування хвороби Паркінсона, що містить
(а) діагностичний засіб, що робить можливим діагностування хвороби Паркінсона та/або схильності до виявлення хвороби Паркінсона на ранній або асимптоматичній стадії, та
(b) медикамент згідно з п. 14.
16. Комплект за п. 15, де діагностичний засіб (а) вибрано з групи:
(і) засіб або діагностичний комплект для визначення нейромеланіну,
(іі) засіб або діагностичний комплект для визначення семафорину 3,
(ііі) засіб або діагностичний комплект для визначення альфа-синуклеїну та/або його агрегатів, або
(iv) засіб або діагностичний комплект для генетичного визначення мутації, асоційованої з виявом хвороби Паркінсона, та/або алелі, асоційованої з більш частим виявом хвороби Паркінсона.
Текст
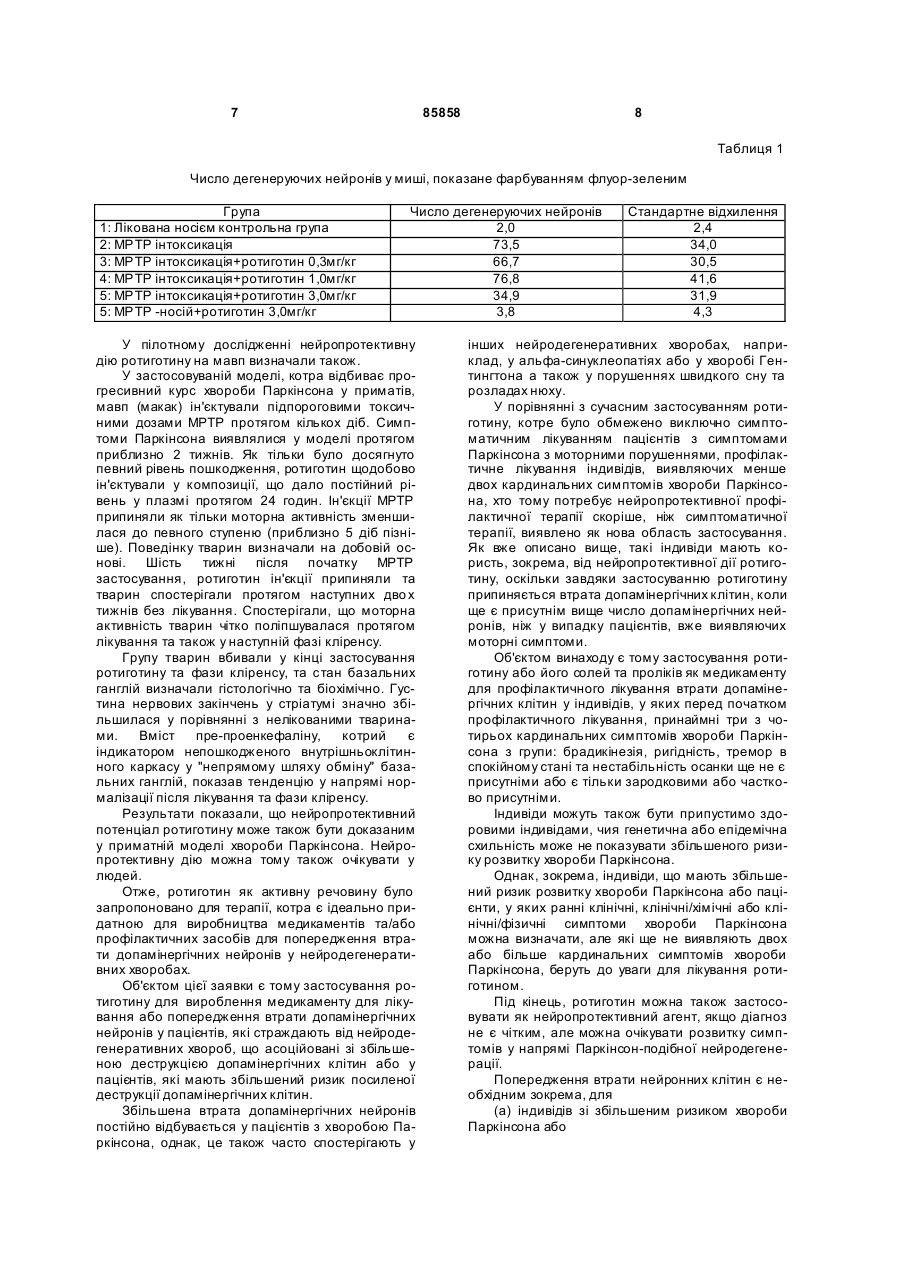
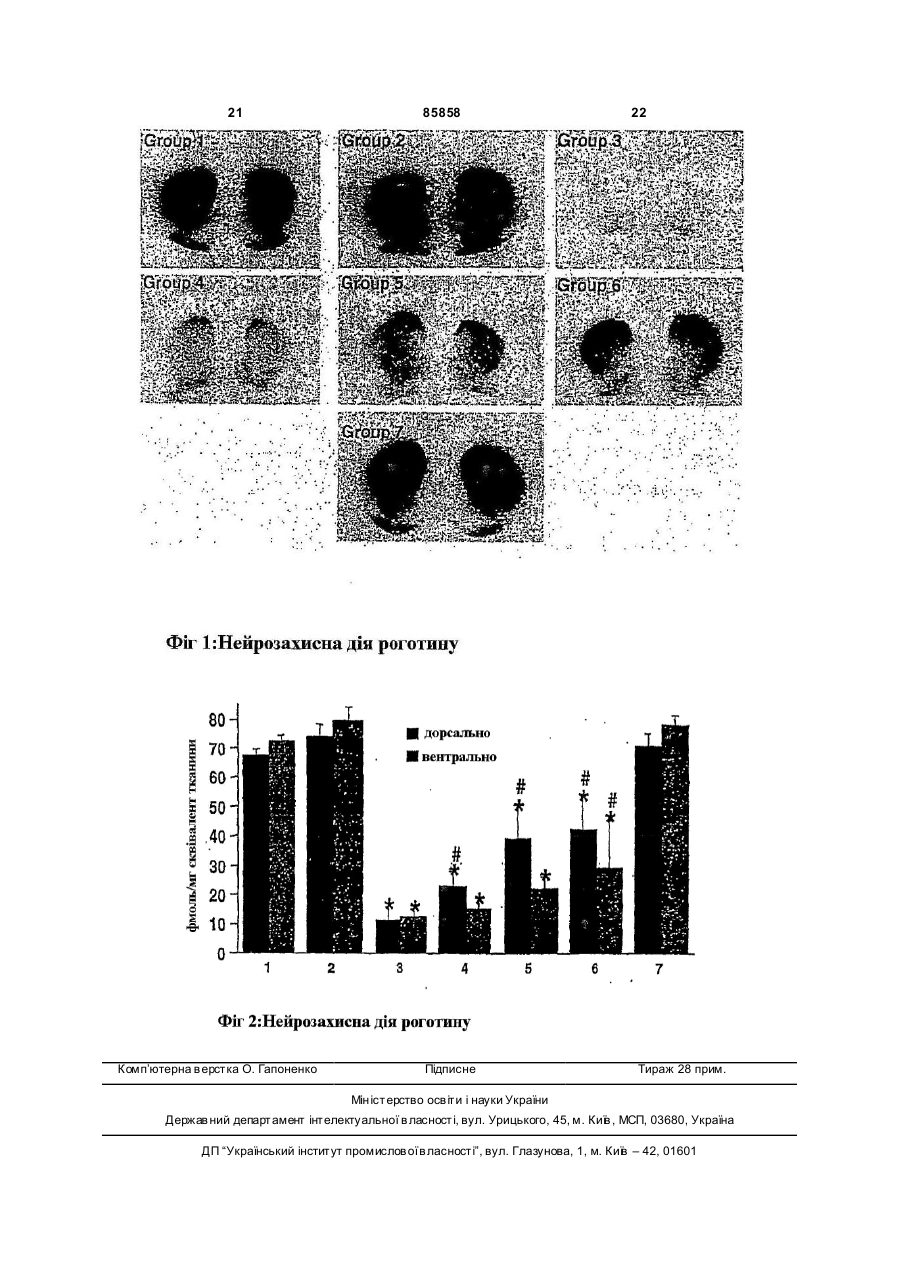
1. Застосування ротиготину, його солей або проліків для виробництва медикаменту для лікування або профілактики захворювань, пов'язаних зі збільшеною деструкцією де лікування або профілактику здійснюють на індопамінергічних клітин, дивідах, яких вибрано з групи: (a) індивіди без симптомів хвороби Паркінсона, але зі збільшеним ризиком розвитку хвороби Паркінсона, які проявляють мутацію в ПАРК-гені та/або піддаються дії сильних інсектицидів; та/або (b) індивіди з ранніми симптомами хвороби Паркінсона, у яких ще не присутні принаймні три з чотирьох кардинальних симптомів хвороби Паркінсона (ригідність, тремор в спокійному стані, брадикінезія, нестабільність осанки), де проліками ротиготину є естери, карбонати, карбамати, ацеталі, кеталі, ацилоксіалкілові етери, фосфа ти, фосфонати, сульфати, сульфонати, тіокарбонільні естери, окситіокарбонільні естери, 2 (19) 1 3 85858 4 13. Застосування за будь-яким з попередніх пункфосфа ти, фосфонати, сульфати, сульфонати, тів, де медикамент містить на додаток до ротиготіокарбонільні естери, окситіокарбонільні естери, тину одну речовину з антиапоптотичною дією, таку тіокарбамати, етери та силілові етери фенольної як Міноциклін, FK-506, Циклоспорин А або zVAD гідроксильної групи ротиготину. та/або нейротрофіни. 15. Комплект для діагностування та профілактич14. Медикамент, який містить ротиготин, його солі ного лікування хвороби Паркінсона, що містить або проліки та фармацевтично прийнятні ад'юван(а) діагностичний засіб, що робить можливим діагти, для лікування або профілактики захворювань, ностування хвороби Паркінсона та/або схильності пов'язаних зі збільшеною деструкцією допамінергідо виявлення хвороби Паркінсона на ранній або чних клітин, асимптоматичній стадії, та де лікування або профілактику здійснюють на ін(b) медикамент згідно з п. 14. дивідах, яких вибрано з групи: 16. Комплект за п. 15, де діагностичний засіб (а) (a) індивіди без симптомів хвороби Паркінсона, вибрано з групи: але зі збільшеним ризиком розвитку хвороби Пар(і) засіб або діагностичний комплект для визначенкінсона, які проявляють мутацію в ПАРК-гені ня нейромеланіну, та/або піддаються дії сильних інсектицидів; та/або (іі) засіб або діагностичний комплект для визна(b) індивіди з ранніми симптомами хвороби Паркічення семафорину 3, нсона, у яких ще не присутні принаймні три з чоти(ііі) засіб або діагностичний комплект для визнарьох кардинальних симптомів хвороби Паркінсона чення альфа-синуклеїну та/або його агрегатів, або (ригідність, тремор в спокійному стані, брадикіне(iv) засіб або діагностичний комплект для генетичзія, нестабільність осанки), ного визначення мутації, асоційованої з виявом де проліками ротиготину є естери, карбонати, кархвороби Паркінсона, та/або алелі, асоційованої з бамати, ацеталі, кеталі, ацилоксіалкілові етери, більш частим виявом хвороби Паркінсона. Хвороба Паркінсона відбувається як результат хронічної, прогресивної дегенерації нейронів, причина котрої ще не ясна. Вона клінічно виражається у формі кардинальних симптомів тремору в спокійному стані, ригідності, брадикінезії та нестабільності осанки. Первинно застосовуваними як медикаменти для полегшення моторних симптомів є леводоп, агоністи допаміну, як-то, наприклад, ротиготин, прамірекзол, бромкриптин, ропінірол, каберголін, перголід, апоморфін та лузирид, антихолінергічні засоби, антагоністи NMDA, b-блокатори а також інгібітор МАО-В селегелін та інгібітор СОМТ ентакапон. Більшість цих активних речовин втручається у допамінергічний та/або холінергічний сигнальний каскад та симптоматично впливає таким чином на моторні порушення, що є звичайною хворобою Паркінсона. Терапія хвороби Паркінсона на сьогодні починається з появи кардинальних симптомів. Хвороба Паркінсона, як загалом вважають, клінічно підтверджена, якщо можна визначити принаймні два з чотирьох кардинальних симптомів (брадикінезія, тремор в спокійному стані, ригідність та нестабільність осанки) та має дію L-Допа [Hughes, J Neurol Neurosurg Psychiatry 55, 1992, 181]. На жаль, однак, пацієнти з хворобою Паркінсона тільки виявляють моторне порушення тоді, коли приблизно 70-80% допамінергічних нейронів у чорній субстанції (SN) необоротно пошкоджені [Becker et al, J Neurol 249, 2002, Suppl 3: III, 40; Homykiewicz, Encyclopaedia of Life Science 2001, 1]. Шанси терапії з тривалою дією є мінімальними у цей час. Отже потрібно починати терапію так рано, як можливо. Сучасні клінічні спостереження, а також анатомічні та генетичні дослідження зараз показали, що можливо діагнозувати пацієнтів з хворобою Паркінсона на ранній стадії та дляідентифікації пацієнтів зі збільшеним ризиком. Наступне, наприклад, можна, таким чином, застосовувати як діагностичні маркери: - Біохімічні маркери, як-то нейромеланін [Gerlach, Neurotox Res 5, 2003, 35; WO 02/31499], S-100 бета [Muramatsu, Glia 42, 2003, 307], альфа синуклеїн [WO 03/069332; WO 00/02053] або паркін-білок [Sharma, Neurol Clin N Am 20, 2002, 759] та семафорин [WO 03/007803]. - Генетичні маркери, як-то парк-гени 1-8 [Guttman, CMAJ 4, 2003, 168]; CYP2D6-B [WO 03/012137], хромосома 2q 36-37 [Pankratz, Am J Hum Gen 72, 2003, e-pub], a-синуклеїн [Polimeropoulos, Science. 276, 1997, 2045] або мутації у делеції CYP2D6-B та GSTM1 [WO03/012137]T* - Способи відображення, як-то ультразвукове обстеження розміру SN, можливо у комбінації з іншими способами [Becker et al, J Neural 249,2002, Suppl 3: III, 40] або MRI (відображення магнітного резонансу) [Hutchinson Μ, Raff U., J Neural Neurosurg Psychiatry. 1999 Dec; 67(6): 815- 8]. - Способи відображення, як-то PET (позитронна емісійна томографія) або SPECT (емісійна комп'ютерна томографія) [Prunier С, Bezard E et al, Neuroimage. 2003 July; 19(3): 810-6]. - Сенсорні розлади або анормальності поведінки, як-то розлади сну та нюху, зокрема, розлади швидкого сну типу "REM-поведінковий розлад" (поведінковий розлад при швидкому сні), [Henderson, J Neural Neurosurg Psychiatry 74, 2003, 956] або когнітивні анормальності [Rammsayer, Int J Neurosci. 91, 1997, 45]. - Органічні проблеми, як-то обстипація [Krygowska-Wajs, Funct Neural 15, 2000, 41]. - Депресія [Camicioli R. Prodrugs Today (Bare). 2002 Oct; 38(10): 677-86]. 5 85858 6 - Короткотермінові аномалії руху, як-то хорея Експериментальні тести, однак, зараз несподіабо ортостатичні анормальності. Комбінації вищевано показали, що ротиготин, котрий до цього часу зазначених маркерів [Stern, Annals of Neural 56, застосовували тільки для симптоматичної терапії 2004, 169]. хвороби Паркінсона, має нейропротективні власЦе отже створює сприятливу можливість тивості та/або сприяє регенеративній здатності впливу на процес хвороби у час, коли більше нейнейронних елементів, так що ротиготин можна ронів ще є присутніми, ніж це є у випадку появи тому застосовувати як медикамент та/або профікількох кардинальних моторних симптомів хвороби лактичний агент для попередження втрати допаПаркінсона, а тому для захисту кількісно більшого мінергічних клітин також, а зокрема у дуже ранніх числа нейронів. Можна очікувати, що застосування стадіях хвороби Паркінсона або у пацієнтів зі збіефективного нейропротективного засобу на ранній льшеним ризиком. стадії значно затримуватиме процес хвороби: Фіг.1 показує репрезентативні приклади нейБільш ранню терапію можна починати, отримуючи ропротективної дії ротиготину, виміряної на базі більші шанси довготривалого попередження появи густини транспортерів допаміну як показання гуссимптомів, що знижують якість життя. тини того, нервових закінчень, що залишилися у Існує потреба у медикаментах, що не тільки стріатумі. здатні впливати на допамінергічну передачу та Групи 1-7 лікували так: Група 1: нелікована кополегшення симптомів хвороби Паркінсона на пентрольна група; Група 2: контрольна група, ліковаредових стадіях, але також здатні до реверсуванна носієм для ротиготину та МРТР; Група 3: лікуня, попередження або принаймні значного уповівання МРТР; Група 4: лікування МРТР плюс льнення прогресивної деструкції допамінерпчних ротиготин 0,3мг/кг; Група 5: лікування МРТР плюс нейронів у ранніх, значною мірою моторноротиготин 1,0мг/кг; Група 6: лікування МРТР плюс асимптоматичних стадіях хвороби Паркінсона ротиготин 3,0мг/кг; Група 7: лікування виключно [Dawson, Nature Neuroscience Supplement 5, 2002, ротиготином (3,0мг/кг). 1058]. Фіг.2 показує зв'язування транспортеру допаРотиготин [(-)-5,6,7,8-тетрагідро-6-[пропіл[2-(2міну (DAT) у дорсальній та вентральній частині тієніл)етил]аміно]-1-нафтол] відомий у рівні техніки стріатуму у різних групах виміром густини DAT як агоніст допаміну та як терапевтичний агент визгідно з експериментом, показаним у Фіг.1. Гістоключно для симптомів хвороби Паркінсона. [WO грами 1-7 відповідають групам 1-7, показаним у 02/089777] описує, наприклад, трансдермальне Фіг.1. Групи, помічені *, показували значне падіння застосування ротиготину до пацієнтів з хворобою зв'язування DAT у порівнянні з контрольною груПаркінсона та асоційоване поліпшення за показнипою 2. Групи, помічені #, показували значний виком UPDRS (уніфікована шкала оцінок хвороби граш зв'язування DAT у порівнянні з МРТРПаркінсона). Шкала UPDRS є важливим інструмелікованою групою 3. нтом для діагностики та моніторингу прогресуванПроцеси апоптозу, як припускають, грають ваня та/або терапії пацієнтів з хворобою Паркінсона жливу роль у деструкції допамінергічних нейронів [Fahn S, Elton RL, Members of UPDRS Development у патогенезі хвороби Паркінсона [Barzilai, Cell Мої Committee (1987) Unified Parkinson's Disease Rating Neurobiol 21, 2001, 215]. Нейропротективні речоScale (уніфікована шкала оцінок хвороби Паркінвини, що можуть зупинити або навіть реверсувати сона). У: Fahn, S, CD Marsden, DB Calne, Μ деструкцію допамінергічних клітин є тому потрібGoldstein (eds) Recent Developments in Parkinson's ними. МРТР-модель таким чином, можна вважати, Disease. Vol. II. Macmillan Healthcare Information, є прогнозувальною стосовно необхідних нейроFlorham Park (NT), pages 153-163, 293-304]. Однак, протективних характеристик [Dawson, Nature шкала UPDRS тільки реєструє дію активної речоNeuroscience Supplement 5, 2002, 1058]. вини на симптоми хвороби Паркінсона. Це не доРотиготин несподівано показує потрібний фазволяє робити будь-яких заяв, стосовно того чи рмакологічний профіль як у гострій, так і підгострій має активна речовина вплив на деструкцію допаМРТР-моделі. Тест-результати свідчать, що промінергічних клітин, котрі лежать в основі симптоцеси апоптозу попереджуються ротиготином. мів. Ротиготин таким чином виявляє нейропротекMetman et al [Clin Neuropharmacol 24, 2001, тивну дію у мишачій моделі хвороби Паркінсона: 163] також описують дію ротиготину на моторні Після гострого застосування МРТР, котре викликає порушення, асоційовані з хворобою Паркінсона. синдром Паркінсона у людей та мавп, число дегеЛіковані пацієнти вже мали чітку дискінезію, котру неруючих нейронів у гострій фазі вимірювали з поліпшували застосуванням ротиготину. одного боку (Таблиця 1), а функціональну цілісОтже, ротиготин відомий у рівні техніки як агоність стріатуму у підгострій фазі оцінювали з іншоніст допаміну для симптоматичного лікування хвого визначенням густин транспортеру допаміну у роби Паркінсона. Однак, медикаменти для цього, термінальних нервових закінченнях (Фіг.1 та 2). Це що мають тільки дію на симптоми не обіцяють можна було б продемонструвати в обох випадках, будь-яких переваг стосовно випереджувального що ротиготин мав нейропротективну дію: 3 одного лікування хвороби Паркінсона, оскільки вони не боку, число дегенеруючих нейронів у мезенцефамають будь-якого впливу на деструкцію допамінелоні зменшувалося після застосування ротиготину ргічних клітин або на прогресування та/або інтента з іншого боку, допамінергічна іннервація стріасивність хвороби. туму була майже повністю відновленою або збереженою. 7 85858 8 Таблиця 1 Число дегенеруючих нейронів у миші, показане фарбуванням флуор-зеленим Група 1: Лікована носієм контрольна група 2: МРТР інтоксикація 3: МРТР інтоксикація+ротиготин 0,3мг/кг 4: МРТР інтоксикація+ротиготин 1,0мг/кг 5: МРТР інтоксикація+ротиготин 3,0мг/кг 5: МРТР -носій+ротиготин 3,0мг/кг Число дегенеруючих нейронів 2,0 73,5 66,7 76,8 34,9 3,8 У пілотному дослідженні нейропротективну дію ротиготину на мавп визначали також. У застосовуваній моделі, котра відбиває прогресивний курс хвороби Паркінсона у приматів, мавп (макак) ін'єктували підпороговими токсичними дозами МРТР протягом кількох діб. Симптоми Паркінсона виявлялися у моделі протягом приблизно 2 тижнів. Як тільки було досягнуто певний рівень пошкодження, ротиготин щодобово ін'єктували у композиції, що дало постійний рівень у плазмі протягом 24 годин. Ін'єкції МРТР припиняли як тільки моторна активність зменшилася до певного ступеню (приблизно 5 діб пізніше). Поведінку тварин визначали на добовій основі. Шість тижні після початку МРТР застосування, ротиготин ін'єкції припиняли та тварин спостерігали протягом наступних дво х тижнів без лікування. Спостерігали, що моторна активність тварин чітко поліпшувалася протягом лікування та також у наступній фазі кліренсу. Групу тварин вбивали у кінці застосування ротиготину та фази кліренсу, та стан базальних ганглій визначали гістологічно та біохімічно. Густина нервових закінчень у стріатумі значно збільшилася у порівнянні з нелікованими тваринами. Вміст пре-проенкефаліну, котрий є індикатором непошкодженого внутрішньоклітинного каркасу у "непрямому шляху обміну" базальних ганглій, показав тенденцію у напрямі нормалізації після лікування та фази кліренсу. Результати показали, що нейропротективний потенціал ротиготину може також бути доказаним у приматній моделі хвороби Паркінсона. Нейропротективну дію можна тому також очікувати у людей. Отже, ротиготин як активну речовину було запропоновано для терапії, котра є ідеально придатною для виробництва медикаментів та/або профілактичних засобів для попередження втрати допамінергічних нейронів у нейродегенеративних хворобах. Об'єктом цієї заявки є тому застосування ротиготину для вироблення медикаменту для лікування або попередження втрати допамінергічних нейронів у пацієнтів, які страждають від нейродегенеративних хвороб, що асоційовані зі збільшеною деструкцією допамінергічних клітин або у пацієнтів, які мають збільшений ризик посиленої деструкції допамінергічних клітин. Збільшена втрата допамінергічних нейронів постійно відбувається у пацієнтів з хворобою Паркінсона, однак, це також часто спостерігають у Стандартне відхилення 2,4 34,0 30,5 41,6 31,9 4,3 інших нейродегенеративних хворобах, наприклад, у альфа-синуклеопатіях або у хворобі Гентингтона а також у порушеннях швидкого сну та розладах нюху. У порівнянні з сучасним застосуванням ротиготину, котре було обмежено виключно симптоматичним лікуванням пацієнтів з симптомами Паркінсона з моторними порушеннями, профілактичне лікування індивідів, виявляючих менше двох кардинальних симптомів хвороби Паркінсона, хто тому потребує нейропротективної профілактичної терапії скоріше, ніж симптоматичної терапії, виявлено як нова область застосування. Як вже описано вище, такі індивіди мають користь, зокрема, від нейропротективної дії ротиготину, оскільки завдяки застосуванню ротиготину припиняється втрата допамінергічних клітин, коли ще є присутнім вище число допамінергічних нейронів, ніж у випадку пацієнтів, вже виявляючих моторні симптоми. Об'єктом винаходу є тому застосування ротиготину або його солей та проліків як медикаменту для профілактичного лікування втрати допамінергічних клітин у індивідів, у яких перед початком профілактичного лікування, принаймні три з чотирьох кардинальних симптомів хвороби Паркінсона з групи: брадикінезія, ригідність, тремор в спокійному стані та нестабільність осанки ще не є присутніми або є тільки зародковими або частково присутніми. Індивіди можуть також бути припустимо здоровими індивідами, чия генетична або епідемічна схильність може не показувати збільшеного ризику розвитку хвороби Паркінсона. Однак, зокрема, індивіди, що мають збільшений ризик розвитку хвороби Паркінсона або пацієнти, у яких ранні клінічні, клінічні/хімічні або клінічні/фізичні симптоми хвороби Паркінсона можна визначати, але які ще не виявляють двох або більше кардинальних симптомів хвороби Паркінсона, беруть до уваги для лікування ротиготином. Під кінець, ротиготин можна також застосовувати як нейропротективний агент, якщо діагноз не є чітким, але можна очікувати розвитку симптомів у напрямі Паркінсон-подібної нейродегенерації. Попередження втрати нейронних клітин є необхідним зокрема, для (a) індивідів зі збільшеним ризиком хвороби Паркінсона або 9 85858 10 (b) індивідів з ранніми симптомами хвороби ланіновій системі. Такі модифікації можуть бути Паркінсона. обумовленими, наприклад, експресією генетичТермін "хвороба Паркінсона" у цій патентній них варіантів, наприклад, альфа синуклеїну, роззаявці охоплює ідіопатичну та генетичну хворобу витком агрегатів чи волокон, наприклад, альфа Паркінсона. Так званий синдром Паркінсон-Плюс синуклеїну, або збільшеним вивільненням з цеа також вторинний паркінсонізм є диференційолюлярних резервів, наприклад, з цитоплазми ваним звідси. клітин, що руйн уються, як у випадку з нейромеТермін "кардинальні симптоми" хвороби Парланіном. кінсона слід розуміти у цій патентній заявці як Ранні клінічні/фізичні симптоми можуть бути один або більше симптомів брадикінезії, ригідноструктурними або функціональними змінами мозсті, тремору в спокійному стані та нестабільності ку, котрі можна фізично визначати, наприклад, осанки. засобами PET та SPECT, досліджень засобами "Індивідів зі збільшеним ризиком хвороби Патранскраніальної сонографії [Becker, J Neurol ркінсона" слід розуміти у цій патентній заявці зок249, Suppl 3, 2002,111/40; Prunier С, et al, рема, як індивідів, які ще не виявляють будь-яких Neuroimage. 2003 Jul; 19(3): 810-6] або визначенвизначуваних симптомів хвороби Паркінсона, але ням біохімічних маркерів, як-то нейромеланіну мають певні фактори ризику. [WO 02/31499]. Такими факторами ризику можуть бути генеРанніми клінічними симптомами можуть бути тичні мутації (Nussbaum NEJM 348, 2003, 25). розлади нюху, депресія, порушення візуальних та Наприклад, паркін-ген на хромосомі 6q25,2-27 когнітивних функцій або розлади сну, завдяки (PARK2) асоційований з ювенільним паркінсонізчому комбінацію відмінних тестів можна також мом та відбувається більше часто у родинах з застосовувати для раннього діагнозу [Becker, J автосомною рецесивною спадковістю до паркінNeurol 249, Suppl 3, 2002,111/40; Stern, Annals of сонізму [Matsumine, Am. J. Hum. Genet., 60, 1997, Neurol 56, 2004, 169]. 588; Kitada, Nature 392, 1998, 605; Abbas, Hum. Як вже обговорено вище, приблизно 70-80% Mol. Genet. 8, 1999, 567; Tassin, Am. J. Hum. допамінергічних нейронів чорної субстанції вже Genet., 63, 1998, 88 und Lucking, N. Engl. J. Med. зруйновані на час, коли принаймні два з чотирьох 342, 2000, 1560-7]. Інші генні локуси, наприклад, кардинальних симптомів самі виражені вперше. PARK6 та PARK7, були також виявлені зі збільДля ефективного застосування несподіваного шеною частотою у родинах з ювенільною, реценейропротективного потенціалу ротиготину просивно-спадковою хворобою Паркінсона [Valente, філактичне лікування пацієнтів тому переважно Am. J. Hum. Genet. 68, 2001, 895; van Dujin, Am. J. починають на стадії, коли пацієнти мають нижчу Hum. Genet. 69, 2001, 629]. Мутації у альфавтрату допамінергічних клітин чорної субстанції синуклеїновому гені (PARK1) визначали у роди(SN). Індивіди, виявляючі один або не виявляючі нах з ювенільною, автосомною домінантножодного з кардинальних симптомів хвороби Парспадковою хворобою Паркінсона [Polimeropoulos, кінсона у чіткій формі є тому лікованими переваScience 276, 1997, 2045]. На додаток до генетичжно. ної схильності, впливи зовнішнього середовища, Індивіди, виявляючі втрату допамінергічних як-то високий вплив, наприклад, інсектицидів клітин у SN менше 70%, 60%, 50% та особливо [Vanacore, Neural Sci., Sep; 23 Suppl 2, 2002, page краще менше 40%, 30%, 20% або 10% є лікова119] може також бути фактори ризику. ними переважно. У цій патентній заявці, "індивідів з ранніми Два показника можна застосовувати як допосимптомами хвороби Паркінсона" слід розуміти, міжні засоби для діагностики та контролю терапії зокрема, як індивідів, у яких принаймні три з чопацієнтів, вже виявляючих помітні моторні порутирьох кардинальних симптомів (ригідність, трешення, тобто шкала UPDRS та шкала Hoehn та мор в спокійному стані, брадикінезія та нестабіYahr. льність осанки) відсутні або є тільки зародковими Згідно з кращим аспектом винаходу, гр упа або частково присутніми, але які виявляють діагпацієнтів профілактично лікованих ротиготином ностично придатні ранні клінічні, клінічні/біохімічні крім того має модифікований показник Hoehn та та/або клінічні/фізичні симптоми. Yahr 0-2, особливо краще 0-1 та найкраще 0. Клінічні/біохімічні маркери можуть бути модифікаціями у альфа синуклеїновій або нейромеТаблиця 2 Визначення модифіков аних стадій згідно[Hoehn, The natural history of Parkinson's disease in the pre-levodopa and postlevodopa eras. Neurologic Clinics (Природна історія хв ороби Паркінсона у періоді пре-лев одопа та пост-лев одопа), Neurologic Clinics 10, 1992,331] Стадія 0 = нема ознак хвороби. Стадія 1 = Одностороння хв ороба Стадія 1,5 = Одностороння плюс аксіальний баланс. Стадія 2 = Дв остороння хвороба без порушення балансу. Стадія 2,5 = М'яка дв остороння хвороба з пов ерненням на тягов е в ипробування. Стадія 3 = Дв остороння хвороба в ід м'якої до помірної: слабка нестабільність осанки; фізична незалежність. Стадія 4 = Сув ора безпомічність; ще є здатність до ходьби або стояння без допомоги. Стадія 5 = Прив'язаність до кріс ла або ліжка без допомоги 11 Пацієнтів з показником за шкалою UPDRS, частина III (дивись втілення 5), принаймні 10 звичайно класифікують як пацієнтів, яких можна піддавати допамінергічній терапії. Однак, група пацієнтів, придатних для отримання користі від нейропротективної дії роти готи ну переважно має дуже низький або невизначуваний моторний показник UPDRS (частин III). В межах сенсу заявленого винаходу, випереджувальне лікування ротиготином слід тому переважно проводити на пацієнтах, що мають моторний показник UPDRS менше 10, 9, 8, 7, 6, 5, 4, 3, 2 або 1. Особливо краще, коли пацієнти досі не виявляли будь-яких моторних порушень. Терміни "попередження", "профілактика" та "випереджувальне лікування" застосовано як синоніми у цій патентній заявці. Вони охоплюють, зокрема, застосування медикаменту до індивідів, у яких принаймні три з чотирьох кардинальних симптомів хвороби Паркінсона (ригідність, тремор в спокійному стані, брадикінезія, нестабільність осанки), відсутні або є тільки зародковими або частково присутніми, для попередження або затримки вияву або значного розвитку моторних симптомів хвороби Паркінсона та/або наступної втрати допамінергічних нейронів, особливо у чорній субстанції. Індивіди, яких слід профілактично лікувати, переважно ще не виявляють будь-яких кардинальних симптомів у чі ткій формі. Сполуки формули І є оптично активними та можуть бути рацематами або як чистими (R)- або (S)-енантіомерами. У цій патентній заявці, термін "чистий енантіомер" означає, що речовина переважно присутня принаймні на 90мол% у формі одного енантіомеру, наприклад, у (S) формі, вміст відповідного іншого енантіомер, наприклад, (R) форми, є відповідно низьким. Якщо, наприклад, ротиготин [(-)-5,6,7,8-тетрагідро-6-[пропіл[2(2-тієніл)етил]аміно]-1-нафтол] застосовують для виробництва медикаментів згідно з винаходом, вміст (R)-(+)-енантіомеру переважно менше 10мол%, особливо краще менше 2мол% та найкраще менше 1%, на основі загально кількості ротиготину у профілактичному засобі для хвороби Паркінсона. Індивіди, яких слід профілактично лікувати, переважно мають показник UPDRS менше 10, менше 9, 8, 7 або 6, а особливо краще менше 5, 4, 3, 2 або 1. У цій патентній заявці, "проліки" ротиготину слід розуміти зокрема, як сполуки, що розщеплюються, перетворюються або метаболізуються у ротиготин у тілі людини у терапевтично ефективній кількості, зокрема, у плазмі або при проходженні через шкіру або слизову мембрану. Ротиготин має формулу 85858 12 Зокрема, похідні від фенольних гідроксигруп слід брати до уваги як проліки, наприклад, естери, наприклад, арилкарбонілові естери, алкілкарбонілові естери або циклоалкілкарбонілові естери, зокрема, алкілкарбонілові естери та циклоалкілкарбонілові естери з числом атомів карбону до 6; карбонати; карбамати; ацеталі; кеталі; ацилоксіалкілові етери; фосфати; фосфонати; сульфати; сульфонати; тіокарбонілові естери; окситіокарбонілові естери; тіокарбамати; етери та силілові етери. Термін "алкілкарбонілові естери" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -С(О)алкіл. Термін "циклоалкілкарбонілові естери" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -С(О)циклоалкіл. Термін "арилкарбонілові естери" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -С(О)арил. Термін "карбонати" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з гр упою -C(O)-O-R. Термін "карбамат" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -C(O)-NRR1, -C(O)-NH-R1, або C(O)-NH2. Термін "ацеталі" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -CH(OR)R1. Термін "кеталі" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -C(OR)R1R2. Термін "ацилоксіалкілові етери" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -CHR-OC(O)-R1 або СН2-О-С(О)-R1. Термін "фосфат" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -P(O2H)OR. Термін "фосфонат" о хоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з гр упою -P(O2H)R. Термін "сульфат" о хоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -S(O)2OR. Термін "сульфонат" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з гр упою -S(O)2R. Термін "тіокарбонілові естери" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -C(=S)-R. Термін "окситіокарбонілові естери" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -C(=S)-OR. Термін "тіокарбамат" охоплює сполуки, у котрих атом оксигену ротиготину є зв'язаним у кожному випадку з групою -C(=S)-N-RR1, -C(=S)-NHR1 або -C(=S)-NH2. 13 85858 14 Термін "етери" охоплює сполуки, у котрих та особливо краще між 0.1 та 10нг/мл плазми, атом оксигену ротиготину є зв'язаним у кожному таким чином вважають як ефективні концентрації. випадку з групою -R. Ротиготин є S(-)-енантіомером 5,6,7,8У вищенаведеному визначенні проліків, R, R1 тетрагідро-6-[пропіл[2-(2-тієніл)етил]-аміно]-1та R2 кожний незалежно, вибрані з групи: гідронафтолу. Це означає, що згідно з винаходом, ген, алкіл, циклоалкіл або арил, та переважно з вміст (R)-енантіомеру, котрий є неактивним у групи: С1-6 алкіл, С3-10 циклоалкіл та феніл. моделі хвороби Паркінсона, у медикаменті є ниR3 - алкіл, зокрема, С1-6 алкіл. зьким. (R)-енантіомер є переважно присутній у "Алкіл" може бути з лінійним чи розгалужемедикаменті у пропорції
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of rotigotine for the treatment or prevention of dopaminergic neurone loss
Автори англійськоюScheller Dieter, Dressen Frank
Назва патенту російськоюПрименение ротиготина для лечения или предупреждения потери допаминергических нейронов
Автори російськоюШеллер Дитер, Дрессен Франк
МПК / Мітки
МПК: A61K 31/381, A61P 25/16
Мітки: допамінергічних, нейронів, втрати, попередження, ротиготину, лікування, застосування
Код посилання
<a href="https://ua.patents.su/11-85858-zastosuvannya-rotigotinu-dlya-likuvannya-abo-poperedzhennya-vtrati-dopaminergichnikh-nejjroniv.html" target="_blank" rel="follow" title="База патентів України">Застосування ротиготину для лікування або попередження втрати допамінергічних нейронів</a>
Попередній патент: Підшипник ковзання для малих питомих навантажень
Наступний патент: Теплоізолюючий контейнер (ті-бокс)
Випадковий патент: Спосіб клипіювання поперекових артерій при операції резекції аневризми черевної аорти