Каталізатор для застосування в реакції з високотемпературним зсувом та спосіб збагачення суміші синтез-газу воднем або монооксидом вуглецю
Формула / Реферат
1. Каталізатор для застосування в реакції з високотемпературним зсувом, який в своїй активній формі складається з суміші цинк-алюмінієвої шпінелі ZnAl2O4 та оксиду цинку у комбінації з лужним металом, вибраним з групи, яка складається з Na, K, Rb, Cs та їх сумішей, молярне співвідношення Zn/Al вказаного каталізатора знаходиться в діапазоні 0,5-1,0, та вміст лужного металу знаходиться в діапазоні 0,4-8,0 мас. % від маси окисленого каталізатора.
2. Каталізатор за п. 1, де лужним металом є калій та він є наявним у кількості від 1 до 3 мас. %.
3. Каталізатор за п. 1, де лужним металом є цезій та він є наявним у кількості від 5 до 10 мас. %.
4. Каталізатор за будь-яким з пп. 1-3, де молярне співвідношення Zn/Al у каталізаторі знаходиться в діапазоні 0,5-0,8.
5. Каталізатор за п. 1 або 2, де молярне співвідношення Zn/Al знаходиться в діапазоні 0,65-0,7 та каталізатор містить 31-34 мас. % Zn та 2,7-3,0 мас. % K.
6. Каталізатор за пп. 1 або 3, де молярне співвідношення Zn/Al становить 0,7, та каталізатор містить 34-36 мас. % Zn та 7-8 мас. % Cs.
7. Спосіб збагачення суміші синтез-газу воднем або монооксидом вуглецю шляхом взаємодії вказаної суміші синтез-газу з каталізатором за будь-яким з пп. 1-6.
8. Спосіб за п. 7, де суміш збагачують воднем та молярне співвідношення пари до сухого газу знаходиться в діапазоні від 0,05 до 0,9, температура 300-400 °С, та реактор працює при тиску, який знаходиться в діапазоні від 2,3 до 6,5 МПа.
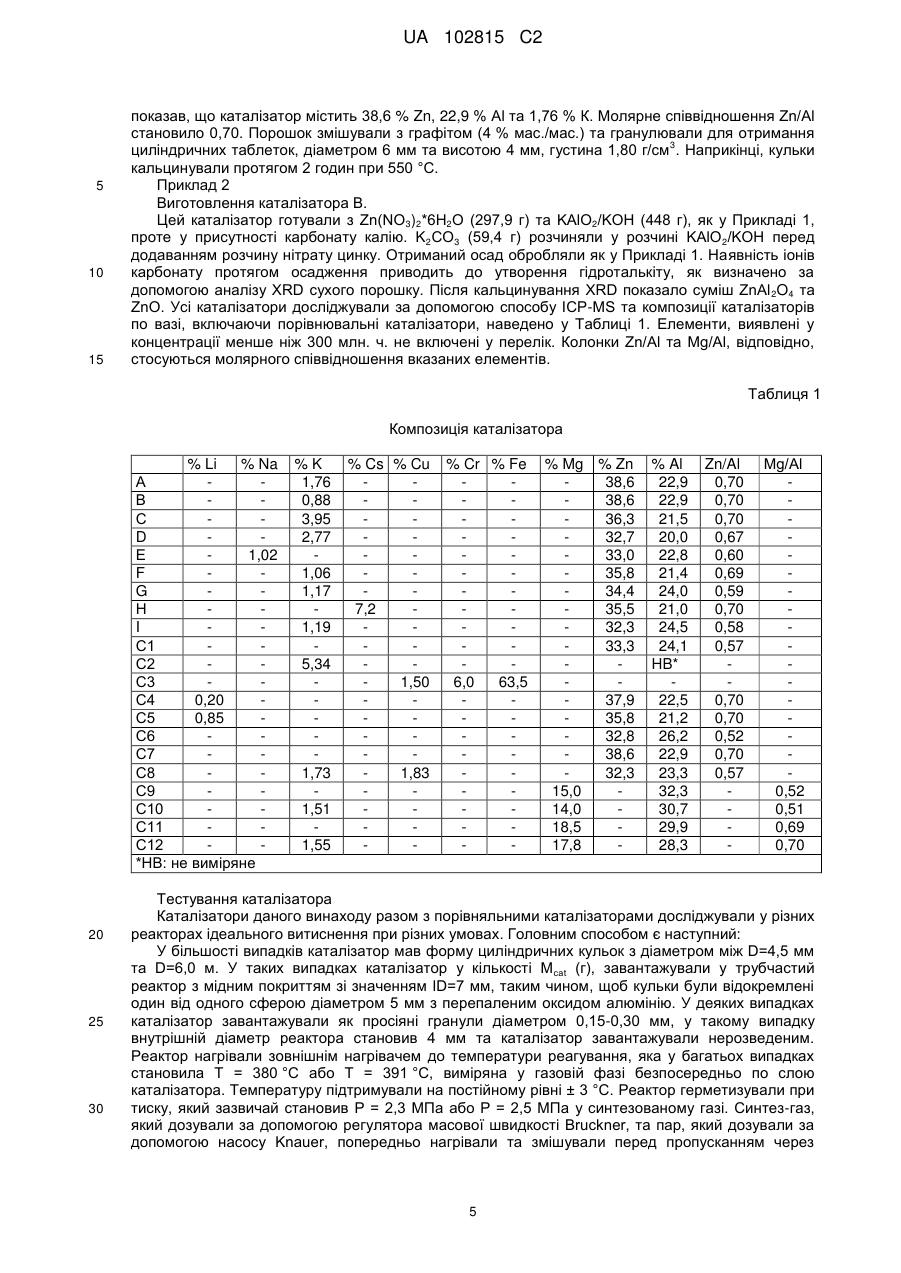
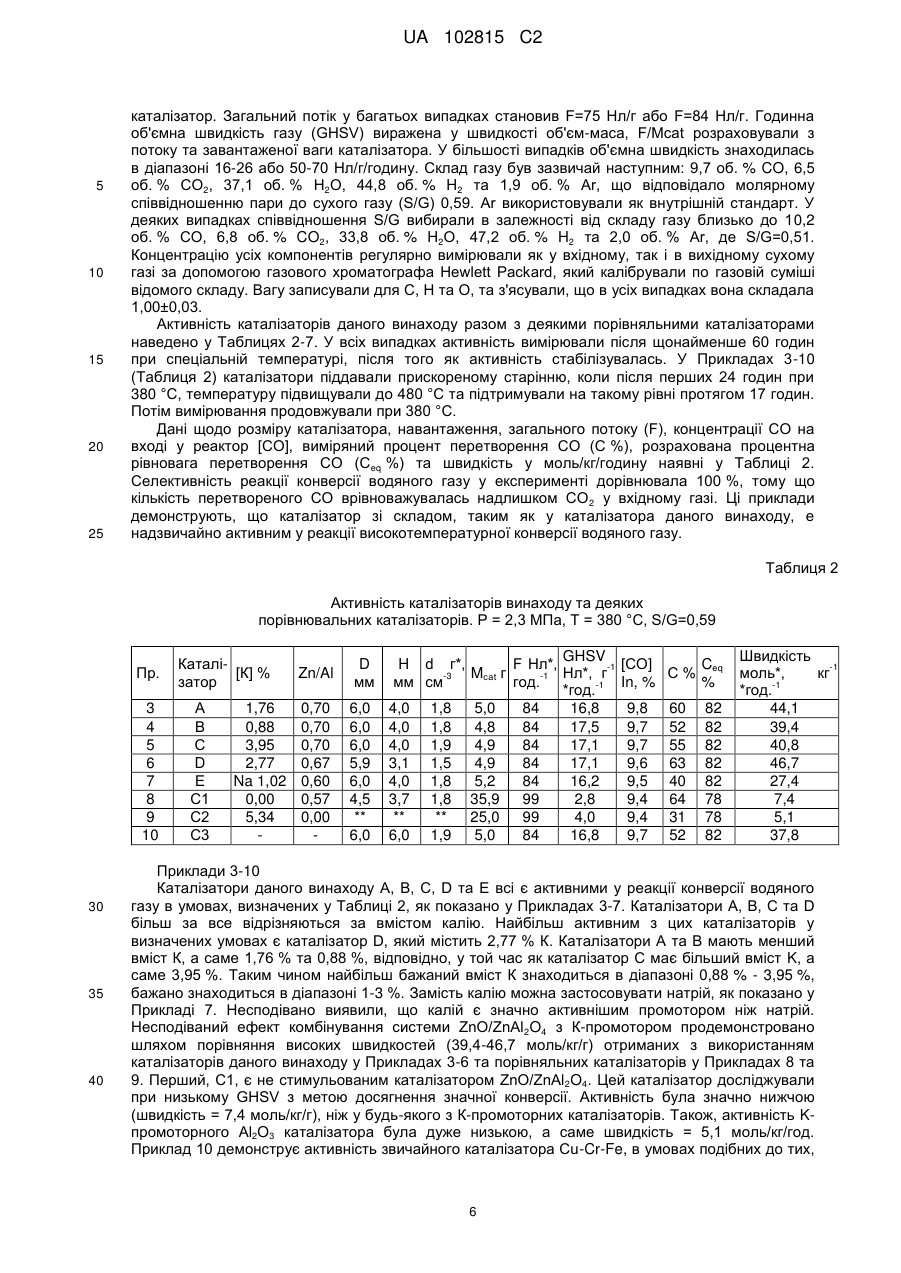
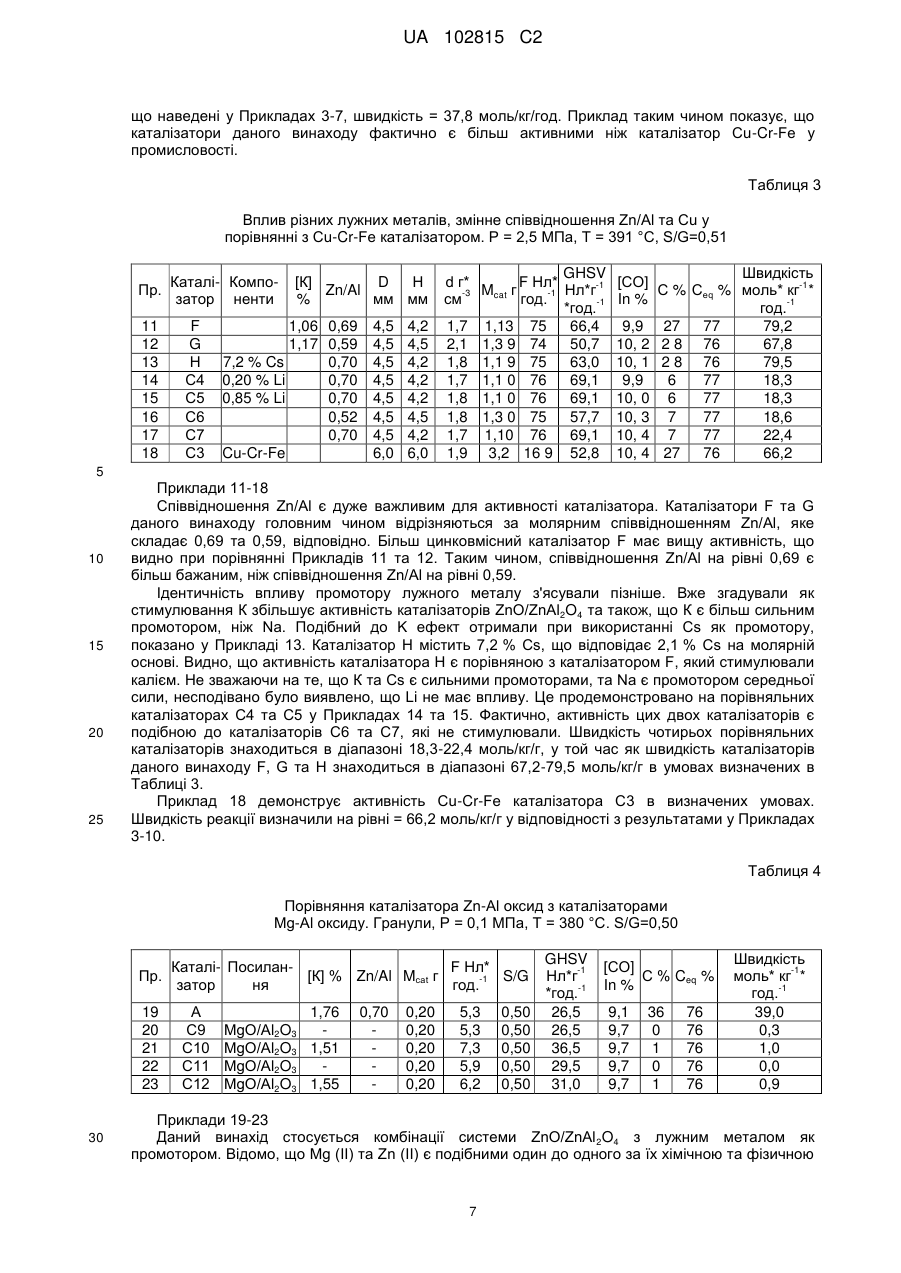
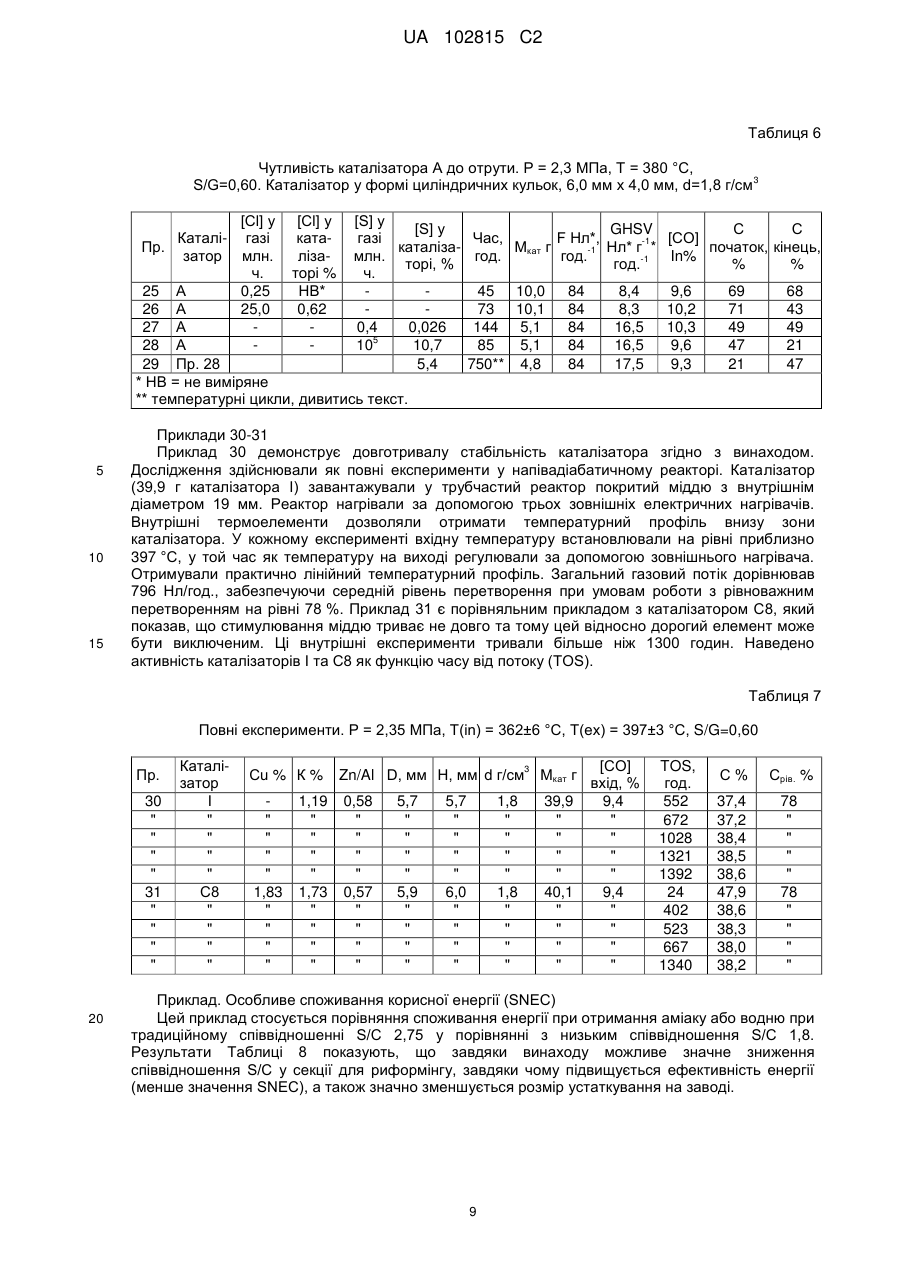
Текст
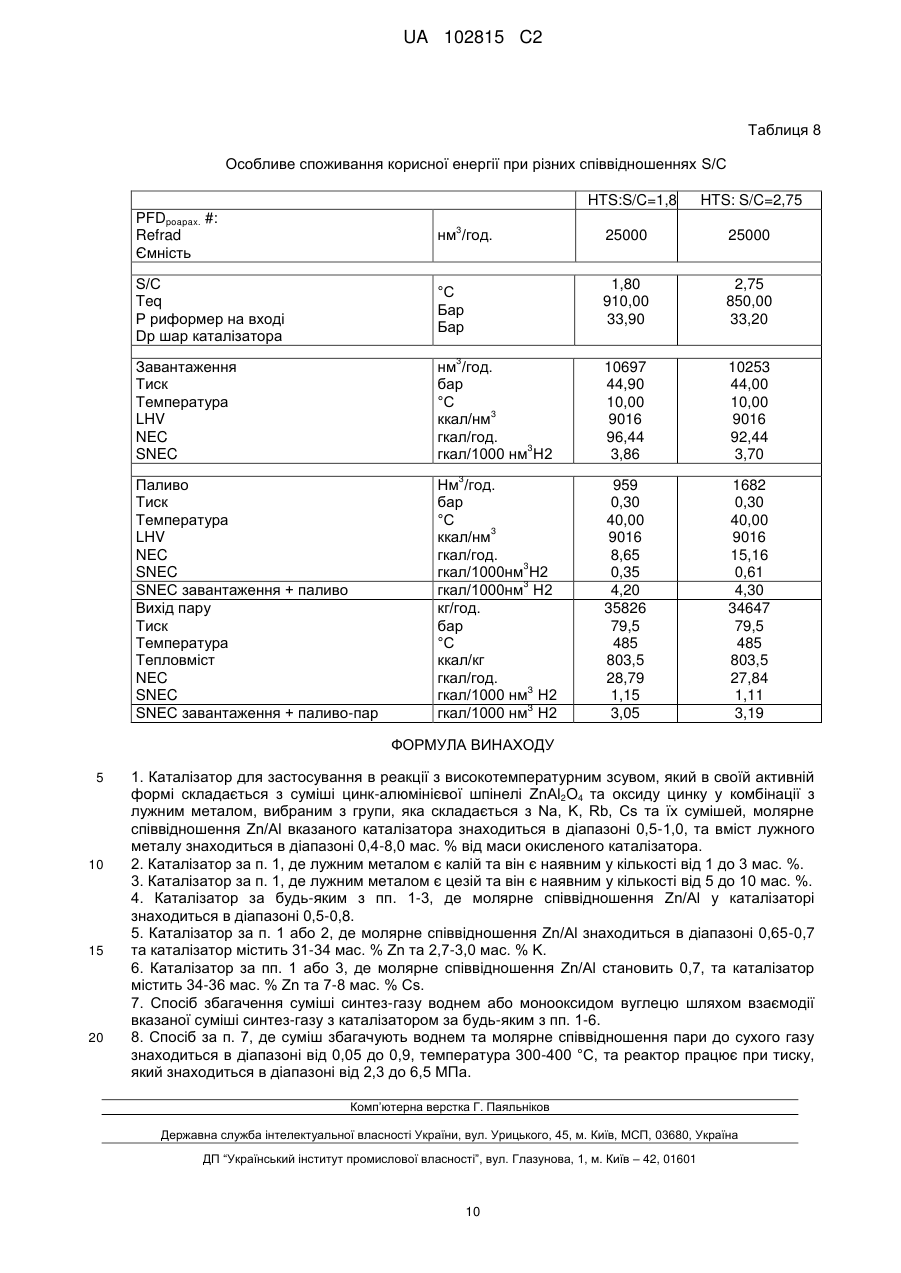
Реферат: Каталізатор для застосування у реакціях з високотемпературним зсувом, який містить у активній формі суміш цинк-алюмінієвої шпінелі та оксиду цинку у комбінації з лужними металами, вибраними з групи, яка складається з Na, K, Rb, Cs та їх сумішей. UA 102815 C2 (12) UA 102815 C2 UA 102815 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід стосується покращеного каталізатора конверсії водяного газу. Зокрема винахід стосується вільного від хрому каталізатора високотемпературного зсуву (HTS) та способу його застосування. Отримання водню з природного газу, олії, вугілля, коксу, нафти та вуглецевмісних джерел зазвичай здійснюють за допомогою риформінгу паром, автотермічного риформінгу або газифікації. У будь-якій з цих реакцій одержують пар синтез-газу (син-газ). Синтез-газ містить водень, монооксид вуглецю, діоксид вуглецю та воду як головні компоненти. З метою отримання максимального виходу водню синтез-газ додатково перетворюють за допомогою реакції конверсії водяного пару СО + Н2O=CO2+H2. Для того, щоб ця реакція проходила зі значною швидкістю синтез-газ перетворюють за допомогою каталізатора у реакторі. Реакція конверсії водяного газу є обмежено рівноважною, екзотермічною реакцією. Вихід водню внаслідок цього оптимізують шляхом проведення реакції у двох окремих адіабатичних реакторах з міжстадійним охолодженням. Перший з цих реакторів зазвичай позначають як реактор високотемпературного зсуву (HTS), який містить каталізатор високотемпературного зсуву, та другий позначають як реактор низькотемпературного зсуву (LTS), який містить каталізатор низькотемпературного зсуву. Деякі промислові заводи оснащені тільки реактором високотемпературного зсуву. На деяких заводах отримують монооксид вуглецю. Суміш синтез-газу може бути збагачена монооксидом вуглецю за допомогою реакції конверсії водяного пару, у цьому випадку її деколи називають зворотною реакцією конверсії водяного пару. Отриману суміш синтез-газу будуть піддавати зсуву з метою або збагачення воднем, або монооксидом вуглецю, в залежності від температури та складу газу. У реакціях низькотемпературного зсуву Cu/Zn/Al каталізатори зазвичай застосовують з температурою входу у LTS-реактор приблизно 200 °C або 20 °C вище температури конденсації газу. Температура виходу з LTS-реактору знаходиться в діапазоні 220 °C-250 °C. В операціях високотемпературного зсуву промислова практика базується на застосуванні каталізатора високотемпературного зсуву, який містить залізо (Fe), хром (Сr) та мідь (Сu), головним чином у формі оксидів. Такий каталізатор діє у температурному діапазоні 300 °C500 °C з нижньою границею, відповідною температурі входу у HTS-реактор, та верхньою границею, відповідною температурі виходу. Зазвичай діючий тиск знаходиться в діапазоні 2,36,5 МПа. Хоча цю каталітичну систему використовували протягом десятиріч, вона має декілька важливих недоліків. Одним з недоліків є наявність хрому у каталізаторі, що становить ризик для навколишнього середовища та здоров'я. Особливо внаслідок того, що оксид хрому (VI), СrО 3, та супровідні сполуки хрому у окисленому стані VI легко утворюються шляхом окислення каталізатора. Усі маніпулювання з каталізатором протягом виготовлення, транспортування, завантаження та розвантаження становлять потенційний ризик. Іншим недоліком є потреба у певному надлишку водяного пару у порівнянні з монооксидом вуглецю для попередження надлишкового відновлення каталізатора. Таким чином, якщо молярне співвідношення пару до вуглецю (S/C співвідношення) у синтезованому газі є надто низьким на вході у реактор високотемпературного зсуву, або еквівалентним, якщо молярне співвідношення пару до сухого газу (S/G співвідношення) у самому реакторі високотемпературного зсуву, або еквівалентним, якщо молярне співвідношення кисню до вуглецю (O/С співвідношення) є надто низьким, буде стимулюватись утворення карбідів заліза та/або заліза у HTS-каталізаторі. Таке надмірне відновлення викликає значну втрату механічної сили каталізатора, також як і надлишкове утворення метану, що супроводжується зменшенням утворення водню. Певний надлишок потрібного водяного пару вимірюють у спеціальних операційних умовах та складі газу. Надлишок води є додатковою затратою промислових заводів з огляду на те, що енергія втрачається на її випаровування та нагрівання. Іншими словами, шляхом використання низького співвідношення S/C у блоках всередині реактору-HTS, зокрема блоках перетворення пару, та тому також з низьким співвідношенням S/C на вході у реакторHTS, отримують значне збереження енергії. Низьке співвідношення S/C на вході у HTS-реактор виражається у низькому співвідношенні O/С та S/G. Ще одним недоліком є чутливість до отрути. Відомо, що сполуки елементів таких як хлор, сірка, лужні метали, кремній та інші мають негативний вплив на активність та селективність HTS-каталізатора на основі заліза. Попередні спроби розроблення HTS каталізатора вільного від хрому базувались на каталізаторах на основі заліза, наприклад, що активуються алюмінієм та церієм [Q. Liu, W. Ma, R. He and Z. Мu, Catalysis Today 2005, 52-56] або алюмінієм та міддю [S. Natesakhawat, X. Wang, L. Zhang and U. S. Ozkan, J. Моi. Catal. A: Chemical 2006, 82-94]. Вважають, що такі каталізатори все ще будуть мати вищезгадані недоліки. 1 UA 102815 C2 5 10 15 20 25 30 35 40 45 50 55 Бажано було б мати HTS-каталізатор, який не буде мати вищезгаданих недоліків, завдяки тому, що він буде вільний від небезпечних елементів, зокрема, хрому, здатний до маніпулювання при низькому співвідношенні пару до вуглецю у HTS-реакторі, а також є більш толерантними до присутності отрути. Заявка на патент JP No. 2004-321924 (JP 2004321924 А) описує каталізатор мідь-лужний метал для реакції конверсії водяного пару при наявності цинк-алюмінієвих оксидів. Мідь є активним каталізатором, у той час як цинк-алюмінієві оксиди є тільки основою. Каталізатор тестували при 400 °C та атмосферному тиску, який відповідає умовам у автоматичній промисловості та виходить за рамки рівнів промислового виробництва HTS, 2,3-6,5 МПа. Мідь є головною частиною системи каталізатора та потрібний вміст міді становить 2-20 %. З огляду на те, що мідь не найбільш дорогим компонентом каталізатора, його отримання становить значну частину витрат на отримання каталізатора. Задачею даного винаходу є забезпечення HTS-каталізатором, вільним від хрому, таким чином він є більш безпечним до навколишнього середовища та використання, ніж існуючі Cu/Cr/Fe каталізатори. Іншою задачею даного винаходу є забезпечення HTS-каталізатором, який є активним при низькому співвідношенні О/С у газі у HTS-реакторі, еквівалентно при низькому співвідношенні S/C, або еквівалентно при низькому співвідношенні S/G (пар-до-газу молярне співвідношення) на вході у HTS-реактор, що не призведе до надлишкового утворення метану та не призведе до утворення надмірного перепаду тиску у реакторі. Іншою задачею даного винаходу є забезпечення HTS-каталізатором, який має високу термічну стабільність, наприклад, активність якого підтримується протягом довгого періоду часу. Іншою задачею даного винаходу є забезпечення HTS-каталізатором, який має високу толерантність до забруднення у газовій фазі, яка містить сірку та хлор. Іншою задачею даного винаходу є забезпечення більш дешевим каталізатором, ніж наявні у галузі каталізатори. Даний винахід стосується вказаних та інших об'єктів. Відповідно, перш за все, даний винахід стосується каталізатора для застосування у реакція з високим температурним зсувом, який існує у своїй активній формі як суміш цинк-алюмінієвої шпінелі та оксиду цинку у комбінації з лужним металом, вибраним з групи, яка складається з Na, К, Rb, Cs та їх сумішей, вказаний каталізатор має молярне співвідношення Zn/Al у діапазоні 0,51,0, та вміст лужного металу у діапазоні 0,4-8,0 мас. % від маси окисленого каталізатора. Використаний у даному документі термін "у своїй активній формі" стосується фаз каталізатора протягом реакції. Таким чином, суміш одного молю ZnO та одного молю Аl 2О3 буде щонайменше частково перетворюватись у ZnAl2O4 протягом реакції. Каталізатор, який складається з цинку у формі оксиду цинку, алюмінію у формі оксиду алюмінію та сполук лужного металу є таким чином активним згідно з винаходом, тому що оксид цинку та оксид алюмінію будуть взаємодіяти з утворенням цинк-алюмінієвої шпінелі протягом реакції. Використаний у даному документі термін "від маси окисленого каталізатора" означає певну кількість компонента від ваги каталізатора у його окисленій формі. Наприклад, коли зазначено, що каталізатор містить 1,75 мас. % калію, це означає 1,75 г калію на 100 г окисленого каталізатора. Каталізатори даного винаходу дозволяють композиції суміші синтез-газу досягти рівноважного стану. Вони характеризуються тим, що вони входять до складу суміші оксиду цинку та цинк-алюмінієвої шпінелі у комбінації з промотором лужного металу. Вже давно відомо, що ZnO самостійно має низьку активність у реакції конверсії водяного пару. Сполуки лужного металу на основі, наприклад, лужний метал на основі окисі алюмінію, також проявляють низьку активність у реакції конверсії водяного пару. Також за допомогою винаходу отримали неочікуваний результат при такій комбінації, завдяки тому, що активність підтримується на високому рівні протягом довгого часу, без потреби міді у композиції. Цинк-алюмінієва шпінель, ZnAl2O4, утворюється за допомогою реакції ZnO + АІ 2О3=ZnAl2O4. Цинкову шпінель розглядають як каталізатор для зворотної реакції конверсії водяного пару. Однак, каталітична активність, як ZnAl2O4 та К2СО3/АІ2О3 є значно нижчою, ніж каталізатора Cu-Fe-Cr, який є прийнятним у галузі як каталізатор для реакції високотемпературної конверсії водяного пару. Винахідники також несподівано з'ясували, що сполуки лужних металів, окрім літію, коли знаходяться на основі ZnAl2O4 у комбінації з ZnO при деяких умовах проявляють більшу HTS активність, ніж каталізатор Cu-Cr-Fe. Це є прямою протилежністю каталізаторам, таким як МgО/МgАl2O4, стимульований калієм, який майже не проявляє активності у реакції конверсії 2 UA 102815 C2 5 10 15 20 25 30 35 40 45 50 55 60 водяного газу. Більш того, несподіваним є те, що К та Cs є значно сильнішими промоторами, ніж Na та також, що Li майже не має стимулюючого впливу. Винахідники з'ясували, що при високих температурах та тиску звичайних для роботи у HTSреакторі, наявність міді є незначною, та що активність каталізаторів вільних від міді, є дуже схожою, зокрема при довготривалих операціях, таких як 500 годин або довше. Це є дуже вигідним, тому що HTS-каталізатори повинні бути здатними для застосування у придатних умовах (без значної втрати активності) протягом років. З огляду на те, що мідь є дорогою сировиною у порівнянні із цинком та алюмінієм, то невикористання міді робить вироблення каталізаторів більш дешевим. Причинами того, що мідь не сприяє активності, є швидка агломерація частинок міді при високих температурах у HTS процесах (300-500 °C) та висока чутливість Сu до отрут, таких як сірка та хлор. Відповідно, відсутність міді у каталізаторах винаходу призводить до того, що каталізатори є толерантними до цих отрут та є активними у реакції HTS протягом довгого часу. Більш детально з'ясували, що каталізатор після поглинання сірки протягом довгого часу, наприклад, після 500 годин реагування або більше (безперервно, TOS), може щонайменше відновлювати первинну активність каталізатора вільного від сірки. Каталізатори даного винаходу не містять хрому, заліза та міді. Вони містять тільки відносно небезпечні сполуки, зокрема оксид цинку, оксид алюмінію, цинк-алюмінієву шпінель та сполуки лужних металів, бажано у формі карбонатів лужного металу. Каталізатори даного винаходу, таким чином, є більш безпечними для використання та зовнішнього середовища, у порівнянні з наявними у промисловості HTS каталізаторами. Каталізатори даного винаходу є високо стабільними, наприклад, вони є активними протягом довгого часу реагування. Більш того, вони можуть діяти при низькому співвідношенні S/C та, таким чином, низькому співвідношенні S/G на вході у реакторі HTS без утворення надлишкової кількості метану та інших гідрокарбонатів, та це дозволяє композиції суміші синтез-газу досягнути рівноважного стану. У загальному варіанті здійснення винаходу каталізатор у його активній формі складається з елементів цинку, алюмінію та щонайменше одного лужного металу, вибраного з Na, К, Rb, Cs та сумішей вказаних елементів у формі оксидів, та/або карбонатів та/або бікарбонатів у різних ступенях гідратації, композицію певного каталізатора визначають за молярним співвідношенням цинку та алюмінію (Zn/Al), яке становить 0,5-1,0 та утворює суміш цинк-алюмінієвої шпінелі та оксиду цинку, та промотор лужного металу знаходиться у кількості 0,4-8,0 % від ваги каталізатора у його окисленій формі. Молярне співвідношення Zn/Al бажано знаходиться у діапазоні 0,5-0,8, більш бажано у діапазоні 0,60-0,70. Кількість Аl бажано становить 20 мас. % - 30 мас. % від ваги окисленого каталізатора, наприклад 21, 22, 23, 24, 25 ваг. %. Кількість Zn бажано становить 30 мас. % - 40 мас. % від ваги окисленого каталізатора, наприклад 32, 34, 35, 36, 38 мас. %. Кількість промотору лужного металу становить, наприклад, 0,5, 0,6, 0,8, 0,9, 1,3, 1,5, 1,7, 1,8, 2,0, 2,5, 2,7, 3,0, 3,2, 3,5, 3,7, 4,0, 5,0, 6,0, 7,2, 7,5 мас. %. Бажано промотором лужного металу є калій та його кількість становить 1-3 мас. % від ваги окисленого каталізатора. У ще одному варіанті здійснення лужним металом є цезій у кількості 5 мас. % - 10 мас. %. З'ясували, що при таких концентраціях калію або цезію у каталізаторі отримують надзвичайно високу активність каталізатора, що виражається у швидкості реакції. Швидкість реакції визначають як кількість монооксиду вуглецю, який споживається у реакції за одиницю часу поділену на масу каталізатора. Зокрема, бажаним каталізатором є каталізатор, молярне співвідношення Zn/Al якого становить 0,65-0,70, бажано 0,7, та каталізатор додатково містить 31-34 мас. % Zn, бажано 33 мас. % Zn, та 2,7-3,0 мас. % К, бажано 2,8 мас. % К від ваги окисленого каталізатора. Вміст Аl повністю показано як молярне співвідношення Zn/Al та вміст Zn у каталізаторі. Каталізатор в рамках композиції проявляє несподівано високу активність, що виражається у швидкості реакції. Збільшення або зменшення концентрації калію призводить до зменшення швидкості реакції. У іншому бажаному каталізаторі молярне співвідношення Zn/Al становить приблизно 0,7, та каталізатор додатково містить 34-36 мас. % Zn, бажано 35 або 35,5 мас. % Zn, та 7-8 мас. % Cs, бажано 7,2 мас. % Cs, від ваги окисленого каталізатора. Вміст Аl повністю показано як молярне співвідношення Zn/Al та вміст Zn у каталізаторі. Цей каталізатор також проявляє несподівано високу активність. Каталізатори винаходу використовують у високотемпературній конверсії водяного пару з метою збагачення газу воднем (для збільшення вмісту водню у газі) та також у зворотній конверсії водяного пару з метою збагачення газу монооксидом вуглецю. Відповідно, винахід 3 UA 102815 C2 5 10 15 20 25 30 35 40 45 50 55 60 стосується способу збагачення суміші синтез-газу воднем шляхом взаємодії вказаної суміші синтез-газу з каталізатором винаходу за п. 7. Винахід також стосується способу збагачення суміші синтез-газу монооксидом вуглецю шляхом взаємодії вказаної суміші синтез-газу з каталізатором винаходу за п. 8. Умови процесу є наступними, тиск у HTS-реакторі знаходиться в діапазоні 2,3-6,5 МПа, бажано 2,5-4,5 МПа, у той час як температура синтезу суміші на вході в реактор знаходиться в діапазоні 300 °C-400 °C, бажано 330 °C, та температура виходу становить 420 °C – 520 °C, бажано 450 °C. Молярне співвідношення пару до сухого газу (S/G співвідношення) у HTSреакторі бажано знаходиться в діапазоні 0,05-0,9, більш бажано 0,1-0,9. Співвідношення S/G визначають як молярне співвідношення води до залишків синтез-газу, який потрапив у HTSреактор, наприклад, на сухій основі. Синтез-газ, який входить у HTS-реактор зазвичай містить 550 об. % СО, 5-50 об. % СO2, 20-60 об. % Н2, 15-50 об. % H2O, 0-30 об. % N2; наприклад 9 об. % CO, 7 об. % CO2, 25 об. % Н2, 33 об. % Н2O, 27 об. % N2. У бажаному варіанті здійснення співвідношення S/G суміші синтез-газу становить 0,05-0,9, температуру 300 °C-400 °C та реактор працює при тиску, який знаходиться в діапазоні 2,3-6,5 МПа. Спосіб даного винаходу є стабільним протягом довгого періоду часу, наприклад, протягом більше ніж 500 годин, завдяки високій стабільності каталізатора. Тому, уникають зупинок процесу протягом часу життя каталізатора або щонайменше значно знижають їх. Спосіб є більш толерантним до присутності сірки при обробці синтез-газу. Існує можливість роботи при жорстких навколишніх вимогах, тому що хром не потрібен у каталізаторі, та у той же час не має ризику надмірного утворення метану або вуглеводню, зокрема при пониженому співвідношенні S/C у відділеннях перетворення пару та, таким чином, при низькому співвідношенні О/С синтезгазу у реакторі зсуву. Завдяки роботі при низькому співвідношенні O/С або еквівалентно низькому співвідношенні S/C отримують значні збереження енергії. Це є надзвичайно важливим на аміачних заводах, які зазвичай працюють при високому співвідношенні S/C у відділі риформінгу синтез-газу заводу, наприклад, співвідношенні S/C 2,50 або 2,75. Завдяки винаходу зараз є можливість зменшити співвідношення S/C у секції для риформінгу до 1,8 або навіть нижче, таким чином збільшуючи енергетичну ефективність аміачного заводу, також значно зменшуючи розмір заводського устаткування. Приклади Виготовлення каталізатора. Каталізатори даного винаходу виготовляють багатьма шляхами, включаючи співосадження солей цинку та алюмінію з основою, такою як амоній, гідроксиди лужних металів та карбонати лужних металів та бікарбонати. Придатними солями цинку та алюмінію є нітрати, сульфати, ацетати, галіди та їх суміші. Альтернативно розчин солі цинку (II), такої як нітрат цинку, осаджують алюмінатом лужного металу, як описано у Прикладі 1. Іншим альтернативним способом виготовлення є співосадження солей цинку та алюмінію з органічними амінами. Іншим альтернативним способом виготовлення є співосадження солей цинку та алюмінію шляхом гідролізу сечовини. Каталізатори зазвичай насичують промоторами у виді розчинів сполук відповідних лужних металів. Бажаними сполуками є карбонати лужних металів, бікарбонати, нітрати, карбоксилати та гідроксиди. Виготовлення каталізатора у будь-якому випадку завершується кальцинацією при температурі, яка знаходиться в діапазоні 200-800 °C, бажано знаходиться в діапазоні 450-650 °C. У наступних Прикладах, каталізатори А - І є каталізаторами даного винаходу, у той час як каталізатори С1 - С12 є порівняльними каталізаторами. Усі композиції каталізаторів наведені на Таблиці 1, у той час як на Таблицях 2-7 наведено результати дослідження активності. Приклад 1 Виготовлення каталізатора А. Розчин гексагідрату нітрату цинку одержували розчиненням 208,3 г Zn (NO 3)2*6H2O у 3 деіонізованій воді та доведенням до об'єму 600 см . 254,5 г розчину КАlO2, який містить 3 надлишок КОМ (10,6 % Al, 22,9 % К, концентрація = 1,57 г/см ), розводили деіонізованою водою 3 до загального об'єму 600 см . Два розчини змішували в результаті чого отримували осад. Струшену суспензію нагрівали до 95 °C протягом однієї години, після чого рН встановлювали на рівні 8 шляхом додавання 10 % азотної кислоти. Осад профільтровували, промивали декілька разів гарячою деіонізованою водою та висушували при 100 °C. Висушений проміжний продукт кальцинували при 500 °C протягом 2 годин. Отриманий порошок аналізували за допомогою порошкової рентгеноструктурної кристалографії (XRD), яка показала суміш цинк-алюмінієвої шпінелі (ZnAl2O4) та ZnO. Порошок просочували розчином K2СО3 у воді шляхом просочування по вологоємності та висушували при 100 °C. Аналіз складу здійснювали способом ІСР, який 4 UA 102815 C2 5 10 15 показав, що каталізатор містить 38,6 % Zn, 22,9 % Al та 1,76 % К. Молярне співвідношення Zn/Al становило 0,70. Порошок змішували з графітом (4 % мас./мас.) та гранулювали для отримання 3 циліндричних таблеток, діаметром 6 мм та висотою 4 мм, густина 1,80 г/см . Наприкінці, кульки кальцинували протягом 2 годин при 550 °C. Приклад 2 Виготовлення каталізатора В. Цей каталізатор готували з Zn(NО3)2*6Н2O (297,9 г) та KAlO2/KOH (448 г), як у Прикладі 1, проте у присутності карбонату калію. K2СО3 (59,4 г) розчиняли у розчині KAlO2/KOH перед додаванням розчину нітрату цинку. Отриманий осад обробляли як у Прикладі 1. Наявність іонів карбонату протягом осадження приводить до утворення гідроталькіту, як визначено за допомогою аналізу XRD сухого порошку. Після кальцинування XRD показало суміш ZnAl 2O4 та ZnO. Усі каталізатори досліджували за допомогою способу ICP-MS та композиції каталізаторів по вазі, включаючи порівнювальні каталізатори, наведено у Таблиці 1. Елементи, виявлені у концентрації менше ніж 300 млн. ч. не включені у перелік. Колонки Zn/Al та Мg/Аl, відповідно, стосуються молярного співвідношення вказаних елементів. Таблиця 1 Композиція каталізатора % Li % Na А В С D Е 1,02 F G Н I С1 С2 С3 С4 0,20 С5 0,85 С6 С7 С8 С9 С10 С11 С12 *НВ: не виміряне 20 25 30 %K 1,76 0,88 3,95 2,77 1,06 1,17 1,19 5,34 1,73 1,51 1,55 % Cs % Cu 7,2 1,50 1,83 % Cr % Fe 6,0 63,5 % Mg % Zn 38,6 38,6 36,3 32,7 33,0 35,8 34,4 35,5 32,3 33,3 37,9 35,8 32,8 38,6 32,3 15,0 14,0 18,5 17,8 % Al 22,9 22,9 21,5 20,0 22,8 21,4 24,0 21,0 24,5 24,1 HB* 22,5 21,2 26,2 22,9 23,3 32,3 30,7 29,9 28,3 Zn/Al 0,70 0,70 0,70 0,67 0,60 0,69 0,59 0,70 0,58 0,57 0,70 0,70 0,52 0,70 0,57 Мg/Аl 0,52 0,51 0,69 0,70 Тестування каталізатора Каталізатори даного винаходу разом з порівняльними каталізаторами досліджували у різних реакторах ідеального витиснення при різних умовах. Головним способом є наступний: У більшості випадків каталізатор мав форму циліндричних кульок з діаметром між D=4,5 мм та D=6,0 м. У таких випадках каталізатор у кількості Мсаt (г), завантажували у трубчастий реактор з мідним покриттям зі значенням ID=7 мм, таким чином, щоб кульки були відокремлені один від одного сферою діаметром 5 мм з перепаленим оксидом алюмінію. У деяких випадках каталізатор завантажували як просіяні гранули діаметром 0,15-0,30 мм, у такому випадку внутрішній діаметр реактора становив 4 мм та каталізатор завантажували нерозведеним. Реактор нагрівали зовнішнім нагрівачем до температури реагування, яка у багатьох випадках становила Т = 380 °C або Т = 391 °C, виміряна у газовій фазі безпосередньо по слою каталізатора. Температуру підтримували на постійному рівні ± 3 °C. Реактор герметизували при тиску, який зазвичай становив Р = 2,3 МПа або Р = 2,5 МПа у синтезованому газі. Синтез-газ, який дозували за допомогою регулятора масової швидкості Bruckner, та пар, який дозували за допомогою насосу Knauer, попередньо нагрівали та змішували перед пропусканням через 5 UA 102815 C2 5 10 15 20 25 каталізатор. Загальний потік у багатьох випадках становив F=75 Нл/г або F=84 Нл/г. Годинна об'ємна швидкість газу (GHSV) виражена у швидкості об'єм-маса, F/Mcat розраховували з потоку та завантаженої ваги каталізатора. У більшості випадків об'ємна швидкість знаходилась в діапазоні 16-26 або 50-70 Нл/г/годину. Склад газу був зазвичай наступним: 9,7 об. % CO, 6,5 об. % СO2, 37,1 об. % Н2O, 44,8 об. % H2 та 1,9 об. % Аr, що відповідало молярному співвідношенню пари до сухого газу (S/G) 0,59. Аr використовували як внутрішній стандарт. У деяких випадках співвідношення S/G вибирали в залежності від складу газу близько до 10,2 об. % CO, 6,8 об. % CO2, 33,8 об. % H2O, 47,2 об. % H2 та 2,0 об. % Аr, де S/G=0,51. Концентрацію усіх компонентів регулярно вимірювали як у вхідному, так і в вихідному сухому газі за допомогою газового хроматографа Hewlett Packard, який калібрували по газовій суміші відомого складу. Вагу записували для С, Н та О, та з'ясували, що в усіх випадках вона складала 1,00±0,03. Активність каталізаторів даного винаходу разом з деякими порівняльними каталізаторами наведено у Таблицях 2-7. У всіх випадках активність вимірювали після щонайменше 60 годин при спеціальній температурі, після того як активність стабілізувалась. У Прикладах 3-10 (Таблиця 2) каталізатори піддавали прискореному старінню, коли після перших 24 годин при 380 °C, температуру підвищували до 480 °C та підтримували на такому рівні протягом 17 годин. Потім вимірювання продовжували при 380 °C. Дані щодо розміру каталізатора, навантаження, загального потоку (F), концентрації CO на вході у реактор [CO], виміряний процент перетворення СО (С %), розрахована процентна рівновага перетворення CO (Ceq %) та швидкість у моль/кг/годину наявні у Таблиці 2. Селективність реакції конверсії водяного газу у експерименті дорівнювала 100 %, тому що кількість перетвореного CO врівноважувалась надлишком CO 2 у вхідному газі. Ці приклади демонструють, що каталізатор зі складом, таким як у каталізатора даного винаходу, е надзвичайно активним у реакції високотемпературної конверсії водяного газу. Таблиця 2 Активність каталізаторів винаходу та деяких порівнювальних каталізаторів. Р = 2,3 МПа, Т = 380 °C, S/G=0,59 Пр. 3 4 5 6 7 8 9 10 30 35 40 Каталі[К] % затор А В С D Е С1 С2 С3 1,76 0,88 3,95 2,77 Na 1,02 0,00 5,34 Zn/Al D мм 0,70 0,70 0,70 0,67 0,60 0,57 0,00 6,0 6,0 6,0 5,9 6,0 4,5 ** 6,0 GHSV H d г*, F Нл*, -1 Mсat г -3 -1 Нл*, г мм см год. -1 *год. 4,0 1,8 5,0 84 16,8 4,0 1,8 4,8 84 17,5 4,0 1,9 4,9 84 17,1 3,1 1,5 4,9 84 17,1 4,0 1,8 5,2 84 16,2 3,7 1,8 35,9 99 2,8 ** ** 25,0 99 4,0 6,0 1,9 5,0 84 16,8 [СО] C С % eq In, % % 9,8 9,7 9,7 9,6 9,5 9,4 9,4 9,7 60 52 55 63 40 64 31 52 82 82 82 82 82 78 78 82 Швидкість -1 моль*, кг -1 *год. 44,1 39,4 40,8 46,7 27,4 7,4 5,1 37,8 Приклади 3-10 Каталізатори даного винаходу А, В, С, D та Е всі є активними у реакції конверсії водяного газу в умовах, визначених у Таблиці 2, як показано у Прикладах 3-7. Каталізатори А, В, С та D більш за все відрізняються за вмістом калію. Найбільш активним з цих каталізаторів у визначених умовах є каталізатор D, який містить 2,77 % К. Каталізатори А та В мають менший вміст К, а саме 1,76 % та 0,88 %, відповідно, у той час як каталізатор С має більший вміст K, а саме 3,95 %. Таким чином найбільш бажаний вміст К знаходиться в діапазоні 0,88 % - 3,95 %, бажано знаходиться в діапазоні 1-3 %. Замість калію можна застосовувати натрій, як показано у Прикладі 7. Несподівано виявили, що калій є значно активнішим промотором ніж натрій. Несподіваний ефект комбінування системи ZnO/ZnAl2O4 з К-промотором продемонстровано шляхом порівняння високих швидкостей (39,4-46,7 моль/кг/г) отриманих з використанням каталізаторів даного винаходу у Прикладах 3-6 та порівняльних каталізаторів у Прикладах 8 та 9. Перший, С1, є не стимульованим каталізатором ZnO/ZnAl2O4. Цей каталізатор досліджували при низькому GHSV з метою досягнення значної конверсії. Активність була значно нижчою (швидкість = 7,4 моль/кг/г), ніж у будь-якого з К-промоторних каталізаторів. Також, активність Kпромоторного Аl2O3 каталізатора була дуже низькою, а саме швидкість = 5,1 моль/кг/год. Приклад 10 демонструє активність звичайного каталізатора Cu-Cr-Fe, в умовах подібних до тих, 6 UA 102815 C2 що наведені у Прикладах 3-7, швидкість = 37,8 моль/кг/год. Приклад таким чином показує, що каталізатори даного винаходу фактично є більш активними ніж каталізатор Сu-Cr-Fe у промисловості. Таблиця 3 Вплив різних лужних металів, змінне співвідношення Zn/Al та Сu у порівнянні з Cu-Cr-Fe каталізатором. Р = 2,5 МПа, Т = 391 °C, S/G=0,51 Пр. 11 12 13 14 15 16 17 18 Каталі- Композатор ненти F G Н С4 С5 С6 С7 С3 [К] D Н Zn/Al % мм мм 1,06 0,69 1,17 0,59 7,2 % Cs 0,70 0,20 % Li 0,70 0,85 % Li 0,70 0,52 0,70 Cu-Cr-Fe 4,5 4,5 4,5 4,5 4,5 4,5 4,5 6,0 4,2 4,5 4,2 4,2 4,2 4,5 4,2 6,0 GHSV d г* F Нл* -1 -3 Mcat г -1 Нл*г см год. -1 *год. 1,7 1,13 75 66,4 2,1 1,3 9 74 50,7 1,8 1,1 9 75 63,0 1,7 1,1 0 76 69,1 1,8 1,1 0 76 69,1 1,8 1,3 0 75 57,7 1,7 1,10 76 69,1 1,9 3,2 16 9 52,8 Швидкість [СО] -1 С % Сеq % моль* кг * In % -1 год. 9,9 27 77 79,2 10, 2 2 8 76 67,8 10, 1 2 8 76 79,5 9,9 6 77 18,3 10, 0 6 77 18,3 10, 3 7 77 18,6 10, 4 7 77 22,4 10, 4 27 76 66,2 5 10 15 20 25 Приклади 11-18 Співвідношення Zn/Al є дуже важливим для активності каталізатора. Каталізатори F та G даного винаходу головним чином відрізняються за молярним співвідношенням Zn/Al, яке складає 0,69 та 0,59, відповідно. Більш цинковмісний каталізатор F має вищу активність, що видно при порівнянні Прикладів 11 та 12. Таким чином, співвідношення Zn/Al на рівні 0,69 є більш бажаним, ніж співвідношення Zn/Al на рівні 0,59. Ідентичність впливу промотору лужного металу з'ясували пізніше. Вже згадували як стимулювання К збільшує активність каталізаторів ZnO/ZnAl2O4 та також, що К є більш сильним промотором, ніж Na. Подібний до K ефект отримали при використанні Cs як промотору, показано у Прикладі 13. Каталізатор Н містить 7,2 % Cs, що відповідає 2,1 % Cs на молярній основі. Видно, що активність каталізатора Н є порівняною з каталізатором F, який стимулювали калієм. Не зважаючи на те, що К та Cs є сильними промоторами, та Na є промотором середньої сили, несподівано було виявлено, що Li не має впливу. Це продемонстровано на порівняльних каталізаторах С4 та С5 у Прикладах 14 та 15. Фактично, активність цих двох каталізаторів є подібною до каталізаторів С6 та С7, які не стимулювали. Швидкість чотирьох порівняльних каталізаторів знаходиться в діапазоні 18,3-22,4 моль/кг/г, у той час як швидкість каталізаторів даного винаходу F, G та Н знаходиться в діапазоні 67,2-79,5 моль/кг/г в умовах визначених в Таблиці 3. Приклад 18 демонструє активність Cu-Cr-Fe каталізатора С3 в визначених умовах. Швидкість реакції визначили на рівні = 66,2 моль/кг/г у відповідності з результатами у Прикладах 3-10. Таблиця 4 Порівняння каталізатора Zn-Al оксид з каталізаторами Мg-Аl оксиду. Гранули, Р = 0,1 МПа, Т = 380 °C. S/G=0,50 Пр. 19 20 21 22 23 30 Каталі- ПосиланF Нл* [К] % Zn/Al Mсat г S/G -1 затор ня год. А С9 С10 С11 С12 1,76 МgО/Аl2O3 МgО/Аl2O3 1,51 МgО/Аl2O3 МgО/Аl2O3 1,55 0,70 0,20 0,20 0,20 0,20 0,20 5,3 5,3 7,3 5,9 6,2 0,50 0,50 0,50 0,50 0,50 GHSV -1 Нл*г -1 *год. 26,5 26,5 36,5 29,5 31,0 [СО] С % Ceq % In % 9,1 9,7 9,7 9,7 9,7 36 0 1 0 1 76 76 76 76 76 Швидкість -1 моль* кг * -1 год. 39,0 0,3 1,0 0,0 0,9 Приклади 19-23 Даний винахід стосується комбінації системи ZnO/ZnAl 2O4 з лужним металом як промотором. Відомо, що Мg (II) та Zn (II) є подібними один до одного за їх хімічною та фізичною 7 UA 102815 C2 5 10 15 поведінкою: в обох випадках з основних оксидів, які здатні утворювати стабільну шпінель з оксидом алюмінію. Також несподівано виявили, що майже не мають активності як у стимульованих, так і у нестимульованих каталізаторах МgО/МgАl2O4. Ці каталізатори досліджували при низькому тиску, та, таким чином, здійснювали подібний приклад з каталізатором А даного винаходу. З Таблиці 4 видно, що у той час як каталізатор А проявляє значну активність, виражену у швидкості = 39,0 моль/кг/г, швидкість реакції викликана каталізаторами С9, С10, С11 та С12, на основі магнію, з різним співвідношенням Мg/Аl та різним вмістом К, становила 1,0 моль/кг/год. або менше. Приклад 24 Досліджування каталізатора G даного винаходу при високому тиску та низькому співвідношенні S/G. Цей приклад демонструє, що активність реакції конверсії водяного газу досягається при певному наборі робочих параметрів, та селективність реакції конверсії водяного газу залишається високою. Аналіз вихідного газу показав 660 млн. ч. СН 3ОН та 35 млн. ч. СН4 у газовій фазі після контакту з каталізатором. Швидкість є низькою у порівнянні з попередніми прикладами, внаслідок низького вмісту пару у газі. Таблиця 5 Каталізатор G, досліджений при високій температурі та низькому співвідношенні S/G. Р = 6,5 МПа, Т = 394 °C, S/G=0,14 Пр. 24 20 25 30 35 40 45 50 Каталі-3 D мм H мм d г*см Mсat г затор G 4,5 4,5 2,1 50,0 F Нл* -1 год. 684 GHSV -1 Нл*г * 1 год.13,7 [СО] In % 13,0 С% С 28 еq % 36 Швидкість -1 Моль* кг -1 *год. 22,2 Приклади 25-29 Ці приклади демонструють поведінку звичайного каталізатора даного винаходу при обробці хлором та сіркою. Хлор та сірка є типовими отрутами для каталізаторів, та більшість каталізаторів стають менш активними при взаємодії зі сполуками даних елементів. Приклад 25 здійснювали як описано у прикладі 3 з тією різницею, що до живильної води додавали хлорид амонію, з метою створення концентрації хлору 0,25 млн. ч. у газовій фазі. Обробка газом, який містив хлор, тривала протягом 45 годин, протягом яких перетворення (С) несуттєво зменшувалось, від 69 % до 68 %. Приклад 26 здійснювали таким же чином, проте з концентрацією хлору у газі 25 млн. ч. Сl. У цьому випадку обробка тривала протягом 73 годин, протягом цього часу перетворення значно зменшувалось, а саме від 71 % до 43 %. Після дослідження каталізатор аналізували та виявили, що вміст хлору становить в середньому 0,62 % по внутрішній поверхні каталізатора. У теперішній промисловості газ рідко містить хлор більше ніж на рівні млн. ч., або не містить зовсім. Можна зробити висновок, що каталізатор має велику ємність до хлору та є нечутливим до цієї отрути. Дані наведено у Таблиці 6. Приклад 27 демонструє толерантність каталізатора А до низьких концентрацій сірки. H 2S вироблявся у низьких концентраціях шляхом почергового завантаження кульок каталізатора та кульок ZnS, таким чином виробляючи H2S завдяки реакції ZnS+H2O (д) = ZnO+H2S (д). При рівновазі ця реакція продукує 0,4 млн.ч. H2S, ця концентрація представляє верхню границю дійсної концентрації H2S. Експеримент здійснювали шляхом почергового завантаження кульок каталізатора та кульок ZnS. Дослідження тривало 144 години, протягом яких перетворення СО (С) було постійним на рівні 49 %. Після дослідження каталізатор аналізували та виявили вміст сірки на рівні 260 млн.ч. У прикладі 28 завантажували свіжий зразок каталізатора А. Рівень перетворення становив 47 %. Після цього каталізатор обробляли 10 % H2S у водні протягом 4 годин, після чого каталізатор виймали та визначили вміст сірки на рівні 10,7 %. Каталізатор знов завантажували у реактор та продовжували дослідження. Рівень перетворення становив 21 %, таким чином це менше ніж половина від нормального рівня перетворення. Після 30 годин при 380 °C рівень перетворення збільшився до 22,5 %. Після цього температуру підвищували до 480 °C протягом 30 годин та знов знижували до 380 °C протягом ще 30 годин. Такий цикл температур повторювали декілька разів, та кожен раз спостерігали підвищення рівня перетворення. Після 12 циклів (750 годин) рівень перетворення досягнув нормального рівня 47 %. Каталізатор виймали та аналізували на вміст сірки. Несподівано з'ясували, що каталізатор містив 5,4 % S, що означало, що цей частково насичений сіркою каталізатор мав однакову активність з вихідним, вільним від сірки каталізатором. Дані наведено у Таблиці 6. 8 UA 102815 C2 Таблиця 6 Чутливість каталізатора А до отрути. Р = 2,3 МПа, Т = 380 °C, 3 S/G=0,60. Каталізатор у формі циліндричних кульок, 6,0 мм х 4,0 мм, d=1,8 г/см [Сl] у [Сl] у [S] у [S] у Каталі- газі катагазі Пр. каталізазатор млн. лізамлн. торі, % ч. торі % ч. 25 А 0,25 НВ* 26 А 25,0 0,62 27 А 0,4 0,026 5 28 А 10 10,7 29 Пр. 28 5,4 * НВ = не виміряне ** температурні цикли, дивитись текст. 5 10 15 GHSV С С Час, F Нл*, [СО] -1 Мкат г початок, кінець, -1 Нл* г * год. год. In% -1 год. % % 45 10,0 73 10,1 144 5,1 85 5,1 750** 4,8 84 84 84 84 84 8,4 8,3 16,5 16,5 17,5 9,6 10,2 10,3 9,6 9,3 69 71 49 47 21 68 43 49 21 47 Приклади 30-31 Приклад 30 демонструє довготривалу стабільність каталізатора згідно з винаходом. Дослідження здійснювали як повні експерименти у напівадіабатичному реакторі. Каталізатор (39,9 г каталізатора І) завантажували у трубчастий реактор покритий міддю з внутрішнім діаметром 19 мм. Реактор нагрівали за допомогою трьох зовнішніх електричних нагрівачів. Внутрішні термоелементи дозволяли отримати температурний профіль внизу зони каталізатора. У кожному експерименті вхідну температуру встановлювали на рівні приблизно 397 °C, у той час як температуру на виході регулювали за допомогою зовнішнього нагрівача. Отримували практично лінійний температурний профіль. Загальний газовий потік дорівнював 796 Нл/год., забезпечуючи середній рівень перетворення при умовам роботи з рівноважним перетворенням на рівні 78 %. Приклад 31 є порівняльним прикладом з каталізатором С8, який показав, що стимулювання міддю триває не довго та тому цей відносно дорогий елемент може бути виключеним. Ці внутрішні експерименти тривали більше ніж 1300 годин. Наведено активність каталізаторів І та С8 як функцію часу від потоку (TOS). Таблиця 7 Повні експерименти. Р = 2,35 МПа, Т(іn) = 362±6 °C, Т(ех) = 397±3 °C, S/G=0,60 Пр. 30 " " " " 31 " " " " 20 Каталізатор І " " " " С8 " " " " 3 Сu % К % Zn/Al D, мм H, мм d г/см Мкат г " " " " 1,83 " " " " 0,58 " " " " 0,57 " " " " 39,9 " " " " 40,1 " " " " 1,19 " " " " 1,73 " " " " 5,7 " " " " 5,9 " " " " 5,7 " " " " 6,0 " " " " 1,8 " " " " 1,8 " " " " [СО] вхід, % 9,4 " " " " 9,4 " " " " TOS, год. 552 672 1028 1321 1392 24 402 523 667 1340 С% Срів. % 37,4 37,2 38,4 38,5 38,6 47,9 38,6 38,3 38,0 38,2 78 " " " " 78 " " " " Приклад. Особливе споживання корисної енергії (SNEC) Цей приклад стосується порівняння споживання енергії при отримання аміаку або водню при традиційному співвідношенні S/C 2,75 у порівнянні з низьким співвідношення S/C 1,8. Результати Таблиці 8 показують, що завдяки винаходу можливе значне зниження співвідношення S/С у секції для риформінгу, завдяки чому підвищується ефективність енергії (менше значення SNEC), а також значно зменшується розмір устаткування на заводі. 9 UA 102815 C2 Таблиця 8 Особливе споживання корисної енергії при різних співвідношеннях S/С HTS:S/C=1,8 HTS: S/C=2,75 PFDpoapax. #: Refrad Ємність нм /год. 25000 25000 S/С Teq Р риформер на вході Dp шар каталізатора °С Бар Бар 1,80 910,00 33,90 2,75 850,00 33,20 Завантаження Тиск Температура LHV NEC SNEC нм /год. бар °С 3 ккал/нм гкал/год. 3 гкал/1000 нм Н2 3 10697 44,90 10,00 9016 96,44 3,86 10253 44,00 10,00 9016 92,44 3,70 Паливо Тиск Температура LHV NEC SNEC SNEC завантаження + паливо Вихід пару Тиск Температура Тепловміст NEC SNEC SNEC завантаження + паливо-пар Нм /год. бар °С 3 ккал/нм гкал/год. 3 гкал/1000нм Н2 3 гкал/1000нм Н2 кг/год. бар °С ккал/кг гкал/год. З гкал/1000 нм Н2 З гкал/1000 нм Н2 3 959 0,30 40,00 9016 8,65 0,35 4,20 35826 79,5 485 803,5 28,79 1,15 3,05 1682 0,30 40,00 9016 15,16 0,61 4,30 34647 79,5 485 803,5 27,84 1,11 3,19 3 ФОРМУЛА ВИНАХОДУ 5 10 15 20 1. Каталізатор для застосування в реакції з високотемпературним зсувом, який в своїй активній формі складається з суміші цинк-алюмінієвої шпінелі ZnAl2O4 та оксиду цинку у комбінації з лужним металом, вибраним з групи, яка складається з Na, K, Rb, Cs та їх сумішей, молярне співвідношення Zn/Al вказаного каталізатора знаходиться в діапазоні 0,5-1,0, та вміст лужного металу знаходиться в діапазоні 0,4-8,0 мас. % від маси окисленого каталізатора. 2. Каталізатор за п. 1, де лужним металом є калій та він є наявним у кількості від 1 до 3 мас. %. 3. Каталізатор за п. 1, де лужним металом є цезій та він є наявним у кількості від 5 до 10 мас. %. 4. Каталізатор за будь-яким з пп. 1-3, де молярне співвідношення Zn/Al у каталізаторі знаходиться в діапазоні 0,5-0,8. 5. Каталізатор за п. 1 або 2, де молярне співвідношення Zn/Al знаходиться в діапазоні 0,65-0,7 та каталізатор містить 31-34 мас. % Zn та 2,7-3,0 мас. % K. 6. Каталізатор за пп. 1 або 3, де молярне співвідношення Zn/Al становить 0,7, та каталізатор містить 34-36 мас. % Zn та 7-8 мас. % Cs. 7. Спосіб збагачення суміші синтез-газу воднем або монооксидом вуглецю шляхом взаємодії вказаної суміші синтез-газу з каталізатором за будь-яким з пп. 1-6. 8. Спосіб за п. 7, де суміш збагачують воднем та молярне співвідношення пари до сухого газу знаходиться в діапазоні від 0,05 до 0,9, температура 300-400 °С, та реактор працює при тиску, який знаходиться в діапазоні від 2,3 до 6,5 МПа. Комп’ютерна верстка Г. Паяльніков Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 10
ДивитисяДодаткова інформація
Назва патенту англійськоюCatalyst for use in high temperature shift reactions and method of enrichment of mixture of synthetic gas by hydrogen and carbon monoxide
Автори англійськоюSchiodt Niels Christian
Назва патенту російськоюКатализатор для применения в реакциях с высокотемпературным сдвигом и способ обогащения смеси синтез-газа водородом или монооксидом углерода
Автори російськоюСкьйодт Нильс Кристиан
МПК / Мітки
МПК: B01J 23/06, B01J 23/04, B01J 21/00, C01B 3/16
Мітки: синтез-газу, зсувом, реакції, вуглецю, каталізатор, високотемпературним, застосування, спосіб, монооксидом, збагачення, суміші, воднем
Код посилання
<a href="https://ua.patents.su/12-102815-katalizator-dlya-zastosuvannya-v-reakci-z-visokotemperaturnim-zsuvom-ta-sposib-zbagachennya-sumishi-sintez-gazu-vodnem-abo-monooksidom-vuglecyu.html" target="_blank" rel="follow" title="База патентів України">Каталізатор для застосування в реакції з високотемпературним зсувом та спосіб збагачення суміші синтез-газу воднем або монооксидом вуглецю</a>
Попередній патент: Система для ущільнення верхньої частини затравки у формі для безперервної розливки при формуванні великогабаритних попередніх заготовок
Наступний патент: Спосіб синтезу кристалічної форми v агомелатину
Випадковий патент: Спосіб вимірювання точки роси і пристрій для його здійснення