Спосіб комплектування пристрою для введення в організм лікарського засобу, зокрема, у вигляді аерозолю та пристрій для введення в організм лікарського засобу, зокрема, у вигляді аерозолю
Номер патенту: 95928
Опубліковано: 26.09.2011
Автори: Гезер Йоханнес, Хаусманн Маттіас, Файєртаг Хрістіан, Бок Георг, Кьольбель Ханс-Юрген, Айхер Йоахим
Формула / Реферат
1. Спосіб комплектування пристрою (1) для введення в організм лікарського засобу, зокрема, у вигляді аерозолю (А), з покращеною точністю дозування, в якому
використовують щонайменше один перший і один другий компоненти, які входять в щільне сполучення один з одним або притискаються один до одного,
причому перший компонент виробляється партіями,
й щонайменше одна істотна характеристика першого компонента в кожній партії визначається тільки за допомогою випадкової вибірки,
щонайменше одна вирішальна істотна характеристика для всіх перших компонентів відповідної партії визначається на основі щонайменше однієї істотної характеристики,
другий компонент розділений на групи, які розрізняються щонайменше на одну істотну характеристику других компонентів,
залежно від щонайменше однієї вирішальної істотної характеристики вибрана група, сумісна з відповідною вирішальною істотною характеристикою і, таким чином, вибрана відповідна партія,
перший компонент партії скомбінований з другим компонентом групи, яка сумісна з цією партією, із забезпеченням оптимального ущільнення між цими двома компонентами для поліпшення точності дозування, причому ці два компоненти переміщають один відносно одного для здійснення процесу подачі,
та причому всі перші компоненти є ущільненнями необхідної форми, а кожний з других компонентів має заглиблення, що служить для поміщення першого компонента.
2. Спосіб за п. 1, який відрізняється тим, що перші компоненти виготовлені литтям підтиском.
3. Спосіб за п. 1 або 2, який відрізняється тим, що перші компоненти, що являють собою ущільнення (5), переважно мають переважно кільцеподібну форму, зокрема, форму ущільнюючого кільця.
4. Спосіб за одним з попередніх пунктів, який відрізняється тим, що як істотна характеристика або характеристики виступають або визначені вимірювання, які стосуються інструменту, об'єм і (або) стисливість перших компонентів.
5. Спосіб за одним з попередніх пунктів, який відрізняється тим, що як істотні характеристики зареєстровано або визначено середнє значення і стандартне відхилення.
6. Спосіб за одним з попередніх пунктів, який відрізняється тим, що кожний з других компонентів має заглиблення (6) у вигляді заплечика або виїмки, що служить для поміщення першого компонента та переважно утворює направляючу трубку для поршня (4).
7. Спосіб за п. 6, який відрізняється тим, що використовують як істотну характеристику для розділення на групи вимірювання, що стосується інструменту, зокрема глибину і (або) ширину заглиблення.
8. Спосіб за одним з попередніх пунктів, який відрізняється тим, що використовують як істотні характеристики для розділення на групи середнє значення і стандартне відхилення.
9. Спосіб за одним з попередніх пунктів, який відрізняється тим, що другі компоненти виготовлені з різними суттєвими характеристиками, і, зокрема, різниця між суттєвими характеристиками різних груп більше, ніж виробничий допуск.
10. Спосіб за одним з попередніх пунктів, який відрізняється тим, що другі компоненти виготовлені партіями, причому істотна характеристика других компонентів в кожній партії визначена тільки за допомогою випадкової вибірки і з цього визначена істотна характеристика для всіх других компонентів відповідної партії, яка використовується для розділення на групи.
11. Спосіб за одним з попередніх пунктів, який відрізняється тим, що використовують пристрій (1), який містить на додаток до перших і других компонентів щонайменше ще один додатковий компонент, зокрема поршень (4), який ущільнюється першим компонентом, і (або) опорне кільце (7) для осьового скріплення першого компонента з другим компонентом.
12. Спосіб за п. 11, який відрізняється тим, що додатковий компонент, зокрема поршень (4), виготовлений партіями, і щонайменше одна істотна характеристика, така як діаметр, визначена тільки за допомогою випадкової вибірки в кожній партії.
13. Спосіб за п. 11 або 12, який відрізняється тим, що визначена(і) щонайменше одна або більше істотна(і) характеристика(и), зокрема такі, що стосуються інструменту вимірювання додаткового компонента або компонентів, зокрема діаметр поршня (4) і (або) осьова ефективна довжина підтримуючого кільця, яка(і) береться(уться) до уваги як додаткова(і) істотна(і) характеристика(и) на додаток до вирішальної істотної характеристики при виборі сумісної групи.
14. Спосіб за одним з попередніх пунктів, який відрізняється тим, що відповідна група вибрана таким чином, що вирішальна істотна характеристика разом з необов'язковою щонайменше однією додатковою істотною характеристикою додаткового компонента і разом з істотною(ними) характеристикою(ами) веде до шуканого значення, зокрема до бажаного рівня заповнення заглиблення ущільненням і (або) прокладкою.
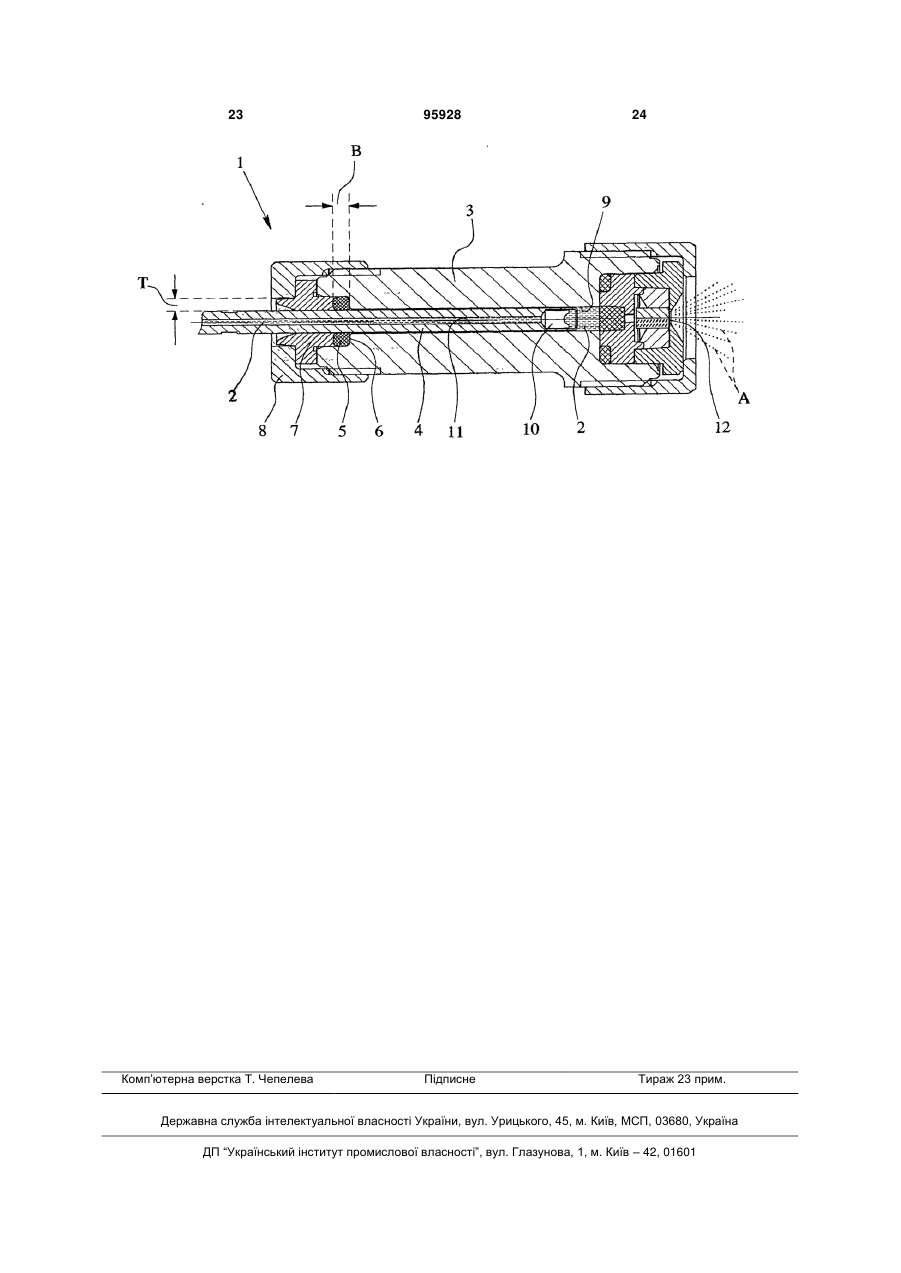
15. Пристрій (1) для введення в організм лікарського засобу, зокрема, у вигляді аерозолю (А), з покращеною точністю дозування, який має направляючу трубку (3), поршень (4), який направляється з можливістю переміщення всередині трубки в подовжньому напрямі, ущільнення (5) певної форми, що служить для ізоляції направляючої трубки (3) і поршня (4), і заглиблення (6), що служить для розміщення ущільнення (5) необхідної форми, який відрізняється тим, що ущільнення (5) певної форми конкретної партії скомбіновано з направляючою трубкою (3) сумісної групи направляючих трубок (3), вибраної з декількох груп направляючих трубок (3), залежно від щонайменше однієї істотної характеристики партії для заповнення заглиблення (6) за допомогою ущільнення (5) певної форми на бажану глибину заповнення і таким чином отримання оптимального ущільнення між ущільненням (5) і направляючою трубкою (3), щоб покращити точність дозування.
16. Пристрій за п. 15, який відрізняється тим, що заглиблення (6) виконано у вигляді виїмки або заплечика і (або) має кільцеподібну форму.
17. Пристрій за п. 15 або 16, який відрізняється тим, що заглиблення (6) сформовано або обмежено за допомогою направляючої трубки (3).
18. Пристрій за одним з пп. 15-17, який відрізняється тим, що має підтримуюче кільце (7) для осьового закріплення ущільнення (5) певної форми в заглибленні (6) і (або) для встановлення меж заглиблення (6).
19. Пристрій за одним з пп. 15-18, який відрізняється тим, що ущільнення (5) певної форми має кільцеподібну конструкцію, зокрема, форму ущільнюючого кільця.
20. Пристрій за одним з пп. 15-19, який відрізняється тим, що ущільнення (5) певної форми втиснуте в заглиблення (6) і (або) еластично деформоване заглибленням (6) і поршнем (4).
21. Пристрій за одним з пп. 15-20, який відрізняється тим, що діаметр поршня (4) складає від 0,25 до 4 мм, переважно від 0,5 до 3 мм, а більш переважно від 0,75 до 2,25 мм.
22. Пристрій за одним з пп. 15-21, який відрізняється тим, що об'єм пристрою (1), який нагнітається за один хід поршня, складає від 1 мкл до 1 мл, переважно від 1 до 500 мкл, більш переважно від 5 до 100 мкл, і найбільш переважно від 5 до 30 мкл.
23. Пристрій за одним з пп. 15-22, який відрізняється тим, що бажаний рівень заповнення рівний в середньому щонайменше 90 %, зокрема щонайменше 59 %, при допуску не більше 5 %, зокрема 4 % і менше.
24. Пристрій за одним з пп. 16-23, який відрізняється тим, що виконаний у вигляді розпилювача, інгалятора, інжектора, генератора тиску або дозуючого насоса і (або) медичного пристрою для аерозольної терапії.
Текст
1. Спосіб комплектування пристрою (1) для введення в організм лікарського засобу, зокрема, у вигляді аерозолю (А), з покращеною точністю дозування, в якому використовують щонайменше один перший і один другий компоненти, які входять в щільне сполучення один з одним або притискаються один до одного, причому перший компонент виробляється партіями, й щонайменше одна істотна характеристика першого компонента в кожній партії визначається тільки за допомогою випадкової вибірки, щонайменше одна вирішальна істотна характеристика для всіх перших компонентів відповідної партії визначається на основі щонайменше однієї істотної характеристики, другий компонент розділений на групи, які розрізняються щонайменше на одну істотну характеристику других компонентів, залежно від щонайменше однієї вирішальної істотної характеристики вибрана група, сумісна з відповідною вирішальною істотною характеристикою і, таким чином, вибрана відповідна партія, перший компонент партії скомбінований з другим компонентом групи, яка сумісна з цією партією, із забезпеченням оптимального ущільнення між цими двома компонентами для поліпшення точності дозування, причому ці два компоненти переміща 2 (19) 1 3 95928 4 компонентів в кожній партії визначена тільки за допомогою випадкової вибірки і з цього визначена істотна характеристика для всіх других компонентів відповідної партії, яка використовується для розділення на групи. 11. Спосіб за одним З попередніх пунктів, який відрізняється тим, що використовують пристрій (1), який містить на додаток до перших і других компонентів щонайменше ще один додатковий компонент, зокрема поршень (4), який ущільнюється першим компонентом, і (або) опорне кільце (7) для осьового скріплення першого компонента з другим компонентом. 12. Спосіб за п. 11, який відрізняється тим, що додатковий компонент, зокрема поршень (4), виготовлений партіями, і щонайменше одна істотна характеристика, така як діаметр, визначена тільки за допомогою випадкової вибірки в кожній партії. 13. Спосіб за п. 11 або 12, який відрізняється тим, що визначена(і) щонайменше одна або більше істотна(і) характеристика(и), зокрема такі, що стосуються інструменту вимірювання додаткового компонента або компонентів, зокрема діаметр поршня (4) і (або) осьова ефективна довжина підтримуючого кільця, яка(і) береться(уться) до уваги як додаткова(і) істотна(і) характеристика(и) на додаток до вирішальної істотної характеристики при виборі сумісної групи. 14. Спосіб за одним з попередніх пунктів, який відрізняється тим, що відповідна група вибрана таким чином, що вирішальна істотна характеристика разом з необов'язковою щонайменше однією додатковою істотною характеристикою додаткового компонента і разом з істотною(ними) характеристикою(ами) веде до шуканого значення, зокрема до бажаного рівня заповнення заглиблення ущільненням і (або) прокладкою. 15. Пристрій (1) для введення в організм лікарського засобу, зокрема, у вигляді аерозолю (А), з покращеною точністю дозування, який має направляючу трубку (3), поршень (4), який направляється з можливістю переміщення всередині трубки в подовжньому напрямі, ущільнення (5) певної форми, що служить для ізоляції направляючої трубки (3) і поршня (4), і заглиблення (6), що служить для розміщення ущільнення (5) необхідної форми, який відрізняється тим, що ущільнення (5) певної форми конкретної партії скомбіновано з направ ляючою трубкою (3) сумісної групи направляючих трубок (3), вибраної з декількох груп направляючих трубок (3), залежно від щонайменше однієї істотної характеристики партії для заповнення заглиблення (6) за допомогою ущільнення (5) певної форми на бажану глибину заповнення і таким чином отримання оптимального ущільнення між ущільненням (5) і направляючою трубкою (3), щоб покращити точність дозування. 16. Пристрій за п. 15, який відрізняється тим, що заглиблення (6) виконано у вигляді виїмки або заплечика і (або) має кільцеподібну форму. 17. Пристрій за п. 15 або 16, який відрізняється тим, що заглиблення (6) сформовано або обмежено за допомогою направляючої трубки (3). 18. Пристрій за одним з пп. 15-17, який відрізняється тим, що має підтримуюче кільце (7) для осьового закріплення ущільнення (5) певної форми в заглибленні (6) і (або) для встановлення меж заглиблення (6). 19. Пристрій за одним з пп. 15-18, який відрізняється тим, що ущільнення (5) певної форми має кільцеподібну конструкцію, зокрема, форму ущільнюючого кільця. 20. Пристрій за одним з пп. 15-19, який відрізняється тим, що ущільнення (5) певної форми втиснуте в заглиблення (6) і (або) еластично деформоване заглибленням (6) і поршнем (4). 21. Пристрій за одним з пп. 15-20, який відрізняється тим, що діаметр поршня (4) складає від 0,25 до 4 мм, переважно від 0,5 до 3 мм, а більш переважно від 0,75 до 2,25 мм. 22. Пристрій за одним з пп. 15-21, який відрізняється тим, що об'єм пристрою (1), який нагнітається за один хід поршня, складає від 1 мкл до 1 мл, переважно від 1 до 500 мкл, більш переважно від 5 до 100 мкл, і найбільш переважно від 5 до 30 мкл. 23. Пристрій за одним з пп. 15-22, який відрізняється тим, що бажаний рівень заповнення рівний в середньому щонайменше 90 %, зокрема щонайменше 59 %, при допуску не більше 5 %, зокрема 4 % і менше. 24. Пристрій за одним з пп. 16-23, який відрізняється тим, що виконаний у вигляді розпилювача, інгалятора, інжектора, генератора тиску або дозуючого насоса і (або) медичного пристрою для аерозольної терапії. Дійсний винахід відноситься до способу подачі (доставки) лікарського засобу, зокрема, у вигляді аерозолю, який володіє покращеною точністю дозування, а також до пристрою для введення в організм пацієнта лікарського засобу, зокрема у вигляді аерозолю, який володіє покращеною точністю дозування, згідно з преамбулою до пункту 15 формули винаходу. Згідно дійсного винаходу під терміном "лікарські засоби", зокрема, також розуміють лікарські препарати або суміші лікарських засобів. Переважно, щоб лікарський засіб був представлений у вигляді рідини, хоча він також може бути представлений у вигляді суспензії, розчину або суміші суспензії і розчину (в англійській мові для позначення такої суміші використовується термін "суслюшен" (suslution)). Також він може бути представлений у вигляді порошку. Подальший опис дійсного винаходу в основному направлений на опис вживання лікарського засобу у вигляді рідини, і, отже, при його згадці часто використовується термін "рідина". Проте дійсний винахід також відповідно застосовний і відносно інших видів лікарських засобів і співставних речовин. 5 Публікація ЕР 1426662 А1, яка є відправною точкою дійсного винаходу, описує пристрій для нагнітання і, переважно, для подачі рідини, зокрема, лікарської рідини. Такий відомий пристрій має направляючу трубку з поршнем, який може переміщатися усередині цієї трубки в подовжньому напрямі повністю на всю її довжину, а також кільцеву ущільнюючу прокладку, що служить як ущільнення між направляючою трубкою і поршнем. Кільцева ущільнююча прокладка розташовується у виїмці направляючої трубки. Щоб забезпечити належний рівень ущільнення, кільцева ущільнююча прокладка повинна заповнювати виїмку більше ніж на 90%. На практиці ж було знайдено, що допуски індивідуальних компонентів конструкції приводять до неадекватного рівня ущільнення, який не повністю перешкоджає, зокрема, проникненню повітря, що може привести до недостатньої точності дозування. Точне ж дозування, проте, є вельми важливим чинником, особливо при введенні лікарських засобів в організм пацієнта або чого-небудь подібного, як і у разі дійсного винаходу. В основу дійсного винаходу покладена задача створення способу і пристрою для поліпшеної точності дозування при подачі і введенні лікарських засобів в організм пацієнта, зокрема лікарських засобів у вигляді аерозолю. Вищезгадана задача досягається за допомогою способу згідно пункту 1 формули винаходу або ж пристрою згідно пункту 15 формули винаходу. Переважні варіанти здійснення винаходу розкриті в залежних пунктах формули винаходу. У пропонованому в дійсному винаході способі для подачі лікарського засобу використовують перший і другий компоненти конструкції, при цьому перший компонент виробляється партіями, і щонайменше одна істотна характеристика перших компонентів кожної партії визначена випадковим чином, внаслідок чого визначається щонайменше одна вирішальна (має вирішальне значення) істотна характеристика для всіх перших компонентів відповідної партії, тоді як другий компонент ділиться на групи, які розрізняються на щонайменше одну істотну характеристику других компонентів, при цьому вибирається функція щонайменше однієї вирішальної істотної характеристики відповідної (підходящої) групи і перший компонент партії переважно комбінується виключно з другим компонентом групи відповідним цій партії або включеним в неї. Вибираючи відповідну підходящу групу других компонентів можна одержати поліпшене ущільнення між скомбінованими компонентами, які, переважно, переміщуються один відносно іншого для того, щоб доставити лікарський засіб. Таким чином досягається поліпшена точність дозування. Цей прийом особливо придатний для дуже малих компонентів, які виробляють, наприклад, завдяки мікроінженерії або тих, які мають розміри, що знаходяться в інтервалі лише від 10 μм до приблизно 3 мм. Наприклад, перші компоненти виготовляють за допомогою заливки матеріалу у форму під тиском методом впорскування і утворюють ущільнення, що мають певну форму, пере 95928 6 важно кільцеподібну, і особливо переважно мають форму ущільнюючих кілець. Як істотні характеристики перших компонентів, зокрема, у разі ущільнень, що мають кільцеподібну форму, таких як ущільнення у вигляді ущільнюючих кілець, переважно визначають їх об'єми і(або) здатність стискатись. Було виявлено, що як істотні характеристики перших компонентів достатньо визначити лише середню величину і стандартне відхилення, наприклад, об'єму і здатності стискатись перших компонентів. Це вимагає відносно невеликих зусиль. Другі компоненти, переважно, мають заглиблення, зокрема у вигляді заплечика або виїмки, що служить для розміщення в ньому першого компоненту і для формування, зокрема, направляючої трубки для поршня пристрою. Переважно, щоб істотна характеристика для розділення других компонентів на групи була б величиною, що відноситься до заглиблення, така як глибина і(або) ширина заглиблення. Було встановлено, що ці величини або розміри є достатніми для процесу розділення, так що потрібні лише відносно невеликі зусилля. Є переважним, щоб середнє і стандартне відхилення, зокрема, глибина і(або) ширина заглиблення знову б застосовувалися як істотні характеристики для розділення на групи. Другі компоненти, переважно, навмисно виготовляються з різними суттєвими характеристиками, які відрізняються одна від одної на величину більшу, ніж величина виробничого допуску, так щоб дозволити здійснити виробництво і тримати в готовності різні групи других компонентів. Виробництво з різними суттєвими характеристиками переважно здійснюється залежно від вимог або статистичної вірогідності. Другі компоненти, переважно, також виробляються партіями, але, зокрема, з іншими суттєвими характеристиками, і істотна характеристика других компонентів лише випадково визначається в кожній партії, а з цього визначається істотна характеристика для всіх других компонентів у відповідній партії. Таким чином можна уникнути індивідуального вимірювання других компонентів, що в цілому може втримати затрати на низькому рівні. Зокрема є переважним, щоб пристрій містив, на додаток до перших і других компонентів, щонайменше ще один додатковий компонент, зокрема, декілька додаткових компонентів, таких як поршень, який був би герметично ущільнений за допомогою першого компоненту, а також підтримуюче кільце для осьового закріплення цього компоненту на другому компоненті. Якщо потім будуть комбінуватись різні партії перших і других компонентів, то бажане задане значення може бути досягнуте за допомогою вибору відповідної групи другого компоненту, який, таким чином, є "змінною величиною", щонайменше, з погляду його істотної характеристики. Для такої зміни є особливо придатним вимірювання глибини заглиблення, тобто направляючої трубки і(або) ширини (осьової довжини) заглиблення, тобто, наприклад, підтримую 7 чого кільця для закріплення ущільнення в якості першого компонента в заглибленні. Щоб дозволити здійснювати вибір сумісної групи, в той момент, коли пристрій містить щонайменше один інший компонент на додаток до перших і других компонентів, визначається або береться до уваги одна(ні) або більше суттєва(і) характеристика(и) іншого компоненту або компонентів, зокрема, діаметр поршня і(або) осьова корисна довжина підтримуючого кільця, визначається(ються) і береться(уться) до уваги в якості однієї(их) або більше істотної(их) характеристики(к) на додаток до вирішальної істотної характеристики при виборі сумісної групи. Як вже було пояснено, сумісна група вибирається так, щоб вирішальна істотна характеристика разом з факультативними іншими суттєвими характеристиками і істотною характеристикою в кінцевому пристрої приводила б, щонайменше в середньому, до специфічного бажаного значення, зокрема до бажаного рівня заповнення заглиблення ущільнювачем, що має певну форму. Такий вибір робиться, зокрема, за допомогою комп'ютера, беручи до уваги розповсюджені помилки або статистичні способи. Як термін "рівень заповнення" в дійсному винаході, зокрема, розуміється відношення характеристики встановленого ущільнення до величини заглиблення. Як термін "ущільнення, що має певну форму" в дійсному винаході розуміють як плоскі ущільнення, так і кільцеві ущільнення, рівно як і інші ущільнення, що мають певну форму, тобто мають різні поперечні форми. Є переважним, щоб ущільнення, що мають певну форму, виготовлялися б у вигляді нескінченного круга. Пропонований процес був описаний вище у загальних рисах, але з посиланням на його переважне вживання з пристроєм для нагнітання або дозування і, переважно, для витіснення рідини або лікарського засобу. Пропонований процес звичайно застосовний зі всіма видами пристроїв. Є переважним його використання з пристроями, виготовленими з мікрокомпонентів, при цьому індивідуальний підбір розмірів або вимірювання таких компонентів вимагає надмірних зусиль або ж буде повністю неможливим. Опис, який слідує нижче, в основному відноситься до пропонованого пристрою. Пропонований в дійсному винаході пристрій для введення в організм пацієнта лікарського засобу, зокрема, пристрій для нагнітання або дозування і, переважно, для витіснення рідини, має направляючу трубку з поршнем, який може переміщатися усередині даної трубки в подовжньому напрямі, ущільнення, що має певну форму, що служить для утворення ущільнення між направляючою трубкою і поршнем, а також заглиблення для розміщення цього ущільнення, при цьому ущільнення вибирається із специфічної партії ущільнень, комбінуючись з направляючою трубкою із сумісної специфічної групи, дана група вибирається з декількох груп направляючих трубок залежно від щонайменше однієї вирішальної істотної характеристики партії, що необхідно для заповнення 95928 8 заглиблення до бажаного рівня за допомогою ущільнення певної форми. Таким чином, специфічний бажаний рівень заповнення, який забезпечується бажаним ущільненням, а, отже, і поліпшена точність дозування можуть бути досягнуті відносно простим чином. При виборі сумісної групи, допуски або характеристики інших компонентів, зокрема значні характеристики партій подальших компонентів, такі як діаметр поршня, ефективна осьова довжина підтримуючого кільця, що служить для осьової підтримки ущільнення певної форми або меж виїмки, або чого-небудь подібного, також можуть братися до уваги. Інші аспекти, характеристики, переваги і особливості дійсного винаходу стануть ясними з пунктів формули винаходу і подальшого опису переважного варіанту здійснення винаходу з посиланням на креслення. Єдине креслення зображає схематичний розріз деталі пропонованого пристрою. Пропонований пристрій 1 для введення (лікарського засобу) в організм пацієнта або подачі, зокрема, для нагнітання або дозування лікарського засобу, переважно рідини 2, сконструйовано спеціально для дозування дуже малих об'ємів, що нагнітаються. Такий об'єм, що нагнітається, у разі зображеного переважного варіанту здійснення винаходу, знаходиться в інтервалі від 1 μл до 1 μл, переважно в інтервалі від 1 μл до 500 μл, більш переважно в інтервалі від 5 μл до 100 μл і найбільш переважно в інтервалі від 5 μл до 30 μл, зокрема, будучи рівним 15 μл, що подається під час одного ходу поршня. Для того, щоб мати можливість забезпечити точну подачу і дозування бажаного об'єму, зокрема, навіть під час першого використання після тривалого періоду бездіяльності, важливо, щоб ніяка кількість повітря не могла б проникнути в пристрій 1, зокрема, тоді як він не використовується, оскільки інакше дозування більше не може бути здійснене з бажаною точністю. Пристрій 1 має направляючу трубку 3 (другий компонент), поршень 4, який направляється, щоб бути переміщуваним усередині трубки в подовжньому напрямі (додатковий компонент), а також ущільнення 5 певної форми, (перший компонент) в поглибленні 6 і необов'язкове опорне кільце 7 (додатковий компонент) для підтримки ущільнення 5 певної форми. Направляюча трубка 3 опціонально, разом з опорним кільцем 7, утворює заглиблення 6, що кільце подібно оточує поршень 4, маючи будову, зокрема, у вигляді вирізу, а в даному випадку кільцеподібного вирізу. У разі зображеного переважного варіанту здійснення винаходу опорне кільце 7 утворює осьову сторону або межу заглиблення 6, так що направляюча трубка 3 по суті утворює кільцеподібний заплечик і радіальну зовнішню межу заглиблення 6. Якщо необхідно, заглиблення 6 також може бути утворено без використання направляючої трубки 3. У разі зображеного переважного варіанту здійснення винаходу поршень 4 має округлий попере 9 чний перетин з діаметром, що знаходиться в інтервалі від 0,25 мм до 4 мм, переважно в інтервалі від 0,5 мм до 3 мм, а більш конкретно в інтервалі від 0,75 мм до 2,25 мм. Поршень 4 переважно виготовляється з металу, зокрема, з неіржавіючої сталі. Конструкція його, зокрема, має форму порожньої трубки або капілярної трубки. Поршень 4 переважно відведений назад і відповідно має малий допуск діаметра. Ущільнення 5, що має певну форму, переважно має безперервну кільцеподібну форму, щоб відповідати формі заглиблення 6. Зокрема, ущільнення 5 певної форми є кільцевою прокладкою ущільнювача, яка в невстановленому положенні має, принаймні в основному, круглий поперечний перетин. Поперечний перетин або товщина матеріалу невстановленого ущільнення 5, що має певну форму, у разі зображеного переважного варіанту здійснення винаходу знаходиться в інтервалі від 0,3 мм до 3 мм, переважно в інтервалі від 0,5 мм до 2 мм, зокрема в інтервалі від 1 мм до 1,5 мм. Внутрішній діаметр в основному відповідає діаметру поршня. Ущільнення 5, що має певну форму, переважно складається з силікону або якогось іншого каучукоподібного матеріалу, який, зокрема, придатний для використання у фармацевтичній або харчовій промисловості. У встановленому стані (тобто коли пристрій 1 є зібраним) ущільнення 5 певної форми, принаймні в основному, розташовується в заглибленні 6. Підтримуюче кільце 7 спирається на нього і фіксує ущільнення 5 певної форми в осьовому напрямі в заглибленні 6. На додаток до цього ущільнення 5 певної форми спирається в радіальному напрямі на поршень 4, який проходить крізь ущільнення 5 певної форми, щільно прилягаючи до нього. Ущільнення 5 певної форми вдавлюється або, деформуючись, поміщається в заглиблення 6. При переході з невстановленого положення поперечний перетин ущільнення 5 певної форми стає по суті прямокутним, або щонайменше одна з його контактних сторін ущільнення стає плоскою для прилягання до поршня 4. "Рівень заповнення" відповідає відношенню об'єму встановленого ущільнення 5 певної форми до об'єму заглиблення 6. Для того, щоб мати можливість одержати хороший рівень ущільнення і відповідно домогтися точного дозування за допомогою пристрою 1, бажаний рівень заповнення, тобто "шуканий рівень заповнення" в середньому повинен бути рівний 90%, а конкретніше, щонайменше 95% з допуском щонайбільше 5%, а конкретніше 4% або менше. У разі зображеного переважного варіанту здійснення винаходу підтримуюче кільце 7 переважно приєднується до трубки 3, яка подає, за допомогою пробкоподібного утримуючого елементу 8 або чого-небудь подібного. За допомогою відповідних осьових або торцевих контактних поверхонь можливо досягти обумовленого положення підтримуючого кільця 7 і, отже, обумовленої ширини В (до 95928 10 вжини по осі) заглиблення 6 для ущільнення 5 певної форми. Більш того, об'єм заглиблення 6 явно задається глибиною Τ заглиблення 6 в трубці 3, яка подає, тобто радіальною протяжністю заглиблення 6. Поршень 4 розмежовує напірну камеру 9 в трубці 3, яка подає. Поршень 4 переважно оснащується зворотним клапаном 10, який встановлюється, зокрема, в кінці поршня 4 передньою своєю частиною до напірної камери 9. Переважно порожній поршень 4 утворює канал 11, який подає, для рідини 2 у разі зображеного переважного варіанту здійснення винаходу. Рідина 2 може подаватися, а конкретніше втягуватися через канал 11, який подає, через отвір впускання або зворотний клапан 10 в напірну камеру 9 разом з відповідним осьовим переміщенням поршня. На стороні стиснення або стороні подачі пристрою 1 опціонально присутній випускний отвір (не показано) і, наприклад, розпилювальна головка 12 для подачі і опціонального розпилювання рідини 2. Ущільнення 5, що мають певну форму, виготовляються партіями, тобто груповим чином. Зокрема, партія виробляється з обумовленої кількості початкового матеріалу, який є якомога більш однорідним. Ущільнення 5, що мають певну форму, переважно виготовляються під тиском способом уприскування, зокрема за допомогою інструменту (не показаний) для заливки матеріалу під тиском у форму, яка має безліч западин. Відповідно в ході кожного процесу заливки матеріалу виробляється безліч ущільнень 5, які мають певну форму. Ущільнення 5, які мають певну форму, можуть відрізнятися один від одного залежно від партії, особливо з погляду їх істотних характеристик, таких як діаметр кільця, поперечний перетин, об'єм, стисливість або що-небудь подібне. Окрім цих характеристик, які залежать від інструменту для заливки матеріалу у форму під тиском, можуть розрізнятися і змінні, які визначаються матеріалами або технічними параметрами, задіяними у виробничому процесі, такі змінні, як стисливість. Ущільнення 5, які мають певну форму, є першими компонентами згідно запропонованого способу здійснення винаходу. Істотні характеристики (зокрема лише об'єм і стисливість) ущільнень 5, які мають певну форму, переважно визначаються лише для деяких ущільнень 5, які мають певну форму, зі всієї кількості ущільнень партії, а за ними вже визначаються вирішальні істотні характеристики, зокрема середнє і стандартне відхилення, що здійснюється беручи до уваги різні впливи пов'язаних з інструментом для заливки матеріалу у форму під тиском характеристик і допусків в сукупності з іншими характеристиками, і, якщо це можливо, беручи до уваги функції розподілу. Трубка 3, яка подає, класифікується згідно даній пропозиції переважно лише однією істотною характеристикою, тобто у разі цього переважного варіанту здійснення винаходу, базуючись на глибині Τ заглиблення 6. Трубки З, які подають, є другими компонентами для задач запропонованого способу і, таким чином, вони підрозділяються на різні групи згідно їх глибині Т. Зокрема, трубки 3, 11 які подають, виробляються з різними глибинами Τ для того, щоб забезпечити наявність необхідних груп трубок 3, які подають. Переважно, щоб групи відрізнялися б одна від одної згідно їх глибині Τ на величину, яка перевищує виробничий допуск. Пропонується, що перший компонент, тобто ущільнення 5, що має певну форму, певної партії комбінувалося б або з'єднувалося б лише з одним другим компонентом, тобто з трубкою 3, яка подає, групи, яка відповідає або співпадає з певною партією. Специфічна партія, сумісна з групою, вибирається як функція, залежна від щонайменше однієї вирішальної істотної характеристики цієї партії, тобто, зокрема, як функція, залежна від середнього значення стандартного відхилення об'єму і здатності стискатись тобто ущільнення 5, що має певну форму, даної партії, так що істотна характеристика, тобто, зокрема, глибина Τ заглиблення 6 певної групи приводить до цільового значення, в даному випадку до бажаного рівня заповнення, або до специфічного ущільнення в пристрої 1. Даний вибір здійснюється, зокрема, беручи до уваги розповсюдження помилки і наявні групи. У разі зображеного переважного варіанту здійснення винаходу пристрій 1 має додаткові компоненти, а саме, поршень 4 і опорне кільце 7, характеристики або розміри яких є критичними для досягнення бажаного значення, тобто бажаного рівня заповнення відповідного пристрою 1. Відповідним чином істотні характеристики додаткових компонентів, зокрема діаметр поршня 4 в партії поршнів 4 і ширина В заглиблення 6, а більш конкретно характеристики опорного кільця 7 і трубки 3, яка подає, які є критичними в даному випадку, переважно визначаються шляхом відбору випадкових зразків, на основі яких і визначаються подальші істотні характеристики, зокрема середнє значення і стандартне відхилення. Ці подальші істотні характеристики переважно також беруться до уваги в ході вищезазначеного вибору групи трубок 3, які подають, що необхідно для досягнення бажаної цільової характеристики, тобто бажаного рівня наповнення, а, отже, і бажаного ущільнення і точності дозування. Задані характеристики, такі як об'єм, стисливість, глибина, ширина або що-небудь подібне є єдино можливими суттєвими характеристиками, визначуваними за допомогою прикладу. Залежно від конструкції і дизайну пристрою 1 виробництво компонентів і особливо допуски компонентів, подальші і(або) інші характеристики можуть використовуватися як важливі і(або) істотні характеристики. Альтернативним чином або додатково замість рівня заповнення як цільова характеристика можуть використовуватися інші характеристики. Замість трубки 3, яка подає, як "змінні" компоненти можуть також комбінуватися інші компоненти тобто компоненти з різними суттєвими характеристиками діляться на групи - з партіями інших компонентів, що необхідно для досягнення цільової характеристики або поліпшеної точності дозування завершеного пристрою 1. Для того, щоб доставити рідину 2 або лікарський засіб перші і другі компоненти, тобто, зокрема, трубка 3, яка подає, і ущільнення 5 певної форми ' 95928 12 переміщаються по відношенню один до одного, пропонована комбінація компонентів веде до отримання оптимального ущільнення між компонентами, що у свою чергу приводить до поліпшеної точності дозування під час подачі або вживання. У разі зображеного переважного варіанту здійснення винаходу пропонований пристрій 1 виготовляється, зокрема, як розпилювач або інгалятор (апарат для інгаляційної терапії). Рідина 2 засмоктується в напірну камеру 9 за допомогою поршня 4 у міру його почергового поворотно-поступального осьового переміщення по каналу 11, який подає, або ж на неї виявляється тиск і вона витісняється через розпилювальну головку 12 і доставляється або вводиться в організм пацієнта, будучи переважно розпиленою, тобто з рідини 2 утворюється розпилений туман або аерозоль А, як це показано на кресленні. У переважному варіанті пристрій 1 є розпилювачем або інгалятором, як це описано в публікації WO 91/14468 А1 і у разі специфічного переважного варіанту здійснення винаходу згідно публікації WO 97/12687 А1 (фіг. 6а, 6б) і на фіг. 1 і 2 публікації WO 2005/080001 А1. Зокрема це може бути розпилювач або інгалятор, який продається компанією Boehringer Ingelheim GmbH під торговою маркою "Respimat". Проте пристрій 1 може, наприклад, також використовуватися як насос дозування, зокрема для акуратної подачі лікарських засобів або чогонебудь подібного, зокрема, як це описується в публікації ЕР 1426662 А1. Зокрема, пристрій 1 є медичним пристроєм. Рідина 2 переважно є лікарським складом, як це вже було пояснено раніше в даному документі, або лікарським засобом, терапевтичним засобом, діагностуючим засобом або чим-небудь подібним. Зокрема пристрій 1 може також використовуватися для того, щоб одночасно доставляти певну кількість активних хімічних речовин або лікарських засобів. В цьому випадку рідина 2, зокрема, є сумішшю типу "суслюшен" (сумішшю суспензії і розчину). Принцип "суслюшен" базується на складанні рецептури з певної кількості активних речовин, які знаходяться разом одна поряд з іншою в одному препараті у вигляді розчину і суспензії. В цьому відношенні посилання робиться на публікацію ЕР 1087750 А1, зміст якої включений в дійсний опис як додаткове розкриття предмету винаходу. Проте пристрій 1 може також теоретично використовуватися для косметичних і інших цілей. Переважні інгредієнти і(або) препарати лікарського засобу або рідини 2 включені в нижче приведений список: Нижче приведені суміші можуть використовуватися як самі по собі, так і в комбінації з іншими активними речовинами для вживання в пристрої згідно даному винаходу. Вони, зокрема, включають бета-міметики, антихолінергічні засоби, адренокортикостероїди, інгібітори PDE IV, антагоністи LTD4, EGFR-інгібітори, агоністи допаміну, протиалергічні засоби, антагоністи PAF і інгібітори РІ3кінази, але також вони включають і комбінації двох або трьох активних речовин, тобто: 13 - бета-міметиків з адренокортикостерїдами, інгібіторів PDE IV, EGFR-інгібіторів або антагоністів LTD4, - антихолінергічних засобів з бета-міметиками, адренокортикостероїдів, інгібіторів PDE IV, EGFRінгібіторів або антагоністів LTD4, - адренокортикостероїдів з інгібіторами PDE IV, EGFR-інгібіторів або антагоністів LTD4, - інгібіторів PDE IV з EGFR-інгібіторами або антагоністами LTD4, - EGFR-інгібіторів з антагоністами LTD4. Приклади переважних бета-міметиків, які можуть бути згадані, включають албутерол, арформотерол, бамбутерол, бітолтерол, броксатерол, карбутерол, кленбутерол, фенотерол, формотерол, гексопреналін, ібутерол, ізоетарін, ізопреналін, левосалбутамол, мабутерол, мелуадрін, метапротеренол, оркипреналін, пірбутерол, прокатерол, репротерол, римітерол, ритодрін, салмефамол, салметерол, сотеренол, сульфонтерол, тербуталін, тіарамід, толубутерол, зінтерол, CHF-1035, HOKU-81, KUL-1248 і 3-(4-{6-[2-гідрокси-2-(4-гідрокси-3гідроксиметилфеніл)-етиламіно]-гексилокси}бутил-1)-бензолсульфонамід 5-[2-(5,6-діетиліндан-2-іламіно)-1гідроксіетил]-8-гідрокси-1Н-хінолін-2-он - 4-гідрокси-7-[2-{[2-{[3-(2-фенілетокси)-пропіл]сульфоніл}-етил]-аміно}-етил]-2(3Н)-бензотіазолон 1-(2-фторо-4-гідроксифеніл)-2-[4-(1бензімідазоліл)-2-метил-2-бутиламіно]етанол 1-[3-(4-метоксибензиламіно)-4гідроксифеніл]-2-[4-(1-бензімідазоліл)-2-метил-2бутиламіно]етанол - 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8іл]-2-[3-(4-N,N-диметиламінофеніл)-2-метил-2пропіламіно]етанол - 1-[2Н-5-гідрокси-3-окси-4Н-1,4-бензоксазин-8іл]-2-[3-(4-метоксифеніл)-2-метил-2-пропіламіно] етанол - 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8іл]-2-[3-(4-n-бутилоксифеніл)-2-метил-2пропіламіно]етанол - 1-[2Н-5-гідрокси-3-оксо-4Н-1,4-бензоксазин-8іл]-2-{4-[3-(4-метоксифеніл)-1,2,4-тріазол-3-іл]-2метил-2-бутиламіно}етанол 5-гідрокси-8-(1-гідрокси-2ізопропіламінобутил)-2Н-1,4-бензоксазин-3-(4Н)-он - 1-(4-аміно-3-хлоро-5-трифторометилфеніл)2-тpет-бутиламіно)-етанол 6-гідрокси-8-{1-гідрокси-2-[2-(4метоксифеніл)-1,1-диметилетиламіно]-етил}-4Нбензо[1,4]оксазин-3-он - 6-гідрокси-8-{1-гідрокси-2-[2-(4-етиловий ефір феноксіоцтової кислоти)-1,1-диметилетиламіно]етил}-4Н-бензо[1,4]оксазин-3-он - 6-гідрокси-8-{1-гідрокси-2-[2-(4-феноксіоцтова кислота)-1,1-диметилетиламіно]-етил}-4Нбензо[1,4]оксазин-3-он 8-{2-[1,1-диметил-2-(2,4,6-триметилфеніл)етиламіно]-1-гідроксіетил}-6-гідрокси-4Нбензо[1,4]оксазин-3-он 6-гідрокси-8-{1-гідрокси-2-[2-(4гідроксифеніл)-1,1-диметилетиламіно]-етил}-4Нбензо[1,4]оксазин-3-он 95928 14 6-гідрокси-8-{1-гідрокси-2-[2-(4-ізопропілфеніл)-1,1-диметилетиламіно]-етил}-4Нбензо[1,4]оксазин-3-он - 8-{2-[2-(4-етилфеніл)-1,1-диметилетиламіно]1-гідроксіетил}-6-гідрокси-4Н-бензо[1,4]оксазин-3он 8-{2-[2-(4-етоксифеніл)-1,1диметилетиламіно]-1-гідроксіетил}-6-гідрокси-4Нбензо[1,4]оксазин-3-он 4-(4-{2-[2-гідрокси-2(6-гідрокси-3-оксо-3,4дигідро-2Н-бензо[1,4]оксазин-8-іл)-етиламіно]-2метилпропіл}-фенокси)-масляна кислота 8-{2-[2-(3,4-дифторофеніл)-1,1диметилетиламіно]-1-гідроксіетил}-6-гідрокси-4Нбензо[1,4]оксазин-3-он 1-(4-етоксикарбоніламіно-3-ціано-5фторофеніл)-2-(тpет-бутиламіно)-етанол - 2-гідрокси-5-(1-гідрокси-2-{2-(4-(2-гідрокси-2фенілетиламіно)-феніл]-етиламіно]-етил)бензальдегід - N-[2-гідрокси-5-(1-гідрокси-2-{2-[4-(2-гідрокси2-фенілетиламіно)-феніл]-етиламіно}-етил)феніл]-формамід 8-гідрокси-5-(1-гідрокси-2-{2-[4метоксибіфеніл-3-іламіно)-феніл]-етиламіно}етил)-1Н-хінолін-2-он - 8-гідрокси-5-(1-гідрокси-2-(6-фенілетиламіногексиламіно)-етил)-1Н-хінолін-2-он 5-[2-(2-{4-[4[(2-аміно-2-метил-пропокси)феніламіно]-феніл}-етиламіно)-1-гідроксіетил]-8гідрокси-1Н-хінолін-2-он [3-(4-{6-[2-гідрокси-2-(4-гідрокси-3гідроксиметилфеніл)-етиламіно]-гексилокси}бутил)-5-метилфеніл]- сечовина 4-(2-{6-[2-(2,6-дилоробензилокси)-етокси]гексиламіно}-1-гідроксіетил)-2-гідроксиетилфенол 3-(4-{6-[2-гідрокси-2-(4-гідрокси-3гідроксиметилфеніл)-етиламіно]-гексилокси}бутил)-бензол сульфамід 3-(4-{7-[2-гідрокси-2-(4-гідрокси-3гідроксиметилфеніл)-етиламіно]-гептилокси}пропіл)-бензолсульфамід 4-(2-{6-[4-(3-циклопентансульфонілфеніл)бутокси]-гексиламіно}-1-гідроксіетил)-2гідроксиметилфенол N-адамантан-2-іл-2-(3-{2-[2-гідрокси-2-(4гідрокси-3-гідроксиметилфеніл)-етиламіно]пропіл}-феніл)-ацетамід необов'язково у вигляді рацематів, енантіомерів, діастереомерів або у вигляді фармакологічно сумісних солей, сольватів або гідратів. Переважними є солі вибирані з групи, яка включає гідрохлорид, гідробромід, гідройодид, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцитрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцинат, гідробензонат і гідро-n-толуолсульфонат. Приклади переважних антихолінергічних засобів, які можуть бути згадані, включають солі тіотропію, переважною є сіль броміду, солі окситропію, переважною є сіль броміду, солі флутропію, переважною є сіль броміду, солі іпратропію, переважною є сіль броміду, солі глікопіронію, переважною є сіль броміду, солі троспію, переважною є сіль броміду, толтеродін. З вище перелічених со 15 лей фармакологічно активна частина представлена катіонами, можливі аніони представлені хлоридом, бромідом, йодидом, сульфатом, фосфатом, метансульфонатом, нітратом, малеатом, ацетатом, цитратом, фумаратом, тартратом, оксалатом, сукцинатом, бензоатом, p-толуолсульфонатом. Додатково до цього - 2,2-дифенілпропіонової кислоти, метобромід тропенолового ефіру - 2,2-дифенілпропіонової кислоти, метобромід скопінового ефіру - 2-фторо-2,2-дифенілоцтової кислоти, метобромід скопінового ефіру - 2-фторо-2,2-дифенілоцтової кислоти, метобромід тропенолового ефіру - 3,3',4,4'-тетрафторобензилової кислоти, метобромід тропенолового ефіру - 3,3',4,4'-тетрафторобензилової кислоти, метобромід скопінового ефіру - 4,4'-дифторобензилової кислоти, метобромід тропенолового ефіру - 4,4'-дифторобензилової кислоти, метобромід скопінового ефіру - 3,3'-дифторобензилової кислоти, метобромід тропенолового ефіру - 3,3'-дифторобензилової кислоти, метобромід скопінового ефіру - 9-гідроксифлуорен-9-карбонової кислоти, метобромід тропенолового ефіру - 9-фторофлуорен-9-карбонової кислоти, метобромід тропенолового ефіру - 9-гідроксифлуорен-9-карбонової кислоти, метобромід скопінового ефіру - 9-фторофлуорен-9-карбонової кислоти, метобромід скопінового ефіру - 9-метилфлуорен-9-карбонової кислоти, метобромід тропенолового ефіру - 9-метилфлуорен-9-карбонової кислоти, метобромід скопінового ефіру - метобромід циклопропілтропінового ефіру бензилової кислоти - метобромід циклопропілтропінового ефіру 2,2-дифенілпропіонової кислоти - метобромід циклопропілтропінового ефіру 9гідроксиксантен-9-карбонової кислоти - метобромід циклопропілтропінового ефіру 9метилфлуорен-9-карбонової кислоти - метобромід циклопропілтропінового ефіру 9метилксантен-9-карбонової кислоти - метобромід циклопропілтропінового ефіру 9гідроксифлуорен-9-карбонової кислоти - метобромід циклопропілтропінового ефіру метилового ефіру 4,4'-дифторобензилової кислоти - метобромід тропенолового ефіру 9гідроксиксантен-9-карбонової кислоти метобромід скопінового ефіру 9гідроксиксантен-9-карбонової кислоти - метобромід тропенолового ефіру 9метилксантен-9-карбонової кислоти метобромід скопінового ефіру 9метилксантен-9-карбонової кислоти - метобромід тропенолового ефіру 9-ефір ксантен-9-карбонової кислоти - метобромід тропенолового ефіру 9дфторометилксантен-9-карбонової кислоти 95928 16 метобромід скопінового ефіру 9гідроксиметил-9-карбонової кислоти Приклади переважних кортикостероїдів, які можуть бути згадані в цьому документі, включають беклометазон, бетаметазон, бутиксокорт, циклесонид, дефлазакорт, дексаметазон, етипрендол, флунісолід, флутиказон, лотепреднол, мометазон, преднізолон, преднізон, триамцинолін, RPR106541, NS-126, ST-26 і - (S)-фторометиловий ефір 6,9-дифторо-17[(2-фуранілкарбоніл)-окси]-11-гідрокси-16-метил-3оксоандроста-1,4-дієн-17-карботіонової кислоти - (S)-(2-оксотетрагідрофуран-3S-іловий) ефір 6,9-дифторо-11-гідрокси-16-метил-3-оксо-17пропіонілоксиандроста-1,4-дієн-17-карботіонової кислоти - ціанометиловий ефір 6α,9α-дифторо-11βгідрокси-16α-метил-3-оксо-17α-(2,2,3,3тетраметилциклопропілкарбоніл)-оксиандроста1,4-дієн-17β-карботіонової кислоти необов'язково у вигляді їх рацематів, таких як енантіомери, діастереомери і необов'язково у вигляді їх фармакологічно сумісних солей, сольватів або гідратів. Прикладом переважних солей і їх похідних служать лужні солі, тобто солі натрію і калію, сульфобензонати, фосфати, ізонікотинати, ацетати, дихлороацетати, пропіонати, дигідрофосфати, пальмітати, півалати і фуроати. Приклади переважних інгібіторів PDE IV, які можуть бути згадані, включають енпрофілін, теофілін, рофлуміласт, аріфло (циломіласт), тофілімаст, пумафентин, ліриміласт, арофілін, атізорам, D-4418, Bay-198004, BY343, СР-325, 366, D-4396 (Sch-351591), AWD-12-281 (GW-842470), NCS-613, CDP-840, D-4418, PD-168787, Т-440, Т-2585, V11294A, С1-1018, CDC-801, CDC-3052, D-22888, YM-58997, Z-15370 і N-(3,5-дилоро-1-оксопіридин-4-іл)-4дифторометокси-3-циклопропілметоксибензамід . (-)n-[(4aR*,10bS*)-9-eтокси-1,2,3,4,4а,10bгексагідро-8-метокси-2-метилбензо[s][1,6]нафтиридин]-6-іл-N,N-діізопротлбензамід (R)-(+)-1-(4-бромобензил)-4-[(3циклопентилокси)-4-метоксифеніл]-2-піролідон - 3-(циклопентилокси-4-бромобензил)-1-(4-N'[N-2-ціано-S-метилізотіоуреїдо]-бензил)-2піролідон цис-[4-ціано-4-(3-циклопентилокси-4метоксифеніл)-циклогексан-1-карбонову кислоту] 2-карбометокси-4-ціано-4-(3циклопропілметокси-4-дифторометоксифеніл)циклогексан-1-он цис-[4-ціано-4-(3-циклопропілметокси-4дифторометоксифеніл)-циклогексан-1-ол] (R)-(+)-етил[4-(3-циклопентилокси-4метоксифеніл)-піролідін-2-іліден]ацетат (S)-(-)-етил[4-(3-циклопентилокси-4метоксифеніл)-піролідін-2-іліден]ацетат - 9-циклопентил-5,6-дигідро-7-етил-3-(2-тієніл)9Н-піразоло[3,4-с]-1,2,4-тріазоло[4,3-а]піридин 9-циклопентил-5,6-дигідро-7-етил-3-(третбутил)-9Н-піразоло[3,4-с]-1,2,4-тріазоло[4,3а]піридин необов'язково у вигляді їх рацематів, таких як енантіомери, діастереомери і необов'язково у ви 17 гляді їх фармакологічно сумісних солей, сольватів або гідратів. Переважними є солі, вибирані з групи, яка включає гідрохлорид, гідробромід, гідройодид, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцитрат, гідрофумарат, гідротартрат, гідрооксилат, гідросуцинат, гідробензоат і гідро-n-толуолсульфонат. Приклади переважних антагоністів LTD4, які можуть бути згадані в цьому документі, включають монтелукаст, пранлукаст, зафірлукаст, МСС-847 (ZD-3523), MN-001, MEN-91507 (LM-1507), VUF5078, VUF-K-8707, L-733321 і - 1-(((R)-(3-(2-(6,7-дифторо-2-хінолініл)-етеніл)феніл)-3-(2-(2-гідрокси-2-пропіл)-феніл)-тіо)метилциклопропаноцтову кислоту 1-(((1(R)-3(3-(2-(2,3-дилоротієно[3,2b]піридин-5-іл)-(Е)-етеніл)-феніл)-3-(2-(1-гідрокси1-метилетил)-феніл)-пропіл)-тіо)-метил)циклопропаноцтову кислоту [2-[[2-(4-трет-бутил-2-тиазоліл)-5бензофураніл]-оксиметил]-феніл]-оцтову кислоту необов'язково у вигляді їх рацематів, таких як енантіомери, діастереомери або необов'язково у вигляді їх фармакологічно сумісних солей, сольватів або гідратів. Переважними є солі, вибирані з групи, яка включає гідрохлорид, гідробромід, гідройодид, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцитрат, гідрофумарат, гідротартрат, гідрооксилат, гідросуцинат, гідробензоат і гідро-nтолуолсульфонат. Іншими прикладами необов'язково переважних солей і похідних служать лужні солі, тобто солі натрію і калію, сульфобензонати, фосфати, ізонікотинати, ацетати, пропіонати, дигідрофосфати, пальмітати, ι пивалати і фуроати. Приклади переважних інгібіторів EGFR-кінази, які можуть бути згадані, включають цетуксимаб, трастузумаб, ABX-EGF, Mab ICR-62 і 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4(морфолін)-1-оксо-2-бутен-1-іл]-аміно}-7циклопропілметоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-(N,Nдіетиламіно)-1-оксо-2-бутен-1-іл]-аміно}-7циклопропілметоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-(N,Nдиметиламіно)-1-оксо-2-бутен-1-іл]-аміно}-7циклопропілметоксихіназолін - 4-[(R)-(1-фенілетил)-аміно]-6-{[4-(морфолін-4іл)-1-оксо-2-бутен-1-іл]-аміно}-7циклопентилоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-((R)-6метил-2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-циклопропілметоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-((R)-6метил-2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-[(S)-(тетрагідрофуран-3-іл)-окси]-хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-((R)-2метоксиметил-2-оксоморфолін-4-іл)-1-оксо-2бутен-1-іл]-аміно}-7-циклопропілметоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[2-((S)-6метил-2-оксоморфолін-4-іл)-етокси]-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-({4-[N-(2метоксіетил)-N-метиламіно]-1-оксо-2-бутен-1-іл}аміно)-7-циклопропілметоксихіназолін 95928 18 - 4-[(3-хлоро-4-фторофен1л)-аміно]-6-({4-[N,Nдиметиламіно)-1-оксо-2-бутен-1-іл}-аміно)-7циклопентилоксихіназолін - 4-[(R)-(1-фенілетил)-аміно]-6-({4-[N,N-біс-(2метоксіетил)-аміно]-1-оксо-2-бутен-1-іл}-аміно}-7циклопропілметоксихіназолін 4-[(R)-(1-фенілетил)-аміно]-6-({4-[Nметоксіетил)-N-етиламіно]-1-оксо-2-бутен-1-іл}аміно}-7-циклопропілметоксихіназолін 4-[(R)-(1-фенілетил)-аміно]-6-({4-[Nметоксіетил)-N-метиламіно]-1-оксо-2-бутен-1-іл}аміно}-7-циклопропілметоксихіназолін 4-[(R)-(1-фенілетил)-аміно]-6-({4-[N(тетрагідропіран)-N-метиламіно]-1-оксо-2-бутен-1іл}-аміно)-7-циклопропілметоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-(N,Nдиметиламіно)-1-оксо-2-бутен-1-іл]-аміно}-7-((R)тетрагідрофуран)-хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-(N,Nдиметиламіно)-1-оксо-2-бутен-1-іл]-аміно}-7-((S)тетрагідрофуран)-хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-({4-[N-(2метоксіетил)-N-метиламіно]-1-оксо-2-бутен-1-іл}аміно)-7-циклопентилоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-({4-[Nциклопропіл-N-метиламіно)-1-оксо-2-бутен-1-іл}аміно)-7-циклопентилоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-(N,Nдиметиламіно)-1-оксо-2-бутен-1-іл]-аміно}-7-[(R)(тетрагідрофуран-2-іл)-метокси]-хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-(N,Nдиметиламіно)-1-оксо-2-бутен-1-іл]-аміно}-7-[(S)(тетрагідрофуран-2-іл)-метокси]-хіназолін 4-[(3-етинілфеніл)-аміно]-6,7-біс-(2метоксиетокси)-хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-7-[3(морфолін)-пропілокси]-6-[(вінілкарбоніл)-аміно]хіназолін 4-[(R)-(1-фенілетил)-аміно]-6-(4гідроксифеніл)-7Н-піроло[2,3-d]піримідин - 3-ціано-4-[(3-хлоро-4-фторофеніл)-аміно]-6{[4-(N,N-диметиламіно)-1-оксо-2-бутен-1-іл]-аміно}7-етоксихінолін 4-{[3-хлоро-4-(3-фторобензилокси)-феніл]аміно}-6(5-{[(2-метансульфоніл-етил)-аміно]метил}-фуран-2-іл)-хіназолін - 4-[(R)-(1-фенілетил)-аміно]-6-{[4-((R)-6-метил2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]-аміно}-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4(морфолін-4-іл)-1-оксо-2-бутен-1-іл]-аміно}-7[(тетрагідрофуран-2-іл)-метокси]-хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{[4-[N,Nбіс-(2-метоксіетил)-аміно)-7-[(тетрагідрофуран-2іл)-метокси]-хіназолін - 4-[(3-етинілфеніл)-аміно]-6-{[4-(5,5-диметил2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]-аміно}хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[2-(2,2диметил-6-оксоморфолін-4-іл)-етокси]-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[2-(2,2диметил-6-оксоморфолін-4-іл)-етокси]-7-[(R)(тетрагідрофуран-2-іл)-метокси]-хіназолін 19 4-[(3-хлоро-4-фторофеніл)-аміно]-7-[2-(2,2диметил-6-оксоморфолін-4-іл)-етокси]-6-[(S)(тетрагідрофуран-2-іл)-метокси]-хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{2-[4-(2оксоморфолін-4-іл)-піперидин-1-іл]-етокси}-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[1-(тpетбутилоксикарбоніл)-піперидин-4-ілоксі]-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(тpанс-4аміноциклогексан-1-ілокси)-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(тpанс-4метансульфоніламіноциклогексан-1-ілокси)-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6(тетрагідропіран-3-ілокси)-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1метилпіперидин-4-ілокси)-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1[(морфолін-4-іл)-карбоніл]-піперидин-4-ілокси}-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1[(метоксиметил)-карбоніл]-піперидин-4-ілокси}-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6(піперидин-3-ілокси)-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[1-(2ацетиламіно-етил)-піперидин-4-ілокси]-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6(тетрагідропіран-4-ілоксі)-7-етоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-((S)тетрагідрофуран-4-ілокси)-7-гідроксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6(тетрагідропіран-4-ілокси)-7-(2-метоксиетокси)хіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{транс-4[(диметиламіно)-сульфоніламіно]-циклогексан-1ілокси}-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{транс-4[(морфолін-4-іл)-карбоніламіно]-циклогексан-1ілокси}-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{транс-4[(морфолін)-сульфоніламіно]-циклогексан-1ілокси}-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6(тетрагідропропан-4-ілоксі}-7-(2-ацетиламіноетокси)-хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6(тетрагідропропан-4-ілокси}-7-(2метансульфоніламіно-етокси)-хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1[(піперидин-1-іл)-карбоніл]-піперидин-4-ілокси}-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1амінокарбонілметилпіперидин-4-ілокси)-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4-{N[(тетрагідропропан-4-іл)-карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4-{N[(морфолін-4-іл)-карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін 95928 20 - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4-{N[(морфолін-4-іл)-сульфоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(тpанс-4етансульфоніламіноциклогексан-1-ілокси)-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1метансульфонілпіперидин-4-ілоксі)-7етоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1метансульфонілпіперидин-4-ілокси)-7-(2метоксиетокси)-хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[1-(2метоксіацетил)-піперидин-4-ілокси]-7-(2метоксиетокси)-хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4ацетиламіноциклогексан-1-ілокси)-7метоксихіназолін 4-[(3-етинілфеніл)-аміно]-6-[1-(третбутилоксикарбоніл)-піперидин-4-ілокси]-7метоксихіназолін - 4-[(3-етинілфеніл)-аміно]-6-(тетрагідропіран4-ілокси]-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4-{N[(піперидин-1-іл)-карбоніл]-N-метиламiно}циклогексан-1-ілокси)-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4-{N[(4-метилпіперазин-1-іл)-карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{цис-4[(морфолін-4-іл)-карбоніламіно]-циклогексан-1ілокси}-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[2-(2оксопіролідін-1-іл)-етил]-піперидин-4-ілокси}-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1[(морфолін-4-іл)-карбоніл]-піперидин-4-ілокси}-7(2-метоксиетокси)-хіназолін 4-[(3-етинілфеніл)-аміно]-6-(1ацетилпіперидин-4-ілокси)-7-метоксихіназолін 4-[(3-етинілфеніл)-аміно]-6-(1метилпіперидин-4-ілокси)-7-метоксихіназолін 4-[(3-етинілфеніл)-аміно]-6-(1метансульфонілпіперидин-4-ілокси)-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1метилпіперидин-4-ілоксі)-7-(2-метоксиетокси)хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1ізопропілоксикарбоніл-піперидин-4-ілокси)-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(цис-4метиламіноциклогексан-1-ілокси)-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{цис-4-[N(2-метоксіацетил)-N-метиламіно]-циклогексан-1ілокси}-7-метоксихіназолін 4-[(3-етинілфеніл)-аміно]-6-(піперидин-4ілокси)-7-метоксихіназолін 4-[(3-етинілфеніл)-аміно]-6-[1-(2метоксіацетил)-піперидин-4-ілокси]-7метоксихіназолін - 4-[(3-етинілфеніл)-аміно]-6-{1-[(морфолін-4іл)-карбоніл]-піперидин-4-ілокси}-7метоксихіназолін 21 - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[(цис2,6-диметилморфолін-4-іл)-карбоніл]-піперидин-4ілокси}-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[(цис2,6-диметилморфолін-4-іл)-карбоніл]-піперидин-4ілокси}-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[2метилморфолін-4-іл)-карбоніл]-піперидин}-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[(цис2,6-диметилморфолін-4-іл)-карбоніл]-піперидин-4ілокси}-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[(2метилморфолін-4-іл)-карбоніл]-піперидин-4ілокси}-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-(S,S)(2-oкca-5-aзa-біцикло[2.2.1]гепт-5-іл)-карбоніл]піперидин-4-ілокси}-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[(Νметил-Ν-2-метоксіетиламіно)-карбоніл]-піперидин4-ілокси}-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1етилпіперидин-4-ілокси)-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-(2метоксіетил)-карбоніл]-піперидин-4-ілокси}-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-{1-[(3метоксипропіламіно)-карбоніл]-піперидин-4ілокси}-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[цис-4-(Nметансульфоніл-N-метиламіно)-циклогексан-1ілокси]-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[цис-4-(Nацетил-N-метиламіно)-циклогексан-1-ілокси]-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(транс-4метиламіноциклогексан-1-ілокси)-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[транс-4(N-метансульфоніл-N-метиламіно)-циклогексан-1ілокси]-7-метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(транс-4диметиламіноциклогексан-1-ілокси)-7метоксихіназолін - 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(транс-4{N-[(морфолін-4-іл)-карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-[2-(2,2диметил-6-оксоморфолін-4-іл)-етокси]-7-[(S)(тетрагідрофуран-2-іл)-метокси]-хіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1метансульфонілпіперидин-4-ілокси)-7метоксихіназолін 4-[(3-хлоро-4-фторофеніл)-аміно]-6-(1ціанопіперидин-4-ілокси)-7-метоксихіназолін 95928 22 необов'язково у вигляді їх рацематів, таких як енантіомери, діастереомери або необов'язково у вигляді їх фармакологічно сумісних солей, сольватів або гідратів. Переважними є солі, вибирані з групи, яка включає гідрохлорид, гідробромід, гідройодид, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцитрат, гідрофумарат, гідротартрат, гідрооксилат, гідросуцинат, гідробензоат і гідро-nтолуолсульфонат. Приклади переважних допамінових антагоністів, які можуть бути згадані в цьому документі, включають бромокриптин, каберголін, альфадигідроергокриптин, лізурид, перголід, праміпексол, роксиндол, ропінірол, таліпексол, тергурид і віозан необов'язково у вигляді рацематів, таких як енантіомери, діастереомери або необов'язково у вигляді їх фармакологічно сумісних солей, сольватів або гідратів. Переважними є солі, вибирані з групи, яка включає гідрохлорид, гідробромід, гідройодид, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцитрат, гідрофумарат, гідротартрат, гідрооксилат, гідросуцинат, гідробензоат і гідро-nтолуолсульфонат. Приклади переважних протиалергичних речовин, які можуть бути згадані в цьому документі, включають епінастін, цетиризин, азеластин, фексофенадін, левокабастин, лоратудін, мізоластин, кетотифен, емедастин, диметинден, клемастин, бамипин, сексхлорофенірамін, фенірамін, доксиламін, хлорофеноксамін, діменгідринат, прометазин, ебастин, деслоратидін і меклозин необов'язково у вигляді рацематів, таких як енантіомери, діастереомери або необов'язково у вигляді їх фармакологічно сумісних солей, сольватів або гідратів. Переважними є солі, вибирані з групи, яка включає гідрохлорид, гідробромід, гідройодид, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцитрат, гідрофумарат, гідротартрат, гідрооксилат, гідросуцинат, гідробензоат і гідро-n-толуолсульфонат. Крім цього макромолекули, що вдихаються, можуть бути використані як фармакологічно активні субстанції, як розкривається в публікації ЕР 1003478 А1 або СА 2297174 А1. Крім цього суміш може бути представлена у вигляді групи похідних алкалоїдів спорині, триптана, антагоністів CGRP, інгібіторів PDE V необов'язково у вигляді рацематів, таких як енантіомери, діастереомери і необов'язково у вигляді їх фармакологічно прийнятних солей приєднання кислоти і гідратів. У якості похідним алкалоїдів служать дигідроерготамін, ерготамін. 23 Комп’ютерна верстка Т. Чепелева 95928 Підписне 24 Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod completing a device for administration of medicament, in particular in aerosol form, and a device for administration of medicament, in particular in device for administration of medicament, in particular in aerosol form
Автори англійськоюBoeck Georg, Geser Johannes, Hausmann Matthias, Koelbel Hans-Juergen, Eicher Joachim, Feiertag Christian
Назва патенту російськоюСпособ комплектования устройства для введения в организм лекарственного средства, в частности, в виде аэрозоля и устройство для введения в организм лекарственного средства, в частности, в виде аэрозоля
Автори російськоюБьёк Георг, Гезер Йоханнес, Хаусманн Маттиас, Кьёльбель Ханс-Юрген, Айхер Йоахим, Файертаг Христиан
МПК / Мітки
МПК: B05B 11/02, A61M 15/00
Мітки: зокрема, пристрій, організм, засобу, спосіб, лікарського, пристрою, вигляді, аерозолю, комплектування, введення
Код посилання
<a href="https://ua.patents.su/12-95928-sposib-komplektuvannya-pristroyu-dlya-vvedennya-v-organizm-likarskogo-zasobu-zokrema-u-viglyadi-aerozolyu-ta-pristrijj-dlya-vvedennya-v-organizm-likarskogo-zasobu-zokrema-u-viglyad.html" target="_blank" rel="follow" title="База патентів України">Спосіб комплектування пристрою для введення в організм лікарського засобу, зокрема, у вигляді аерозолю та пристрій для введення в організм лікарського засобу, зокрема, у вигляді аерозолю</a>
Попередній патент: Спосіб виготовлення алкогольного напою (варіанти)
Наступний патент: Спосіб безперервного контролю процесу подрібнення у кульовому млині
Випадковий патент: 5-(пірид-2'-ил)тіо- та 5-алілтіо-2-п-толілтіазол-4-ілтрифенілфосфоній йодиди, що проявляють фунгицидні властивості