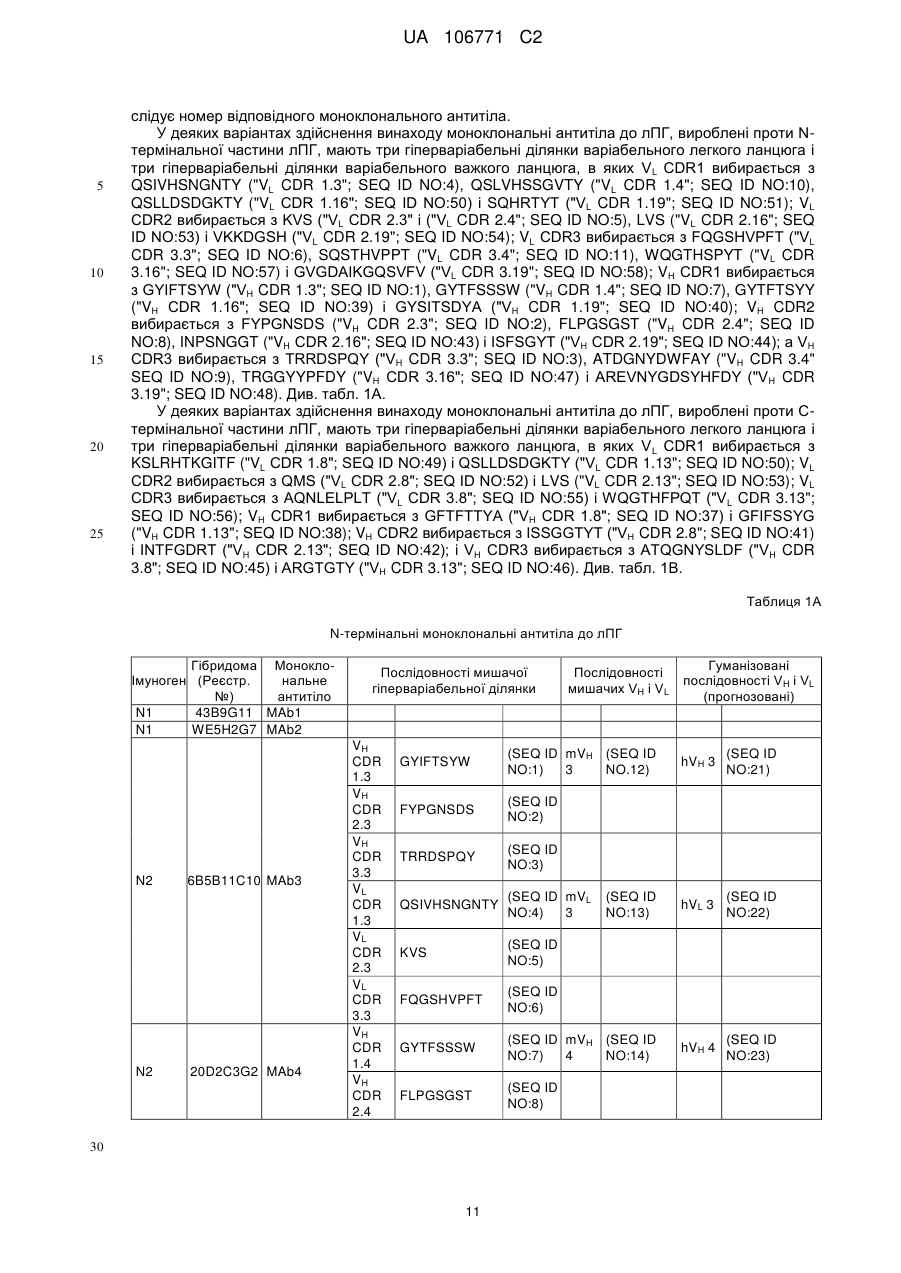
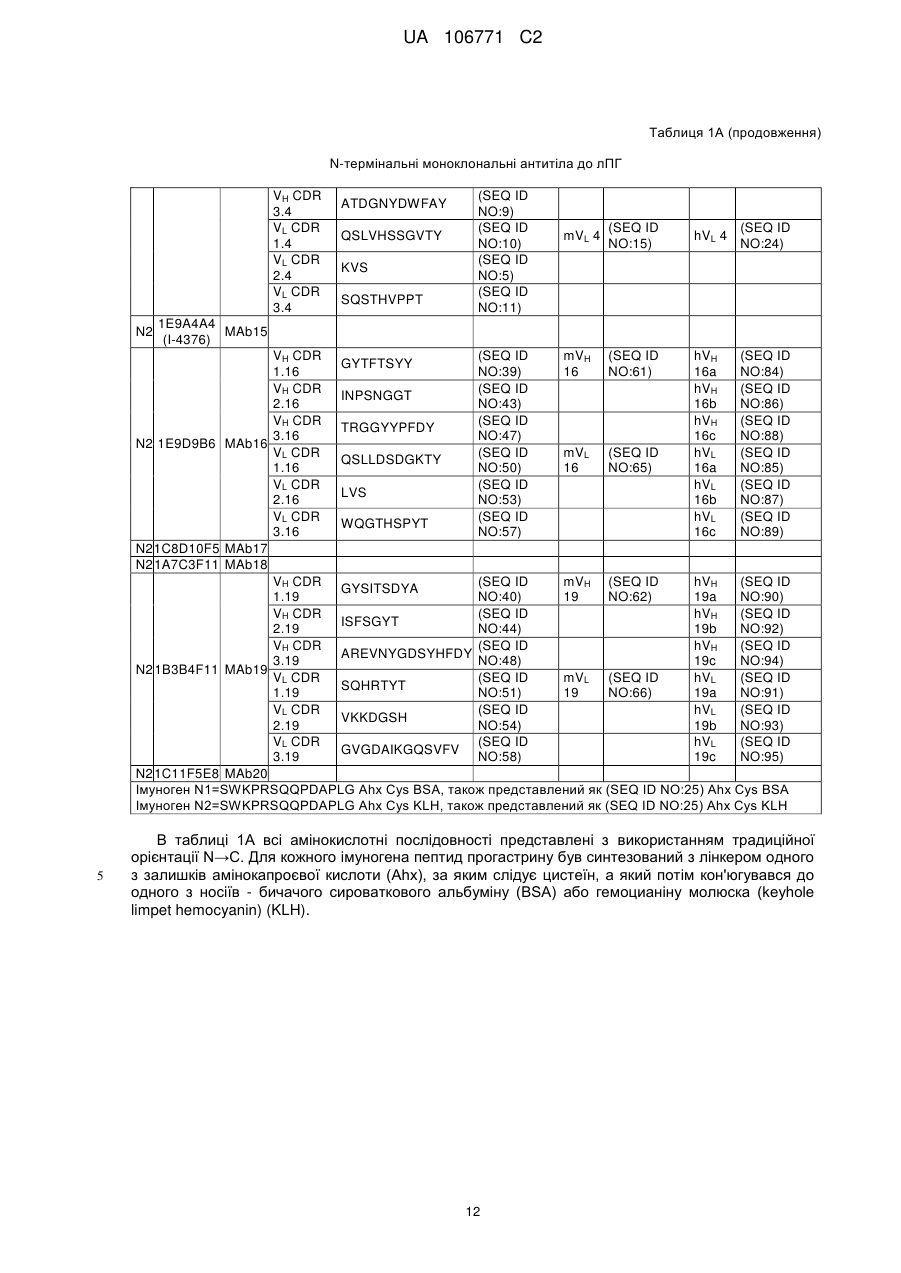
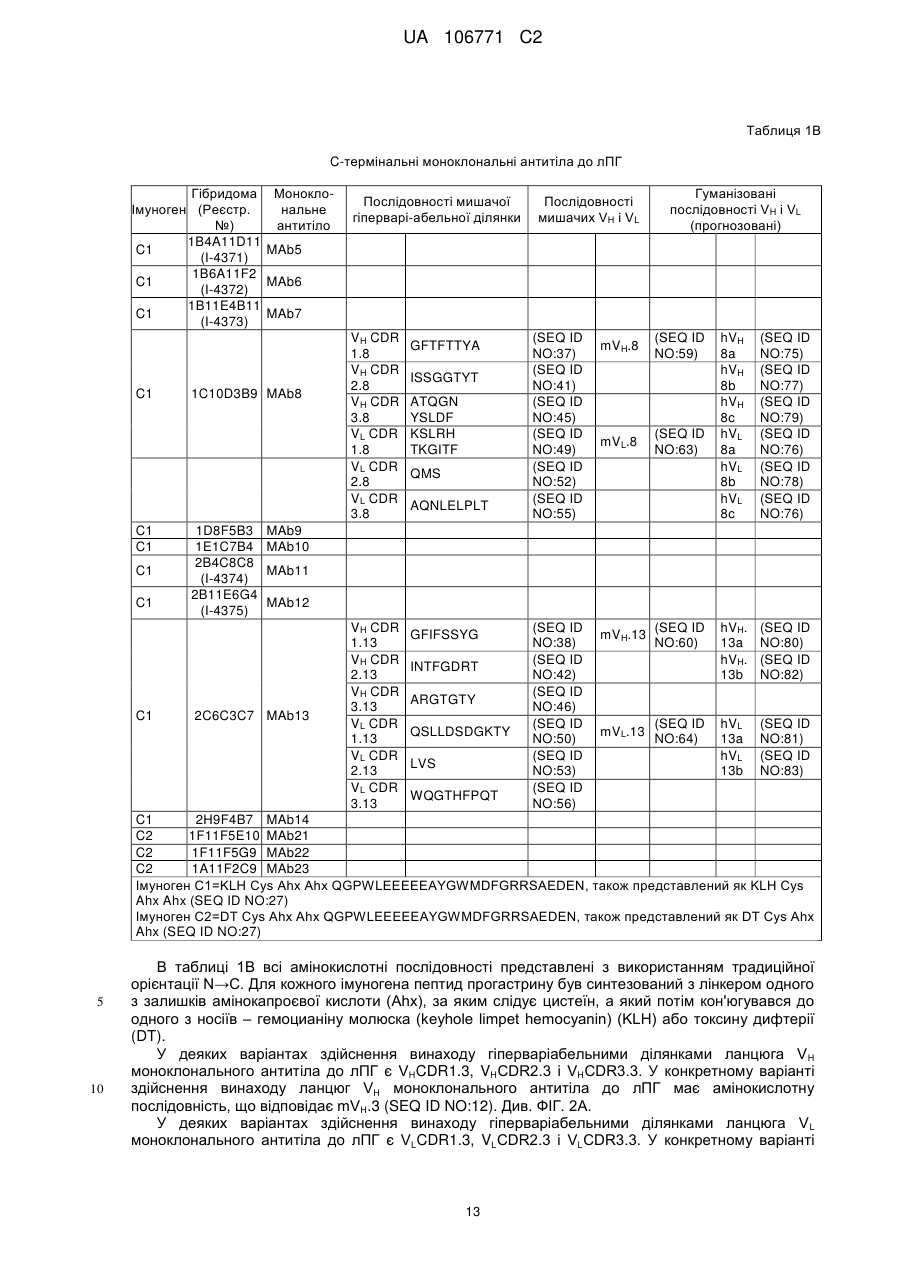
Моноклональні антитіла до прогастрину та їх використання
Номер патенту: 106771
Опубліковано: 10.10.2014
Автори: Оланде Фредерік, Жюбер Домінік, Паннекан Жюлі, Будієр Лор
Формула / Реферат
1. Моноклональне антитіло до лПГ, яке специфічно зв'язує С-термінальну ділянку прогастрину людини (лПГ), де вказане антитіло отримується з використанням імуногена, який включає пептидний антиген, що містить амінокислотну послідовність, яка відповідає SEQ ID NO: 27.
2. Моноклональне антитіло за п. 1, яке відрізняється тим, що конкурує за зв'язування лПГ з контрольним моноклональним антитілом до лПГ, одержуваним з гібридоми, вибраної з групи, що включає 1B4A11D11, яку зареєстровано під № CNCM 1-4371, 1B6A11F2, яку зареєстровано під № CNCM 1-4372, 1В11Е4В11, яку зареєстровано під № CNCM 1-4373, 2В4С8С8, яку зареєстровано під № CNCM I-4374, та 2B11E6G4, яку зареєстровано під № CNCM 1-4375.
3. Моноклональне антитіло за будь-яким з пп. 1, 2, яке відрізняється тим, що містить гіперваріабельні ділянки VH і VL, що містять послідовності, які вибирають з однієї з наступних груп послідосностей гіперваріабельних ділянок VH і VL:
(і) VH CDR1 з SEQ ID NO: 37, VH CDR2 з SEQ ID NO: 41, VH CDR3 з SEQ ID NO: 45, VL CDR1 з SEQ ID NO: 49, VL CDR2 з SEQ ID NO: 52 і VL CDR3 з SEQ ID NO: 55;
і
(іі) VH CDR1 3 SEQ ID NO: 38, VH CDR2 з SEQ ID NO: 42, VH CDR3 з SEQ ID NO: 46, VL CDR1 з SEQ ID NO: 50, VL CDR2 з SEQ ID NO: 53 і VL CDR3 з SEQ ID NO: 56.
4. Моноклональне антитіло за будь-яким з пп. 1-3, яке відрізняється тим, що є гуманізованим.
5. Моноклональне антитіло за п. 4, яке відрізняється тим, що містить ланцюги VH і VL, що містять послідовності, вибрані з однієї з наступних груп послідовностей VH і VL:
(і) VH з SEQ ID NO: 75 і VL з SEQ ID NO: 76;
(іі) VH з SEQ ID NO: 77 і VL з SEQ ID NO: 78;
(ііі) VH з SEQ ID NO: 79 і VL з SEQ ID NO: 76;
(iv) VH з SEQ ID NO: 80 і VL з SEQ ID NO: 81; і
(v) VH з SEQ ID NO: 82 і VL з SEQ ID NO: 83.
6. Моноклональне антитіло за будь-яким з пп. 1-5, яке відрізняється тим, що має спорідненість у діапазоні від приблизно 1 нМ до приблизно 7 нМ.
7. Моноклональне антитіло за будь-яким з пп. 1-6, яке відрізняється тим, що зв'язується з епітопом, який містить амінокислотну послідовність, яка відповідає послідовності, вибраній з групи, яка включає SEQ ID NO: 33, 34, 35 і 36.
8. Моноклональне антитіло за будь-яким з пп. 1-7, яке відрізняється тим, що конкурує за зв'язування лПГ з контрольним антитілом, вибраним з групи, яка включає: mAb5, продуковане гібридомою, яку депоновано під № CNCM 1-4371, mAb6, продуковане гібридомою, яку депоновано під № CNCM 1-4372, mAb7, продуковане гібридомою, яку депоновано під № CNCM 1-4373, mAb11, продуковане гібридомою, яку депоновано під № CNCM 1-4374, mAb12, продуковане гібридомою, яку депоновано під № CNCM 1-4375.
9. Моноклональне антитіло за будь-яким з пп. 1-8, яке відрізняється тим, що вказані лінії клітин колоректального раку являють собою LS174T клітини.
10. Композиція, яка містить моноклональне антитіло за будь-яким з пп. 1-9 і допоміжну речовину, носій і/або розчинник.
11. Композиція за п. 10, яка відрізняється тим, що її рецептура приготована для фармацевтичного застосування.
12. Полінуклеотид, що кодує варіабельний легкий ланцюг (VL) для моноклонального антитіла до лПГ, вказаного в будь-якому з пп. 1-9.
13. Полінуклеотид, що кодує варіабельний важкий ланцюг (VH) для моноклонального антитіла до лПГ, вказаного в будь-якому з пп. 1-9.
14. Експресійний вектор, який містить полінуклеотид, що кодує варіабельний легкий ланцюг (VL) для моноклонального антитіла до лПГ, вказаного в будь-якому з пп. 1-9.
15. Експресійний вектор, який містить полінуклеотид, що кодує варіабельний важкий ланцюг (VH) для моноклонального антитіла до лПГ, вказаного в будь-якому з пп. 1-9.
16. Клітина-господар, трансформована парами полінуклеотидів, які підходять для експресії моноклонального антитіла до лПГ, вказаного в будь-якому з пп. 1-9.
17. Гібридома, здатна секретувати моноклональне антитіло до лПГ, вказане в будь-якому з пп. 1-9.
18. Гібридома за п. 17, яка відрізняється тим, що вибрана з групи, що включає: 1B4A11D11, яку зареєстровано під № CNCM 1-4371, 1B6A11F2, яку зареєстровано під № CNCM 1-4372, 1В11Е4В11, яку зареєстровано під № CNCM I-4373, 2В4С8С8, яку зареєстровано під № CNCM 1-4374, 2B11E6G4, яку зареєстровано під № CNCM 1-4375.
19. Спосіб отримання моноклонального антитіла до лПГ, що включає:
(а) культивування гібридоми, вказаної у п. 18, у відповідних умовах; і
(б) відновлення моноклонального антитіла до лПГ з культурального середовища або клітин гібридоми.
20. Застосування моноклонального антитіла до лПГ, вказаного в будь-якому з пп. 1-9, у виготовленні лікарського засобу для лікування колоректального раку.
21. Спосіб діагностування колоректального раку у суб'єкта, який полягає у кількісному визначенні рівня прогастрину у пробі сироватки, взятої у суб'єкта, використовуючи щонайменше одне моноклональне антитіло, вказане у будь-якому з пп. 1-9, в якому кількість прогастрину у діапазоні від 20 до 400 пМ вказує на наявність колоректального раку.
22. Спосіб вибору пацієнта, який підходить для лікування антитілами до лПГ, що полягає у кількісному визначенні рівня прогастрину у пробі сироватки, взятої у хворого на колоректальний рак, використовуючи щонайменше одне моноклональне антитіло, вказане у будь-якому з пп. 1-9, в якому кількість прогастрину у діапазоні від 20 до 400 пМ вказує на придатність лікування антитілами до лПГ.
23. Спосіб контролю ефективності лікування колоректального раку, який включає кількісне визначення рівня прогастрину у крові суб'єкта, який проходить лікування від колоректального раку, залежно від часу, використовуючи щонайменше одне моноклональне антитіло, вказане у будь-якому з пп. 1-9, в якому залежне від часу зниження рівня прогастрину в сироватці суб'єкта вказує на ефективність лікування.
Текст
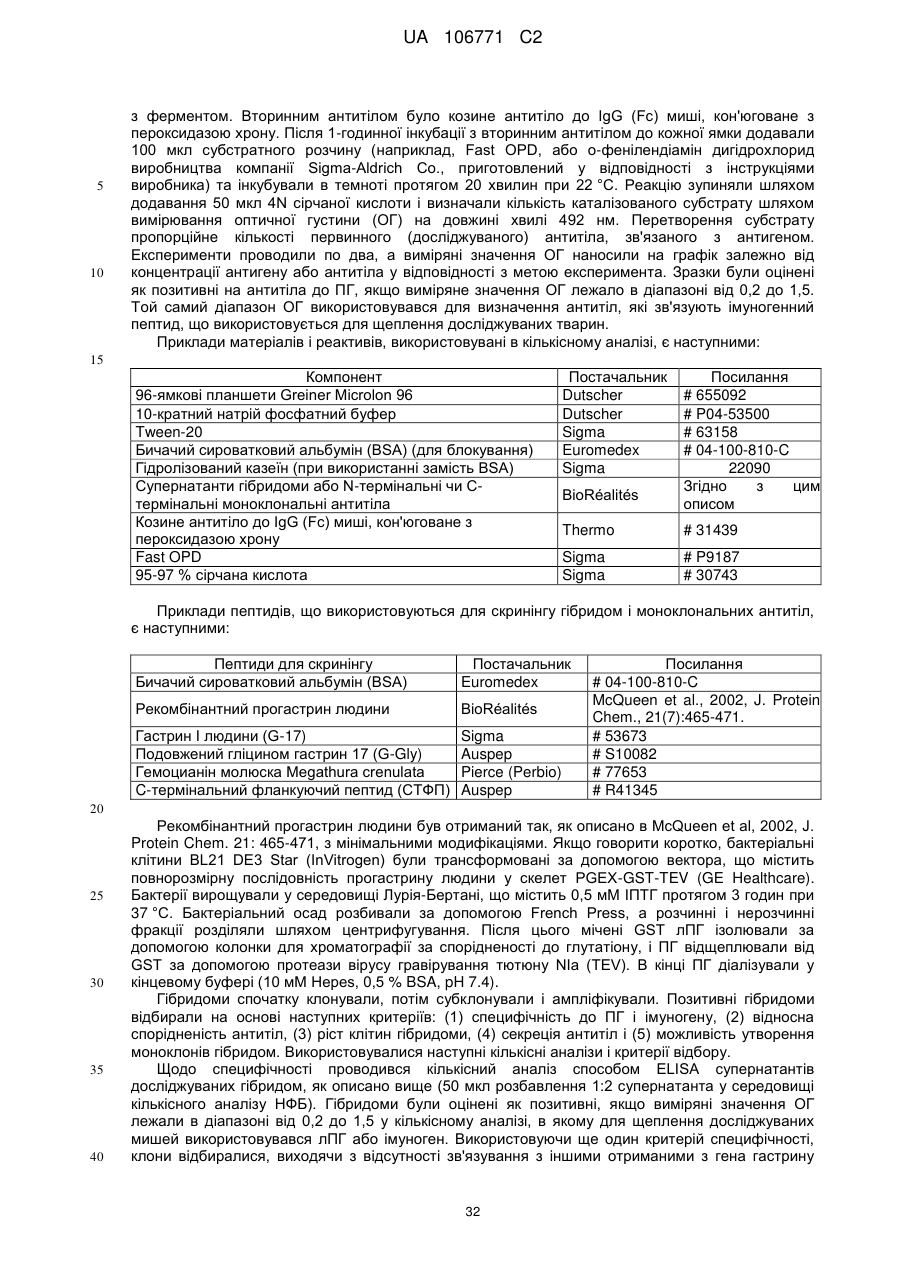
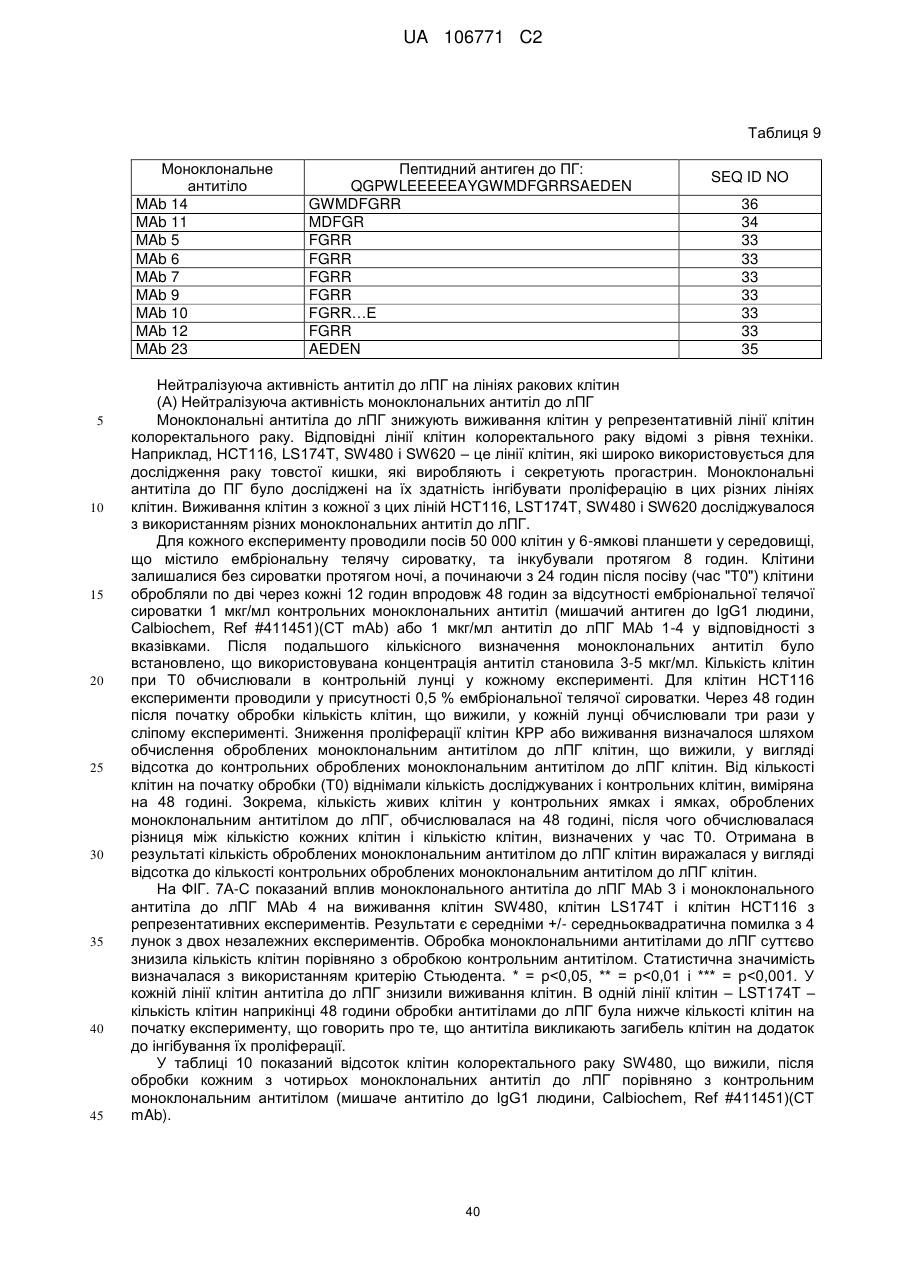
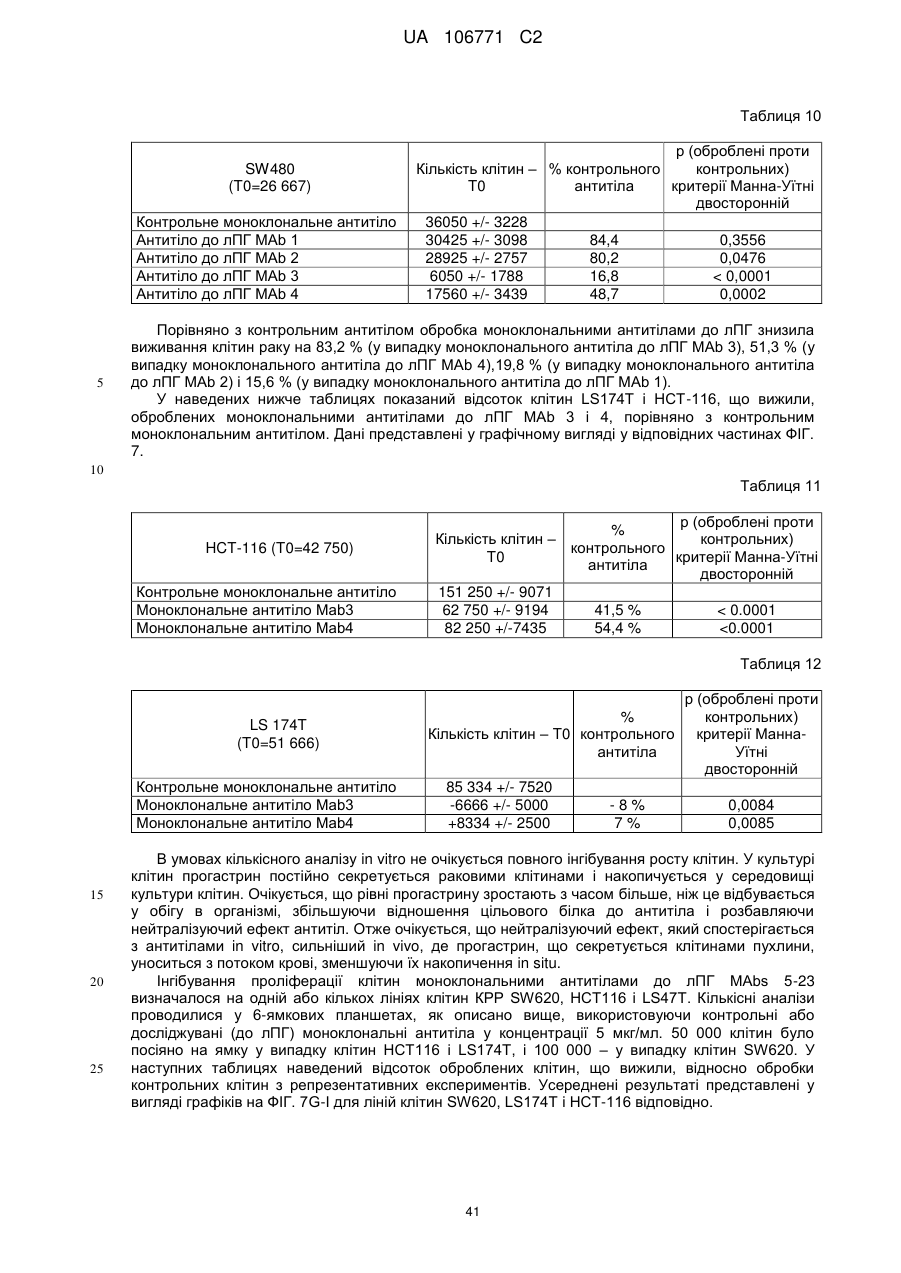
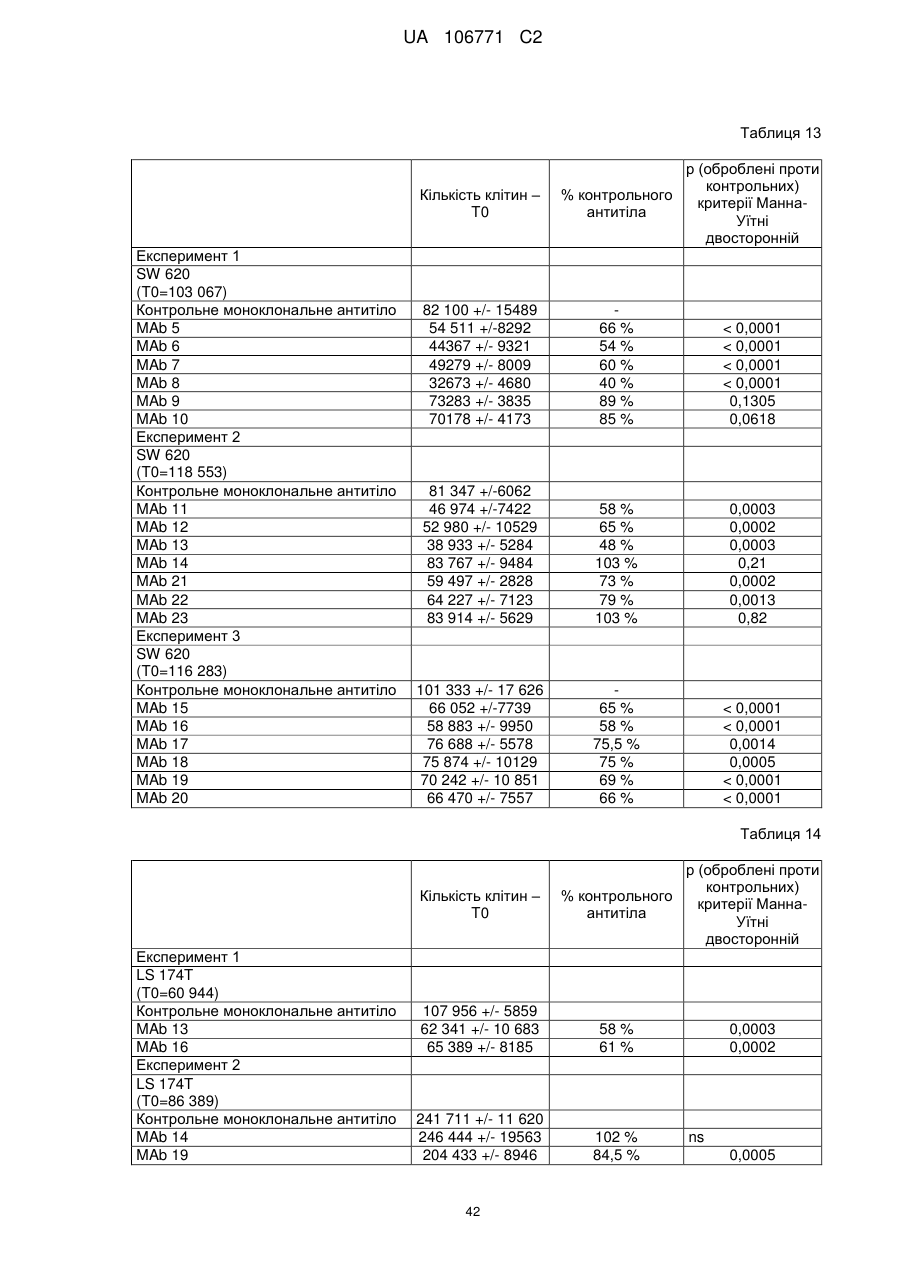
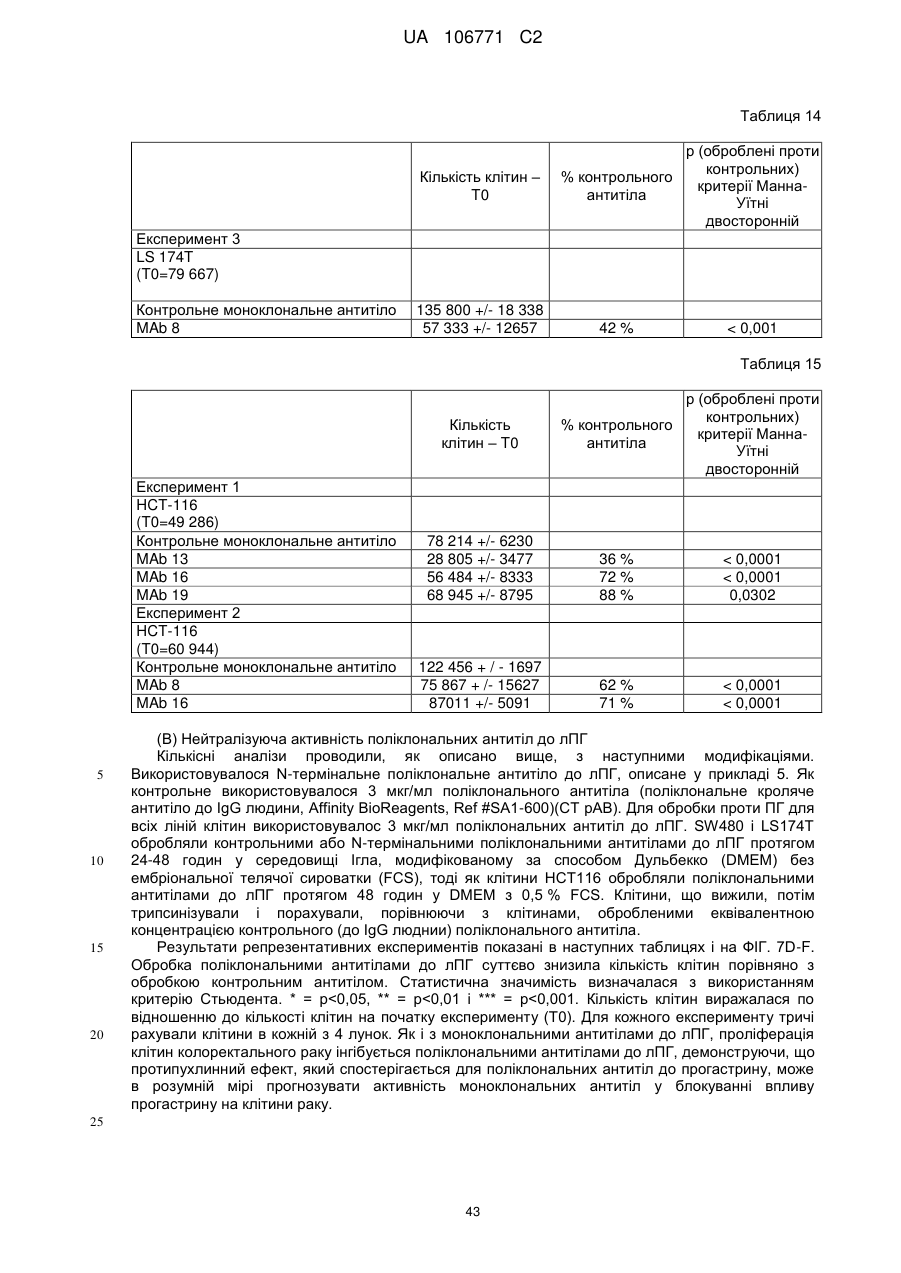
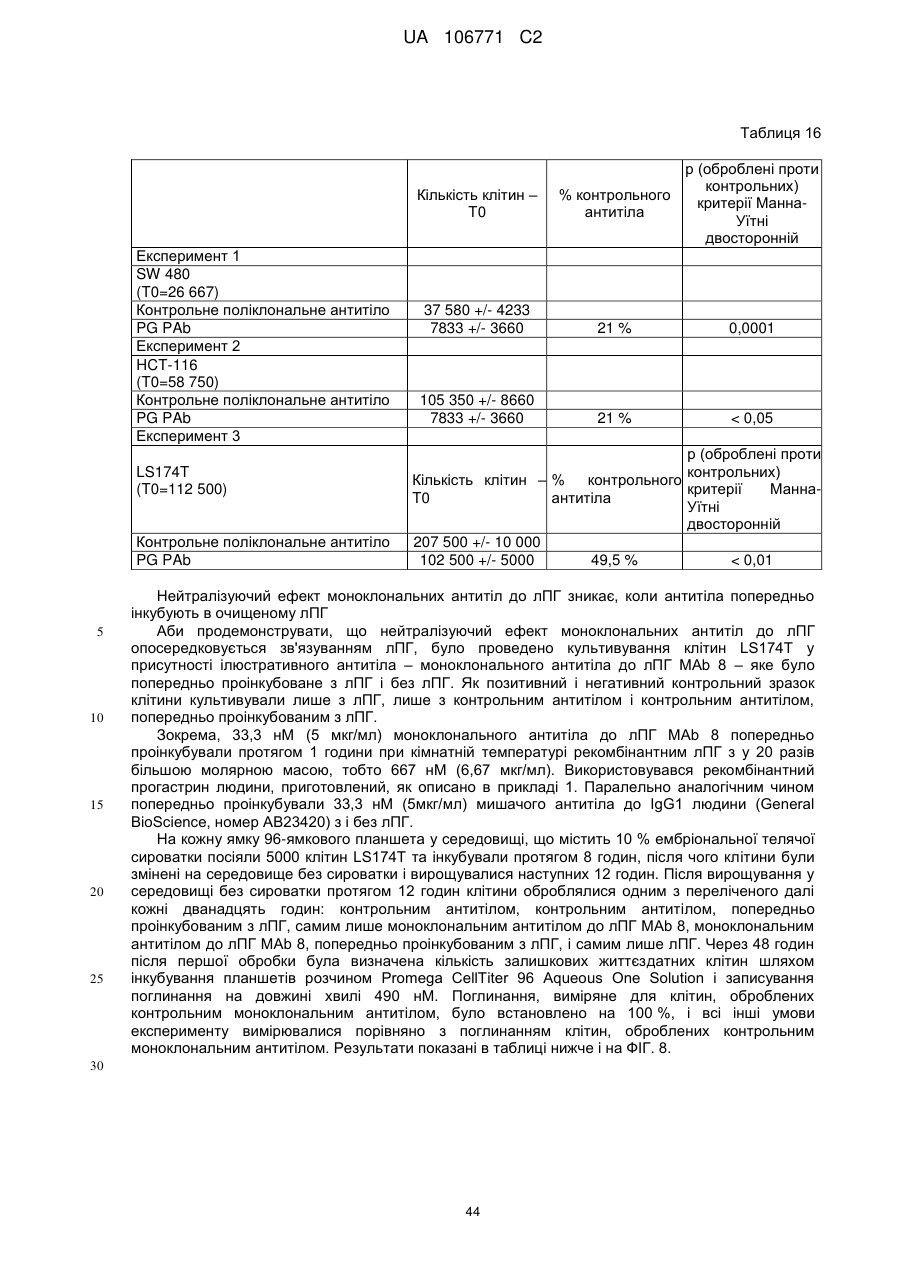
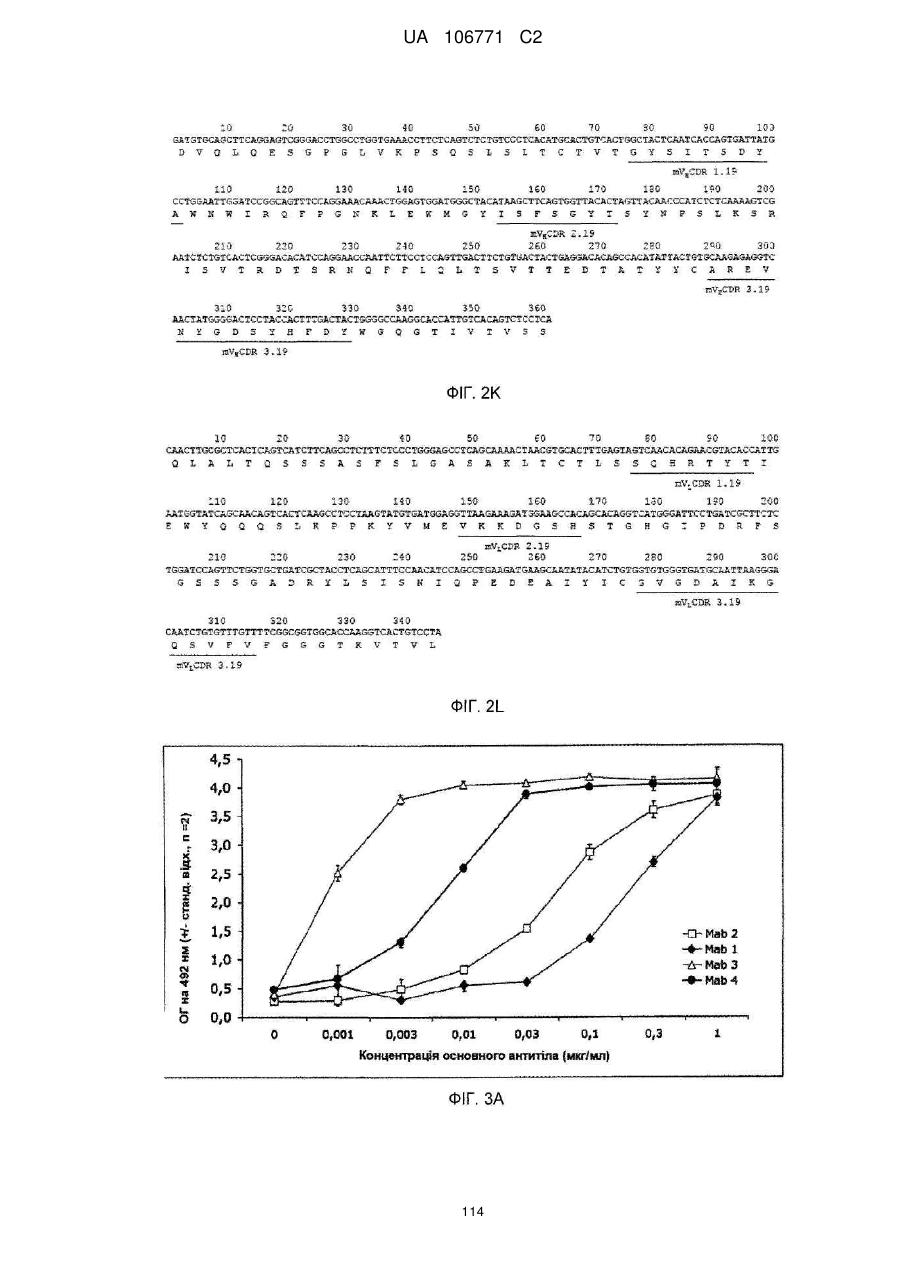
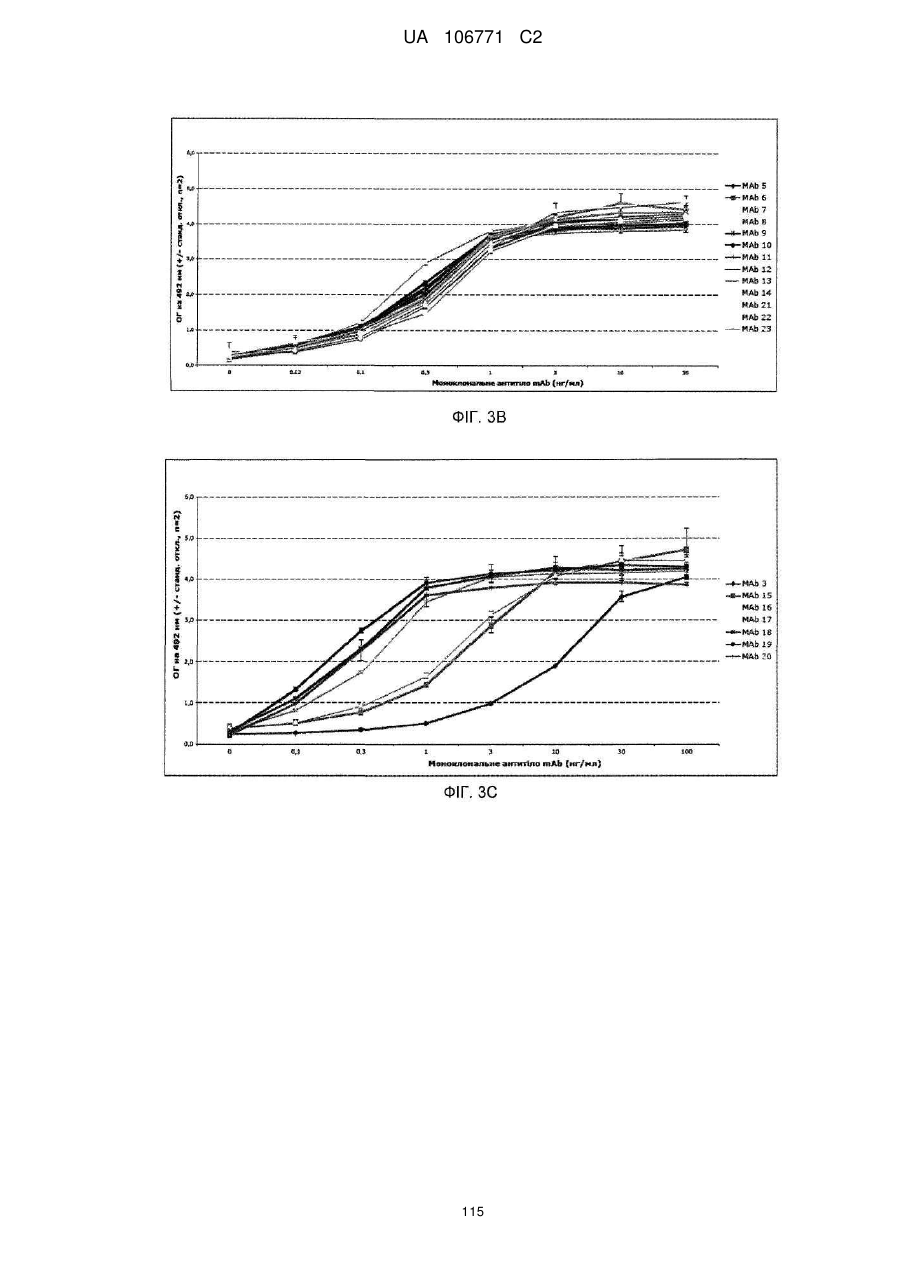
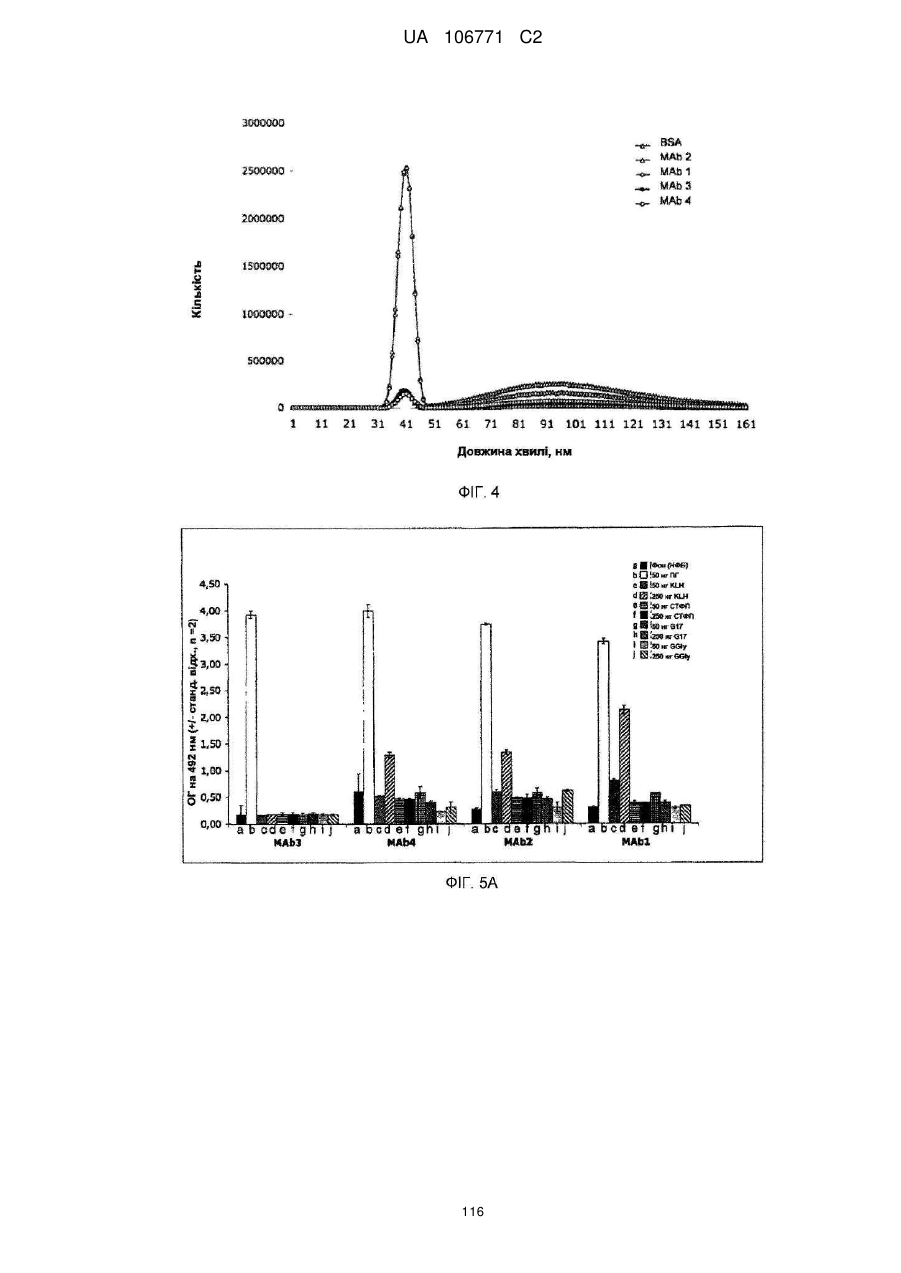
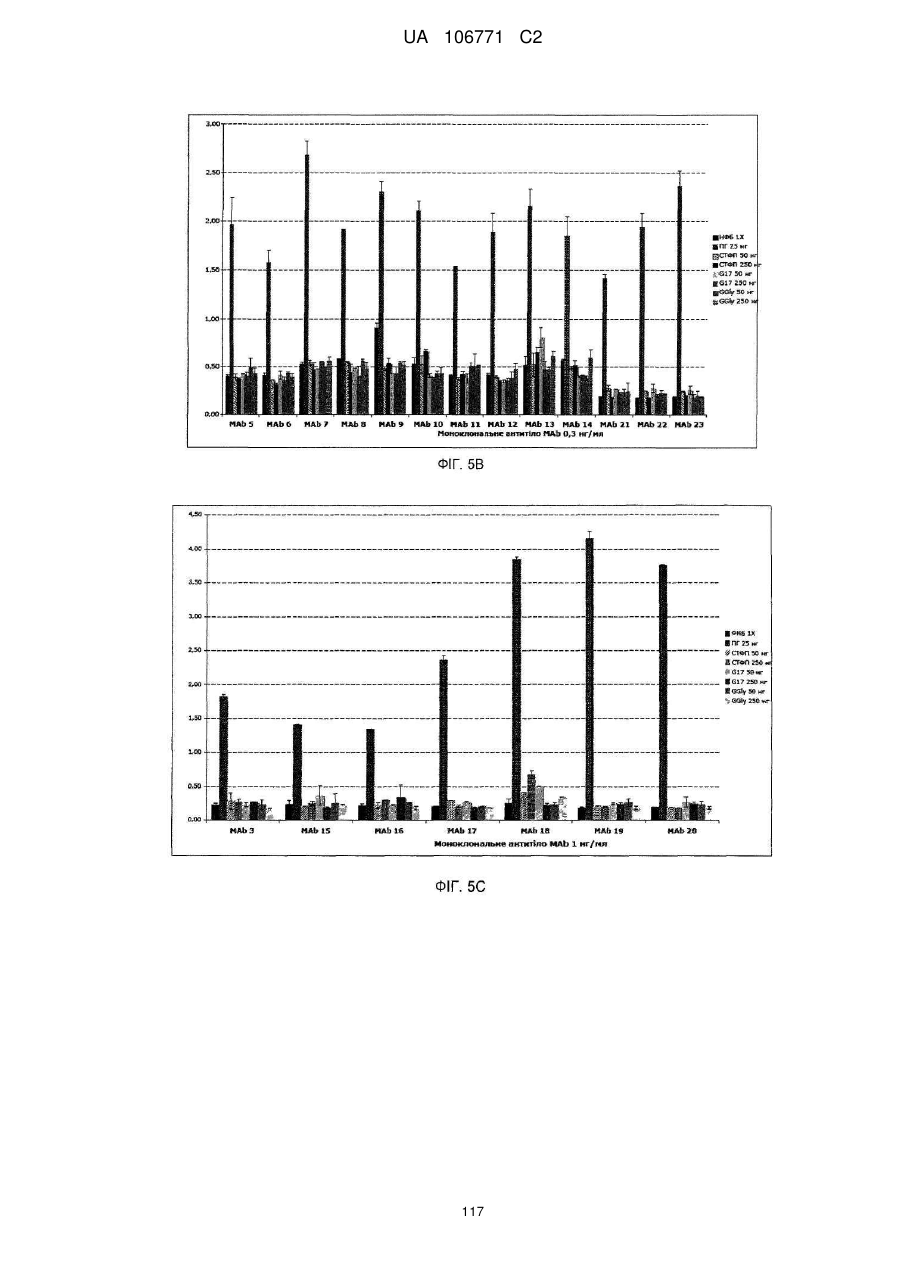
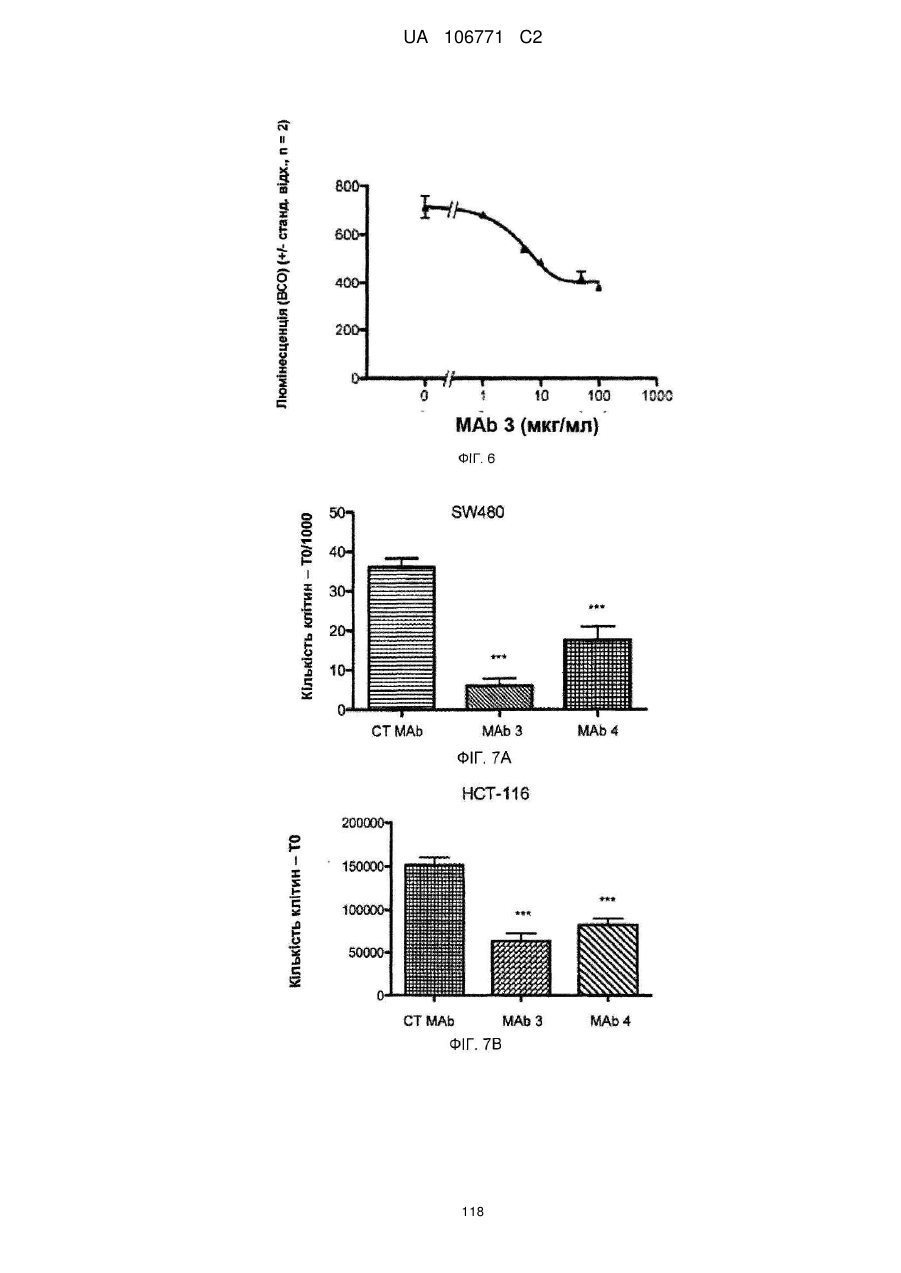
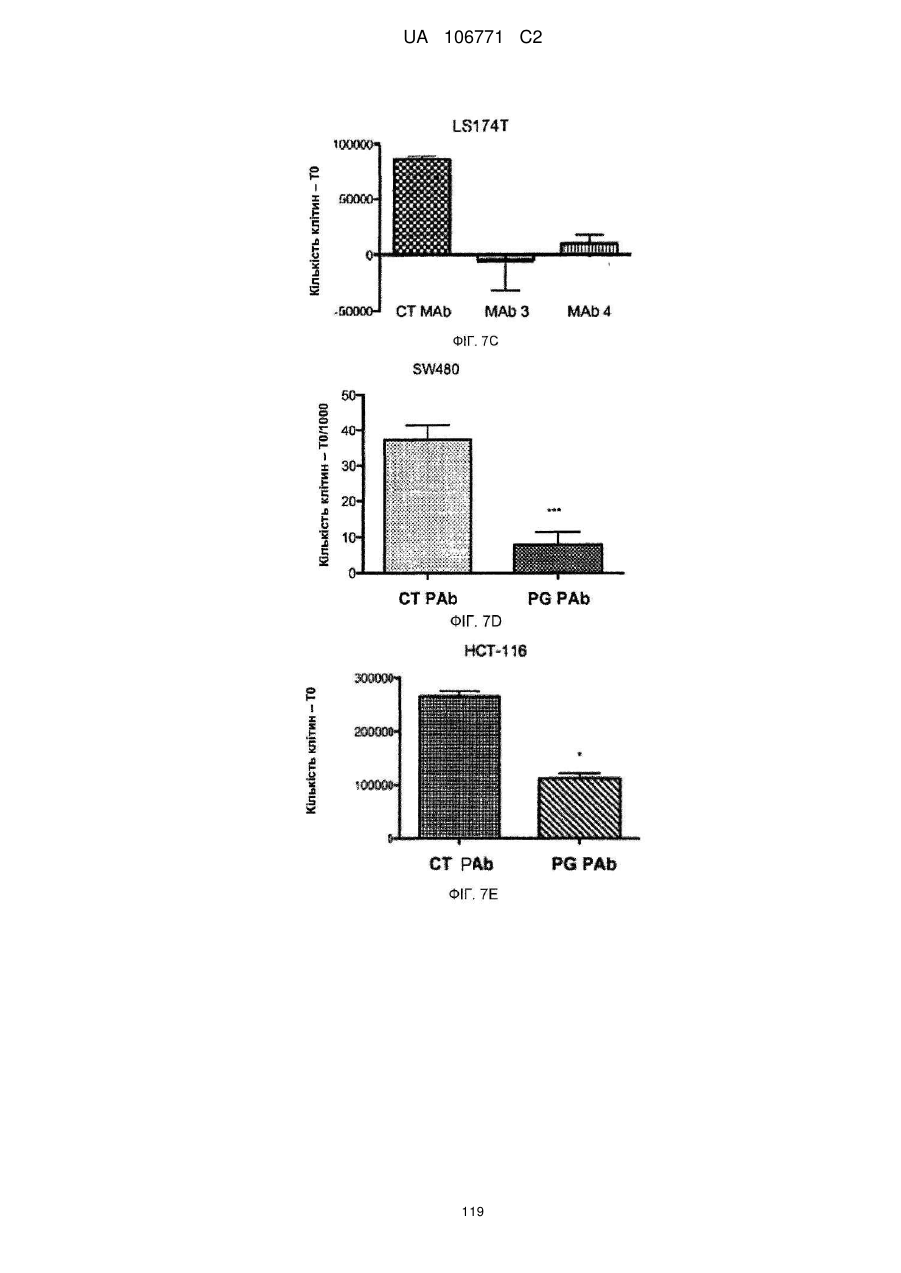
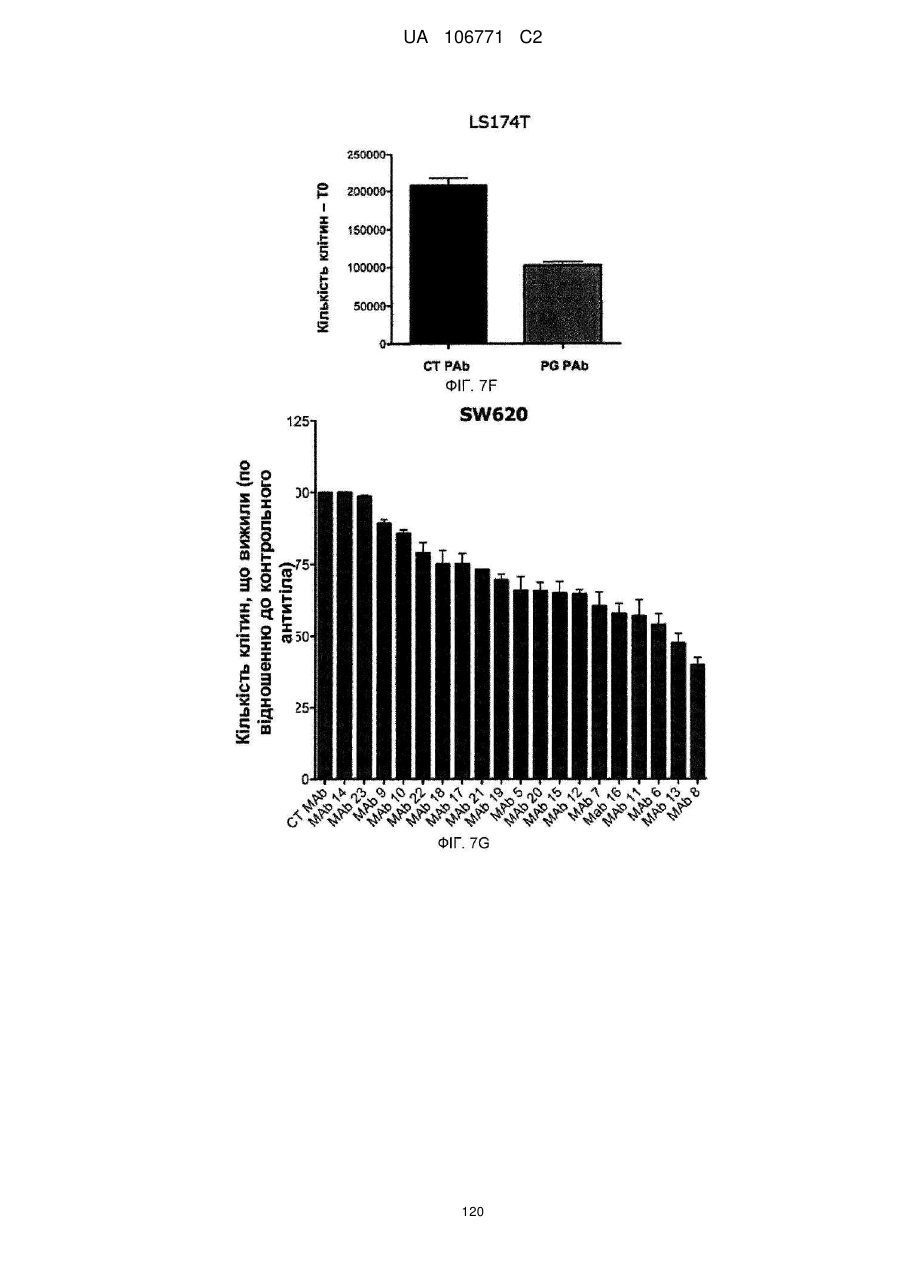
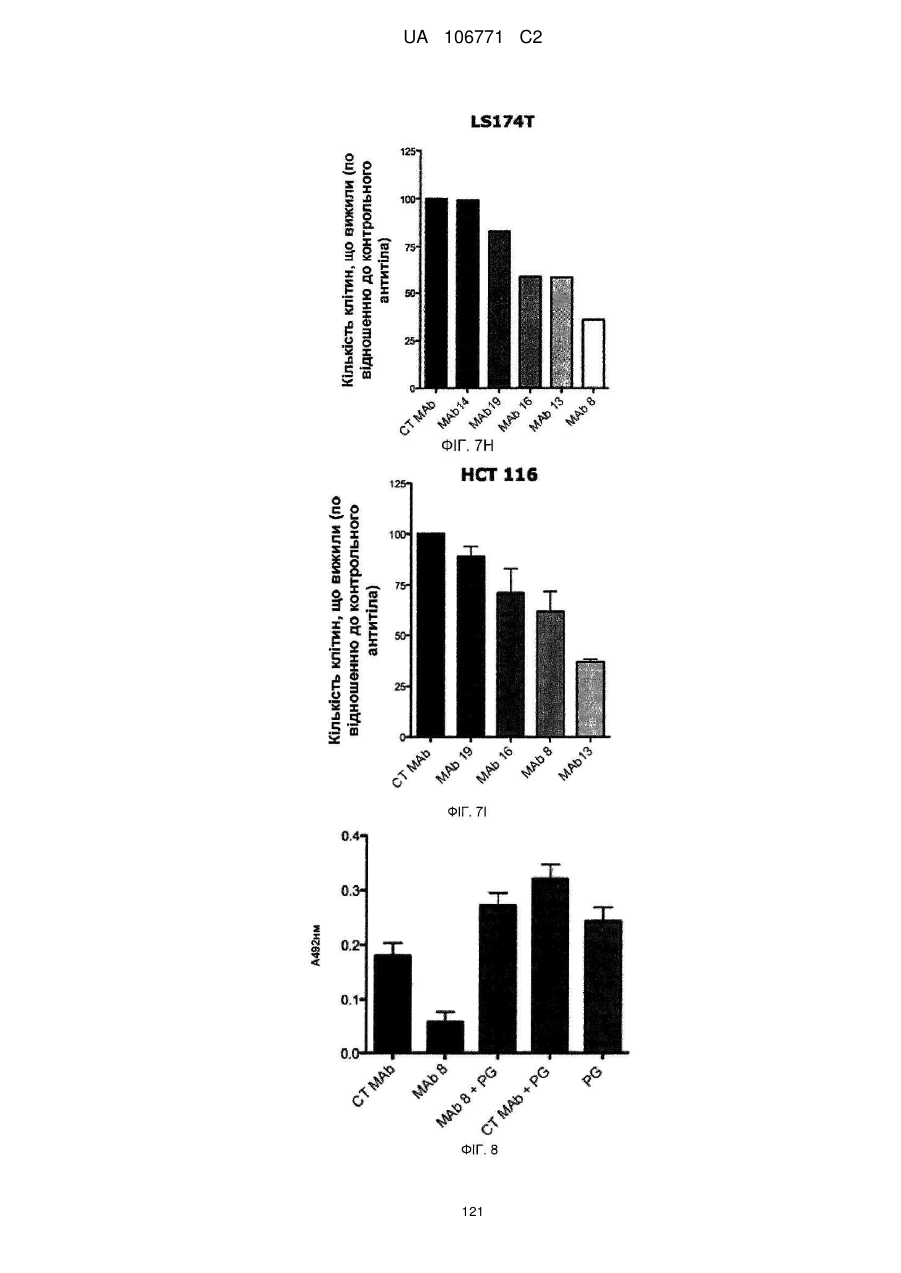
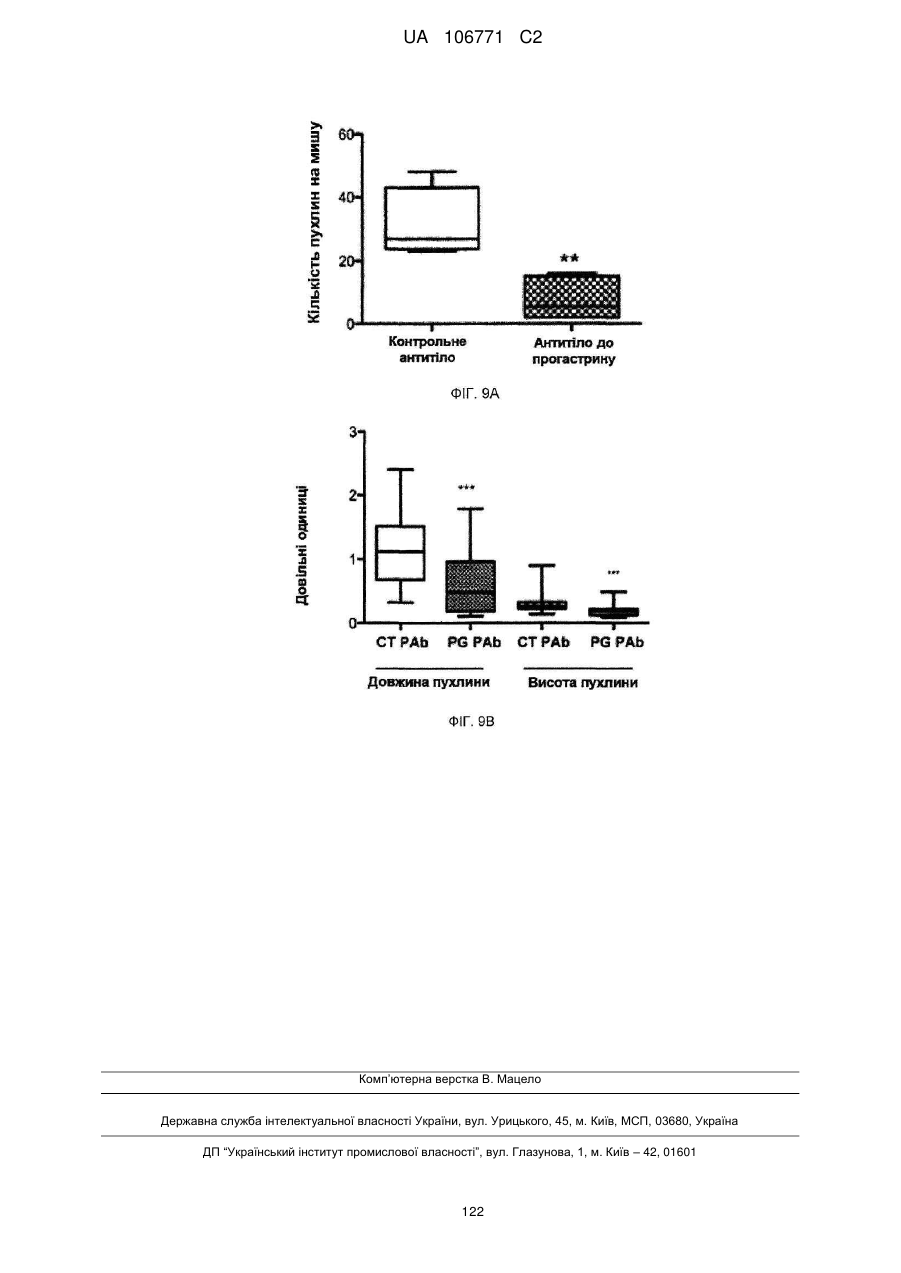
Реферат: UA 106771 C2 (21) Номер заявки: a 2012 05759 (22) Дата подання заявки: 15.10.2010 (24) Дата, з якої є чинними 10.10.2014 UA 106771 C2 Цей опис винаходу стосується моноклональних антитіл до прогастрину, його фрагментів, композицій, які включають моноклональні антитіла до прогастрину, а також способи виготовлення і використання моноклональних антитіл до прогастрину та їх композицій. Цей опис винаходу стосується способів лікування колоректального раку моноклональними антитілами до прогастрину і композиціями, що включають моноклональні антитіла до прогастрину або їх фрагменти. Цей опис винаходу також стосується способів, які включають визначення прогастрину, у тому числі способів діагностування колоректального раку і способів контролю ефективності протиракової терапії у суб'єктів, які страждають колоректальним раком. UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 ПЕРЕХРЕСНЕ ПОСИЛАННЯ НА СПОРІДНЕНІ ЗАЯВКИ Цей винахід заявляє перевагу пріоритету згідно з § 119(e) Розділу 35 Зводу законів США попередньої заявки № 61/252 625, поданої 16 жовтня 2009 року, зміст якої повністю включений в цей опис винаходу шляхом посилання. ЗАЯВА ПРО НАУКОВО-ДОСЛІДНІ РОБОТИ, фінансовані з федерального бюджету Немає. СТОРОНИ ДОГОВОРУ СПІЛЬНИХ ДОСЛІДЖЕНЬ Немає. ПОСИЛАННЯ НА перелік ПОСЛІДОВНОСТЕЙ, ТАБЛИЦЮ АБО КОМП'ЮТЕРНУ ПРОГРАМУ До цього опису додається перелік послідовностей. ГАЛУЗЬ ТЕХНІКИ Цей винахід стосується, серед іншого, моноклональних антитіл до прогастрину, складів і способів створення таких антитіл, способів використання таких антитіл, наприклад, у діагностиці і/або лікуванні колоректального раку. РІВЕНЬ ТЕХНІКИ Колоректальний рак (КРР) – це велика проблема охорони здоров'я, яка вражає 1 000 000 осіб щорічно і є причиною більше 500 000 смертей кожен рік. КРР – це друга основна причина смерті через рак. Лише у Сполучених Штатах у 2009 році повідомлялося приблизно про 147 000 нових випадків і більше 49 900 смертей через КРР. Існує три форми КРР: спорадичний КРР; спадковий неполіпозний колоректальний рак (СНПКРР), спричинений генеративною мутацією у генах репарації помилок спарювання основ ДНК; сімейний аденоматозний поліпоз (САП) через генеративну мутацію в гені APC. Спорадичний КРР трапляється приблизно у 85 % випадків, тоді як СНПКРР десь у 5 %, а САП – близько 1 % (Heyer et al., 1999, Oncogene 18:5325-5333). Клінічне лікування КРР зазвичай включає хірургічну резекцію пухлин, яка часто супроводжується хіміотерапією. На сьогоднішній день приблизно 50 % хворих на КРР помирають впродовж п'яти років після діагностування. Відсутність надійних скринінг-тестів та неефективність існуючих видів лікування – це основні причини високої смертності. Існує нагальна потреба у нових клінічних підходах до діагностування КРР, а також видах лікування, ефективних проти пухлин колоректального раку, що мають мінімальний несприятливий вплив на здорові тканини. СУТНІСТЬ ВИНАХОДУ У цьому описі представлені склади і способи, корисні для діагностування і/або лікування колоректального раку (КРР) у тварин, у тому числі у людей. Різні винаходи, описані в заявці, частково базуються на відкритті заявниками моноклональних антитіл, що специфічно зв'язують прогастрин (ПГ), наприклад прогастрин людини (лПГ) – поліпептид, який виробляється клітинами пухлини КРР, і що проявляють антипроліферативні властивості на моделях КРР in vitro. Прогастрин виробляється клітинами колоректальної пухлини і вважається, що він стимулює проліферацію цих клітин, запускаючи шлях сигнальної трансдукції, який блокує процеси нормальної диференціації клітин, у тому числі процеси, які призводять до загибелі клітин. Виснаження транскрипту гена гастрину, який кодує прогастрин, індукує диференціацію клітин і запрограмовану загибель клітин пухлини на моделях КРР in vitro і in vivo, що знижує проліферацію клітин пухлини. Без прив'язування до будь-якої методики використання вважається, що антитіла до лПГ шляхом зв'язування ПГ блокують або інгібують його здатність до взаємодії зі своїм(и) сигнальним(и) партнером(ами). Це, у свою чергу, інгібує шлях сигнальної трансдукції у клітинах колоректальної пухлини, який інакше призвів би до проліферації. Відповідно, в одному аспекті у цьому описі представлені моноклональні антитіла, які специфічно зв'язують ПГ, наприклад, лПГ, і не зв'язують інші продукти гена гастрину. Як показано на ФІГ. 1, ген гастрину транслюється в поліпептид з 101 амінокислотою, який називається пре-прогастрином, що містить сигнальну послідовність (підкреслена), яка розщеплюється, утворюючи прогастрин, тобто поліпептид з 80 амінокислот. Прогастрин у свою чергу розщеплюється, утворюючи продукт з 34 амінокислот, що відповідає залишкам 38-71 прогастрину, який потім подовжується на карбокси-кінці залишком гліцину, генеруючи подовжений гліцином G34 (G34-Gly). Побічним продуктом цього розщеплення є пептид з 5 амінокислотами, що називається С-термінальним фланкуючим пептидом, або СКФП, який включає залишки 75-80 прогастрину. G34-Gly потім далі розщеплюється, утворюючи поліпептид з 17 залишків, що відповідає послідовності залишків 55-71 прогастрину, який називається G17Gly. Видалення С-термінальних гліцинів G34-Gly і G17-Gly, за яким слідує С-термінальне амідування, дає в результаті G34 і G17 відповідно, обидва з яких С-термінально амідовані. 1 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 Таким чином, тоді як перші 37 залишків прогастрину є унікальними для нього (тобто не присутні у його продуктах процесингу, таких як G34, G34-Gly, G17, G17-Gly чи СКФП), залишки 38-80 присутні також у посттрансляційних продуктах гена гастрину. Заявники відкрили, що моноклональні антитіла до ПГ можуть бути вироблені з використанням способів, відомих фахівцям в даній галузі, важливу роль відіграє відбір антигену. Не всі антигени, отримані з лПГ, стимулюють вироблення моноклональних антитіл, що специфічно зв'язують лПГ за фізіологічних умов. Як описано нижче, різні антигени, що використовуються для вироблення поліклональних антитіл до лПГ, такі як повнорозмірний рекомбінантний людський прогастрин (див., напр., Singh WO 08/076454) і пептиди, що відповідають останнім десяти амінокислотам на С-термінальному кінці лПГ (див., напр., Hollande WO 07/135542), не змогли генерувати моноклональних антитіл до лПГ. Однак заявники відкрили антигенні N- і C-термінальні послідовності всередині послідовності лПГ, які можуть використовуватися для генерування моноклональних антитіл, що специфічно зв'язують лПГ. Зовсім несподівано заявники відкрили, що не потрібно обмежувати антигенні послідовності фрагментами послідовності ПГ, що є унікальними для нього, щоб отримати моноклональні антитіла, які специфічно зв'язують ПГ, а не інші отримані з гена гастрину продукти. Пептидні антигени, які мають спільні послідовності з іншими продуктами гена гастрину, наприклад, G17, G34 і СКФП, утворювали моноклональні антитіла, які не лише зв'язують лПГ, але й зв'язують його специфічно. Заявники генерували моноклональні антитіла з використанням антигенів, отриманих з різних ділянок молекули лПГ. Моноклональні антитіла до ПГ, які можна отримати з використанням пептидного антигену, що має послідовність, яка відповідає N-термінальній ділянці лПГ, називаються в цьому описі "N-термінальні моноклональні антитіла до лПГ". Специфічна ілюстративна антигенна ділянка, яка може використовуватися для побудови імуногену, корисного для отримання N-термінальних моноклональних антитіл до ПГ, відповідає залишкам 1-14 лПГ. SWKPRSQQPDAPLG (SEQ ID NO:25). Приклади імуногенів, у тому числі цей антиген, корисний для отримання N-термінальних моноклональних антитіл до ПГ, описані в таблиці 1А і розділі "Приклади". Моноклональні антитіла до ПГ, які можна отримати з використанням пептидного антигену, що має послідовність, яка відповідає C-термінальній ділянці лПГ і/або зв'язують C-термінальну ділянку лПГ, називаються в цьому описі "C-термінальні моноклональні антитіла до лПГ". Специфічна ілюстративна антигенна ділянка, яка може використовуватися для побудови імуногену, корисного для отримання C-термінальних моноклональних антитіл до ПГ, відповідає залишкам 55-80 лПГ. QGPWLEEEEEAYGWMDFG RRSAEDEN (SEQ ID NO:27). Приклади імуногенів, у тому числі цей антиген, корисний для отримання C-термінальних моноклональних антитіл до ПГ, описані в таблиці 1B і розділі "Приклади". Для деяких використань бажано мати моноклональні антитіла до лПГ з високою спорідненістю до лПГ. Для деяких використань, наприклад, терапевтичних цілей, бажано мати спорідненість не менше приблизно 100 нМ, хоча можуть бути бажаними антитіла з більшою спорідненістю, наприклад, спорідненістю не менше приблизно 90 нМ, 80 нМ, 70 нМ, 60 нМ, 50 нМ, 40 нМ, 30 нМ, 25 нМ, 20 нМ, 15 нМ, 10 нМ, 7 нМ, 6 нМ, 5 нМ, 4 нМ, 3 нМ, 2 нМ, 1 нМ, 0,1 нМ, 0,01 нМ або навіть більше. Різні специфічні ілюстративні моноклональні антитіла до ПГ, описані -6 -12 в цьому документі, демонструють спорідненість в діапазоні від 10 до 10 М (див. таблицю 6). Моноклональне антитіло до ПГ, що має спорідненість, яка особливо добре підходить для конкретного бажаного застосування, можна легко відібрати серед них, генерувати або розробити з використанням різних імуногенів, послідовностей ділянки, що визначає компліментарність (гіперваріабельної ділянки - CDR), послідовностей варіабельної частини важкого VH і варіабельної частини легкого VL ланцюга, а також описаних тут способів. Спорідненість будь-якого конкретного моноклонального антитіла до ПГ можна визначати з використанням способів, добре відомих в даній галузі або описаних в цьому документі, таких як, наприклад, ELISA (твердофазний імуноферментний аналіз), ізотермічна титраційна калориметрія (ІТК), BIAcore або флуоресцентний поляризаційний імуноаналіз. лПГ – це відносно малий поліпептид, який має в довжину лише 80 амінокислот. Можна було б очікувати, що будь-яке моноклональне антитіло, яке специфічно зв'язує лПГ з відносно високою спорідненістю (наприклад, не менше приблизно 10 нМ) вплине на здатність ПГ взаємодіяти з його сигнальним(и) партнером(ами), а отже й інгібує проліферацію клітин КРР. Однак заявники відкрили, що не всі моноклональні антитіла до ПГ мають нейтралізуючу дію (тобто не всі моноклональні антитіла, що зв'язують ПГ, інгібують або впливають на його біологічну сигнальну активність). Справді, як буде детальніше описано в розділі "Приклади", заявники відкрили, що деякі моноклональні антитіла до ПГ, незважаючи на те, що вони 2 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 проявляють високу специфічність і високу спорідненість до ПГ, не нейтралізують ПГ. Наприклад, антитіло до лПГ MAb14 зв'язує лПГ з KD, який дорівнює приблизно 6 пМ, однак не інгібує росту клітин КРР in vitro, як описано нижче в розділі "Приклади". Тоді як ненейтралізуючі моноклональні антитіла, які специфічно зв'язують лПГ, корисні для діагностичних цілей, ті моноклональні антитіла до лПГ, які нейтралізують ПГ, особливо добре підходять для терапевтичних цілей для лікування КРР. Використовуваний в цьому описі термін "нейтралізуюче моноклональне антитіло до лПГ" – це моноклональне антитіло до лПГ, яке забезпечує суттєве зниження кількості живих клітин КРР у випробуваному зразку, обробленому моноклональних антитілом до лПГ, порівняно з контрольним зразком, обробленим неспецифічним моноклональним антитілом. Конкретний кількісний аналіз для оцінки здатності будь-якого конкретного моноклонального антитіла до лПГ нейтралізувати лПГ описаний в розділі "Детальний опис винаходу" нижче. Ті моноклональні антитіла до лПГ, які демонструють не менше приблизно 50 % зниження кількості живих клітин у цьому кількісному аналізі, вважаються особливо корисними у лікуванні КРР, хоча очікується, що моноклональні антитіла до лПГ, які демонструють менші рівні нейтралізуючої активності, наприклад, статистично значне зниження на 40 %, 30 %, 20 %, 15 % або навіть 10 % кількості живих клітин у цьому кількісному аналізі, також мають сприятливий терапевтичний ефект. Відповідно, у деяких варіантах здійснення винаходу моноклональні антитіла до ПГ є нейтралізуючими моноклональними антитілами до ПГ. Було відкрито, що здатність моноклонального антитіла до ПГ нейтралізувати ПГ не залежить від епітопу. Як показано у розділі "Приклади", як N-термінальні, так і C-термінальні антитіла до ПГ мають нейтралізуючу активність. Отже, у деяких варіантах здійснення винаходу нейтралізуючі моноклональні антитіла до ПГ є N-термінальними нейтралізуючими антитілами, в інших варіантах здійснення винаходу моноклональні антитіла до ПГ є C-термінальними нейтралізуючими антитілами. Картування епітопів показує, що не всі N-термінальні моноклональні антитіла до ПГ зв'язують один і той самий епітоп, навіть при виробленні проти одного і того ж імуногену. Те ж стосується C-термінальних моноклональних антитіл до лПГ. Епітопи, що зв'язуються з ілюстративними N-термінальними і C-термінальними моноклональними антитілами до лПГ, що визначається шляхом сканування аланіном і за допомогою SPOT-тесту, наведені в розділі "Приклади", в таблицях 8 і 9. У деяких варіантах здійснення винаходу моноклональні антитіла до лПГ зв'язують епітоп, у тому числі амінокислотну послідовність, що відповідає N-термінальній ділянці лПГ. У конкретних варіантах здійснення винаходу N-термінальні моноклональні антитіла до лПГ зв'язують епітоп, що включає залишки 10-14 лПГ (SEQ ID NO:28), залишки 9-14 лПГ (SEQ ID NO:29), залишки 410 лПГ (SEQ ID NO:30), залишки 2-10 лПГ (SEQ ID NO:31) або залишки 2-14 лПГ (SEQ ID NO:32). У деяких варіантах здійснення винаходу моноклональні антитіла до лПГ зв'язують епітоп, у тому числі амінокислотну послідовність, що відповідає C-термінальній ділянці лПГ. У конкретних варіантах здійснення винаходу C-термінальні моноклональні антитіла до лПГ зв'язують епітоп, що включає залишки 71-74 лПГ (SEQ ID NO:33), залишки 69-73 лПГ (SEQ ID NO:34), залишки 76-80 лПГ (SEQ ID NO:35) або залишки 67-74 лПГ (SEQ ID NO:36). Очікується, що відповідні гіперваріабельні ділянки і/або ланцюги V H і VL моноклональних антитіл до лПГ, які зв'язують приблизно ті ж епітопи, можуть бути взаємозамінними для вироблення нових моноклональних антитіл до лПГ. Наприклад, як зазначено в таблиці 9, ілюстративні моноклональні антитіла до лПГ MAb 5 і MAb 6 зв'язують один і той самий епітоп. Може бути розроблене моноклональне антитіло до лПГ, що включає у своєму ланцюгу V L різні комбінації гіперваріабельних ділянок VL цих двох антитіл і/або у своєму ланцюгу V H – різні комбінації гіперваріабельних ділянок VH цих двох антитіл. Як конкретний приклад для ілюстрації різних можливих комбінацій, таке антитіло може включати у своєму ланцюгу V L гіперваріабельні ділянки 1 і 2 MAb 5 (VL CDR1.5 і VL CDR2.5 відповідно) і гіперваріабельну ділянку 3 MAb 6 (V L CDR3.6), а у своєму ланцюгу VH – гіперваріабельну ділянку 1 MAb 6 (VH CDR1.6) і гіперваріабельні ділянки 2 і 3 MAb 5 (VH CDR2.5 і VH CDR3.5 відповідно). Було виявлено кілька моноклональних антитіл до лПГ, які мають високу специфічність і спорідненість до лПГ і демонструють високу протипухлинну активність в аналізах in vitro, і у деяких випадках були визначені послідовності їх гіперваріабельних ділянок, послідовності їх ланцюгів VH і VL і/або послідовності запропонованих ланцюгів VH і VL для гуманізованих версій. Були зареєстровані деякі гібридоми. Всі ці ілюстративні моноклональні антитіла до лПГ, а також інші конкретні варіанти здійснення моноклональних антитіл до лПГ, корисні в різних описаних в цьому документі наборах і способах, наприклад, моноклональні антитіла, які конкурують у зв'язуванні ПГ з контрольним антитілом, докладніше описані у розділі "Детальний опис 3 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 винаходу". Моноклональні антитіла до лПГ за цим описом включають антитіла, які конкурують з контрольним моноклональним антитілом до лПГ у зв'язуванні лПГ. Контрольним моноклональним антитілом до лПГ може бути будь-яке з описаних в цьому документі моноклональних антитіл до лПГ. До прикладів, що не мають обмежувального характеру, відносяться: антитіла, що включають три гіперваріабельні ділянки V L і три гіперваріабельні ділянки VH, описані в цьому документі; антитіла, що включають ланцюг V H і ланцюг VL, що мають визначені в цьому документі амінокислотні послідовності; антитіла, що включають визначені в цьому документі гуманізовані поліпептиди важких і легких ланцюгів; антитіла, вироблені з однієї з описаних в цьому документі гібридом; антитіла, які зв'язуються до описаного в цьому документі епітопу в лПГ. Описані в цьому документі моноклональні антитіла до лПГ можуть бути в формі повнорозмірних антитіл, багатоланцюгових і одноланцюгових антитіл, фрагментів таких антитіл, що селективно зв'язують ПГ (у тому числі, зокрема, Fab, Fab', (Fab') 2, Fv і scFv), сурогатних антитіл (у тому числі сурогатних легколанцюгових конструкцій), однодоменних антитіл, гуманізованих антитіл, камелізованих антитіл тощо. Вони також можуть відноситися до будьякого ізотипу або бути отриманими з будь-якого ізотипу, у тому числі, наприклад, IgA (наприклад, IgA1 або IgA2), IgD, IgE, IgG (наприклад, IgG1, IgG2, IgG3 або IgG4) чи IgM. У деяких варіантах здійснення винаходу антитіло до ПГ є IgG (наприклад, IgG1, IgG2, IgG3 або IgG4). Моноклональні антитіла до ПГ можуть бути людського і нелюдського походження. Прикладами антитіл до ПГ нелюдського походження є, зокрема, антитіла, що походять від ссавців (наприклад, мавп, щурів, козлів і кроликів). Краще, аби моноклональні антитіла до ПГ для терапевтичного використання у людей були гуманізовані. В іншому аспекті у цьому описі наводяться нуклеїнові кислоти, які можуть використовуватися для вироблення моноклональних антитіл до ПГ. Наведені нуклеїнові кислоти, які кодують легкі і важкі поліпептидні ланцюги імуноглобуліну для моноклональних антитіл до лПГ, що описані в цьому документі, і вектори, які включають нуклеїнові кислоти. Крім того, наведені клітини-господарі прокаріотів і еукаріотів, трансформовані такими векторами, а також клітини-господарі еукаріотів, наприклад, ссавців, розроблені для експресії легких і важких поліпептидних ланцюгів моноклональних антитіл до лПГ. Наведені також клітини-господарі, здатні експресувати легкі і важкі ланцюги і секретувати моноклональні антитіла, описані в цьому документі, у середовище, в якому вирощуються клітини-господарі. У деяких варіантах здійснення винаходу клітина-господар – це гібридома. Наведені також способи вироблення моноклональних антитіл до лПГ шляхом вирощування клітин-господарів. Нейтралізуючі моноклональні антитіла до ПГ, такі як моноклональні антитіла до лПГ, зв'язують ПГ і блокують залежну від ПГ передачу сигналу, що призводить до інгібування індукованих ПГ відповідей у клітинах пухлини КРР. Відповідно також наведені способи інгібування індукованих ПГ відповідей клітин КРР, що включає пригнічення диференціації клітин, пригнічення загибелі клітин і/або стимуляцію проліферації клітин. Загалом спосіб включає контактування клітини КРР з нейтралізуючим моноклональним антитілом до ПГ або піддання клітинної популяції впливу нейтралізуючого моноклонального антитіла до ПГ, у кількості, яка здатна інгібувати одну або більше індукованих ПГ відповідей клітин КРР. Цей спосіб може бути реалізований in vitro або in vivo шляхом введення нейтралізуючого моноклонального антитіла до лПГ у середовище, що містить клітини КРР, яким може бути клітинна культура або пухлина. Описані в цьому документі нейтралізуючі моноклональні антитіла до ПГ інгібують залежну від ПГ проліферацію клітин пухлини КРР, що робить їх корисними терапевтичними засобами для лікування колоректального раку. Відповідно також наведені фармацевтичні композиції, які включають нейтралізуюче моноклональне антитіло до ПГ, і способи використання моноклональних антитіл до ПГ і/або фармацевтичних композицій для лікування КРР. Рецептура фармацевтичних композицій може бути приготована для будь-якого зручного шляху введення, у тому числі для парентеральної, підшкірної або внутрішньовенної ін'єкції, і зазвичай включає нейтралізуюче моноклональне антитіло до лПГ, один або більше прийнятних носіїв, допоміжних речовин і/або розчинник, що підходять для бажаного способу введення, і може включати інші необов'язкові компоненти, які будуть описані далі у розділі "Детальний опис винаходу". Для терапевтичного використання препарати можна розфасувати в одиночні лікарські форми для спрощення застосування. До способів лікування загалом відносяться введення суб'єкту, якому потрібне лікування, наприклад, суб'єкту, у якого діагностовано КРР, такої кількості нейтралізуючого моноклонального антитіла до ПГ і/або його фармацевтичної композиції, що здатна забезпечити 4 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 сприятливий терапевтичний ефект. Сприятливим терапевтичним ефектом, який детальніше описується нижче, вважається будь-яке покращення КРР, наприклад, сповільнення або зупинка прогресування КРР, зниження тяжкості КРР, інгібування росту пухлин КРР або проліферації клітин КРР, зниження розміру пухлин КРР і/або зниження рівнів ПГ у сироватці крові хворих на КРР. Суб'єктом може бути людина або не людина, у тому числі приручена тварина (наприклад, кішка, собака, корова, свиня, кінь) або неприручена тварина. Краще, щоб моноклональне антитіло до ПГ було специфічним до ПГ видів, яких лікують. Наприклад, антитіло до лПГ вводять людині, антитіло до ПГ собаки вводять собаці і т.д. Терапія за допомогою моноклональних антитіл до лПГ може бути корисною для наступних суб'єктів: пацієнти на будьякій стадії прогресування хвороби (наприклад, на стадії КРР 0, I, II, III або IV), пацієнти, які проходили лікування від КРР (наприклад, хіміотерапію, променеву терапію, хірургічну резекцію) або пацієнти, які проходять інше лікування від КРР. Лікування за допомогою описаних в цьому документі моноклональних антитіл до ПГ може комбінуватися з іншою терапією або бути додатковим до іншої терапії. До прикладів інших видів лікування КРР, що не мають обмежувального характеру, відносяться хіміотерапія, променева терапія, хірургічна резекція та лікування антитілами, що описані в цьому документі. У конкретному прикладі моноклональні антитіла до лПГ вводять в комбінації з хіміотерапевтичними речовинами. В іншому конкретному прикладі моноклональні антитіла до лПГ вводять на додаток до хірургічної резекції. Моноклональні антитіла до ПГ можуть також використовуватися у комбінації один з одним. У індивідуумів з пухлинами КРР часто спостерігаються підвищені рівні циркулюючого ПГ (наприклад, у сироватці або плазмі). Відповідно моноклональні антитіла до лПГ можуть використовуватися для виявлення рівнів ПГ для діагностування КРР. Крім того, у пацієнтів, у яких вже був діагностований КРР, моноклональні антитіла до лПГ можуть використовуватися для відбору суб'єктів, які підходять для проходження терапії проти ПГ або контролю ефективності лікування. Як описано в цьому документі, спосіб діагностування колоректального раку у суб'єкта включає визначення того, чи кількість прогастрину у пробі, взятій у суб'єкта, наприклад, у пробі крові або пробі сироватки, що вимірюється з використанням моноклонального антитіла до лПГ згідно з цим описом, перевищує граничний рівень. У конкретному варіанті здійснення винаходу граничний рівень становить 50 пМ. У деяких варіантах здійснення винаходу використовується два антитіла до ПГ, один з яких розпізнає Cтермінальну ділянку ПГ, а інший –N-термінальну ділянку ПГ. У цьому варіанті здійснення винаходу N-термінальне або C-термінальне антитіло чи обидва ці антитіла є описаним в цьому документі моноклональним антитілом до ПГ. Краще, якщо будуть використовуватися Nтермінальні і C-термінальні моноклональні антитіла до ПГ. Антитіла можуть, однак не обов'язково повинні бути нейтралізуючими. З метою контролю ефективності лікування моноклональні антитіла до ПГ можуть використовуватися для визначення того, чи знижується з часом рівень прогастрину в пробах, взятих у суб'єкта, який проходив або проходить лікування від КРР, шляхом порівняння кількості ПГ у пробах, взятих в різні періоди часу. У цьому кількісному аналізі можуть також використовуватися конкретні варіанти здійснення антитіл до ПГ, описані в попередньому пункті. Наведені також набори, придатні для проведення різних діагностичних, контрольних та інших способів, описаних в цьому документі. До складу таких наборів зазвичай входить моноклональне антитіло до ПГ, описане в цьому документі і, факультативно, додаткові антитіла до ПГ і/або реактиви, що підходять для виконання конкретного кількісного аналізу. У деяких варіантах здійснення винаходу один або більше включених у набір антитіл до ПГ, маркуються міткою, яка може бути виявлена, такою як флуорофор. У конкретному варіанті здійснення винаходу до набору входить антитіло до ПГ, яке специфічно зв'язує N-термінальну ділянку ПГ, антитіло до ПГ, яке специфічно зв'язує C-термінальну ділянку ПГ, і факультативно – реактиви, що підходять для проведення діагностичного кількісного аналізу, в якому N-термінальним специфічним антитілом є N-термінальне моноклональне антитіло до ПГ, описане в цьому документі, і/або C-термінальним специфічним антитілом є C-термінальним моноклональним антитілом до ПГ, описаним в цьому документі. Характерні особливості і переваги різних винаходів, описаних в цьому документі, стануть очевиднішими з наступного докладного опису ілюстративних варіантів здійснення винаходу. КОРОТКИЙ ОПИС ФІГУР На ФІГ. 1 наведені амінокислотні послідовності пре-прогастрину, прогастрину і продуктів процесингу прогастрину, у тому числі G34, G34-Gly, G17, G17-Gly і C-термінального фланкуючого пептиду, СТФП. На ФІГ. 2 наведено поліпептид і відповідний полінуклеотид, послідовності ланцюгів V H і VL 5 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 для ілюстративних мишачих моноклональних антитіл до лПГ: антитіло до лПГ MAb 3 (SEQ ID NOS 16, 12, 17 і 13 відповідно, у порядку появи) (ФІГ. 2A, 2B), антитіло до лПГ MAb 4 (SEQ ID NOS 18, 14, 19 і 15 відповідно, у порядку появи) (ФІГ. 2C, 2D), антитіло до лПГ MAb 8 (SEQ ID NOS 67, 59, 71 і 63 відповідно, у порядку появи) (ФІГ. 2E, 2F), антитіло до лПГ Mab 13 (SEQ ID NOS 68, 60, 72 і 64 відповідно, у порядку появи) (ФІГ. 2G, 2H), антитіло до лПГ MAb 16 (SEQ ID NOS 69, 61, 73 і 65 відповідно, у порядку появи) (ФІГ. 2I, 2J), та антитіло до лПГ MAb 19 (SEQ ID NOS 70, 62, 74 і 66 відповідно, у порядку появи) (ФІГ. 2K, 2L), в яких три гіперваріабельні ділянки кожного ланцюга підкреслені. На ФІГ. 3A-C наведені графіки, що ілюструють відносну спорідненість зв'язування (що вимірюється як поглинання на довжині хвилі 492 нм) при зростанні концентрації антитіл (мкг/мл) ілюстративних мишачих моноклональних антитіл до лПГ, MAbs 1-4 (ФІГ. 3A); MAbs 5-14 і 20-23 (ФІГ. 3B); і MAbs 3 та 15-19 (ФІГ. 3C). На ФІГ.4 наведено графік, який ілюструє відношення абсорбції (оптичної густини) на довжині хвилі 280 нм і 330 нм для чотирьох різних ілюстративних мишачих моноклональних антитіл до лПГ порівняно з контрольним зразком бичачого сироваткового альбуміну (довільні одиниці). На ФІГ. 5A-C наведені графіки, які ілюструють зв'язування 23 різних ілюстративних мишачих моноклональних антитіл до лПГ з 25 або 50 нг лПГ порівняно з: самим буфером (негативним контрольним зразком), 250 нг KLH (негативним контрольним зразком) і пептидами, отриманими з гена гастрину (50 і 250 нг СТФП, G17 або G17-Gly (на фігурі позначений "G-Gly"), як зазначено. На ФІГ. 5A показане зв'язування антитіла до лПГ MAbs 1-4, на ФІГ. 5B показане зв'язування антитіла до лПГ MAbs 5-14 і 21-23, а на ФІГ. 5C – показане зв'язування антитіла до лПГ MAbs 3 і 15-20. На ФІГ. 6 наведено графік, який ілюструє зв'язування N-термінального антитіла до лПГ з лПГ при збільшенні концентрації антитіла до лПГ MAb3. На ФІГ. 7 наведені графіки, які ілюструють проліферацію репрезентативних ліній клітин КРР, лікування від яких проводиться з використанням моноклональних антитіл до лПГ наступним чином: SW480, HCT-116, LS174T, як зазначено, лікування від яких проводилося ілюстративними моноклональними антитілами до лПГ MAb 3 і MAb 4 (ФІГ. 7A, 7B, 7C відповідно, на яких показана зміна кількості живих клітин по завершенні лікування порівняно з початком лікування (T0) антитілом), або поліклональним антитілом до лПГ (ФІГ. 7D, 7E, 7F відповідно, на яких показана зміна кількості живих клітин по завершенні лікування порівняно з початком лікування (T0) антитілом); проліферація клітинної лінії SW620 КРР, лікування якої проводилося за допомогою антитіл до лПГ MAb 5-MAb 23 (ФІГ. 7G, на якій показані ліковані антитілом до лПГ клітини у вигляді відсотка кількості клітин, вилікуваних контрольним антитілом, по завершенні лікування порівняно з початком лікування (T0)); проліферація клітин LS174T, лікування якої відбувалося антитілами до лПГ MAb 8, 13, 14, 16 і 19 (ФІГ. 7H, на якій показані живі вилікувані антитілом до лПГ клітини у вигляді відсотка кількості клітин, вилікуваних контрольним антитілом, по завершенні лікування порівняно з початком лікування (T0)); і проліферація клітин HCT-116, лікування якої відбувалося моноклональними антитілами до лПГ MAb 8, 13, 14, 16, 19 (ФІГ. 7I, на якій показані живі вилікувані антитілом до лПГ клітини у вигляді відсотка кількості клітин, вилікуваних контрольним антитілом, по завершенні лікування порівняно з початком лікування (T0)). На ФІГ. 8 наведено графік, на якому ілюструється кількість живих клітин LS174T через 48 годин після 4 циклів лікування контрольним моноклональним антитілом, антитілом до лПГ MAb 8 (5 мкг/мл), антитілом до лПГ MAb 8, попередньо інкубованим з лПГ, контрольним антитілом, попередньо інкубованим з лПГ або самим лПГ. На ФІГ. 9 наведені графіки, на яких ілюструється кількість пухлин на мишу (ФІГ. 9А) і середня довжина і висота пухлини (ФІГ. 9В) у мишей, яких лікували антитілами до лПГ, порівняно з контрольним поліклональним антитілом. детальний опис ілюстративних варіантів здійснення винаходу Детальний опис Прогастрин (ПГ) вперше був визначений як попередник гастрину, пептидного гормону кишок, який стимулює секрецію кислоти шлункового соку. Гастрин існує в низці різних молекулярних форм (G17, G34, подовжений гліцином G17, подовжений гліцином G34), отриманих з прогастрину. Див. ФІГ. 1. Ген гастрину кодує продукт зі 101 амінокислоти – препрогастрин. Перше розщеплення видаляє сигнальний пептид з 21 амінокислотних залишків (підкреслені на ФІГ. 1) і дає в результаті ПГ – пептид з 80 амінокислот. У SEQ ID NO:20 наведена, зрозуміло, відома поліпептидна послідовність ПГ людини (лПГ). Як показано на ФІГ. 1, амінокислотні залишки лПГ пронумеровані від 1 до 80, при цьому найбільш амінним залишком є положення 1. Послідовності в межах перших 40 амінокислот прогастрину називаються "N-кінцем", тоді як 6 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 послідовності, які знаходяться між 41 і 80 залишком, називаються "C-кінцем". Нещодавні дослідження показали, що рівні прогастрину підвищені у пацієнтів, хворих на КРР. За нормальних фізіологічних умов прогастрин відповідає менше ніж за 10 % загального секретованого пептиду у людей. При колоректальному раку рівні прогастрину суттєво підвищені як в плазмі, так і в тканині пухлини, можливо в результаті підвищеної експресії гена гастрину, спареного з неповним процесингом продукту гена. Результати одного дослідження показали суттєво вищі рівні прогастрину у сироватці у хворих на КРР порівняно з контрольними пацієнтами, однак таких змін не було помічено у більш процесованих формах гастрину (Siddheshwar et al., 2001, Gut 48:47-52). У досліджених зразках пухлин КРР 80-100 % зразків мали підвищені рівні ПГ. Див., наприклад, Ciccotosto et al., 1995, Gastroenterology 109:1142-1153; Baldwin et al., 1998, Gut 42:581-584; Van Solinge, 1993, Gastroenterology 104:1099-1107. Роль ПГ у КРР була додатково обґрунтована експериментами, які показали, що миші, які експресують рекомбінантний ПГ людини і яким був введений канцерогенний азоксиметан, мають суттєво більшу кількість осередків аберантних крипт, аденом і аденокарцином у товстому кишечнику порівняно з мишами дикого типу, які експресують амідовані гастрини (Singh et al. 2000, Gastroenterology 119:162-171). Нещодавно Hollande et al. показали, що прогастрин стимулює шлях бета-катенін/Tcf4 шляхом репресування ICAT – негативного регулятора передачі сигналу бета-катенін/Tcf4, і що блокування прогастрину веде до експресії ICAT de novo. Див. WO 2007/135542. Не маючи на меті прив'язування до будь-якої методики використання, вважається, що блокування передачі сигналу прогастрину веде до репресії проліферації, індукованої бета-катеніном/Tcf4, в результаті підвищеної експресії ICAT. За відсутності неперервної залежної від ПГ передачі сигналів, проліферація клітин інгібується, і запускається диференціація і/або смерть клітин (у тому числі апоптоз). Незважаючи на нагальну потребу у нових клінічних підходах до лікування і діагностування КРР, той факт, що ПГ стимулює проліферацію клітин пухлини КРР, а також незважаючи на підвищений акцент на терапію з використанням моноклональних антитіл для лікування раку, на сьогоднішній день немає звітів, які б показували моноклональне антитіло, здатне заблокувати залежну від ПГ проліферацію клітин пухлини або навіть зв'язати ПГ. Такі антитіла, представлені в цьому документі вперше, виявилося важко розробити. Першою проблемою було те, що заявники виявили, що рекомбінантний прогастрин людини, який може використовуватися для генерування поліклональних антитіл до лПГ не індукував моноклональної імуногенної відповіді у дослідних мишей. Тому знадобилося розробити імуногени з використанням лише пептидних фрагментів ПГ для генерування антитіл, специфічних до прогастрину, а не до інших продуктів гену гастрину. Хоча одного разу клони гібридоми генерували антитіла, що зв'язують антигенний пептид, було виявлено, що зв'язування з пептидом не було передвісником здатності зв'язування ПГ, специфічно чи взагалі. Як детальніше показано у розділі "Приклади" нижче, багато гібридом генерували антитіла, які зв'язують пептид антигену ПГ, використовуваний в імуногенні, однак не зв'язують ПГ. У цьому описі наведені моноклональні антитіла лПГ, які не лише зв'язують пептидний антиген, проти якого вони були вирощені, однак також і специфічно зв'язують лПГ. Цілком несподівано були отримані моноклональні антитіла, високоспецифічні до лПГ по відношенню до його продуктів процесингу (наприклад, G34, G34-Gly, G17, G17-Gly, CTФП), з антигенами, які у деяких випадках не є унікальними для лПГ, а включають ділянки амінокислотної послідовності, спільні для одного або кількох продуктів процесингу прогастрину. Крім того, несподівано було відкрито, що незважаючи на відносно невеликий розмір лПГ (80 амінокислот), не всі моноклональні антитіла до лПГ, навіть ті, які демонструють високий ступінь спорідненості і специфічності до лПГ, нейтралізують його біологічну активність. Моноклональні антитіла до лПГ Заявники відкрили пептидні антигени, корисні для вироблення моноклональних антитіл до лПГ. Пептиди, корисні для вироблення антитіл до лПГ за цим описом, включають специфічні до прогастрину послідовності, які не знаходять у більш процесованих формах поліпептиду, таких як подовжені гліцином або амідовані гастрини чи СТФП, однак які також можуть включати послідовності, які знаходять у процесованих формах лПГ. У деяких варіантах здійснення винаходу моноклональні антитіла до лПГ виробляють проти пептидного антигену з амінокислотною послідовністю, що відповідає N-термінальній ділянці лПГ, і називають їх Nтермінальні моноклональні антитіла до лПГ. Специфічна ілюстративна антигенна ділянка, яка може використовуватися для побудови імуногену, корисного для отримання N-термінальних моноклональних антитіл до ПГ, відповідає залишкам 1-14 лПГ (SWKPRSQQPDAPLG (SEQ ID NO: 25)), зв'язаним з лінкерною послідовністю. У деяких варіантах здійснення винаходу моноклональні антитіла до лПГ виробляють проти пептидний антиген з амінокислотною 7 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 послідовністю, що відповідає C-термінальній ділянці лПГ, і називають їх C-термінальні моноклональні антитіла до лПГ. Специфічна ілюстративна антигенна ділянка, яка може використовуватися для побудови імуногену, корисного для отримання C-термінальних моноклональних антитіл до ПГ, відповідає залишкам 55-80 лПГ (SEQ ID NO:27), зв'язаним з лінкерною послідовністю. Див. табл. 1. Моноклональні антитіла до лПГ за цим описом зв'язують ПГ і корисні для виявлення та ізолювання ПГ від складних сумішей. Крім того, моноклональні антитіла до лПГ за цим описом унікально підходять для терапевтичних і/або діагностичних цілей при колоректальному раку. У різних варіантах здійснення моноклональні антитіла до лПГ (1) специфічно зв'язують ПГ на відміну від інших продуктів гену гастрину, (2) мають високу спорідненість до лПГ, (3) інгібують проліферацію клітин колоректального раку in vitro і in vivo, (4) знижують розмір і кількість пухлин in vivo, (5) виявляють ПГ у складних сумішах, що містять інші отримані з гену гастрину пептиди. Ген гастрину експресують і широко процесують для отримання кількох білкових продуктів, що відіграють певну роль в нормальному гомеостазі. З іншого боку, прогастрин зазвичай не виявляється у кровообігу здорових суб'єктів. Мішенню моноклональних антитіл за цим описом є прогастрин, однак не інші пептиди, отримані з гену гастрину. Відповідно моноклональні антитіла до лПГ специфічно зв'язуються з прогастрином людей та інших тварин, однак не з іншими продуктами гену гастрину, такими як, зокрема, подовжені гліцином або амідовані гастрини чи Cтермінальний фланкуючий пептид (СТФП). Специфічність моноклональних антитіл до лПГ можна визначити з використанням ELISA наступним чином. 96-ямкові планшети інкубують вночі при температурі 4 °C з відповідною(ими) концентрацією(ями) досліджуваного поліпептиду (наприклад, 25 і 50 нг рекомбінантного ПГ людини, та 50 і 250 нг СТФП чи інших отриманих з гастрину генних продуктів) у натрійфосфатному буфері (НФБ), після чого ямки промивають тричі розчином промивання (НФБ і 0,1 % Tween-20), а потім інкубують протягом 2 годин при температурі 22 °C з 100 мкл блокувального розчину (НФБ, 0,1 % Tween-20, 0,1 % бичачого сироваткового альбуміну чи гідролізату казеїну) на ямку. Після блокування ямки промивають тричі, і додається антитіло (досліджуване антитіло), що має бути піддане кількісному аналізу. До кожної ямки додають 100 мкл досліджуваного антитіла (з концентрацією 0,3-1 нг/мл) у НФБ і 0,1 % Tween-20. Планшети потім інкубують протягом 2 годин при 22 °C, після чого розчин досліджуваного антитіла знищують і заміняють після кроку промивання (тричі по 100 мкл розчин для промивання, як зазначено вище) на блокувальний розчин, який містить вторинне антитіло – козине антитіло до IgG (Fc) миші, кон'юговане з пероксидазою хрону. Після 1-годинної інкубації з вторинним антитілом до кожної ямки додають 100 мкл субстратного розчину (наприклад, Fast OPD, або офенілендіамін дигідрохлорид виробництва компанії Sigma-Aldrich Co., приготовлений у відповідності з інструкціями виробника) та інкубують в темноті протягом 20 хвилин при 22 °C. Реакцію зупиняють шляхом додавання 50 мкл 4N сірчаної кислоти і визначають кількість каталізованого субстрату шляхом вимірювання оптичної густини (ОГ) на довжині хвилі 492 нм. Перетворення субстрату пропорційне кількості первинного (досліджуваного) антитіла, зв'язаного з антигеном. Експерименти проводять по два, а виміряні значення ОГ наносять на графік залежно від концентрації антигену. Досліджувані антитіла вважають специфічними до ПГ, якщо виміряне значення ОГ знаходиться в діапазоні від 0.2 до 1,5 для лПГ, і відсутній статистично суттєвий сигнал вище фону з СТФП чи будь-якими іншими отриманими з гена гастрину пептидами, де фон – це середній сигнал з контрольних лунок, що містяться лише НФБ. Було встановлено, що деякі моноклональні антитіла до лПГ за цим описом є високоспецифічними. У деяких варіантах здійснення моноклональні антитіла до лПГ демонструють у 100 разів вищу специфічність до прогастрину порівняно з іншими продуктами гена гастрину. У таких варіантах здійснення потрібно у 100 разів більше антигену (наприклад, подовженого гліцином або амідованого гастрину) для отримання того зв'язування, що спостерігається, коли антигеном є прогастрин. До інших способів визначення зв'язування відносяться, зокрема, імунофлуоресцентний спосіб, твердофазний імуноферментний аналіз (ELISA), імунологічна мічена радіоактивним матеріалом проба (RIA), сандвічевий аналіз ELISA (Настанова з проведення експериментів з моноклональними антитілами (опублікувана Kodansha Scientific, 1987), Друга серія курсу біохімічних експериментів, том 5, спосіб імунобіохімічного дослідження, опублікована Tokyo Kagaku Dojin (1986)). Моноклональні антитіла до лПГ з високою спорідненістю до ПГ є бажаними для терапевтичних і діагностичних цілей. Для деяких використань, наприклад, терапевтичних цілей, бажано мати спорідненість не менше приблизно 100 нМ, хоча можуть бути бажаними антитіла з більшою спорідненістю, наприклад, спорідненістю не менше приблизно 90 нМ, 80 нМ, 70 нМ, 60 8 UA 106771 C2 5 10 15 20 25 30 35 40 45 50 55 60 нМ, 50 нМ, 40 нМ, 30 нМ, 25 нМ, 20 нМ, 15 нМ, 10 нМ, 7 нМ, 6 нМ, 5 нМ, 4 нМ, 3 нМ, 2 нМ, 1 нМ, 0,1 нМ, 0,01 нМ, 10 пМ, 1 пМ або навіть більше. У деяких варіантах здійснення моноклональні антитіла до лПГ специфічно зв'язують лПГ зі спорідненістю в діапазоні приблизно від 1 пМ до 100 нМ чи спорідненістю у діапазоні між будь-якими з зазначених вище значень. Спорідненість моноклональних антитіл до лПГ можна визначати з використанням способів, добре відомих в даній галузі або описаних в цьому документі, таких як, наприклад, (без обмеження) ELISA (твердофазний імуноферментний аналіз), ізотермічна титраційна калориметрія (ІТК), BIAcore, Proteon або флуоресцентний поляризаційний імуноаналіз. З використанням антигенів з N- і C-термінальних ділянок лПГ можна генерувати антитіла, які розпізнають різні епітопи лПГ. Епітоп, що розпізнається моноклональним антитілом, залежить від конкретного антигену, який використовується для вироблення антитіла, і може бути картований з використанням способів, відомих досвідченому фахівцю, таких як сканування аланіном і SPOT-тест (див. розділ "Приклади" нижче). Наприклад, картування епітопу виявляє, що антитіла до лПГ MAb 2 і MAb 4 зв'язують один і той самий епітоп; антитіла до лПГ MAb 1 і MAb 3 зв'язують приблизно один і той самий епітоп; MAb 17, MAb 18, MAb 19 і MAb 20 зв'язують приблизно один і той самий епітоп; MAb 15 і MAb 16 зв'язують приблизно один і той самий епітоп; антитіла до лПГ MAb 5, MAb 6, MAb 7, MAb 9 і MAb 12 зв'язують один і той самий епітоп і зв'язують приблизно один і той самий епітоп, що й антитіло до лПГ MAb 10; а антитіла до лПГ MAb 11 і MAb 14 зв'язують приблизно один і той самий епітоп. Чи розпізнає моноклональне антитіло до лПГ конкретний епітоп, можна визначити з використанням описаного в цьому документі конкурентного кількісного аналізу, в якому відомий епітоп, що зв'язується контрольним антитілом. У деяких варіантах здійснення винаходу моноклональне антитіло до лПГ конкурує з контрольним антитілом, яке зв'язує епітоп, що має амінокислотну послідовність, яка відповідає N-термінальній ділянці лПГ. У конкретних варіантах здійснення винаходу моноклональні антитіла до лПГ конкурують з контрольним антитілом, яке зв'язує епітоп, що включає залишки 10-14 лПГ (SEQ ID NO:28), залишки 9-14 лПГ (SEQ ID NO:29), залишки 4-10 лПГ (SEQ ID NO:30), залишки 2-10 лПГ (SEQ ID NO:31) або залишки 2-14 лПГ (SEQ ID NO:32). У деяких варіантах здійснення винаходу моноклональне антитіло до лПГ конкурує з контрольним антитілом, яке зв'язує епітоп, що має амінокислотну послідовність, яка відповідає C-термінальній ділянці лПГ. У конкретних варіантах здійснення винаходу моноклональні антитіла до лПГ конкурують з контрольним антитілом, яке зв'язує епітоп, що включає залишки 71-74 лПГ (SEQ ID NO:33), залишки 69-73 лПГ (SEQ ID NO:34), залишки 76-80 лПГ (SEQ ID NO:35) або залишки 67-74 лПГ (SEQ ID NO:36). Моноклональні антитіла до ПГ можуть бути нейтралізуючими. Без прив'язування до будьякої методики використання вважається, що нейтралізуючі моноклональні антитіла до лПГ шляхом зв'язування ПГ блокують або інгібують його здатність до взаємодії зі своїм(и) сигнальним(и) партнером(ами). Це, у свою чергу, інгібує шлях сигнальної трансдукції у клітинах колоректальної пухлини, який інакше призвів би до проліферації, зниженої диференціації і загибелі клітин. У деяких варіантах здійснення винаходу нейтралізуючі моноклональні антитіла до ПГ зв'язують N-термінальну ділянку лПГ. У конкретних варіантах здійснення винаходу нейтралізуючі моноклональні антитіла до ПГ конкурують за зв'язування ПГ з антитілами до лПГ MAb1, MAb2, MAb3, MAb4, MAb15, MAb 16, MAb 17, MAb 18, MAb 19 або MAb 20. В інших варіантах здійснення нейтралізуючі моноклональні антитіла до ПГ зв'язують C-термінальну ділянку лПГ. У конкретних варіантах здійснення винаходу нейтралізуючі моноклональні антитіла до ПГ конкурують за зв'язування ПГ з антитілами до лПГ MAb 5, MAb 6, MAb 7, MAb8, MAb9, MAb10, MAb11, MAb12, MAb13, MAb21, MAb 22 або MAb23. Специфічний аналіз для визначення того, чи є моноклональне антитіло до ПГ нейтралізуючим, може бути проведений наступним чином. Виконують посів клітин LS174T КРР у 6-ямковий планшет, як описано в Прикладі 7 нижче, приблизно 50 000 клітин на ямку. Після цього клітини обробляють з 12-годинним інтервалом впродовж 48 годин досліджуваним моноклональним антитілом до ПГ чи контрольним моноклональним антитілом, як зазначено в Прикладі 7 при концентрації антитіла приблизно 5 мкг/мл. Досліджуване антитіло визначається як нейтралізуюче в кількісному аналізі, якщо кількість ракових клітин КРР, оброблених досліджуваним антитілом, демонструє статистично суттєве зниження не менше ніж на 10 % кількості клітин, що вижили, порівняно з кількістю клітин, оброблених контрольним неспецифічним антитілом, з використанням двостороннього критерію Манна-Уїтні (відмінності вважаються значними, якщо p
ДивитисяДодаткова інформація
Автори англійськоюPannequin, Julie, Boudier, Laure, Joubert, Dominique, Hollande, Frederic
Автори російськоюПаннекан Жюли, Будиер Лор, Жюбер Доминик, Оланде Фредерик
МПК / Мітки
МПК: C07K 16/26, A61P 35/00, A61K 39/395
Мітки: використання, прогастрину, моноклональні, антитіла
Код посилання
<a href="https://ua.patents.su/124-106771-monoklonalni-antitila-do-progastrinu-ta-kh-vikoristannya.html" target="_blank" rel="follow" title="База патентів України">Моноклональні антитіла до прогастрину та їх використання</a>
Попередній патент: Спосіб та пристрій для формування та пакування окремих формованих тютюнових виробів
Наступний патент: Спосіб отримання зв’язуючого для волокон і отверджуване зв’язуюче для волокон
Випадковий патент: Кавітаційний спосіб визначення коефіцієнтів стиснення і швидкості струменя рідини при витіканні крізь отвори і насадки