Складні ефіри гіалуронової кислоти з реїном, спосіб їх одержання і композиція, що містить ці ефіри
Формула / Реферат
1. Складний ефір гіалуронової кислоти формули (І)
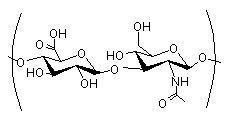 , (I)
, (I)
з реїном формули (II)
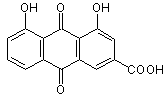 (II)
(II)
або його похідною;
де спиртові групи гіалуронової кислоти естерифіковані реїном;
у вільному вигляді або у формі похідної сполуки, або у формі солі.
2. Сполука за п. 1, в якій реїном естерифіковано не менш за 5 % спиртових груп гіалуронової кислоти, що піддаються естерифікації.
3. Сполука за п. 2, в якій реїном естерифіковано від 5 % до 50 % спиртових груп гіалуронової кислоти, що піддаються естерифікації.
4. Сполука за п. 3, в якій реїном естерифіковано від 5 % до 20 % спиртових груп гіалуронової кислоти, що піддаються естерифікації.
5. Сполука за п. 4, в якій реїном естерифіковано 10 % спиртових груп гіалуронової кислоти, що піддаються естерифікації.
6. Натрієва сіль сполуки за будь-яким із пп. 1-5.
7. Спосіб одержання сполуки або її солі за будь-яким із пп. 1-6, який включає проведення реакції хлорангідриду реїну у вільному вигляді або у формі похідної сполуки з гіалуроновою кислотою.
8. Спосіб за п. 7, який відрізняється тим, що хлорангідрид реїну і гіалуронову кислоту застосовують в таких кількостях, що процентне відношення між кількістю мілімолів хлорангідриду реїну і кількістю міліеквівалентів спиртових груп гіалуронової кислоти, що піддаються естерифікації, становить не менше 5 %.
9. Спосіб за п. 8, який відрізняється тим, що згадане процентне відношення становить від 5 % до 50 %.
10. Спосіб за п. 9, який відрізняється тим, що згадане процентне відношення становить від 5 % до 20 %.
11. Спосіб за п. 10, який відрізняється тим, що згадане процентне відношення становить 10 %.
12. Спосіб за будь-яким із пп. 7-11, який включає такі стадії:
a) приготування суспензії гіалуронової кислоти в апротонному неполярному розчиннику;
b) додання хлорангідриду реїну, розчиненого в апротонному неполярному розчиннику, і акцептора водневих іонів;
c) витримання суміші при перемішуванні і нагріванні зі зворотним холодильником протягом часу, достатнього для проходження реакції естерифікації; і
d) випарювання розчинника.
13. Спосіб за п. 12, який відрізняється тим, що згаданим апротонним неполярним розчинником на стадії а) є циклогексан.
14. Спосіб за п. 12 або п. 13, який відрізняється тим, що згаданим акцептором водневих іонів на стадії b) є NЕt3.
15. Спосіб за будь-яким із пп. 12-14, який відрізняється тим, що на стадії с) реакційну суміш витримують при нагріванні зі зворотним холодильником протягом не менше 20 год.
16. Спосіб за будь-яким із пп. 7-15, який відрізняється тим, що хлорангідрид реїну одержують за способом, що включає такі стадії:
а') приготування суспензії реїну в апротонному неполярному розчиннику;
b') додання SOС12 в такій кількості, щоб молярне відношення SOСl2 до реїну перевищувало 10;
с') витримання суміші при перемішуванні і нагріванні зі зворотним холодильником в інертній атмосфері протягом часу, достатнього для утворення хлорангідриду реїну; і
d') видалення розчинника і надлишку SOСl2, що не вступив в реакцію, шляхом дистилювання.
17. Спосіб за п. 16, який відрізняється тим, що згаданим апротонним неполярним розчинником на стадії а') є хлорвмісний розчинник.
18. Спосіб за п. 17, який відрізняється тим, що згаданим хлорвмісним розчинником є СН2Сl2.
19. Спосіб за будь-яким із пп. 16-18, який відрізняється тим, що на стадії с') реакційну суміш витримують при нагріванні зі зворотним холодильником протягом не менше за 3 год.
20. Спосіб за будь-яким із пп. 7-19, який додатково включає кінцеву стадію очищення.
21. Спосіб за п. 20, який відрізняється тим, що згадану стадію очищення виконують із застосуванням діалізної мембрани.
22. Фармацевтична композиція, яка містить сполуку або її сіль за будь-яким із пп. 1-6 у поєднанні з відповідними наповнювачами і/або розріджувачами.
23. Фармацевтична композиція за п. 22, яка має склад, придатний для місцево-регіонарного застосування.
24. Фармацевтична композиція за п. 23, придатна для застосування шляхом внутрішньосуглобової інфільтрації.
25. Фармацевтична композиція за п. 23, придатна для застосування шляхом введення в око.
26. Фармацевтична композиція за п. 23, придатна для застосування шляхом місцевого введення.
27. Фармацевтична композиція за будь-яким із пп. 22-26 у формі водної дисперсії.
28. Фармацевтична композиція за п. 27, яка відрізняється тим, що зовнішньою фазою згаданої дисперсії є буферний розчин, що має рН 7,4.
29. Фармацевтична композиція за п. 27 або п. 28, яка відрізняється тим, що згадана сполука міститься в концентрації в межах від 0,1 % до 2 % маси на об'єм.
30. Фармацевтична композиція за п. 29, яка відрізняється тим, що згадана сполука міститься в концентрації 1 % маси на об'єм.
31. Лікарський засіб для людей або для застосування у ветеринарії, який містить фармацевтичну композицію за будь-яким із пп. 22-30.
32. Застосування сполуки або солі за будь-яким із пп. 1-6 для виготовлення лікарського засобу для лікування запальних захворювань.
33. Застосування за п. 32, де згаданими запальними захворюваннями є запальні захворювання суглобів.
34. Застосування сполуки або солі за будь-яким із пп. 1-6 для виготовлення лікарського засобу для відновлення тканин, причому тканиною є хрящ або шкіра.
35. Застосування сполуки або солі за будь-яким із пп. 1-6 для приготування біоактивних матеріалів.
Текст
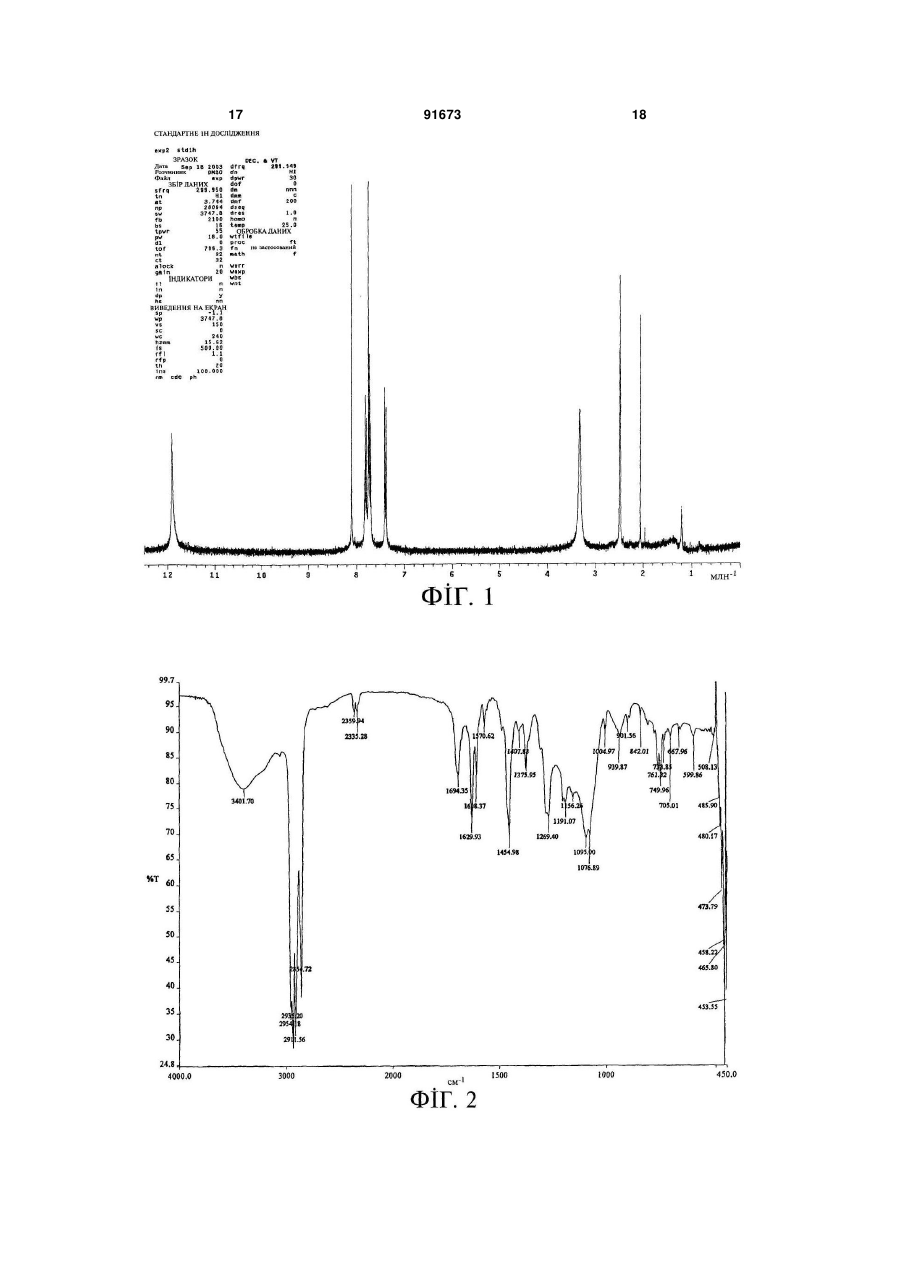
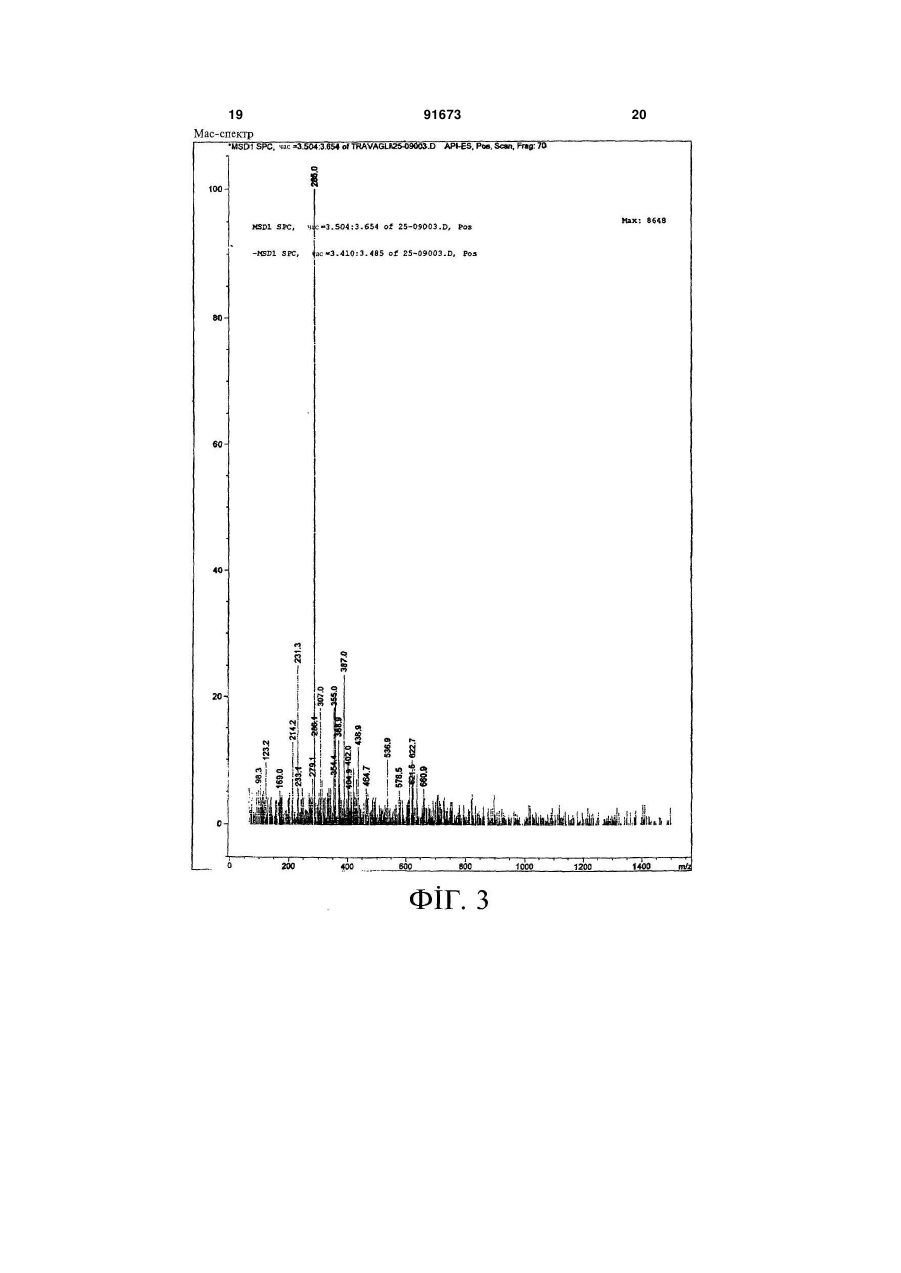
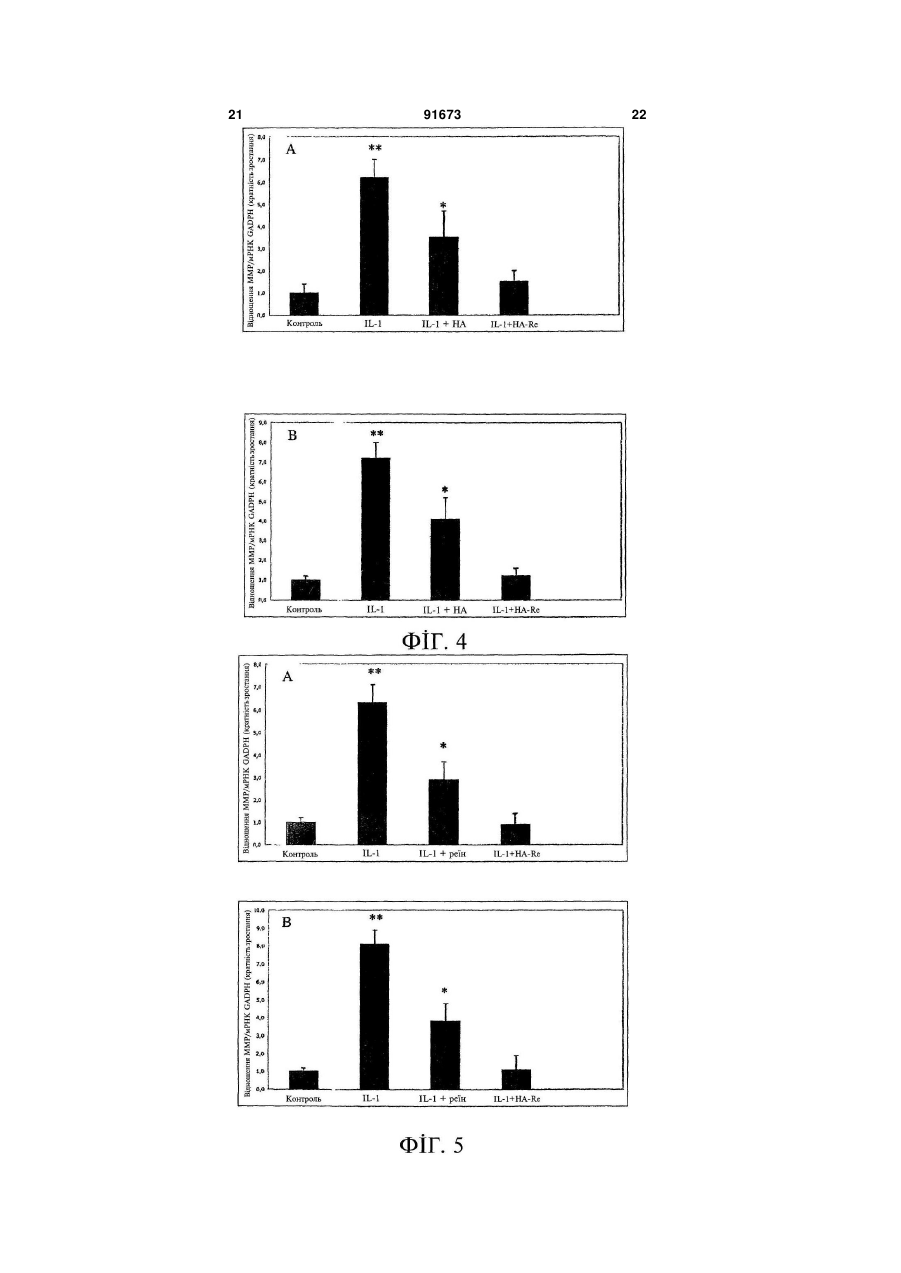
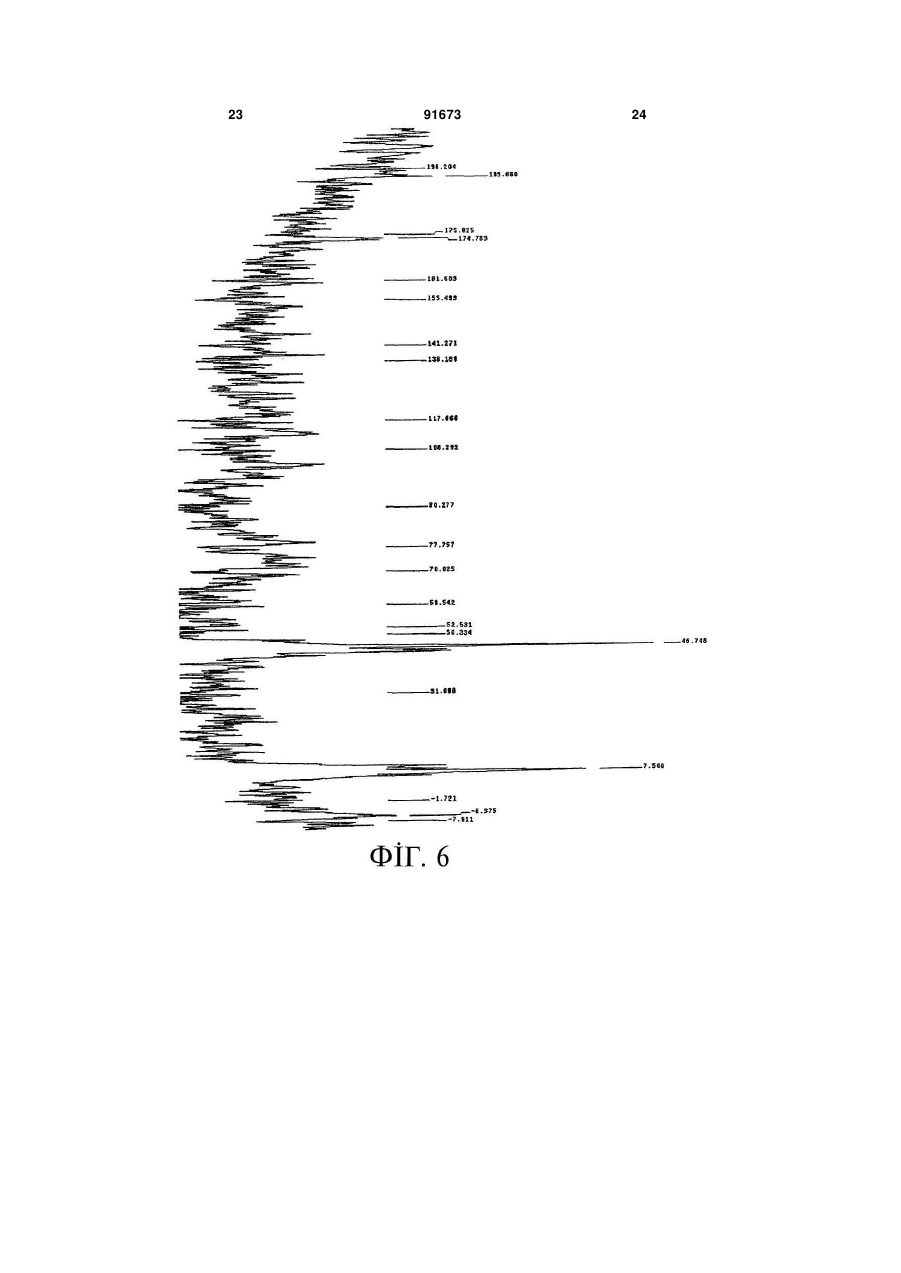
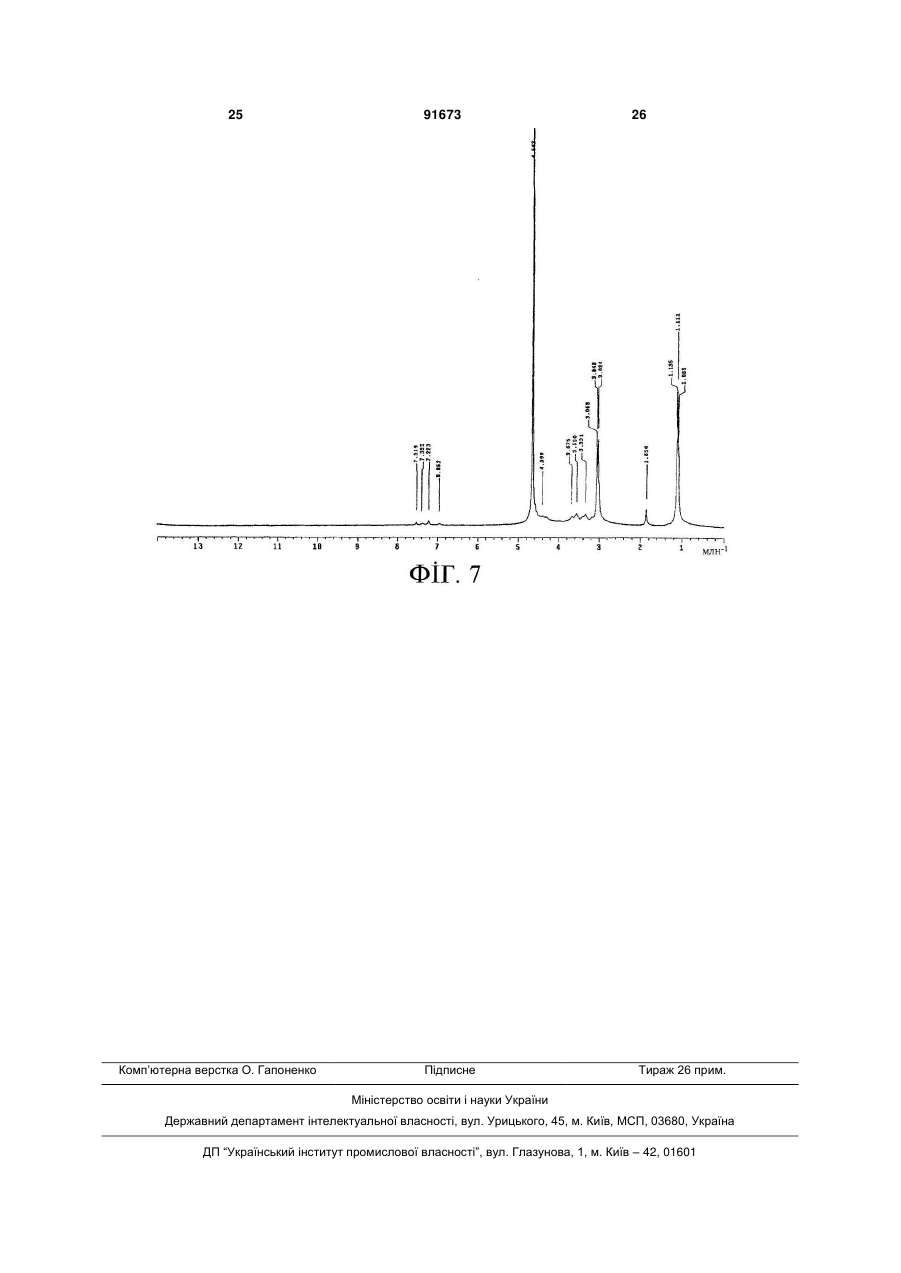
1. Складний ефір гіалуронової кислоти формули (І) C2 2 (19) 1 3 91673 4 тримують при нагріванні зі зворотним холодильни24. Фармацевтична композиція за п. 23, придатна ком протягом не менше 20 год. для застосування шляхом внутрішньосуглобової 16. Спосіб за будь-яким із пп. 7-15, який відрізняінфільтрації. ється тим, що хлорангідрид реїну одержують за 25. Фармацевтична композиція за п. 23, придатна способом, що включає такі стадії: для застосування шляхом введення в око. а') приготування суспензії реїну в апротонному 26. Фармацевтична композиція за п. 23, придатна неполярному розчиннику; для застосування шляхом місцевого введення. b') додання SOС12 в такій кількості, щоб молярне 27. Фармацевтична композиція за будь-яким із пп. відношення SOСl2 до реїну перевищувало 10; 22-26 у формі водної дисперсії. 28. Фармацевтична композиція за п. 27, яка відріс') витримання суміші при перемішуванні і нагрізняється тим, що зовнішньою фазою згаданої ванні зі зворотним холодильником в інертній атмосфері протягом часу, достатнього для утворення дисперсії є буферний розчин, що має рН 7,4. хлорангідриду реїну; і 29. Фармацевтична композиція за п. 27 або п. 28, яка відрізняється тим, що згадана сполука місd') видалення розчинника і надлишку SOСl2, що не вступив в реакцію, шляхом дистилювання. титься в концентрації в межах від 0,1 % до 2 % 17. Спосіб за п. 16, який відрізняється тим, що маси на об'єм. 30. Фармацевтична композиція за п. 29, яка відрізгаданим апротонним неполярним розчинником на зняється тим, що згадана сполука міститься в стадії а') є хлорвмісний розчинник. 18. Спосіб за п. 17, який відрізняється тим, що концентрації 1 % маси на об'єм. згаданим хлорвмісним розчинником є СН2Сl2. 31. Лікарський засіб для людей або для застосу19. Спосіб за будь-яким із пп. 16-18, який відрізвання у ветеринарії, який містить фармацевтичну няється тим, що на стадії с') реакційну суміш викомпозицію за будь-яким із пп. 22-30. тримують при нагріванні зі зворотним холодильни32. Застосування сполуки або солі за будь-яким із ком протягом не менше за 3 год. пп. 1-6 для виготовлення лікарського засобу для 20. Спосіб за будь-яким із пп. 7-19, який додатково лікування запальних захворювань. включає кінцеву стадію очищення. 33. Застосування за п. 32, де згаданими запаль21. Спосіб за п. 20, який відрізняється тим, що ними захворюваннями є запальні захворювання згадану стадію очищення виконують із застосусуглобів. ванням діалізної мембрани. 34. Застосування сполуки або солі за будь-яким із 22. Фармацевтична композиція, яка містить сполупп. 1-6 для виготовлення лікарського засобу для ку або її сіль за будь-яким із пп. 1-6 у поєднанні з відновлення тканин, причому тканиною є хрящ або відповідними наповнювачами і/або розріджувачашкіра. ми. 35. Застосування сполуки або солі за будь-яким із 23. Фармацевтична композиція за п. 22, яка має пп. 1-6 для приготування біоактивних матеріалів. склад, придатний для місцево-регіонарного застосування. Цей винахід стосується складних ефірів гіалуронової кислоти (НА) з реїном, більш конкретно, сполуки на основі гіалуронової кислоти, де спиртові групи гіалуронової кислоти естерифіковані реїном, способу одержання згаданої сполуки і фармацевтичної композиції, що містить згадану сполуку. Реїном називається алкалоїд, що одержується з александрійського листа (сенни), що має протизапальні і тканинозахисні властивості. Реїн (хімічна назва 4,5-дигідрокси-9,10дигідро-9,10-діоксо-2-антраценкарбонова кислота) має загальну формулу (І) де R=H. Цю речовину вводять в організм пероральним шляхом, звичайно в формі діацетилреїну - похідної сполуки вищенаведеної загальної формули (І), де кожна група R є ацетилом, яка має підвищену біодоступність і застосовується, в основному, при лікуванні запалень суглобів. Однак як реїн так і діацетилреїн мають недолік, що полягає в значній послаблюючій дії, яка може призводити навіть до діареї і, таким чином, обумовлює неприйнятність цього засобу для немолодих або ослаблених пацієнтів. Крім того, внаслідок нерозчинності реїну і діацетилреїну у воді, цього побічного ефекту не вдається уникнути шляхом введення цих активних речовин парентеральним або внутрішньосуглобовим шляхом. Гіалуронова кислота є природним мукополісахаридом, що складається з ланок D-глюкуронової кислоти, що чергуються, і N-ацетилглюкозаміну, як показано в загальному вигляді на нижчеприведеній схемі: 5 91673 6 гіалуронової кислоти і реїну, вживаних окремо, і яка, крім того, може застосовуватися шляхом місцевого введення з усуненням таким чином недоліків, пов'язаних із пероральним застосуванням реїну. Згідно з другим аспектом, цей винахід стосується способу одержання сполуки або її солі за першим аспектом, який включає проведення реакції хлорангідриду кислоти реїну у вільному вигляді Глюкуронова кислота N-ацетилглюкозамін які або у формі похідної сполуки з гіалуроновою кисутворюють лінійний ланцюг із молекулярною малотою. 6 сою до 13 10 Да. Згідно з третім аспектом, цей винахід стосуГіалуронова кислота присутня у всіх м'яких ється фармацевтичної композиції, що містить спотканинах організму і в багатьох біологічних рідилуку або її сіль за першим аспектом у сполученні з нах, наприклад, у синовіальній рідині суглобів і в відповідними наповнювачами і/або розріджувачасклоподібному тілі ока. ми. Гіалуронова кислота в кислотній або сольовій Згідно з подальшими аспектами, цей винахід формах застосовується для багатьох клінічних стосується лікарського продукту або лікувального цілей. пристрою для застосування в медицині або ветеЗокрема, вона з великим успіхом застосовуринарії, утвореному композицією за третім аспекється при запаленнях суглобів, при цьому її ввотом, та застосування сполуки або її солі за пердять шляхом інфільтрації безпосередньо в суглоб, шим аспектом для приготування лікарського і її дія побудована на подвійному механізмі: з одзасобу для лікування запальних захворювань або ного боку, на ослабленні запалення суглоба і з для відновлення тканин, або для приготування іншого боку, на підвищенні в'язкості синовіальної біоактивних матеріалів. рідини, яке сприятливо впливає на хрящ, змащуІнші переваги даного винаходу будуть ясні з вання якого в результаті поліпшується. нижчеприведеного докладного опису. Гіалуронова кислота може застосовуватися На Фіг. 1 зображений спектр 1Н-ЯМР реїну, також в офтальмології, де її використання обумоодержаного шляхом омилення сполуки НА-Re за влене її захисними і протизапальними властивосданим винаходом. тями, і для відновлення тканин внаслідок її анабоНа Фіг. 2 зображений ІЧ-спектр реїну, одержалічно-реконструктивної дії на хрящові тканини і на ного шляхом омилення сполуки НА-Re за даним шкіру. винаходом. Однак, як відомо, гіалуронова кислота схильна На Фіг. 3 зображений аналіз реїну, одержаного до розкладання. шляхом омилення сполуки НА-Re за даним винаЄ відомості, що розкладання гіалуронової кисходом, методом РХВЕ-МС. лоти є наслідком гідролізу, що залежить від рН і На Фіг. 4 подані результати, одержані в експеконцентрації катіонів [див., наприклад, Uchiyama риментах методом RT-PCR щодо зіставлення Η. et al. J. Biol. Chem. 1990; 265: 7753-7759; Tokita ефекту гіалуронової кислоти у фармакологічній Y. and Okamoto A., Polymer Degr. and Stab. 1995; концентрації з ефектом сполуки НА-Re за даним 48: 269-273; Hawkins C.L. and Davies M.J. Free винаходом в тих самих концентраціях. Rad. Biol. Med. 1998; 24: 1396-1410; Schiller J. et al. На Фіг. 5 подані результати, одержані в експеCurrent Med. Chem. 2003; 10:2123-2145]. риментах методом RT-PCR щодо зіставлення Після обширних досліджень автори даного виефекту реїну у фармакологічній дозі з ефектом находу встановили, що гіалуронова кислота, в якій сполуки HA-Re за даним винаходом в аналогічній спиртові групи естерифіковані реїном, несподівано дозі. набуває підвищену стабільність у порівнянні з гіаНа Фіг. 6 зображений спектр 13С-ЯМР сполуки луроновою кислотою і, крім того, має підвищену HA-Re за даним винаходом. фармакологічну активність у порівнянні з тією, яка На Фіг. 7 зображений спектр 1Н-ЯМР сполуки спостерігається для гіалуронової кислоти і реїну, HA-Re за даним винаходом. вживаних окремо. Нижче цей винахід описаний більш детально. Крім того, автори даного винаходу встановили, Даний винахід пропонує сполуку на основі гіащо гіалуронова кислота, в якій спиртові групи еслуронової кислоти, де спиртові групи гіалуронової терифіковані реїном, може бути успішно застосокислоти естерифіковані реїном, у вільному вигляді вана шляхом місцевого введення, тим самим усуабо у формі похідної сполуки або солі. ваються недоліки, пов'язані з пероральним У цьому описі сполука за даним винаходом застосуванням реїну. позначається також як "сполука HA-Re". Цей винахід грунтується на цих результатах. Потрібно мати на увазі, що в даному описі і у Згідно з першим аспектом, цей винахід стосуформулі винаходу термін "реїн" означає реїн у ється сполуки на основі гіалуронової кислоти, де вільному вигляді або в формі похідної сполуки. спиртові групи гіалуронової кислоти естерифіковаСолі сполуки HA-Re за даним винаходом ні реїном, у вільному вигляді або у формі похідної включають відповідно до варіанта, якому віддасполуки або солі, яка не тільки має підвищену стається перевага, фармацевтично прийнятні солі, більність у порівнянні з гіалуроновою кислотою, наприклад, натрієву сіль, калієву сіль, магнієву але також має підвищену фармакологічну активсіль, кальцієву сіль або інші звичайні фармацевтиність у порівнянні з тією, яка спостерігається для 7 91673 8 чно прийнятні солі, відповідно до варіанта, якому Відповідно до варіанта, якому віддається певіддається більша перевага, натрієву сіль. ревага, вищезазначений спосіб за даним винахоЗгідно з даним винаходом, термін "форма подом включає такі стадії: хідної сполуки" реїну охоплює будь-яку похідну a) приготування суспензії гіалуронової кислоти сполуку реїну, фармакологічно активну in vivo, і в в апротонному неполярному розчиннику; якій кислотна група реїну доступна для утворення b) додання хлорангідриду реїну, розчиненого в складноефірного зв'язку з гідроксильними групами мінімальній кількості апротонного неполярного гіалуронової кислоти. розчинника, і акцептора водневих іонів; Перевага віддається похідним сполукам реїну, c) втримання суміші при перемішуванні і нагріякі забезпечують доступність згаданого антрахінованні зі зворотним холодильником протягом часу, ну in vivo. достатнього для проходження реакції естерифікаПриклади реїну в формі похідних сполук за ції; і даним винаходом включають реїн, представлений d) випарювання розчинника. нижчеприведеною формулою Прикладами апротонних неполярних розчинників, які можуть бути застосовані на стадії а), є циклогексан, тетрагідрофуран, толуол, дихлорметан, к-гексан, згідно з варіантом, якому віддається більша перевага, застосування циклогексану. Вибір апротонного неполярного розчинника, який може бути застосований для розчинення хлорангідриду реїну, не є обмежувальною вимогою, але відповідно до варіанта, якому віддається перевага, вибирається той самий розчинник, який , застосовується на стадії а). Прикладами акцепторів водневих іонів, які моде кожний із замісників R незалежно від іншого жуть бути додані на стадії b), є піридин, триетилає будь-якою відповідною групою захисту гідроксимін, згідно з варіантом, якому віддається більша лу, відповідно до варіанта, якому віддається переперевага, застосування Et3N. вага, ацильною групою, необмежувальними прикЧас витримання суміші при нагріванні зі звороладами якої є ацетил, пропіоніл, бутирил або тним холодильником не є обмежувальною вимопівалоїл. гою, але відповідно до варіанта, якому віддається Згідно з варіантом здійснення даного винахоперевага, повинно становити не менше за 20 год. ду, якому віддається перевага, реїн застосовують Гіалуронова кислота, яка може бути застосоу формі похідної сполуки, згідно з варіантом, якому вана для одержання сполуки НА-Re за даним вивіддається більша перевага, у формі діацетилреїнаходом, відповідно до варіанта, якому віддається ну. перевага, має молекулярну масу від 500000 Да до Згідно з даним винаходом, реїном відповідно 3000000 Да, згідно з варіантом, якому віддається до варіанта, якому віддається перевага, естерифібільша перевага, приблизно 600000 Да. ковано не менше за 5% спиртових груп гіалуроноМолекулярну масу гіалуронової кислоти можна вої кислоти, що піддаються естерифікації, згідно з визначити відомим способом, наприклад, за доповаріантом, якому віддається більша перевага, від могою гель-проникної хроматографії (GPC). 5% до 50%, за варіантом, якому віддається ще Гіалуронову кислоту, яка може бути застособільша перевага, від 5% до 20%. вана для одержання сполуки НА-Re за даним виОсоблива перевага віддається сполуці, де ренаходом, можна придбати на ринку (наприклад, їном естерифіковано 10% спиртових груп гіалуропродукт фірми Fidia Farmaceutici SpA - Abano T. нової кислоти, що піддаються естерифікації. PD) або одержати, наприклад, шляхом екстракції з Згадану сполуку НА-Re можна одержати спопівнячих гребенів, ферментації бактерій, що мають собом за даним винаходом, який включає провемуциновий шар, або іншими відомими способами дення реакції хлорангідриду реїну з гіалуроновою (порівняй Proteoglycan Protocols, Humana Press, кислотою, відповідно до варіанта, якому віддаєтьR.V. Iozzo, Ed., Totowa 2001). ся перевага, в такій кількості, що процентні відноХлорангідрид реїну, який може бути застосошення між кількістю мілімолів хлорангідриду реїну ваний для одержання сполуки HA-Re за даним і кількістю міліеквівалентів спиртових груп гіалуровинаходом, можна одержати за способом, що нової кислоти, що піддаються естерифікації, перевключає такі стадії: вищують 5%, згідно з варіантом, якому віддається а') приготування суспензії реїну в апротонному більша перевага, становить від 5% до 50%, згідно неполярному розчиннику; з варіантом, якому віддається ще більша переваb') додання SOCI2 в такій кількості, щоб моляга, становить від 5% до 20% і згідно з варіантом, рне відношення SOCI2 до реїну перевищувало 10; якому віддається особлива перевага, дорівнює с') витримання суміші при перемішуванні і на10%. гріванні зі зворотним холодильником в інертній При розробці способу враховувався вибір розатмосфері протягом часу, достатнього для утвочинників у залежності від прийнятності їхніх залирення хлорангідриду реїну; і шкових кількостей (ІСН - Міжнародна конференція d') видалення розчинника і надлишку SOCI2, з гармонізації технічних вимог для реєстрації ліщо не вступив в реакцію, шляхом дистилювання. карських засобів для застосування в медицині). Прикладами апротонних неполярних розчинників, які можуть бути застосовані на стадії а'), є 9 91673 10 циклогексан, тетрагідрофуран, толуол, дихлормеЗовнішньою фазою згаданої дисперсії відповітан, н-гексан, віддається перевага застосуванню дно до варіанта, якому віддається перевага, є бухлорвмісного розчинника, за варіантом, якому відферний розчин, що має фізіологічне значення рН, дають більшу перевагу, СН2СІ2. відповідно до варіанта, якому віддають більшу Час витримання суміші при нагріванні зі звороперевагу, рН 7,4, наприклад, сольовий розчин із тним холодильником на стадії с') не є обмежувафосфатним буфером, приготований згідно з Італьною вимогою, але відповідно до варіанта, якому лійською фармакопеєю (Official Italian віддається перевага, повинно становити не менше Pharmacopoeia, XI edition). за 3 год. Відповідно до одного застосування, якому відРеїн у вільному вигляді або у формі похідної дається особлива перевага, сполука НА-Re або її сполуки, який може бути застосований на стадії а') сіль за даним винаходом присутня в фармацевтидля одержання хлорангідриду реїну, можна придчній композиції за даним винаходом в концентрації бати на ринку (наприклад, продукт фірми Aldrich) в межах від 0,5% до 2% маси на об'єм, відповідно або синтезувати за відомими методиками (див. до варіанта, якому віддається перевага, в конценNawa Η. et al., J. Org. Chem. 1961; 26:979-981 і трації 1% маси на об'єм. посилання, вказані в цій роботі; Smith C.W. et al. Ще одним предметом даного винаходу є заTetrahedron Lett. 1993; 34; 7447-7450; Gallagher стосування сполуки HA-Re або її солі за даним P.T. et al. Tetrahedron Lett. 1994; 35:289-292). винаходом для приготування лікарського засобу Відповідно до одного варіанта застосування, для лікування запальних захворювань, відповідно якому віддається особлива перевага, сполуку НАдо варіанта, якому віддається перевага, включаюRe за даним винаходом, одержану за способом чи запальні захворювання суглобів, зокрема, остевідповідно до даного винаходу, піддають очищеноартрит і ревматоїдний артрит. ню. Ще одним предметом даного винаходу є заЦе очищення відповідно до варіанта, якому стосування сполуки HA-Re або її солі за даним віддається перевага, виконують із застосуванням винаходом для приготування лікарського засобу діалізної мембрани. для відновлення тканин, при якому згаданими ткаУ цьому випадку, як буде описано в нижчепрининами є хрящ або шкіра. ведених прикладах, перевага віддається застосуКрім того, сполуку HA-Re або її сіль за даним ванню наявної на ринку діалізної мембрани під винаходом можна застосовувати для приготування торговим найменуванням "Slide-A-Lyzer 3.5K" (вибіоактивних матеріалів, наприклад, марлі для лікуробник фірма Pierce, Rockford, IL, USA) згідно з вання ран або опіків і матриць для вирощування інструкціями виробника. клітин, призначених для лікування опіків і для імЯк вже зазначалось вище, сполука НА-Re за плантацій. даним винаходом має перевагу, що полягає у виЦей винахід більш детально ілюструється нисокої стабільності, будучи стійкою протягом не жчеприведеними експериментальними прикладаменш 36 місяців при температурі 4±0,5°С у водноми, а також фігурами. му розчині, відповідно до варіанта, якому віддаПриклади ється перевага, буферованому при рН 7,4, наприПриклад 1 клад, у сольовому розчині з фосфатним буфером, Одержання хлорангідриду реїну приготованим згідно з Італійською фармакопеєю Реїн (продукт фірми Aldrich) (21,5 мг, 0,075 (Official Italian Pharmacopoeia, XI edition). ммоль) завантажували в круглодонну колбу місткіСполука HA-Re за даним винаходом має простю 50 мл і додавали в колбу СН2СІ2 (15 мл). Сутизапальні, загоювальні, реконструктивні і анабоспензія набувала оранжевого кольору. Потім до лічні властивості відносно шкіри і хрящової тканисуспензії додавали SOCI2 (0,5 мл, 6,9 ммоль). Реани. кцію проводили при перемішуванні і нагріванні зі Таким чином, цей винахід стосується також зворотним холодильником (50°С) в інертній атмофармацевтичної композиції, що містить сполуку сфері (N2). Витримували реакційну суміш при наHA-Re за даним винаходом у сполученні з відповігріванні зі зворотним холодильником протягом 3 дними наповнювачами і/або розріджувачами. год, при цьому розчин набував світлого оранжевоЗокрема, фармацевтична композиція за даним жовтого кольору. З метою видалення СН2СІ2 і винаходом може бути лікувальним пристроєм і/або надлишку SOCI2, що не вступив в реакцію, до сулікарським продуктом для застосування в медициміші додавали толуол (приблизно 5 мл), і суміш ні або ветеринарії. переганяли при 500 мм рт. ст., що відповідає Фармацевтична композиція за даним винахо6,6 104Па, не менш 4 разів, одержуючи 23 мг недом відповідно до варіанта, якому віддається пеочищеного хлорангідриду реїну (вихід кількісний). ревага, має склад, придатний для місцевоПродукт був ідентифікований шляхом ТШХ (елюрегіонарного застосування. ент етилацетат). Фармацевтичною композицією за даним винаПриклад 2 ходом, якій віддається особлива перевага, є комОдержання сполуки НА-Re позиція, придатна для застосування шляхом внутГіалуронову кислоту (продукт фірми Fidia рішньосуглобової інфільтрації, шляхом введення в Farmaceutici SpA - Abano Т. PD; середня молекуоко, наприклад, у формі очних крапель і очних лярна маса приблизно 600000 Да) (277,3 мг, мазей, і шляхом місцевого введення. 4,6 10-4 ммоль; відповідає 0,75 мекв. первинних Композиція за даним винаходом відповідно до спиртових груп, що піддаються естерифікації) суваріанта, якому віддається перевага, має форму спендували в циклогексані (20 мл). Додавали хловодної дисперсії. рангідрид реїну, одержаний, як описано в Прикладі 11 91673 12 1 (21,5 мг, 0,075 ммоль), розчинений в мінімальній Спектр 1Н-ЯМР сполуки HA-Re, одержаної в кількості СН2СІ2. Потім додавали Εt3Ν (3 мл). СуПрикладі 2, одержували в дейтерованому буферспензія набувала червоного кольору. Реакцію проному розчині, застосовуючи спектрометр Varian водили при перемішуванні і нагріванні зі зворотVRX300. Однак при інтерпретації цього спектра ним холодильником (70°С) в інертній атмосфері виникали ускладнення, оскільки частка реїну, що (N2). Через нетривалий час суспензія набувала реагує з гіалуроновою кислотою, виявилася недочервоно-оранжевого кольору, який приблизно честатньою для ідентифікації ароматичного циклу. рез 3 год ставав темніше. Через 20 год реакцію Тому, з урахуванням низької розчинності реїну у припиняли, і розчинник випарювали досуха під водному середовищі і оборотності реакції естеризниженим тиском (650 мм рт. ст., що відповідає фікації, було проведене омилення, тобто основний гідроліз, з метою одержання реїну зі сполуки HA8,7 104 Па), одержуючи сполуку HA-Re у вигляді Re. Продукт омилення був осаджений. Спектр 1Нсвітло-жовтого осаду. ЯМР продукту гідролізу був одержаний в диметилПриклад 3 сульфоксиді (ДМСО) на спектрометрі Varian Очищення сполуки HA-Re VRX300. Одержаний спектр, зображений на Фіг. 1, a) Підготовка проби повністю співпадає зі спектром реїну. До сполуки HA-Re (0,1019 г), одержаної, як 3) ІЧ аналіз описано в Прикладі 2, додавали сольовий розчин Був одержаний ІЧ спектр продукту, одержаноіз фосфатним буфером (рН 7,4; 5 мл). Одержуваго при омиленні сполуки HA-RE за даним винахоли двофазну систему, де розчин набував оранжедом, в середовищі нуджолу (Nujol) з використанво-жовтого кольору, тоді як залишок являв собою ням системи апаратури ВХ FT-IR (Perkin-Elmer). Як масу желатиноподібної консистенції жовтовидно з Фіг. 2, одержаний спектр співпадає зі спеккоричневого кольору. Після витримування протятром чистого реїну. гом не менше за 24 год одержували в'язку колоїд4) РХВЕ-МС ну систему коричневого кольору. Аналіз продукту омилення сполуки НА-Re за b) Очищення даним винаходом методом рідинної хроматографії Діалізну мембрану "Slide-A-Lyzer 3.5K" (вировисокої ефективності з мас-спектрометрією бник фірма Pierce, Rockford, IL, USA) гідратували (РХВЕ-МС) проводили на установці Agilent 1100, за відповідною методикою в сольовому розчині з комплект LC/MSD, використовуючи як рухому фазу фосфатним буфером (рН 7,4). Згідно з інструкціяметанольно-водну суміш (80:20), що містить 2,5% ми виробника, додавали відповідну кількість спомурашиної кислоти, при швидкості потоку 0,8 луки HA-Re, що підлягає очищенню. Діаліз провомл/хв. Як видно з Фіг. 3, маса продукту відповідає дили протягом 2 год відносно фосфатного буфера масі реїну. (рН 7,4) (буферний розчин набував жовтуватого Приклад 5 кольору вже через 20 хв). Цю операцію повторюВизначення технологічних характеристик сповали не менш 3 разів до досягнення безбарвності луки НА-Re за даним винаходом буферного розчину, контролюючи відсутність пог1) Визначення стійкості до гідролізу линання у видимому діапазоні спектра. Очищену Сполуку HA-Re за даним винаходом, одержасполуку HA-Re відновлювали з мембрани шляхом ну, як описано в Прикладі 2, і не очищену шляхом діалізу. Чистота одержаної таким чином сполуки діалізу, зберігали протягом більш за 6 місяців у HA-Re становила 99,8%. сухому стані у флаконах у темряві при температурі Приклад 4 навколишнього середовища (22°С). Потім цей зраАналіз одержаної сполуки HA-Re за даним визок очищали за допомогою діалізу, як описано в находом Прикладі 3, і визначали концентрацію реїну, засто1) Випробування із застосуванням UY-VIS спесовуючи UV-VIS спектрофотометр. Знайдена конктрофотометра центрація дорівнювала концентрації, визначеній в Концентрацію реїну в очищеній сполуці HA-Re, свіжосинтезованому продукті. Таким чином, реодержаній, як описано в Прикладі 3, визначали зультати експерименту свідчать про відсутність шляхом вимірювання спектрофотометричного сигрозкладання в сухому стані. Крім того, сполуку HAналу на довжині хвилі 430 нм, застосовуючи "груRe за даним винаходом, одержану, як описано в бе" градуювання в діапазоні 10-5-10-3 (R2=0,9999). Прикладі 2, і очищену шляхом діалізу, як описано Ця довжина хвилі була вибрана в зв'язку з тим, що в Прикладі 3, зберігали протягом 6 місяців в 2% гіалуронова кислота поглинає в УФ діапазоні, що розчині фосфатного буфера при рН 7,4 у флакоутрудняє кількісне визначення реїну. На основі нах у темряві при температурі 4°С. Виявлено приспектрофотометричних вимірювань знайдено, що сутність сторонніх речовин у зразку внаслідок вивихід за реакцією естерифікації в перерахунку на користання нестерильного матеріалу і реїн становить 58%. невикористання консервантів. Потім зразок знову У Прикладі 2 кількість реїну, використовуванопіддавали діалізу за методом, описаним у Приклаго при реакції, було вибрано з розрахунком на есді 3, при тривалості діалізу не менш 4 діб. При витерифікацію максимум 10% придатних для естепробуванні методом UV-VIS спектрометрії не вдарифікування первинних спиртових груп лося виявити виділення реїну в різні буферні гіалуронової кислоти. Оскільки вихід за реакцією розчини, застосовані для діалізу. Таким чином, і в естерифікації в перерахунку на реїн становить цьому випадку підтверджена хімічна стійкість спо58%, частку придатних для естерифікування спирлуки, оскільки відщеплення реїну від сполуки HAтових груп гіалуронової кислоти можна оцінити як Re не виявлено, принаймні в кількостях, що під5,8%. даються виявленню сучасними аналітичними ме2) 1Н-ЯМР аналіз 13 91673 14 тодами. Таким чином, гідролітичне розкладання не c) 1% (маси на об'єм) сполуки HA-Re за даним спостерігалося навіть в розчині. винаходом в сольовому розчині з фосфатним буОдержані результати дозволяють стверджувафером, рН 7,4. ти, що сполука HA-Re за даним винаходом стійка Визначали в'язкість зразків із застосуванням протягом не менш 24 місяців в умовах охолодженвіскозиметра VISCOSIMATE MODEL VM-10A ня (при 4±0,5°С) у водному розчині. Це тверджен(скляна пробірка; 3 мл; при відсутності перемішуня грунтується на відсутності якого-небудь помітвання; температура 20+0,2°С), причому одержуного гідролітичного розкладання. вали такі результати: Крім того, з метою виключення можливості гідa) =78,4 мПа с; ролітичного розкладання гіалуронової кислоти в b) =64,8 мПа с; процесі реакції естерифікації реїном, був виконаc) =47,9 мПа с. ний холостий експеримент по проведенню такої Одержані результати свідчать, що сполука HAреакції. Конкретно, були застосовані ті самі умови, Re за даним винаходом більш придатна для уприщо при проведенні конденсації реїну з гіалуроноскування, ніж високомолекулярна і низькомолекувою кислотою, але у відсутності згаданого реїну. лярна гіалуронові кислоти в природному стані. Це Зокрема, гіалуронову кислоту (100 мг) додавали пов'язано з тим, що 1% (маси на об'єм) розчин до суміші циклогексану (10 мл), дихлорметану (1 сполуки HA-Re за даним винаходом має більш мл) і триетиламіну (1 мл), і одержану суміш нагрінизьку в'язкість в порівнянні з 1% (маси на об'єм) вали зі зворотним холодильником (70°С) в інертній розчином низькомолекулярної гіалуронової кислоатмосфері (N2) протягом 24 год; після закінчення ти, який, в свою чергу, має більш низьку в'язкість, цього часу розчинники видаляли з реакційної суніж 1% (маси на об'єм) розчин високомолекулярної міші в атмосфері азоту. Одержана речовина мала гіалуронової кислоти. значно меншу розчинність у воді, ніж гіалуронова Пониження в'язкості, яке спостерігалося ранікислота в природному стані, характеризувалася ше і свідчило про відсутність реакції деполімерив'язкістю дисперсії, що не піддавалася визначенню зації гіалуронової кислоти після реакції естерифічерез 24 год. Це означає, що деполімеризацію кації, можна пояснити ковалентним характером можна виключити з розгляду, оскільки вона повинвзаємодії між реїном і гіалуроновою кислотою. на була б призвести до збільшення розчинності у Приклад 6 воді і, таким чином, до пониження в'язкості. Визначення фармакологічної активності споНарешті, була перевірена стійкість до гідролізу луки HA-Re за даним винаходом in vitro очищеної сполуки HA-Re за даним винаходом, У п'яти пацієнтів (3 чоловіків і 2 жінок, середодержаної, як описано в Прикладі 3, у процесі стенього віку 59,3±5,1 років) під час хірургічних оперилізації. Як вказано вище, було виявлено, що рацій з приводу травматичних переломів тазостегвнаслідок використання нестерильного матеріалу і нового суглоба або стегна були взяті нормальні невикористання консервантів у пробах сполуки за біопсії хряща. У пацієнтів, відібраних для досліданим винаходом можлива присутність сторонніх дження, були відсутні біохімічні або клінічні ознаки речовин. Конкретно, був приготований 1% розчин запалення або захворювання суглобів, і хрящова сполуки HA-Re за даним винаходом, очищеної із тканина була нормальною як на макроскопічному, застосуванням діалізної мембрани, в сольовому так і на мікроскопічному рівні. Хрящові проби відрозчині з фосфатним буфером при рН 7,4. З урабирали в стерильних умовах і негайно обробляли хуванням експериментальних даних, що свідчать для виділення хондроцитів. Проби спочатку очипро термочутливість молекули гіалуронової кислощали від залишків м'язової, з'єднувальної або субти (Biomaterials 23 (2002), 4503-4513), одержаний хондральної кісткової тканини, потім подрібнювали таким чином зразок стерилізували із застосувандо розміру шматків 1-3 мм3 і промивали сольовим ням насиченої пари під тиском в автоклаві при розчином із фосфатним буфером, рН 7,2 (PBS). 121°С протягом 20 хв. Потім зразок знову піддаваПотім виділяли окремі хондроцити шляхом багали діалізу із застосуванням мембрани з метою торазової ферментації тривалістю 60-75 хв при визначення присутності реїну в діалізованій рідині; 37°С у присутності 0,25% трипсину, 400 ОД/мл слідів реїну не виявлено. Ці результати дозволяколагенази І, 1000 ОД/мл колагенази II і 1 мг/мл ють зробити висновок, що згаданий зразок стійкий гіалуронідази. Клітини збирали, промивали велидо гідролізу при тепловій стерилізації. кою кількістю PBS і висівали при високій густині на 2) Аналіз реологічних характеристик і придатЗ5-міліметрові пластини (45 103 клітин на см2). ності для уприскування Культури вирощували в модифікованому за Куном Аналізувалася придатність сполуки HA-Re за (Coon) середовищі F12 Хема (Ham) з домішкою даним винаходом для уприскування в порівнянні 10% сироватки плоду корови (FCS) (виробник як з низькомолекулярною, так і високомолекулярMascia Brunelli, Milano, Italy). Підтримку фенотипу ною гіалуроновою кислотою. хондроцитів контролювали шляхом детектування Конкретно, були приготовані три таких зразки: колагену типу II після пепсинової ферментації наa) 1% (маси на об'єм) високомолекулярної гіадосадового шару культури. Життєздатність клітин луронової кислоти (середня молекулярна маса визначали шляхом проби на ексклюзію трипановоприблизно 1200000) в сольовому розчині з фосго синього. Через регулярні проміжки часу визнафатним буфером, рН 7,4; чали дуплікацію клітин шляхом трипсинізації кульb) 1% (маси на об'єм) низькомолекулярної гіатури і визначення кількості клітин. Експерименти луронової кислоти (середня молекулярна маса по стимулюванню виконували після досягнення приблизно 600000) в сольовому розчині з фосфазлиття первинних культур (пасаж 0). Потім клітини тним буфером, рН 7,4; культивували протягом 2 діб у присутності аскор 15 91673 16 бінової кислоти (50 мкг/мл) і після цього інкубували Результати, одержані в експериментах RTпротягом 20 год у відсутності або в присутності PCR, подані на Фіг. 4 і Фіг. 5. Для всіх проб виконували по три паралельні рекомбінантного інтерлейкіну-1 людини (rh IL-1 ) випробування. У кожному експерименті зміна екс(5 нг/мл), із домішкою або без домішки гіалуронопресії мРНК GAPDH виражена як кратне в поріввої кислоти (НА), сполуки за даним винаходом нянні з експресією в необроблених клітинах. Пока(НА-Re) або реїну в різних концентраціях. зані середні значення і стандартні відхилення для Згідно з наявними відомостями, як гіалуронова трьох експериментів. Для визначення значущості кислота, так і реїн виявляють цілющу дію при ефектів різних обробок застосовувався парний tостеоартриті внаслідок їх здатності інгібувати актест за Стьюдентом. Представлені також статистивність металопротеаз (ММР), що приймає тичні різниці між обробленими і контрольними участь в катаболізмі хряща. пробами: * - р
ДивитисяДодаткова інформація
Назва патенту англійськоюEsters of hyaluronic acid with rhein, process for their preparation and compositions comprising the same
Автори англійськоюPietrangelo Antonello, Travagli Valter
Назва патенту російськоюСложные эфиры гиалуроновой кислоты с реином, способ их получения и композиция, которая содержит эти эфиры
Автори російськоюПьетранджело Антонелло, Травальи Вальтер
МПК / Мітки
МПК: C08B 37/00
Мітки: складні, містить, ефіри, гіалуронової, композиція, спосіб, кислоти, одержання, реїном
Код посилання
<a href="https://ua.patents.su/13-91673-skladni-efiri-gialuronovo-kisloti-z-renom-sposib-kh-oderzhannya-i-kompoziciya-shho-mistit-ci-efiri.html" target="_blank" rel="follow" title="База патентів України">Складні ефіри гіалуронової кислоти з реїном, спосіб їх одержання і композиція, що містить ці ефіри</a>
Попередній патент: Водонепроникна та повітропроникна підошва для взуття (варіанти), водонепроникне та повітропроникне взуття (варіанти)
Наступний патент: Система і спосіб, що дозволяє використовувати технологію wusb при здійсненні розподіленого керування доступом до надширокосмугового середовища передавання даних
Випадковий патент: Грохот