Ефіри 2,6-диметил-1,4-дигідропіридин-3-карбонової кислоти, що є блокаторами кальцієвих каналів, спосіб їх одержання та фармацевтична композиція
Текст
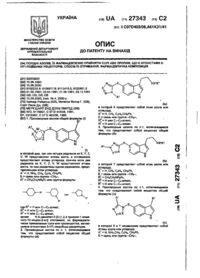
(11) (19) (13) (51)6 C07D401/12, А61К31/44 МІНІСТЕРСТВО ОСВІТИ 1 НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНО! ВЛАСНОСТІ *T! {54} ЕФІРИ 2(3-ДИМЕТМЛ-1,4-ДИПДРОЗїРИДИН-3-КДРБОИОВОї' КИСЛОТИ, ЩО Є БЛОКА10РАМИ КАЛЬЦІЄВИХ КАНАЛІВ, СПОСІБ'i v ОДРРЖЗДНЛ І Д ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ (21)93002192 (22) 18.06.1993 (24)16 10.2000 (31)9100201 (32) 09.01.1991 (33) FR (Щ 15 10 2000 Бюл 2000 (72) Лзфон Льчс, ГЧ І?Ь) Лаборатуар Л.Лафсн, FR (56) 1. US, 398575S, 10 1976 2. US, 4303603,02.1989 3. ЕР, 0106275,04 1984 4. ЕР, 0214094,03 1986 (57) 1. Зфиры 2,6-ди(йЄїия-1,4-дигидрс'Пі*ридин-3карбоновой кислоты формулы (І/ н,с « R,OOC н с н Y™ 5. Способ получения эфирсв 2,6-диметил-1,4-дигидропиридин-З-карбоноаой кислоты формулы (!)• н к,е п МЛ \ Аг MeO Л где Аг представляет сэбой групг,у, &ыбраиную из 2-нитрофенила, 3-нитрофенила, 2-хлорфенила, 2,6-дихлорфснила, 2-трифторметилфенила и 3трифторметилфенила, Ri представляет собой ( d Сд)алкильную группу и А представляет собой группу, выбранную из групп / • ОМеО МеО ОМе где Аг представляет собой группу, выбранную чз 2-нитрофечилз, 3-нмтрофенкла, 2-хг'Орфенила, 2,6-д«хлорфенилг, 2-трифтормегилфе-ила и 3трифторметилсЬенила, Чл -.редитавляет собой (СіСд)а л (сильною группу и А представляет собой группу, выбранную из групп и их фармзцсатичес-си приемлемых солей путем взаимодействия хлорзнгидрида кислоты, полученного in situ дєііствием оксалил хлорида на кислоту, со спиртом з присутствии основания, отличающейся -ем, что Б качестве кислоты использукг ішслоту формулы ILC СОО •л их фармацевтически приемлемые соли, являющиеся блокаторами кальциевых кэьзлов 2. Эфиры по г,. 1, представляющие собой 2,6диметил-4-(3'Нйтрофекип)-5-метоксикар6онил-1,4дигидропиридин-3-карбоксилат Ы-[3-'2,4,6-триметроксибензоил)пропил]пиперидин-3'-илЕ и его фармацевтически приемлемые СОЛИ 3 Эфиры по п 2, представляющие собой (-r)-(4S, 3'Є)-2,6-диметил-4-(3-читрофенил)-5-метоксикарбонил-1,4-дигидропиридин-З-карбоксилат N-[3-(2, 4,6-триметроксибензоил)пролилЗлиперидин-3'-ил£ и его фармацевтически приемлемые соли. 4. Эфиры по п 2, представляющие собой (-)-(4R, 3'К)-2,6-диметил-4-(3-нитрофенил)-5-метоксикарбонил-1,4-дигидропиридин-З-карбоксилат N-[3-(2, 4,6-триметроксибензоил)пропил]пиперидин-3'-ила и его фармацевтически приемлемые соли а 8 качестве спирта используют спирт формулы о м.-о НО' КІеО "-ОМе где А имеет значения, указанные выше 6 Фармацевтическая композиция, обладающая свойством блокировать каналы кальция содержащая актизное начало и фармацевтически приемлемые носитель и разбавитепь, отличающаяся тем, что в качестве активного начала она содержит эффективное количество соединения формулы (I): 27719 2,6-дихлорфенила, 2-трифторметилфенила и 3трифторм етил фен ила, Ri представляет собой { d С^алкильную группу и А представляет собой группу, выбранную из групп н R,OOC І X Аг OMcO ЧСН,).OMe MeO (I) где Аг представляет собой группу, выбранную из 2-нитрофенила, 3-нитрофенила, 2-хпорфенила, Изобретение относится к эфирам 2,6-диметил-1,4-дигидропиридин-З-карбоновой кислоты, являющемся блокзторами капьцьевых рецептороа, к способу их получении и к фармацевтической ксмпозиции на их основе В патенте Франции 2218107 описаны различные эфиры 2,6~диметил-4-(3-нитрофенил)-5-метоксикарбонил-1,4-лигидропиридин~3-карбоновоЙ кислоты, Б частности, 2-[метил-(фенилметил)амино] этиловый эфир, известный под названием никардипин Никардипин известен как кальциевый ингибитор и используется в хер;-т',ш кзк вззодилвтатор и антигиг.$рт8нзиьчый -»гент Задачей изобретения яалзяется разработка новых соединений, которые являлись &ы кальциевыми ингибиторами и обладали 5ы значительным и длительным антигипертензизным эффектом Эта задача решается с помощью соединений общей формулы (I). ОМеО MeO в которой Аг представляет собой группу, выбранную из 2-нитрофенил, З-читр^сЬенил, 2-хлорфенил, 2,6-диУЛсрфениг 2-TpfcbTopметилфенкл А 3-трифторметил фенил, Rозначает СІ-СІалкильную группу и. А представляет собой группу, выбранную из группы О N—ы и их фармацєатически ііриемлемьіх солей Под фармацевтически -фмемл^мими солями понимают соли с фермаце&тическ-1 npp/iewiPMw^H кислотами, которые имеет Ьі^чс vNf-сую активность свободны)- оснований, но без ке'чегательного эффекта Такими солями могут бьчь еолк с минеральными кислотами, такими как соляная, брсмистородпоодчая, серная, азотная, фосфорная кислоты, соли металлсодержащих кислот, таких как динатр:ійфосфат или кислый сульфат калия, и орани^ескими кислотами ИзоЬр&тенне относится также к сгособу получения эфиров 2 6диметил-1,4-дигидропиридин-3-чарбоновой кислоты формулы (!), заключающемуся во взаимодействии хлорангидрида кислоты, полученього in situ действием оксалил хлорида на кислоту, оо спиртом в присутствии основания причем в каче остальное - носитель и разбавитель стве кислоты используют кислоту формулы н ск, н,с R,OOC* V ^ "COOH в которой Аг и Ri имеют указанное выше значение, а в качестве спирта используют спир г формулы ОМеО Mel) где А имеет значение, указанное выше Аддитивные соли получают по классическим методикам реакцией соединения формулы (I) с фармацевтически приемлемой кислотой в подходящем растворителе И, напротив, основания могут быть получаны и; зддитизных солей обработкой их сильным основанием Кисго^ы формулы (ПІ моп.'т быть получше! классическим методом реакцией альдегида формулы. Аг-СНО (IV) с ацетоацетатом 2-циеноэтила и З-аминокротоната формупы RiOOC-Ch=C4-NHa (V) СНз с получением соединения формулы' сн, R,OіЯ ф г хн, хн. L (X) подвергнуть частичному ги&ролиэу, наприь'Зр. з смеси 1-диГ(/!этмламиио-С-ррог1еио:',и.г«дрол.ид натрия/воды с получением рацемической смеси формулы. соон КООС' (XI) подвергнуть рацемат разделению перекоисталлизацией его соли с оптически активным основанием; преобразовать изомер из формы соли в кислоту Изобретение относится также к фармацевтической композиции, обладающей свойством блокировать каналы кальция, содержащей в качестве активного начала эффективное количество соединения формулы (!). о МсО МсО в которой Аг представляет собой группу, выбранную из 2-нитрофенила, 3-нитрофенмла 2-хлорфенила, 2,6-дихлорфенила, 2-трифторметилфенила и 3-трифторметилфенила, Ri означает С1-С4алкильную группу и А представляет собой группу, выбранную из группы: -N ' ^ й остальное - носитель и разбавитель Нижеприведенные примеры иллюстрируют получение соединений согласно изобретению. Пример 1 Получение 2,6-диметил-4-(3-нитрофенил)-5метоксикарбонил-1,4-дигидропиридин-3-карбоксилата Ы-/3-(2,4,6-триметоксибензоил)пропил/пиперидин-З'-илэ хлоргидрата (CRL 41895) а) Получение зцетоацетэта 2-цианоэтила Нагревают при 90-100°С в течение 4,5 час смесь 16,33 г (0,23 мол) 3-гидроксипропионитрила и 28,4 г (0,20 мол) 2,2,6-триметил-1,3-диоксан-4она в присутствии 0,1 мл триэтиламина Реакционную смесь очищаю' перегонкой при п'ічижекном давлении с получением 23,3 г слегка желтого масла Т кип 154-156°С/4 мм. Выход 75,2%. б) Получение 2,6-диметил-4-(3-нитрофечил)-5метоксикарбонил-1,4-дигидропиридин-3-карбсг;силата 2-цианоэтила Кипятят с обратным холодильником в течение 20 час в атмосфере азота смесь 54 г (0,348 мол) продукта, полученного по а), 40 г {0,3^8 мол) меч>ло-3»аммнокротокатз и 5? 6 г (0,348 мол) 3читро-оензальдеі идэ в 500 мг этанола Обрабэтывгют теплую оеакцч-*онную смесь в темноте СХА, концентрируют до 2/3 и после охлаждения выделяют фильтрацией 101,5 г желтого порошка. Т пл. (Кофлер) 126°С. Выход 75,8% Б) Получение 2,6-дяметил-4-{3-нитрофегіил)-5метилкарбонил-1,4-дигидропиридин-3-кар6оноэой КИСЛОТЫ. Прибавляют в течение 2 час при комнатной температуре раствор 19,25 г (0,05 мол) продукта, полученного по б), и 6 г (0,05 мол) соды в таблетках к 75 мл 1,2-диметоксиэтана в 150 мл воды. Разбавляют реакционную смесь водой, которую затем промывают хлористым метиленом, органическую фазу далее обрабатывают разбавленной соляной кислотой и отделяют осадок фильтрацией. Этот продукт очищают промывкой теплым этанолом с получением 14 г белого порошка Т. пл 260Х. Выход 84,34% г) Получение 1-(2,4,б-триметоксибепзоил)-3хлорпропана Поддерживая температуру раствора, содержащего 67,2 г (0,400 мол) 1,3,5-триметоксибензола и 61 г (0,432 мол) хлорида 4-хлорбутирила в 300 мл бензола, равной +5°С, приливают к нему в течение 3,5 час раствор 121 г (0,464 мол) тетрахлорэтана в 150 мл бензола Выдерживают 4 часа при комнатной температуре и выливают реакционную смесь в 500 мл ледяной воды и 100 мл 12 н соляной кислоты Отделяют органическую фазу, которую промывают водой и высушивают над сухим сульфатом натрия. Маслянистый осадок промывают гексаном с получением 97,2 г слегка серого порошка. Т пл (Кофлер) 48°С Выход 89,2% 27719 д) Получение 1-(2 4,6-триметоксибензоил)-3(З-гидрсксипиперидино)пропана хлоргидрата При кипячении с обратным холодильником к раствору 30 г (0,297 мол) 3-гидроксипиперидина в 80 мл толуола приливают э течение 1 час раствор 40,5 г {0,148 мол) продукта, полученного по г), а 30 мл толуола. Продолжают кипячение с обратным холодильником 3 час, разбавляют реакционную смесь этилацетатом, отделяют нерастворимый остаток фильтрацией и экстрагируют фильтрат разбавленным раствором соляной кислоты Водную фазу подщелачивают содой, экстрагируют, в свою очередь, этилацетатом, который посла сушки над сухим сульфатом натрия обрабатываю': солянокислым изопропанолом ОсздоїС отделяют фильтрацией и очищают кристаллизацией а абсолютном этаноле с получением 2& г белого порошка. Тпл. 1Кофлер)175°С. Выход 50,7% е) Получение 2,6-димет«л-4-(3-нитрофенил)-5~ метоксикарбонил-1,4-дигидроп«ридин-3-карбоксклатЫ-/3-(2,4,5-тримегоксиб8изоип)пропил/пиперидин-3'- ил хлор; идрата При -25UC к раствору, содержащему 66 мл аиметилформамида и 38,5 мл ацстонитрила, приливают в течение 1G УЙН раствор Е г (0,070 моя) ? хлорида оксалила з 25 мл ацетонитрила, выдерживают 15 мин при -25°С и вводят 16,75 г (0,050 мол) продукта, полученного по 1в). После выдерживания з течение 1 час при -15°С охлаждают до 25°С и добавляют раствор 17 г (0,030 мол) продукта, полученного по 1д), (в форме основания) s £2,5 мл ги-фидииз ',*• 11 мл диметил&ормгмидз Выдерживают в течение 20 час при комнатной температуре, выливают реакционную смесь в 500 мл ледяной воды и ?5
ДивитисяДодаткова інформація
Назва патенту англійськоюEsters of 2,6-dimethyl-4-(3-nitrophenyl)-5-methoxycarbonyl-1,4-dihydropyridine-3-carboxylic acid known to be a calcium inhibitors, process for preparation thereof and pharmaceutical composition
Автори англійськоюLafon Louis
Назва патенту російськоюЭфиры 2, диметил-1,4-дигидропиридин-3-карбоновой кислоты, являющиеся блокираторами кальциевых каналов, способ их получения и фармацевтическая композиция
Автори російськоюЛафон Льюс
МПК / Мітки
МПК: A61K 31/4433, A61P 9/12, C07D 211/90, A61K 31/445, A61K 31/455, A61K 31/435, C07D 409/14, A61K 31/4427, C07D 401/12, A61K 31/451, A61P 9/08
Мітки: блокаторами, композиція, спосіб, 2,6-диметил-1,4-дигідропіридин-3-карбонової, ефіри, кислоти, одержання, каналів, кальцієвих, фармацевтична
Код посилання
<a href="https://ua.patents.su/10-27719-efiri-26-dimetil-14-digidropiridin-3-karbonovo-kisloti-shho-eh-blokatorami-kalciehvikh-kanaliv-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Ефіри 2,6-диметил-1,4-дигідропіридин-3-карбонової кислоти, що є блокаторами кальцієвих каналів, спосіб їх одержання та фармацевтична композиція</a>
Попередній патент: Спосіб визначення фізико-механічних властивостей абразивного інструменту
Наступний патент: Опора лінії електропередачі
Випадковий патент: Спосіб підвищення приростів молодняку великої рогатої худоби