Комбіновані препарати з вмістом біфепруноксу та l-dopa
Номер патенту: 94465
Опубліковано: 10.05.2011
Автори: ван Шарренбург Густаф Й.М., Тульп Мартінус Т.М., МакКрірі Ендрю К.
Формула / Реферат
1. Комбінований препарат, який містить (і) біфепрунокс або його N-оксид:

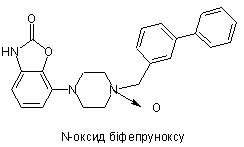
або фармакологічно прийнятні солі зазначених сполук і (iі) L-DOPA або її фармакологічно прийнятні солі, для одночасного, роздільного або послідовного застосування при лікуванні розладів, що потребують відновлення допамінергійної функції.
2. Препарат як заявлено в п. 1, який також містить інгібітор декарбоксилази.
3. Препарат як заявлено в пп. 1 або 2, який також містить інгібітор СОМТ.
4. Препарат як заявлено в будь-якому з пп. 1, 2 або 3, який також містить інгібітор МАО-В.
5. Застосування препарату як заявлено в будь-якому з пп. 1-4 при одержанні засобу для лікування розладів, що потребують відновлення допамінергійної функції.
6. Застосування як заявлено в п. 5, де зазначеним розладом є хвороба Паркінсона.
7. Застосування як заявлено в п. 5, де зазначеним розладом є синдром неспокійних ніг.
8. Фармацевтична композиція, яка містить, на додаток до фармацевтично прийнятного носія та/або принаймні однієї допоміжної речовини, фармакологічно дійову кількість препарату як заявлено в будь-якому з пп. 1-4 як діючої речовини.
9. Спосіб лікування хвороби Паркінсона або синдрому неспокійних ніг у хворих людей або тварин, що потребують такого лікування, згідно з яким хворому одночасно, нарізно або послідовно вводять кількість біфепруноксу або його N-оксиду чи фармакологічно прийнятної солі зазначених сполук та кількість L-DOPA, достатні для ефективного лікування.
10. Спосіб за п. 9, згідно з яким додатково вводять інгібітор декарбоксилази та/або інгібітор СОМТ, та/або інгібітор МАО-В.
11. Застосування біфепруноксу або його N-оксиду при одержанні засобу для лікування синдрому неспокійних ніг.
Текст
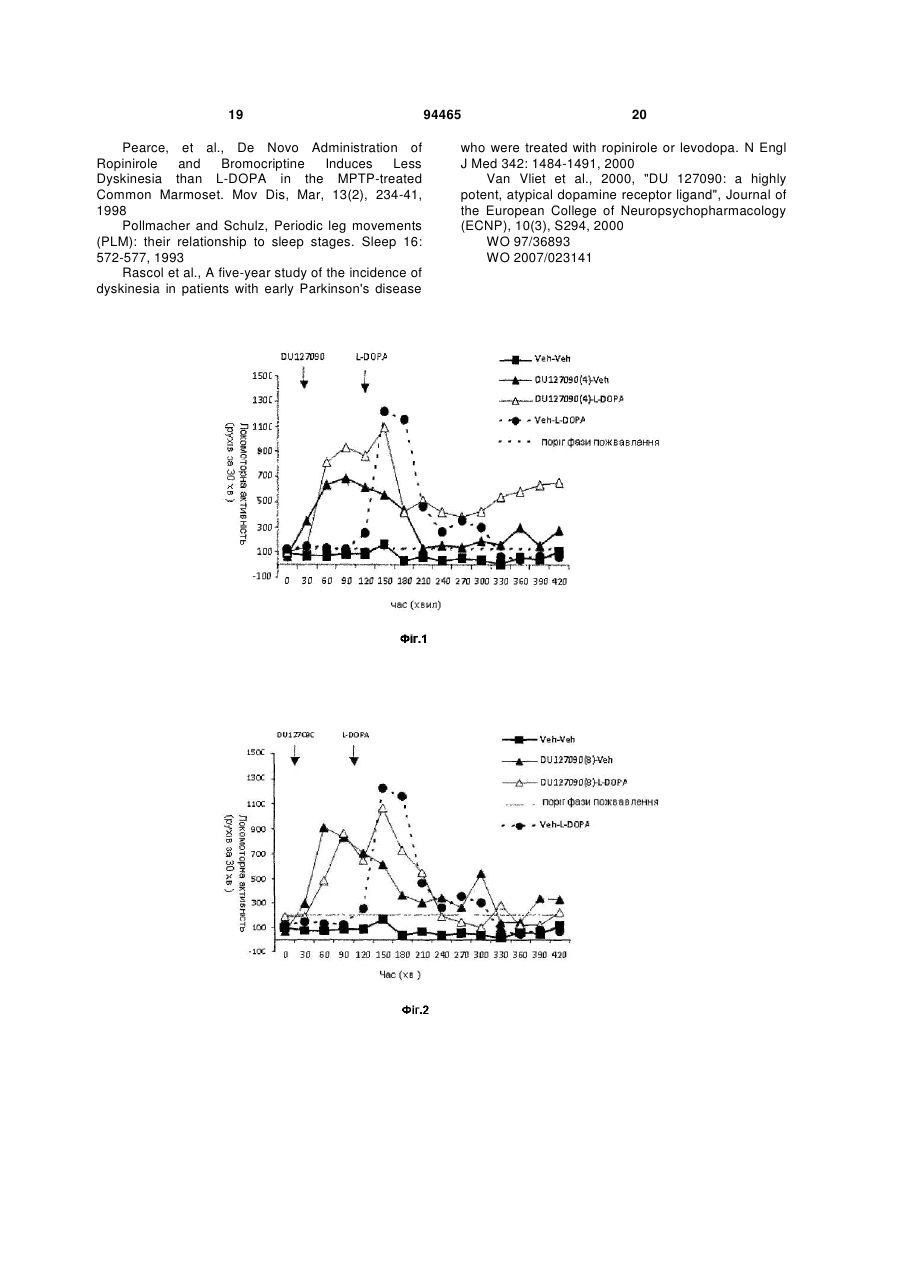
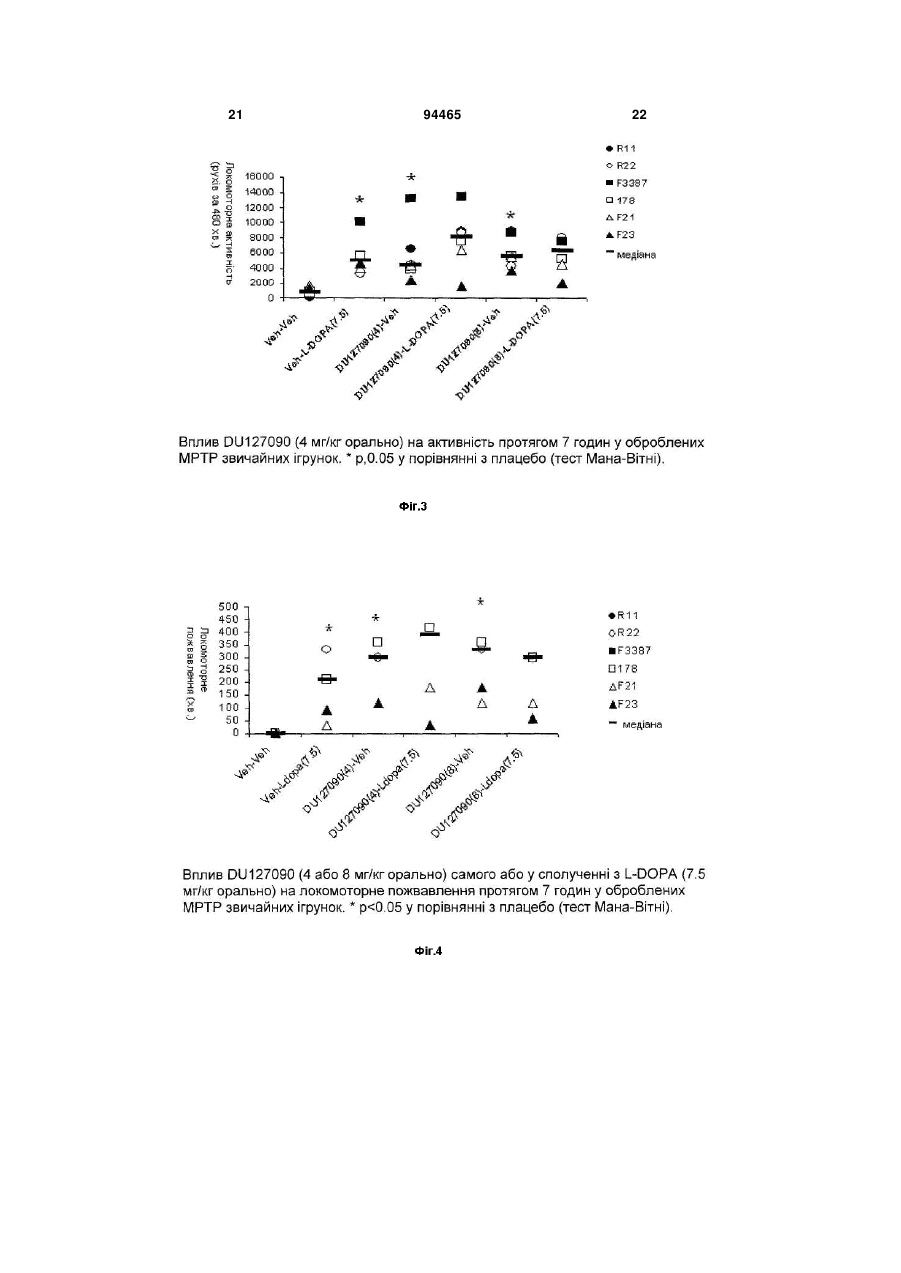
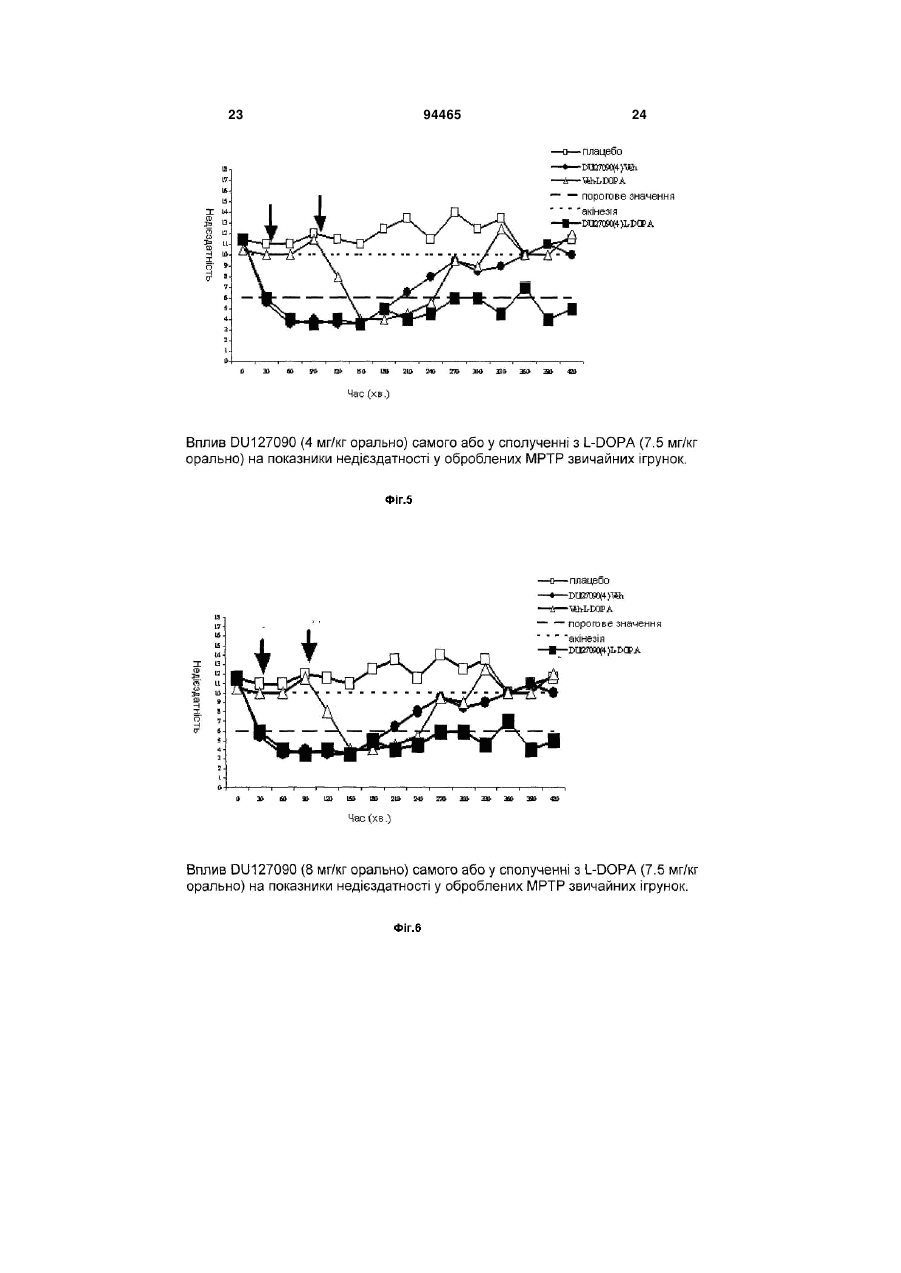
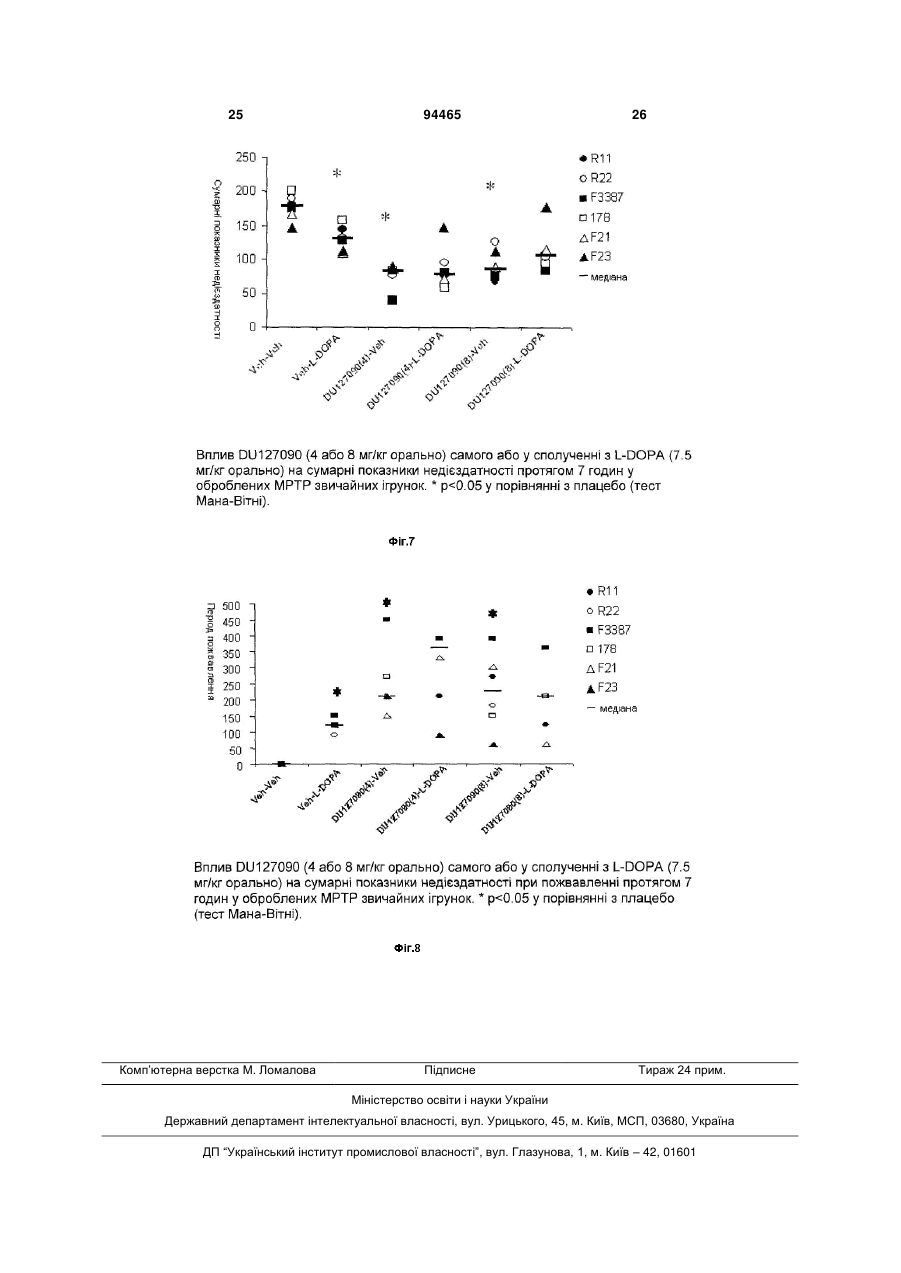
1. Комбінований препарат, який містить (і) біфепрунокс або його N-оксид: 2 3 9. Спосіб лікування хвороби Паркінсона або синдрому неспокійних ніг у хворих людей або тварин, що потребують такого лікування, згідно з яким хворому одночасно, нарізно або послідовно вводять кількість біфепруноксу або його N-оксиду чи фармакологічно прийнятної солі зазначених сполук та кількість L-DOPA, достатні для ефективного лікування. 94465 4 10. Спосіб за п. 9, згідно з яким додатково вводять інгібітор декарбоксилази та/або інгібітор СОМТ, та/або інгібітор МАО-В. 11. Застосування біфепруноксу або його N-оксиду при одержанні засобу для лікування синдрому неспокійних ніг. Галузь техніки Винахід стосується застосування комбінованого препарату біфепруноксу або його N-оксиду, або фармакологічно прийнятних солей цих сполук: Біфепрунокс та L-DOPA для одночасного, нарізного або послідовного прийому при лікуванні розладів, що потребують відновлення допамінергійної функції, зокрема, хвороби Паркінсона та синдрому бентежних ніг. ПЕРЕДУМОВИ СТВОРЕННЯ ВИНАХОДУ Такі симптоми, як постійна дриґота рук та ніг, рухи тіла, що поступово стають незграбними, уповільненими та послабленими, нерухомий вираз обличчя, мають місце протягом усієї історії людства. У 1817 р. Джеймс Паркінсон описав цю сукупність симптомів як 'paralysis agitans', а незабаром хворобу було названо іменем лікаря, котрий першим її описав. Патологічною причиною хвороби Паркінсона є руйнування нервових клітин у substantia nigra, ("темній речовині") - частині мозку, пов'язаній з м'язовими рухами. Втрата до 80% стріарного допаміну при хворобі Паркінсона призводить до чітких симптомів акінезії, закляклості та брадикінезії (Hornykiewicz, 1966). У хворих утруднені рухи, вони втрачають просторову стабільність та координацію. Сучасна фармакотерапія хвороби Паркінсона будується на відновленні допамінергійної функції (Blandini, 2000; Lledó, 2000). Допамін не долає кров'яний бар'єр мозку й не може безпосередньо використовуватися для лікування хвороби Паркінсона, тому користуються його безпосереднім прекурсором L-DOPA (лівозакрученим енантіомером 3,4-дігідроксіфенілаланину, або леводопа), який здатний проникати до мозку, де декарбоксилюється до допаміну. Але леводопа декарбоксилюється також і у периферійних тканинах, а тому лише незначна частка введеної леводопи потрапляє до мозку. Карбідопа інгібує декарбоксилювання лево N-оксид біфепруноксу допи у периферійних тканинах, але сама не долає кров'яний бар'єр мозку і не впливає на метаболізм леводопи у мозку. Сполучення карбідопи та леводопи вважається найефективнішими ліками від симптомів хвороби Паркінсона. Втім, за п'ять років застосування цього методу стали очевидні деякі його вади. Мірою поширення хвороби кожна доза діє усе коротший час ("ефект зношення"), а у деяких хворих мають місце непередбачувані переходи від пожвавлення до нерухомості й навпаки ("ефект маятника"). Періоди пожвавлення звичайно пов'язані з високими рівнями леводопи у плазмі й часто супроводжуються аномальними неконтрольованими рухами, наприклад, дискінезією. Періоди нерухомості корелюють з низькими рівнями леводопи та епізодами брадикінезії (Jankovic, 1993; Rascol, 2000). Це вимушує практичних лікарів проводити лікування допамінергійними агоністами, перш ніж вдаватися до L-DOPA-терапії. Однак застосування повних агоністів рецепторів допаміну, наприклад, апоморфину, бромкриптину, лізуриду, перголіду, праміпексолу або ропініролу, також має певні обмеження. Вони сприяють дискінезії, спричинюють психотичні симптоми, у тому числі галюцинації, ортостатичну гіпотензію, сонливість та інші бічні явища (Lozano, 1998; Bennett, 1999). Припускають, що це можна подолати застосуванням часткових агоністів рецепторів допаміну D2/3 (тобто сполук, які не стимулюють рецептори допаміну D2/3 у максимальному ступені) (Jenner 2002). Вважається, що такі сполуки можуть стимулювати рецептори допаміну D2/3 при низькому допамінергійному тонусі, водночас протидіючи надмірному стимулюванню рецепторів допаміну D2 при високому допамінергійному тонусі, що при 5 зведе до "стабілізації" передачі допаміну у мозку (Jenner, 2002). Агоністи рецепторів 5-НТ1А можуть попередити появу дискінезії, оскільки тандоспірон - агоніст рецепторів 5-НТ1А - зменшує дискінезію у хворих на хворобу Паркінсона, яких лікували L-DOPA (Kаnnаrі, 2002), та спричинені галоперидолом екстрапірамідальні бічні ефекти у приматів (Christoffersen, 1998). Нещодавно висунуто припущення, що саризотан - агоніст рецепторів 5-НТ1А та ліганд рецепторів допаміну - поліпшує симптоми дискінезії (Olanow, 2004; Bara-Jimenez, 2005; Bibbiani, 2001). Присутність агоністів рецепторів 5НТ1А може сприяти лікувальній дії часткових агоністів рецепторів D2/3 (Johnston, 2003). Останнім часом з'явилися різні комбіновані препарати, які містять L-DOPA та один або кілька інших інгібіторів ферментів. Відомі комбінації LDOPA/карбідопа (наприклад, Sinemet®), LDOPA/бенсеразид (наприклад, Madopar®) та LDOPA/карбідопа/ентакапон (наприклад, Stalevo®, (Jost, 2005)). Потім були запропоновані інгібітори катехоламін-О-метилтрансферази (СОМТ), наприклад, толкапон та ентакапон, як додаткова терапія до L-DOPA. Ці сполуки подовжують період напіврозпаду L-DOPA, не підвищуючи суттєво Сmах. Отже, вони відстрочують знесення, але водночас підвищують інтенсивність бічних ефектів, у тому числі дискінезії внаслідок пікових доз. Толкапон у деяких хворих виявляється токсичним для печінки. Іншим шляхом уповільнення метаболізму допаміну є застосування інгібіторів моноаміноксидази-В (МАО-В) у сполученні з L-DOPA. Втім, введення інгібіторів МАО пов'язане з низкою дебілізуючих ефектів, наприклад, нудотою, запамороченням, легкодумністю, непритомністю, черевним болем, розсіяністю, галюцинаціями, сухістю в роті, маренням наяву, дискінезією та головним болем, що обмежує їх застосування. Комбіновані препарати існують у найрізноманітніших сполученнях доз, оскільки з розвитком хвороби потрібні все більші дози L-DOPA, щоб утримати її під контролем. Комбіновані препарати у вигляді таблеток з фіксованим вмістом ліків є зручні у застосуванні, але обмежують гнучкість. Прикладом того, що комбінації з незмінними дозами не завжди корисні, є застосування селегілину - селективного інгібітору МАО-В для лікування хвороби Паркінсона. На ранній стадії хвороби селегілин може бути єдиним терапевтичним засобом; він у достатньому ступені уповільнює метаболізм ендогенного допаміну, щоб утримувати симптоми у припустимих межах. Але на подальших стадіях хвороби стає необхідним застосування L-DOPA. Коли ефективність L-DOPA починає зменшуватися, першим заходом стає застосування інгібітору декарбоксилази, наприклад, тієї ж карбідопи (див. вище), а коли й цього не вистачає, спільна терапія з селегілином поновлює ефективність L-DOPA, зменшуючи розклад допа 94465 6 міну, який утворюється з L-DOPA. Отже, на практиці L-DOPA та селегілин вводять в окремих формах - одночасно або послідовно. Хворі на синдром бентежних ніг (RLS; також відомий як синдром Екбома) по суті нездатні сидіти або навіть стояти спокійно. Вони не можуть займатися діяльністю, яка потребує нерухомого сидіння при обмеженій розумовій стимуляції (їзда у будь-якому транспорті, присутність на довгих нарадах, лекціях, у театрі або кіно тощо). Найбільше такі хворі страждають уночі. Хворі на RLS по суті неспроможні спати, а їхнє життя перетворюється на кошмар. Потреба рухатися, яка загострюється під час відпочинку, може бути задоволена лише рухом, наприклад, ходінням. Втім, лише-но рух припиняється, симптоми повертаються з ще більшою силою. Якщо хворого на RLS примусити лежати спокійно, симптоми наростають, як стиснута пружина, поки ноги не почнуть мимовільно рухатися, миттєво повертаючи симптоми. У хворого, який намагається лежати, ноги ритмічно або напівритмічно смикаються (Pollmacher, 1993). Ці рухи називають дискінезією наяву (DWA) (Неnіng, 1986) або частіше періодичним скороченням кінцівок наяву (PLMW). У клініці RLS діагностують за чотирма критеріями: (1) відчуттям позиву рухати кінцівками (звичайно ногами); (2) моторним збудженням, щоб пригасити це відчуття; (3) поверненням або підсиленням симптомів під час відпочинку; (4) чітко вираженими добовими загостреннями симптомів RLS; тобто симптоми погіршуються увечері та вночі (Allen, 2001). Існують різні методики лікування RLS, усі пов'язані з небажаними бічними ефектами. Лікування може включати застосування агоністів допаміну, інших допамінергійних засобів, бензодіазепинів, опіатів та протиконвульсійних засобів. Коли RLS є наслідком іншого стану, наприклад, вагітності, запущеної хвороби нирок, прийому еритропоетину або дефіциту заліза, усунення причини, наприклад, пологи або традиційна залізна дієта, здатні усунути або пом'якшити симптоми принаймні у деяких випадках (Allen, 2001). Однак лікувати RLS первинного походження ("ідіопатичний" RLS) набагато складніше. Допамінергійні засоби, як от леводопа, спочатку дають ефект, але з плином часу спостерігається звикання та й навіть підсилення симптомів у 80% хворих на RLS (Allen, 1996); те саме має місце з агоністами допаміну (Earley, 1996). Альтернативні засоби - бензодіазепини опіати та протиконвульсійні ліки - менш ефективні, ніж допамінергійні агенти (Chesson,1999; Неnіng, 1999). Незважаючи на варіювання режимів лікування, для 15-20% хворих будь-які ліки виявляються непридатними внаслідок шкідливих бічних ефектів та відсутності зрушень. Для 15-20% хворих будь-які ліки виявляються непридатними внаслідок бічних ефектів та малої ефективності. 7 Біфепрунокс DU 127090, 7-[4-([1,1'-біфеніл]-3-ілметил)-1піперазиніл]-2(3Н)-бензоксазолон, відомий як біфепрунокс, прив'язується до рецепторів типу допаміну D2 та рецепторів 5-НТ1А; він є частковим агоністом рецепторів допаміну D2/3 і частковим агоністом рецепторів серотоніну 5-НТ1А (WO 97/36893; Van Vliet, 2000; Feenstra, 2001, 2002; a,b Hesselink, 2003 ; Mealy, 2004). З WO 2007/023141 відомо, що in vivo N-оксид біфепруноксу швидко перетворюється на вихідну сполуку, отже, діє як "прекурсор". ДОКЛАДНИЙ ОПИС ВИНАХОДУ Метою винаходу є створення способу лікування, не менш ефективного, ніж L-DOPA, але позбавленого його бічних ефектів, зокрема, "ефекту маятника", що призводить до дискінезіїу фазі пожвавлення та епізодів брадикінезії у фазі нерухомості. Несподівано при дослідженні ігрунок, яких лікували МРТР (тваринна модель, що має прогнозну цінність для хвороби Паркінсона), було встановлено, що комбіноване лікування L-DOPA та біфепруноксом знижує пікову локомоторну активність, спричинену прийомом одного L-DOPA, настільки, що гіперактивність не спостерігається. Тривалість фази пожвавлення після прийому L-DOPA збільшується при спільному прийомі біфепруноксу. Сутність винаходу полягає у комбінованих препаратах біфепруноксу, або його N-оксиду, або їх фармакологічно прийнятних солей, гідратів чи сольватів з L-DOPA, а за бажанням також з інгібітором декарбоксилази, та/або, за бажанням, інгібітором СОМТ (катехоламін-О-метилтрансферази), та/або, за бажанням, інгібітором МАО-В (моноаміноксидази-В), для одночасного, нарізного або послідовного застосування при лікуванні розладів, що потребують відновлення допамінергійної функції, зокрема, хвороби Паркінсона та синдрому бентежних ніг. Винахід стосується використання біфепруноксу або його N-оксиду, справжнього прекурсору, у випадках, коли L-DOPA спричинює або може провокувати дискінезії. У таких випадках специфічна фармакологічна активність сполуки, а саме частковий агонізм до рецепторів допаміну D2 та допаміну D3, а також повний агонізм до рецепторів серотоніну 5-НТ1А, дозволяє блокувати дискінезію, не зменшуючи терапевтичну дію L-DOPA Винахід стосується фармацевтичних композицій, які містять (і) біфепрунокс, його N-оксид, або їх фармакологічно прийнятні солі, гідрати чи сольвати, 94465 8 N-оксид біфепруноксу (іі) L-DOPA у суміші з фармакологічно прийнятним ад'ювантом, розбавником або носієм Винахід також стосується наборів, які містять (і) посудину з вмістом біфепруноксу, його Nоксиду, або їх фармакологічно прийнятних солей, гідратів чи сольватів, за бажанням з домішкою фармацевтично прийнятного ад'юванта, розбавника або носія, (іі) посудину з вмістом L-DOPA, за бажанням з домішкою фармацевтично прийнятного ад'юванта, розбавника або носія, (ііі) вказівки для одночасного, нарізного або послідовного введення біфепруноксу та L-DOPA хворому, який їх потребує. Згідно з іншим аспектом винаходу пропонується спосіб виготовлення зазначеного набору або його елементів, за яким сполучують зазначений компонент (і) із зазначеним компонентом (іі) таким чином, що обидва компоненти стають придатними для введення у сполученні один з одним При сполученні обох компонентів компоненти (і) та (іі) можуть (і) постачатися як окремі композиції (незалежні одна від одної), які потім сполучають для спільного застосування у комбінованій терапії, або (іі) пакуватися та постачатися разом як окремі компоненти "комбінованої упаковки" для спільного застосування у комбінованій терапії. Також винахід пропонує спосіб лікування хворого, який страждає або є схильним до стану, при якому необхідне або бажане відновлення допамінерпйної функції, згідно з яким хворому вводять терапевтично ефективну кількість (і) біфепруноксу, його N-оксиду, або їх фармакологічно прийнятних солей, гідратів чи сольватів, за бажанням з домішкою фармакологічно прийнятного ад'юванта, розбавника або носія, (ii) L-DOPA, за бажанням з домішкою фармакологічно прийнятного ад'юванта, розбавника або носія. В іншому аспекті винаходу пропонується застосування фармацевтичних композицій, які містять: (і) біфепрунокс, його N-оксид, або їх фармакологічно прийнятні солі, гідрати чи сольвати, (ii) L-DOPA з домішкою фармакологічно прийнятного ад'юванта, розбавника або носія, для виготовлення засобу для лікування стану, при якому необхідне або бажане відновлення допамінергійної функції. 9 ВИЗНАЧЕННЯ Приклади інгібіторів декарбоксилази: карбідопа та бенсеразид. Приклади інгібіторів катехоламін-О-метилтрансферази (СОМТ): ентакапон, нітекапон та толкапон. До інгібіторів моноаміноксидази-В (МАО-В) належать: депренил, (-)-депренил (селегілин), десметилдепренил, Nпропаргіл-1-(R)-аміноіндан (разагалин), фенелзин (нарділ), транилципромин (парнат), CGP3466, фуразолідон, ізокарбоксазид, паргілин, метиклотіазид та прокарбазин. З метою точнішого опису деякі кількісні показники наводяться з виразом "біля". Незалежно від наявності або відсутності цього "біля" усі наведені кількісні значення є фактичні, а ступінь наближення цієї величини цілком зрозумілий для фахівця з урахуванням експериментальних та/або вимірювальних умов для такої величини. В описі та формулі термін "містити" та його варіанти на зразок "такий, що містить" або "містять" не включає інших добавок, компонентів, цілих чисел або операцій. Термін "композиція" у цьому винаході охоплює продукти, що містять зазначені компоненти у завданих кількостях або пропорціях, а також продукти, що утворюються прямо чи непрямо з комбінації зазначених компонентів у зазначених кількостях. Відносно фармацевтичних композицій йдеться про продукт, який містить один або кілька діючих компонентів та, за бажанням, носій з інертних компонентів, а також продукт, що є прямим або непрямим результатом комбінації, комплексоутворення або агрегатування двох чи більше компонентів, або розкладу одного чи кількох компонентів, або інших видів реакцій чи взаємодій між компонентами. Як правило, фармацевтичні композиції одержують рівномірним та ретельним змішуванням діючого компонента з рідким або подрібненим твердим носієм чи обома, після чого за потреби продукту надають завдану форму. У фармацевтичній композиції діючу сполуку вводять у достатній кількості для досягнення потрібної дії на хід стану або хвороби. Відповідно фармацевтичною композицією за винаходом є будь-яка композиція, одержана змішуванням сполуки за винаходом з фармацевтично прийнятним носієм. "Фармацевтично прийнятним" є носій, розбавник або наповнювач, сумісний з іншими інгредієнтами композиції та не шкідливий для хворого. У цьому описі під 'комбінованим препаратом' розуміється як власне комбінація біфепруноксу та інших засобів, фізично комбінованих в одному препараті, наприклад, таблетці або розчині для ін'єкцій, так і 'набір', що містить біфепрунокс та LDOPA у нарізних випускних формах разом з інструкцією, можливо з додатковими засобами, що полегшують користування компонентами, наприклад, етикеткою або кресленням. Власне комбінації за визначенням вводяться одночасно. Вміст набору можна вводити як одночасно, так і нарізно через будь-який проміжок часу. Терапія є одночасною або послідовною у залежності від властивостей інших ліків, як от початок та тривалість дії, рівні у плазмі, рівень допуску тощо, а також 94465 10 характеру хвороби, її стадії та особливостей даного хворого. Доза композиції, яка вводиться, залежить від показань, віку, ваги та статі хворого й визначається лікарем. Переважно доза становить від 0.01 мг/кг до 10 мг/кг. Типова добова доза діючих компонентів коливається у широких межах і залежить від різноманітних факторів, як от показання, спосіб введення, вік, вага та стать хворого, й визначається лікарем. Як правило, оральні та парентеральні дози знаходяться у межах від 0,1 до 1,000 мг суми діючих речовин на добу. Ця величина є достатньою, щоб викликати помітну лікувальну реакцію або поліпшення у системі тканин людини чи тварини. Точна ефективна кількість для даного хворого визначається його вагою та станом здоров'я, характером та стадією стану, який лікується, рекомендацій лікаря (дослідника, ветеринара, терапевта абощо) та обраної лікувальної процедури або комбінації процедур. Термін "терапевтично ефективна кількість" означає кількість лікарського засобу, яка здатна вилікувати або попередити той чи інший стан шляхом прийому сполуки за винаходом. Це достатня кількість для того, щоб спричинити відчутну реакцію загоєння, попередження або поліпшення стану у тканинній системі, у людини чи у тварини, наприклад, вилікувати або попередити один з тих станів, що перелічені тут. Точна ефективна кількість для даного суб'єкта залежить від його ваги, стану здоров'я, характеру та ступеню захворювання, від якого його лікують, рекомендацій лікаря (дослідника, ветеринара, терапевта або іншого клініциста), а також обраних ліків або сполучення ліків. Через те визначати ефективну терапевтичну кількість наперед недоцільно. Термін "фармацевтично прийнятна сіль" охоплює солі, які, на здоровий медичний розсуд, є придатні для застосування у контакті з тканинами людей та тварин, не спричинюючи небажаної токсичності, подразнення, алергічної реакції тощо, й відповідають позитивному критерію ефект/ризик. Фармацевтично прийнятні солі добре відомі фахівцям. Їх можна готувати на місці з виділених та очищених сполук за винаходом або уособицю реакцією з фармацевтично прийнятними нетоксичними основами чи кислотами, включаючи органічні та неорганічні кислоти, неорганічні та органічні основи. Фармацевтично прийнятні солі можна одержувати відомими прийомами, наприклад, змішуванням сполуки за винаходом з відповідною кислотою, наприклад, органічною чи неорганічною. "Введення у сполученні з" означає, що відповідні композиції біфепруноксу та L-DOPA вводять послідовно, нарізно та/або одночасно у ході лікування відповідного стану, який може бути хронічним або гострим. Переважно обидві композиції вводять (за бажанням повторно) через досить короткі проміжки часу, щоб чинити більшу цілющу дію для хворого протягом курсу лікування відповідного стану, ніж коли кожну з двох композицій вводять (за бажанням повторно) поодинці, у відсутності другої композиції, протягом такого ж курсу лікування. Визначення того, чи краще вводити таку комбінацію протягом курсу лікування того чи іншо 11 го стану, залежить від характеру стану, який лікують або попереджають, але це не становить труднощів для фахівця. Отже, термін "у сполученні з" стосується того, чи вводити одну або іншу з двох композицій (за бажанням повторно) до, після та/або водночас з другим компонентом. У такому разі терміни "введення одночасно" та "введення водночас" означають, що розрив у часі між введенням окремих доз біфепруноксу та L-DOPA не перевищує 48 годин, тобто 24 години, 18 годин, 12 годин, 6 годин, 3 години, 2 години, 1 година або 30 хвилин. Термін "лікування" стосується будь-якого лікування станів або хвороб ссавців, переважно людей, і включає: (1) інгібування хвороби або стану, тобто припинення її поширення, (2) вилікування хвороби або стану, коли її примушують відступити, або (3) усунення симптомів хвороби. Термін "медична терапія" охоплює профілактичні, діагностичні або лікувальні процедури, що проводяться in vivo або ex vivo на людях та інших ссавцях. "Суб'єктом" у цьому описі є тварина, зокрема, ссавець, переважно людина, котра є об'єктом лікування, нагляду або експерименту. ПРИКЛАДИ Обробка нейротоксином МРТР (1-метил-4феніл-1,2,3,6-тетрагідропіридин) призводить до вичерпання допаміну у хвістоподібному відростку та "паркінсонівській" поведінці у людей та приматів (Lange, 1992; Langston, 1984; Langston, 1986). ПРИКЛАД 1: Взаємодія між біфепруноксом та L-DOPA Тварини: у дослідах використовують дорослих ігрунок (Callithrix jacchus; n=6, вік від 3 до 5 років; 5 самок та 1 самець), оброблених МРТР (2 мг/кг підшкірно кожного дня протягом 5 діб), які виявляли стабільний моторний дефіцит. Ці тварини реагували на L-DOPA. В них не викликали попередньо дискінезію з метою експерименту, хоча деякі ознаки дискінезії мали місце. Медикаментозне лікування: Біфепрунокс мезилат суспендують у 10% розчині сахарози та вводять орально через зонд у дозі 2.0 мл/кг. L-DOPA: Метилефір L-3,4-дігідроксіфенілаланіну (L-DOPA) (фірми Sigma, Велика Британія) розчиняють у 10% сахарози та вводять дозу 2 мг/кг через зонд. Карбідопу (фірми Merck, Sharp and Dohme, Велика Британія) суспендують у 10% сахарози та вводять дозу 2 мл/кг прямо до рота тваринам. Домперидон: (2.0 мг/кг орально, фірми Sigma, Велика Британія) розчиняють у 10% сахарозі та вводять за 60 хв. до біфепруноксу у дозі 2.0 мл/кг. Біфепрунокс (4 або 8 мг/кг орально у перерахунку на вільну основу) або його носій (10% розчин сахарози) вводять окремо та у комбінації з L-DOPA (7.5 мг/кг орально у перерахунку на вільну основу, у комбінації з карбідопою, 12.5 мг/кг орально) обробленим МРТР ігрункам (n=6). Тварини одержують біфепрунокс або його носій за 90 хв. до введення LDOPA або її носія. Карбідопу дають за 30 хв. до введення L-DOPA. Домперидон дають за 60 хв. до введення біфепруноксу. Вивчення поведінки: В усіх дослідах тваринам дають акліматизуватися до клітин для вивчення 94465 12 поведінки за 1 годину до введення препаратів. Тварин вміщують поодинці до дослідницьких кліток (506070 см) з прозорими дверима для спостереження. Кожна клітка обладнана 8 горизонтально орієнтованими випромінювальними інфрачервоними фотоелементами та достатньою кількістю датчиків, щоб спостерігати якнайбільше рухів. Локомоторну активність визначають як кількість перетинів світлового променю внаслідок рухів тварини за 10-хвилинні інтервали у період до 7 годин. Тваринам дають 60 хвилин на акліматизацію й визначають вихідну активність до прийому ліків. Поріг фази пожвавлення визначають як 3кратне перевищення рівня активності до прийому ліків у мавп, оброблених МРТР. Гіперактивністю вважається 3-кратне перевищення рівня активності нормальних мавп, яких не піддавали експерименту. Пожвавленням вважається період часу у хвилинах, коли активність перевищує цей поріг. Тваринам дають біфепрунокс, плацебо та/або LDOPA. Після введення ліків тваринам дають принаймні 3 дні відпочинку перед наступним дослідом, щоб забезпечити адекватну оцінку їх стану. Локомоторну активність, рушійну неспроможність та наявність дискінезії визначають наступним чином: Локомоторна активність: В усіх дослідах тваринам дають акліматизуватися до клітин для вивчення поведінки за 1 годину, після чого здійснюють введення відповідних препаратів. Далі оцінюють протипаркінсонівську активність тварин у проміжках часу до 6 годин за допомогою автоматизованих кліток для дослідження активності, причому недієздатність оцінює спостерігач, не знайомий з тим, якій тварині який препарат введено. Локомоторним пожвавленням вважається проміжок часу, коли активність тварин втричі перевищує вихідну активність або активність, прийняту за 100, у залежності від того, що більше. Ранжування недієздатності та дискінезії: Недієздатність та дискінезію оцінюють до початку досліду та протягом останніх 10 хвилин кожного 30хвилинного періоду після введення біфепруноксу на протязі 6 годин після введення. Використовують таку шкалу рейтингу недієздатності: Рейтинг недієздатності: Дисфункцію вимірюють за шкалою недієздатності; жвавість (нормальна = 0, сонність 2); стриманість рухів (присутня = 0, зменшена = 1, відсутня = 2); уважність та рухи очей (нормальна 0, ненормальна 1); поза (нормальна = 0, ненормальне положення тулуба +1, ненормальне положення хвоста + 1, ненормальне положення кінцівок + 1, особливо ненормальна поза = 4); утримання рівноваги та координації рухів (нормальне = 0, погіршене = 1, нестійкість = 2, часті падіння = 3); вокалізація (нормальна = 0, знижена = 1, відсутня = 2); рухливість (нормальна = 0, брадикінезія або гіперкінезія = 1, акінезія або гостра гіперкінезія = 2). За потреби дають заспокійливі препарати. Пожвавлення визначають як період, коли сума очок показників недієздатності становить 6 або менше (порогове значення). Дані та статистичний аналіз: Дані представлені як медіанна локомоторна активність (рухів за 30 хв.) або кількість очок недієздатності (за 10 хв. 13 30-хвилинного періоду) протягом 7 годин експерименту, або ж як сумарна локомоторна активність (рухів за 420 хв.) чи недієздатність (сума очок за 420 хв.). Дані аналізують дисперсійним аналізом за Краскалом-Воллісом та апостеріорним тестом Мана-Вітні, де потрібно. Поправку на численні порівняння вносять за формулою: Припустима імовірність = /кількість порівнянь, де =5% Групі тварин, відокремленій від піддослідних, дають плацебо та використовують їх для статистичного порівняння. ПРИКЛАД 2: Вплив біфепруноксу на спричинене L-DOPA послаблення рушійної неспроможності Локомоторна активність: L-DOPA (7.5 мг/кг орально) плюс карбідопа (12.5 мг/кг орально за 30 хв. до L-DOPA) підвищує локомоторну активність у порівнянні з плацебо (фіг.1, 2, 3 та 4) одразу після введення. Пікова активність (медіанна 1627, інтервал 832-2289 рухів за 30 хв.) досягається у період від 60 до 180 хв. після введення LDOPA. Медіанна тривалість активності (пожвавлення) становить 180 хв/420 хв. (фіг.4). Сумарна локомоторна активність та локомоторне пожвавлення довші, ніж у тварин, які отримують плацебо (р
ДивитисяДодаткова інформація
Назва патенту англійськоюCombination preparations comprising bifeprunox and l-dopa
Автори англійськоюMccreary Andrew C., van Scharrenburg Gustaaf J.M., Tulp Martinus T. M.
Назва патенту російськоюКомбинированные препараты с содержанием бифепрунокса и l-dopa
Автори російськоюМаккрири Эндрю К., ван Шарренбург Густаф Й.М., Тульп Мартинус Т.М.
МПК / Мітки
МПК: A61K 31/496, A61P 25/14, A61P 25/16, A61K 31/195
Мітки: вмістом, l-dopa, біфепруноксу, комбіновані, препарати
Код посилання
<a href="https://ua.patents.su/13-94465-kombinovani-preparati-z-vmistom-bifeprunoksu-ta-l-dopa.html" target="_blank" rel="follow" title="База патентів України">Комбіновані препарати з вмістом біфепруноксу та l-dopa</a>
Попередній патент: Виділене антитіло до dll4 та його застосування
Наступний патент: Комбіновані препарати з вмістом slv308 та l-dopa
Випадковий патент: Пристрій для очищення, збирання та складування електростатично заряджених матеріалів