Спосіб отримання похідних тіазолу та їх солей з лужними металами
Номер патенту: 5585
Опубліковано: 28.12.1994
Автори: Хітосі Мііда, Масакі Сінода, Томеі Огурі, Єсіо Хаясі, Мікіо Цуцуі, Кацуо Такахасі
Формула / Реферат
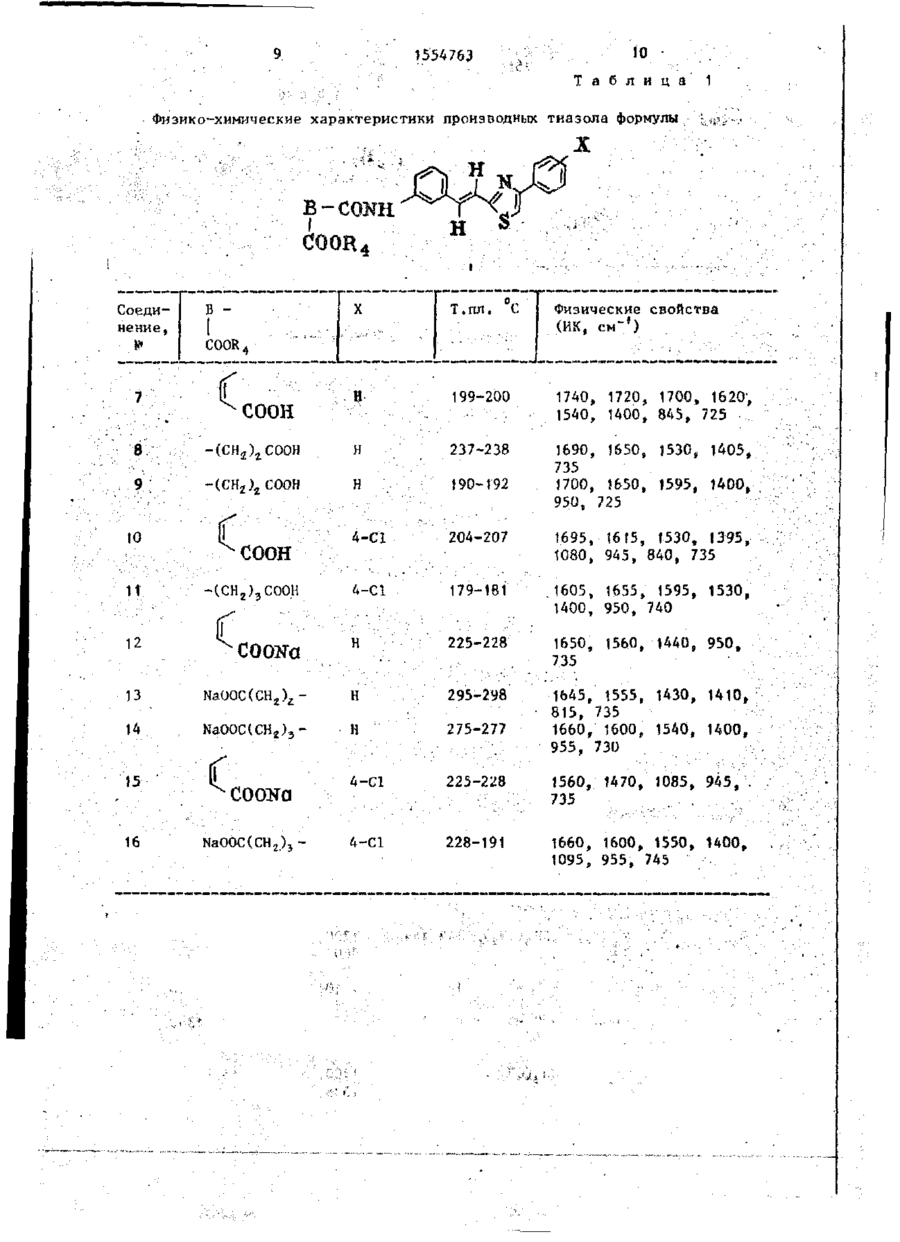
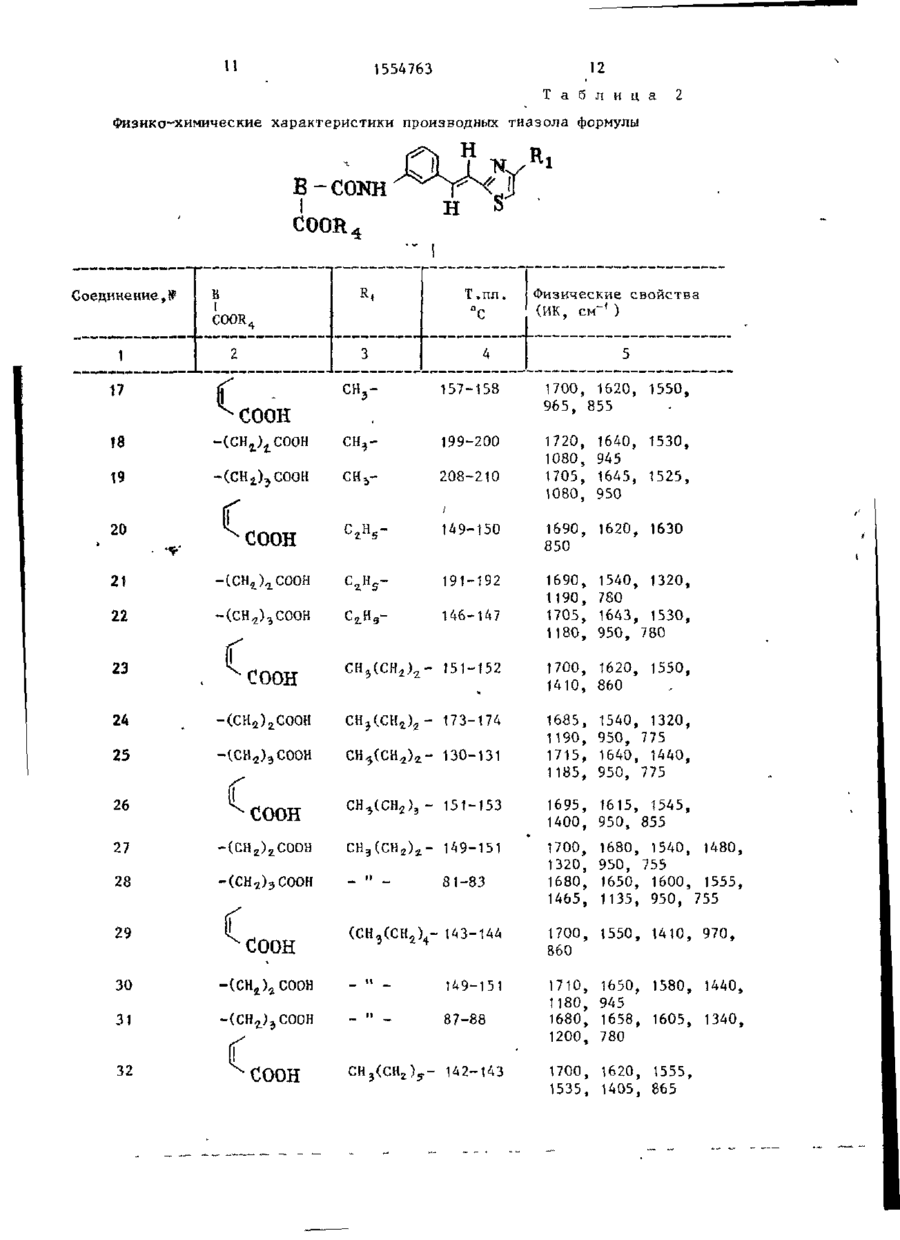
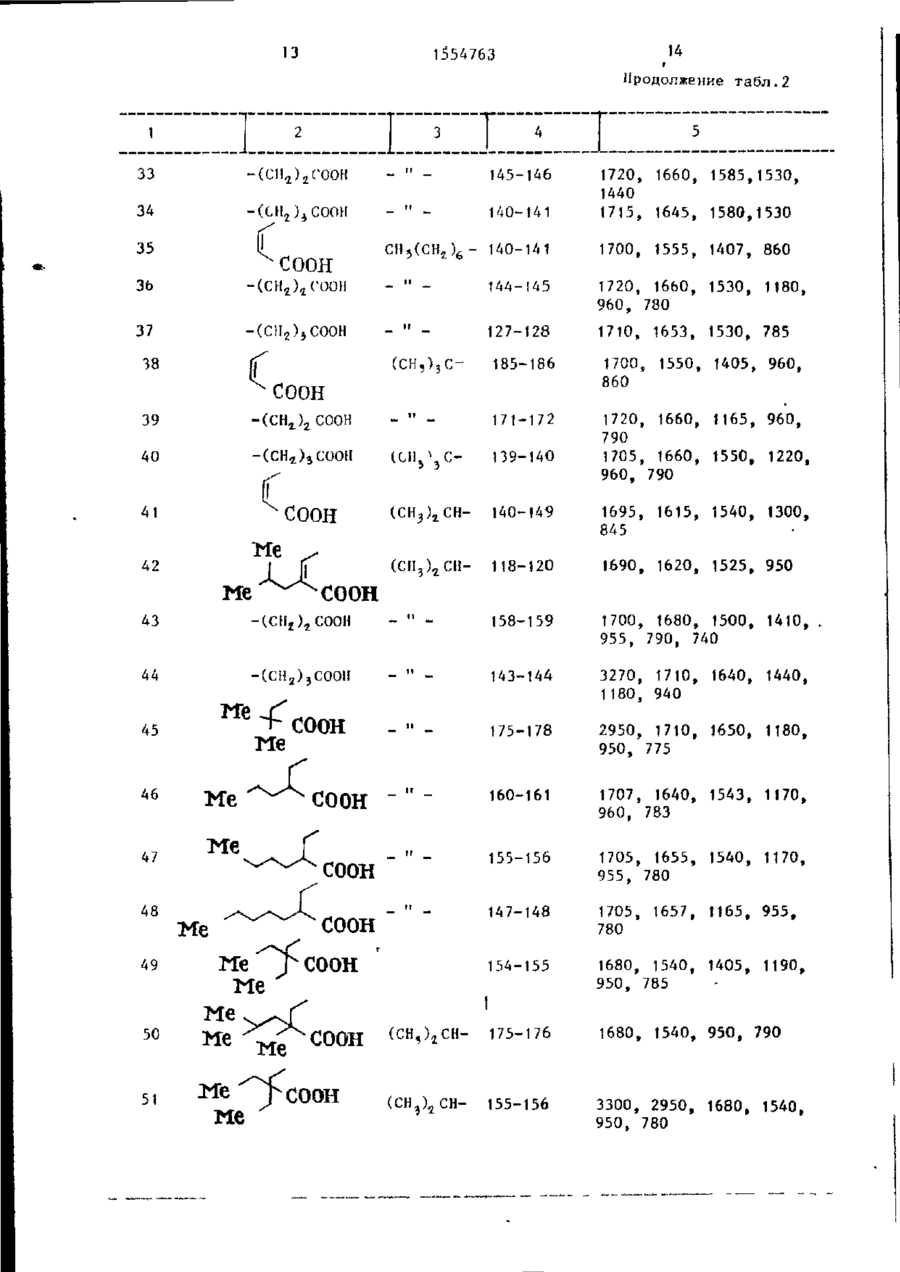
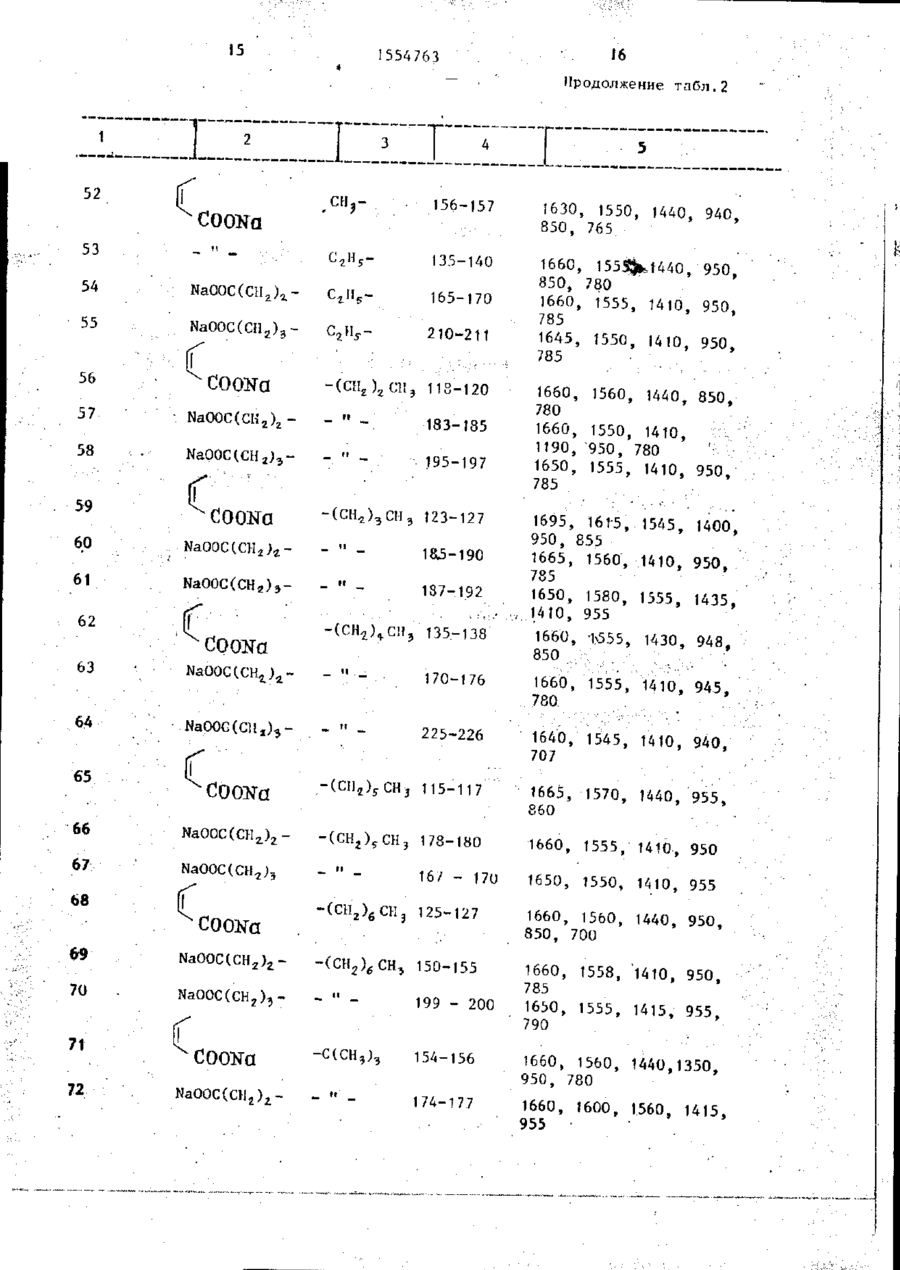
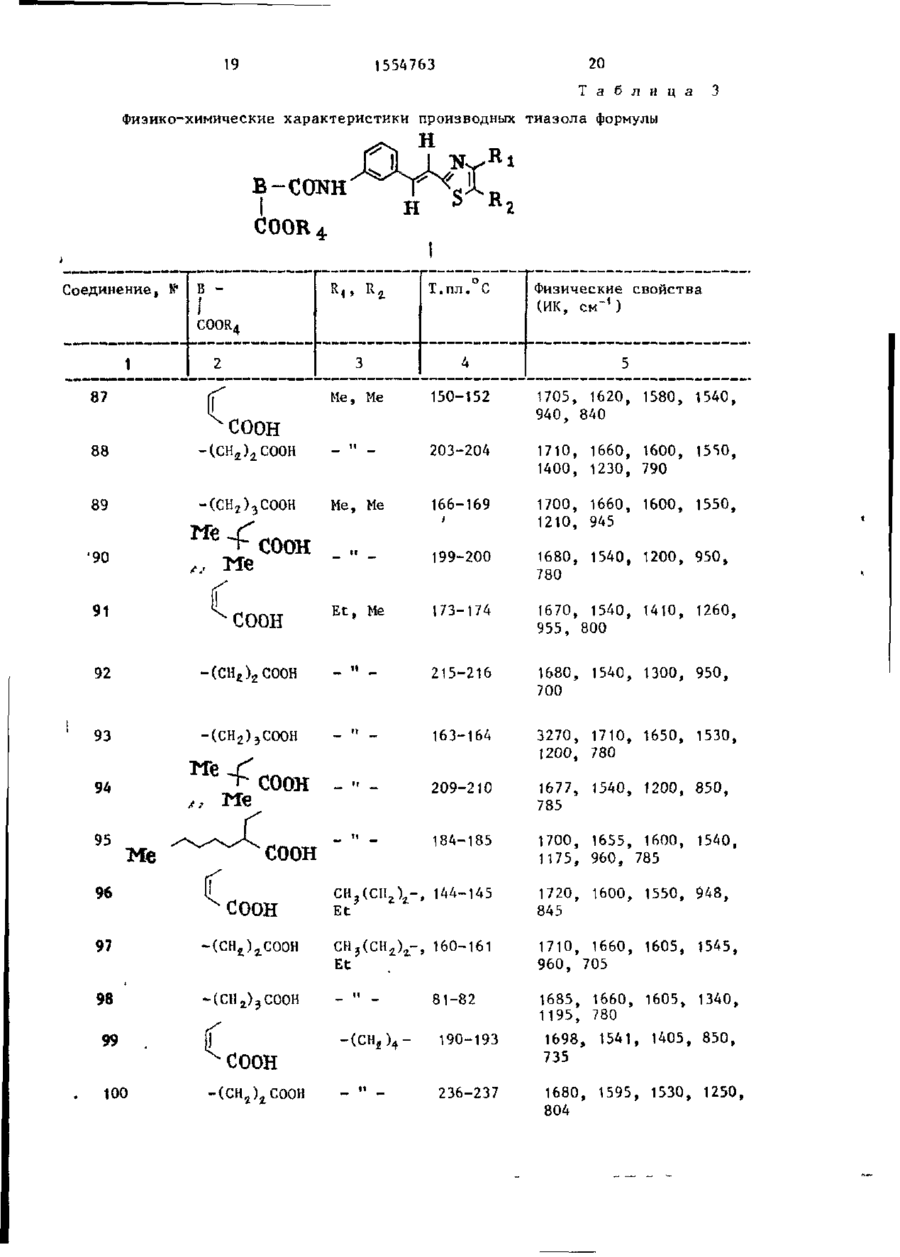
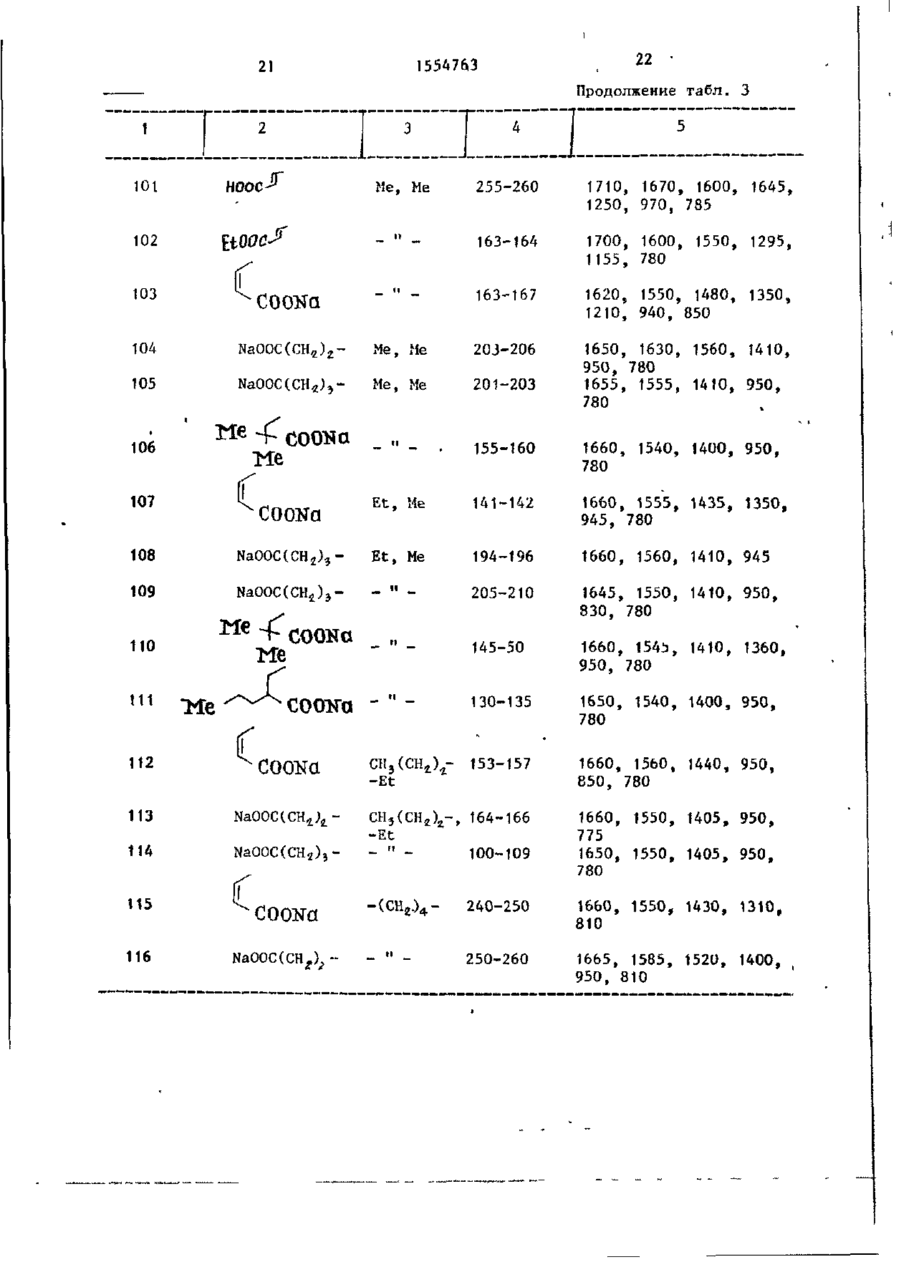
Способ получения производных тиазола общей формулы
где R1 - С1-С8-алкил, С1-С4-алкоксикарбонил, фенил или фенил, замещенный атомом галогена, С1-С4-алкилом, С1-С4-алкоксирадикалом или С1-С4-алкоксикарбонилом;
R2 - водород или С1-С8-алкил или R1 и R2 вместе образуют тетраметиленовую группу, соответствующую конденсированному циклогексановому кольцу, или бутадиениленовую группу, незамещенную или замещенную атомом галогена, С1-С4-алкилом, С1-С4-алкоксильным радикалом или С1-С4-алкоксикарбонилом, соответствующую конденсированному бензольному кольцу;
R3 - водород или галоген, гидрокси- или С1-С5-алк
оксигруппа;
R4 - водород или С1-С5-алкил,
А-С2-С3-алкилен, в котором одна метиленовая группа может быть замещена на атом кислорода или группу NН, винилен, карбоамидо- или виниламидогруппа;
В - простая химическая связь или двухвалентная углеводородная группа, содержащая 1-3 атома углерода в связующей цепи, или в случае, когда R4 водород, или их солей с щелочными металлами, отличающийся тем, что соединение общей формулы
где R1, R2, R3 и A имеют указанные значения, подвергают взаимодействию с соединением общей формулы
Z-В-СООR4,
где В и R4 имеют указанные значения,
Z - группа -СОХ, где Х- атом галогена, или 2 и R4 совместно образуют группу -СО-; в среде в качестве растворителя ароматического углеводорода, простого эфира или галогенирован-ного углеводорода, при температуре от 0°С до температуры кипения реакционной смеси в случае, когда Z и R4 совместно образуют группу -СО-, или в присутствии органического или неорганического основания при температуре от 0 до 100°С, когда Z руппа -СОХ, где Х имеет указанное значение, и целевой продукт выделяют в свободном виде или в случае, когда R4 - водород, в виде соли с щелочным металлом.
Текст
Изобретение относится к гетероциклическим соединениям, в частности к получению производных тиазола ф-лы 1 ОХ со 1554763 * по каплям при 0°С при перемешивании действием в отношении леикотриена и и нагревают при 50°С 1,5 ч. Реакционмогут найти применение в медицине ную смесь выливают в ледяную воду, для профилактики и лечения аллергиобразованные кристаллы собирают фильтческих заболеваний, вызванных лейрованием и высушивают. Последующая котриеном. перекристаллизация из хлороформа Целью изобретения является полудает 2,5 г (выход 90%) указанного чение новых соединений ряда тиазола, в заголовке вещества. обладающих новым видом биологической активности в этом ряду соединеТ.пл. 193-194°С. 10 1 ний. ИК, ^ , ct-Г : 3325; 1715; 1700; 1300, 730. П р и м е р 1, Получение 2П р и м е р 4, Получение 2-[транс-З-(цис-З-карбоксипропенамид) -Гтранс-3-(цис-3-ндоамилоксикарбонилстиршГ]бензотиазола (соединение № 1 ) . пропенамидо стирил]] бензотиазола К 8 мл толуола добавляют 158 мг (соединение № 4 ) . 2-(транс-3-аминостирил)-бензотиазола и 71 мг малеиноэого ангидрида и К 6 мл гексаметилфосфортриамида смесь нагревают при 80°С в течение добавляют 1,0 г натриевой соли 21 ч. После охлаждения до комнатной -транс-З-(цис-З-карбоксипропенамидо) температуры образованные кристаллы 20 стирил бензотиазола и 2,13 г изособирают фильтрованием и перекристаламилйодида и перемешивают смесь при лизовывают из этанола, что дает комнатной температуре 4 ч. Реакцион194 мг (выход 88%) указанного в загоную смесь экстрагируют толуолом ловке соединения в виде желтоватообычным образом, экстракт высушивают белого вещества. 25 над безводным сульфатом магния, Т.пл. 190-191°С. растворитель выпаривают при пониженИК,3 , см"1 : 1700; 1625; 1550; ном давлении. Последующая перекрис1490,- 1405;- 953. таллизация остатка из смеси этилового эфира с толуолом дает 616 мг (выход Здесь и далее ИК снимают с исполь55%) указанного в заголовке соединезованием таблеток КВг. 30 ния. П р и м е р 2. Получение 2Т.пл. 82-83°С. ~(транс-3-оксалиламиностирил)-4-феИК,3 , с м " 1 : 3400; 1720; 1660; нилтиазола (соединение № 2 ) . 1580; 1440; 1200; 755. К суспензии 1,0 г 2-(транс-3Пример 5. Получение 2-этилоксалиламиностирил)-4-фенил35 -|Гтранс-3-(цнс-3-карбоксипропенами~ тиазола, получаемого по примеру 3, до) стирилТ бензотиазола натриевой в 40 мл диоксана добавляют при интенсоли (соединение № 5 ) . сивном перемешивании, 1 мл 20%-ного водного раствора гидроокиси калия и К 350 мл метанола добавляют 17,3 г проводят гидролиз при комнатной 2-[Уранс-3-(цис-3-карбоксипропенами~ 40 до) стирил]]бензотиазола и затем расттемпературе в течение 1 ч. К реакционной смеси добавляют 20%-ную хловор 9,1 г бикарбоната натрия в ристо-водородную кислоту для доведе75 мл воды, после чего нагревают ния рН до 1-2, Образованные желтые с обратным холодильником в течение осадки собирают фильтрованием, промы1 ч. Растворитель выпаривают при по45 ниженном давлении и неочищенные крисвают этанолом и хлороформом, затем высушивают при пониженном давлении, таллы остатка промывают этанолом и что дает 870 мг (выход 94%) указанэтиловым эфиром. После высушивания ного в заголовке соединения. при пониженном давлении получают Т.пл. 291-292°С. 1,11 г (выход 97%) указанного в за50 головке соединения. ИК, 3 , см- 1 : 1715; 1685; 1590; 1520; 1300; 1180; 740. Т.пл. 239-240°С. П р и м е р 3. Получение 2ИК,$ , с м " ' : 1360; 1570; 1410; -(транс-3-этилоксалиламиностирил)-4940; 760. -фенилтиазола (соединение № 3 ) . П р и м е р 6. Получение 255 -Гтранс-3-(цис-2-карбоксициклогекК 30 мл толуола добавляют 0,7 г саноил) аминостиршЛбензотиазол пиридина, 2,0 г 2-(транс-3-аминости- ' К-метил-О-глюкаминовой соли (соедирил)-4-фенилтиаэола и раствор 1,1 г нение № в) . этилоксалил хлорида в 5 мл толуола, 5 . 1 554763 6 динение I 5 ) , 10 г триглицерида f В растворяющую соль 6 мл метанола насыщенной жирной кислоты, имеющей и 1 мл воды добавляют 96 мг N-месреднюю длину цепи и 0t2 г моноолетилЧЗ-глюкамина и 200 мг 2-[трансата сорбитана хорошо перемешивают и -3-(цис-2-карбоксициклотексаноил) ^ каждые 15,2 мг смеси отвешивают в аминостирил] бензотиазола и смесь 5 мл алюминиевый сосуд для аэрозоля. перемешивают при комнатной темпераЗатем каждый сосуд заполняют при туре 30 мин. После выпаривания растнизкой температуре порцией 84,8 мг ворителя при пониженном давлении фреона 12/1 14 (смесь 1:1), сосуд получаются неочищенные кристаллы, 10 снабжен дозатором для количественной которые перекристаллизовывают из подачи активного препарата в размеэтанола с этиловым эфиром, что дает . ре 100 гаї на 1 опрыскивание. Это 215 мг (выход 73%) соединения, укапозволяет получить прибор для ингазанного в заголовке. ., ляции, обеспечивающий количественТ.пл. 111-115°С, 245-246°С. ную дозу опрыскивания, 5 мл сосуд м ИК, 3 , с м : 1680; 15А0; 1410; которого содержит 5 мг указанного 1080; 750. выше соединения,, Аналогично примерам 1-6 получают П р и м е р 10. Установление производные тиазола, физико-химичес20 антагонистического действия относикие характеристики которых припедены тельно SKS (медленно реагирующего в табл. 1-4, вещества) in vitro. У самца морской свинки породы "Хартлей" весом П р и м е р 7. Изготовление таб2ОО-4ЬО г удаляют концевую часть леток. 1000 г тщательно измельчен-,с подвздошной кишки и после промывания ной до порошкообразного состоянии просвета протока закрепляют в 5 мл натриевой соли 2-Гтранс-3-(цис-3ванночке для обработки тканей, со-карбоксипропенамидо) стирил"] беи зодержащей раствор Тайлорда следующего тиазола (соединение N 5 ) , 5900 г лак* состава, мМ: NaCl 136; КС1 2,7; тозы, 2000 г кристаллической целлюлозы, 100 г оксипропилцеллюлозы с ма- ^п NaHCO^ 11,9-, M g C U 1.05; СаС1 а 1.8; NaH^PO^ 0,4 и глюкоза 5,6. Темпелой степенью замещения и 100 г стеаратуру в ванночке поддерживают 37 С.' рата магния тщательно перемешивают Аэрацию производят смесью 95%-ного и формуют в виде плоских таблеток кислорода и 5%-нсго углекислого газа» по методу непосредственного таблетиВо избежание сокращения под дейстрования. Каждая таблетка содержит 35 виєм гистамина и ацетнлхолина, к 10 мг указанного соединения в указанному раствору добавляют 100 мг массы таблетки. На плоскую Ю ~ 7 г/мл мениламина н 5 М 0 ~ г/мл таблетку наносят покрытие из сахара атропина. Изотоническое измерение или же пленочное покрытие Таким изменения напряжения в граммах пропутем получают осахаренную таблетку и таблетку с пленочным покрытием. 40 водят посредством изотонического преобразователя (trausducer) (ТоргоП р и м е р 8. Изготовление капвое наименование ТД-112 S, фирма сул. 1000 г тщательно измельченного изготовитель Ниппон Коден), конвердо порошкообразного состояния 2тора смещения напряжения и регистри-[транс-3-Сцис-3-карбокеипропеламирующего прибора "Ректикодер" (Торгодо) стирилІбєнзотиазола в виде натвое наименование RTG-4124, фирма изриевой соли (соединение N 5), 30U0 г " готовитель Ниппон Коден). Отрезок кукурузного крахмала, 6900 г лактоподвздошной кишки подвергают пассивзы, 1000 г кристаллической целлюлоной нагрузке при растягивающем усизы и 100 г стеарата магния перемеши^ лии 0,5 г и получают реакцию в виде вают и используют для заполнения сокращения кишки под воздействием капсул, каждая из них содержит 10 мг SRS, экстрагированного из легкого указанного соединения в 120 мг капморской свинки. Для контроля испольсуле. зуют степень сохраняющегося сокращеП р и м е р 9. Изготовление преSS ния от воздействия 1 единицы SRS парата для ингаляции. 5 г натриевой (соответствующей 5 нг гистамина),. соли 2-[транс~3-(цис~3-карбоксипраВ ванночку для ткани добавляют пенамидо) стиршт] бензотиазола, тщаиспытуемые лекарственные препараты тельно измельченного в порошок (сое 8 1554763 в различных концентрациях. Результаты, выраженные в единицах минимальной эффективной концентрации, которая представляет концентрацию испытуемого лекарственного препарата, ослабляющую сокращение при контрольном опыте на 50% ( 1 С 5 0 ) , показаны в табл.5. П р и м е р 11. Антагонистичес10 кое действие относительно ГГДд при опыте in vivo. У 4 самцов морской свинки породы "Хартлей" весом 350500 г измеряют под уретановым наркозом сопротивляемость пути для про15 хождения воздуха, применяя респиратор типа Гарварда, соответственно модифицированному методу КонцеттаРасслера. Результаты вычисления ингибирования (%), достигнутого бла20 годаря интрадуоденальному введению с лечебной целью испытуемого лекарственного препарата против повышения сопротивляемости пути для прохождения воздуха, обусловленного 25 внутривенным введением ЪТД 4 в количестве 0,1-1,0 мкг/кг, показаны в табл.6„ с П р и м е р 12. Испытание на острую токсичность. От 4 до 5 самцам 30 мышей породы "ddy" возрастом 6 недель в качестве 1 группы, вводят через рот соединение согласно предлагаемому способу в виде суспензии в 1%-ном растворе трагананта. Наблюдение проводят в течение 7 дней. Изучают число погибших мышей. Полученные результаты приведены в табл.7. Таким образом, производные тиазола, получаемые по предлагаемому спо40 собу, проявляют антагонистическое действие в отношении лейкотриена и являются очень мало токсичными соединениями. Ф о р м у л а и з о б р е т е н и я де метиленовую группу, соответствующую конденсированному циклогексановому кольцу, или бутадиениленовую группу, незамещенную или замещенную атомом галогена, С
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for preparation of thiazole derivatives and salts thereof with alkali metals
Назва патенту російською?????? ????????? ??????????? ??????? ? ?? ????? ?? ????????? ?????????
МПК / Мітки
МПК: A61K 31/428, A61P 37/08, C07D 277/20, C07D 277/24, C07D 277/28, C07D 417/12, A61K 31/426, A61P 43/00, C07D 277/22, C07D 277/56, C07D 277/64, C07D 277/30, A61K 31/425, C07D 277/82
Мітки: лужними, отримання, спосіб, солей, металами, похідних, тіазолу
Код посилання
<a href="https://ua.patents.su/14-5585-sposib-otrimannya-pokhidnikh-tiazolu-ta-kh-solejj-z-luzhnimi-metalami.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання похідних тіазолу та їх солей з лужними металами</a>
Попередній патент: Спосіб боротьби з бур’янами у посівах сорго
Наступний патент: Машина для глибоког0 друку
Випадковий патент: Біологічно активна композиція і безалкогольний освіжаючий напій