Композиція антитіла офатумумабу
Номер патенту: 107557
Опубліковано: 26.01.2015
Автори: Брісбейн Шарлін Е., Лешмар Улла Тове, Кеткар Амол Шарад
Формула / Реферат
1. Композиція антитіла офатумумабу, що містить офатумумаб у концентрації 20-300 мг/мл, де композиція додатково містить 50 мМ ацетату натрію, 51 мМ хлориду натрію, 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН якої скоректований до 5,5.
2. Композиція за п. 1, представлена у формі, придатній для введення внутрішньовенним або підшкірним шляхом ссавцеві, що цього потребує.
3. Композиція за п. 2, де ссавець страждає на захворювання, в якому задіяні клітини, що експресують CD20, вибрані з групи, що складається з онкогенних та імунних захворювань.
4. Композиція за п. 3, де захворювання, в якому задіяні клітини, що експресують CD20, вибрані з групи, що складається з онкогенних та імунних захворювань.
5. Композиція за п. 4, де онкогенними захворюваннями є В-клітинні лімфоми, вибрані з групи, що складається з: лімфобластного лейкозу/лімфоми з попередників В-клітин і пухлини із зрілих В-клітин, такі як В-клітинний хронічний лімфоцитарний лейкоз (СLL)/дрібноклітинна лімфоцитарна лімфома (SLL), В-клітинний пролімфоцитарний лейкоз, лімфоплазматична лімфома, лімфома з клітин мантійної зони (MCL), фолікулярна лімфома (FL), включаючи низькодиференційовану, середньодиференційовану і високодиференційовану FL, шкірну лімфому з клітин фолікулярного центру, В-клітинну лімфому з клітин маргінальної зони (MALT тип, вузловий або селезінковий тип), волосатоклітинний лейкоз, дифузна В-крупноклітинна лімфома, лімфома Беркітта, плазмоцитома, мієломна хвороба, посттранплантаційний лімфопроліферативний синдром, макроглобулінемію Валденстрема, анапластичну крупноклітинну лімфому (ALCL).
6. Композиція за п. 4, де імунне захворювання вибране з групи, що складається з: псоріазу, псоріатичного артриту, дерматиту, системної склеродермії та склерозу, запальних захворювань кишечнику (IBD), хвороби Крону, виразкового коліту, респіраторного дистрес-синдрому, менінгіту, енцефаліту, увеїту, гломерулонефриту, екземи, астми, атеросклерозу, порушення адгезії лейкоцитів, розсіяного склерозу, синдрому Рейно, синдрому Шегрена, ювенільного діабету, синдрому Рейтера, синдрому Бехчета, імунокомплексного нефриту, ІgА нефропатії, ІgМ полінейропатії, імуно-опосередкованої тромбоцитопенії, такої як гостра ідіопатична тромбоцитопенічна пурпура і хронічна ідіопатична тромбоцитопенічна пурпура, гемолітичної анемії, міастенії гравіс, вовчакового нефриту, системного червоного вовчаку, ревматоїдного артриту (РА), атопічного дерматиту, пухирчатки, хвороби Грейвса, тиреоїдиту Хашимото, грануломатоза Вегенера, синдрому Оменна, хронічної ниркової недостатності, гострого інфекційного мононуклеозу, ВІЛ і захворювань, пов'язаних з вірусом герпесу.
Текст
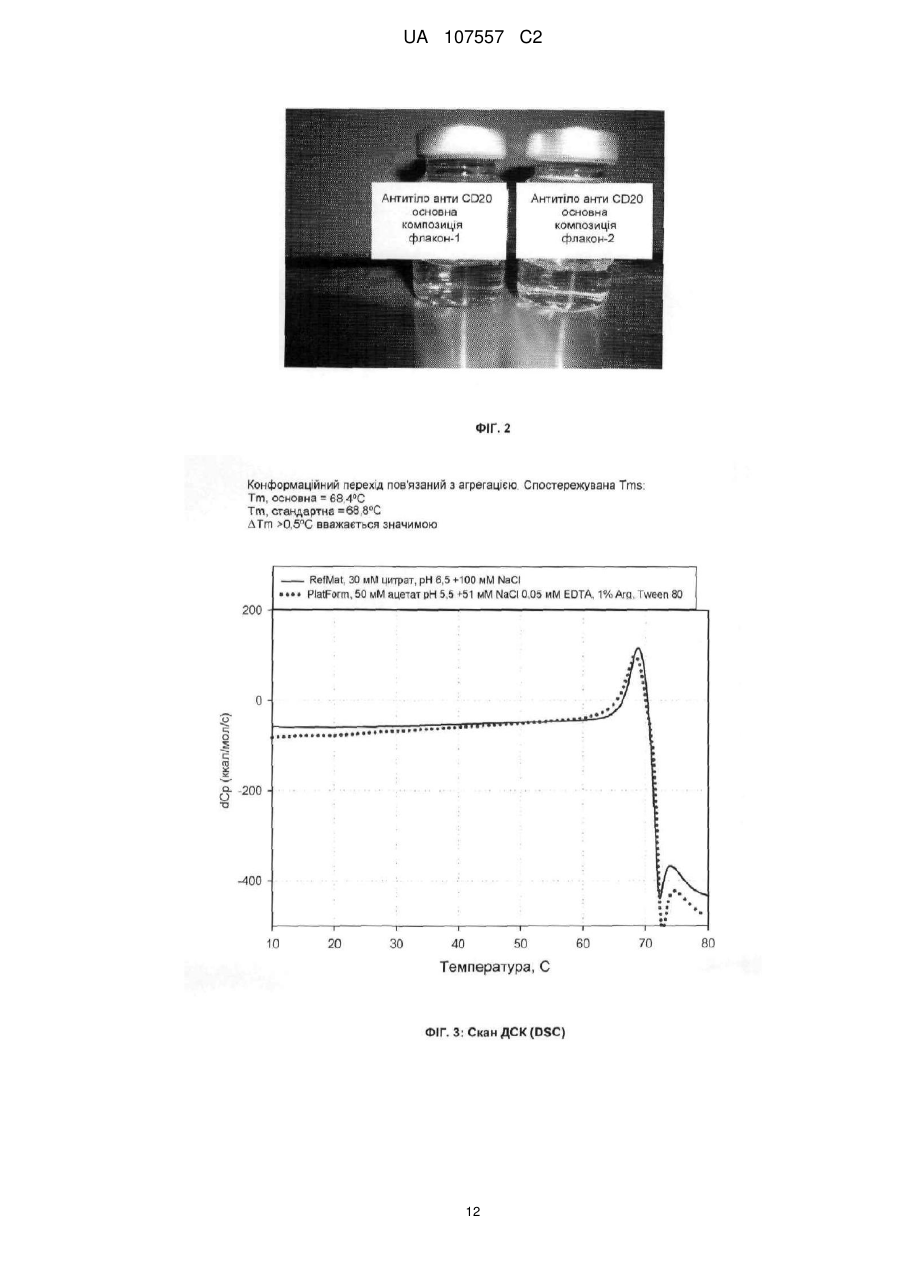
Реферат: Винахід належить до композиції антитіла офатумумабу, стійкої до механічної і температурної дії. Композиція антитіла офатумумабу містить офатумумаб у концентрації 20 - 300 мг/мл, 50 мМ ацетату натрію, 51 мМ хлориду натрію, 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН якої скоректований до 5,5. UA 107557 C2 (12) UA 107557 C2 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 60 ОПИС Галузь техніки Даний винахід стосується композицій антитіл, стійких до механічної і температурної дії. Рівень техніки Білки є більшими й складнішими, ніж традиційні органічні й неорганічні лікарські засоби (тобто мають багаточисельні функціональні групи на додаток до складних тривимірних структур), і отримання вказаних білків пов'язане з певними проблемами. Для того щоб білок зберіг біологічну активність, композиція має зберігати незмінною конформаційну цілісність щонайменше кодової послідовності амінокислот білка, в той же час захищаючи множинні функціональні групи від руйнування. Шляхи деградації білків можуть включати хімічну нестабільність (тобто який-небудь процес, який включає модифікацію білка, розривом зв'язку, що призводить до утворення нової хімічної молекули) або фізичну нестабільність (тобто змінами структури білка вищого порядку). Хімічна нестабільність може бути результатом дезамінування, рацемізації, гідролізу, окислення, бета-елімінування або дисульфідного обміну. Фізична нестабільність може бути викликана, наприклад, денатурацією, агрегацією, осадженням або адсорбцією. Три основні шляхи руйнування білка є агрегацією, дезамінуванням і окисленням білка. Cleland et al. Critical reviews in Therapeutic Drug Carrier systems 10(4):307-377 (1993). Молекула СD20 (так званий антиген, що обмежує диференціювання людських В-лімфоцитів або Вр35) є гідрофобним трансмембранним білком з молекулярною масою приблизно 35 кD, розташованим на пре-В і зрілих В-лімфоцитах (Valentine et al.(1989) J. Biol.Chem. 264(19):1128211287; і Einfield et al. (1988)ЕМВО J. 7(3):711-717). СD20 виявлені на поверхні більше ніж 90 % В-клітин з периферичної крові або лімфоїдних органів, і експресовані протягом раннього розвитку пре-В клітин і зберігаються до клітинного диференціювання плазмоцитів. CD20 представлені й на нормальних В-клітинах, і на злоякісних В-клітинах. Зокрема, CD20 експресовані на більше ніж 90 % В-клітин неходжкінської лімфоми (NHL) (Anderson et al. (1984) Blood 63(6):1424-1433), але не виявлені на гемопоетичних стволових клітинах, про-В клітинах, нормальних плазматичних клітинах або інших нормальних тканинах (Tedder et al. (1985) J. Immunol. 135(2):973-979). 85 амінокислотних карбоксикінцевих ділянок CD20 білка розташовані в цитоплазмі. Довжина вказаної ділянки відрізняється від довжини інших специфічних для В-клітин поверхневих структур, таких як важкі ланцюжки IgM, IgD і IgG-ланцюжки антигенів гістосумісності класу II альфа або бета, які мають відносно короткі інтрацитоплазматичні ділянки 3,3, 28, 15 і 16 амінокислот, відповідно (Komaromy et al. (1983) NAR 11:6775-6785). З 61 карбоксикінцевих амінокислот, 21 є кислими залишками, тоді як лише 2 є основними, виявляючи, що вказана ділянка має сильний негативний заряд. Nо. реєстрації GenBank NP. Sub.-690605. Вважається, що СD20 можуть брати участь у регуляції раннього етапу (етапів) у процесах активації й диференціювання В-клітин (Tedder et al. (1986) Eur. J. Immunol.16:881-887) і можуть діяти як кальцієвий іонний канал (Tedder et al. (1990)J. Cell. Biochem. 14D:195). Попри неясність відносно реальної функції СD20 у посиленні проліферації та/або диференціювання В-клітин, вони є важливою метою для терапії, опосередкованої антитілами, для контролю або знищення В-клітин, що беруть участь у механізмі ракових захворювань і аутоіммунних порушень. Зокрема, експресія СD20 на пухлинних клітинах, наприклад NHL, робить їх важливою мішенню для терапії, опосередкованої антитілами, для специфічних цільових лікарських засобів проти CD20-позитивних неопластичних клітин. HuMax-CD20ТМ (офатумумаб), описаний як 2F2 антитіло у Міжнародному Патенті 2004/035607, є повним людським IgG1, високоафінне антитіло, що направлене на молекулу СD20 у клітинній мембрані В-клітин. HuMax-CD20ТМ є клінічною розробкою для лікування неходжкінської лімфоми (NHL), хронічного лімфоцитарного лейкозу (CLL) і ревматоїдного артриту (RA). Див. також Teeling et al., Blood, 104, стор. 1793 (2004); і Teeling et al.,J.Immunology, 177, стор. 362-371(2007). Існує необхідність для отримання стійкої до механічної й температурної дії фармацевтичної композиції, що містить антитіло, яка є прийнятною для терапевтичного застосування. В одному варіанті здійснення антитіло може бути моноклональним антитілом. У іншому варіанті здійснення антитіло може бути анти-CD20 антитілом, включаючи, але не обмежуючись перерахованим, офатумумаб, ритуксимаб, тозитумомаб, окрелізумаб (2Н7.v16), 11В8 або 7D8 (розкриті в Міжнародному Патенті 2004/035607), анти-CD20 антитілом, розкритим у WO2005/103081, таким як С6, анти-СD антитілом, розкритим у WO 2003/68821, таким як IMMU106 (з Immunomedics), анти-СD20 антитілом, розкритим у WO 2004/103404, таким як АМЕ-133 (з Applied Molecular Evolution/Lilly), і анти-СD20 антитілом, розкритим у Патенті США 2003/0118592, 1 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 60 таким як TRU-015 (з Trubion Pharmaceuticals Inc). Суть винаходу Даний винахід відноситься до водної композиції антитіл, стійкої до механічної й температурної дії. Рамки даного винаходу не обмежені окремими варіантами здійснення, описаними в даному документі. Більше того, різні модифікації даного винаходу, на додаток до описаних у даному документі, стануть зрозумілі фахівцеві в галузі техніки з опису, наведеного далі. Вказані модифікації повністю знаходяться в рамках формули винаходу. Хоча один варіант здійснення адаптований до композиції повнорозмірного анти-СD20 антитіла, воно може бути також використане для композиції антитіл інших класів, наприклад, поліклональних антитіл, або фрагментів моноклональних або поліклональних антитіл. У одному варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, що містить терапевтично ефективну кількість анти-СD20 антитіл, у якій композиція додатково містить від 10 до 100 мМ ацетату натрію, від 25 до 100 мМ хлориду натрію, від 0,5 до 5 % вільної основи аргініну, від 0,02 до 0,2 мМ EDTA, від 0,01 до 0,2 % полісорбату 80 і рН якої скоректований до значення від 5,0 до 7,0. В іншому варіанті здійснення винахід стосується композиції анти-СD20 антитіл, що містить анти-СD20 антитіла в концентрації 20-300 мг/мл, де композиція додатково містить 50 мМ ацетату натрію, 51 мМ хлориду натрію, 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН якої скоректований до 5,5. У ще одному варіанті здійснення, антитілом є фрагментом анти-СD20 антитіла, такого як фрагмент моноклонального антитіла. Бажаним антитілом анти-СD20 є офатумумаб. В одному варіанті здійснення винахід відноситься до композиції офатумумабу, що містить терапевтично ефективну кількість офатумумабу, де композиція додатково містить від 10 до 100 мМ ацетату натрію, від 25 до 100 мМ хлориду натрію, від 0,5 до 5 % вільної основи аргініну, від 0,02 до 0,2 мМ EDTA, від 0,01 до 0,2 % полісорбату 80 і рН якої скоректований до значення від 5,0 до 7,0. У ще одному варіанті здійснення винахід відноситься до композиції офатумумабу, що містить офатумумаб, у концентрації 20-300 мг/мл, де композиція додатково містить 50 мМ ацетату натрію, 51 мМ хлориду натрію, 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН якої скоректований до 5,5. У ще одному варіанті здійснення, винахід відноситься до композиції анти-СD20 антитіл, де композиція стабільна протягом щонайменше 2 років. В іншому варіанті здійснення, винахід стосується композиції анти-СD20 антитіл, де композиція стабільна при температурах до щонайменше 55 °C. У ще одному варіанті здійснення, винахід відноситься до композиції антиСD20 антитіл, де композиція стабільна при температурі приблизно 5 °C протягом щонайменше 2 років. У іншому варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, у якому композиція стабільна при температурі приблизно 25 °C протягом щонайменше 3 місяців. В іншому варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, де композиція стабільна при температурі приблизно 40 °C протягом щонайменше 1 місяця. В іншому варіанті здійснення, винахід відноситься до композиції анти-СD20 антитіл, де композиція стабільна при температурі приблизно 55 °C протягом щонайменше 1 дня. В іншому варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, де композиція стабільна при температурі приблизно від 5 до 25 °C, від 5 до 35 °C, від 5 до 45 °C, від 10 до 25 °C, від 10 до 35 °C, від 10 до 45 °C, від 10 до 55 °C, від 20 до 35 °C, від 20 до 45 °C, від 20 до 55 °C протягом щонайменше 1 дня при струшуванні. В іншому варіанті здійснення винахід відноситься до композиції анти-CD20 антитіл, в якій ацетат натрію представлений у кількості приблизно 50 мМ, 40 мМ, 45мМ, 55 мМ, або 60 мМ. В інших варіантах здійснення ацетат натрію може бути представлений у кількості від 10 до 100 мМ, від 20 до 100 мМ, від 30 до 100 мМ, від 40 до 100 мМ, від 50 до 100 мМ, від 60 до 100 мМ, від 70 до 100 мМ, від 25 до 80 мМ або від 30 до 70 мМ. У ще одному варіанті здійснення рН може бути скоректований до рН 5,0, 6,0, 6,5 або 7,0. В інших варіантах здійснення винаходу NаOH або HCl використовують для корекції рН до 5,0, 6,0, 6,5 або 7,0. У ще одному варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, у якій хлорид натрію представлений у кількості приблизно 51 мМ, 45 мМ, 46мМ, 47 мМ, 48 мМ, 49 мМ, 50 мМ, 52 мМ, 53 мМ, 54 мМ, 55 мМ. В інших варіантах здійснення хлорид натрію може бути представлений у кількості від 25 до 100 мМ, від 35 до 90 мМ, від 45 до 80 мМ, від 25 до 70 мМ, або від 45 до 70 мМ. В іншому варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, у якій 2 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 60 вільна основа аргініну представлена в кількості приблизно 1 %, 0,7 %, 1,3 % або 2,0 %. В інших варіантах винаходу вільна основа аргініну може бути представлена від 0,5 до 5,0 %, від 0,5 до 2,0 %, від 0,5 до 2,5 %, від 0,5 до 3,0 %, від 0,5 до 3,5 %, від 0,5 до 4,0 %, або від 0,5 до 4,5 %. В іншому варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, у якій EDTA представлений у кількості приблизно 0,05 мМ, 0,03 мМ, 0,04 мМ або 0,06 мМ. В інших варіантах здійснення EDTA може бути представлений у кількості 0,02 мМ - 0,2 мМ, 0,02 мМ - 0,1 мМ, 0,02 мМ - 0,15 мМ, 0,04 мМ - 0,1 мМ, 0,03 мМ - 0,15 мМ або 0,03 мМ - 0,2 мМ. В іншому варіанті здійснення винахід відноситься до композиції анти-СD20 антитіл, у якій полісорбат 80 представлений у кількості, приблизно 0,02 %, 0,015 % або 0,025 %. В інших варіантах здійснення полісорбат 80 може бути представлений у кількості 0,01-0,2 %, 0,010,15 %, 0,02-0,2 %, 0,02-0,15 %, 0,01-0,25 % або 0,01-0,05 %. В іншому варіанті здійснення винахід відноситься до способу лікування захворювання, в якому задіяні клітини, що експресують СD20, шляхом введення ссавцеві композиції анти-СD20 антитіл згідно з даним винаходом, що містить терапевтично ефективну кількість антитіл антиCD20, в якій композиція додатково містить від 10 до 100 мМ ацетату натрію, від 25 до 100 мМ хлориду натрію, від 0,5 до 5 % вільної основи аргініну, від 0,02 до 0,2 мМ EDTA, від 0,01 до 0,2 % полісорбату 80 і з рН, скоректованим до значень від 5,0 до 7,0. Типові "захворювання, в яких задіяні клітини, що експресують СD20", які можуть бути піддані лікуванню (наприклад, пом'якшені) або профілактиці, включають, але не обмежуються перерахованим, пухлинні захворювання та імунні захворювання, наприклад, аутоімунні захворювання. Приклади пухлинних захворювань, які можуть бути піддані лікуванню та/або профілактиці, включають Вклітинну лімфому, наприклад, NHL, хронічний лімфобластний лейкоз/лімфому з попередників Вклітин і пухлини зі зрілих В-клітин, такі як В-клітинний хронічний лімфоцитарний лейкоз (CLL)/ дрібноклітинна лімфоцитарна лімфома (SLL), В-клітинний пролімфоцитарний лейкоз, лімфоплазматична лімфома, лімфома з клітин мантійной зони (MCL), фолікулярна лімфома (FL), включаючи низькодиференційовану, средньодиференційовану і високодиференційовану FL, шкірну лімфому з клітин фолікулярного центру, В-клітинну лімфому з клітин маргінальної зони (MALT тип, вузловий або селезінковий тип), волосатоклітинний лейкоз, дифузна Вкрупноклітинна лімфома, лімфома Беркітта, плазмоцитома, мієломна хвороба, посттрансплантаційний лімфопроліферативний синдром, макроглобулінемію Валденстрема, анапластичну крупноклітинну лімфому (ALCL). Приклади імунних порушень, у яких задіяні Вклітини, що експресують CD20, які можуть бути піддані лікуванню та/або профілактиці, включають псоріаз, псоріатичний артрит, дерматит, системну склеродермію й склероз, запальні захворювання кишечнику (IBD), хвороба Крона, виразковий коліт, респіраторний дистрессиндром, менінгіт, енцефаліт, увеїт, гломерулонефрит, екзему, астму, атеросклероз, порушення адгезії лейкоцитів, розсіяний склероз, синдром Рейно, синдром Шегрена, ювенільний діабет, синдром Рейтера, синдром Бехчета, імунокомплексний нефрит, IgA нефропатія, IgM полінейропатія, імуно-опосередкована тромбоцитопенія, така як гостра ідіопатична тромбоцитопенічна пурпура й хронічна ідіопатична тромбоцитопенічна пурпура, гемолітична анемія, міастенія гравіс, вовчаковий нефрит, системний червоний вовчак, ревматоїдний артрит (РА), атопічний дерматит, пухирчатка, хвороба Грейвса, тиріоїдит Хашімото, грануломатоз Вегенера, синдром Оменна, хронічну ниркову недостатність, гострий інфекційний мононуклеоз, ВІЛ, і захворювання, пов'язані з вірусом герпесу. Додатковими прикладами є важкий респіраторний дистрес-синдром і хореоретиніт. Іншими додатковими прикладами є захворювання й розлади, викликані інфікуванням В-клітин вірусом, таким як вірусом ЕпштейнБарра (ЕБВ). Також додатковим прикладом є ХОБЛ. У ще одному варіанті здійснення винахід відноситься до способу лікування захворювання, в якому задіяні клітини, що експресують СD20, шляхом введення ссавцеві композиції анти-СD20 антитіл згідно з даним винаходом, що містить терапевтично ефективну кількість антитіл антиCD20, в якій композиція додатково містить від 10 до 100 мМ ацетату натрію, від 25 до 100 мМ хлориду натрію, від 0,5 до 5 % вільної основи аргініну, від 0,02 до 0,2 мМ EDTA, від 0,01 до 0,2 % полісорбату 80 і з рН, скоректованим до значень від 5,0 до 7,0 і в якому стійку композицію антитіл уводять ссавцеві перорально, парентерально, інтраназально, вагінально, ректально, лінгвально, сублінгвально, букально, трансшкірно, внутрішньовенно або підшкірно. У ще одному варіанті здійснення винахід відноситься до способу лікування захворювання, в якому задіяні клітини, що експресують СD20, шляхом введення ссавцеві композиції анти-СD20 антитіл згідно з даним винаходом, що містить анти-СD20 антитіла в концентрації 20-300 мг/мл, в якому композиція додатково містить 50мМ ацетату натрію, 51 мМ хлориду натрію, 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН якою скоректовано до 5,5. Бажаним анти-СD20 антитіло є офатумумаб. 3 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 60 Зрозуміло, що й описана раніше суть винаходу, й наведений далі детальний опис є зразковими і пояснюючими, й призначені додатково пояснювати заявлений винахід. Супровідні креслення надані для додаткового розуміння винаходу і є частиною даного опису, ілюструють деякі варіанти здійснення й спільно з описом служать для пояснення принципів винаходу. Короткий опис креслень Фіг. 1 ілюструє стандартну композицію (RefMat) анти-СD20 антитіла 20 мг/мл (30 мМ цитрат, 100 мМ NaCl, рН 6,5) у двох примірниках. Фіг. 2 ілюструє один варіант здійснення композиції анти-CD20 антитіл за винаходом (PlatForm) 20 мг/мл (50 мМ ацетату натрію, хлориду натрію (51 мМ), 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН скоректованим до 5,5 HCl) у двох примірниках. Фіг. 3 графічно ілюструє порівняння стійкості анти-СD20 антитіла до температури в композиції за винаходом (PlatForm) і стандартних буферів композиції (PlatForm) DSC. Термодинамічно, дві композиції схожі, як видно з їхніх DSC профілів, оскільки зміни у видимій Tm менше, ніж 0,5 °C між композиціями. Детальний опис винаходу Один варіант здійснення даного винаходу стосується композицій антитіл, стійких до механічної й температурної дії. В іншому варіанті здійснення винахід забезпечує неочікувану стійкість, що проявляється композицією за одночасних стресових умов підвищеної температури й струшування при 55 °C. Додатковий варіант винаходу є стабільнішою композицією в порівнянні зі стандартною композицією (такою як 30 мМ цитрату, 100 мМ NaCl, рН 6,5). Композиція згідно з даним винаходом демонструвала зменшене осадження (залишалася прозорою) при дії стресових умов, а стандартна композиція була агрегованою. Цей результат був непередбачуваний, оскільки термодинамічно дві композиції є схожими, як видно з профілів ДСК (диференціальної скануючої калориметрії). В описі даного винаходу деякі терміни використані згідно з наведеним нижче визначенням. Термін "білкова композиція" або "композиція антитіл" означає композиції, які представлені в такій формі, яка дозволяє ефективність біологічної дії активних інгредієнтів, і які не містять додаткових компонентів, токсичних для пацієнтів, яким уводять композицію. "Фармацевтично прийнятними" допоміжними речовинами (носіями, добавками) є ті допоміжні речовини, які можуть бути введені ссавцеві для надання ефективної дози активного інгредієнта, що використовується. Наприклад, концентрація допоміжної речовини також важлива для можливості застосовувати композицію як ін'єкцію. "Стабільна" композиція є композицією, в якій білок переважно зберігає свою фізичну та/або хімічну стабільність та/або біологічну активність при зберіганні. Різні методики аналізу для вимірювання стабільності білків доступні в галузі техніки і розглянуті в Peptide and Protein Drug Delivery, 247-301, Vincent lee Ed., Marcel Dekker, Inc., Нью-Йорк, N.Y., Pubs (1991) and Jones, A.Adv. Drug Delivery Rev.10:29-90 (1993), наприклад. Стабільність може бути оцінена при певній температурі протягом певного періоду часу. Бажано, композиція стабільна при температурі довкілля або при 40 °C протягом щонайменше 1 місяця та/або стабільна при 2-8 °C протягом щонайменше від 1 до 2 років. Більше того, бажано, щоб композиція була стабільна при заморожуванні (наприклад, до -70 °C) і відтаванні продукту. Білок "зберігає свою фізичну стабільність" у біофармацевтичній композиції, якщо він демонструє незначні або відсутність змін в агрегації, осадженні й денатурації, що реєструється візуальним спостереженням кольору та/або прозорості, або вимірюють розсіюванням УФ випромінювання (оцінюють видимі агрегати) або ексклюзійною хроматографією (SEC). SEC оцінює розчинні агрегати, які необов'язково є попередниками видимих агрегатів. Білок "зберігає свою хімічну стабільність" у біофармацевтичній композиції, якщо хімічна стабільність при даному часі така, що білок зберігає свою біологічну активність відповідно до визначення, наведеного далі. Види, що хімічно деградували, можуть бути біологічно активними й хімічно нестабільними. Хімічна стабільність може бути досліджена визначенням і кількісним підрахунком хімічно пошкоджених форм білка. Хімічне пошкодження може включати зміну розміру (наприклад, кліпінг), яка може бути оцінена використовуючи SEC, SDS-PAGE та/або часоплинну мас-спектрометрію з лазерною іонізацією й десорбцією з рідкої матриці (MALDI/TOF MS), наприклад. Інші типи хімічного пошкодження включають зміну заряду (наприклад, що з'являється в результаті дезамінування), яка може бути оцінена іонообмінною хроматографією, наприклад. Антитіло "зберігає свою біологічну активність" у фармацевтичній композиції, якщо зміна в біологічній активності антитіла за певний час у межах 10 % (в межах погрішності вимірювання) 4 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 60 біологічної активності, що проявляється, фармацевтичною композицією при отриманні, що визначають у дослідженні зв'язування антигена, наприклад. Інші дослідження "біологічної активності" для антитіл представлені в даному документі далі. Термін "ізотонічний" означає, що композиція має по суті такий самий осмотичний тиск, як і людська кров. В одному варіанті здійснення винаходу ізотонічні композиції за винаходом у загальному випадку мають осмотичний тиск від 250 до 350мосм. В інших варіантах здійснення ізотонічні композиції за винаходом мають осмотичний тиск від приблизно 350 до 450 мосм. У ще одному варіанті здійснення осмотичний тиск складає більше 450 мосм. Ізотонічність можна виміряти, наприклад, використовуючи парофазний або кріоскопічний тип осмометра. У рамках винаходу "буфер" стосується буферного розчину, який чинить опір зміні рН, дією компонентів зв'язаної кислоти-основи. В одному варіанті здійснення буфер згідно із даним винаходом має рН від приблизно 4,5 до приблизно 6,0; у іншому варіанті здійснення від приблизно 4,8 до приблизно 5,8; і в додатковому варіанті здійснення рН приблизно 5,5. Приклади буферів, які контролюватимуть рН у цьому інтервалі, включають ацетат (наприклад, ацетат натрію), сукцинат (такий як сукцинат натрію), глюконат, гістидин, цитрат та інші органічні кислі буфера. Якщо необхідна композиція, стійка до заморожування-розморожування, буфер бажано не є фосфатом. З погляду фармакології, в контексті даного винаходу "терапевтично ефективна кількість" антитіл означає кількість, ефективну в запобіганні або лікуванні розладу, для лікування якого антитіла ефективні. "Порушенням" є який-небудь стан, який успішно лікується антитілами. Вказане порушення включає хронічні й гострі порушення або захворювання, включаючи патологічні стани, які прихиляють ссавця до порушення, про яке йдеться. В бажаному варіанті здійснення "порушенням" є захворювання, в якому задіяні клітини, що експресують CD20. "Консервантом" є сполука, яка може бути включена в композицію для істотного зменшення дії бактерій, таким чином, сприяючи одержанню багатоцільової композиції, наприклад. Приклади можливих консервантів включають октадецилдиметилбензил хлорид амонію, гексаметоній хлорид, бензалконій хлорид (суміш алкілбензилдиметиламонію хлоридів, у яких алкільними групами є довголанцюжкові сполуки), і хлорид бензалконію. Інші типи консервантів включають ароматичні спирти, такі як феноловий, бутиловий і бензиловий спирт, алкілпарабени, такі як метил або пропілпарабен, катехол, резорцин, циклогексан, 3-пентан і мкрезол. Найбільш бажаний консервант згідно з даним винаходом є бензиловим спиртом. Термін "антитіло" використаний у широкому сенсі й охоплює моноклональні антитіла (включаючи повноланцюжкові антитіла), поліклональні антитіла, мультиспецифічні антитіла (наприклад, біспецифічні антитіла), й фрагменти антитіл такої довжини, до якої вони проявляють потрібну біологічну активність. "Фрагменти антитіла" включають частину повноланцюжкового антитіла, в загальному випадку антиген-зв'язуючу або її різні ділянки. Приклади фрагментів антитіл включають Fab, Fab", F(ab")2 і Fv фрагменти; діантитіла; лінійні антитіла; одноланцюжкові молекули антитіл; і мультиспецифічні антитіла, утворені з фрагментів антитіл. Термін "моноклональне антитіло" в рамках винаходу відноситься до антитіла, отриманого з популяції по суті моноклональних антитіл, тобто окремих антитіл, що містяться в популяції, які є однаковими, виключаючи можливі, природно виникаючі мутації, які можуть бути представлені у мінімальній кількості. Моноклональні антитіла високо специфічні, направлені на єдину ділянку антигену. Більше того, на відміну від загальноприйнятого (поліклонального) антитіла, композиції, які зазвичай включають різні антитіла, направлені на різні детермінанти (епітопи), кожне моноклональне антитіло направлене проти єдиної певної ділянки на антигені. Визначення "моноклональний" виявляє характерні особливості антитіла, те, що його отримують, переважно, з популяції моноклональних антитіл, і не має розумітися, як такий, що вимагає отримання якимнебудь окремим способом. Наприклад, моноклональні антитіла, що використовуються відповідно до даного винаходу, можуть бути отримані гібридомним способом, вперше описаним Kohler et al., Nature 256:495 (1975), або можуть бути отримані способами рекомбінантної ДНК (див. наприклад, Патент США Nо.4 816567). "Моноклональні антитіла" можуть бути також виділені з банку фагових антитіл, використовуючи методику, описану в Clackson et al., Nature 352^624-626 (1991) і Marks et al., J.Mol.Biol. 222:581-597(1991), наприклад. "Гуманізовані" форми антитіл, що не належать до людських (наприклад, мишачих), є химерними антитілами, які містять мінімальні послідовності, отримані з імуноглобуліну, що не відноситься до людського. В основному, гуманізовані антитіла є людськими імуноглобулінами (антитіло-реципієнт), в яких залишки з гіперваріабельної ділянки реципієнта замінені залишками з гіперваріабельної ділянки видів, що не належать до людей (антитіло-донор), таких як миші, щури, кролі або людиноподібні примати, що мають необхідну специфічність, афінітет і 5 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 60 функціональні можливості. В деяких прикладах, FR залишки людського імуноглобуліну заміщають відповідними залишками імуноглобуліну, видів, відмінних від людини. Крім того, гуманізовані антитіла можуть містити залишки, які не виявлені в реципієнтному антитілі або в донорському антитілі. Вказані модифікації отримані для додаткового точного представлення антитіла. В загальному випадку, в основному всі гуманізовані антитіла містять щонайменше одне і зазвичай два різних домени, в яких всі або більшість гіперваріабельних ділянок відповідають гіперваріабельним ділянкам імуноглобуліну, що не належить до людського, і всі або більшість FR ділянок є послідовностями імуноглобуліну людини. Гуманізоване антитіло необов'язково також містить щонайменше частину константної ділянки імуноглобуліну (Fc), зазвичай імуноглобуліну людини. Детальніше див. Jones et al. Nature 321:522-525 (1986); Riechmann et al., Nature 332:323-329 (1988); і Presta, Curr. Op. Struct. Biol. 2:593-596 (1992). "Одноланцюжковий Fv" або "sFv" фрагменти антитіл, що містять Vн і VL домени антитіла, в яких вказані домени є одним поліпептидним ланцюгом. У загальному випадку, Fv поліпептид додатково містить поліпептидний лінкер між Vн і VL доменами, які дають можливість SFv утворювати бажану структуру для зв'язування антигену. Відносно sFv див. Pluckthun in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds. Springer-Verlag, N.Y., стор. 269-315 (1994). Термін "діатіло" стосується невеликих фрагментів антитіл з двома антигенз'вязуючими центрами антитіла, які містять важкий ланцюг варіабельного домену (VH), сполучений з легким ланцюгом варіабельного домену (VL) в тому самому поліпептидному ланцюзі (VH і VL). Використовуючи лінкер, який дуже короткий для об'єднання двох доменів на тому самому ланцюзі, домени вимушені об'єднуватись з комплементарним доменом іншого ланцюга й створювати два антигенз'вязуючі центри антитіла. Діатіла детальніше описані, наприклад, у ЕP 404097; WO 93/11161; і Holinger et al., Proc. Natl. Acad. Sci. США 90:6444-6448 (1993). Вираз "лінійне антитіло", що використовується впродовж всієї заявки, стосується антитіл, описаних у Zapata et al., Protein Eng. 8(10):1057-1062 (1995). Коротко, вказані антитіла містять пару об'єднаних Fd сегментів (VH-CH-VH1-CH1), які утворюють пару антигенз'вязуючих центрів антитіла. Лінійні антитіла можуть бути біспецифічними і моноспецифічними. Отримане антитіло бажано переважно не містить домішок і бажано по суті є моноклональним (тобто вільним від забруднення білками і т. д.). Антитіло "що переважно не містить домішок" означає композицію, що містить щонайменше приблизно 90 % мас. антитіл, виходячи із загальної маси композиції, бажано щонайменше приблизно 95 % мас. "По суті моноклональні" антитіла означають композицію, що містить щонайменше приблизно 99 % мас. антитіл, виходячи із загальної маси композиції. "Лікування" стосується терапевтичної дії й профілактичних або застережливих заходів. Ті, які потребують лікування, включають і тих пацієнтів, які вже мають порушення, і тих, в яких порушенню запобігають. "Ссавець" з метою лікування відноситься до якої-небудь тварини, що належить до класу ссавців, включаючи, але не обмежуючись перерахованим, людей, домашніх і господарських тварин, і тварин зоопарків, спортивних і кімнатних тварин, таких як собаки, коні, кішки й корови. "Стресова умова" стосується довкілля, яке хімічно або фізично несприятливе для білка й може створювати неприйнятну стабільність білка (наприклад, теплова, механічна, хімічна дія). Гель-хроматографія є способом хроматографії, в якому частки розділяють виходячи з їх розміру або гідродинамічного об'єму. Динамічним розсіянням світла є спосіб, який вимірює тимчасову залежність розсіювання світла білком. Зазвичай, указану часову залежність піддають обробці для отримання гідродинамічного радіусу молекули. "DSC" відноситься до різних скануючих калориметрів: DSC параметри зйомки: можуть бути, але не обмежуються перерахованим, 1 мг/мл білка, сканування від 5 до 80 °C з швидкістю сканування 70 °C на годину і 15 хвилин попереднього очікування. Сканування буфер-буфер може бути зняте першим і вирахувано з даних, не підданих обробці. Дані можуть бути скоректовані для буфера й нормалізовані для концентрації білка при побудові графіка. Агрегацію можна попередити коректуванням лінії відліку. Наведені далі приклади додатково ілюструють даний винахід. Приклади не призначені обмежувати рамки даного винаходу й надані для додаткового пояснення винаходу. ПРИКЛАДИ Винахід додатково ілюструють наступними прикладами, які призначені для пояснення винаходу. Ці приклади не призначені обмежувати рамки даного винаходу. Модифікації та зміни даного винаходу можливі з погляду методик, описаних у даному документі й, отже, знаходяться 6 UA 107557 C2 5 10 15 20 25 30 35 40 в рамках даного винаходу. Приклади, наведені далі, виконують, використовуючи стандартні методики, і вказані стандартні методики добре відомі й звичайні для фахівця в галузі техніки, виключаючи ті, які описані детально. Приклад 1.1: Отримання основного буфера композиції В одному варіанті здійснення винаходу, отримують 4 літри ацетатного буфера. У вказаному варіанті здійснення, кінцевий буфер містить 50 мМ ацетату натрію, 0,05мМ EDTA, 51 мМ NaCl, 0,1 % аргініну, 0,02 % полісорбату 80, рН5,5. Буфер отримують розчиненням триводного ацетату натрію, динатрію едетату (EDTA), полісорбату 80 і вільної основи L-аргініну в 3,5 л деіонізованої води. Коли рН скоректували до 5,5, використовуючи 3Н HCl, об'єм доводять до 4,0 л і буфер фільтрують, використовуючи 0,45 μм фільтрувальний елемент. Потім буфер можна зберігати при 2-8С до використання. «%» композиції, описаний у даній заявці, відноситься до «% об'єм". Приклад 2.1: Отримання офатумумабу в основному буфері композиції В одному варіанті здійснення винаходу, офатумумаб діафільтрують в основну композицію (50 мМ ацетату натрію, 0,05 мМ EDTA, 51 мМ NaCl, 0,02 % полісорбату 80 і 0,1 % аргініну(вільна основа)) концентрують до стабільності. Офатумумаб діафільтрують в основну композицію, використовуючи лабораторну систему фільтрації в поперечному потоці з трьома мембранами. Після діафільтрації в основний буфер, офатумумаб концентрують до максимальної концентрації 179мг/мл. Весь процес займає три робочих дні до завершення, й вихід продукту складає 96,1 %. Деяку частину розведення основним буфером композиції так, щоб концентрація приблизно склала 20-179 мг/мл, можна досліджувати. Приклад 3:1: Отримання офатумумабу в стандартній і основній композиції для безпосереднього порівняння зовнішнього вигляду (ЗВ) Антитіло анти-CD20 (офатумумаб) отримують у стандартній і основній (один варіант здійснення даного винаходу) композиції в концентрації 20 мг/мл для безпосереднього порівняння зовнішнього вигляду впродовж 12 тижнів і для випробувань струшуванням. Антитіло анти-CD20 у стандартній і основній композиції фільтрують, використовуючи низькобілковий зв'язуючий мембранний фільтр 0,2 μм. Після фільтрації кожну композицію розливають по 3 мл в 5 сс флакони, закривають пробкою й закупорюють у стерильних умовах під очищаючою витяжною шафою. Флакони струшують при 325 об/хв при температурі 55С. Під час струшування з нагріванням, спостерігають за зовнішнім виглядом, як описано в прикладі 3.2, періодично через 42-годинні проміжки часу. Фіг.1 і 2 демонструють стандартну і основну композиції, відповідно, після 18,5 годин струшування з нагріванням. Результати вивчення струшування виявляють, що стандартна композиція з часом утворює частки при струшуванні при температурі 55С швидше, ніж основна композиція. Приклад 3.2: GA(зовнішній вигляд ЗВ), 18,5 годин випробування струшуванням - Зовнішній вигляд офатумумабу 20 і 100 мг/мл Зовнішній вигляд (GA, ЗВ) зразків анти-СD20, що піддалися випробуванню струшуванням, представлений у таблиці, наведеній далі. Оцінку GA (ЗВ) виконують, використовуючи загальний спосіб, який може бути використаний для розчину антитіл IgG, який описує колір, прозорість і видимі частки речовини. Момент часу струшування Зовнішній вигляд Початково Стандартна Прозора, безбарвна, представлені 1-2 частки Основна Прозора, безбарвна, часток не містить 18,5 години Стандартна Прозора, безбарвна, представлено декілька крупних часток Основна Прозора, безбарвна, часток не містить 9-42 години Стандартна Каламутна, безбарвна, представлено декілька крупних часток Основна Злегка каламутна, безбарвна, часток не містить 7 UA 107557 C2 5 10 15 Приклад 4: Визначити температурну стійкість розчину офатумумабу в стандартному й основному буфері диференціальною скануючою калориметрією (ДСК) Для правильного здійснення дослідження ДСК, сканують один буфер і буфери з білком. Білок у стандартній і основній композиції розводять до 1 мг/мл, як представлено в Прикладі 4.1. Дані отримують з показників DSC для скану при 5-80С, швидкості сканування 70С на годину з 15 хвилинним калібруванням перед кожним сканом. Об'єм клітин зразка ДСК (DSC) ~0,5 мл. Після того, як отримали скани буфера й білка, скани буфера віднімають із скана білка. Концентрацію білка в зразках отримують для внесення поправки на концентрацію в кожному скані (див. приклад 4.2). Значення для Тun, °C, початку розгортання, Тm, °C, температуру денатурації (при максимумі транзиції) і Т1/2, °C, ширина піку на напіввисоті (відображає зміни в третинній структурі і кооперативність транзиції) отримують для офатумумабу для кожної композиції (див. приклад 4.3). Дійсні скани DSC можна побачити на Фіг.3. Виходячи з результатів DSC, офатумумаб або в стандартній композиції, або в основній композиції мають схожі профілі ДСК і отже, імовірно мають схожу температурну стійкість. Приклад 4.1: Отримання зразка для біофізичних характеристик дослідження рН офатумумабу: 1.РОЗВЕДЕННЯ Початкова концентрація мг/мл Буфер pH Розведення до 1 мл/мл для ВСК мл зразка 17 6,5 Стандартна композиція 30 мМ цитрату, 100 мМ NaCl 5,5 Основна композиція 50 мМ ацетату, 51 мМ NaCl, 0,05 мМ EDTA, 1 % арг., 0,02 % Tween 80 мл буфера 0,1 1,6 20 0,075 1,43 20 Приклад 4.2:А280 ВИМІРювання Виміряна конц. розведення Початкова концентрація 0,5 мг/мл мг/мл мг/мл мМ* Буфер pH 6,5 Стандартна композиція 30 мМ цитрату, 100 мМ NaCl 5,5 Основна композиція 50 мМ ацетату, 51 мМ NaCl, 0,05 мМ EDTA, 1 % арг., 0,02 % Tween 80 17 0,517 0,00345 20 0,444 0,00296 *використання для нормалізації ДСК сканів Отримують один зразок, ємність з відповідним буфером, зчитують 3 рази. Використовують 1 см кювету. Поглинання субстрату А320 після ділення на коефіцієнт поглинання (1.49). Приклад 4.3: Результати ДСК 25 8 UA 107557 C2 Зразок Стандартна композиція Основна композиція T C pH Буфер 6,5 30 мМ цитрату, 100 мМ NaCl 5,5 50 мМ ацетату, 51 мМ NaCl, 0,05 мМ EDTA, 1 % арг., 0,02 % Tween 80 T C T1/2 C 62 68,8 2,9* 60 68,4 3,2* Зауваження Схоже із стандартною композицією *Значення Т1/2 визначають вручну. Екзотермічний унесок з агрегатів спотворює вихідну лінію, отже, вказані значення можуть бути штучно занижені. 5 10 15 20 25 30 35 40 45 У конкретних варіантах здійснення, композиція анти-СD20 антитіл даного винаходу може бути використана для лікування пацієнта з онкогенними порушеннями, наприклад, порушенням, що характеризується наявністю пухлинних клітин, що експресують СD20, включаючи, наприклад, В-клітинну лімфому, наприклад, NHL. Приклади онкогенних захворювань, які можуть бути піддані лікуванню та/або попередженню, включають В-клітинну лімфому, наприклад, NHL, хронічний лімфобластний лейкоз/лімфому з попередників В-клітин і пухлини із зрілих В-клітин, такі як В-клітинний хронічний лімфоцитарний лейкоз (CLL)/дрібноклітинна лімфоцитарна лімфома (SLL), В-клітинний пролімфоцитарний лейкоз, лімфоплазматична лімфома, лімфома з клітин мантійной зони (MCL), фолікулярна лімфома (FL), включаючи низькодиференційовану, средньодиференційовану й високодиференційовану FL, шкірну лімфому з клітин фолікулярного центру, В-клітинну лімфому з клітин маргінальної зони (MALT тип, вузловий або селезінковий тип), волосатоклітинний лейкоз, дифузна В-крупноклітинна лімфома, лімфома Беркітта, плазмоцитома, мієломна хвороба, посттранплантаційний лімфопроліферативний синдром, макроглобулінемія Валденстрема, анапластична крупноклітинна лімфома (ALCL). Додатковими прикладами В-клітинної неходжкінської лімфоми є лімфоматоїдний грануломатоз, первинна ексудативна лімфома, внутрішньосудинна В-крупноклітинна лімфома, медіастинальна В-крупноклітинна лімфома, хвороби важких ланцюгів (включаючи гамма, мю і альфа-хвороби), лімфоми, викликані терапією імунодепресантами, такі як лімфома, викликана циклоспорином і метотрексатом. У додатковому варіанті здійснення, композиція анти-СD20 антитіл даного винаходу може бути використана для терапії лімфоми Ходжкіна. Приклади імунних порушень (захворювань), при яких клітини експресують СD20, які можуть бути піддані лікуванню та/або попереджені композицією анти-СD20 антитіл даного винаходу, включають аутоіммунні захворювання, такі як псоріаз, псоріатичний артрит, дерматит, системну склеродермію й склероз, запальні захворювання кишечнику (IBD), хворобу Крону, виразковий коліт, респіраторний дистрес-синдром, менінгіт, енцефаліт, увеїт, гломерулонефрит, екзему, астму, атеросклероз, порушення адгезії лейкоцитів, розсіяний склероз, синдром Рейно, синдром Шегрена, ювенільний діабет, синдром Рейтера, синдром Бехчета, імунокомплексний нефрит, IgA нефропатія, IgM полінейропатія, імуно-опосередкована тромбоцитопенія, така як гостра ідіопатична тромбоцитопенічна пурпура і хронічна ідіопатична тромбоцитопенічна пурпура, гемолітична анемія, міастенія гравіс, вовчаковий нефрит, системний червоний вовчак, ревматоїдний артрит (РА), атопічний дерматит, пухирчатка, хвороба Грейвса, тиріоїдит Хашімото, грануломатоз Вегенера, синдром Оменна, хронічна ниркова недостатність, гострий інфекційний мононуклеоз, ВІЛ, і захворювання, пов'язане з вірусом герпесу. Додатковими прикладами є важкий респіраторний дистрес-синдром і хореоретиніт. Іншими додатковими прикладами є захворювання й розлади, викликані інфікуванням В-клітин вірусом, таким як вірусом Епштейн-Барра (EBV). Додаткові приклади запальних, імунних та/або аутоіммунних порушень, у яких на перший план виходять аутоантитіла та/або зайва В-лімфоцитарна активність і які можуть бути піддані лікуванню та/або попереджені композицією анти-СD20 антитіл даного винаходу, включають наступне: васкуліти та інші судинні порушення, такі як мікроскопічний поліангіїт, синдром ЧерджаШтрауса, та інші АНСА-асоційовані васкуліти, вузликовий поліартеріїт, есенціальний кріоглобулінемічний васкуліт, шкірний лейкоцитокластичний ангіїт, хворобу Кавасакі, артеріїт Такаясу, гігантоклітинний артрит, хворобу Шенлейн-Геноха, первинний і ізольований церебральний ангіїт, вузлову еритему, облітеруючий тромбангіїт, тромботичну 9 UA 107557 C2 5 10 15 20 25 30 35 40 45 50 55 тромбоцитопенічну пурпуру (включаючи гемолітичний уремічний синдром) і вторинні васкуліти, включаючи шкірний лейкоцитокластичний ангіїт (наприклад, вторинний гепатиту В, гепатиту С, макроглобулінемія Вальденстрема, В-клітинні новоутворення, ревматоїдний артрит, синдром Шегрена або системний червоний вовчак); додаткові приклади є вузликовою еритемою, алергічним васкулітом, панікулітом, хворобою Крістіана-Вебера, гіперглобулінемічна пурпура і хвороба Бюргера; шкірні порушення, такі як контактний дерматит, лінійний дерматит, пов'язаний з IgA, вітиліго, гангренозна піодермія, природжена пухирчатка, звичайна пухирчатка (включаючи рубцеву пухирчатку і бульозну пухирчатку), осередкову алопецію (включаючи універсальну алопецію й тотальну алопецію), герпетичний дерматит, мультиформну еритему й хронічну аутоіммунну кропив'янку (включаючи ангіоневротичний набряк і уртикарний васкуліт); імунну цитопенію, таку як аутоімунна нейтропенія й аплазія лише еритроцитів; хвороби сполучної тканини, такі як CNS вовчак, дискоїдний червоний вовчак, KREST-синдром, змішані захворювання сполучної тканини, поліміозит/дерматоміозит, міозит із включеними тельцями, вторинний амілоїдоз, кріоглобулінемія типу I і II, фіброміалгію, антифосфоліпідний синдром, вторинну гемофілію, рецидивуючий поліхондрит, саркоїдоз, синдром ригідної людини, й ревматичну лихоманку; додатковим прикладом є еозинофільний фасціїт; артрити, такі як анкілозуючий спондиліт, ювенільний хронічний артрит, захворювання Стілла дорослих, і SAPHO синдром; додатковими прикладами є сакроїлеїт, реактивний артрит, хвороба Стілла і подагра; гематологічні порушення, такі як апластична анемія, первинна гемолітична анемія (включаючи синдром холодової аглютинації), гемолітична анемія, вторинна стосовно до СLL(ХЛЛ) або системного червоного вовчаку; POEMS синдром, перніціозна анемія і гіперглобулінемічна пурпура Вальденстрема; додаткові приклади є агранулоцитозом, аутоіммунною нейтропенією, хворобою Франкліна, хворобою Селігмана, хворобою мю-ланцюгів, паранеопластичним синдромом, вторинним стосовно до тимоми й лімфоми, і утворенням інгібітору чинника VIII; ендокринопатії, такі як поліендокринопатія, і хвороба Аддісона; додаткові приклади є аутоіммунною гіпоглікемією, аутоіммунним гіпотиріозом, аутоіммунним інсуліновим синдромом, тиріоідитом де Карвена, і опосередкованою антитілами толерантністю до інсуліну інсулінових рецепторів; гепатогастроінтестинальними синдромами, такими як целіакія, хвороба Віпла, первинний біліарний цироз, хронічний активний гепатит, і первинносклерозуючий холангіт; додатковим прикладом є аутоіммунний гастрит; нефропатії, такі як швидко прогресуючий гломерулонефрит, постстрептококовий поста нефрит, синдром Гудспатчера, мембранозний гломерулонефрит і кріоглобулінемічний нефрит; додатковим прикладом є захворювання з мінімальними змінами; неврологічні порушення, такі як аутоіммунні нейропатії, множинний мононеврит, міастенічний синдром Ітона-Ламберта, хорея Сиденгама, сухотка спинного мозку й синдром Джиліана-Бара; додаткові приклади є мієлопатією/місцевою спастичною парестезією, міастенією гравіс, гострою запальною демієлінізуючою полінейропатією і хронічною запальною демієлінізуючою полінейропатією; серцеві й легеневі захворювання, такі як хронічна обструктивна хвороба легенів (ХОБЛ), фіброзуючий альвеоліт, облітеруючий бронхіоліт, алергічний аспергілез, муковісцидоз, синдром Лоффлера, міокардит і перикардит; додатковими прикладами є гіперчутливий пневмоніт і паранеопластичний синдром, вторинний до раку легенів; алергічні порушення, такі як бронхіальна астма й синдром гіпер-IgE; додатковий приклад є скороминущою сліпотою; офтальмологічні захворювання, такі як ідіопатичний хореоретиніт; інфекційні хвороби, такі як інфекція паравірусом В (включаючи синдром кистей-іступнів); і акушерсько-гінекологічні захворювання, такі як рецидивуючі викидні, рецидивуючі народження мертвого плоду і затримка внутрішньоутробного розвитку; додатковим прикладом є паранеопластичний синдром, вторинний стосовно до новоутворень жіночих статевих органів; репродуктивні порушення в чоловіків, такі як паранеопластичний синдром, вторинний стосовно до новоутворень яєчок; і посттрансплантаційні розлади, такі як відторгнення ало- або ксенотрансплантату і хвороба "трансплантат проти господаря". В одному варіанті здійснення, захворювання із залученням клітин, що експресують СD20 є запальним, імунним та/або аутоіммунним порушенням, вибраним з виразкового коліту, хвороби Крону, ювенільного діабету, розсіяного склерозу, імуноопосредкованих тромбоцитопеній, таких як тромбоцитопенічна пурпура й хронічна ідіопатична тромбоцитопенічна пурпура, гемолітична анемія (включаючи аутоіммунну гемолітичну анемію), міастенія гравіс, склеродермія й звичайна пухирчатка. Даний винахід не обмежений окремими варіантами здійснення, описаними в даному документі. Більше того, різні модифікації винаходу, на додаток до описаних в даному документі, будуть зрозумілі для фахівця в галузі техніки з попереднього опису. Вказані модифікації повністю знаходяться в рамках формули винаходу. 60 10 UA 107557 C2 ФОРМУЛА ВИНАХОДУ 5 10 15 20 25 30 1. Композиція антитіла офатумумабу, що містить офатумумаб у концентрації 20-300 мг/мл, де композиція додатково містить 50 мМ ацетату натрію, 51 мМ хлориду натрію, 1 % вільної основи аргініну, 0,05 мМ EDTA, 0,02 % полісорбату 80 і рН якої скоректований до 5,5. 2. Композиція за п. 1, представлена у формі, придатній для введення внутрішньовенним або підшкірним шляхом ссавцеві, що цього потребує. 3. Композиція за п. 2, де ссавець страждає на захворювання, в якому задіяні клітини, що експресують CD20, вибрані з групи, що складається з онкогенних та імунних захворювань. 4. Композиція за п. 3, де захворювання, в якому задіяні клітини, що експресують CD20, вибрані з групи, що складається з онкогенних та імунних захворювань. 5. Композиція за п. 4, де онкогенними захворюваннями є В-клітинні лімфоми, вибрані з групи, що складається з: лімфобластного лейкозу/лімфоми з попередників В-клітин і пухлини із зрілих В-клітин, такі як В-клітинний хронічний лімфоцитарний лейкоз (СLL)/дрібноклітинна лімфоцитарна лімфома (SLL), В-клітинний пролімфоцитарний лейкоз, лімфоплазматична лімфома, лімфома з клітин мантійної зони (MCL), фолікулярна лімфома (FL), включаючи низькодиференційовану, середньодиференційовану і високодиференційовану FL, шкірну лімфому з клітин фолікулярного центру, В-клітинну лімфому з клітин маргінальної зони (MALT тип, вузловий або селезінковий тип), волосатоклітинний лейкоз, дифузна В-крупноклітинна лімфома, лімфома Беркітта, плазмоцитома, мієломна хвороба, посттранплантаційний лімфопроліферативний синдром, макроглобулінемію Валденстрема, анапластичну крупноклітинну лімфому (ALCL). 6. Композиція за п. 4, де імунне захворювання вибране з групи, що складається з: псоріазу, псоріатичного артриту, дерматиту, системної склеродермії та склерозу, запальних захворювань кишечнику (IBD), хвороби Крону, виразкового коліту, респіраторного дистрес-синдрому, менінгіту, енцефаліту, увеїту, гломерулонефриту, екземи, астми, атеросклерозу, порушення адгезії лейкоцитів, розсіяного склерозу, синдрому Рейно, синдрому Шегрена, ювенільного діабету, синдрому Рейтера, синдрому Бехчета, імунокомплексного нефриту, ІgА нефропатії, ІgМ полінейропатії, імуно-опосередкованої тромбоцитопенії, такої як гостра ідіопатична тромбоцитопенічна пурпура і хронічна ідіопатична тромбоцитопенічна пурпура, гемолітичної анемії, міастенії гравіс, вовчакового нефриту, системного червоного вовчаку, ревматоїдного артриту (РА), атопічного дерматиту, пухирчатки, хвороби Грейвса, тиреоїдиту Хашимото, грануломатоза Вегенера, синдрому Оменна, хронічної ниркової недостатності, гострого інфекційного мононуклеозу, ВІЛ і захворювань, пов'язаних з вірусом герпесу. 11 UA 107557 C2 12 UA 107557 C2 Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 13
ДивитисяДодаткова інформація
Назва патенту англійськоюAntibody formulations
Автори російськоюBrisbane, Charlene, E., Ketkar, Amol, Sharad, Lashmar, Ulla, Tove
МПК / Мітки
МПК: A61K 39/395
Мітки: офатумумабу, антитіла, композиція
Код посилання
<a href="https://ua.patents.su/15-107557-kompoziciya-antitila-ofatumumabu.html" target="_blank" rel="follow" title="База патентів України">Композиція антитіла офатумумабу</a>
Попередній патент: Зварна бокова рама візка вантажного залізничного вагона
Наступний патент: Збиральна приставка для машини для збору врожаю
Випадковий патент: Пристрій для блокування відкриття стулок вікон або дверей