Продукт cпівмікронізації, який включає селективний модулятор рецептора прогестерону
Номер патенту: 115573
Опубліковано: 27.11.2017
Автори: Батюн Флоріан, Ек Жером, Колен Оде, Жувен П'єр-Ів
Формула / Реферат
1. Продукт співмікронізації, який містить:
діючу речовину, вибрану із групи, яка складається із селективних модуляторів рецептора прогестерону формули (Іа)
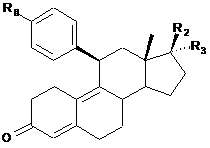 , (Iа)
, (Iа)
в якій:
R2 являє собою -ОН, алкоксигрупу С1-С5 або -C(O)R4, і
R3 являє собою -ОН, алкоксигрупу С1-С5, алкініл С2-С5, алкеніл С2-С5 або ОС(O)-R5,
R4 і R5 незалежно вибрані з алкільної групи С1-С3 і алкоксигрупи С1-С5,
R6 являє собою NR7R8, де R7 і R8 незалежно означають -Н або алкіл С1-С3;
CH=N-O-R9, в якому R9 означає -Н або - C(O)-X-R10, де R10 являє собою C1-С3алкілом, і X являє собою O, NH або S; або
C(O)R11, де R11 означає С1-С3алкіл; і
полімерну допоміжну речовину, вибрану із групи, яка складається з полімерів на основі N-вініл-2-піролідону і їх сумішей.
2. Продукт співмікронізації за п. 1, який відрізняється тим, що діюча речовина вибрана із групи, яка складається з 17a-ацетокси-11b-(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3, 20-діону, 17a-ацетокси-11b-(4-амінофеніл)-19-норпрегна-4,9-дієн-3,20-діону, ацетату уліпристалу і їх сумішей.
3. Продукт співмікронізації за пп. 1-2, який відрізняється тим, що масове співвідношення "діюча речовина/полімерна допоміжна речовина" знаходиться у діапазоні 0,1-10, переважно 0,5-4.
4. Продукт співмікронізації за будь-яким з пп. 1-3, який відрізняється тим, що:
діюча речовина є ацетатом уліпристалу й
полімерна допоміжна речовина вибрана із групи, яка складається з незшитого полівінілпіролідону, зшитого полівінілпіролідону і їх сумішей.
5. Продукт співмікронізації за будь-яким з пп. 1-4, який відрізняється тим, що він додатково включає тверду поверхнево-активну речовину, переважно додецилсульфат натрію.
6. Продукт співмікронізації за будь-яким з пп. 1-5, який відрізняється тим, що має:
d50 менше 20 мкм, переважно менше 15 мкм, і/або
d90 менше 50 мкм, переважно менше 40 мкм.
7. Спосіб одержання продукту співмікронізації за будь-яким з пп. 1-6, який включає стадії, на яких:
a) забезпечують діючу речовину за п. 1;
b) змішують діючу речовину стадії а) з полімерною допоміжною речовиною за п. 1, і
c) співмікронізують суміш, отриману на стадії b).
8. Спосіб за п. 7, який відрізняється тим, що на стадії b) діючу речовину і полімерну допоміжну речовину змішують з твердою поверхнево-активною речовиною.
9. Фармацевтична композиція, яка містить продукт співмікронізації за будь-яким з пп. 1-6 і фармацевтично прийнятну допоміжну речовину.
10. Фармацевтична композиція за п. 9, яка відрізняється тим, що фармацевтично прийнятна допоміжна речовина вибрана із групи, яка складається з розріджувача, зв'язуючого, добавки, що перешкоджає злежуванню й грудкуванню, змащувальної речовини, дезінтегранта і їх сумішей.
11. Фармацевтична композиція за п. 9 або 10, яка відрізняється тим, що містить:
0,5-80 % продукту співмікронізації,
15-95 % розріджувача, і
0-5 % змащувальної речовини,
де відсотки є масовими відносно загальної маси композиції.
12. Фармацевтична композиція за будь-яким з пп. 9-11, яка відрізняється тим, що вона включає 1-100, переважно 1-40 мг діючої речовини на одиницю дози.
13. Фармацевтична композиція за будь-яким з пп. 9-12, яка відрізняється тим, що вона придатна для перорального введення.
14. Фармацевтична композиція за будь-яким з пп. 9-13, яка відрізняється тим, що вона має форму порошку, гранули, таблетки із плівковим покриттям або без покриття, або капсули.
15. Продукт співмікронізації за будь-яким з пп. 1-6 або фармацевтична композиція за будь-яким із пп. 9-14, для застосування їх як протизаплідного засобу.
16. Продукт співмікронізації за будь-яким із пп. 1-6 або фармацевтична композиція за будь-яким з пп. 9-14 для застосування в лікуванні або профілактиці гінекологічних розладів, що переважно уражають матку.
Текст
Реферат: Предметом даного винаходу є продукт співмікронізації, який містить: діючу речовину, вибрану із групи, яка складається із селективних модуляторів рецептора прогестерону, їхніх метаболітів і їх сумішей, і полімерну допоміжну речовину на основі вініл-2-піролідону. Винахід також стосується фармацевтичної композиції, яка містить зазначений продукт співмікронізації, і їхнього терапевтичного застосування. UA 115573 C2 (12) UA 115573 C2 UA 115573 C2 5 10 15 20 25 30 35 40 45 Галузь техніки, до якої відноситься винахід Даний винахід відноситься до нової галенової форми селективного модулятора прогестерона (SPRM), більш конкретно до продукту спів-мікронізації, а також до фармацевтичних композицій, що містять зазначену галенову форму. Рівень техніки Ацетат уліпристалу (скорочено UPA) відповідає 17α-ацетокси-11β-[4-(N, Nдиметиламінофеніл]-19-норпрегна-4,9-дієн-3,20-діону (номенклатура ІЮПАК) і має наступну хімічну формулу: Його синтез описаний, зокрема, у патенті ЕР 0 422 100 і в заявці ЕР 1 602 662. Ацетат уліпристалу є синтетичним селективним модулятором рецептора прогестерона (SPRM). У силу своєї дії на рецептор прогестерона ацетат уліпристалу здатний виявляти протизаплідну дію шляхом інгібування або затримки овуляції. Клінічні дослідження показали, що ацетат уліпристалу, що вводиться у вигляді однократної дози 30 мг, дозволяє запобігти небажаній вагітності, коли його вводять протягом 120 годин після незахищеного або слабо захищеного статевого акту (Glasier et al., Lancet. 2010, 375 (9714):. 555-62; Fine і ін. Obstet Gynecol 2010, 115: 257-63). Ацетат уліпристалу, із цієї причини, сертифікований у якості екстреного контрацептиву й зареєстрований для продажу під торговельної маркою Ellaone® у Європі. Інші терапевтичні області застосування ацетату уліпристалу були запропоновані у відомому рівні техніки. Останні клінічні випробування показали, що тривалий прийом ацетату уліпристалу (5 мг або 10 мг у день) дозволяє значно полегшити симптоми, пов'язані з фібромою матки й забезпечує терапевтичний ефект, кращий, ніж в еталонного лікування, а саме ацетату лейпроліду (Donnez et al., N Engl J Med 2012; 366 (5): 421-32). На основі цих клінічних випробувань, Європейське агентство з лікарських засобів (EMEA) зареєструвало в лютому 2012 року патентований лікарський засіб Esmya® (5 мг ацетату уліпристалу) для передопераційного лікування симптомів, пов'язаних з фібромою матки. Фармацевтичні композиції, зареєстровані для продажу, у цей час включають ацетат уліпристалу в мікронізованій формі. Запатентований препарат Esmya® поставляється у вигляді таблетки без оболонки, яка включає 5 мг мікронізованого ацетату уліпристалу в комбінації з наступними допоміжними речовинами: мікрокристалічна целюлоза, маніт, кроскармелоза натрію, тальк і стеарат магнію. Ellaone®, у свою чергу, поставляється у вигляді таблетки без оболонки, яка включає 30 мг мікронізованого ацетату уліпристалу й наступні допоміжні речовини: моногідрат лактози, повідон K30, кроскармелоза натрію й стеарат магнію. Додаткові фармацевтичні композиції були описані в WO 2010/066749. Розробка нових галенових форм, придатних для введення селективних модуляторів рецептора прогестерона, таких як ацетат уліпристалу, залишається серйозною проблемою для їхнього використання в лікувальною і контрацептивною метою. У зв'язку із цим, на даний час існує потреба в нових фармацевтичних препаратах, які містять селективний модулятор рецептора прогестерона, такий як ацетат уліпристалу, і мають придатні характеристики вивільнення й біологічної доступності. Короткий виклад сутності винаходу Предметом даного винаходу є продукт спів-мікронізації, який включає: - діючу речовину, обрану із групи, яка складається із селективних модуляторів рецептора прогестерона, їхніх метаболітів і їх сумішей, і - полімерну допоміжну речовину, обрану з полімерів на основі вініл-2-піролідону і їх сумішей. У кращому здійсненні діюча речовина обрана із групи, яка складається з 17α-ацетокси-11β(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3,20-діону, 17α-ацетокси-11β-(4-амінофеніл)-19 1 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 норпрегна-4,9-дієн-3,20-діону, ацетату уліпристалу і їх сумішей. У деяких здійсненнях продукт спів-мікронізації відповідно до винаходу характеризується одним або декількома наступними ознаками: - масове співвідношення діюча речовина/полімерна допоміжна речовина становить 0,1-10, переважно 0,5-4, - діюча речовина є ацетатом уліпристалу, і полімерна допоміжна речовина обрана із групи, яка складається зі зшитого полівінілпіролідону, незшитого полівінілпіролідону і їх сумішей, - продукт спів-мікронізації також може включати тверду поверхнево-активну речовину, переважно додецилсульфат натрію, - d50 менше 20 мкм, переважно менше 15 мкм, і/або d90 менше 50 мкм, переважно менше 40 мкм. Предметом даного винаходу є також спосіб одержання продукту спів-мікронізації, як він визначений вище, який включає стадії, що складаються із: а) одержання діючої речовини, визначеної вище; b) змішування діючої речовини стадії а) з полімерною допоміжною речовиною, визначеної вище, і необов'язково із твердою поверхнево-активною речовиною, переважно додецилсульфатом натрію; і c) спів-мікронізації суміші, отриманої на стадії b). Додатковою метою даного винаходу є фармацевтична композиція, що включає продукт співмікронізації й фармацевтично прийнятну допоміжну речовину. Фармацевтично прийнятну допоміжну речовину краще обрати із групи, яка складається з розріджувача, що зв'язуючого, добавки, яка перешкоджає злежуванню й грудкуванню речовини, змащувальної речовини, дезинтегранта і їх сумішей. У деяких здійсненнях фармацевтична композиція відповідно до винаходу включає: - 0,5-80 % продукту спів-мікронізації, - 15-95 % розріджувача, і - 0-5 % змащувальної речовини, масовий процентний вміст виражений щодо загальної маси композиції. Фармацевтична композиція відповідно до винаходу може включати 1-100 мг, переважно від 1-40 мг діючої речовини на одиницю дози. Вона може бути придатна для перорального введення, і може бути у формі порошку, гранул, таблеток із плівковим покриттям або без покриття або капсул. Метою даного винаходу також є продукт спів-мікронізації або фармацевтична композиція, як вона визначена вище, для використання як протизаплідного засобу, наприклад у якості звичайного контрацептиву або в якості екстреного контрацептиву. Нарешті, метою даного винаходу також є продукт спів-мікронізації або фармацевтична композиція, як вони визначені вище, для використання в лікуванні або профілактиці гінекологічних хвороб, що переважно вражають матку. Короткий опис креслень Фіг. 1 представляє криві розчинення різних спів-мікронізатів in vitro (приклад 1 нижче): UPA/повідон 7/3 (відкриті квадрати), UPA/кросповідон (суцільні квадрати), UPA/Kollicoat® IR 7/3 (хрестики), UPA/моногідрат лимонної кислоти 7/3 (відкриті ромби), UPA/фумарова кислота 7/3 (відкриті кружечки). Контрольний експеримент: подрібнений UPA (один, у відсутності допоміжної речовини) (суцільні ромби). Вісь ординат: відсоток вивільненого UPA (%), вісь абсцис: час у хвилинах. Фіг. 2 представляє криві розчинення різних матриць діючої речовини in vitro: спів-мікронізат UPA/кросповідон/SLS 5/2/3 (відкриті трикутники), спів-мікронізат UPA/кросповідон 7/3 (суцільні квадрати), суміш спів-мікронізат UPA/кросповідона + SLS (5/2/3) (хрестики). Контрольний експеримент: подрібнений UPA (один - у відсутності допоміжної речовини) (суцільні кружечки)). Вісь ординат: відсоток вивільненого UPA (%), вісь абсцис: час у хвилинах. Докладний опис винаходу Продукт спів-мікронізації за винаходом і спосіб приготування У результаті тривалих досліджень заявник показав, що можна значно поліпшити розчинення ацетату уліпристалу (далі UPA) in vitro, завдяки технології со-мікронізації. Заявник показав, що продукт, отриманий спів-мікронізацією ацетату уліпристалу з полімерною допоміжною речовиною типу полівінілпіролідону, має властивості розчинення in vitro, зокрема швидкість розчинення за 45 хвилин, значно більш високу, ніж мікронізований сам UPA за відсутності допоміжної речовини. Це поліпшення властивостей розчинення UPA in vitro, як очікується, корелюють із поліпшенням біодоступності in vivo. У силу своїх поліпшених властивостей продукт спів-мікронізації дозволить знизити дози UPA, що вводяться для одержання бажаного 2 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 терапевтичного або контрацептивного ефекту. Зниження дози UPA повинне дозволити, серед іншого, підвищити нешкідливість, зокрема відсутність токсичності готових фармацевтичних композицій. Слід зазначити, що спів-мікронізація UPA не приводить однозначно до поліпшення його властивостей розчинності. Випробувані заявником полімерні допоміжні речовини співмікронізації, відмінні від полімерів на основі N-вінілпіролідону (приклад 1, таблиця 1 далі), не дозволяють поліпшити властивості розчинення UPA in vitro. Крім того, зненацька спів-мікронізація UPA з органічною кислотою привела до чіткого зменшення швидкості розчинення UPA in vitro (дивися приклад 1 нижче). Крім того, продукт, отриманий спів-мікронізацією UPA з полімерною допоміжною речовиною типу PEG-PVA, має швидкість розчинення UPA in vitro, яка значно нижче, ніж швидкість, яка спостерігається для подрібненого UPA. Таким чином, предметом даного винаходу є нова галенова форма, більш конкретно продукт спів-мікронізації, який включає: - діючу речовину, обрану із групи, яка складається із селективних модуляторів рецептора прогестерона, їхніх метаболітів і їх сумішей, і - допоміжну речовину на основі полімерного вініл-2-піролідону. Термін "продукт спів-мікронізації" (далі також позначений спів-мікронізат) означає продукт, отриманий мікронізацією суміші, яка включає діючу речовину й щонайменше одну допоміжну речовину. "Мікронізація" означає спосіб, який дозволяє зменшити розмір часток порошку, наприклад розмелюванням. Зменшення розміру часток підтверджується зменшенням щонайменше на 10 % параметра, обраного з d50, d10 і d90. Зменшення "щонайменше на 10 %” включає зменшення щонайменше на 20 %, щонайменше на 30 %, щонайменше на 40 %. Мікронізація може бути здійснена за допомогою комерційно доступного обладнання, такого як кульові або струменеві пневматичні млини. У контексті даного винаходу термін "мікронізований продукт" означає продукт, який перебуває у вигляді порошку, що має d90 менше 50 мкм. Таким чином, продукт спів-мікронізації відповідно до винаходу переважно має d90 менше 50 мкм. Вираз "продукт спів-мікронізації, що має d90 менше 50 мкм" означає продукт співмікронізації у вигляді порошку, у якому щонайменше 90 % часток мають розмір менше 50 мкм. Вираз "полімерна допоміжна речовина на основі вініл-2-піролідону" або, у якості альтернативного варіанта, "полімер на основі вініл-2-піролідону" означає полімер, який містить вініл-2-піролідон у якості мономера. Такі полімери охоплюють гомополімери вініл-2-піролідону й співполімери вініл-2-піролідону. Полімерна допоміжна речовина може бути зшитою або незшитою. "Співполімер" означає полімер, який містить щонайменше два різні типи мономерів. Цей термін може відноситися до статистичних співполімерів, у яких різні типи мономерів зв'язані довільно, або до блокових полімерів. Прикладом співполімеру на основі вініл-2-піролідону є, наприклад, коповідон, який є співполімером вініл-2-піролідону й вінілацетату. У деяких здійсненнях полімерна допоміжна речовина обрана із групи, яка складається зі зшитого полівінілпіролідону (далі кросповідон), незшитого полівінілпіролідону (далі повідон), коповідону і їх сумішей. Переважно, полімерна допоміжна речовина обрана із групи, яка складається зі зшитого полівінілпіролідону, незшитого полівінілпіролідону, коповідону і їх сумішей. Для цілей даного винаходу незшитий полівінілпіролідон складається з вільних полімерних ланцюгів, не зв'язаних один з одним ковалентними зв'язками. Зшитий полівінілпіролідон є мережею, яка складається з полімерних ланцюгів, зв'язаних один з одним ковалентними зв'язками. Зшиті або незшиті полівінілпіролідони є комерційно доступними. Як приклад можна згадати кросповідон Polyplasdone® XL-10, що поставляється ISP, і повідон К29 Plasdone®- К32, що поставляється BASF. У деяких здійсненнях полімерна допоміжна речовина обрана з повідонів, що мають середню 3 7 -1 4 -1 молекулярну масу в діапазоні 10 -10 г.моль , переважно 3-9×10 г.моль . Повідон, що має 4 -1 середню молекулярну масу в діапазоні 3-9×10 г.моль , включає середню молекулярну масу в -1 -1 -1 діапазоні 30000-40000 г.моль , 40000-50000 г.моль , 50000-60000 г.моль , 60000-70000 г.моль 1 -1 -1 , 70000-80000 г.моль і 80000-90000 г.моль . Як приклад придатною полімерною допоміжною речовиною може бути повідон, який має середню молекулярну масу в діапазоні 55000-65 000 -1 г.моль . В інших здійсненнях полімерна допоміжна речовина обрана із групи, яка складається із 3 UA 115573 C2 5 10 15 20 25 30 35 40 кросповідонів. Термін "селективний модулятор рецептора прогестерона" означає ліганд рецептора прогестерона, який володіє агоністичною, антагоністичною активністю або тканеспецифічною змішаною агоністичною/антагоністичною активністю, переважно агоністичною або змішаною агоністичною/антагоністичною активністю. У силу своїх загальних знань фахівці в даній області техніки можуть визначити за допомогою рутинних експериментів, чи є сполука SPRM, зокрема, звертаючись до статей Smith і O'malley, Endocrine Review, 25 (1):45-71, і Chabbert-Buffet і ін. Human Reproduction Update, 2005, 11, 293-307. SPRM сполука переважно є похідним стероїду. Приклади стероїдних SPRM надані в наступних публікаціях: Rao і ін, Steroids, 1998, 63: 523-530 і Chabbert-Buffet і ін, Human Reproduction Update, 2005, 11, 293-307. Зокрема, Chabbert-Buffe і ін. указує міфепристон, онапристон, асоприсніл, ацетат уліпристалу, Org 33628 і Org 31710, як речовини, , що є SPRM. Конкретні модулятори рецептора прогестерона переважно є стероїдними похідними, заміщеними в положенні 11β арильною групою. Таким чином, у переважному здійсненні SPRM, присутні в спів-мікронізаті, обране(і) зі сполук наступної формули (I): (I) у якій: - R1 представляє собою арильну групу, необов'язково заміщену однією або декількома групами, незалежно в орто-, пара- або метаположенні, - R2 представляє собою -ОН, алкоксигрупу С1-С5 або -C(O)R4, і - R3 представляє собою -ОН, алкоксигрупу С1-С5, алкиніл С2-С5, алкеніл С2-С5 або OC(O)-R5, R4 і R5 незалежно обрані з алкільної групи С1-С3 і алкоксигрупи С1-С5, а також їх фармацевтично прийнятних солей. Алкіл С1-С3 включає метил, етил, пропіл і ізопропіл. Алкоксигрупа С1-С5 включає групи формули -(CH2)nO(CH2)(y-n)СН3, n представляє собою ціле число в діапазоні 0-4, y представляє собою ціле число 0-4, враховуючи, що (y-n) дорівнює 0 або більше. В одному кращому здійсненні SPRM обране із групи SPRM сполук наступної формули (Ia): (Ia) у якій: - R6 представляє: - -NR7R8, де R7 і R8 незалежно позначають -Н або алкіл C1-C3, R7 і R8 переважно обрані з Н і СН3; - -CH=N-O-R9, у якому R9 позначає -Н або -C(O)-X-R10, де R10 є С1-С3 алкілом, і Х представляє О, NH або S; або -C(O)R11, де R11 означає С1-С3 алкіл; - R2 і R3 є такими, як визначено раніше. Такі сполуки включають, але без обмеження, міфепристон, ацетат уліпристалу, асопрінсил і телапристон. Зокрема, міфепристон відповідає сполуці формули (Ia), у якій R 6 є -N(СН3)2, R2 є ОН і R3 є -С C-СН3. 4 UA 115573 C2 5 10 15 В одному кращому здійсненні SPRM обране із групи SPRM сполук формули (Ia), у якій: - R2 представляє -OH, -OCH3, -C(O)СН3 або -С(O)-СН2-O-СН3 - R3 представляє -CH2-O-CH3, або - O-С(O)СН3 - R6 представляє -NH2, -NHCH3, -N(СН3)2 або -CH=N-OR9, де R9 представляє Н, -C(O)-S-С2Н5 або -C(O)-NH-С2Н5. Ця група сполук включає, зокрема, телапристон, асопрінсил і ацетат уліпристалу і їх деякі метаболіти. У деяких здійсненнях SPRM обране зі сполук формули (Ia), у якій R 6 є -CH=NO-R9. Такі сполуки включають: - асопріснил (R9 є Н, R2 є OMe і R3 є -CH2OMe), - J912 (R9 є Н, R2 є Н і R3 є -CH2OMe), - J956 (також відомий як Asoprisnil ecamate) (R9 є -С(О)-NH-С2Н5, R2 є -OMe і R3 є -CH2OMe), і - J1042 (R9 є -С(О)-S-С2Н5, R2 є ОСН3 і R3 є -CH2OMe). В інших здійсненнях SPRM обране зі сполук формули (Ia), у якій R 6 є -NH2, -NHCH3, або N(СН3)2. В одному кращому здійсненні діюча речовина, що присутня у спів-мікронізаті, обрана із групи, яка складається з ацетату уліпристалу, метаболітів ацетату уліпристалу і їх сумішей. Метаболіти UPA описані, зокрема, в Attardi et al. Journal of Steroid Biochemistry and Molecular Biology, 2004, 88:. 277-288 і проілюстровані нижче: 20 Монодеметильоване похідне UPA Дидеметильоване похідне UPA 17α-гідрокси похідне UPA похідне UPA, що включає ароматичне кільце 25 30 35 40 Переважно, метаболіт ацетату уліпристалу обраний з: 17α-ацетокси-11β-(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3,20-діону (монодеметильоване похідне) і 17α-ацетокси-11β-(4-амінофеніл)-19-норпрегна-4,9-дієн-3,20-діону (дидеметильоване похідне). У кращому здійсненні спів-мікронізата відповідно до винаходу діюча речовина обрана із групи, яка складається з 17α-ацетокси-11β-(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3,20діону, 17α-ацетокси-11β-(4-амінофеніл)-19-норпрегна-4,9-дієн-3,20-діону, ацетату уліпристалу і їх сумішей. В іншому кращому здійсненні продукт спів-мікронізації за винаходом включає: - діючу речовину, обрану із групи, яка складається з ацетату уліпристалу, 17α-ацетокси-11β(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3,20-діону, 17α-ацетокси-11β-(4-амінофеніл)-19норпрегна-4,9-дієн-3,20-діону і їх сумішей, і - полімерну допоміжну речовину, обрану із групи, яка складається зі зшитих полівінілпіролідонів, незшитих полівінілпіролідонів і їх сумішей. В одному додатковому здійсненні продукт спів-мікронізації за винаходом включає: - діючу речовину, а саме ацетат уліпристалу, і - полімерну допоміжну речовину, обрану зі зшитих полівінілпіролідонів і їх сумішей. Як приклад, продукт спів-мікронізації за винаходом може включати ацетат уліпристалу в якості діючої речовини й кросповідон у якості полімерної допоміжної речовини. Масове співвідношення діючої речовини до полімерної допоміжної речовини в співмікронізаті за винаходом може перебувати в діапазоні 0,1-10, переважно 0,5-4. Масове співвідношення "діюча речовина/полімерна допоміжна речовина" 0,5-4 включає масові 5 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 співвідношення в діапазонах 0,5-1, 1-1,5, 1,5-2, 2-2,5, 3-3,5 і 3,5-4. Переважно, масове співвідношення "діюча речовина до полімерної допоміжної речовини" перебуває в діапазоні 1,54. Придатне масове співвідношення "діюча речовина/полімерна допоміжна речовина" становить, наприклад, масове співвідношення близько 2,3. У деяких здійсненнях спів-мікронізат відповідно до винаходу може включати додаткову допоміжну речовину. Ця додаткова допоміжна речовина може підсилювати дію повідону або кросповідону на розчинення ацетату уліпристалу. Ця допоміжна речовина може бути обрана з поверхнево-активних речовин, зазвичай використовуваних у галенових препаратах і яка може бути піддана спів-мікронізації, зазвичай методом розмелювання. Термін "тверда поверхнево-активна речовина" означає поверхнево-активну речовину, яка є твердою за температури навколишнього середовища, тобто зазвичай за температури близько 20 °C. У деяких кращих здійсненнях поверхнево-активна речовина має високу температуру плавлення, переважно вище 50 °C і більш переважно вище 100 °C. Переважно, поверхневоактивна речовина може бути обрана з С8-С20, переважно С10-С14 солей алкілсульфату і їх сумішей. В одному кращому здійсненні поверхнево-активна речовина обрана із солей додецилсульфату, переважно його солей лужних або лужноземельних металів, таких як солі натрію, магнію або кальцію. Поверхнево-активна речовина, що особливо придатна для одержання продукту спів-мікронізації відповідно до винаходу, є SDS, тобто додецилсульфатом натрію. Таким чином, у кращому здійсненні поверхнево-активна речовина є додецилсульфатом натрію. В одному конкретному здійсненні продукт спів-мікронізації включає: - діючу речовину, обрану із групи, яка складається з ацетату уліпристалу, 17α-ацетокси-11β(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3,20-діону, 17α-ацетокси-11β-(4-амінофеніл)-19норпрегна-4,9-дієн-3,20-діону і їх сумішей, переважно ацетату уліпристалу, - полімерну допоміжну речовину, обрану зі зшитих полівінілпіролідонів, незшитих полівінілпіролідонів і їх сумішей, і - тверду поверхнево-активну речовину, переважно SDS. Масове співвідношення діючої речовини до поверхнево-активної речовини зазвичай становить 0,1-10, переважно 0,5-4. Придатним масовим співвідношенням "діюча речовина/поверхнево-активна речовина" є, наприклад, масове співвідношення близько 1,7. Як приклад, спів-мікронізат відповідно до винаходу може включати діючу речовину, полімерну допоміжну речовину й поверхнево-активну речовину в кількостях, які відповідають наступним масовим співвідношенням: - масове співвідношення "діюча речовина/поверхнево-активна речовина" 1-2, переважно близько 1,7 і - масове співвідношення "діюча речовина/полімерна допоміжна речовина" 2-4, переважно близько 2,5. Гранулометричний склад (тобто розподіл часток за розміром) продукту спів-мікронізації може мати вплив на розчинність UPA. Переважно, щоб d50 продукту спів-мікронізації був менше 25 мкм, переважно менше 20 мкм, або навіть менше 15 мкм. d50 менше 15 мкм включає d50 менше 12 мкм, 11 мкм, 10 мкм, 9 мкм, 8 мкм, 7 мкм, 6 мкм, 5 мкм і 4 мкм. Також переважно, щоб d90 продукту спів-мікронізації був менше 50 мкм, або навіть менше 40 мкм. d90 менше 40 мкм включає d90 менше 38 мкм, 37 мкм, 36 мкм, 35 мкм, 34 мкм, 33 мкм, 32 мкм, 31 мкм, 30 мкм, 29 мкм, 28 мкм, 27 мкм, 26 мкм, 25 мкм, 24 мкм, 23 мкм, 22 мкм, 21 мкм, 20 мкм, 19 мкм, 18 мкм, 17 мкм, 16 мкм, 15 мкм, 14 мкм, 13 мкм, 12 мкм, 11 мкм, і 10 мкм. У деяких здійсненнях продукт спів-мікронізації відповідно до винаходу характеризується тим, що його гранулометричний склад включає: - d50 менше 20 мкм, переважно менше 15 мкм, і/або - d90 менше 50 мкм, переважно менше 40 мкм і більш переважно менше 30 мкм. Як приклад, спів-мікронізат відповідно до винаходу може мати d50 менше 5 мкм і/або d90 менше 15 мкм. d10 спів-мікронізата відповідно до винаходу звичайно становить більше 0,05 мкм. У контексті даного винаходу "d50 менше Х мкм" означає, що щонайменше 50 % часток співмікронізата мають розмір менший за X мкм. "d90 менше Y мкм" означає, що щонайменше 90 % часток спів-мікронізата мають розмір 6 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 менший за Y мкм. Аналогічно, "d10 більше Z мкм" означає, що щонайменше 90 % часток спів-мікронізата мають розмір часток більший Z мкм. Гранулометрія, тобто розподіл часток за розмірами, продукту спів-мікронізації й, зокрема, параметри d10, d50 і d90, можуть бути визначені за допомогою будь-якого способу, відомого фахівцям у даній області. Переважно, буде використовуватися лазерна дифракція. Продукт спів-мікронізації має поліпшені властивості розчинення діючої речовини in vitro. У деяких здійсненнях продукт спів-мікронізації відповідно до винаходу характеризується тим, що щонайменше 55 % присутньої діючої речовини вивільняється протягом 45 хвилин, коли зазначений продукт спів-мікронізації випробовують на розчинність in vitro, переважно як визначено в Європейській фармакопеї §2.9.3. Випробування на розчинність in vitro може бути здійснене з використанням будь-якого комерційно доступного обладнання. Приклад 1 далі представляє умови визначення in vitro швидкості розчинення спів-мікронізата за винаходом. Коротко, спів-мікронізат зі вмістом діючої речовини 30 мг розміщають у капсулі з желатинового гелю. Цю желатинову капсулу потім поміщають в 900 мл буферного середовища із рН шлункового соку, що включає 0,1 % SDS, за 37±0,5 °C, і перемішують при 50 обертах на хвилину (RPM) (швидкість обертання лопатей обладнання розчинення). Розчинення діючої речовини в середовищі можна контролювати спектрофотометрично при довжині хвилі максимального поглинання. Для цілей даного винаходу рН шлункового соку звичайно становить рН 1-3. "Щонайменше 55 % діючої речовини, що вивільняється протягом 45 хвилин" включає щонайменше 55 %, щонайменше 60 %, щонайменше 65 %, щонайменше 70 %, щонайменше 75 %, щонайменше 80 % діючої речовини вивільняється протягом 45 хвилин. Переважно, щонайменше 60 % діючої речовини вивільняється протягом 45 хвилин. Продукт спів-мікронізації також може бути охарактеризований тим, що щонайменше 45 % діючої речовини, яку він містить, вивільняється протягом 30 хвилин, коли він випробовується на розчинення in vitro, як описано вище. Предметом даного винаходу також є спосіб приготування вищеописаного спів-мікронізата, що включає стадії, які полягають в: a) одержанні діючої речовини, обраної із групи, яка складається з ацетату уліпристалу, метаболіту ацетату уліпристалу і їх сумішей, b) змішуванні діючої речовини стадії а) з полімерною допоміжною речовиною, і c) спів-мікронізації суміші, отриманої на стадії b), слід розуміти, що діюча речовина й полімерна допоміжна речовина відповідають наведеним вище визначенням. Діюча речовина, отримана на стадії а), може бути в мікронізованій або не мікронізованій формі. Крім того діюча речовина може бути аморфною або кристалічною. Переважно діюча речовина, отримана на стадії а), перебуває в кристалічній формі. У деяких здійсненнях стадія b) може, крім того, включати змішування діючої речовини з фармацевтичною допоміжною речовиною, переважно поверхнево-активною речовиною. Це змішування може бути здійснене до, одночасно або після змішування діючої речовини з полімерною допоміжною речовиною. Додаткова фармацевтична допоміжна речовина може бути в мікронізованій або не мікронізованій формі. Стадія мікронізації с) може бути виконана з використанням комерційно доступної системи мікронізації. Зокрема, вона може бути здійснена з використанням струменево-пневматичного або кульового млина. Фахівці в даній області на основі загальних знань і результатів рутинних експериментів зможуть визначити умови проведення стадії с) для одержання продукту співмікронізації, що має потрібний розподіл часток за розмірами. Як приклад, коли стадію с) проводять із використанням струменево-пневматичного млина, фахівець у даній області зможе змінювати потік подачі порошку й тиск повітряних струменів для того, щоб змінити розподіл часток за розмірами кінцевого спів-мікронізату. Фармацевтична композиція за винаходом Продукт спів-мікронізації призначений в основному для терапевтичного використання або в якості протизаплідних засобів. З цією метою він може бути введений безпосередньо, або вставлений в обладнання доставки, таке як вагінальні кільця, пластир, внутрішньоматкова спіраль або імплантат. Як правило, продукт спів-мікронізації відповідно до винаходу інтегрований у фармацевтичну композицію, щоб полегшити його введення. Таким чином, додатковим предметом даного винаходу є фармацевтична композиція, що включає продукт спів-мікронізації, як він визначений 7 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 вище, і щонайменше одна фармацевтично прийнятна допоміжна речовина. Фахівці в даній області техніки зможуть вибрати допоміжну речовину(а), поєднувану із продуктом спів-мікронізації, відповідно до остаточної форми фармацевтичної композиції, бажаного способу введення й бажаного профілю вивільнення діючої речовини. Для цього фахівець у даній області техніки буде мати можливість звернутися до наступних довідкових матеріалів: Remington: The Science and Practice of Pharmacy (Lippincott Williams & Wilkins; Twenty first Edition, 2005) і Handbook of Pharmaceuticals Excipients, American Pharmaceutical Association (Pharmaceutical Press; 6th revised edition, 2009). Фармацевтична композиція й спів-мікронізат за винаходом можуть бути введені будь-яким шляхом, зокрема оральним, трансбукальним, назальним, сублінгвальним, вагінальним, внутрішньоматковим, ректальним, трансдермальним шляхом або парентеральним шляхом, наприклад шляхом внутрішньовенної ін'єкції. Кращими шляхами введення є трансбукальний, оральний, внутрішньоматковий і вагінальний. Фармацевтична композиція відповідно до винаходу може бути в будь-якій формі, наприклад у формі таблетки, порошку, капсули, пігулки, супозиторія, вагінального супозиторія, облатки, суспензії, водного, спиртового або масляного розчину, сиропу, гелю, мазі, емульсії, ліофілізату або плівки для розсмоктування. Спосіб уведення й галенова форми фармацевтичної композиції можуть залежати від бажаного терапевтичного або контрацептивного ефекту. У деяких здійсненнях фармацевтична композиція відповідно до винаходу може бути інтегрована в обладнання, що забезпечує тривале введення діючої речовини. Фармацевтична композиція може бути, зокрема, включена у вагінальне кільце, внутрішньоматкову спіраль, пластир, наприклад трансдермальний або мукоадгезивний пластир або в імплантат, наприклад імплантат контрацептивного типу. Приклади вагінальних кілець, придатних для здійснення винаходу, можна знайти в WO 2006/10097. У додаткових здійсненнях фармацевтична композиція відповідно до винаходу перебуває у твердій формі. Переважно, фармацевтична композиція відповідно до винаходу є твердою й призначена для перорального введення. У деяких здійсненнях фармацевтична композиція відповідно до винаходу характеризується тим, що фармацевтично прийнятна допоміжна речовина обрана із групи, яка складається з розріджувача, зв'язуючого, добавки, що перешкоджає злежуванню й грудкуванню, змащувальної речовини, дезинтегранта та їх сумішей. Для цілей даного винаходу розріджувач може бути представлений однією або кількома сполуками, здатними ущільнювати діючу речовину таким чином, щоб одержати потрібну масу. Розріджувачі включають неорганічні фосфати, моносахариди й поліоли, такі як ксиліт, сорбіт, лактоза, галактоза, ксилоза або маніт, дисахариди, такі як сахароза, олігосахариди, полісахариди, такі як целюлоза і її похідні, крохмалі і їх суміші. Розріджувач може мати безводну або гідратовану форму. Як приклад, придатний розріджувач може бути обраний з мікрокристалічної целюлози, маніту, лактози і їх сумішей. Зв'язуюче може бути одним або декількома сполуками, здатними поліпшити зчеплення діючої речовини з розріджувачем. Як приклад зв'язуючих можна згадати гідроксипропілцелюлозу, гідроксипропілметилцелюлозу, повідон (полівінілпіролідон), співполімери вініл-2-піролідону й вінілацетату (коповідон) і їх суміші. Змащувальна речовина може бути однією або декількома сполуками, здатними запобігати проблемам, пов'язаним з виготовленням сухих галенових форм, такі як прилипання й/або проблеми захоплення, які виникають у машинах при пресуванні або заповненні. Кращими змащувальними речовинами є жирні кислоти або похідні жирних кислот, такі як стеарат кальцію, гліцерилмоностеарат, гліцерилпальмітостеарат, стеарат магнію, стеарат цинку або стеаринова кислота, поліалкіленгліколі, зокрема поліетиленгліколь, бензоат натрію або тальк. Змащувальні речовини, які відповідно до винаходу, є кращими є солями стеарату і їх сумішами. Підходящою змащувальною речовиною є, наприклад, стеарат магнію. Добавка, що перешкоджає злежуванню й грудкуванню, необов'язково використовувана відповідно до винаходу, може бути обрана зі сполук, що містять кремній, наприклад, тальк, безводний колоїдний диоксид кремнію або осаджений диоксид кремнію. Дезинтегрант може використовуватися для поліпшення вивільнення діючої речовини. Він може бути обраний, наприклад, зі зшитого полівінілпіролідону (кросповідон), зшитої карбоксиметилцелюлози (наприклад, кроскармелоза натрію) або незшитих карбоксиметилцелюлози, крохмалів і їх суміші. Дезинтегрант переважно обраний із групи, яка складається із кроскармеллози натрію, кросповідона та їх сумішей. У деяких здійсненнях композиція за даним винаходом включає: 8 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 - 0,5-80 % продукту спів-мікронізації, як він визначений вище, - 15-95 % розріджувача, переважно обраного з маніту, лактози, мікрокристалічної целюлози і їх сумішей, і - 0-5 % змащувальної речовини, переважно стеарату, такого як стеарат магнію, масовий процентний вміст виражений відносно загальної маси композиції. Композиція за даним винаходом може бути додатково охарактеризована тим, що вона включає 0-20 % мас. зв'язуючого, 0-10 % розпушувача й 0-5 % мас. добавки, що перешкоджає злежуванню й грудкуванню. Слід зазначити, що масовий процентний вміст дезінтегратора фармацевтичної композиції відповідно до винаходу не враховує кросповідон, що необов'язково міститься в спів-мікронізаті. Аналогічно, масовий процентний вміст зв'язуючого у фармацевтичній композиції відповідно до винаходу не включає повідон, що необов'язково міститься в спів-мікронізаті. В інших здійсненнях фармацевтична композиція відповідно до винаходу включає: - 1-60 % мас. продукту спів-мікронізації, як він описаний вище, - 30-95 % мас. розріджувача, - 0-10 % мас. дезінтегратора, - 0-10 % мас. зв'язуючого, - 0-5 % мас. добавки, що перешкоджає злежуванню й грудкуванню, і - 0,1-2 % змащувальної речовини, масовий процентний вміст виражений відносно загальної маси композиції. Фармацевтична композиція відповідно до винаходу також може включати одну або декілька допоміжних речовин на додаток до вищевказаних допоміжних речовин. Додаткова допоміжна речовина(и) може бути обрана із групи, яка складається з поверхнево-активних речовин, таких як SDS, покриваючих речовин, таких як покриваючі речовини на основі полівінілового спирту або гідроксипропілметилцелюлози, пігментів, таких як оксид алюмінію або оксид заліза, ароматизаторів, зволожувачів, восків, диспергаторів, стабілізаторів і консервантів. Фармацевтична композиція відповідно до винаходу може бути приготовлена будь-яким зі способів, зазвичай використовуваних для галенових препаратів. Ці способи звичайно включають змішування продукту спів-мікронізації відповідно до винаходу з одним або декількома допоміжними речовинами, потім формування отриманої суміші. Як приклад, коли вона має форму таблетки, фармацевтична композиція відповідно до винаходу може бути виготовлена прямим пресуванням або пресуванням після сухої або вологої грануляції. Продукт спів-мікронізації, присутній у фармацевтичній композиції відповідно до винаходу, може мати будь-яку з ознак, описаних у даній заявці. Зокрема, продукт спів-мікронізації фармацевтичної композиції має одну або декілька (1, 2, 3, 4, 5, 6, 7 або 8) з наступних ознак: i. діючою речовиною є UPA, ii. полімерна допоміжна речовина обрана із групи, яка складається з повідонів, кросповідонів і їх сумішей, iii. "масове співвідношення діюча речовина/полімерна допоміжна речовина" перебуває в діапазоні 0,5-4, iv. додатково включає поверхнево-активну речовину, переважно SDS, v. коли присутня поверхнево-активна речовина, "масове співвідношення діюча речовина/поверхнево-активна речовина" становить 0,5-4, vi. d50 продукту спів-мікронізації становить менше 20 мкм, переважно менше 15 мкм, vii. d90 продукту спів-мікронізації становить менше 50 мкм, переважно менше 40 мкм, і viii. щонайменше 55 % діючої речовини, що міститься в продукті спів-мікронізації, вивільняється протягом 45 хвилин, коли зазначений продукт спів-мікронізації випробовують на розчинення in vitro, переважно за наступних умов: - обладнання: лопатеве обладнання розчинення, - зразок: желатинові капсули, що містять спів-мікронізат у кількості, що відповідає 30 мг діючої речовини, - середовище розчинення: 900 мл буферного водного розчину при рН шлункового соку, що включає 0,1 % SDS, - температура: 37±0,5 °C, і - швидкість обертання лопатей: 50 обертів на хвилину (об/хв.). Як зазначено вище, композиція за винаходом може перебувати у вигляді порошку, гранул, таблеток із плівковим покриттям або без плівкового покриття або гелевих капсул і переважно призначених для перорального введення. У деяких здійсненнях фармацевтична композиція відповідно до винаходу перебуває у вигляді таблеток без плівкового покриття, призначених для перорального введення. 9 UA 115573 C2 5 10 15 20 25 30 35 40 45 50 55 60 Композиція відповідно до винаходу може бути фармацевтичною композицією з контрольованим, негайним, пролонгованим або вповільненим вивільненням. Переважно, композиція відповідно до винаходу є композицією з негайним вивільненням. Термін "композиція з негайним вивільненням" означає фармацевтичну композицію, що характеризується тим, що щонайменше 75 % діючої речовини, що спочатку міститься в одиниці дози фармацевтичної композиції, вивільняється протягом 45 хвилин, коли зазначена одиниця дози зазнає випробування in vitro на розчинність, наприклад, як визначено в Європейській Фармакопеї §2.9.3, і переважно за наступних умов: - лопатеве обладнання розчинення, - середовище розчинення: буферний водний розчин при рН шлункового соку, що містить 0,1 % SDS, - температура: 37±0,5 °C, і - швидкість обертання: 50 об/хв. Обсяг середовища розчинення залежить від кількості діючої речовини, що міститься в одиниці дози. Для одиниці дози, що включає 5 мг діючої речовини, використовують 500 мл середовища розчинення. Для одиниці дози, що містить 30 мг діючої речовини, використовують 900 мл середовища розчинення. Звичайно фармацевтична композиція містить 1-100 мг діючої речовини на одиницю дози, переважно 1-40 мг або навіть 2-30 мг діючої речовини на одиницю дози. Доза діючої речовини залежить від терапевтичного або контрацептивного ефекту й від бажаної схеми введення. Наприклад, для деяких здійснень кількість UPA на одиницю дози може становити 1-5 мг. При екстреній контрацепції діюча речовина може бути присутня у кількості 20-40 мг на одиницю дози. При звичайній контрацепції діюча речовина може бути присутня у кількості 2-5 мг на одиницю дози. Для терапевтичних цілей, таких як лікування фіброми матки, діюча речовина може бути присутня у кількості 3-15 мг на одиницю дози. Доза діючої речовини й схема введення також може залежати від особистих параметрів пацієнта, зокрема ваги, віку, статі, загального стану здоров'я й раціону, захворювання, на яке страждає пацієнт і т.д. Нарешті, фармацевтична композиція відповідно до винаходу може включати додаткову діючу речовину. Ця додаткова діюча речовина може виявляти дію, відмінну від UPA або його метаболітів. Вона також може підсилювати терапевтичний ефект UPA або його метаболітів. Терапевтичне або контрацептивне використання спів-мікронізата й фармацевтичної композиції за даним винаходом У додатковому аспекті об'єктом даного винаходу також є продукт спів-мікронізації або фармацевтична композиція, як вони описані вище, для застосування їх як лікарського засобу. Продукт спів-мікронізації або композиція відповідно до винаходу є особливо придатними для використання в якості систематичної або екстренної контрацепції. Вони також можуть бути використані для лікування або профілактики гормональних, гінекологічних або ендокринних розладів, таких як хвороба Кушинга. Композиція або продукт спів-мікронізації відповідно до винаходу можуть бути використані, зокрема, при лікуванні або профілактиці гінекологічних розладів, що переважно вражають матку, включаючи доброякісні гінекологічні порушення. Гінекологічні порушення включають (але не обмежуються цим) фіброму матки і її симптоми, аденоміоз, ендометріоз, болі, пов'язані з дислокацією ендометрію й надмірна маткова кровотеча. Додатковим об'єктом даного винаходу є застосування продукту спів-мікронізації відповідно до винаходу для приготування протизаплідного засобу або приготування лікарського засобу, призначеного для лікування або профілактики кожного з перерахованих вище захворювань. Предметом винаходу також є спосіб контрацепції, що включає введення пацієнтові протизаплідної дози продукту спів-мікронізації або фармацевтичної композиції відповідно до винаходу. Термін "спосіб контрацепції" означає спосіб, який дозволяє запобігти виникненню вагітності в пацієнта дітородного віку. У розглянутому випадку це може бути спосіб екстреної контрацепції. У цьому випадку одну дозу переважно вводять пацієнтові протягом відповідного періоду часу після незахищеного або недостатньо захищеного статевого акту, як правило в межах 120 год. після незахищеного або недостатньо захищеного статевого акту. Спосіб контрацепції може бути також способом звичайної контрацепції, у якому композицію або продукт спів-мікронізації вводять пацієнтові постійно й циклічно або безупинно за допомогою обладнання, такого як імплантат або вагінальне кільце. В альтернативному варіанті спосіб контрацепції може бути 10 UA 115573 C2 5 10 15 20 25 30 35 40 способом контрацепції "за необхідності", як описано в WO 2010/119029. Нарешті, об'єктом даного винаходу є також спосіб лікування захворювання або розладу в пацієнта, який включає введення терапевтично ефективної дози продукту спів-мікронізації або фармацевтичної композиції відповідно до винаходу пацієнтові, переважно пацієнтові жіночої статі. Терапевтичний спосіб відповідно до винаходу переважно відноситься до кожного з вищевказаних захворювань або розладів. Зрозуміло, що для реалізації вищеописаних способів і застосувань продукт спів-мікронізації й фармацевтична композиція за даним винаходом можуть мати одну або кілька ознак, докладно описаних у даному описі. Метою нижченаведених прикладів є більш повна ілюстрація винаходу, однак без обмеження його обсягу. Приклади Приклад 1. Приготування спів-мікронізатів і скринінг допоміжних речовин 1. Матеріали й способи - Приготування спів-мікронізатів Продукти спів-мікронізації ацетату уліпристалу (далі "спів-мікронізати") готують у такий спосіб: ацетат уліпристалу й тестовану допоміжну речовину спів-мікронізації змішують у потрібному масовому співвідношенні в ступці й розтирають до одержання однорідної суміші. Отриману суміш потім мікронізують у кульовому млині-гомогенізаторі для одержання бажаного гранулометричного складу. - Розчинення спів-мікронізатів UPA in vitro Для кожного отриманого спів-мікронізата готують тверді желатинові капсули, що містять кількість спів-мікронізата, що відповідає 30 мг на капсулу UPA. Дослідження розчинення in vitro спів-мікронізата UPA проводять із використанням цих капсул відповідно до Європейської Фармакопеї §2.9.3, використовуючи лопатеве обладнання розчинення. Для кожного спів-мікронізата желатинову капсулу, що містить зазначений спів-мікронізат, поміщають у ємність обладнання для розчинення, що містить 900 мл середовища розчинення. Середовище розчинення є водним буферним розчином із рН шлункового соку, яке містить 0,1 % мас. SDS. Умови проведення розчинення in vitro наступні: - швидкість обертання лопатей: 50 обертів на хвилину (об/хв.) - температура: 37 °C±0,5 °C Розчинення UPA контролюють спектрофотометрично. У якості контрольного експерименту використовують желатинові капсули, що містять 30 мг тільки мікронізованого ацетату уліпристалу (тобто UPA мікронізований за відсутності будь-якої допоміжної речовини спів-мікронізації). Для кожного спів-мікронізата експеримент з розчинення відтворюють 3 рази. 2. Результати - Серія експериментів 1: Скринінг допоміжної речовини спів-мікронізації У таблиці 1 нижче й на Фіг 1 представлені результати з розчинення, отримані для кожного приготовленого спів-мікронізата. Відсоток розчинення виражений щодо вихідної кількості UPA, що міститься в кожній желатиновій капсулі. Таблиця 1 Результати випробувань на розчинення in vitro приготовлених спів-мікронізатів UPA/допоміжна речовина. Масове співвідношення UPA/допоміжна речовина 7/3. Контрольний експеримент: один мікронізований UPA Відсоток UPA, що вивільнився, виражений відносно вихідної кількості UPA, що міститься в капсулі (Середнє значення 3 експериментів) Повідон Кросповідон Моногідрат Час Мікронізований Фумарова (Plasdone® (Polyplasdone® Kollicoat® IR лимонної (хв.) UPA кислота K29-32) XL10) кислоти 0 0,00 0,00 0,00 0,00 0,00 0,00 1 0,00 0,40 0,00 0,20 0,10 1,10 5 5,50 1,00 0,50 0,50 0,50 1,20 7.5 15,00 1,70 2,60 0,70 0,60 1,80 10 22,30 4,10 6,80 0,90 0,80 2,10 15 30,00 14,50 17,10 1,10 1,10 2,30 20 34,30 30,60 34,80 1,40 1,60 2,90 11 UA 115573 C2 Час Мікронізований (хв.) UPA 30 45 60 5 10 15 39,50 47,50 53,80 Повідон (Plasdone® K29-32) 52,50 63,20 69,10 Кросповідон (Polyplasdone® XL10) 69,90 88,90 92,60 Kollicoat® IR 2,50 5,30 8,80 Моногідрат лимонної кислоти 2,60 4,70 7,10 Фумарова кислота 5,70 11,00 16,40 Kollicoat IR® є привитим співполімером поліетиленгліколь/полівініловий спирт. Ці результати показують, що спів-мікронізація ацетату уліпристалу із кросповідоном або повідоном дозволяє значно поліпшити кінцеву кількість (при t=60 хв.) вивільненого UPA і, отже, загальну швидкість розчинення. Слід зазначити, що відсоток вивільненого ацетату уліпристалу в середовищі при t=30 хв. становить близько 52 % для гелевої капсули, яка містить співмікронізат UPA/повідон, і близько 69 % для гелевої капсули, яка містить спів-мікронізат UPA/кросповідон, у той час як тільки близько 39 % для капсули, яка містить мікронізований ацетат уліпристалу. Спів-мікронізат UPA і Kollicoat IR® має швидкість вивільнення UPA, яка набагато нижче, ніж спостерігається для мікронізованого UPA, тому що після 60 хв., вивільняється менше 10 % UPA, що початково міститься в спів-мікронізатах. Оскільки розчинність ацетату уліпристалу залежить від рН (див таблицю 2 нижче), очікувалося, що спів-мікронізація ацетату уліпристалу з кислою допоміжною речовиною, такою як лимонна кислота або фумарова кислота, дозволить поліпшити розчинення ацетату уліпристалу за рахунок зниження рН у найближчому оточенні лікарської форми й, отже, локального збільшення його розчинності. Таблиця 2 Розчинність UPA залежно від рН ph 1,2 4,5 6,8 20 25 30 35 Розчинність UPA (г/л) 22,7 0,039 0,005 Несподівано виявилося, що спів-мікронізація UPA з органічною кислотою приводить до явного зниження швидкості розчинення UPA і кінцевої швидкості розчинення (при t=60 хв.) UPA. Висновок Спів-мікронізація в присутності полімеру на основі N-вінілпіролідону, такого як повідон або кросповідон, дозволила поліпшити профіль розчинення UPA in vitro у порівнянні з UPA у мікронізованій формі. З іншого боку, всупереч тому, що можна було б очікувати, інші випробувані в цьому прикладі допоміжні речовини спів-мікронізації, явно негативно впливають на вивільнення UPA. - Серія експериментів 2: вплив додавання поверхнево-активної речовини Готують наступні спів-мікронізати: - спів-мікронізат UPA/кросповідон 7/3 і - спів-мікронізат UPA/кросповідон/SDS 5/2/3. Також готують матрицю шляхом змішування спів-мікронізата UPA/кросповідон 5/2 з SDS для одержання суміші UPA/кросповідон/SDS 5/2/3. Ця матриця далі називається UPA/Кросповідон/зовнішній SDS. У якості контрольного експерименту використовують порошок мікронізованого UPA. Ці різні матриці діючої речовини випробовують in vitro на розчинення, як описано вище в розділі "Матеріали й способи". Отримане розчинення in vitro показане на Фіг. 2, і презентовано в таблиці 3 нижче. 12 UA 115573 C2 Таблиця 3 У пробірці результатів розчинення Час (хв.) 0 1 5 7,5 10 15 20 30 45 60 5 Відсоток UPA, що вивільнився, виражений відносно вихідної кількості UPA, що міститься в капсулі (Середнє значення 3 експериментів)) UPA/ кросповідон/ UPA/ кросповідон UPA/ кросповідон/ Мікронізований UPA додатковий SDS 7/3 SDS (5/2/3) (порівняння) (5/2/3) (винахід) (винахід) (винахід і порівняння) 0,00 0,00 0,00 0,00 0,00 0,00 0,40 0,00 5,50 0,50 7,10 2,80 15,00 2,60 18,00 10,30 22,30 6,80 28,00 25,80 30,00 17,10 58,30 40,70 34,30 34,80 67,60 48,10 39,50 69,90 80,70 58,70 47,50 88,90 85,40 66,10 53,80 92,60 86,80 70,40 Поліпшення розчинення in vitro спостерігається для всіх випробуваних спів-мікронізатів. Поліпшення менш помітне для матриці UPA/Кросповідон/додатковий SDS, що ілюструє специфічний ефект спів-мікронізації (у порівнянні з фізичною сумішшю). Приклад 2. Фармацевтичні композиції, що включають спів-мікронізат відповідно до винаходу Таблиці 4 і 5 далі представляють приклади фармацевтичної композиції відповідно до винаходу. Ці фармацевтичні композиції можуть бути отримані шляхом прямого пресування суміші, що містить спів-мікронізат і різні допоміжні речовини. 10 Таблиця 4 Приклад композиції відповідно до винаходу, що містить 5 мг UPA Інгредієнти Функція Спів-мікронізат UPA/кросповідон 7/3 Матриця діючої речовини Мікрокристалічна целюлоза Розріджувач Маніт Розріджувач Кросповідон Дезинтегрант Стеарат магнію Ковзна речовина Усього % мас. мг/таблетку 4,7 7,1 (т.б.5 мг UPA) 60,8 91,2 29,0 43,5 4,9 7,4 0,5 0,8 150 Ця композиція може бути використана, наприклад, для лікування фіброми матки. Таблиця 5 Приклад композиції відповідно до винаходу, що містить 30 мг UPA Інгредієнти Спів-мікронізат UPA/кросповідон 7/3 Мікрокристалічна целюлоза Маніт Кросповідон Стеарат магнію Усього 15 Функція Матриця діючої речовини Розріджувач Розріджувач Дезинтегрант змащувальна речовина % мас. мг/таблетку 28,4 42,6 (тобто 30 мг UPA) 37,1 55,7 29,0 43,5 4,9 7,4 0,5 0,8 150 Ця композиція може бути використана, наприклад, для екстреної контрацепції. 13 UA 115573 C2 ФОРМУЛА ВИНАХОДУ 5 1. Продукт співмікронізації, який містить: діючу речовину, вибрану із групи, яка складається із селективних модуляторів рецептора прогестерону формули (Іа) R6 R2 R3 O 10 15 20 25 30 35 40 45 50 , (Iа) в якій: R2 являє собою -ОН, алкоксигрупу С1-С5 або -C(O)R4, і R3 являє собою -ОН, алкоксигрупу С1-С5, алкініл С2-С5, алкеніл С2-С5 або ОС(O)-R5, R4 і R5 незалежно вибрані з алкільної групи С1-С3 і алкоксигрупи С1-С5, R6 являє собою NR7R8, де R7 і R8 незалежно означають -Н або алкіл С1-С3; CH=N-O-R9, в якому R9 означає -Н або - C(O)-X-R10, де R10 являє собою C1-С3алкілом, і X являє собою O, NH або S; або C(O)R11, де R11 означає С1-С3алкіл; і полімерну допоміжну речовину, вибрану із групи, яка складається з полімерів на основі N-вініл2-піролідону і їх сумішей. 2. Продукт співмікронізації за п. 1, який відрізняється тим, що діюча речовина вибрана із групи, яка складається з 17-ацетокси-11-(4-N-метиламінофеніл)-19-норпрегна-4,9-дієн-3, 20-діону, 17-ацетоксі-11-(4-амінофеніл)-19-норпрегна-4,9-дієн-3,20-діону, ацетату уліпристалу і їх сумішей. 3. Продукт співмікронізації за пп. 1-2, який відрізняється тим, що масове співвідношення "діюча речовина/полімерна допоміжна речовина" знаходиться у діапазоні 0,1-10, переважно 0,5-4. 4. Продукт співмікронізації за будь-яким з пп. 1-3, який відрізняється тим, що: діюча речовина є ацетатом уліпристалу й полімерна допоміжна речовина вибрана із групи, яка складається з незшитого полівінілпіролідону, зшитого полівінілпіролідону і їх сумішей. 5. Продукт співмікронізації за будь-яким з пп. 1-4, який відрізняється тим, що він додатково включає тверду поверхнево-активну речовину, переважно додецилсульфат натрію. 6. Продукт співмікронізації за будь-яким з пп. 1-5, який відрізняється тим, що має: d50 менше 20 мкм, переважно менше 15 мкм і/або d90 менше 50 мкм, переважно менше 40 мкм. 7. Спосіб одержання продукту співмікронізації за будь-яким з пп. 1-6, який включає стадії, на яких: a) забезпечують діючу речовину за п. 1; b) змішують діючу речовину стадії а) з полімерною допоміжною речовиною за п. 1, і c) співмікронізують суміш, отриману на стадії b). 8. Спосіб за п. 7, який відрізняється тим, що на стадії b) діючу речовину і полімерну допоміжну речовину змішують з твердою поверхнево-активною речовиною. 9. Фармацевтична композиція, яка містить продукт співмікронізації за будь-яким з пп. 1-6 і фармацевтично прийнятну допоміжну речовину. 10. Фармацевтична композиція за п. 9, яка відрізняється тим, що фармацевтично прийнятна допоміжна речовина вибрана із групи, яка складається з розріджувача, зв'язуючого, добавки, що перешкоджає злежуванню й грудкуванню, змащувальної речовини, дезінтегранта і їх сумішей. 11. Фармацевтична композиція за п. 9 або 10, яка відрізняється тим, що містить: 0,5-80 % продукту співмікронізації, 15-95 % розріджувача, і 0-5 % змащувальної речовини, де відсотки є масовими відносно загальної маси композиції. 14 UA 115573 C2 5 10 12. Фармацевтична композиція за будь-яким з пп. 9-11, яка відрізняється тим, що вона включає 1-100, переважно 1-40 мг діючої речовини на одиницю дози. 13. Фармацевтична композиція за будь-яким з пп. 9-12, яка відрізняється тим, що вона придатна для перорального введення. 14. Фармацевтична композиція за будь-яким з пп. 9-13, яка відрізняється тим, що вона має форму порошку, гранули, таблетки із плівковим покриттям або без покриття або капсули. 15. Продукт співмікронізації за будь-яким з пп. 1-6 або фармацевтична композиція за будь-яким із пп. 9-14 для застосування їх як протизаплідного засобу. 16. Продукт співмікронізації за будь-яким із пп. 1-6 або фармацевтична композиція за будь-яким з пп. 9-14 для застосування в лікуванні або профілактиці гінекологічних розладів, що переважно уражають матку. 15 UA 115573 C2 Комп’ютерна верстка В. Мацело Міністерство економічного розвитку і торгівлі України, вул. М. Грушевського, 12/2, м. Київ, 01008, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 16
ДивитисяДодаткова інформація
Назва патенту англійськоюCo-micronisation product comprising a selective progesterone-receptor modulator
Автори англійськоюBattung, Florian, Juvin, Pierre-Yves, Hecq, Jerome, Colin, Aude
Автори російськоюБатюн Флориан, Жувэн Пьер-Ив, Эк Жэром, Колен Одэ
МПК / Мітки
МПК: A61K 31/57, A61K 9/14, A61K 47/32
Мітки: прогестерону, включає, рецептора, селективний, cпівмікронізації, продукт, модулятор
Код посилання
<a href="https://ua.patents.su/18-115573-produkt-cpivmikronizaci-yakijj-vklyuchaeh-selektivnijj-modulyator-receptora-progesteronu.html" target="_blank" rel="follow" title="База патентів України">Продукт cпівмікронізації, який включає селективний модулятор рецептора прогестерону</a>
Попередній патент: Спосіб коригування вихідного сигналу сенсора при вимірюванні тиску в умовах швидкозмінного термовпливу
Наступний патент: Контейнер, спосіб і система керування
Випадковий патент: Система автоматичного керування просторовим рухом підводного апарата підвищеної точності






















