Вакцина, яка містить бактерії, які є збудником верхніх дихальних шляхів і статевих шляхів курчат
Номер патенту: 96948
Опубліковано: 26.12.2011
Автори: Вазкез Марія Елена, Кампогаррідо Рауль, Сіванандан Вайсінасан, Гонзалес-Ернандес Карлос
Формула / Реферат
1. Вакцина, що містить в інактивованій формі грамнегативну, плеоморфну бактерію, яка має форму паличок та є збудником захворювання верхніх дихальних шляхів і статевих шляхів курчат, де бактерію вибирають із групи, що включає бактерії, депоновані під реєстраційними номерами АТСС No. PTA-3667, АТСС No. PTA-3668, АТСС No. PTA-3669 або бактерії, які мають ідентичні до зазначених бактерій характеристики та які належать до Pasteurella trehalosi або Mannheimia haemolytica, та є позитивними у відношенні бета-гемолізу, позитивними у відношенні оксидази, позитивними у відношенні каталази, негативними у відношенні уреази, позитивними у відношенні нітратів, негативними у відношенні індолу, MacConkey-позитивними, позитивними у відношенні глюкози, позитивними у відношенні сахарози, позитивними у відношенні маніту, негативними у відношенні арабінози, негативними у відношенні целобіози, позитивними у відношенні ксилози, негативними у відношенні саліцину, негативними у відношенні орнітину, негативними у відношенні ескуліну, негативними у відношенні альфа-фукозидази, позитивними в відношенні бета-галактозидази.
2. Вакцина за п. 1, де вакцина містить інактивовані бактерії двох різних штамів, вибраних з групи, що включає бактерії, депоновані під реєстраційним номером АТСС No. PTA-3667, під реєстраційним номером АТСС No. PTA-3668 та під реєстраційним номером АТСС No. PTA-3669.
3. Вакцина за п. 1 або п. 2, де вакцина містить принаймні один інший антиген з вірусу або мікроорганізму, патогенного для курчат.
Текст
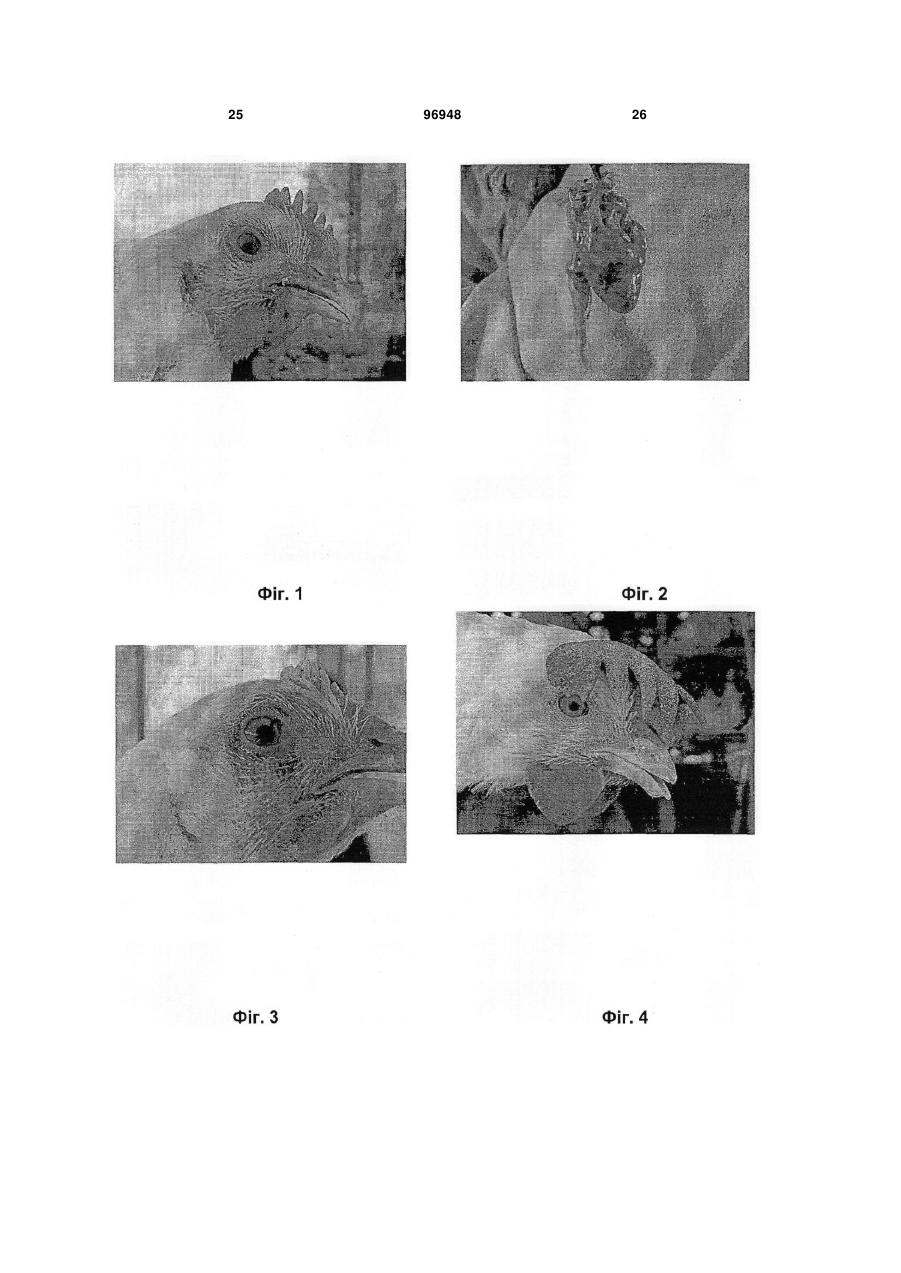
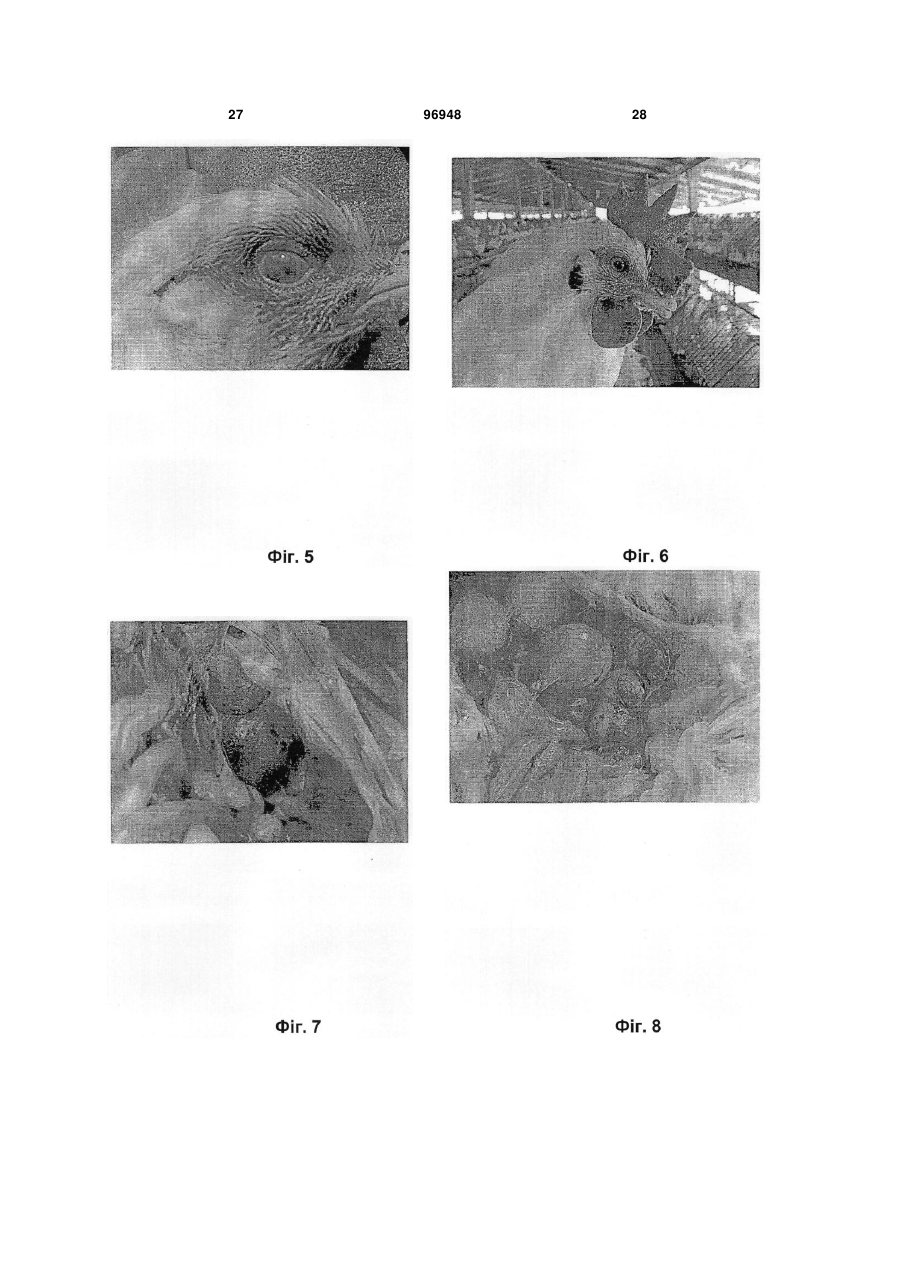
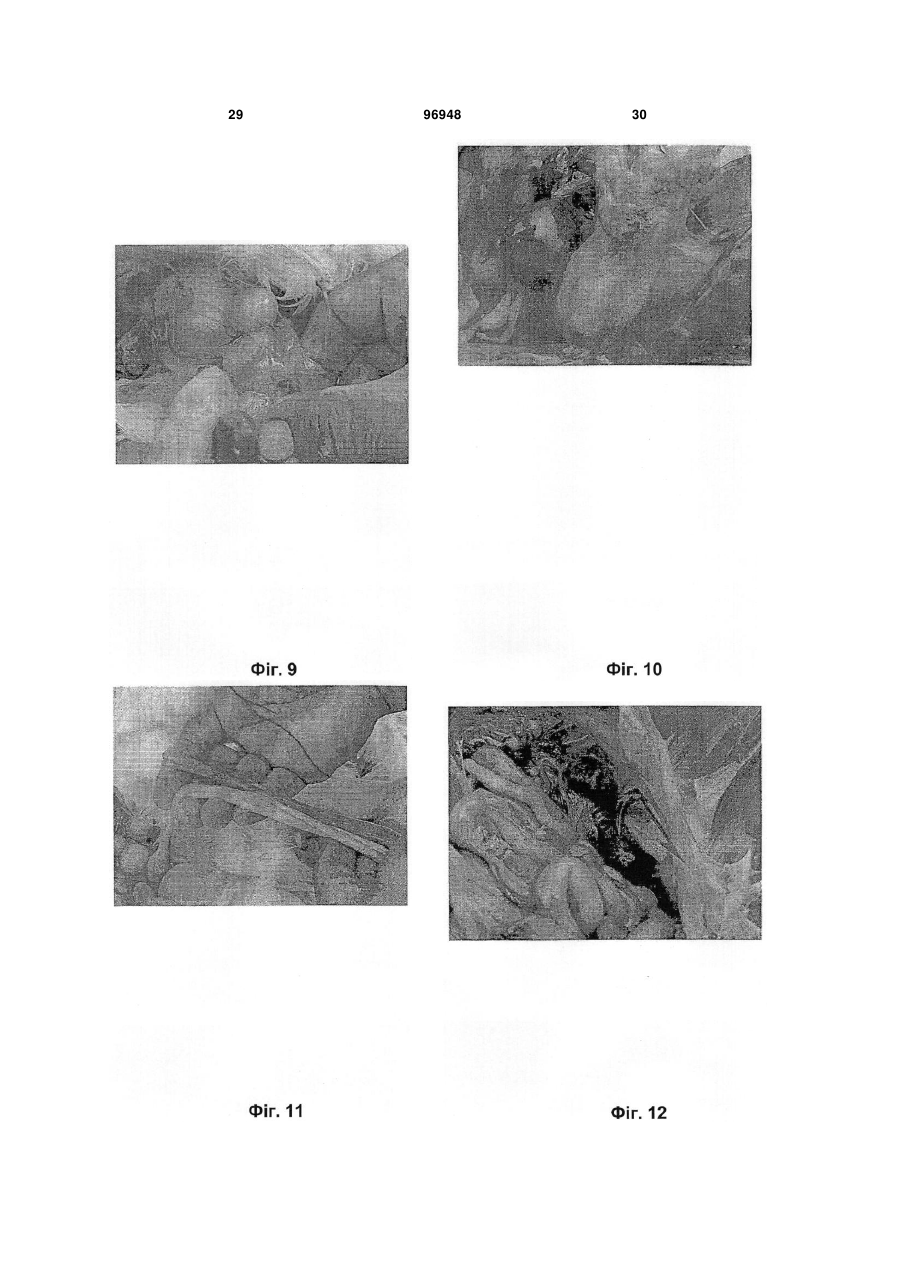
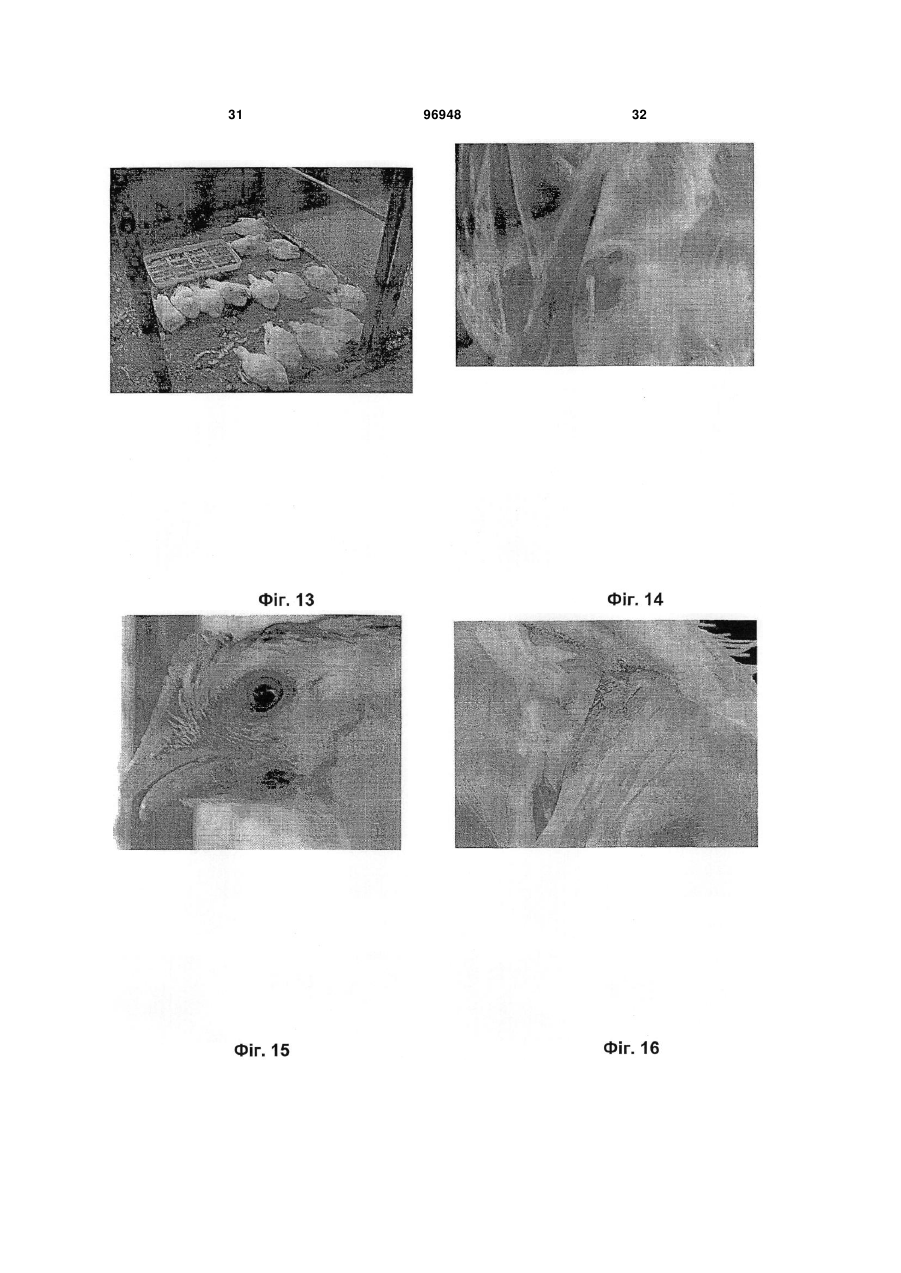
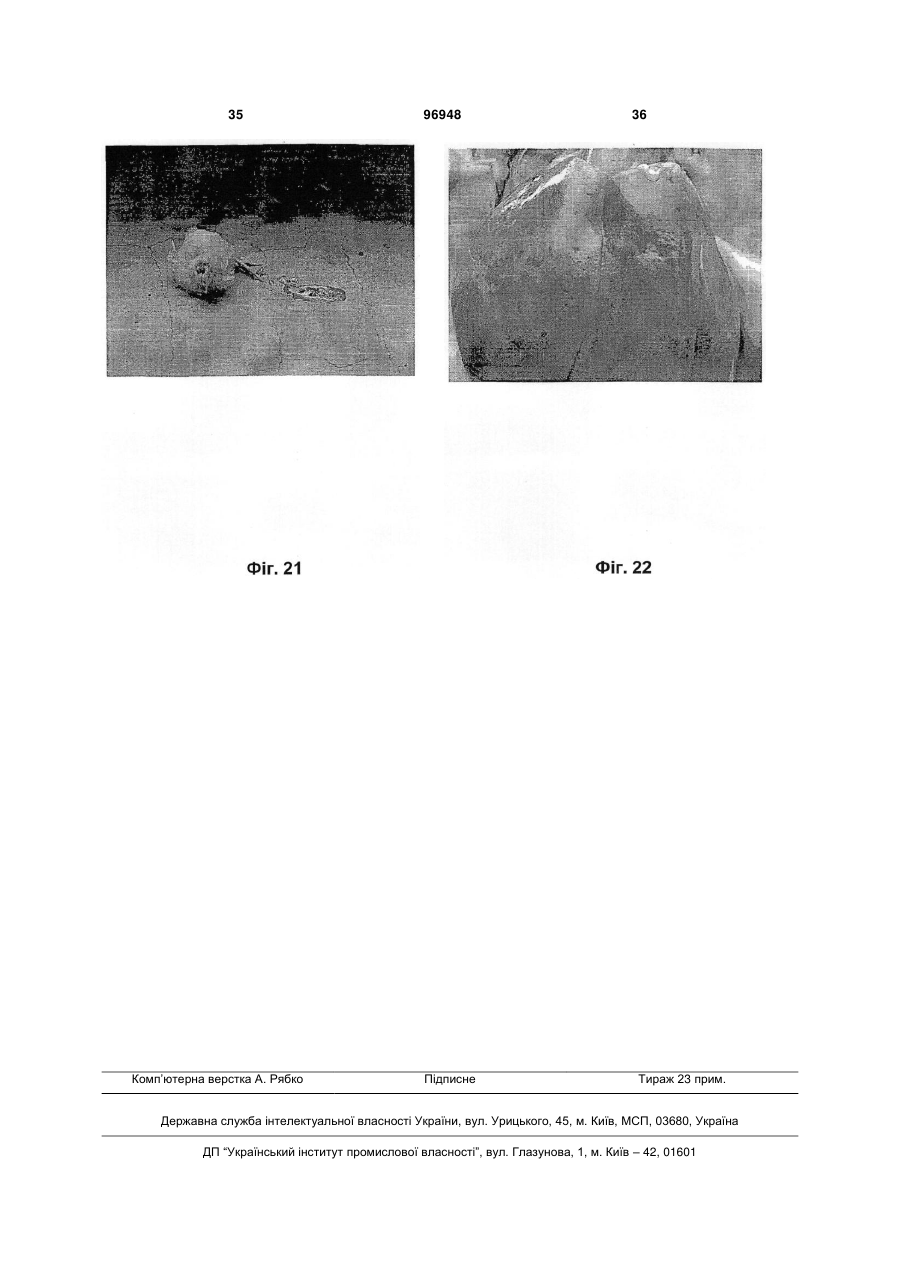
1. Вакцина, що містить в інактивованій формі грамнегативну, плеоморфну бактерію, яка має форму паличок та є збудником захворювання верхніх дихальних шляхів і статевих шляхів курчат, де бактерію вибирають із групи, що включає бактерії, депоновані під реєстраційними номерами АТСС C2 2 (19) 1 3 птахів (септичної), і хвороби, які викликаються Е. соІі. Таким чином, в основу даного винаходу була покладена задача ідентифікувати нове бактеріальне захворювання свійських птахів, виявити збудника захворювання і розробити вакцину для того, щоб запобігати захворюванню. Опис креслень А) Спалахи захворювання в природних умовах Фіг.1) Бройлери: Виділення з носа і припухлі ділянки навколо ока. Фіг.2) Бройлери: Кровотеча в серці і коронарній жировій клітковині. Фіг.3) Бройлери: Кон'юнктивіти і запалення навколо очей. Фіг.4) Несучки: Виділення з носа і прояв ціанозу гребінця. Фіг.5) Несучки: Запалення і кровотеча навколо очей. Фіг.6) Несучки: Кровотеча в шкірній тканині за слуховим отвором. Фіг.7) Несучки: Запалення нирок. Фіг.8) Несучки: Кровотеча в яйцепроводі. Фіг.9) Несучки: Деформовані яєчникові фолікули. Фіг.10) Несучки: Кровотеча в ділянці стику залозистого шлунка і м'язового шлунка. Фіг.11) Несучки: Застій і кровотеча в яйцепроводі. Б) Експериментальне зараження Фіг.12) Несучки: Запалення і кровотеча в нирці. Фіг.13) SPF (що не містять специфічний патоген): Прострація. Фіг.14) Несучки: Кровотеча в суглобі і м'язі. Фіг.15) Несучки: Виділення з носа і блідий гребінець. Фіг.16) Несучки: Кровотеча в м'язі. Фіг.17) SPF: Кровотеча в серце й у коронарній жировій клітковині. Фіг.18) Несучки: Здоровий птах ліворуч і хворий птах праворуч із складеними крилами. Фіг.19) Несучки: Діарея зеленуватого кольору. Фіг.20) SPF: Кровотеча в м'язі. Фіг.21) SPF: Прострація (порушення рухової функції) і діарея зеленуватого кольору. Фіг.22) Несучки: Збільшена печінка з наявністю кровотечі. Визначення понять, які застосовуються в описі: Перед описом варіантів здійснення даного винаходу слід зазначити, що в контексті даного опису й у наведеній нижче формулі винаходу, якщо спеціально не вказано інше, то поняття, наведене в однині, також включає множину. Так, наприклад, поняття "Pasteurella trehalosi" включає всю множину бактерій Pasteurella trehalosi, поняття "клітина" включає одну або багато клітин і їх еквіваленти, відомі фахівцям у даній галузі, і т.д. Незалежно від того, чи починається слово з великої літери чи ні, наприклад, "Арабіноза" і "арабіноза", воно має однакове значення, якщо спеціально не вказано інше. Якщо не вказано інше, усі технічні і наукові поняття мають загальноприйняті значення, відомі фахівцям в галузі, до якої належить винахід. Хоча 96948 4 для практичного втілення або тестування даного винаходу можна застосовувати будь-які методи і матеріали, аналогічні або еквівалентні до наведених у даному описі, нижче представлені переважні методи, пристрої і матеріали. Усі згадані в даному описі публікації включені в нього як посилання для характеризації й опису клітинних ліній, векторів і методологій, які описані в публікаціях і які можна застосовувати в контексті винаходу. Нічого з вищевикладеного не повинно тлумачитися в тому розумінні, що винахід не має права претендувати на більш ранній пріоритет. При створенні винаходу несподівано було відкрите нове бактеріальне захворювання свійських птахів, яке зустрічається насамперед у несучок і рідше бройлерів. Захворювання виявлене в курчат, які були вакциновані проти бактерій Haemophilus paragallinarum (збудник катару верхніх дихальних шляхів птахів) і Pasteurella multocida (збудник холери птахів). Симптоми цього нового захворювання відрізняються від специфічних симптомів катару верхніх дихальних шляхів. З урахуванням того факту, що для знову відкритого захворювання, як це буде описано нижче, характерні клінічні симптоми інфекції верхніх дихальних шляхів, то його збудником не може бути Η. paragallinarum. Першим об'єктом даного винаходу є грамнегативні, факультативно анаеробні, плеоморфі бактерії, які мають форму паличок, які є збудниками нового захворювання верхніх дихальних шляхів і статевих шляхів свійських птахів, де бактерії вибирають із групи, яка включає Pasteurella trehalosi і/або Mannheimia haemolytica. Бактерії, описані у винаході, можна виділяти з заражених трахей, піднебінної щілини, яєчника, печінки, серця, нирок і гонад (бройлери). Відповідно до винаходу їх можна ідентифікувати як Pasteurella trehalosi і/або Mannheimia haemolytica на основі вказаних нижче тестів: Бета-гемоліз + Фарбування штаму за Грамом Оксидаза + Каталаза + Уреаза Нітрати + Індол Бактеріальні ізоляти можна очищати і здійснювати їх біотипування відповідно до методу, описаному в Jaworski і ін. (1). Цей метод також описаний у прикладах. Важливим методом класифікації бактерій є гібридизація ДНК-ДНК, REA (аналіз за допомогою рестриктаз, див., наприклад, у J. Clinical Microbiol, 31, 1993, стор. 831-835) і риботипування. Фахівець у даній галузі може застосовувати ці методи для того, щоб встановити, чи підпадають бактерії під обсяг даного винаходу. Метод контрольного зараження для підтвердження постулату Коха також наведений у прикладах. Таким чином, важливим варіантом здійснення даного винаходу є бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, де ці види Pasteurella і/або Mannheimia є позитивними у відношенні бета()-гемолізу, грамнегативними, пози 5 тивними у відношенні оксидази, позитивними у відношенні каталази, негативними у відношенні уреази, позитивними у відношенні нітратів і негативними у відношенні індолу. Переважно бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані в даному винаході, є також MacConkeyпозитивними. Ще більш переважні відповідно до винаходу бактерії Pasteurella trehalosi і/або Mannheimia haemolytica додатково є позитивними у відношенні глюкози, позитивними у відношенні сахарози, позитивними у відношенні маніту, негативними у відношенні арабінози, негативними у відношенні целобіози, позитивними у відношенні ксилози, негативними у відношенні саліцину, негативними у відношенні орнітину, негативними у відношенні ескуліну, негативними у відношенні альфа-фукозидази, позитивними у відношенні бетагалактозидази. Найбільше переважними відповідно до винаходу є бактерії Pasteurella trehalosi, коли Pasteurella є також негативними у відношенні арабінози і позитивними у відношенні трегалози. Переважно також відповідно до винаходу, щоб Pasteurella trehalosi були також залежно від біотипу негативними або позитивними у відношенні бета()-глюкозидази. Також найбільш переважними відповідно до винаходу є бактерії Mannheimia haemolytica, де Mannheimia крім того є негативними у відношенні арабінози і негативними у відношенні трегалози. Переважно також відповідно до винаходу, щоб Mannheimia haemolytica були також негативними у відношенні бета-глюкозидази. Ці характерні властивості описаних у винаході бактерій дозволяють розглядати ці бактерії як нові в порівнянні з відомими бактеріальними патогенами свійських птахів (Diseases of Poultry, 10-е вид., під ред. B.W. Calnek, вид-во Iowa State University Press, Iowa, U.S.A. 1997). Іншим переважним варіантом здійснення даного винаходу є описані у винаході бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, де свійських птахів вибирають із групи, яка включає курчат, індичок, качок, гусок, лісових голубів, свійських голубів і перепелів. Винахід стосується також нового типу грамнегативних, факультативно анаеробних, плеоморфних бактерій, які мають форму паличок, для цього нового типу бактерій характерні бактерії, депоновані в американській колекції типових культур (АТСС), 1081, University Boulevard, Манассас, шт. Віргінія, 20110-2209, USA, під наступними реєстраційними номерами: Pasteurella trehalosi АТСС No. PTA-3667 (позначення для внутрішнього використання BIV4985); Pasteurella trehalosi АТСС No. PTA-3668 (позначення для внутрішнього використання BIVAVICOR); Mannheimia haemolytica АТСС No. PTA-3669 (позначення для внутрішнього використання BIV07990). Дата депонування 22 серпня 2001 р. Таким чином, найбільш переважним варіантом здійснення даного винаходу є бактерії Pasteurella trehalosi, депоновані під реєстраційним номером АТСС No. PTA-3667. Ці бактерії додатково описані в таблиці 3 прикладу 1. 96948 6 Іншим найбільш переважним варіантом здійснення даного винаходу є бактерії Pasteurella trehalosi, депоновані під реєстраційним номером АТСС No. РТА-3668. Ці бактерії додатково описані в таблиці 2 прикладу 1. Ще одним найбільш переважним варіантом здійснення даного винаходу є бактерії Mannheimia haemolytica, депоновані під реєстраційним номером АТСС No. PTA-3669. Ці бактерії додатково описані в таблиці 1 прикладу 1. Результати тестів, наведених у розділах А і Б у прикладах (таблиці 1, 2 і 3) підтверджують, що бактерії BIV-4895; АТСС No. PTA-3667 і BIVAVICOR; АТСС No. РТА-3668 належать до родини Pasteurellaceae (Pasteurella trehalosi, які є позитивними у відношенні трегалози і негативними у відношенні арабінози), у той час як бактерії BIV07990; АТСС No. PTA-3669 належать до родини Mannheimia (Mannheimia haemolytica, які є негативними у відношенні трегалози і негативними у відношенні арабінози). Винахід стосується також мікробіологічної культури, яка містить бактерії за винаходом, як вони описані вище. Культуру можна одержувати, вирощуючи ці бактерії при температурі 35-37 °C. Бактерії можна вирощувати при нормальному атмосферному тиску кисню. Бактерії можна вирощувати в багатьох різних середовищах, залежно від загальної задачі, які підсилюють ріст бактерій і які відомі фахівцю в даній галузі, таких як триптозний бульйон (ТВ), триптиказеїн-соєвий бульйон або бульйон із серцево-мозковим екстрактом або будь-які збагачені середовища. Бактерії можна вирощувати також на агарі з овечою кров'ю, інкубованому при 37 °C протягом 24 год. У даній галузі відомі різні фізичні і хімічні методи інактивації бактерій. Фізичну інактивацію можна здійснювати, наприклад, за допомогою УФвипромінювання, рентгенівського випромінювання, гамма-випромінювання і нагрівання. Прикладами інактивуючих хімічних сполук є бета-пропіолактон, глутаровий альдегід, бета-етиленімін і формальдегід. Переважно бактерії, описані у винаході, інактивують формальдегідом. При створенні винаходу несподівано було встановлено, що застосування формальдегіду в кінцевій концентрації 0,2 % є дуже хорошим методом інактивації бактерій, описаних у винаході. Таким чином, ще одним важливим об'єктом винаходу є спосіб інактивації бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, який полягає в застосуванні формальдегіду в кінцевій концентрації 0,2 %. Під обсяг даного винаходу підпадають бактерії, описані у винаході, інактивовані вказаними вище методами й іншими методами інактивації бактерій, які відомі фахівцю в даній галузі. Таким чином, ще одним важливим об'єктом винаходу є інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, які можна одержувати за допомогою способу, запропонованого у винаході, або методу, відомого в даній галузі. Переважно інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, виби 7 рають із групи, яка включає Pasteurella trehalosi ATCC No. PTA-3667, Pasteurella trehalosi ATCC No. PTA-3668 і/або Mannheimia haemolytica ATCC No. PTA-3669. Таким чином, ще одним важливим об'єктом винаходу є живі ослаблені бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, які можна одержувати за допомогою методу, відомого в даній галузі. Переважно ці живі ослаблені бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, вибирають із групи, яка включає Pasteurella trehalosi ATCC No. PTA-3667, Pasteurella trehalosi ATCC No. PTA-3668 і/або Mannheimia haemolytica ATCC No. PTA-3669. Бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, ослабляють шляхом багатьох пасажів у відповідних культуральних середовищах або за допомогою будь-якого іншого методу, відомого в даній галузі. У контексті даного опису під поняттям "інактивований" мається на увазі, що бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, гинуть і не можуть реплікуватися, викликаючи клінічне захворювання. У контексті даного опису під поняттям "ослаблений" мається на увазі, що бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, являють собою живі бактерії, які можуть реплікуватися, але не викликають при цьому клінічного захворювання. Ще одним важливим об'єктом винаходу є фракції або фрагменти бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, які можна одержувати за допомогою методу, відомого в даній галузі. Фрагменти можна одержувати солюбілізацією бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, з використанням детергенту або за допомогою будь-якого іншого методу, відомого в даній галузі. Переважно фракції або фрагменти являють собою очищені антигени бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході. Переважно фракції/фрагменти являють собою протеши зовнішньої мембрани бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході. Поняття "фрагмент" у контексті даного опису означає будь-яку імуногенну субодиницю бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, тобто будь-який піднабір поліпептидів. Таким чином, винахід стосується фрагментів, які містять принаймні один антиген бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході. Найбільш переважно фрагменти містять принаймні один антиген бактерії, вибраної з групи, яка включає Pasteurella trehalosi ATCC No. PTA-3667, Pasteurella trehalosi ATCC No. PTA-3668 і/або Mannheimia haemolytica ATCC No. PTA-3669. Фрагмент може являти собою всю бактеріальну клітину вказаного(их) штаму(ів), бактеріальні екстракти, фракції зовнішніх мембран, бактеріальні екзо- і/або ендотоксини й очищені протеши. Антигенні поліпептиди або їх фрагменти можна одержувати, наприклад, з очищених бакте 96948 8 ріальних протеїнів або шляхом експресії відповідного генетичного продукту в деяких прокаріотичних або еукаріотичних системах експресії або шляхом хімічного органічного синтезу. Вказані методи добре відомі фахівцю в даній галузі. Винахід стосується також живих і/або живих ослаблених і/або інактивованих бактерій Pasteurella trehalosi і/або Mannheimia haemolytica описаних у винаході, і/або фракцій Pasteurella trehalosi і/або Mannheimia haemolytica, призначених для застосування у вигляді вакцин. Винахід стосується також вакцини, отриманої з описаних вище вперше ідентифікованих бактерій. Таким чином, винахід стосується також композиції вакцини, яка містить живі і/або живі ослаблені і/або інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і/або фракції Pasteurella trehalosi і/або Mannheimia haemolytica. У контексті даного опису під поняттям "вакцина" розуміють вакцину для застосування у ветеринарії, яка містить антигенні субстанції і яку вводять з метою індукції специфічного й активного або пасивного імунітету проти захворювання, яка викликається бактеріями Pasteurella trehalosi і/або Mannheimia haemolytica. Живі або живі ослаблені бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, обумовлюють активний імунітет, який може пасивно переноситися через антитіла матері і виявляти дію у відношенні імуногенів, які вони містять, і іноді у відношенні організмів, споріднених до антигену. Інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і/або фракції Pasteurella trehalosi і/або Mannheimia haemolytica обумовлюють пасивний імунітет. Додаткові компоненти, призначені для посилення імунної відповіді, являють собою інгредієнти, які звичайно називають ад'ювантами, наприклад, типу гідроксиду алюмінію, мінеральних або інших масел або допоміжних молекул, які додаються в вакцину або які утворилися в організмі після відповідної індукції такими додатковими компонентами, які включають (але не обмежуючись ними) інтерферони, інтерлейкіни або фактори росту. Відповідно до переважного варіанта здійснення винаходу вакцина містить інактивовані бактерії. Переважно вакцина, запропонована у винаході, стосується вказаних вище вакцин, у яких один імунологічно активний компонент являє собою живі бактерії Pasteurella trehalosi і/або Mannheimia haemolytica. Поняття "жива вакцина" стосується вакцини, яка містить частинку, яка має здатність до поділу/розмноженню. Переважно також вакцина, запропонована у винаході, містить ослаблені бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і фармацевтично прийнятний носій або ексципієнт. Цю вакцину можна вводити як об'єднану вакцину, яка містить два або більшу кількість штамів живих і/або живих ослаблених і/або інактивованих бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, і/або фракцій двох або більшої кількості штамів 9 Pasteurella trehalosi і/або Mannheimia haemolytica. Найбільш переважно живі і/або живі ослаблені і/або інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і/або фракції Pasteurella trehalosi і/або Mannheimia haemolytica у вакцині вибирають із групи, яка включає Pasteurella trehalosi ATCC No. PTA-3667. Pasteurella trehalosi ATCC No. PTA-3668 і/або Mannheimia haemolytica ATCC No. PTA-3669. Переважно вакцина, запропонована у винаході, містить також інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і фармацевтично прийнятний носій або ексципієнт. Вакцину можна вводити також у вигляді об'єднаної вакцини, які містить два або більшу кількість штамів інактивованих бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Крім того, як прийнятний імуноген у вакцині, запропонованій у винаході, можна застосовувати також фракції цілих клітин. При цьому переважно вакцина, запропонована у винаході, містить фракції бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, і фармацевтично прийнятний носій або ексципієнт. Таку вакцину можна вводити також у вигляді об'єднаної вакцини, яка містить два або більшу кількість штамів інактивованих бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Зокрема, винахід стосується вакцин, що містять фрагменти, які несуть принаймні один антиген бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході. Найбільш переважно винахід стосується вакцин, що містять фрагменти, які несуть принаймні один антиген бактерій, вибраних із групи, яка включає Pasteurella trehalosi ATCC No. PTA-3667, Pasteurella trehalosi ATCC No. PTA-3668 і/або Mannheimia haemolytica ATCC No. PTA-3669. Вказаний фрагмент може містити цілі бактеріальні клітини, бактеріальні екстракти, фракції зовнішніх мембран, бактеріальні екзо- і/або ендотоксини й очищені протеїни. Антигенні поліпептиди або їх фрагменти можна одержувати, наприклад, з очищених бактеріальних протеїнів або шляхом експресії відповідного генетичного продукту в деяких прокаріотичних або еукаріотичних системах експресії або шляхом хімічного органічного синтезу. Вказані методи відомі фахівцю в даній галузі. Переважно вакцина, запропонована у винаході, містить також ад'ювант. Таким чином, винахід стосується також композиції вакцини, запропонованої у винаході, яка додатково містить один або декілька прийнятних ад'ювантів і/або ексципієнтів і/або носіїв. Ад'юванти, які застосовують відповідно до винаходу, включають субстанції, які викликають бустер-імунізацію тварини, що піддається ін'єкції. У даній галузі відомий цілий ряд різних ад'ювантів. Ад'юванти, які застосовують згідно із даним винаходом, включають повний і неповний ад'ювант Фрейнда, вітамін Ε, неіонні блокспівполімери, мурамілдипептиди, Quil А, мінеральне і не мінеральна масло, рослинну олію і карбопол (гомополімер). Відповідно до переважного варіанта здійснення винаходу вакцина, тобто бактерії, містить ад'ювант у вигляді емульсії типу вода/масло. Така вакцина, 96948 10 яка називається також бактерином, містить інактивовані (вбиті) бактерії, описані у винаході, і ад'ювант у вигляді емульсії типу вода/масло. Під обсяг даного винаходу підпадають також інші шляхи посилення властивостей бактерій за допомогою ад'ювантів, відомі фахівцям у даній галузі. Переважно вакцина, запропонована у винаході, може містити також один або декілька прийнятних емульгаторів, наприклад спан (Span) або твін (Tween). Переважно також живі і/або живі ослаблені і/або інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і/або фракції вказаних бактерій Pasteurella trehalosi і/або Mannheimia haemolytica у вакцині вибирають із групи, яка включає Pasteurella trehalosi ATCC No. PTA-3667, Pasteurella trehalosi ATCC No. PTA-3668 і/або Mannheimia haemolytica ATCC No. PTA-3669. Переважно вакцина, запропонована в даному винаході, містить принаймні один антиген бактерій, вибраних із групи, яка включає Pasteurella trehalosi ATCC No. РТА-3667, Pasteurella trehalosi ATCC No. РТА- 3668 і/або Mannheimia haemolytica ATCC No. РТА-3669. Вакцина може містити цілі бактеріальні клітини вказаного(их) штаму(ів), бактеріальні екстракти, фракції зовнішньої мембрани, бактеріальні екзо- і/або ендотоксини й очищені протеїни. Антигенні поліпептиди або їх фрагменти, можна одержувати, наприклад, з очищених бактеріальних протеїнів або шляхом експресії відповідного генетичного матеріалу в деяких прокаріотичних або еукаріотичних системах експресії або шляхом хімічного органічного синтезу. Такі методи відомі фахівцям у даній галузі. Найбільш переважно винахід стосується також композиції вакцини, запропонованої у винаході, яка додатково містить принаймні ще один антиген вірусу або мікроорганізму, патогенного для свійських птахів. Переважно цей антиген знаходиться у формі живих, ослаблених або інактивованих вірусів або мікроорганізмів або їх фрагментів. Фрагмент може містити цілі бактеріальні клітини або вірусні частинки, бактеріальні екстракти, вірусні антигени, вірусні субодиниці, фракції зовнішньої мембрани, бактеріальні екзо- і/або ендотоксини й очищені протеїни. Антигенні поліпептиди або їх фрагменти можна одержувати, наприклад, з очищених бактеріальних протеїнів або шляхом експресії відповідного генетичного матеріалу в деяких прокаріотичних або еукаріотичних системах експресії або шляхом хімічного органічного синтезу. Такі методи відомі фахівцям у даній галузі. Найбільш переважно винахід стосується також композиції вакцини, запропонованої у винаході, яка додатково містить принаймні ще один антиген вірусу або мікроорганізму, патогенного для свійських птахів, де вірус або мікроорганізм являє собою (але не обмежуючись ними) вірус інфекційного бронхіту, вірус ньюкасльської хвороби, вірус інфекційного бурситу птахів (захворювання: Гумборо (Gumboro)), вірус анемії курчат, пташиний реовірус, Mycoplasma gallisepticum, вірус пташиної пневмонії, Haemophilus paragallinarum (захворювання: Коріза (Coryza)), вірус віспи птахів, вірус пташиного енцефаломієліту, Pasteurella multocida і Ε. coli. 11 "Фармацевтична композиція" насамперед містить один або декілька інгредієнтів, які можуть модифікувати фізіологічні, наприклад, імунологічні функції організму, у який її вводять, або організмів, які живуть у цьому організмі або на ньому. Поняття включає (але не обмежуючись ними) антибіотики або антипаразитичні агенти, а також інші складові, які звичайно застосовують для досягнення певної мети, такі як (але не обмежуючись ними) характеристики процесінгу, стерильність, стабільність, придатність для введення композиції за допомогою ентерального або парентерального шляхів, наприклад, пероральним, внутрішньоназальним, внутрішньовенним, внутрішньом'язовим, підшкірним, внутрішньошкірним або іншим прийнятним шляхом, толерантність після введення, здатність до контрольованого вивільнення. Таким чином, іншим важливим об'єктом винаходу є фармацевтична композиція, яка містить живі і/або живі ослаблені і/або інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica, описані у винаході, і/або фракції бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Винахід стосується також способу лікування тварин, які належать до свійських птахів, інфікованих Pasteurella trehalosi і/або Mannheimia haemolytica. (наприклад, інфікованих живими вказаними вище бактеріями), який полягає в тому, що живі, ослаблені, інактивовані бактерії Pasteurella trehalosi і/або Mannheimia haemolytica і/або їх фракції і/або фрагменти за винаходом, як вони описані вище, вводять тварині, яка цього потребує, що належить до свійських птахів, у придатних дозах, які відомі фахівцям у даній галузі, і оцінюють зменшення симптомів, що викликані зараженням Pasteurella trehalosi і/або Mannheimia haemolytica. Таке лікування переважно можна повторювати. Ще одним важливим варіантом здійснення винаходу є спосіб імунізації свійських птахів проти захворювання дихальних і статевих шляхів, яке викликається бактеріями Pasteurella trehalosi і/або Mannheimia haemolytica (наприклад, описаними вище живими бактеріями), який полягає у введенні імунологічно ефективної кількості вакцини, запропонованої у винаході, і оцінці зменшення симптомів, які викликані зараженням бактеріями Pasteurella trehalosi і/або Mannheimia haemolytica. Наступним важливим варіантом здійснення винаходу є застосування інактивованих бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, і/або живих бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, і/або живих ослаблених бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, і/або фрагментів або фракцій бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході, для приготування вакцини для профілактики інфекцій, які викликаються бактеріями Pasteurella trehalosi і/або Mannheimia haemolytica. Винахід стосується також способу діагностики захворювання, який включає стадії одержання зразка з організму свійських птахів, де зразок вибирають із групи, яка включає кров, сироватку, плазму, тканинні зскрібки, змиви, мазки, тканину, і 96948 12 аналізи зразка на присутність бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, описаних у винаході. Відповідно до переважного варіанта здійснення наявність бактерій Pasteurella trehalosi і/або Mannheimia haemolytica визначають за допомогою імунологічного тесту. Для проведення імунологічного тесту застосовують моноклональні антитіла або поліклональну антисироватку, специфічну до бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Одержання моноклональних антитіл відомо в даній галузі (3, 4). Імунологічні тести включають методи оцінки, відомі в даній галузі, такі як тест ELISA (твердофазний імуноферментний аналіз) або так званий аналіз сендвіч-ELISA, дот-блот аналіз, імуно-блот аналіз, радіоімунологічні тести (радіоімунологічний аналіз, РІА), заснований на дифузії тест Оухтерлоні або "ракетні" імунофлуоресцентні аналізи або реакції аглютинації (експрес-реакції аглютинації на планшеті або мікропланшеті). Інший імунологічний аналіз являє собою так званий Вестерн-блот-аналіз (який називається також перенесенням за Вестерном або Вестерн-блотинг). Аналіз методом Вестернблотингу передбачає перенесення протеїнів або поліпептидів, розділених за допомогою електрофорезу в поліакриламідному гелі, на нітроцелюлозний фільтр або інший прийнятний носій з одночасним збереженням відносних положень протеїнів або поліпептидів, отриманих з гелів для електрофорезу. Потім Вестерн-блот інкубують з антитілом, яке специфічно зв'язується з розглянутим протеїном або поліпептидом. Ці методи виявлення може використовувати звичайний фахівець у даній галузі при здійсненні описаного винаходу. Літературні посилання, у яких фахівець може знайти опис вищевказаних методів, а також інші методи виявлення перераховані в: An Introduction to Radioimmunoassay and Related Techniques, вид-во Science Publishers, Amsterdam, The Netherlands (1986); Bullock і ін., Techniques in Immunocytochemistry, вид-во Academic Press, Orlando, FL том 1 (1982), том. 2 (1983), том. 3 (1985); Tijssen, вид-во Elsevier Science Publishers, Amsterdam, The Netherlands (1985). Відповідно до іншого найбільш переважного варіанту здійснення винаходу вказаний вище зразок інкубують з антитілами, специфічними для бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, і визначають наявність комплексу антиген/антитіло, який утворився при цьому. Згідно з особливо переважним варіантом способу, запропонованого у винаході, присутність бактерій Pasteurella trehalosi і/або Mannheimia haemolytica у вказаному вище зразку визначають за допомогою методів молекулярної біології. У контексті даного опису під методами молекулярної біології розуміють методи виявлення, які, наприклад, включають полімеразну ланцюгову реакцію (ПЛР), полімеразну ланцюгову реакцію із зворотною транскриптазою (ЗТ-ПЛР) або Нозерн- або Саузерн-блотинг, ці методифахівець у даній галузі може знайти в стандартних посібниках (наприклад, Sambrook і ін. (1989) Molecular Cloning: A Laboratory Manual, 2-е вид., вид-во Cold Spring 13 96948 Harbor Laboratory Press, Cold Spring Harbor, New York і Bertram, S. і Gassen, H.G. Gentechnische Methoden, вид-во G. Fischer Verlag, Stuttgart, New York, 1991). Винахід стосується також діагностичного тестнабору, запропонованому у винаході, який відрізняється тим, що містить усі необхідні елементи для виявлення бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Діагностичний тест-набір являє собою набір, який містить усі компоненти для здійснення способу діагностики, запропонованого у винаході. Як деякі приклади (але не обмежуючись ними) інших елементів, призначених для здійснення способу, запропонованого у винаході, можна вказати контейнери, такі як 96-лункові або титраційні мікропланшети, лабораторні пробірки, інші придатні контейнери, поверхні і субстрати, мембрани, такі як нітроцелюлозний фільтр, реагенти для відмивання і буфери. Діагностичний тест-набір може містити також реагенти, які можуть виявляти зв'язані антитіла, такі, наприклад, як мічені вторинні антитіла, хромофори, ферменти (наприклад, кон'юговані з антитілами) і їх субстрати або інші субстанції, які можуть зв'язуватися з антитілами. Винахід стосується також діагностичного тестнабору, запропонованому у винаході, який відрізняється тим, що він містить усі необхідні елементи для здійснення ПЛР або ЗТ-ПЛР із метою виявлення ДНК або РНК, специфічних для бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Такий набір може містити (але не обмежуючись ними) крім лабораторних пробірок або 96-лункових планшетів, або титраційних мікропланшетів, інших прийнятних контейнерів, поверхонь і субстратів, мембран, таких як нітроцелюлозні фільтри, буферів для відмивання і реакційних буферів (які мо 14 жуть відрізнятися за значеннями рН і концентраціями магнію), стерильну воду, мінеральне масло, БСА (бичачий сироватковий альбумін), MgCl2, (NH4)2SO4, ДМСО (диметилсульфоксид), меркаптоетанол, нуклеотиди (дНТФ), ферменти, такі як Taq-полімераза і зворотна транскриптаза, і як ДНК-матрицю ДНК або кДНК, специфічну для бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, олігонуклеотиди, специфічні для ДНК або РНК бактерій Pasteurella trehalosi і/або Mannheimia haemolytica, контрольну матрицю, DEPC-воду, ДНКазу, РНКазу й інші сполуки, відомі фахівцю в даній галузі. Олігонуклеотиди, запропоновані у винаході, являють собою короткі молекули нуклеїнових кислот, довжиною від приблизно 15 до приблизно 100 нуклеотидів, які зв'язуються в строгих умовах з нуклеотидною послідовністю, комплементарною до послідовності протеїну бактерій Pasteurella trehalosi і/або Mannheimia haemolytica. Під строгими умовами фахівець у даній галузі розуміє умови, які дозволяють відбирати послідовності, гомологічні більш ніж на 85 %, переважно більш ніж на 90 % (порівн. Sambrook і ін. (1989) Molecular Cloning: A Laboratory Manual, 2-е вид., вид-во Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York, і Bertram S. і Gassen H.G. Gentechnische Methoden, вид-во G. Fischer Verlag, Stuttgart, New York, 1991). Нижче винахід більш докладно проілюстрований на прикладах, які не обмежують його обсяг. Приклад I Спалахи в польових умовах захворювань, пов'язаних з бактеріями Pasteurella trehalosi і Mannheimia haemolytica Клінічні симптоми За результатами польових досліджень Несучки Бройлери Слабке ураження верхніх дихальних / статевих шля- Серйозне ураження верхніх дихальних / статевих хів шляхів Вік: 22 тижні Вік: 7 тижнів Виділення з носа Чхання з хрипом Опухлі ділянки навколо ока Опухла голова Знижене споживання корму Знижене споживання корму Білувата діарея Депресія Знижене виробництво яєць Не однорідний ріст Невисокий рівень смертності Складені крила Опущений!! гребінець Прострація Ціаноз гребінця Смертність 8 % Серйозні ураження Атрофія яєчників, яка супроводжується кровотечами і регресом Деформація яєчникових фолікул Збільшена печінка Запалення нирок Кровотечі в черевній жировій клітковині Кровотечі в грудній порожнині Кровотечі в яйцепроводі Кровотечі в коронарній жировій клітковині Кровотечі в гонадах Кровотечі у верхній ділянці трахей Збільшена печінка з ознаками кровотеч Аеросакуліт Збільшена селезінка з ознаками кровотеч Кровотечі в м'язовій тканині Кровотечі в серце і водянка перикарда Кровотечі в грудній порожнині 15 96948 Три штами грамнегативних, факультативно анаеробних, плеоморфних бактерій, які мають форму паличок, нового типу були депоновані в Американській колекції типових культур (АТСС), 1081, University Boulevard, Манассас, шт. Віргінія 20110-2209, США, під реєстраційними номерами: АТСС No. РТА-3667 для штаму Pasteurella trehalosi BIV-4985; АТСС No. РТА-3668 для штаму Pasteurella trehalosi BIV-AVICOR і АТСС No. PTA3669 для штаму Mannheimia haemolytica BIV07990. Дата депонування 22 серпня 2001 р. Депоновані бактерії типували за допомогою стандартних методів оцінки на основі посібника Bergey's Manual of Systematic Bacteriology, том І (1984, Williams і Wilkins, 428 East Preston Street Baltimore, USA.) Таблиця 1 Mannheimia haemolytica: BIV-07990 (біотип І); АТСС No. PTA-3669 Макроскопічна морфологія Колонії, вирощені на агарі з додаванням овечої крові протягом 24 год., діаметром 1,0-1,5 мм, яскраві напівпрозорі, слабовипуклі, гладкі і кремоподібні, -гемоліз. Мікроскопічна морфологія Грамнегативні, нерухомі, плеоморфні палички, які часто мають біполярне забарвлення. Біохімічні й інші тести Розділ А Тест Оксидаза Каталаза Індол Глюкоза Сахароза MacConkey Уреаза Нітрати Реакція + + + + + + Розділ Б Мальтоза Маніт Арабіноза Целобіоза Сорбіт Ксилоза Трегалоза Саліцин Орнітин Ескулін -глюкозидаза -фукозидаза -галактозидаза + + + + + Таблиця 2 Pasteurella trehalosi BIV-AVICOR (біотип 2); АТСС No. PTA-3668 Макроскопічна морфологія Колонії, вирощені на агарі з додаванням овечої крові протягом 24 год., діаметром 1,0-1,5 мм, 16 яскраві напівпрозорі, слабовипуклі, гладкі і кремоподібні, -гемоліз. Мікроскопічна морфологія Грамнегативні, нерухомі, плеоморфні палички, які часто мають біполярне забарвлення. Біохімічні й інші тести Розділ А Тест Оксидаза Каталаза Індол Глюкоза Сахароза MacConkey Уреаза Нітрати Реакція + + + + + + Розділ Б Мальтоза Маніт Арабіноза Целобіоза Сорбіт Ксилоза Трегалоза Саліцин Орнітин Ескулін -глюкозидаза -фукозидаза -галактозидаза + + + + + +* + * 80 % позитивні Таблиця 3 Pasteurella trehalosi: BIV-4895 (біотип 4); АТСС No. PTA-3667 Макроскопічна морфологія Колонії, вирощені на агарі з додаванням овечої крові протягом 24 год., діаметром 1,0-1,5 мм, яскраві напівпрозорі, слабовипуклі, які складаються з частинок і сухі, -гемоліз. Мікроскопічна морфологія Грамнегативні, нерухомі, плеоморфні палички, які часто мають біполярне забарвлення. Біохімічні й інші тести Розділ А Тест Оксидаза Каталаза Індол Глюкоза Сахароза MacConkev Уреаза Нітрати Розділ Б Реакція + + + + + + 17 Мальтоза Маніт Арабіноза Целобіоза Сорбіт Ксилоза Трегалоза Саліцин Орнітин Ескулін -глюкозидаза -фукозидаза -галактозидаза 96948 Нітрати + Індол Не виділено вірусів або яких-небудь інших бактерій. Біотипування: Бактеріальні ізоляти очищали і біотипували відповідно до методу, описаному в Jaworski і ін.(1). Було виявлено 3 різних біотипи (4, 2, 1). У цілому метод полягає в наступному: з очищених ізолятів індивідуальною колонією інокулювали пробірки, які містять по 3 мл триптозного бульйону, і інкубували при 37 °C протягом 8 год. Петлею брали інокулят (20 мкл) із пробірки і потім переносили в іншу пробірку, що підлягає тестуванню, яка містила 3 мл 1 %-ного цукру, і інкубували протягом 7 днів при 37 °C до оцінки результатів. Модель контрольного зараження: Після очищення бактерій ізоляти вирощували в триптозних середовищах, одержуючи великі кількості чистих патогенів. Для підтвердження постулату Коха три різні групи (по 20 птахів у кожній групі) курчат, які не містять специфічний патоген (SPF), віком 13 тижнів заражали внутрішньовенно 8 бактеріями кожного біотипу (0,2 мл /птаха; 3*10 КОО/мл). Птахів обстежували щодня протягом 3 днів у відношенні захворюваності і смертності. До кінця третього дня всіх птахів умертвляли, після розтину трупів оцінювали ушкодження і зразки органів (печінку і гонади) брали для повторного виділення. Також аналізували ушкодження після розтину трупів птахів, які загинули своєю смертю. Результати Клінічні симптоми: прострація, кульгавість, опущений гребінець, складені крила, ціаноз верхівки гребінця. Ураження: + + + + + Результати тестів, пред сталені в розділах А і Б (таблиці 1, 2 і 3), підтверджують, що бактерії штаму BIV-4895; АТСС No. PTA-3667 і штаму BIVAVICOR; АТСС No. РТА-3668 належать до родини Pasteurellaceae (Pasteurella trehalosi, вони є позитивними у відношенні трегалози і негативними у відношенні арабінози), у той час як бактерії штаму BIV-07990; АТСС No. РТА-3669 належать до родини Mannheimia (Mannheimia haemolytica, вони є негативними у відношенні трегалози і негативними у відношенні арабінози). Ідентифікація збудника Бактерії виділяли з заражений трахей, піднебінної щілини, яєчника, печінки, серця, нирки і гонад (бройлери). На основі вказаних нижче тестів вони ідентифіковані як Pasteurella trehalosi і Mannheimia haemolytica: Бета-гемоліз + Фарбування за Грамом Оксидаза + Каталаза + MacConkey + Уреаза Ураження BIV-4895 (біотип 4) Набряк серця Кровотечі в серце Кровотечі в коронарній жировій клітковині Перикардит Кровотечі в грудній порожнині Кровотечі в яєчнику Запалення нирок Кровотечі в нирках Збільшена печінка з ознаками кровотеч Аеросакуліт Кровотечі в м'язі Смертність 73 % 90 % 90 % 73 % --64 % 64 % 55 % --64 % --46 % Приклад II Вирощування бактерій, описаних у винаході, одержання вакцини і вакцинація SPF-птахів Штами вирощували на триптозному бульйоні (ТВ). Збір здійснювали на логарифмічній фазі росту приблизно через 6-8 год. після інокуляції залежно від штаму. Зчитування планшета здійснювали титруванням на агарі з овечою кров'ю. Визначали кількість колонієутворюючих одиниць на мілілітр 18 BIV-Avicor (біотип 2) BIV-07990 (біотип 1) 37 % --37 % 46 % 19 % 9% 46 % 46 % 73 % --37 % 19 % 90 % 70 % 50 % 30 % 40 % 20 % 60 % 20 % -------- (КОО/мл), використовуючи розведення збору 1:10. Клітини вбивали, додаючи формальдегід до кінцевої концентрації 0,2 %. Після оцінки стерильності цієї суспензії до кінцевої вакцини додавали міні8 мальний титр, що становить 10 КОО/мл. Вакцину одержували змішуванням двох штамів (BIV-4895, АТСС No. РТА-3667 і BIV-AVICOR, АТСС No. РТА-3668) і масляного ад'юванта (емульсія типу вода/масло на основі мінерального ма 19 96948 сла із співвідношенням 60 % масла/40 % води) до 7,0 мінімальної концентрації 10 КОО/штаму/мл. Курчат, які не містять специфічний патоген (SPF), вакцинували у віці 2, 5 і 9 тижнів шляхом ін'єкції 0,5 мл вакцини підшкірно в ділянку, розташовану на середині довжини шиї. Приклад ІІІ Одержання штамів для контрольного зараження і зараження вакцинованих і контрольних груп Бактеріальні штами BIV-4895, АТСС No. PTA3667 і BIV-AVICOR, АТСС No. РТА-3668 вирощували на агарі з овечою кров'ю протягом 24 год. при 37 °C. Клітини збирали в триптозному бульйоні (ТВ) до досягнення оптичної густини суспензії 2,0, використовуючи спектрофотометр із довжиною хвилі 540 нм. Для контрольного зараження готували препарати, які містять наступну кількість клітин Групи птахів Негативний контроль Позитивний контроль Вакцинований позитивний контроль Вакцинована Вакцинована 20 у кінцевому об'ємі проби для контрольного зараження: 9 3×10 КОО/мл BIV-AVICOR; АТСС No. PTA3668 10 1,45×10 КОО/мл BIV-4895; АТСС No. PTA3667 Заражали 20 вакцинованих і 20 невакцинованих птахів віком 13 тижнів шляхом внутрішньовен8,0 ного введення 0,2 мл інокуляту (принаймні 10 КОО/особину). Птахів обстежували протягом 3 днів у відношенні ознак захворювання й оцінювали їх смертність. Після триденного обстеження всіх птахів, які залишилися живими, умертвляли й у кожного птаха повторно виділяли бактерії з печінки і гонад. Також здійснювали посмертну оцінку загиблих птахів. Результати Немає АТСС No. PTA-3667 Дані, отримані для загиблих птахів і після повторного виділення органів птахів, що вижили 0 77 Не застосовно 23 АТСС No. PTA-3668 54 46 АТСС No. PTA-3667 АТСС No. PTA-3668 0 5 100 95 Інокулят для зараження Приклад IV Вирощування бактерій, описаних у винаході, одержання вакцини і вакцинація SPF-птахів Штами вирощували на триптозному бульйоні (ТВ). Збір здійснювали на логарифмічній фазі росту приблизно через 6-8 год. після інокуляції залежно від штаму. Зчитування планшета здійснювали титруванням на агарі з овечою кров'ю. Визначали кількість колонієутворюючих одиниць на мілілітр (КОО/мл), використовуючи розведення збору 1:10. Клітини вбивали, додаючи формальдегід до кінцевої концентрації 0,2 %. Після оцінки стерильності цієї суспензії до кінцевої вакцини додавали мінімальний титр, що стано8 вить 10 КОО/мл. Вакцину одержували змішуванням трьох штамів (BIV-4895, АТСС No. РТА-3667, BIVAVICOR, АТСС No. РТА-3668 і BIV-07990, АТСС No. РТА-3669) і масляного ад'юванта (емульсія типу вода/масло на основі мінерального масла із співвідношенням 60 % масла/40 % води) до міні7,0 мальної концентрації 10 КОО/штаму/мл. Курчат, які не містять специфічний патоген (SPF), вакцинували у віці 2, 5 і 9 тижнів шляхом ін'єкції 0,5 мл вакцини підшкірно в ділянку, розташовану на середині довжини шиї. Приклад V Одержання штамів для контрольного зараження і зараження вакцинованих і контрольних груп Захисна дія % Бактеріальні штами BIV-4895, АТСС No. РТА3667, BIV-AVICOR, АТСС No. РТА-3668 і BIV07990, АТСС No. PTA-3669 вирощували на агарі з овечою кров'ю протягом 24 год. при 37 °C. Клітини збирали в триптозному бульйоні (ТВ) до досягнення оптичної густини суспензії 2,0, використовуючи спектрофотометр із довжиною хвилі 540 нм. Для контрольного зараження готували препарати, які містять наступну кількість клітин у кінцевому об'ємі проби для контрольного зараження: 9 8,3×10 КОО/мл BIV-AVICOR; АТСС No. PTA3668 9 2,2×10 КОО/мл BIV-4895; АТСС No. РТА3667 10 1,0×10 КОО/мл BIV-07990, АТСС No. PTA3669 Заражали 20 вакцинованих і 20 невакцинованих птахів віком 13 тижнів шляхом внутрішньовенного введення 0,2 мл інокуляту (принаймні 8,0 10 КОО/особину). Птахів обстежували протягом 3 днів у відношенні ознак захворювання й оцінювали їх смертність. Після триденного обстеження всіх птахів, які залишилися живими, умертвляли й у кожного птаха повторно виділяли бактерії з печінки і гонад. Також здійснювали посмертну оцінку загиблих птахів. Результати 21 96948 Групи птахів Негативний вакцинований контроль Негативний не вакцинований контроль Вакцинована Вакцинована Вакцинована Позитивний контроль Позитивний контроль Позитивний контроль Дані, отримані для загиблих птахів і після Інокулят для зараження повторного виділення органів птахів, що вижили Немає 0 Немає 1 + 2 + 3 + 4 + 5 + 6 + 7 + 8 + 9 10 11 + + + - - - - 4 + 5 + 6 + 7 + 8 + 9 10 11 - - - - + + + 2 Розведення (log ) Антигенний біотип 4 Антисироватка 1 2 4 1 + 2 + 3 + Захисна дія (%) Не застосовно 0 Не застосовно 27,3 20,9 16,7 53,3 53,3 64,3 АТСС No. PTA-3669 АТСС No. PTA-3668 АТСС No. PTA-3667 АТСС No. PTA-3669 АТСС No. PTA-3668 АТСС No. PTA-3667 Серологічний тест Гіперімунну сироватку одержували в кроликах за допомогою репрезентативного для кожного біотипу ізоляту відповідно до методу Biberstein і ін. (2). Ізоляти вирощували протягом ночі на кров'яному агарі, потім збирали у фізіологічний розчин, який містить 0,3 % формаліну. Клітини однократно промивали і для ін'єкції доводили коефіцієнт пропускання до 10 % при довжині хвилі 575 нм. Введення здійснювали за допомогою внутрішньовенної ін'єкції (IV) відповідно до наступної схеми: 0,5, 1,0, 2,0, 3,0, 3,0, 3,0 мл з 4-денними інтервалами й у всіх кроликів брали зразки крові через 4 дні після останньої ін'єкції. Гіперімунну сироватку тестували у відношенні її специфічності з використанням штамів 3 біотипів і оцінювали реакцію з гомологічною і гетерологічною кролячою антисироваткою (2-кратні розведення) за допомогою методу швидкої аглютинації на планшетах. Антисироватку кожного біотипу розбавляли до того часу, поки не визначали кінцевий титр, який дає позитивну відповідь, встановлюючи тим самим найбільше можливе розведення. 2 Розведення (log ) Антигенний біотип 1 Антисироватка 1 2 4 22 72,7 79,1 83,7 46,7 46,7 35,7 2 Розведення (log ) Антигенний біотип 2 Антисироватка 1 2 4 1 + 2 + 3 + 4 + 5 + 6 + 7 + 8 + 9 10 11 - - + + + - - Специфічну для біотипу гіперімунну сироватку потім застосовували як позитивний контроль при здійсненні серологічної реакції аглютинації на мікропланшеті. Приклад VI Одержання штамів для контрольного зараження і зараження вакцинованих і контрольних груп Бактеріальні штами BIV-4895, АТСС No. РТА3667, BIV-AVICOR, АТСС No. РТА-3668 і BIV07990, АТСС No. PTA-3669 вирощували на агарі з овечою кров'ю протягом 24 год. при 37 °C. Клітини збирали в триптозному бульйоні (ТВ) до досягнення оптичної густини суспензії 2,0, використовуючи спектрофотометр із довжиною хвилі 540 нм. Для контрольного зараження готували препарати, які містять наступну кількість клітин у кінцевому об'ємі проби для контрольного зараження: 10 1,5×10 КОО/мл BIV-AVICOR; АТСС No. PTA-3668 10 1,7×10 КОО/мл BIV-4895; АТСС No. РТА3667 10 1,6×10 КОО/мл BIV-07990, АТСС No. PTA3669 Заражали 20 вакцинованих і 20 невакцинованих птахів віком 13 тижнів шляхом внутрішньовенного введення 0,2 мл інокуляту (принаймні 8,0 10 КОО/особину). Птахів обстежували протягом 3 днів у відношенні ознак захворювання й оцінювали їх смертність. Після триденного обстеження всіх птахів, які залишилися живими, умертвляли й у кожного птаха повторно виділяли бактерії з печінки, серця і гонад. Результати 23 96948 24 Таблиця 1 Оцінка активності вакцини на основі даних про смертність і даних, отриманих після повторного виділення органів птахів, що вижили Групи птахів Негативний не вакцинований контроль Позитивний контроль Позитивний контроль Позитивний контроль Вакцинована Вакцинована Вакцинована Інокулят для зараження Дані, отримані для загиблих птахів і після повторного виділення органів птахів, що вижили Захисна дія % Немає Не застосовно 70 80 88,8 10 10 15 30 20 11,2 90 90 85 Немає BIV-4895 BIV-AVICOR BIV-07990 BIV-4895 BIV-AVICOR BIV-07990 Таблиця 2 Оцінка активності вакцини на основі даних про виражені ушкодження після контрольного зараження Групи птахів Негативний невакцинований контроль Позитивний контроль Позитивний контроль Позитивний контроль Вакцинована Вакцинована Вакцинована Інокулят для зараження Немає BIV-4895 BIV-AVICOR BIV-07990 BIV-4895 BIV-AVICOR BIV-07990 Посилання 1) Jaworski M.D., D.L. Hunter, А.С.S. Ward. Biovariants of isolates of Pasteurella from domestic і wild ruminants. J. Vet. Invest. 10, 1988, стор. 49-55. 2) Biberstein E.L., Meyer M.E. and Kenedy P.C. Colonial variation of Pasteurella haemolytica isolated from sheep. J. Bact. 76, 1958, стор. 445452. Ушкодження, % Захисна дія, % Немає Не застосовно 74,4 27,0 7,0 4,0 1,1 2,4 25,6 73,0 93,0 96,0 99,0 98,0 3) Kearney J.F., Radbruch Α., Liesegang В., Rajewski K. A new mouse myeloma cell line that has lost imunoglobulin expression but permits construction of antibody-secreting hybrid cell lines. J. Immunol. 123, 1979, стор. 1548-1550. 4) Kohler G., Milstein С. Continous culture of fused cells secreting antibody of predefined specifity. Nature 265, 1975, cтop. 495-497. 25 96948 26 27 96948 28 29 96948 30 31 96948 32 33 96948 34 35 Комп’ютерна верстка А. Рябко 96948 Підписне 36 Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюVaccine composition comprising bacteria causing a disease of the upper respiratory and of the reproductive tract of chicken
Автори англійськоюVazquez Maria Elena, Campogarrido Raul, Gonzales-Hernandez Carlos, Sivanandan Vaithianathan
Назва патенту російськоюВакцина, которая содержит бактерии, которые являются возбудителем верхних дыхательных путей и половых путей цыплят
Автори російськоюВазкез Мария Елена, Кампогарридо Рауль, Гонзалес-Эрнандес Карлос, Сиванандан Вайсинасан
МПК / Мітки
МПК: A61K 39/102
Мітки: курчат, верхніх, містить, дихальних, вакцина, яка, статевих, шляхів, збудником, бактерії
Код посилання
<a href="https://ua.patents.su/18-96948-vakcina-yaka-mistit-bakteri-yaki-eh-zbudnikom-verkhnikh-dikhalnikh-shlyakhiv-i-statevikh-shlyakhiv-kurchat.html" target="_blank" rel="follow" title="База патентів України">Вакцина, яка містить бактерії, які є збудником верхніх дихальних шляхів і статевих шляхів курчат</a>
Попередній патент: Похідні цинамоїл-піперазину та їх застосування як антагоністів par-1
Наступний патент: Петля для кришки і спосіб виготовлення такої петлі
Випадковий патент: Горизонтальний барабанний вузол з автобалансирами для відцентрових машин