Застосування фрагмента аb16-23 для лікування хвороби альцгеймера
Номер патенту: 87453
Опубліковано: 27.07.2009
Автори: Бард Фредерік, Васквез Нікі, Єднок Тед, Сьюберт Пітер А.
Формула / Реферат
1. Застосування
і) фрагмента Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, або
іі) фрагмента Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, де фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, де молекула-носій допомагає викликати імунну реакцію на фрагмент,
у виробництві лікарського засобу для ефективного лікування або профілактики хвороби Альцгеймера у пацієнта.
2. Застосування за п. 1, де фрагмент Аβ індукує антитіла, які зв'язуються з розчинним Аβ у пацієнта, таким чином інгібуючи утворення амілоїдних відкладень Аβ в мозку з розчинного Аβ, і, таким чином, забезпечуючи ефективне лікування або профілактику хвороби.
3. Застосування полінуклеотиду, що кодує
і) фрагмент Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, або
іі) фрагмент Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, де фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, і де молекула-носій допомагає викликати імунну реакцію на фрагмент,
у виробництві лікарського засобу для ефективного лікування або профілактики хвороби Альцгеймера у пацієнта.
4. Застосування за п. 3, де полінуклеотид придатний для експресії в організмі пацієнта з метою продукування фрагмента Аβ, і фрагмент Аβ індукує антитіла, які зв'язуються з розчинним Аβ у пацієнта, таким чином, інгібуючи утворення амілоїдних відкладень Аβ в мозку з розчинного Аβ, і, таким чином, забезпечуючи ефективне лікування або профілактику хвороби.
5. Застосування за будь-яким з пп. 1 або 2, де хвороба характеризується розладом когнітивної функції.
6. Застосування за будь-яким з пп. 1, 2 або 5, де пацієнтом є людина.
7. Застосування за будь-яким з пп. 1, 2, 5 або 6, де лікування або ефективна профілактика хвороби включає моніторинг індукованих антитіл у пацієнта.
8. Застосування за будь-яким з пп. 1, 2, 5, 6 або 7 для ефективної профілактики хвороби Альцгеймера у пацієнта, де пацієнт має безсимптомне захворювання.
9. Застосування за будь-яким з пп. 1, 2, 5, 6 або 7 для лікування хвороби Альцгеймера у пацієнта, де пацієнт має симптоми захворювання, і введення засобу інгібує погіршення симптомів у пацієнта.
10. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8 або 9, де вік пацієнта становить менше 50 років.
11. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9 або 10, де пацієнт має успадкований фактор ризику, що вказує на схильність до хвороби Альцгеймера.
12. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9 або 10, де пацієнт не має відомих факторів ризику хвороби Альцгеймера.
13. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9, 10, 11 або 12, де лікарський засіб придатний для введення у вигляді декількох доз протягом періоду часу, який становить щонайменше три місяці.
14. Застосування за п. 13, де доза становить щонайменше 50 мікрограмів.
15. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9, 10, 11, 12 або 13, де лікарський засіб додатково містить ад'ювант, який підвищує рівень антитіл, індукованих фрагментом.
16. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 або 15, де лікарський засіб придатний для внутрішньочеревинного, перорального, інтраназального, підшкірного, внутрішньом'язового, місцевого або внутрішньовенного введення.
17. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 або 16, де лікування або ефективна профілактика хвороби додатково включає моніторинг стану пацієнта з метою спостереження за рівнем індукованих антитіл в крові пацієнта.
18. Застосування за п. 1 або 2, де фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, де молекула-носій допомагає викликати імунну реакцію на фрагмент.
19. Застосування за п. 18, де множинні копії фрагмента з'єднані з молекулою-носієм з метою утворення кон'югата.
20. Застосування за п. 18, де множинні копії фрагмента з'єднані з множинними копіями молекули-носія, які з'єднані одна з одною.
21. Застосування за п. 19, де молекула-носій містить QYIKANSKFIGITEL (SEQ ID NO: 8).
22. Застосування за п. 19, де молекула-носій містить амінокислотну послідовність AKXVAAWTLKAAA (SEQ ID NО: 11).
23. Застосування за п. 19, де молекула-носій індукує реакцію Т-клітин проти гетерологічного поліпептиду, і, таким чином, реакцію В-клітин проти фрагмента.
24. Застосування за будь-яким з пп. 1, 2 або 4, де лікування або ефективна профілактика додатково включає введення ад’юванта, що підвищує титр та/або спорідненість зв'язування індукованих антитіл, в порівнянні з окремим введенням фрагмента.
25. Застосування за п. 24, де лікарський засіб містить ад'ювант і фрагмент.
26. Застосування за п. 24, де ад'ювант придатний для введення до введення фрагмента.
27. Застосування за п. 24, де ад'ювант придатний для введення після введення фрагмента.
28. Застосування за п. 24, де ад'ювант вибраний з групи, що складається з алюмінієвого галуну, монофосфорил ліпіду A (MPL), QS-21 і неповного ад’юванта Фрейнда.
29. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 або 24, де лікарський засіб містить фрагмент в дозі більше 10 мікрограмів.
30. Фрагмент Аβ, який відрізняється тим, що складається з амінокислотної послідовності KLVFFAED (залишки 16-23 SEQ ID NO: 1).
31. Фрагмент за п. 30, який відрізняється тим, що фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, в якому молекула-носій допомагає викликати імунну реакцію на фрагмент.
32. Фрагмент за п 31, який відрізняється тим, що множинні копії фрагмента з'єднані з єдиною копією молекули-носія.
33. Фрагмент за п. 31, який відрізняється тим, що єдина копія фрагмента з'єднана з множинними копіями молекули-носія.
34. Фрагмент за п. 31, який відрізняється тим, що фрагмент з'єднаний з молекулою-носієм через спейсер.
35. Фрагмент за п. 31, який відрізняється тим, що фрагмент зв'язаний з молекулою-носієм хімічним міжмолекулярним зв'язком.
36. Фрагмент за п. 31, який відрізняється тим, що молекула-носій являє собою гетерологічний поліпептид.
37. Фрагмент за п. 36, який відрізняється тим, що молекула-носій містить QYIKANSKFIGITEL (SEQ ID NO: 8).
38. Фрагмент за п. 36, який відрізняється тим, що молекула-носій містить амінокислотну послідовність AKXVAAWTLKAAA (SEQ ID NO: 11).
39. Фрагмент за п. 31, який відрізняється тим, що молекула-носій являє собою анатоксин дифтерії.
40. Фрагмент за п. 30, який відрізняється тим, що додатково містить фармацевтично прийнятний носій.
41. Фармацевтична композиція, яка відрізняється тим, що містить фрагмент Аβ, що складається з амінокислотної послідовоності KLVFFAED (залишки 16-23 SEQ ID NO: 1), і фармацевтично прийнятний носій.
42. Композиція за п. 41, яка відрізняється тим, що фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, де молекула-носій допомагає викликати імунну реакцію на фрагмент.
43. Композиція за п. 41, яка відрізняється тим, що множинні копії фрагмента з'єднані з єдиною копією молекули-носія.
44. Композиція за п. 41, яка відрізняється тим, що єдина копія фрагмента з'єднана з множинними копіями молекули-носія.
45. Композиція за п. 41, яка відрізняється тим, що фрагмент зв'язаний з молекулою-носієм за допомогою спейсера.
46. Композиція за п. 41, яка відрізняється тим, що фрагмент зв'язаний з молекулою-носієм хімічним міжмолекулярним зв'язком.
47. Композиція за п. 42, яка відрізняється тим, що молекула-носій включає QYIDCANSKFIGITEL (SEQ ID NO: 8).
48. Композиція за п. 42, яка відрізняється тим, що молекула-носій включає амінокислотну послідовність AKXVAAWTLKAAA (SEQ ID NO: 11).
49. Композиція за п. 42, яка відрізняється тим, що молекулою-носієм є анатоксин дифтерії.
50. Композиція за пп. 41 або 42, яка відрізняється тим, що додатково містить ад'ювант.
51. Композиція за п. 50, яка відрізняється тим, що ад'ювант являє собою алюмінієвий галун.
52. Композиція за п. 50, яка відрізняється тим, що ад'ювант являє собою монофосфорил ліпід A (MPL).
53. Композиція за п. 50, яка відрізняється тим, що ад'ювант являє собою QS-21.
54. Композиція за п. 50, яка відрізняється тим, що ад'ювант являє собою RC-529.
55. Композиція за п. 41, яка відрізняється тим, що додатково містить поверхнево-активну речовину.
56. Упаковка, яка відрізняється тим, що містить фармацевтичну композицію, яка містить фрагмент Аβ, що складається з амінокислотної послідовності KLVFFAED (залишки 16-23 SEQ ID NO: 1), у фармацевтично придатному носії, та ад'ювант.
Текст
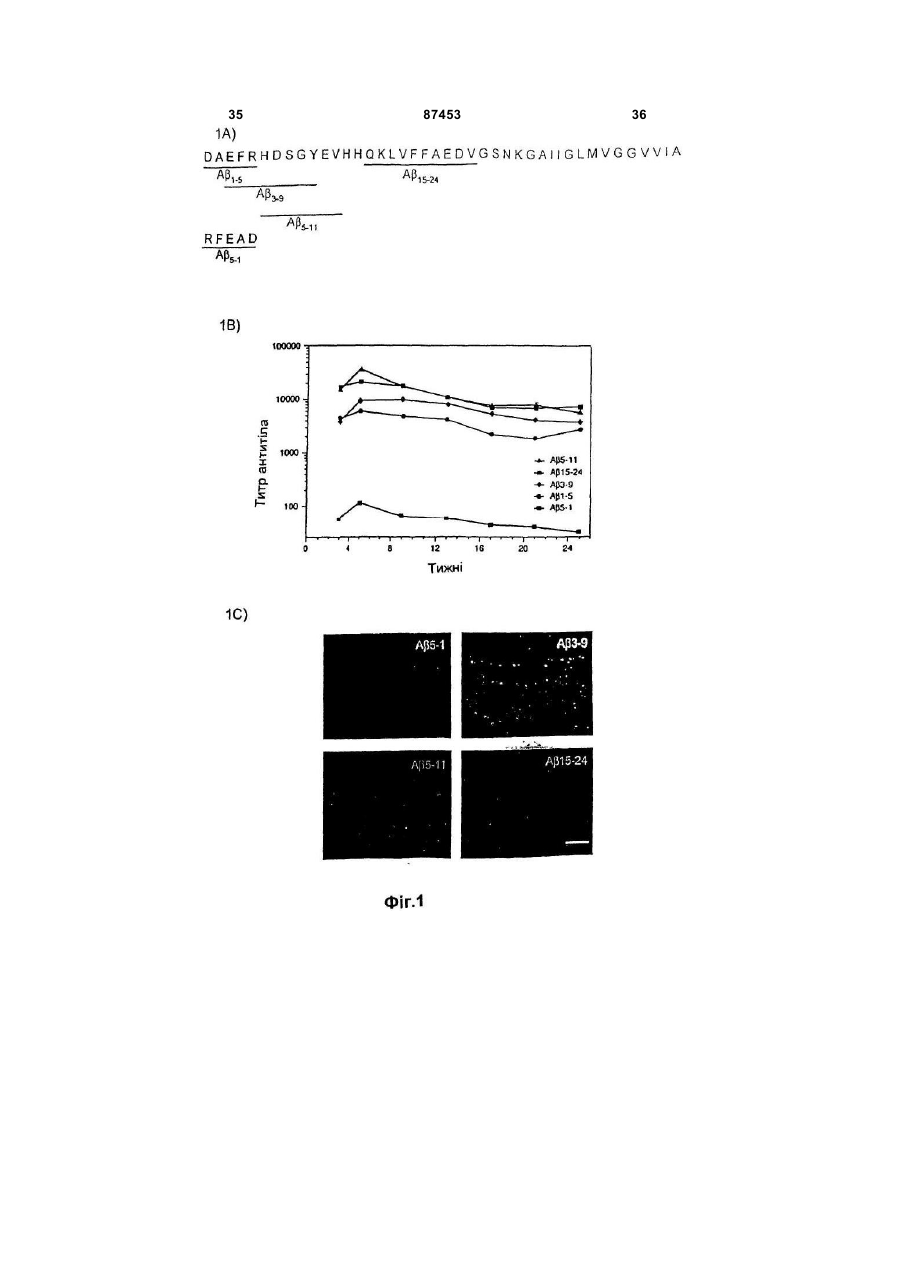
1. Застосування і) фрагмента Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, або іі) фрагмента Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, де фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, де молекула-носій допомагає викликати імунну реакцію на фрагмент, у виробництві лікарського засобу для ефективного лікування або профілактики хвороби Альцгеймера у пацієнта. 2. Застосування за п. 1, де фрагмент Аβ індукує антитіла, які зв'язуються з розчинним Аβ у пацієнта, таким чином інгібуючи утворення амілоїдних відкладень Аβ в мозку з розчинного Аβ, і, таким чином, забезпечуючи ефективне лікування або профілактику хвороби. 3. Застосування полінуклеотиду, що кодує і) фрагмент Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, або іі) фрагмент Аβ, що складається з Аβ16-23 і має амінокислотну послідовність KLVFFAED, де фрагмент зв'язаний з молекулою-носієм з метою утворення кон'югата, і де молекула-носій допомагає викликати імунну реакцію на фрагмент, у виробництві лікарського засобу для ефективного лікування або профілактики хвороби Альцгеймера у пацієнта. 4. Застосування за п. 3, де полінуклеотид придатний для експресії в організмі пацієнта з метою продукування фрагмента Аβ, і фрагмент Аβ інду 2 (19) 1 3 87453 4 зового, місцевого або внутрішньовенного введен35. Фрагмент за п. 31, який відрізняється тим, що ня. фрагмент зв'язаний з молекулою-носієм хімічним 17. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, міжмолекулярним зв'язком. 9, 10, 11, 12, 13, 14, 15 або 16, де лікування або 36. Фрагмент за п. 31, який відрізняється тим, що ефективна профілактика хвороби додатково вклюмолекула-носій являє собою гетерологічний полічає моніторинг стану пацієнта з метою спостерепептид. ження за рівнем індукованих антитіл в крові паціє37. Фрагмент за п. 36, який відрізняється тим, що нта. молекула-носій містить QYIKANSKFIGITEL (SEQ 18. Застосування за п. 1 або 2, де фрагмент зв'яID NO: 8). заний з молекулою-носієм з метою утворення 38. Фрагмент за п. 36, який відрізняється тим, що кон'югата, де молекула-носій допомагає викликати молекула-носій містить амінокислотну послідовімунну реакцію на фрагмент. ність AKXVAAWTLKAAA (SEQ ID NO: 11). 19. Застосування за п. 18, де множинні копії фраг39. Фрагмент за п. 31, який відрізняється тим, що мента з'єднані з молекулою-носієм з метою утвомолекула-носій являє собою анатоксин дифтерії. рення кон'югата. 40. Фрагмент за п. 30, який відрізняється тим, що 20. Застосування за п. 18, де множинні копії фрагдодатково містить фармацевтично прийнятний мента з'єднані з множинними копіями молекулиносій. носія, які з'єднані одна з одною. 41. Фармацевтична композиція, яка відрізняється 21. Застосування за п. 19, де молекула-носій містим, що містить фрагмент Аβ, що складається з тить QYIKANSKFIGITEL (SEQ ID NO: 8). амінокислотної послідовоності KLVFFAED (залиш22. Застосування за п. 19, де молекула-носій міски 16-23 SEQ ID NO: 1), і фармацевтично прийняттить амінокислотну послідовність ний носій. AKXVAAWTLKAAA (SEQ ID NО: 11). 42. Композиція за п. 41, яка відрізняється тим, що 23. Застосування за п. 19, де молекула-носій індуфрагмент зв'язаний з молекулою-носієм з метою кує реакцію Т-клітин проти гетерологічного поліпеутворення кон'югата, де молекула-носій допомагає птиду, і, таким чином, реакцію В-клітин проти фравикликати імунну реакцію на фрагмент. гмента. 43. Композиція за п. 41, яка відрізняється тим, що 24. Застосування за будь-яким з пп. 1, 2 або 4, де множинні копії фрагмента з'єднані з єдиною копією лікування або ефективна профілактика додатково молекули-носія. включає введення ад’юванта, що підвищує титр 44. Композиція за п. 41, яка відрізняється тим, що та/або спорідненість зв'язування індукованих анєдина копія фрагмента з'єднана з множинними титіл, в порівнянні з окремим введенням фрагменкопіями молекули-носія. та. 45. Композиція за п. 41, яка відрізняється тим, що 25. Застосування за п. 24, де лікарський засіб місфрагмент зв'язаний з молекулою-носієм за допотить ад'ювант і фрагмент. могою спейсера. 26. Застосування за п. 24, де ад'ювант придатний 46. Композиція за п. 41, яка відрізняється тим, що для введення до введення фрагмента. фрагмент зв'язаний з молекулою-носієм хімічним 27. Застосування за п. 24, де ад'ювант придатний міжмолекулярним зв'язком. для введення після введення фрагмента. 47. Композиція за п. 42, яка відрізняється тим, що 28. Застосування за п. 24, де ад'ювант вибраний з молекула-носій включає QYIDCANSKFIGITEL групи, що складається з алюмінієвого галуну, мо(SEQ ID NO: 8). нофосфорил ліпіду A (MPL), QS-21 і неповного 48. Композиція за п. 42, яка відрізняється тим, що ад’юванта Фрейнда. молекула-носій включає амінокислотну послідов29. Застосування за будь-яким з пп. 1, 2, 5, 6, 7, 8, ність AKXVAAWTLKAAA (SEQ ID NO: 11). 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 49. Композиція за п. 42, яка відрізняється тим, що або 24, де лікарський засіб містить фрагмент в молекулою-носієм є анатоксин дифтерії. дозі більше 10 мікрограмів. 50. Композиція за пп. 41 або 42, яка відрізняється 30. Фрагмент Аβ, який відрізняється тим, що тим, що додатково містить ад'ювант. складається з амінокислотної послідовності 51. Композиція за п. 50, яка відрізняється тим, що KLVFFAED (залишки 16-23 SEQ ID NO: 1). ад'ювант являє собою алюмінієвий галун. 31. Фрагмент за п. 30, який відрізняється тим, що 52. Композиція за п. 50, яка відрізняється тим, що фрагмент зв'язаний з молекулою-носієм з метою ад'ювант являє собою монофосфорил ліпід A утворення кон'югата, в якому молекула-носій до(MPL). помагає викликати імунну реакцію на фрагмент. 53. Композиція за п. 50, яка відрізняється тим, що 32. Фрагмент за п 31, який відрізняється тим, що ад'ювант являє собою QS-21. множинні копії фрагмента з'єднані з єдиною копією 54. Композиція за п. 50, яка відрізняється тим, що молекули-носія. ад'ювант являє собою RC-529. 33. Фрагмент за п. 31, який відрізняється тим, що 55. Композиція за п. 41, яка відрізняється тим, що єдина копія фрагмента з'єднана з множинними додатково містить поверхнево-активну речовину. копіями молекули-носія. 56. Упаковка, яка відрізняється тим, що містить 34. Фрагмент за п. 31, який відрізняється тим, що фармацевтичну композицію, яка містить фрагмент фрагмент з'єднаний з молекулою-носієм через Аβ, що складається з амінокислотної послідовності спейсер. KLVFFAED (залишки 16-23 SEQ ID NO: 1), у фармацевтично придатному носії, та ад'ювант. 5 Ця заявка проголошує переваги над попередньо зареєстрованою патентною заявкою, США, 35 U.S.С. §119(е). Серійний No 60/444,150, поданою 1 лютого, 2003. Увесь зміст вищезазначеної заявки наведений тут у вигляді довідкової інформації для використання з будь-якою метою. Винахід належить до технічних галузей імунології і медицини. Хвороба Альцгеймера (АХ) - це прогресуюче захворювання, яке призводить до сенільної деменції. [Див. звичайно Selkoe, TINS 16, 403-409 (1993); Hardy et al., WO 92/13069; Selkoe, J. Neuropathol. Exp. Neurol. 53, 438-447 (1994), Duff et al., Nature 373, 476-477 (1995); Games et al., Nature 373, 523 (1995)]. У широкому розумінні, хвороба має 2 форми: пізню форму, яка розпочинається у похилому віці (після 65 років), і ранню, яка розвивається задовго до настання сенільного періоду, тобто, від 35 до 65 років. В обох формах хвороби, патологія однакова, однак порушення більш серйозні і поширені у тих випадках, коли захворювання розпочинається у молодшому віці Хвороба характеризується щонайменше двома типами уражень мозку - утворенням сенільних бляшок і нейрофібрилярних сплетень. Сенільні бляшки - це області дезорганізованого нейропілю, що можуть сягати до 150мкм у діаметрі, з екстрацелюлярними амілоїдними відкладеннями в центрі, які видно при мікроскопічному вивченні зрізів мозкової тканини. Нейрофібрилярні сплетення утворені внутрішньоклітинними відкладеннями мікротрубочок, зв'язаних тау протеїном, що складається з двох ниток, скручених одна з однією в пари. Основним компонентом бляшок є пептид, названий Αb або b-амілоїдний пептид. Αb-пептид - це внутрішній фрагмент, утворений 39-43 амінокислотами попередника білка, який називається попередником амілоїдного білка (АРР - amyloid precursor protein). Був встановлений зв'язок між виникненням кількох мутацій АРР білка і наявністю хвороби Альцгеймера. [Див., наприклад, Goate et al., Nature 349,704) (1991) (валін717 на ізолейцин); Chartier Harlan et al. Nature 353,844 (1991)) (валін717 на гліцин); Murrell et al., Science 254,97 (1991) (валін717 на фенілаланін); Mullan el al., Nature Genet. 1,345 (1992) (подвійна мутація, яка змінює лізин595-метіонін596 на аспарагін595596 лейцин )]. Вважають, що такі мутації викликають хворобу Альцгеймера за рахунок зростання або зміни процесингу АРР до Αb, зокрема процесингу АРР, який супроводжується форми Αb (тобто, ΑβΙ42 і ΑbΙ-43) Вважають, що мутації в інших генах, таких як пресенілін гени, PS1 і PS2, опосередковано впливають на процесинг АРР, що призводить до збільшення кількості довгої форми Αb [див. Hardy TINS 20 154(1997)] Ці дослідження показують, що Αbβ і особливо його довга форма є чинником, що зумовлює розвиток хвороби Альцгеймера. Імунізація трансгенних мишей що є моделями хвороби Альцгеймера імуногенами, похідними bамілоїдного пептиду (Αb) призводить до реакції антитіла яка інгібує утворення і/або очищує аміло 87453 6 їдні бляшки в мозку мишей [Schenk et al., (1999) Nature 400,173-177, Janus et al., (2000) Nature 408, 979-982, Morgan et al. (2000) Nature 408, 982-985, Sigurdsson et al., (2001) Am J. Pathol. 159, 439-447 1-4)] Пасивне введення антитіл до Αb має дати подібні результати. Було зроблено припущення що антитіло-опосередкований, Fc-залежний фагоцитоз мікрогліальними клітинами і/або макрофагами - це один з механізмів, який забезпечує очищення існуючих амілоїдних бляшок [Bard et al., (2000) Nat. Med., 6, 916-919)]. Це припущення основано на тому результаті, що певні антитіла проти Αb, введені периферично входять до ЦНС трансгенної миші, зв'язують амілоїдні бляшки та індукують їх виведення. Крім того було встановлено існування сильної кореляції між антитілами що було підтверджено дослідженнями in vivo та ex vivo за допомогою зрізів мозку PDAPP мишей або хворих на хворобу Альцгеймера, для того щоб визначити активність очищення бляшок Fc рецептори на мікрогліальних клітинах впливали на реакцію очищення в дослідженнях ех vivo. Однак, було встановлено, що ефективність антитіла може бути отримана in vivo завдяки механізмам, які незалежні від Fc взаємодії [Bacskai et al. (2002) J. Neurosci., 22. 7873-7878]. Було встановлено, що антитіло, спрямоване проти середньої частини Αb яке не розпізнає амілоїдні бляшки, зв'язується з розчинним Αb і зменшує накопичення бляшок [DeMattos et al., (2001) Proc Natl Acad Sci USA, 98, 8850-8855]. Встановлено, що короткочасне застосування такого антитіла покращує виконання завдання розпізнавання об'єкта, не впливаючи в той же час на амілоїдні відкладення [Dodart et al., (2002) Nat. Neurosci., 5,452-457]. Цей винахід пов'язаний із заявкою WO 00/72880, поданою 26 травня, 2000, WO 99/27944, поданою 30 листопада, 1998, США, серійний No 60/067,740, поданою 2 грудня, 1997, США, серійний No 60/080,970, поданою 7 квітня, 1998, і заявкою з серійним No 09/201,430, поданою 30 листопада, 1998, кожна з яких у повному обсязі включена тут як посилання для використання з будь-якою метою. Фігури 1А-С. Антитіла, утворені шляхом імунізації N-кінцевими фрагментами Αb, зв'язуються з амілоїдними бляшками Фіг.1А. Пептиди, які включають різні домени ΑbΙ-42 (SEQ ID NO.1) (синтезовані прилеглим до Т-клітини епітопом, який походить від овальбуміну) були використані для імунізації миші PDAPP лінії Реверсемер, Αb5-Ι (SEQ ID NO:2), був використаний як негативний контроль. Фіг.1B. ELISA титри проти зв'язаних Αb142 були значно вищими протягом всього дослідження у Αb5-11 і Αb15-24 груп, ніж у Αb1-5 групи (1:14,457, р
ДивитисяДодаткова інформація
Назва патенту англійськоюUse a fragment ав for treatment of alzheimer's disease
Автори англійськоюBard Frederique, Yednok Ted, Vasquez Nicki, Seubert Peter A
Назва патенту російськоюПрименения фрагмента ав для лечения болезни альцгеймера
Автори російськоюБард Фредерик, Эднок Тед, Васквез Ники, Сьюберт Питер А.
МПК / Мітки
МПК: A61P 25/28, A61K 38/08, A61K 39/00
Мітки: аb16-23, лікування, застосування, альцгеймера, хвороби, фрагмента
Код посилання
<a href="https://ua.patents.su/19-87453-zastosuvannya-fragmenta-ab16-23-dlya-likuvannya-khvorobi-alcgejjmera.html" target="_blank" rel="follow" title="База патентів України">Застосування фрагмента аb16-23 для лікування хвороби альцгеймера</a>