1-фенілалкіл-1,2,3,6-тетрагідропіридини, спосіб їх одержання та фармацевтична композиція для лікування хвороби альцгеймера
Номер патенту: 52707
Опубліковано: 15.01.2003
Автори: БАРОНІ Марко, КАРДАМОН Розанна, ФУРНЬЄ Жаклін, ГУЗЗІ Умберто
Формула / Реферат
1. Сполука формули (І):
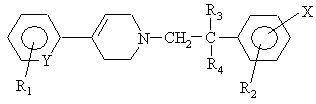 (I),
(I),
в якій:
Y означає -СН- або -N-,
R1 означає водень, галоген, трифторметил, (С1-С4)-алкіл або (С1-С4)-алкоксил,
R2 означає метил або етил,
кожний із радикалів R3 та R4 означає водень або (С1-С3)-алкіл,
Х означає:
(а) (С1-С6)-алкіл, (С1-С6)-алкоксил, карбокси-(С3-С7)-алкіл, (С1-С4)-алкоксикарбоніл-(С1-С6)-алкіл, карбокси-(С3-С7)-алкоксил або (С1-С4)-алкоксикарбоніл-(С1-С6)-алкоксил,
(б) радикал, що його вибирають з (С3-С7)-циклоалкілу, (С3-С7)-циклоалкілоксигрупи, (С3-С7)-циклоалкілметилу, (С3-С7)-циклоалкіламіногрупи і циклогексенілу, причому вищезгаданий радикал може заміщатися галогеном, гідроксилом, (С1-С4)-алкоксилом, карбоксилом, (С1-С4)-алкоксикарбонілом, аміногрупою, моно- або ді[(С1-С4)-алкіл]аміногрупою;
або
(в) групу, що вибирається з фенілу, феноксигрупи, феніламіногрупи, N-(С1-С3)-алкілфеніламіногрупи, фенілметилу, фенілетилу, фенілкарбонілу, фенілтіогрупи, фенілсульфонілу, фенілсульфінілу або стирилу, причому вищезгадана група може бути моно- або полізаміщеною у фенільній групі галогеном, трифторметилом, (С1-С4)-алкілом, (С1-С4)-алкоксилом, ціаногрупою, аміногрупою, моно- або ді[(С1-С4)-алкіл]аміногрупою, (С1-С4)-ациламіногрупою, карбоксилом, (С1-С4)-алкоксикарбонілом, амінокарбонілом, моно- або ді[(С1-С4)-алкіл]амінокарбонілом, аміно-(С1-С4)-алкілом, гідрокси-(С1-С4)-алкілом або галоген-(С1-С4)-алкілом; а також її солі і сольвати та її четвертинні амонієві солі.
2. Сполука по п. 1, в якій Y означає групу -СН- і R1 означає трифторметил.
3. Сполука по п. 1, в якій Y означає атом азоту і R1 означає атом хлору.
4. Сполука по будь-якому з пп. 1-3, в якій Х означає (С1-С6)-алкіл.
5. Сполука по п. 1, в якій Х означає групу (в), де феніл заміщений 1-3-ма атомами галогену, 1-3-ма трифторметильними групами, 1-3-ма (С1-С4)-алкільними групами, 1-3-ма (С1-С4)-алкоксильними групами, 1-3-ма ціаногрупами, 1-3-ма аміногрупами, 1-3-ма моно- або ді[(С1-С4)-алкіл]-аміногрупами, 1-3-ма (С1-С4)-ациламіногрупами, 1-3-ма карбоксильними групами, 1-3-ма (С1-С4)-алкоксикарбонільними групами, 1-3-ма амінокарбонільними групами, 1-3-ма моно- або ді[(С1-С4)-алкіл]амінокарбонільними групами, 1-3-ма аміно-(С1-С4)-алкільними групами, 1-3-ма гідроксі(С1-С4)алкільними групами або 1-3-ма галоген-(С1-С4)-алкільними групами.
6. Сполука по п. 1 формули (I'):
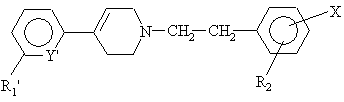 (I'),
(I'),
в якій R1' означає трифторметил і Y' означає СН, або R1' означає хлор і Y' означає азот, a R2 і Х мають зазначені для сполук формули (І) у п. 1 значення, а також її солі, сольвати і четвертинні амонієві солі.
7. Сполука по п. 6, в якій Х означає (С1-С6)-алкіл.
8. Сполука по п. 1, яку вибирають з 1-[2-(3,4-діетилфеніл)етил]-4-(3-трифторметилфеніл)-1,2,3,6-тетрагідропіридину, 1-[2-(3-метил-4-пентилфеніл)етил]-4-(3-трифторметилфеніл)-1,2,3,6-тетрагідропіридину, 1-[2-(4-метил-3-пентилфеніл)-етил]-4-(3-трифторметилфеніл)-1,2,3,6-тетрагідропіридину, 1-[2-(3,4-діетилфеніл)-етил]-4-(6-хлорпірид-2-іл)-1,2,3,6-тетрагідропіридину, а також їх солей, сольватів або четвертинних амонієвих солей.
9. Спосіб одержання сполук формули (І) по п. 1, їх солей або сольватів і їх четвертинних амонієвих солей, який відрізняється тим, що:
(а) арил-1,2,3,6-тетрагідропіридин формули (II):
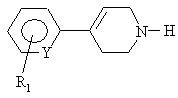 (II),
(II),
в якій Y і R1 мають зазначені для сполук формули (І) у п. 1 значення, вводять у взаємодію з сполукою формули (III):
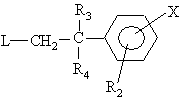 (III),
(III),
в якій R2, R3, R4 та Х мають зазначені для сполук формули (І) у п. 1 значення і L означає відщеплювану групу; і
(б) одержану сполуку формули (І) виділяють і, за необхідністю, перетворюють її на одну з її солей або один з її сольватів або на одну з її четвертинних амонієвих солей.
10. Фармацевтична композиція, яка відрізняється тим, що вона містить сполуку по будь-якому з пп. 1-8 в ефективній кількості як активний агент.
11. Фармацевтична композиція, що містить як активні агенти сполуку по будь-якому з пп. 1-8 і сполуку, призначену для симптоматичного лікування старечого недоумства типу хвороби Альцгеймера (DAT), або їх фармацевтичнo прийнятні солі.
Текст
1 Сполука формули (І) IT, R в якій Y означає -СН- або -N-, Ri означає водень, галоген, трифторметил, ( d С4)-алкіл або (Сі-С^-алкоксил, R2 означає метил або етил, кожний із радикалів R3 та R4 означає водень або (С-і-Сз)-алкіл, X означає (а) (С-і-Сб)-алкіл, (Сі-Сб)-алкоксил, карбокси-(СзСу)-алкіл, (Сі-С4)-алкоксикарбоніл-(Сі-Сб)-алкіл, карбокси-(Сз-С7)-алкоксил або (С1-С4)ал ко кс и карбо н і л - (С і -Сє) -ал ко кс и л, (б) радикал, що його вибирають з (С3-С7)циклоалкілу, (Сз-С7)-циклоалкілоксигрупи, (С3-С7)циклоал кіл метилу, (Сз-С7)-циклоалкіламшогрупи і циклогексенілу, причому вищезгаданий радикал може заміщатися галогеном, гідроксилом, (С1-С4)алкоксилом, карбоксилом, (С1-С4)алкоксикарбонілом, аміногрупою, моно- або ді[(Сг С4)-алкіл]амшогрупою, або (в) групу, що вибирається з фенілу, феноксигрупи, феніламшогрупи, І\І-(Сі-Сз)-алкілфеніламіногрупи, фенілметилу, фенілетилу, феніл карбонілу, фенілтюгрупи, фенілсульфонілу, фенілсульфінілу або стирилу, причому вищезгадана група може бути моно- або полізаміщеною у фенільніи групі галогеном, трифторметилом, (Сі-С4)-алкілом, (С1-С4)алкоксилом, ціаногрупою, аміногрупою, моно- або ді[(Сі-С4)-алкіл]амшогрупою, (С1-С4)ациламшогрупою, карбоксилом, (С1-С4)алкоксикарбонілом, амінокарбонілом, моно- або ді[(Сі-С4)-алкіл]амшокарбонілом, аміно-(Сі-С4)алкілом, пдрокси-(С-і-С4)-алкілом або галоген-(Сг С4)-алкілом, а також и солі і сольвати та и четвертинні амонієві солі 2 Сполука по п 1, в якій Y означає групу -СН- і Ri означає трифторметил 3 Сполука по п 1, в якій Y означає атом азоту і Ri означає атом хлору 4 Сполука по будь-якому з пп 1-3, в якій X означає (С-і-Сб)-алкіл 5 Сполука по п 1, в якій X означає групу (в), де феніл заміщений 1-3-ма атомами галогену, 1-3-ма трифторметил ьними групами, 1-3-ма (С1-С4)алкільними групами, 1-3-ма (Сі-С4)-алкоксильними групами, 1 -3-ма ціаногрупами, 1 -3-ма аміногрупами, 1-3-ма моно- або ді[(С-і-С4)-алкіл]аміногрупами, 1-3-ма (Сі-С4)-ациламшогрупами, 13-ма карбоксильними групами, 1-3-ма (С1-С4)алкоксикарбонільними групами, 1-3-ма амінокарбонільними групами, 1-3-ма моно- або ді[(Сі-С4)-алкіл]амшокарбонільними групами, 1-3ма амшо-(Сі-С4)-алкільними групами, 1-3-ма пдроксі(С-і-С4)алкільними групами або 1-3-ма галоген-(Сі-С4)-алкільними групами 6 Сполука по п 1 формули (Г) сн,—сн. 1 (Iі), в якій R-і означає трифторметил і Y' означає СН, або R-і1 означає хлор і Y означає азот, a R2 і X мають зазначені для сполук формули (І) у п 1 значення, а також и солі, сольвати і четвертинні амонієві солі 7 Сполука по п 6, в якій X означає (С-і-Сб)-алкіл 8 Сполука по п 1, яку вибирають з 1-[2-(3,4діетилфеніл)етил]-4-(3-трифторметилфеніл)1,2,3,6-тетрапдропіридину, 1-[2-(3-метил-4 О і о ю 52707 пентилфеніл)етил]-4-(3-трифторметилфеніл)1,2,3,6-тетрапдропіридину, 1-[2-(4-метил-3пентилфеніл)-етил]-4-(3-трифторметилфеніл)1,2,3,6-тетрапдропіридину, 1-[2-(3,4-діетилфеніл)етил]-4-(6-хлорпірид-2-іл)-1,2,3,6тетрапдропіридину, а також їх солей, сольватів або четвертинних амонієвих солей 9 Спосіб одержання сполук формули (І) по п 1, їх солей або сольватів і їх четвертинних амонієвих солей, який відрізняється тим, що (а) арил-1,2,3,6-тетрапдропіридин формули (II) N - H в якій Y і Ri мають зазначені для сполук формули (І) у п 1 значення, вводять у взаємодію з сполукою формули (III) Цей винахід стосується нових, заміщених У положенні 4 1-фенілалкіл-1,2,3,6тетрапдропіридинів, які відзначаються нейротрофічною та нейрозахисною активністю, способів їх приготування і фармацевтичних композицій, що містять їх У європейському патенті 0 458 696 описано використання 1-(2-нафтилетил)-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридину для одержання лікарських засобів, призначених для лікування мозкових та неиронних порушень У міжнародній заявці 93/11107 описано піперидини і тетрапдропіридини із захисною дією проти розладів, що викликаються ппоксичними та/або ішемічними станами Останнім часом виявлено, що деякі фенілалкіл-1,2,3,6-тетрапдропіридини, заміщені фенільною або піридильною групою, справляють нейротрофічний вплив на нервову систему, подібний до впливу фактора росту нервової тканини (від англійського Nerve Growth Factor) (NGF), і можуть відновлювати функцію ушкоджених або аномальних за своїми фізіологічними функціями клітин Отже, цей винахід, згідно з одним з його аспектів, стосується сполук формули (І) N-CH2-C (І) В ЯКІЙ Y означає -СН- або -N-, Ri означає водень, галоген, трифторметил, (Сі-С4)-алкіл або (Сі-С^-алкоксил, R2 означає метил або етил, кожний з радикалів R3 і R4 означає водень або (С-і-Сз)-алкіл, X означає в якій R2, R3, R4 та X мають зазначені для сполук формули (І) у п 1 значення і L означає відщеплювану групу, і (б) одержану сполуку формули (І) виділяють і, за необхідністю, перетворюють її на одну з и солей або один з її сольватів або на одну з її четвертинних амонієвих солей 10 Фармацевтична композиція, яка відрізняється тим, що вона містить сполуку по будь-якому з пп 1-8 в ефективній КІЛЬКОСТІ як активний агент 11 Фармацевтична композиція, що містить як активні агенти сполуку по будь-якому з пп 1-8 і сполуку, призначену для симптоматичного лікування старечого недоумства типу хвороби Альцгеимера (DAT), або їх фармацевтично прийнятні солі (а) (С-і-Сб)-алкіл, (Сі-Сє)-алкрксил, карбокси(Сз-Су)-алкіл, (Сі-С4)-алкокси карбон іл-(Сі-Сб)алкіл, каррокси-(Сз-С7)-алкоксил, або (С1-С4)ал ко кс и карбо н і л - (С і -Сє) -ал ко кс и л, (б) радикал, що його вибирають серед (С3-С7)циклоалкілу, (Сз-С7)-циклоалкілоксигрупи, (С3-С7)циклоал кіл метилу, (Сз-С7)-циклоалкіламшогрупи і циклогексенілу, причому зазначений радикал може бути заміщений галогеном, гідроксилом, (С1-С4)алкоксилом, карбоксилом, (С1-С4)алкоксикарбонілом, аміногрупою, моно- або ді[(Сг С4)-алкілІ]амшогрупою, або (в) групу, що и вибирають серед фенілу, феноксигрупи, феніл аміногрупи, Г\І-(Сі-Сз)алкілфеніламіногрупи, феніл метилу, фенілетилу, феніл карбонілу, фенілтюгрупи, фенілсульфонілу, фенілсульфінілу або стирилу, причому зазначена група може бути моно- або полізаміщеною у фенільній групі галогеном, трифторметилом, (С1-С4)алкілом, (С|-С4)-алкоксилом, ціаногрупою, аміногрупою, моно- або ді[(Сі-С4)-алкіл]амшогрупою, (Сі-С4)-ациламшогрупою, карбоксилом, (С1-С4)алкоксикарбонтом, амінокарбонілом, моно- або ді[(С-і-С4)-алкіл] амінокарбонілом, аміно-(С-і-С4)алкілом, пдрокси-(С-і-С4)-алкілом або галоген-(Сг С4)-алкілом, також їх солей і сольватів та їх четвертинних амонієвих солей У цьому описі термін «(С-і-Сз)-алкіл» означає метил, етил, н-пропілта ізопропіл Термін «(Сі-С4)-алкіл» означає метил, етил, нпропіл, ізопропіл, н-бутил, ізобутил, втор, -бутил і трет, -бутил Термін «(Сі-Сб)-алкіл» означає вуглеводневий радикал з 1-6 атомами вуглецю, наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор бутил, трет -бутил, н-пентил, ізопентил, неопентил, трет-пентил, н-гексил, ізогексил тощо Термін «алкоксил» означає гідроксил, заміще 52707 ний (Сі-Сб)-алкілом, переважно (Сі-С4)-алкілом, краще (Сі-Сз)-алкілом Коли X означає феніл, номенклатура, що її застосовують до біфенілу, відповідає правилам ІЮПАК, зокрема, нумерація положень обох циклів така 6і 6 5 і радикали, що мають цю структуру, називають таким чином біфеніл-4-іл Наступну оптимальну для реалізації винаходу групу формують сполуки формули (Г), де X означає (С-і-Сб)-алкіл Найкращими сполуками згідно з цим винаходом є такі 1-[2-(3,4-діетилфеніл)етил]-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридин, 1-[2-(3-метил-4-пентилфеніл)етил]-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридин, 1-[2-(4-метил-3-пентилфеніл)етил]-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридин, 1-[2-(3,4-діетилфеніл)етил]-4-(6-[хлорпірид-2іл)-1,2,3,6-тетрапдропіридин, і їх солі, сольвати і четвертинні амонієві солі Згідно З ІНШИМ аспектом даного винаходу він стосується способу приготування сполук формули (І), їх солей або сольватів і їх четвертинних амонієвих солей, який відрізняється тим, що (а) арил-1,2,3,6-тетрапдропіридин формули (II) біфеніл -3-іл в якій Y і Ri мають вищезгадані значення, вводять у реакцію зі сполукою формули (III) R, 5' б' 6 5 _ , _ біфеніл -2-іл Серед сполук формули (І), де X означає групу радикалів (в), кращими сполуками є ті, в яких феніл заміщений 1-3-ма атомами галогену, 1-3-ма трифторметильними групами, 1-3-ма (С1-С4)алкільними групами, 1-3-ма (Сі-С4)-алкоксильними групами, 1-3-ма ціаногрупами, 1-3-ма аміногрупами, 1-3-ма моно-або ді[(Сі-С4)-алкіл]амшогрупами, 1 -3-ма (Сі-С4)-ациламшогрупами, 1 -3-ма карбоксильними групами, 1 -3-ма (С1-С4)алкоксикарбонільними групами, 1-3-ма амінокарбонільними групами, 1-3-ма моно- або ді[(С-і-С4)алкіл]амшокарбонільними групами, 1-3-ма аміно (Сі-С4)-алкільними групами або 1-3-ма пдроксі-(Сг С4)-алкільними групами, або 1-3-ма галоген-(Сг С4)-алкільними групами Іншу оптимальну для реалізації винаходу групу формують сполуки формули (І), де Y означає групу-СН-1 Ri означає трифторметил Наступну оптимальну для реалізації винаходу групу формують сполуки формули (І), де Y означає атом азоту і Ri означає атом хлору Ще одну оптимальну для реалізації винаходу групу формують сполуки формули (І), де X означає (С-і-Сб)-алкіл, особливо етил Найкращими сполуками є сполуки, що відповідають формулі (Iі) в якій R-і1 означає трифторметил і Y' означає СН, або R-і1 означає хлор і Y' означає азот, причому R2 і X мають вищезгадане значення, і їх солі, сольвати і четвертинні амонієві солі , , х L-CH,-C-C(.')/ (IN) в якій R2, R3, R4 та X мають вищезгадані значення і L означає відщеплювану групу, таку як атом хлору, брому, йоду, метансульфонілоксигрупа, птолуолсульфонілоксигрупа, три фтор метансульфонілоксигрупа, і (б) одержану сполуку формули (І) виділяють і, в разі необхідності, перетворюють її на одну з и солей або один з її сольватів або на одну з и четвертинних амонієвих солей Реакцію проводять в органічному розчиннику і у діапазоні температур від кімнатної до температури кипіння зі зворотним охолоджуванням використовуваного розчинника Як кращий органічний розчинник використовують аліфатичний спирт із 1-6 атомами вуглецю, такий як метанол, етанол, ізопропанол, н-бутанол, н-пентанол, проте використовують також ІНШІ розчинники, наприклад, гексан, диметилформамід, д и метил сульфоксид, сульфолан, ацетонітрил, піридин і т п Реакцію переважно проводять у присутності основної речовини, такої як карбонат лужного металу або триетиламш, особливо коли L являє собою атом галогену Температура реакції може змінюватися від кімнатної (близько 20°С) до температури кипіння з використанням зворотного холодильника, і ВІДПОВІДНО до цього змінюється час, протягом якого відбувається реакція Зазвичай реакцію закінчують після кип'ятіння З використанням зворотного холодильника впродовж 6-12 годин, і одержаний у та 52707 кий спосіб цільовий продукт виділяють звичайними способами у вигляді вільної основи або у вигляді однієї з її солей, причому вільну основу, у разі потреби, перетворюють на одну з и солей шляхом простого солеутворення в органічному розчиннику, такому як спирт, переважно етанол або ізопропанол, простий ефір, такий як 1,2-диметоксіетан, етилацетат, ацетон, або вуглеводень, такий як гексан Одержану сполуку формули (І) виділяють звичайними способами і, у разі потреби, перетворюють на одну з її кислотно-адитивних солей, або, якщо є кислотна група, амфотерний характер сполуки дає можливість здійснювати виділення солей або з кислотами, або з основами Якщо солі сполуки формули (І) одержують з метою введення їх як лікарських засобів, необхідно, щоб використовувані кислоти або основи обов'язково були фармацевтичне прийнятними, якщо солі сполуки формули (І) одержують з іншою метою, наприклад, з метою кращого очищення продукту або з метою кращого виконання аналітичних досліджень, використовують будь-яку кислоту або основу До солей з фармацевтичне прийнятними кислотами належать, наприклад, солі неорганічних кислот, такі як пдрохлорид, пдробромід, борат, фосфат, сульфат, гідросульфат, пдрофосфат, дипдрофосфат, і солі органічних кислот, такі як цитрат, бензоат, аскорбат, метилсульфат, нафталш-2-сульфонат, пікрат, фумарат, малеат, малонат, оксалат, сукцинат, ацетат, тартрат, мезилат, тозилат, ізотюнат, а-кетоглутарат, агліцерофосфат, глюкозо-1-фосфат тощо До солей з фармацевтично прийнятними основами сполук формули (І), в якій замісник X містить карбоксил, належать, наприклад, солі лужних або лужноземельних металів, таких як натрій, калій, кальцій, магній, і солі органічних основ, таких як аміни, основні амінокислоти (лізин, аргінін, гістидин), трометамол, N-метилглюкамш тощо ВИХІДНІ аміни формули (II), де Y означає СН, являють собою ВІДОМІ сполуки, або їх одержують способами, аналогічними тим, що їх застосовують для приготування відомих сполук ВИХІДНІ аміни формули (II), де Y означає азот, приготовляють шляхом взаємодії ВІДПОВІДНОГО 2галогенпіридину формули (р) Hal (Р) в якій Ri має вищезгадане значення і Hal означає атом галогену, з 1,2,3,6-тетрапдропіридином формули (q) N-P' (q) в якій Р° означає захисну групу, таку як, наприклад, бензил, і Z означає замісник, що дозволяє здійснювати нуклеофільне заміщення галогену піридином Такими замісниками є, наприклад, тріалкілстанани, зокрема, трибутилстанан, або сполуки Гриньяра Далі здійснюють видалення захисних груп з 1,2,3,6-тетрапдропіридину шляхом відщеплення 8 захисної групи у ВІДПОВІДНИХ умовах Сполуки формули (III) приготовляють - або для одержання сполуки формули (III), в якій R3=R4=H, шляхом взаємодії ВІДПОВІДНОГО бензолу формули (г) Л (О в якій R2Ta X мають вищезгадані значення, з ацилгалогенідом формули І_-СН2-СО-НаІ, де L і Hal мають вищезгадані значення, у присутності кислоти Льюіса згідно з реакцією ФриделяКрафтса і відновленням одержаного у такий спосіб кетону формули (s) 0 L - C H 2 - C у ' ч X """^ (s) Згідно З описаними у спеціальній літературі способами, або шляхом відновлення кислот формули (V) но~с-с (V) ,00 де R2, R3, R4 та X мають вищезгадані значення, у спирті, з подальшим перетворенням гідроксилу у відщеплювану групу Кислоти формули (V) зазвичай являють собою описані в літературі сполуки, або їх приготовляють аналогічним чином Приклади приготування також наведено в експериментальній частині опису Активність сполук формули (І) щодо нервової системи розкрито у дослідженнях in vitro та in vivo згідно з способами, описаними у європейському патенті 0 458 696, а для оцінки нейронної виживаності використовували тест на виживаність in vitro, здійснюваний з використанням нейронів, виділених з розтинів септальної ділянки ембріонів щурів Згідно З ЦИМ тестом, для аналізу під мікроскопом відбирають септальну ділянку ембріонів щурів віком 17 - 18 днів для розтину в стерильних умовах, після чого її розкладають у середовищі, що складається з трипсину та етилендіамштетраоцтовоі кислоти Суспензію клітин поміщають у колбу для культивування в середовищі, що складається з модифікованого за способом Дульбекко середовища Ігла (DME) і живильної суміші Ham's F12 (об'єм на об'єм) [R G Ham, Proc Nat Sci , 53, 288 (1965)], що містить 5% телячої сироватки і 5% конячої сироватки, і витримують при температурі 37°С протягом 90хв Ця обробка дозволяє видаляти не нейронні клітини Після ЦЬОГО проводять висівання нейробластів у лунки титрувального планшета по 17 х 104 клітин на см2, у культуральному середовищі без сироваток, створеному з модифікованого за способом 52707 Дульбекко середовища Ігла і живильної суміші Ham's F12, що містить ЗОнмоль селену і 1,25мкмоль трансферину Кожну лунку перед цим обробляють ПОЛІ-І_-ЛІЗИНОМ Планшети, у які висівали нейробласти, поміщають у термостатований інкубатор (37°С, 5% СО2) Сполуки, що піддають випробуванню, розчиняють у диметилсульфоксиді і розбавляють ВІДПОВІДНИМ культуральним середовищем Нейробласти витримують у планшетах, що містять випробувану сполуку або ВІДПОВІДНИЙ розчинник, протягом чотирьох днів без обмінювання середовища Через 4 дня середовище заміняють тетразолієвою сіллю, розчиненою в культуральному середовищі (0,15мг/мл) Клітини ПІСЛЯ ЦЬОГО витримують у термостаті при температурі 37°С протягом чотирьох годин Мітохондріальні сукцинодепдрогенази живих клітин відновлюють тетразолієву сіль до формазану синього кольору, за яким, після розчинення у диметилсульфоксиді, вимірюють оптичну густину при 540нм Ця густина ЛІНІЙНО корельована з числом живих клітин [Manthorpe та ш , Dev Brain Res , 25, 191 -198 (1988)] Розбіжності між групами, що містять випробувані сполуки, і контрольними зразками оцінюють шляхом статистичного аналізу з використанням двостороннього t-тесту Dunnett («two-tailed Dunnett t-test») У цьому тесті сполуки формули (І) виявилися також активними або більш активними, ніж сполуки, що їх описано в європейському патенті 0 458 696, причому ефективність деяких сполук формули (І) щодо виживаності нейронів є у два рази більшою порівняно зі сполукою А, описаною в європейському патенті 0 458 696 Завдяки цій потужній нейрозахисній активності та їх незначній токсичності, прийнятній для використання як лікарських засобів, сполуки формули (І), так само, як їх фармацевтичне прийнятні солі приєднання (адитивні солі), їх сольвати та їх четвертинні амонієві солі, використовують для приготування фармацевтичних композицій, показаних для лікування та/або профілактики всіх захворювань, що викликають нейронну дегенерацію В оптимальному варіанті сполуки цього винаходу використовують, окремо або при спільному введенні з іншими активними агентами, що впливають на центральну нервову систему, наприклад, інгібіторами ацетилхолінестерази, селективними холінміметичними засобами М1, антагоністами NMDA, ноотропними засобами, такими як пірацетам, насамперед за таких показань розлади пам'яті, васкулярна деменція, постенцефалітні розлади, постапоплексичні розлади, що виникають внаслідок черепно-мозкової травми, посттравматичні синдроми, розлади, пов'язані з церебральною аноксією, хвороба Альцгеймера, старече недоумство, деменція під кірки головного мозку, наприклад, хорея Гентингтона і хвороба Паркінсона, деменція, що провокується СНІДом, нейропатм, що виникають внаслідок загальної захворюваності або ушкодження симпатичних або спенсорних нервів, і захворювання мозку, такі як набряк мозку, і спиноцеребелярні дегенерації, дегенерації мотонейронів, як, наприклад, боковий амютрофічний 10 склероз Введення сполук цього винаходу зазвичай здійснюють пероральним шляхом, парентеральним шляхом, під'язиковим ШЛЯХОМ або крізьшкірним шляхом КІЛЬКІСТЬ активного агента, що його вводять для лікування церебральних та неиронних порушень згідно зі способом цього винаходу, залежить від природи і тяжкості хворобливих станів, що їх лікують, а також від маси тіла хворого При цьому оптимальні разові дози зазвичай становлять 0,25 -700 мг, переважно 0,5 - ЗООмг, краще 1 150мг, наприклад, від 2 до 50мг, а саме 2, 5, 10, 15, 20, 25 або 50мг продукту Ці разові дози звичайно вводять один або декілька разів на день, наприклад, 2, 3, 4 або 5 разів на день, переважно 1 - 3 рази в день, причому загальна доза для людини змінюється в діапазоні від 0,5 до 1400мг на день, переважно від 1 до 900мг на день, наприклад, від 2 до 500мг, краще 2 - 200мг на день Згідно З ІНШИМ аспектом, об'єктом цього винаходу є фармацевтична композиція, що містить як активні агенти сполуку вищенаведеної формули (І) і сполуку, показану для симптоматичного лікування старечого недоумства типу хвороби Альцгеймера (DAT), або їх фармацевтичне прийнятні солі Вираз «сполука, показана для симптоматичного лікування старечого недоумства типу хвороби Альцгеймера (DAT)» означає продукт, здатний покращувати симптоматологічну картину пацієнтів, уражених DAT, без впливу на причини захворювання Такими сполуками є, наприклад, інгібітори ацетилхолінестерази, мускаринові агоністи М-і, холіноміметичні агоністи, антагоністи рецептора NMDA, ноотропні засоби Кращими інгібіторами ацетилхолінестерази є донепезил і такрин Іншими використовуваними інгібіторами ацетилхолінестерази є, наприклад, ривастигмін (SDZENA-713) галантамш, метрифонат, ептастигмін, велнакрин, фізостигмін [Drugs, 53 (5), 752 - 768 (1997), Покажчик фірми Мерк, 12-е видання] Крім того, іншими інгібіторами ацетилхолінестерази є 5,7-дипдро-3-[2-[1-(фенілметил)-4піперидиніл]етил]-6Н-піроло[3,2,1]-1,2бензизоксазол-6-он, називаний також ікопезилом [J Med Chem , 38, 2802 - 2808 (1995)], MDL-73 745 або зіфросилоном [Eur J Pharmacol , 276 93 - 99 (1995)], TAK-147 [J Med Chem, 37, 2292 2299(1994)] До інших інгібіторів ацетилхолінестерази належать, наприклад, такі, що їх описано в заявці на патент Японії 09-095483, міжнародних заявках 97/13754, 97/21681, 97/19929, заявці на патент Південно-Африканської Республіки 96-04565, патенті США 5 455 245, міжнародній заявці 95-21 822, заявці на європейський патент 637 586, патенті США 5 401 749, заявці на європейський патент 742 207, патенті США 5 547 960, міжнародних заявках 96/20176 і 96/02524, заявці на європейський патент 677 516, заявках на патент Японії 07188177 і 07-133274, заявках на європейський патент 649 846 і 648 771, заявці на патент Японії 07048370, патенті США 5 391 553, міжнародній заявці 94/29272, заявці на європейський патент 627 400 12 11 52707 Згідно З наступним аспеїсгом, цей винахід стозвичайними фармацевтичними носіями ВІДПОВІДНІ сується фармацевтичної композиції, що містить як одноразові лікарські форми містять у собі форми активні агенти сполуку формули (І) і агоніст рецепдля перорального введення, такі як таблетки, при тора М-і, або їх фармацевтично прийнятні солі необхідності ПОДІЛЬНІ, желатинові капсули, порошки, гранули і розчини або оральні суспензії, форми Агоністами рецептора Мі є, наприклад, міладля під'язикового І трансбукального введення, фомелін, бесипіридин, талсаклідин, ксаномелін, YMрми для підшкірного, внутрішньом'язового або 796 і YM-954 [Eur J Pharmacol, 187 479 - 486 внутрішньовенного введення, форми для локаль(1990)], 3-[І\І-(2-діетиламіно-2-метилпропіл)-6ного введення і форми для ректального введення феніл-5-пропіл]піридазинамш, називаний також SR-46559 (Biorg Med Chem Let, 2, 833 - 838 Коли приготовляють тверду композицію у ви(1992)], AF-102, CI-979, L-689 660, LU 25-109, Sгляді таблеток, головний активний компонент змі9977-2, SB 202 026, тюпілокарпін, WAL 2014 шують з фармацевтичним інертним наповнюва[Pharmacol Toxicol , 78, 59 - 68 (1996)] чем, таким як желатин, крохмаль, лактоза, стеарат магнію, тальк, гуміарабік або аналогічні продукти ВІДПОВІДНО ДО ІНШОГО аспекту, винахід стосуТаблетки покривають сахарозою або іншими приється фармацевтичної композиції, що містить як датними для цього речовинами, або їх можна таактивні агенти сполуку формули (І) і холіноміметикож обробляти таким чином, щоб вони мали тричний агоніст, або їх фармацевтично прийнятні совалу або уповільнену активність і безперервно лі вивільнювали попередньо задану КІЛЬКІСТЬ активОптимальними холіноміметичними агоністами ного агента є, наприклад, МКС-231 [Biorg Med Chem Let, 5 (14), 1495-1500 (1995)], T-588 [Japan J Pharmacol , Препарат у вигляді желатинових капсул приго62, 81-86 (1993)], ABT-418 (Br J Pharmacol , 120, товляють шляхом змішування активного компоне429-438(1997)] нта з розріджувачем і введення одержаної суміші в м'які або тверді желатинові капсули Згідно З наступним аспектом, винахід стосується фармацевтичної композиції, що містить як Препарат у вигляді сиропу або еліксиру місактивні агенти сполуку формули (І) і антагоніст тить активний компонент разом з підсолоджуварецепторів NMDA, або їх фармацевтично прийнячем, переважно безкалорійним, метилпарабеном тні солі та пропілпарабеном як антисептиками, а також із речовиною, що покращує смак, і з ВІДПОВІДНИМ баКращим антагоністом рецепторів NMDA є, нарвником приклад, мемантин [Arzneim Forsch, 41_, 773780(1991)] Порошки або гранули, дисперговані у воді, міВІДПОВІДНО ДО ІНШОГО аспекту, винахід стять активний компонент у суміші з диспергатостосується фармацевтичної композиції, що містить рами або зволожувачами, або агентами, що ствояк активні агенти сполуку формули (І) і ноотропний рюють суспензію, такими як полівшілпіролідон, а засіб, або їх фармацевтично прийнятні солі також з підсолоджувачами або з речовинами, що покращують смак До ноотропних засобів, що їх використовують згідно з цим винаходом, належать, наприклад, Для ректального уведення використовують сунетирацетам, небрацетам (Покажчик фірми Мерк, позиторії, що їх приготовляють з використанням 12-е видання) зв'язувальних речовин, які плавляться при температурі прямої кишки, таких як олія какао або поліДози двох асоційованих активних агентів заетиленгліколі звичай вибирають з доз, які призначалися б для введення кожного лікарського засобу у разі не Для парентерального уведення використовукомбінованого, а окремого лікування ють водні суспензії, сольові розчини і стерильні розчини для ІН'ЄКЦІЙ, ЩО МІСТЯТЬ фармакологічно Згідно З наступним аспектом, цей винахід стоприйнятні диспергатори та/або зволожувачі, такі як сується також способу лікування старечого недопропіленгліколь або бутиленгліколь умства типу хвороби Альцгеймера, що полягає у введенні в організм пацієнта, який страждає на це Активний агент також може бути перетворений захворювання, ефективної дози сполуки формули у лікарську форму у вигляді мікрокапсул, за необ(І) або одної з и фармацевтичне прийнятних солей хідністю, разом з одним або кількома носіями або і ефективної дози сполуки, показаної для симптодобавками матичного лікування DAT, або одної з и фармацеУ фармацевтичних композиціях згідно з цим втично прийнятних солей, при цьому вищезгадані винаходом активний агент також може знаходивведення є одночасними, послідовними або розтись у вигляді комплексу - включення у циклодексподіленими в часі, а ефективні дози активних агетринах, їх простих ефірах або естерах нтів містяться в окремих одноразових лікарських Наведені далі за текстом приклади докладно формах або, коли активні агенти призначають оділюструють винахід, проте, не обмежуючи його ночасно, два активних агенти В(Оптимальному ваоб'єму ріанті містяться в єдиній фармацевтичній формі Приклад 1 У фармацевтичних композиціях цього винахо1[2-(3,4-Діетилфеніл)етил]-4-(3ду для перорального, під'язикового, підшкірного, трифторметилфеніл)-1,2,3,6внутрішньом'язового, внутрішньовенного, крізьштетрапдропіридинпдрохлорид кірного або ректального уведення в організм тва1а) 1-Бром-2-(3,4-діетилфеніл)етан рини і людини з метою лікування вищезгаданих Суміш 4,4г (О.ОЗЗмоль) 3,4-діетилбензолу, захворювань активний агент вводять у одноразо50мл дихлорметану, 8,8г (0,044моль) бромацетилвих лікарських формах, або у чистому вигляді, броміду охолоджують до температури 0 - 5°С і наприклад, у люфілізованій формі, або у суміші зі додають до неї 5,0г (0,037моль) трихлориду алю 14 13 52707 МІНІЮ Перемішують при температурі 0 - 5°С протярозчинник випарюють в умовах зниженого тиску гом одної години, після цього залишають відстоюОдержують 1,35г цільового продукту ватися протягом ночі при кімнатній температурі 26) 1-Бром-2-(3-метил-4-пентилфеніл)етан і 1Виливають у суміш води з льодом, екстрагують бром-2-(4-метил-3-пентилфеніл)етан дихлорметаном, органічну фазу сушать над сульСуміш 1,17г (0,0054моль) одержаного в попефатом натрію і розчинник випарюють в умовах редній стадії продукту з 0,62мл (0,0072моль) брозниженого тиску 2,9г (0,011 моль) одержаної олії мацетилброміду охолоджують до температури 0 змішують із бмл (0,079моль) трифтороцтової кис5°С і додають до неї 0,81 (О.ООбмоль) трихлориду лоти і 6,7мл (0,057моль) тріетилсилану і нагріваалюмінію Перемішують при температурі 0 - 5°С ють при температурі 80°С протягом чотирьох гопротягом одної години і після цього при кімнатній дин Після ЦЬОГО додають насичений водний температурі протягом чотирьох годин Виливають розчин гідрокарбонату натрію до одержання оснона лід, розділяють на дві фази, органічну фазу вного значення рН, екстрагують діетиловим ефіпромивають водою, сушать її і розчинник випарюром, органічну фазу сушать над сульфатом натрію ють в умовах зниженого тиску Залишок розчиняі розчинник випарюють в умовах зниженого тиску ють у 2,9мл трифтороцтової кислоти і додають Одержану у такий спосіб сиру олію очищають туди 3,1мл (0,0267моль ) тріетилсилану і суміш шляхом хроматографічної обробки на силікагеленагрівають при температурі 80°С протягом 5 говій колонці, використовуючи як елюент циклогекдин Виливають у водний розчин гідрокарбонату сан Одержують цільову сполуку натрію і екстрагують діетиловим ефіром Екстракт промивають водою, сушать над сульфатом на16) 1-Г2-(3,4-Діетилфеніл)етил1-4-(3трію Одержують суміш цільових сполук трифторметилфеніл)-1,2,3,6 тетрапдропіридинпдрохлорид Суміш 2,6г (0,001 моль) 4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридину, 60мл бутанолу, 4,1г (0,025моль) розтертого безводного карбонату калію і 2,6г (0,001 ІЗмоль) одержаного у попередній стадії продукту кип'ятять з використанням зворотного холодильника протягом 5 годин Розчинник випарюють в умовах зниженого тиску, залишок обробляють етилацетатом, органічну фазу промивають водою, сушать над сульфатом натрію і розчинник випарюють в умовах зниженого тиску Гідрохлорид утвореної у такий спосіб олії одержують шляхом обробки насиченим розчином соляної кислоти в ізопропанолі Одержують 1,6г цільової сполуки Т пл становить 220 222°С Приклад 2 1-Г2-(3-Метил-4-пентилфеніл)етил1-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридин і 1Г2-(4-метил-3-пентилфеніл)етил1-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридин та їх оксалати 2а) 1-Метил-2-пентилбензол До розчину 50мл (0,1 моль) 2М розчину нбутилмагнійхлориду у тетрапдрофурані у азотній атмосфері по краплинах додають 4,7г (0,035моль) фталевого альдегіду Суміш спонтанно нагрівають до температури 40 - 45°С Перемішують при кімнатній температурі протягом одної години, виливають у насичений розчин хлориду амонію Екстрагують діетиловим ефіром, екстракт промивають водою, сушать над сульфатом натрію і розчинник випарюють в умовах зниженого тиску Одержану у такий спосіб олію очищають шляхом хроматографічної обробки на силікагелевій колонці, використовуючи як елюент суміш циклогексан/етилацетат = 7/3 Виділяють продукт з більш високим показником Rf Одержують 2,0г олії Сирий продукт реакції розчиняють у 25мл етанолу і додають 1мл концентрованої сірчаної кислоти і 0,15г 10%-ного паладію на вугіллі Гідрують при кімнатній температурі протягом 7 годин Каталізатор відфільтровують, розчинник випарюють в умовах зниженого тиску і залишок обробляють етилацетатом Промивають водним розчином гідрокарбонату натрію, сушать і 2 в) 1 -Г2-(3-Метил-4-пентилфеніл)етил1-4-(3трифтрометилФеніл)1,2,3,6-тетрапдропіридин і 1Г2-(4-метил-3-пентилфеніл)етил1-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридин та їх оксалати Суміш 0,7г (0,0031 моль) 4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридину, 16мл бутанолу, 0,9г (0,0065моль) розтертого безводного карбонату калію й одержаного у попередній стадії продукту (у теоретично розрахованій КІЛЬКОСТІ 0,0054моль) кип'ятять з використанням зворотного холодильника протягом 6 годин Розчинник випарюють в умовах зниженого тиску, обробляють етилацетатом, органічну фазу промивають водою, сушать над сульфатом натрію, і розчинник випарюють в умовах зниженого тиску Одержану у такий спосіб олію очищають шляхом хроматографічної обробки на силікагелевій колонці, використовуючи як елюент суміш циклогексан/етилацетат = 7/3 Виділяють два продукти зі схожими значеннями Rf Продукт з більш високим значенням Rf відповідає 1-[2-(3-метил-4-пентилфеніл)-етил]-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридину Оксалат одержують в ацетоні Одержують 0,12г продукту Т пл становить 140 - 143°С Продукт з меншим значенням Rf відповідає ізомеру 1-[2-(4метил-3-пентилфеніл)етил]-4-(3трифторметилфеніл)-1,2,3,6-тетрапдропіридину Оксалат одержують в ацетоні Продукт кристалізують з ацетону Одержують 0,08г продукту Т пл становить 167- 169°С Приклад З 1-[2-(3,4-Діетилфеніл)етилН6-хлорпірид-2-іл)1,2,3,6-тетрапдропіридинпдрохлорид За) Н-Бензил-1,2,3,6-тетрагідропірид-4іл)трибутилстанан При кімнатній температурі протягом трьох годин перемішують суміш 15,85г (0,0837моль) 1бензил-4-піперидону в 140мл безводного диметоксіетану і 25г (0,0837моль) трисиліл гід разину в 140мл безводного диметоксіетану Розчинник випарюють в умовах зниженого тиску Залишок обробляють за допомогою 420мл безводного гексану і додають туди 420мл безводного тетраметилети 16 15 52707 лендіамшу Суміш охолоджують до температури Приклади 4 -13 78°С і по краплинах додають до неї 156мл нДотримуючись способу, описаного у Прикладі бутиллітію (0,25моль) (1,6М розчин у гексані) Че2, але використовуючи ВІДПОВІДНИЙ галогенід магрез приблизно ЗО хвилин суміш залишають віднію, одержують такі сполуки стоюватися до підвищення температури до 0°С і 1-[2-(3-етил-4-метилфеніл)етил]-4-(3перемішують протягом 15хв Після ЦЬОГО ДО реактрифторметилфеніл)-1,2,3,6-тетрапдропіридин ційної суміші додають 45мл (0,167моль) трибутил(Приклад 4), стананхлориду Через 1 годину дуже обережно 1-[2-(4-етил-3-метилфеніл)етил]-4-(3додають суміш води з льодом Екстрагують діетитрифторметилфеніл)-1,2,3,6-тетрапдропіридин ловим ефіром, органічну фазу промивають водою, (Приклад 5), сушать над сульфатом натрію і розчинник випа1-[2-(3-етил-4-пропілфеніл)етил]-4-(3рюють в умовах зниженого тиску Одержують 70г трифторметилфеніл)-1,2,3,6-тетрапдропіридин сирого продукту, який очищають шляхом хромато(Приклад 6), графічної обробки на силікагелевій колонці, вико1-[2-(4-етил-3-пропілфеніл)етил]-4-(3ристовуючи як елюент суміш циклогектрифторметилфеніл)-1,2,3,6-тетрапдропіридин сан/етилацетат = 95/5 Одержують цільову сполуку (Приклад 7), у вигляді олії 1-[2-(3-бутил-4-метилфеніл)етил]-4-(31 трифторметилфеніл)-1,2,3,6-тетрапдропіридин Н-ЯМР (CDCIs), 5(мд) 0,84 (м, 9М, СН3), (Приклад 8), 1,19-1,58 (м, 18Н, СН2-ланцюг), 2,31 (м, 2Н), 2,53 1-[2-(4-бутил-3-метилфеніл)етил]-4-(3(м, 2Н), 3,02 (м, 2Н), 3,56 (с, 2Н, бензильний метитрифторметилфеніл)-1,2,3,6-тетрапдропіридин лен), 5,76 (м *, 1Н), 7,18-7,41 (м, 5Н, ароматичні) Ч 1 1T7 Ч 1 11Q (Приклад 9), * смуги-сателіти J 4MC ( Н- Sn) і JMMC( Н - Sn) 1-[2-(3-ізобутил-4-метилфеніл)етил]-4-(336) 1 -бензил-4-(6-хлорпірид-2-іл)-1,2,3,6трифторметилфеніл)-1,2,3,6-тетрапдропіридин тетрапдропіридин (Приклад 10), 18,5г (0,04моль) одержаної у попередній стадії 1-[2-(4-ізобутил-3-метилфеніл)етил]-4-(3сполуки розчиняють у азотній атмосфері у 200мл трифторметилфеніл)-1,2,3,6-тетрапдропіридин безводного диметилформаміду До розчину дода(Приклад 11), ють 11,8г (0,08моль) 2,6-дихлорпіридину, 0,64г Pd 1-[2-(3-ізобутил-4-етилфеніл)етил]-4-(3(II) (Ph 3 P)2CI 2 , 4,38г (0,04моль) тетраметиламотрифторметилфеніл)-1,2,3,6-тетрапдропіридин нийхлориду і 2,76г (0,02моль) карбонату калію (Приклад 12), Нагрівають при температурі 110°С протягом 6 го1-[2-(4-ізобутил-3-етилфеніл)етил]-4-(3дин, після цього суміш виливають у 100мл 5%-ного трифторметил феніл )-1,2,3,6-тетрапдропіридин розчину сірчаної кислоти Екстрагують діетиловим (Приклад 13) ефіром, у водну фазу додають гідроксид амонію Приклад 14 до лужного значення рН і суміш екстрагують ети1-[2-(6-Метил-3-біфетпил)етил1-(3лацетатом Об'єднані органічні фази сушать над трифторметилфеніл)-1.2.3.6-тетрапдропіридин сульфатом натрію і розчинник випарюють в умоДотримуючись описаного у Прикладі 2 спосовах зниженого тиску Залишок очищають шляхом бу, але використовуючи феніллітій замість нхроматографічної обробки на силікагелевій колонбутилмагнійхлориду, одержують цільову сполуку ці, використовуючи як елюент суміш циклогекПриклад 15 сан/етилацетат = 1/1 1-Г2-(3,4-Диметилфеніл)етил1-4-(3Одержують цільову сполуку Т пл становить трифторметилфенілі-1,2,3,6100-102°С тетрапдропіридинпдрохлорид З в) 4-(6-хлорпірид-2-іл)-1,2,3,615а) 1-Бром-2-(3.4-диметилфеніл)етан тетрапдропіридинпдрохлорид 4,5г (О.ОЗмоль) 3,4-Диметилацетофенону в Розчин 7,0г (0,024моль) одержаної у попере12мл метанолу охолоджують до температури 0 дній стадії сполуки в 110мл дихлоретану охоло5°С і по краплинах додають туди 1,5мл (0,09моль) джують до температури 0 - 5°С і додають туди брому Перемішують при кімнатній температурі 5,8мл (0,054моль) хлоретилхлорформіату Перепротягом 24-х годин, після цього залишають відмішують протягом 5хв, після цього кип'ятять з вистоюватися протягом ночі при кімнатній темперакористанням зворотного холодильника протягом турі Метанол випарюють і суміш очищають шляпівтора годин Розчинник випарюють в умовах хом хроматографічної обробки на силікагелевій зниженого тиску, залишок обробляють ЮОмл меколонці, використовуючи як елюент суміш циклотанолу і кип'ятять з використанням зворотного гексан/етилацетат = 95/5 5,3г (0,013моль) одерхолодильника протягом 1 години Розчинник випажаного у такий спосіб продукта змішують із 12,5мл рюють, залишок обробляють ізопропанолом і тве(0,162моль) трифтороцтової кислоти і 18,7мл рду речовину відфільтровують Одержують цільо(0,011 моль) тріетилсилану і нагрівають при темпеву сполуку, яку кристалізують із 90%-ного етанолу ратурі 80°С протягом 1 години Після цього додаТ пл становить 305 - 307°С ють насичений водний розчин гідрокарбонату наЗг) 1-(2-(3,4-Діетилфеніл)етил1-4-(6-хлорпіридтрію до лужного значення рН, екстрагують 2-іл)-1.2.3.6-тетрапдропіридинпдрохлорид діетиловим ефіром, органічну фазу сушать над Дотримуються способу, описаного у Прикладі сульфатом натрію, і розчинник випарюють в умо16), але використовуючи одержаний у попередній вах зниженого тиску Одержують 5,2г цільової стадії продукт замість 4-(3-трифторметилфеніл)сполуки 1,2,3,6-тетрапдропіридину, одержують сполуку Т пл, становить 234 - 236°С цільову 18 17 52707 156) 1-Г2-(3,4-ДиметилФеніл)етил1-4-(3рахунок додавання соляної кислоти у присутності 0,7г 10%-ного паладію на вугіллі, нагріваючи при трифторметилфеніл)-1,2,3,6температурі 60°С протягом 8 годин Каталізатор тетрапдропіридинпдрохлорид відфільтровують, і у такий спосіб одержують 2,1г Суміш 1,8г (0,0068моль) 4-(3цільового продукту Т пл становить 247 - 251 °С трифторметилфеніл)-1,2,3,6-тетрапдропіридину, 25мл бутанолу, 2,4г (0,017моль) розтертого без166) 4-(2-Трифторметилфеніл01,2,3,6водного карбонату калію і 2г (0,0094моль) одержатетрапдропіридинпдрохлорид 2,0г (0,007моль) ного у попередній стадії продукту кип'ятять з викоодержаного у попередній стадії продукту розчиняристанням зворотного холодильника протягом 6 ють у 12мл льодяної оцтової кислоти До одержагодин Розчинник випарюють в умовах зниженого ного розчину по краплинах додають Змл конценттиску, залишок обробляють етилацетатом, органірованої сірчаної кислоти і нагрівають при чну фазу промивають водою, сушать над сульфатемпературі 100°С протягом двох годин Виливатом натрію і розчинник випарюють в умовах зниють на лід, до суміші додають концентрований женого тиску Продукт очищають шляхом розчин гідроксиду натрію до лужного значення рН і хроматографічної обробки на силікагелевій колонекстрагують дихлорметаном Органічну фазу суці, використовуючи як елюент суміш циклогекшать і розчинник випарюють в умовах зниженого сан/етилацетат = 7/3 Пдрохлорид одержаної у тиску Продукт обробляють 15мл ізопропанолу і такий спосіб олії одержують шляхом обробки наодержують 4-(2-трифторметилфеніл)-1,2,3,6сиченим розчином соляної кислоти в ізопропанолі тетрапдропіридину Пдрохлорид одержують за Одержують 1,1г цільової сполуки Т пл дорівнює допомогою розчину соляної кислоти в ізопропано270 - 272°С лі Одержують 0,9г цільової сполуки Т пл становить 213 - 215°С Приклад 16 1-Г2-(3,4-Діетилфеніл)етил1-4-(2трифторметилфеніл)-1 2,3,6тетрапдропіридинпдрохлорид 16а)4-Пдрокси-4-(2трифторметилфеніл)піперидинпдрохлорид 3,25 г (0,135 моль) магнію змішують із йодом у КІЛЬКОСТІ "на кінчику шпателя" і по краплинах додають туди розчин 30,4г (0,135моль) 2-бром-1тр и фтор метил бензол у в 125мл тетрапдрофурану Перемішують протягом 1 години при кімнатній температурі і до цієї суміші по краплинах додають 10,1г (0,041моль) бензилпіперидону Перемішують протягом 1 години при кімнатній температурі, і до суміші додають насичений розчин хлориду амонію Екстрагують діетиловим ефіром, органічну фазу сушать і розчинник випарюють в умовах зниженого тиску Продукт очищають шляхом хроматографічної обробки на силікагелевій колонці, використовуючи як елюент суміш циклогексан/етилацетат Одержують 6,8г 1-бензил-4-пдрокси-4-(2трифторметилфеніл)піперидину, який гідрують у 75мл 95%-ного етанолу при кислому значені рН за 16в) 1-Г2-(3,4-Діетилфеніл)етил1-4-(2трифторметилфеніл)-1,2,3,6тетрапдропіридинпдрохлорид 0,4г (0,0015моль) одержаного у попередній стадії продукту і 0,52г (0,0037моль) безводного карбонату калію в 12мл бутанолу кип'ятять з використанням зворотного холодильника протягом ЗОхв Після цього туди додають 0,41г (0,0017моль) одержаного у прикладі 1а) продукту і кип'ятять з використанням зворотного холодильника протягом 6 годин Розчинник випарюють, залишок обробляють етилацетатом, промивають водою, органічну фазу сушать і розчинник випарюють в умовах зниженого тиску Продукт очищають шляхом хроматографічної обробки на силікагелевій колонці, використовуючи як елюент суміш циклогексан/етилацетат = 8/2 У такий спосіб одержують 1-[2-(3,4-діетилфеніл)етил]-4-(2трифторметилфеніл)-1,2,3,6-тетрапдропіридин Пдрохлорид одержують за допомогою розчину соляної кислоти в ізопропанолі Одержують цільову сполуку Т пл становить 184 - 185°С ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійською1-phenylalkyl-1,2,3,6-tetrahydropyridines for alzheimers disease treatment
МПК / Мітки
МПК: A61K 31/444, C07D 211/70, C07D 401/04, A61K 31/4418, A61P 25/28
Мітки: композиція, фармацевтична, спосіб, хвороби, лікування, 1-фенілалкіл-1,2,3,6-тетрагідропіридини, одержання, альцгеймера
Код посилання
<a href="https://ua.patents.su/9-52707-1-fenilalkil-1236-tetragidropiridini-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya-dlya-likuvannya-khvorobi-alcgejjmera.html" target="_blank" rel="follow" title="База патентів України">1-фенілалкіл-1,2,3,6-тетрагідропіридини, спосіб їх одержання та фармацевтична композиція для лікування хвороби альцгеймера</a>
Попередній патент: Спосіб визначення ліпідних порушень у хворих на ішемічну хворобу серця та гіпертонічну хворобу
Наступний патент: Дифенілалкілтетрагідропіридини, спосіб їх одержання і фармацевтичні композиції, що їх містять
Випадковий патент: Індуктор для вирощування кристалів методом безтигельної зонної плавки












