Спосіб одержання залізовмісного коагулянту
Номер патенту: 19416
Опубліковано: 25.12.1997
Автори: Зареченний Володимир Григорович, Бубович Людмила Андріївна, Воробйова Інна Павлівна, Гелета Іван Аполлонович
Формула / Реферат
1. Способ получения железосодержащего коагулянта путем окисления сульфата железа (II) в сернокислом растворе в присутствии кислородсодержащего газа, отличающийся тем, что окисление сульфата железа (II) ведут в присутствии катализатора диоксида марганца при температуре 40-90°С, причем содержание свободной серной кислоты берут в избытке от стехиометрии, а мольное соотношение сульфата железа (II) к диоксиду марганца выдерживают в пределах 2:1.
2. Способ по п. 1, отличающийся тем, что мольное соотношение сульфата железа к свободной серной кислоте берут равным 1:1-1:1,5.
Текст
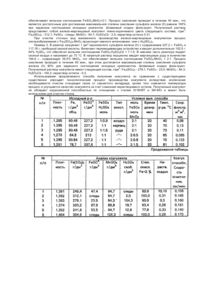
Настоящее изобретение относится к способу получения коагулянта из железосодержащего сернокислого раствора, которые применяются для очистки сточных вод и может быть использован в химической промышленности. Известен способ получения коагулянта путем окисления сульфата железа (II) в сернокислом растворе кислородсодержащим газом [1]. Указанный способ не позволяет получить коагулянт с высокими коагулирующими свойствами, так как процесс идет под давлением и при высокой температуре (более 500°С). Повышение температуры более 500°С резко интенсифицирует процесс окисления, но приводит к частичному разложению сульфата железа (III), в результате чего в готовом продукте повышается содержание нерастворимого остатка до 20%, а в газовую фазу выделяется сернистый ангидрид. Задачей настоящего изобретения является разработка такого способа получения коагулянта, в котором процесс окисления сернокислого раствора сульфата железа ведут в присутствии катализатора, диоксида марганца, что позволяет получить коагулянт с более высокими коагулирующими свойствами за счет снижения содержания нерастворимого осадка, а также упростить процесс в целом за счет исключения стадии очистки отходящих газов, снижения температуры и давления процесса окисления. Поставленная задача решается тем, что железоокисный коагулянт получают путем окисления сульфата железа (II) в сернокислом растворе в среде кислородсодержащего газа, в качестве которого используют сжатый воздух, в присутствии катализатора, диоксида марганца, при температуре 40-90°, причем содержание свободной кислоты берут в избытке от стехиометрии, например, 1:1-1:1,5 по отношению к сульфату железа, причем мольное соотношение сульфата железа (II) к диоксиду марганца выдерживают в пределах 2:1. В качестве диоксида марганца используется марганцовая руда. Способ осуществляется следующим образом. Водный сернокислый раствор сульфата железа (II), являющегося отходом производства двуокиси титана, закачивают в реактор, куда вводится расчетное количество серной кислоты для поддержания заданного соотношения 1:1:1,5. В реакционную смесь при непрерывном перемешивании вводят небольшими порциями расчетное количество диоксида марганца для обеспечения молярного соотношения FeSO4: МnО2 = 2:1. Температуру реакционной смеси устанавливают в пределах 40-90°С, что обеспечивает протекание процесса окисления сульфата железа (II) в течение 40-60 мин, при этом обеспечивают аэрирование реакционной смеси воздухом. При этом протекают следующие физико-химические процессы, Водный раствор сульфата железа (II) окисляется диоксидом марганца по суммарной реакции 2FeSO4 + 2H2SO4 + МnО2 =Fe2(SO4)3 + MnSO4 + 2H2O. Вследствие этого образуется раствор коагулянта содержащий сульфат железа (III) и сульфат марганца. Совместное присутствие в растворе коагулянта сульфата железа (III) и сульфата марганца способствует повышению коагуляционной способности за счет образования гидроокисных соединений железа и марганца в диапазоне рН обрабатываемой воды 4-8, которые сорбируют на своей поверхности загрязнения и осаждают их в донную фазу. Окисление сульфата железа (II) при молярном соотношении свободной серной кислоты менее 1 приводит к снижению степени окисления и образованию труднорастворимых соединений железа, что снижает массовую долю основного вещества - сульфат железа (III) в растворе коагулянта и повышает массовую долю нерастворимого остатка. Повышение молярного соотношения свободной серной кислоты более 1,5 затрудняет процесс окисления сульфата железа (II), степень окисления при этом снижается. Важным фактором в достижении максимальной степени окисления сульфата железа (II) является соблюдение заданного соотношения: FeSO4: МnО2 = 2:1. При полярном соотношении диоксида марганца меньше 1 степень окисления сульфата железа (II) снижается. Повышение соотношения более 1 нецелесообразно, так как приводит к увеличению нормы расхода диоксида марганца при неизменной степени окисления сульфата железа (II) (см. таблицу) Таким образом, выполнение способа позволяет снизить температуру процесса до 40-90°С, процесс осуществлять при атмосферном давлении, получать коагулянт с низким содержанием нерастворимого остатка. Пример 1. В лабораторный реактор, снабженный перемешивающим устройством, загружают 1 дм3 сернокислого раствора сульфата железа (II) с содержанием 227,7 г FeSO4 и 117,18 г свободной серной кислоты, что соответствует мольному соотношению FeSO4: H2SO4св = 1:0,8. Включают перемешивающее устройство и нагревают раствор до 40°С, в нижнюю часть реактора подают сжатый воздух. В нагретый раствор порционно вводят марганцовую руду в количестве 164,6 г, содержащую 39,5% МnО2, что обеспечивает мольное соотношение FeSO4: МnО2 = 2:1. Процесс окисления проводят в течение 60 мин, что является достаточным для достижения максимальной степени окисления сульфата железа (II) в сульфат железа (III) равном 80% при заданном соотношении исходных реагентов. Шламовый осадок, образующийся при разложении марганцовой руды, отделяют от раствора коагулянта методом фильтрации. Полученный продукт представляет собой раствор железо-марганцевого коагулянта темно-коричневого цвета со следующим содержанием компонентов, г/дм; Fe2(SO4)3 - 239,4; FeSO4 - 47,4; MnSO4 - 94,7; H2SO4Cb - Следы; нераствор.остаток - 10,1. Полученный по предлагаемому способу железо-марганцовый коагулянт не уступает по своему качеству выпускаемому промышленностью Al2(SO4)3 ГОСТ 12966-75. Результаты физико-химической очистки вод кожевенного производства с использованием АІ 2(SО4)3 дают меньшую скорость осветления (0,13 см/мин по сравнению с применением железо-марганцового коагулянта (см. таблицу). Кроме того, преимуществом железо-марганцового коагулянта при очистке сточных вод кожевенного производства заключается в том, что происходит химическое обезвреживание и удаление из воды серы сульфидной. Пример 2. В лабораторный реактор загружают 1 дм3 сернокислого раствора сульфата железа (II) с содержанием 227,2 г. FeSO4 и 117,18 г. свободной серной кислоты. Включают перемешивающее устройство и вводят дополнительное количество 29,3 г. 94% H2SO4, что обеспечивает мольное соотношение FeSO4 H2SO4Cb = 1:1. В нижнюю часть реактора подают сжатый воздух и нагревают раствор до 70°С. В нагретый раствор порционно вводят марганцовую руду в количестве 164,6 г., содержащую 39,5% МnО2, что обеспечивает мольное соотношение FeSO4:MnO2=2:1. Процесс окисления проводят в течение 40 мин., что является достаточным для достижения максимальной степени окисления сульфата железа (II) равном 100% при заданном соотношении исходных реагентов. Шламовый осадок фильтруют. Полученный раствор представляет собой железо-марганцовый коагулянт темно-коричневого цвета следующего состава, г/дм3: Fe2(SO4)3 - 312,1; FeSO4 - следы; MnSO4 - 94,7; H2SO4Cb - 2,5; нераствор.остаток 0,31. При очистке сточных вод кожевенного производства железо-марганцовым коагулянтом процесс хлопьеобразования с Fe2(SO4)3-MnO2 происходит намного интенсивнее, чем с Al2(SO4)3. Пример 3. В реактор загружают 1 дм3 сернокислого сульфата железа (II) с содержанием 227,2 г, FeSO4 и 117,18 г, свободной серной кислоты. Включают перемешивающее устройство и вводят дополнительно 102,5 г. 94% H2SO4, что обеспечит мольное соотношение FeSO4:H2SO4Cb = 1:1,5. В нижнюю часть реактора подают сжатый воздух и нагревают до 73 °С. В нагретый раствор порционно вводят марганцовую руду в количестве 164,6 г., содержащую 39,5% МnО2, что обеспечивает мольное соотношение FeSO4:MnO2 = 2:1. Процесс окисления проводят в течение 60 мин., при этом достигается максимальная степень окисления сульфата железа (II) 90% для заданного соотношения исходных компонентов. Шламовый осадок фильтруют. Полученный раствор коагулянта имеет следующий состав, г/дм3: Fe2(SO4)3 - 279,1; FeSO4 - 23,5; MnSO4 - 94,3; H2SO4Cb - 104,3; нераствор.остаток - 0,3. Использование предлагаемого способа получения коагулянта по сравнению с существующими существенно упрощает технологический процесс производства коагулянта вследствие исключения необходимости очистки отходящих газов от сернистого ангидрида, кроме того снижается температура процесс и улучшается качество коагулянта за счет снижения нерастворимого остатка. Полученный коагулянт не обладает коррозионной способностью по отношению к сталям IX18H9T и ЭИ-943 и может быть использован для очистки стоков.
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for obtaining iron-containing coagulant
Автори англійськоюVorobiiova Inna Pavlivna, Zarechennyi Volodymyr Hryhorovych, Heleta Ivan Apollonovych, Bubovych Liudmyla Andriivna
Назва патенту російськоюСпособ получения железосодержащего коагулянта
Автори російськоюВоробьева Инна Павловна, Зареченный Владимир Григорьевич, Гелета Иван Аполлонович, Бубович Людмила Андреевна
МПК / Мітки
МПК: C02F 1/52, B01D 21/01, C01G 49/14
Мітки: одержання, залізовмісного, коагулянту, спосіб
Код посилання
<a href="https://ua.patents.su/2-19416-sposib-oderzhannya-zalizovmisnogo-koagulyantu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання залізовмісного коагулянту</a>
Попередній патент: Спосіб повторного використання води в оборотному циклі водопостачання умовно-чистих вод
Наступний патент: Спосіб прокатування штаб
Випадковий патент: Стоянкове гальмо вагона