Похідні 6-заміщеної бензотіазоліл-2-оксамінової кислоти, які проявляють місцевоанестезуючу та діуретичну активність
Номер патенту: 57905
Опубліковано: 15.07.2003
Автори: Зубкова Ірина Вікторівна, Банний Іван Прокопович, Масалітін Микола Павлович, Черних Валентин Петрович, Березнякова Алла Іллівна
Формула / Реферат
Производное 6-замещенной бензотиазолил-2-оксаминовой кислоты формулы
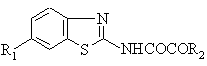
где при R1 - метил;
R2 - п-нитробензоилгидразино-, п-метоксибензилиденгидразино-, изопропилиденгидразино- или фурфурилиденгидразинорадикал, или при R1 - 2-диэтиламиноэтоксикарбонил, R2 - метокси- или этоксигруппа, проявляющие местноанестезирующую и диуретическую активность.
Текст
Изобретение относится к новым биологически активным химическим соединениям, а именно к производным 6-замещенной бензотиазолил-2-оксаминовой кислоты, проявляющим местноанестезирующую и диуретическую активность. Они могут найти применение в медицине в качестве препаратов комплексного действия - местноанестезирующего и ди уретического. Целью изобретения является выявление в ряду производных 6-замещенной бензотиазолил-2оксаминовой кислоты нового сочетания комплексного биологического действия. Пример 1. Получение п-нитробензолгидразида 6-метилбензотиазолил-2-оксаминовой кислоты (соединение І). К 2,5г (0,01 моль) гидразида-6-метилбензотиазолил-2-оксаминовой кислоты в 40мл ледяной уксусной кислоты добавляют 0,8г (0,01 моль) безводного ацетата натрия. Постепенно при перемешивании добавляют 1,86г (0,01 моль) хлорангидрида п-нитробензойной кислоты. Перемешивают при комнатной температуре еще 10 мин, затем слегка нагревают и оставляют на ночь. Осадок отфильтровывают, промывают водой и сушат. Выход 3,46г (87%). Пpимеp 2. Получение п-метоксибензилиденгидразида 6-метилбензотиазолил-2-оксаминовой кислоты (соединение 2). К раствору 2,5г (0,01 моль) гидразида 6-метилбензотиазолил-2-оксаминовой кислоты в 60мл ДМФА прибавляют 1,36г (0,01 моль) п-метоксибензальдегида (анисового альдегида). Смесь нагревают 20 мин и оставляют на 3 ч. За тем к раствору добавляют равный объем воды. Выпавший желтоватый осадок отфильтровывают и суша т. Вы ход 2,3г (62%). Кристаллизуют из водного ДМФА. Аналогично получают изопропилиденгидразид 6-метилбензотиазолил-2-оксаминовой кислоты (соединение 3) и фурфурилиденгидразид 6-метилбензотиазолил-2-оксаминовой кислоты (соединение 4). Пpимеp 3. Получение метилового эфира 6-(2-диэтиламиноэтоксикарбонил)-бензотиазолил-2-оксаминовой кислоты (соединение 5). К раствору 2,93г (0,01 моль) 2-амино-(2-диэтиламиноэтоксикарбонил)-бензотиазола в 40мл сухого ацетона прибавляют 0,79г (0,01 моль) пиридина. К раствору при 0C и тщательном, перемешивании в течение 30 мин прибавляют раствор 1,35г (0,011 моль) метоксалилхлорида в 20мл сухого ацетона. Реакционную смесь перемешивают еще 10 мин при 10°C. Выпавший осадок отфильтровывают и сушат. Вы ход 2,84г (75%). Кристаллизуют из метанола. Аналогично, только используя переосаждение ацетоном из метанола, получают этиловый эфир 6-(2диэтиламиноэтоксикарбонил)бензотиазолил-2-оксаминовой кислоты (соединение 6). Соединение 1 - желтоватое кристаллическое соединение, растворимое в уксусной кислоте, ДМФА, ДМСО, нерастворимое в воде и спирте. Соединения 2 - 4 - бесцветные или светло-желтые кристаллические вещества, растворимые в ДМФА, ДМСО, нерастворимые в воде, спирте. Соединения 5 и 6 - бесцветные кристаллические вещества, растворимые в воде, спирте, плохо растворимые в ацетоне. Строение полученных соединений подтверждено данными элементного анализа и ИК-спектров, индивидуальность контролируют методом тонкослойной хроматографии. Физико-химические характеристики соединений 1 - 6 приведены в табл. 1. Изучение фармакологической активности производных 6-замещенной бензотиазолил-2-оксаминовой кислоты. Исследование местноанестезирующей активности проводили на лягушках обоего пола весом 45 - 47г. Анестезию у лягушек с интактной центральной нервной системой вызывали путем аппликации седалищного нерва ватным тампоном, который пропитывали раствором соединения из расчета 25мг/кг массы животного. У животных препарировали седалищный нерв на уровне верхней трети бедра, затем в этом месте производили аппликацию ватным тампоном шириной 0,5см, который смачивали раствором соединения. По отсутствию общей дви гательной реакции при раздражении проксимальной точки, т.е. на участке выше наложения тампона определяли нарушение проводимости по афферентным волокнам седалищного нерва. О местноанестезирующей активности судили по времени отсутствия общей двигательной реакции при раздражении проксимальной точки. Параллельно исследовали местно-анестезирующую активность новокаина. Всего поставлено 32 опыта. Мочегонные свойства соединений 1 - 6 изучали на 18 - 30 белых мышах массой 18 - 20г, которым внутрижелудочно вводили исследуемое вещество в дозе, эквимолекулярной дозе дихлотиазида, в которой он проявляет максимальный диуретический эффект (50мг/кг),т.е. в дозах соответственно 67, 61, 49, 55, 64 и 66мг/кг массы животного. Вещества вводили на фоне водной нагрузки 1мл. Одновременно с этим другая группа животных получала дихлоазид в дозе 50мг/кг при той же водной нагрузке. Объем мочи, выделенной животными за 5 ч, служил показателем мочегонной активности исследуемого соединения и эталонного препарата. Полученное количество мочи как за каждый час, так и за весь опыт, пересчитывали на 100г массы животного. Контролем служили животные, не получавшие исследуемого соединения. Остр ую токсичность синтезированных соединений и эталонных препаратов изучали на белых мышах массой 15 - 20г. Исследуемые вещества вводили внутрибрюшинно в дозе 100, 200, 500, 1000, 1500, 2000 и 2500мг/кг. На каждую дозу брали 6 мышей, за которыми вели наблюдение в течение суток. Всего было поставлено для разных соединений от 72 до 186 опытов. Результаты всех испытаний приведены в табл. 2. Таким образом, соединения 1 - 6 обладают двумя видами фармакологической активности (местноанестезирующей и диуретической), что значительно расширяет возможность их применения в медицинской практике. Соединения 1 - 6 по местноанестезирующему действию соответственно в 6, 7,7, 13,3, 1,9, 5 и 16 раза активнее новокаина. При этом их острая токсичность в 8,05, 9,4, 7,8, 5,3, 1,4, и 2,1 раза соответственно меньше, чем у новокаина. По диуретическому действию синтезированные соединения в 1,8, 4,0, 2,2, 3,2, 1,4 и 1,1 раза активнее дихлотиазида. При этом их токсичность ниже, чем у дихлотиазида в 1,4 (1), 17, (2) и 1,4 (3) раза, соединение 4 по острой токсичности равно дихлотиазиду, а токсичность соединений 5 и 6 превышает токсичность дихлотиазида. Соединения 1 - 6 не являются производными п-аминобензойной кислоты как новокаин, что не создает противопоказаний к его совместному применению с сульфаниламидными препаратами. Высокая активность соединений 1-6 как местноанестезирующих и ди уретических средств делает перспективным создание их на основе высокоэффективных местных анестетиков с диуретическим эффектом, которые могли бы использоваться при патологических процессах, сопровождающихся отечностью тканей с болевым синдромом.
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of 6-substituted benzothiazolyl-2-oxaminic acid having local anesthetic and diuretic activity
Автори англійськоюChernykh Valentyn Petrovych, Bannyi Ivan Prokopovych, Berezniakova Alla Illivna
Назва патенту російськоюПроизводные 6-замещенной бензотиазолил-2-оксаминовой кислоты, проявляющие местноанестезирующую и диуретическую активность
Автори російськоюЧерных Валентин Петрович, Банный Иван Прокопович, Березнякова Алла Ильинична
МПК / Мітки
МПК: A61P 23/02, A61K 31/428, C07D 277/82, A61P 7/10
Мітки: 6-заміщеної, проявляють, місцевоанестезуючу, бензотіазоліл-2-оксамінової, активність, діуретичну, похідні, кислоти
Код посилання
<a href="https://ua.patents.su/2-57905-pokhidni-6-zamishheno-benzotiazolil-2-oksaminovo-kisloti-yaki-proyavlyayut-miscevoanestezuyuchu-ta-diuretichnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Похідні 6-заміщеної бензотіазоліл-2-оксамінової кислоти, які проявляють місцевоанестезуючу та діуретичну активність</a>
Попередній патент: Гідразиди бензотіазоліл-2-оксамінових кислот, які проявляють протизапальну та анальгетичну активність
Наступний патент: Моноетаноламід n-(6-метоксибензотіазоліл-2)-сукцинамінової кислоти, який проявляє гепатозахисну активність
Випадковий патент: Легкозбірна будівля для утримання корів






