Похідні n-арилгідразину, спосіб їх одержання, спосіб пригнічення комах та композиція для пригнічення комах
Номер патенту: 35563
Опубліковано: 16.04.2001
Автори: Хант Девід Аллен, Кун Девід Джордж, Гроностайскі Сінтіа Емма, Ферч Джозеф Августус, Л'ю Альберт Чін
Формула / Реферат
1. Производные N-арилгидразина общей формулы:
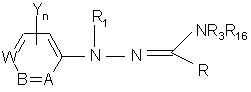 ,
,
где А представляет С-R4; В представляет C-R5; W представляет C-R6; Y представляет галоген, водород; n равно целому числу из 0,1 или 2;
R представляет С1-С10алкил, необязательно замещенный одним-тремя галогенами, фенилом, необязательно замещенным одним-тремя галогенами;
С3-С12 циклоалкил, необязательно замещенный одним или более галогенами,
С1-С6-алкилом, фенилом, необязательно замещенным одним-тремя галогенами;
R1 представляет водород;
R3 и R16 независимо друг от друга представляют водород, С1-С10алкил, необязательно замещенный одним или более галогенами, R10, R11, пиридилом, фенилом, необязательно замещенным одним или более галогенами; С3-С10алкенил, С3-С12-циклоалкил, необязательно замещенный галогеном; фенил, необязательно замещенный галогеном или галоген- С1-С10-алкоксигруппой; или фурфурил; или
R3 и R16 взятые вместе с атомом азота образуют кольцо, представленное структурой
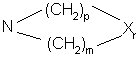 ;
;
R4, R5, R6 независимо друг от друга представляют собой водород, галоген, С1-С6-галогеналкил, при условии, что R4 и один из R3 или R16 являются отличными от водорода,
R10 представляет NR12R13,
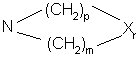 ,
, 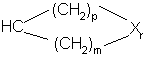 ;
;
R11 представляет
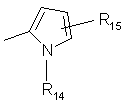 ,
,
R12, R13, R14, R15 независимо друг от друга представляют водород, С1-С4алкил;
Х представляет O или NR14,
r означает 0 или 1,
р и m независимо друг от друга равны целому числу 1 или 2, при условии, что сумма р+m+r должна быть равна 4 или 5, в качестве инсектицидных средств.
2. Соединение по п. 1, имеющее структурную формулу:
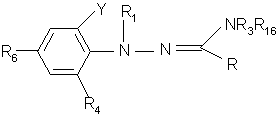 ,
,
где R представляет С1-С10-алкил;
R1 представляет водород;
R1 представляет С1-С10-алкил, фенил, необязательно замещенный галогеном или галоген С1-С10-алкоксигруппой; или фурфурил;
R16 представляет водород, С1-С10-алкил;
R4, R6 независимо друг от друга представляют водород, галоген, С1-С6-галогеналкил;
Y представляет галоген, водород, при условии, что R4 должен быть отличен от водорода.
3. Соединение по п. 2, представляющее собой N-этил-2,2-диметилпропионамид, 2-(2,6-дихлор-α, α, α-трифтор-р-толил)гидразон.
4. Способ получения соединения, имеющего структуру:
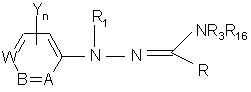 ,
,
где А, В, W, Y, n, R, R1, R3 и R16 имеют значения, определенные в п. 1, отличающийся тем, что соединение, имеющее структуру
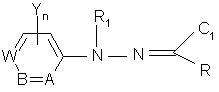 ,
,
подвергают взаимодействию с, по крайней мере, одним молярным эквивалентом амина формулы HNR3R16.
5. Способ подавления насекомых, включающий контактирование указанных вредителей или их корма, места обитания или размножения с производным гидразина, отличающийся тем, что в качестве производного гидразина используют соединение формулы (1)
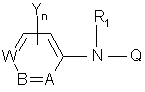 , (1)
, (1)
где А представляет C-R4 или N; В представляет C-R5; или N; W представляет C-R6 при условии, что когда все из А, В и W отличны от N, тогда R не может быть фенилом или замещенным фенилом; Y представляет галоген, n равно целому из 0,1 или 2, Q
представляет
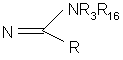 ,
, 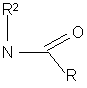 ;
;
R представляет С1-С10-алкил, необязательно замещенный одним или более галогенами, фенилом, необязательно замещенным одним-тремя галогенами;
С3-С12-циклоалкил, необязательно замещенный одним или более галогенами,
С1-С6-алкилом, фенилом;
фенил, необязательно замещенный одним или более галогеном;
R1 и R2 представляют водород;
R1 и R16 независимо друг от друга представляют водород, С1-С10-алкил, необязательно замещенный одним или более галогенами, CONR7R8, R10, R11, фенилом, необязательно замещенным одним или более галогеном, или пиридилом; фенил, необязательно замещенный галогеном или галоген-С1-С10-алкоксигруппой, или фурфурил, С3-С10-алкенил, С3-С12-циклоалкил, или
R3 и R16 могут, взятые вместе с атомом азота, образовывать кольцо, представленное структурой
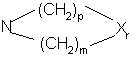 ;
;
R4, R5 и R6 независимо друг от друга представляют водород, галоген, С1-С6-галогеналкил;
R7, R8 независимо друг от друга представляют водород,
R10 представляет NR12R13,
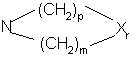 или
или 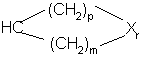 ;
;
R11 представляет
 ,
,
R12, R13, R14 и R15 каждый независимо представляет водород или С1-С4алкил;
Х представляет О или NR14, r представляет целое число из 0 или 1, р и m независимо каждый равны целому числу 1 или 2, при условии, что сумма р+m+r должна быть равна 4 или 5, его соли присоединения кислоты в пестицидно-эффективном количестве.
6. Способ по п. 5, отличающийся тем, что Q представляет
 .
.
7. Способ по п. 6, отличающийся тем, что А представляет C-R4, В представляет СН, Y представляет галоген, n равно 1, R4 и R6 независимо друг от друга представляют галоген или С1-С6-алкил, замещенный одним или более галогенами, и R, Р3 и R16 независимо друг от друга представляют водород или С1-С10-алкил.
8. Способ по п. 5, отличающийся тем, что Q представляет
 .
.
9. Способ по п. 8, отличающийся тем, что R представляет С1-С6-алкил, А представляет С-R4, В представляет C-R5, Y представляет галоген, n равно 1, R4 представляет водород, и R5 представляет С1-С6-алкил, замещенный одним или более галогенами.
10. Способ по п. 9, отличающийся тем, что соединение представляет собой 2,2-диметилпропионовую кислоту, 2-(2,6-дихлор-α, α, α-трифтор-р-толил)гидразин.
11. Композиция для подавления насекомых содержащая инертный жидкий или твердый носитель и производное гидразина, отличающаяся тем, что в качестве производного гидразина она содержит соединение формулы (1)
 , (1)
, (1)
где А, В, W, Y, n, R1 и Q определены в п. 5, при условии, что когда все из А, В и W отличны от N, то R не может быть фенилом или замещенным фенилом, в пестицидно-эффективном количестве.
12. Композиция по п. 11, отличающаяся тем, что соединение формулы (1) имеет структуру
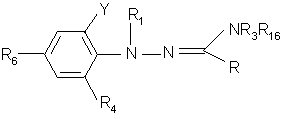
и R представляет C1-C10-алкил, R1 представляет водород, R3 представляет C1-C10-алкил, R16 представляет водород или C1-C10-алкил и R4, R6 и Y независимо друг от друга представляют водород, галоген, C1-C6-галогеналкил.
Текст
1. Производные N-арилгидразина общей формулы: геном или галоген-С1-С10-алкоксигруппой; или фурфурил; или R3 и R16 взятые вместе с атомом азота образуют кольцо, представленное структурой , где А представляет C-R4; В представляет C-R5; W представляет C-R6; Y представляет галоген, водород; n равно целому числу из 0, 1 или 2; R представляет С1-С10алкил, необязательно замещенный одним-тремя галогенами, фенилом, необязательно замещенным одним-тремя галогенами; С3-С12 циклоалкил, необязательно замещенный одним или более галогенами, C1-C6-алкилом, фенилом, необязательно замещенным одним-тремя галогенами; R1 представляет водород; R3 и R16, независимо друг от друга представляют водород, С1-С10 алкил, необязательно замещенный одним или более галогенами, R10, R11, пиридилом, фенилом, необязательно замещенным одним или более галогенами; С3-С10 алкенил, С3С12-циклоалкил, необязательно замещенный галогеном; фенил, необязательно замещенный гало R12, R13, R14, R15 независимо друг от друга представляют водород, С1-С4 алкил; Х представляет О или NR14, r означает 0 или 1, р и m независимо друг от друга равны целому числу 1 или 2, при условии, что сумма р+m+г должна быть равна 4 или 5, в качестве инсектицидных средств. 2. Соединение по п. 1, имеющее структурную формулу: , R4, R5, R6 независимо друг от друга представляют собой водород, галоген, C1-C6-галогеналкил, при условии, что R4 и один из R3 или R16, являются отличньми от водорода, R10 представляет NR12R13, (19) UA (11) 35563 (13) C2 R11, представляет 35563 где R представляет С1-С10-алкил; R1 представляет водород; R3 представляет С1-С10-алкил, фенил, необязательно замещенный галогеном или галоген С1-С10алкоксигруппой; или фурфурил; R16 представляет водород, С1-С10-алкил; R4, R6 независимо друг от друга представляют водород, галоген, C1-C6-галогеналкил; Y представляет галоген, водород, при условии, что R4 должен быть отличен от водорода. 3. Соединение по п. 2, представляющее собой Nэтил-2,2-диметилпропионамид, 2-(2,6-дихлор-a, a,a-трифтор-р-толил)гидразон. 4. Способ получения соединения, имеющего структуру: галогенами; С3-С12-циклоалкил, необязательно замещенный одним или более галогенами, С1-С6-алкилом, фенилом; фенил, необязательно замещенный одним или более галогеном; R1 и R2 представляют водород; R3 и R16 независимо друг от друга представляют водород, С1-С10-алкил, необязательно замещенный одним или более галогенами, CONR7R8, R10, R11, фенилом, необязательно замещенным одним или более галогеном, или пиридилом; фенил, необязательно замещенный галогеном или галогенС1-С10-алкоксигруппой, или фурфурил, С3-С10алкенил, С3-С12-циклоалкил, или R3 и R16 могут, взятые вместе с атомом азота, образовывать кольцо, представленное структурой , R4, R5 и R6 независимо друг от друга представляют водород, галоген, С1-С6-галогеналкил; R7, R8 независимо друг от друга представляют водород, R10 представляет NR12R13, где А, В, W, Y, n, R, R1, R3 и R16, имеют значения, определенные в п. 1, отличающийся тем, что соединение, имеющее структуру Yn R1 W N B A Cl или N , R11 представляет R подвергают взаимодействию с, по крайней мере, одним молярным эквивалентом амина формулы HNR3R16. 5. Способ подавления насекомых, включающий контактирование указанных вредителей или их корма, места обитания или размножения с производным гидразина, отличающийся тем, что в качестве производного гидразина используют соединение формулы (I) R12, R13, R14 и R15 каждый независимо представляет водород или С1-С4 алкил; Х представляет О или NR14, r представляет целое число из 0 или 1, р и m независимо каждый равны целому числу 1 или 2, при условии, что сумма р+m+г должна быть равна 4 или 5, его соли присоединения кислоты в пестицидно-эффективном количестве. 6. Способ по п. 5, отличающийся тем, что Q представляет , (І) где А представляет C-R4 или N; В представляет CR, или N; W представляет C-R6 при условии, что когда все из А, В и W отличны от N, тогда R не может быть фенилом или замещенным фенилом; Y представляет галоген, n равно целому из 0, 1 или 2, Q представляет 7. Способ по п. 6, отличающийся тем, что А представляет C-R4, В представляет СН, Y представляет галоген, n равно 1, R4 и R6 независимо друг от друга представляют галоген или C1-C6алкил, замещенный одним или более галогенами, и R, R3 и R16 независимо друг от друга представляют водород или С1-С10 алкил. 8. Способ но п. 5, отличающийся тем, что Q представляет R представляет С1-С10алкил, необязательно замещенный одним или более галогенами, фенилом, необязательно замещенным одним-тремя 2 35563 где А, В, W, Y, n, R1 и Q определены в п. 5, при условии, что когда все из А, В и W отличны от N, то R не может быть фенилом или замещенньм фенилом, в пестицидно-эффективном количестве. 12. Композиция по п. 11, отличающаяся тем, что соединение формулы (I) имеет структуру 9. Способ по п. 8, отличающийся тем, что R представляет C1-C6-алкил, А представляет C-R4, В представляет C-R5, Y представляет галоген, n равно 1, R4 представляет водород, и R5 представляет С1-С6-алкил, замещенный одним или более галогенами. 10. Способ по п. 9, отличающийся тем, что соединение представляет собой 2,2-диметилпропионовую кислоту, 2-(2,6-дихлор-a,a,a-трифтор-ртолил)гидразин. 11. Композиция для подавления насекомых содержащая инертный жидкий или твердый носитель и производное гидразина, отличающаяся тем, что в качестве производного гидразина она содержит соединение формулы (I) и R представляет С1-С10 алкил, R1 представляет водород, R3 представляет С1-С10-алкил, R16 представляет водород или С1-С10 алкил и R4, R6 и Y независимо друг от друга представляют водород, галоген, C1-C6-галогеналкил. , (I) Некоторые вредители из числа насекомых и клещей являются пагубными и наносят ежегодно громадные потери посевам сельскохозяйственных культур, хранимым продуктам и здоровью человека и животных. Целью данного изобретения является разработка замещенных производных Nарилгидразина, которые являются эффективными средствами контроля вредных насекомых и клещей. Другой целью данного изобретения является разработка способа защиты важных агрономических посевов от вреда и ущерба, наносимого насекомыми и клещами вредителяии. Дополнительной целью денного изобретения является разработка инсектицидных и акарицидных композиций. Настоящее изобретений касается разработки способа контроля за насекомыми и клещами, который включает контактирование указанных насекомых или клещей, или их корма, грунта, в котором они находятся, или их жилища с инсектицидно эффективным количеством производного Nарилгидразина формулы I W представляет C-R или N, при условии, что один из А, В или W должен быть отличен от N. Y представляет водород, галоген, CN, NO2, C1-C6алкил, C1-C6-галогеналкил, C1-C6-алкокси или, C1C6-галогеналкокси; n равно целому из 0, 1 или 2; Q представляет N X1 R , , ; R представляет водород, С1-С10-алкил, необязательно замещенный одним или более галогенами, С3-С6 циклоалкилом, С1-С4алкокси, С1-С4 галогеналкокси, (С1-С4 алкил)SОx, (С1-С4 галогеналкил)SОx, фенилом, необязательно замещенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4 галогеналкокси, (С1-С4 алкил)SОx, (С1-С4 галогеналкил)SОx, NO2 или CN группами, или фенокси, необязательно замещенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1С4 алкокси, С1-С4 галогеналкокси, (С1-С4 алкил) SОx, (С1-С4 галогеналкил)SОx, NO2 или CN группами. С3-С12 циклоалкил, необязательно замещенный одним или более галогенами, С1-С6 алкилом, С1-С6 галогеналкилом, С1-С4 алкокси, С1-С4 галогеналкокси, (С1-С4 алкил)SОx, (С1-С4 галогеналкил)SОx, фенилом, необязательно заме-щенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4 галогеналкокси, NO2 или CN группами, или фенокси, необя , (I) в которой А представляет C-R4 или N; B представляет C-R5 или N; 3 35563 более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, или пиридилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, или R3 и R16 могут вместе образовывать кольцо, представленное формулой зательно замещенным одним-тремя гало-генами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4 галогеналкокси, NO2 или CN группами или фенил, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4 галогеналкокси, NO2 или CN группами или фенил, необязательно замещенный одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1С4-галогеналкокси, NO2 или CN группами; R1и R2 независимо дрyг от дрyга представляют водород или С1-С4 алкил; R3 и R16- независимо друг от друга представляют водород, С1-С10 алкил, необязательно замещенный одним или более галогенами, гидрокси, С1-С4 алкокси, (С1-С4 алкил)SОx, CONR7R8, CO2R9, R10, R11, C3-С6 циклоалкилом, необязательно замещенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галоген-алкокси, NO2 или CN группами, фенилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, или пиридилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, С3-С10 алкенил, необязательно замещенный одним или более галогенами, гидрокси, С1-С4 алкокси, (С1-С4 алкил)SОx, CONR7R8, CO2R9, R10, R11, C3-С6 циклоалкилом, необязательно замещенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, фенилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, или пиридилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, С3-С10 алканил, необязательно замещенный одним или более галогенами, гидрокси, С1-С4 алкокси, (С1-С4 алкил)SОx, CONR7R8, CO2R9, R10, R11, C3-С6 циклоалкилом, необязательно замещенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, фенилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, или пиридилом, необязательно замещенным одним или более галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, С3-С12 циклоалкил, необязательно замещенный одним или более галогенами, гидрокси, С1-С4 алкокси, (С1-С4 алкил)SОx, CONR7R8, CO2R9, R10, R11, C3-С6 циклоалкилом, необязательно замещенным одним-тремя галогенами, С1-С4 алкилом, С1-С4 галогеналкилом, С1-С4 алкокси, С1-С4-галогеналкокси, NO2 или CN группами, фенилом, необязательно замещенным одним или , R4, R5 и R6 независимо друг от друга представляют собой водород, галоген, CN, NO2 (С1-С4 алкил)SОx, (С1-С4 галогеналкил)SОx, С1-С4 алкил, С1С4 галогеналкил, С1-С4 алкокси, С1-С4-галогеналкокси; R7, R8 и R9 независимо друг от друга представляют собой водород или С1-С4 алкил; R10 представляет Nr12R13 или , R11 представляет R12, R13, R14 и R15 каждый независимо представляет водород или С1-С4 алкил; Х1 представляет хлор, бром или фтор; Х представляет О, S или NR14; r равно целому, о или 1; p и m независисмо друг от друга равны целому числу, выбранному из 0, 1, 2 или 3, при условии, что только один из p, m или r может быть равен 0, и что сумма p+m+r должна быть равна 4, 5 или 6; х равно целому из 0, 1 или 2; или его солью присоединения кислоты, при условии, что когда Q представляет N X1 R , R представляет С1-С5 алкил, а Х1 представляет хлор, то либо по крайней мере один из А, В или W должен представлять N, либо R4, R5, R6 и Y должны быть отличными от водорода, и n должно быть равно 0, и при дополнительном условии, что, когда Q представляет R представляет фенил или земещенный фенил, а Х1 представляет хлор, то по крайней мере один из А, В или W должен представлять N. Кроме того, настоящее изобретение касается получения N-ариамидразонов формулы I, в которой А, В, W, Y, n и R1 имеют вышеуказанные значения, а Q представляет 4 35563 шеуказанные значения. Термин галоген, используемый в описании и формуле изобретения, означает хлор, фтор, бром или йод. Термин соли присоединения кислоты означает соли, образуемые кислотами, хорошо известными, такими как хлорид водорода, бромид водорода, биосульфат водорода, сульфат геми-водорода и т.л. В вышеуказанном опеределнии, когда n равно 0, то Y означает водород. Предпочтительными соединениями изобретения являются такие, в которых R, R3 и R16 независимо друг от друга представляют водород или С1-С6 алкил, А представляет С-R4, В представляет С-R5, W представляет C-R6, Y представляет галоген, и n равно 1. Особенно предпочтитетльными соединениями являются те, в которых R1 представляет водород, R4 представляет галоген, R5 представляет водород и/или R6 представляет С1-С6 алкил, замещенный одним или более галогенами, предпочтительно трифторметил. Другими предпочтитетльными соединениями изобретения являются соединения, имеющие структуру , при условии, что когда все А, В и W отличны от N, тогда R и один из R3 или R16 должны быть отличными от водорода, и при допольнительном условии, что, когда один из А, В или W представляет N, то Y, R4, R5 или R6 должны быть отличными от С1-С10 алкила. Также предусматриваются композиции и способы для защиты растущих растений от нападения и заражения насекомыми и клещами. Множество насекомых и клещей наносят большой экономический ущерб, повреждая и уничтожая посевы сельськохозяйственных культур и других ценных растений, содействуя распространению и росту бактерий, грибков, вирусов, которые приводят к болезням растений, и уничтожая или снижая ценность хранимых пищевых продуктов, других продуктов или имущества. Насекомые и клещи представляют некоторые из самых больших проблем фермеров во всем мире. Потребность в альтернативном и эффективном контроле насекомых и клещей является глобальной проблемой. Было обнаружено, что замещенные производные N-арилгидразоне формулы I являются особенно эффективными инсектицидными и акарицидными средствами, в частности, против Coleoptera, Lepidoptera и Acarina. Соединения амидразона формулы Ia настоящего изобретения имеют структурную формулу , в которой R представляет С1-С10-алкил; R1 представляет водород или С1-С4 алкил; R16 представляет водород или С1-С10-алкил; и R4, R6 и Y независимо друг от друга представляют водород, галоген, CN, NO2, С1-С6 алкил, C1-C6-галогеналкил, С1С6 алкокси, С1-С6-галогеналкокси. N-ариламидразоны формулы Iа можно получить путем взаимодействия хлорангидрида кислоты, гидразона (гидразиноил хлорид) форму-лы II с аминным соединением HNR3R16, как показано на схеме процесса I. , (Іа) в которой A, B, W, Y, n, R, R1, R3 и R16 имеют вы Соединения формулы II можно получить путем взаимодействия подходящего арилгидразина формулы III с соответствующим хлорангидридом кислоты, RCOCl для получения N-арилгидразина формулы IV и взаимодействия гидразида форму лы IV с галогенирующим агентом, таким как тионил галогенид, для получения желаемого продукта -N-арилгидразиноил галогенида фор-мулы II. Реакция показана на схеме процесса II. 5 35563 ставляет фтор, можно получить из соединений формулы II, в которых Х1 представляет хлор или бром, путем галогенообменной реакции, используя фторид натрия или фторид водорода, как это описывается Марчем в Advanced Organic Chemistry, 4 изд. (1992), стр. 438 Дополнительные соединения, используемые в способе изобретения, включают замещенные карбоновые кислоты, N-арилгидразиды формулы V. Инсектицидные и акарицидные N-аригидразиды формулы V настоящего изобретения имеют структурную формулу Замещенные производные N-арилгидразина настоящего изобретения являются эффективными для подавления вредителей-насекомых и клещей. Указанные соединения являются также эффективными для защиты растущих или убранных посевов сельскохозяйсственных культур от нападения и заражения такими вредителями. Соединения, используемые в предлагаемом способе, включают N-арилгидразиноил галогениды формулы II. Инсектицидные и акарицидные гидразиноил галогениды формулы II настоящего изобретения имеют структурную формулу Yn W R1 N B A Yn N W R B , (II) в которой A, B, W, Y, n, R, R1, и Х1 имеют вышеуказанные значения. Предпочтительными соединениями формулы II являются такие соединения, в которых R1 представляет водород, A представляет C-R4, B представляет C-R5, W представляет C-R6, Y представляет галоген или нитро, а n равно 1. Особенно предпочтительными являются соеди-нения, в которых R4 представляет галоген, R5 представляет водород, и R6 представляет C1-C6 алкил, замещенный одним или более галогенами, предпочтительно трифторметил. Другими предпочтительными соединениями формулы II являются соединения, в которых R представляет необязательно замещенный C3-C12 циклоалкил или C1-C10 галогеналкил, предпочтительно C1-C6 галогеналкил. Соедиения формулы II, в которых Х1 пред A R1 R2 N X1 N O R , (V) Предпочтительными соединениями формулы V являются такие соединения, в которых R представляет водород или C1-C6 алкил, A представляет C-R4, B представляет C-R5, W представляет C-R6, Y представляет галоген или нитро, а n равно 1. Особенно предпочтительными N-арилгидразидами формулы V являются такие, в которых R4 представляет галоген, R5 представляет водород, и R6 представляет C1-C6 алкил, замещенный одним или более галогенами, предпочтительно трифторметил. Соединения формулы V можно получить путем взаимодействия подходящего арилгидразина формулы IV с соответствующим хлорангидридом кислоты, RCOCl, с получением N-арилгидразида формулы V. Реакция показана на технологической схеме процесса III. 6 35563 Растущие или убранные посевы сельскохозяйственных культур можно защитить от инфицирования или атаки вредоносных насекомых или клещей путем нанесения на листву сельскохозяйственных культур, или на почву или воду, в которой они растут, пестицидно эффективного количества производного N-арилгидразина формулы I. На практике для защиты растений от нападения и заражения насекомыми и клещами обычно бывает эффективным примерно 10-10000 м.д., предпочтительно примерно 100-5000 ч/млн. соединения формулы I, диспергированного в жидком носителе, при нанесении на растения или на почву или воду, в которой они растут. Нанесение на почву соединений формулы I является особенно эффективным для контроля стадий послезародышевого развития Coleoptera и Diptera. Нанесение, такое как нанесение с помощью распыления, композиций изобретения обычно является эффективным при расходах, составляющих примерно 0,125250 кг/га. Конечно, предполагается, что в зависимости от преобладающих окружающих обстоятельств, таких как плотность популяции, степень заражения, стадия роста растений, почвенные условия, погодные условия и т.п., можно использовать более высокие или более низкие дозы расхода при нанесении производных N-арилгидразина. Предпочтительно использовать соединения формулы I вместе или в комбинации с другими средствами биологического и химического контроля, включающими другие инсектициды, нематици ды, акарициды, моллюскициды, фунгициды и бактерициды, такие, как нуклеарные вирусы полиэдроза, пирролы, арипирролы, галогенбензоилмочевины, пиретроиды, карбаматы, фосфаты и т.п. Обычными препаративными формами, пригодными для производных N-арилгидразина формулы I, являются гранулированные композиции, текучие композиции, смачиваемые порошки, дусты, микроэмульсии, эмульгируемые концентраты и т.п. Пригодными являются все композиции, которые приспособлены для нанесения на почву, воду и листву и обеспечивают эффективную защиту растений. Композиции изобретения включают производные N-арилгидразина формулы I, смешанные с инертным твердым или жидким носителем. Когда композиции изобретения необходимо применять в обработках в комбинации с другими биологическими или химическими средствами, композицию можно наносить в виде смеси компонентов, или можно наносить последовательно. Для более ясного понимания изобретения ниже приведены конкретные примеры осуществления изобретения. Эти примеры являются просто иллюстративными, и их не следует рассматривать никоим образом как ограничивающие объем и основополагающие принципы изобретения. Пример 1 Получение 2-(2,6-дихлор-a,a,a-трифтор-р-толил)гидразида 2,2-диметилпропионовой кислоты Раствор 2,6-дихлор-4-(трифторметил)фенилгидразина (50,0 г, 0,20 моль) в метиленхлориде обрабатывали по каплям триметилацетилхлоридом (30,6 г, 0,254 моль), перемешивали в течение 30 минут, обрабатывали 10% водным NaOH и перемешивали в течение 3 часов. Фазы разделяли: органическую фазу промывали водой, высушивали над MgSO4 и выпаривали in vacuo с получением не совсем белого остатка. Твердое вещество перекристаллизовывали из 1,2-дихлорэтана с получением указанного продукта в виде белого твердого вещества, 55 г (82% выход), точка плав ления 140-141ºС, идентифицировано с помощью спектральных анализов 1HNMR, 13CNMR, иYR. Примеры 2-42 Получение замещенных производных N-арилгидразина. При использовании по существу той же самой процедуры, что описана в вышеприведенном примере 1, и замене соответствующих арилгидразина и хлорангидрида кислоты, были получены соединения, приведенные в таблице 1, которые идентифицировали с помощью спектральных анализов 1 HNMR, 13CNMR, и YR. 7 35563 Таблица 1 Номер примера Example Number 2 Точка плавления °С A B W Yn R mp °С C-Cl СН С-СF3 6-Сl (СН3)2СНСН2 135-136 3 C-Cl СН C-Cl 6-Сl (СН3)3С 124-125,5 4 C-Cl СН CH 6-Сl (СН3)3С 114-115 5 C-Br СН С-СF3 6-Вг (СН3)3С 118-120 6 C-Br СН С-СF3 6-Вг СН3 173-175 7 C-Br СН С-СF3 6-Вг C6H5 181-184 8 C-CH3 СН C-Cl H (СН3)3С 103-106 9 C-Cl СН С-СF3 6-Сl (CH3)3CCH2 125-127 10 C-Cl СН C-Cl 6-Сl pClC6H4 183-190 11 C-Cl СН С-СF3 6-Сl (CH3)2CH 158-159 12 C-Cl СН C-Cl 6-Cl 186-188 13 C-Cl СН С-СF3 6-Cl cyclopropyl циклопропил CH3CH2C(CH3)2 121-123 14 C-H СН С-СF3 H (СН3)3С 136-139 15 C-Cl СН С-СF3 H (СН3)3С 143-145 16 C-Cl CH C-CF3 6-Cl 17 C-Cl C-Cl C-Cl 18 N CH C-CF3 5,6 - diCl 5,6 - диCl 6-Cl 19 C-Cl CH C-Cl 6-Cl 125-127 (СН3)3С (СН3)3С 151-151,5 138-140 20 C-Cl CH C-CF3 6-Cl pClC6H4OC(CH3)2 137-139 21 C-CF3 CH CH Н (СН3)3С 93-100 22 C-Cl CH C-CF3 6-Cl 23 C-Cl CH C-Cl 6-Cl 24 C-Cl CH C-CF3 25 C-Cl CH 26 C-Cl 27 C-Cl 101-103 3 6-Cl cyclohexyl циклогексил C6H5C(CH3)2 104-105 C-Cl 6-Cl CF3 CF2 131-132 CH C-Cl 6-Cl (CH3)2CH 164-165 CH C-CF3 6-Cl cyclopropyl циклопропил CH3CH2C(CH3)2 172-174 28 C-Cl CH C-Cl 6-Cl 29 C-Cl CH C-CF3 6-Cl 30 С-Вr CH C-CF3 6-Br (СН3)3С 31 C-Cl CH C-Cl 6-Cl CH3(CH2)5C(CH3)2 8 133-139 132-134 160-162 140-141 35563 Продолжение таблицы 1 Номер примера Точка плавления °С Example Number 32 A B W Yn R mp °С N N C-Cl H (СН3)3С 178-182 33 C-Cl CH C-CF3 6-Cl 121-123 34 C-Cl CH C-CF3 6-Cl pClC6H4C(CH3)2 105-107 35 C-Cl CH C-CF3 6-Cl CICH2C(CH3)2 119-120 36 C-Cl CH C-CF3 6-Cl 37 C-Cl CH C-Cl 6-Cl 174-175 CICH2C(CH3)2 124-125 38 C-Cl CH CH 5-CF3 (СН3)3С 170-177,5 39 C-Cl CH C-CF3 6-Cl 1-methylcyclohexyl 1-метилциклогексил (СН3)3С 105-107 158-160 (СН3)3С 154-157 (СН3)3С 118-120 40 CH C-CF3 CH Н 41 C-F C-F C-F 42 C-Br CH C-F 5,6 - diF 5,6 - диF 6-Br Таблица 2 Номер примера Точка плавления °С Example Number 44 A B W Yn R C-Cl СН C-CF3 6-Сl (СН3)2СНСН2 45 C-Cl СН C-Cl 6-Сl (СН3)3С 46 C-Cl СН СН 6-Сl C-Br СН C-F 6-Вг (СН3)3С 48 C-Br СН C-CF3 6-Вг СН3 49 C-Br СН C-CF3 6-Вг 44,5-45,5 (СН3)3С 47 mp °С C6C5 50 C-Cl CH C-Cl H (СН3)3С 51 C-Cl CH C-CF3 6-Cl (CH3)3CCH2 52 C-Cl CH C-Cl 6-Cl pClC6H4 53 C-Cl CH C-CF3 6-Cl (CH3)2CH 54 C-Cl CH C-Cl 6-Cl 55 C-Cl CH C-CF 6-Cl cyclopropyl циклопропил CH3CH2C(CH3)2 56 C-H CH C-CF3 H (СН3)3С 57 C-Cl CH C-CF H (СН3)3С 9 120 35563 Продолжение таблицы 2 Номер примера Точка плавления °С Example Number 58 A B W Yn C-Cl CH C-CF3 6-Сl 59 C-Cl C-Cl C-Cl R 60 N CH C-CF3 5,6 - diCl 5,6 - диСl 6-Сl 61 C-Cl CH C-C1 6-Сl 62 C-Cl CH C-CF3 6-Сl pClC6H4OC(CH3)2 63 C-CF3 CH CH H (СН3)3С 64 C-Cl CH C-CF3 6-Сl 65 C-Cl C-CH C-Cl 6-Сl mp °С (СН3)3С (СН3)3С 66 C-Cl C-CH C-CF3 6-Сl cyclohexyl циклогeксил C6H5C(CH3)2 67 C-Cl CH C-Cl 6-Сl CF3 CF2 68 C-Cl CH C-Cl 6-Сl (CH3)2CH 69 C-Cl CH C-CF3 6-Сl 70 C-Cl CH C-Cl 6-Сl cyclopropyl циклопропил CH3CH2C(CH3)2 71 C-Cl CH C-CF 6-Cl 110-111 72 C-Br CH C-CF3 6-Br (СН3)3С 73 C-Cl CH C-Cl 6-Cl CH3(CH2)5C(CH3)2 74 N N C-Cl H (СН3)3С 75 C-Cl CH C-CF3 6-Cl 76 C-Cl CH C-CF3 6-Cl pClC6H4OC(CH3)2 CICH2C(CH3)2 77 C-Cl CH C-CF3 6-Cl 78 C-Cl CH CCF3 6-Cl 79 C-Cl CH C-Cl 6-Cl CICH2C(CH3)2 80 C-Cl CH CH 5-CF3 (СН3)3С 81 C-Cl CH C-CF3 6-Cl 82 CH C-CF3 CH H 1-methylcyclohexyl 1-метилциклогексил (СН3)3С 71-73 83 CH CH CH 5-F (СН3)3С 84 С-Вr CH C-F 6-Br (СН3)3С 10 85-88 35563 Пример 43 Получение 1-хлор-2,2-диметилпропиональде гида зона 2-(2,6-дихлор-a,a,a-трифтор-р-толил)гидра Смесь 2,2-диметил-2-(2,6-дихлор-a,a,a-трифтор-р-толил)гидразид пропионовой кислоты (50,о г, 0,152 моль) и тионилхлорида (53,8 г, 0,452 моль) в толуоле нагревали при температуре дефлегмации в течение 8 часов, охлаждали до комнатной тампературы и выпаривали in vacuo с получением масляного остатка. Масло растворяли в гексанах и пропускали через осадок на фильтре из силикагеля. Осадок на фильтре промывали несколькими порциями гексанов. Фильтраты собирали и выпаривали in vacuo с получением указанного продукта в виде желтого масла, 47,2 г (90% выход), идентифицированного с помощью спектральных анализов 1Н ЯМР, 13С ЯМР и ИК. Примеры 44-84 Получение замещенных хлоридов N-арилгидразиноила. Используя по существу ту же процедуру, что и в примере 43, и заменяя соответстующие гидразидные основы, получали соединения, представленные в таблице 2, идентифицированные с помощью спектральных анализов 1Н ЯМР, 13С ЯМР и ИК. Пример 85 Получение N-этил-2,2-диметилпропионамида, 2-(2,6-дихлор-a,a,a-трифтор-р-толил)гидразона Раствор (2,6-дихлор-a,a,a-трифтор-р-толил)гидразон 1-хлор-2,2-диметилпропиональдегида (20,0 г, 0,0575 моль) в тетрагидрофуране обрабатывали по каплям 70% водным этиламином (28,0 г, 0,144 моль) при комнатной температуре, перемешивали в течение 1 часа и выпаривали in vacuo с получением полутвердого остатка. Полутвердное вещество диспергировали в эфире и воде. Фазы разделяли: органическую фазу промывали водой, высушивали над MgSO4 и выпаривали in vacuo с получением указанного продукта в виде желтого масла, 19,8 г (97% выход), идентифицированного с помощью спектральных анализов 1Н ЯМР, 13С ЯМР и ИК. Примеры 86-169 Получение замещенных N-ариламидразонов. Используя по существу ту же процедуру, что и в примере 85, и заменяя соответстующие гидразиноилхлорид и подходящий амин, получали соединения, представленные в таблице 3, которые идентифицировали с помощью спектральных анализов 1Н ЯМР, 13С ЯМР и ИК. Соли гидрохлорида изобретения можно полу чить в соответствии с процедурой, изложенной ниже. Пример 146 Получение N-этил-2,2-диметилпропионамида, 2-(2,6-дихлор-a,a,a-трифтор-р-толил)гидразона гидрохлорида 11 35563 Перемешиваемую смесь N-этил-2,2-диметилпропионамид, 2-(2,6-дихлор-a,a,a-трифтор-р-толил)гидразона (0,1 г, 2,8 моль) и гексана барботировали HCl газом в течение 30 минут. Полученн ную реакционную смесь фильтровали с получением указанного соединения в виде белого твердого вещества, 1,13 г, точка плавления 202-202,50С. Таблица 3 Точка плав ления °С Номер примера Example A Number 86 C-Cl B W Yn R R3 R16 CH C-CF3 6-Cl (СН3)3С pClC6H4 Н 87 C-Cl CH C-Cl 6-Cl (СН3)3С CH3CH2CH2 Н 88 C-Cl CH C-Cl 6-Cl (СН3)2СH CH3CH2CH2 Н 89 C-Cl CH C-CF3 6-Cl (СН3)3СCH2 CH3CH2CH2 Н 90 C-Cl CH C-Cl 6-Cl (СН3)2СH Н 91 C-Cl CH C-CF3 6-Cl (СН3)3СCH2 cyclopropyl циклопропил CH3CH2 Н 92 C-Cl СН C-CF3 6-Сl (СН3)2СH CH3CH2 Н 93 C-Cl СН C-CF3 6-Сl (СН3)3С CF3CH2 Н 94 C-Br СН C-CF3 6-Вг (СН3)3С CH3CH2 Н 95 C-Br СН C-CF3 6-Вг (СН3)3С CH3CH2CH2 mp °С Н 96 C-Br СН C-CF3 6-Вг (СН3)3С C6H5CH2 C-Br СН C-CF3 6-Вг (СН3)3С Н 98 C-Br CH C-CF3 6-Br CH3 furfuryl фурфуpил CH3CH2 62-64 Н 97 48-50 H 99 C-Br CH C-CF3 6-Br C6H5 CH3CH2 H 100 C-Cl CH C-Cl 6-Cl (СН3)3С H H 101 C-Cl CH C-Cl 6-Cl (СН3)3С CH3 CH3 102 C-Cl CH C-Cl 6-Cl (СН3)3С CH3CH2 H 103 C-Cl CH C-CF3 H (СН3)3С CH3CH2CH2 H 104 C-Cl CH CH 6-Cl (СН3)3С CH3CH2CH2 H 105 C-Cl CH C-CF3 6-Cl (СН3)3С H H 106 C-Cl CH C-CF3 6-Cl (СН3)3С CH3 H 107 C-Cl CH C-CF3 6-Cl (СН3)3С CH3 CH3 108 C-Cl CH C-CF3 6-Cl (СН3)3С CH3CH2CH2 C-Cl CH C-CF3 6-Cl (СН3)3С (СН3)3С H (СН3)2СHCH2 H 100102,5 7879,5 H 109 131135 61-63 110 C-Cl CH C-CF3 6-Cl (СН3)3С 111 C-Cl CH C-CF3 6-Cl (СН3)3С 12 -CH2CH2CH2CH2 67,568,5 35563 Продолжение таблицы 3 Номер примера Точка плав ления °С Example A Number 112 C-Cl 113 C-Cl B W Yn R R3 R16 CH C-Cl 6-Cl CH3CH2 H CH C-CF3 6-Cl cyclopropyl циклопропил CH3CH2C(CH3)2 CH3CH2 H (CH3)2CH H 114 C-Br CH C-CF3 6-Br (СН3)3С 115 C-Cl CH C-CF3 H (СН3)3С 116 C-Cl CH C-CF3 6-Cl CH3CH2C(CH3)2 CH3CH2 CH3CH2 117 C-Cl CH C-CF3 H (СН3)3С CH3CH2 mp °С 65-67 H -CH2CH2CH2CH2 118 C-Cl CH C-Cl 6-Cl CH3CH2C(CH3)2 CH3CH2 H 119 C-Cl CH C-CF3 6-Cl C6H5C(CH3)2 CH3CH2 H 120 C-Cl CH C-CF3 H (СН3)3С -CH2CH2CH2CH2 121 CH CH C-CF3 H (СН3)3С CH3CH2 H 122 CH CH C-CF3 6-Cl (CH3)2CHCH2 CH3CH2 H 123 C-Cl CH C-CF3 6-Cl (СН3)3С 86,588,5 -CH2CH2CH2CH2 124 C-Cl CH C-CF3 6-Cl (СН3)3С cyclohexyl циклогeксил H 125 C-Cl CH C-CF3 6-Cl (СН3)3С C6H5CH2CH2 H 126 C-Br CH C-F 6-Br (СН3)3С CH3CH2 H 127 C-Cl C-Cl C-Cl (СН3)3С CH3CH2 H 128 C-Cl CH C-Cl 5,6-diCl 5,6-диСl 6-СІ CH3(CH2)5C(CH3)2 CH3CH2 H 129 C-Cl CH C-CF3 6-Сl CH3CH2 H 130 C-Cl CH C-CF3 6-Cl (СН3)3С CH3(CH2)2CH2 H 131 C-Cl CH C-CF3 6-Cl (СН3)3С (CH3)2CH H 132 C-Cl CH C-CF3 6-Cl (СН3)3С 133 C-Cl CH C-Cl 6-Cl pClC6H4 (CH3)2CH H 134 C-Cl CH C-Cl 6-Cl pClC6H4 CH3CH2 H 135 C-Cl CH C-CF3 6-Cl C6H5C(CH3)2 C6H5CH2CH2 H 136 C-Cl CH C-CF3 6-Cl CH3CH2 H 137 CH CH H (СН3)3С CH3CH2 H 138 CCF3 C-Cl CH C-CF3 H (СН3)3С C6H5CH2CH2 H 139 C-Cl CH C-CF3 H (СН3)3С H 140 CH CH C-CF H (СН3)3С H 141 C-Cl CH C-CF3 6-Cl pClC6H4C(CH3)2 63-65 13 H CH3CH2 H 124127 127132 74-75 35563 Продолжение таблицы 3 Номер примера Точка плав ления °С Example A Number 142 C-Cl B W Yn R R3 R16 CH C-CF3 6-Cl (СН3)3С C6H5CH(CH3) H 143 C-Cl CH C-CF3 6-Cl (СН3)3С (CH3)2NCH2CH2 H 144 C-Cl CH C-CF3 6-Cl (СН3)3С CH3CH2C(CH3)2 H 145 C-Cl CH C-CF3 6-Cl (СН3)3С 146* C-Cl CH C-CF3 6-Cl (СН3)3С 147 С-Br CH C-CF3 6-Br (СН3)3С 148 C-Cl CH C-CF3 6-Cl CH3CH2 H 149 C-Cl CH C-CF3 6-Cl CH3CH2 H 150 C-Cl CH C-CF3 6-Cl CH3CH2C(CH3)2 C6H5CH2CH2 H 151 C-Cl CH C-CF3 6-Cl (СН3)3С C6H5CH2 H 152 C-Cl CH C-CF3 6-Cl (СН3)3С CH3CH2 CH3CH2 153 C-Cl CH C-CF3 6-Cl CH3CH2 H 154 C-Cl CH C-CF3 6-Cl (CH3)2CH H 155 C-Cl CH C-CF3 6-Cl CICH2C(CH3)2 pCF3OC6H4 H 156 C-Cl CH C-CF3 6-Cl (СН3)3С H 157 C-Cl CH C-CF3 6-Cl (СН3)3С neopentyl неопентил H2NCOCHC(CH3)2 158 C-Cl CH C-CF3 6-Cl (СН3)3С 159 C-Cl CH C-CF3 6-Cl (СН3)3С 160 C-Cl CH C-CF3 6-Cl (СН3)3С H 161 C-Cl CH C-CF3 6-Cl (СН3)3С H 162 C-Cl CH C-CF3 6-Cl (СН3)3С CH3(CH2)4CH(CH3) mp °С H CH3CH2 H H H H pClC6H4-CH2CH2 H H 163 C-Cl CH C-CF3 6-Cl (СН3)3С (С2H5)2N(CH2)3CH(CH3) H 164 C-Cl CH C-CF3 6-Cl (СН3)3С CH -CHCH H 165 C-Cl CH C-CF3 6-Cl CH3CH2 H 166 C-Cl CH CH 5-CF3 1-methylcyclohexyl 1-метилциклогексил (СН3)3С CH3CH2 H 14 100,5 101,5 202202,5 203205 160162 35563 Продолжение таблицы 3 Номер примера Точка плав ления °С Example Number 167 A B W Yn R R3 R16 C-F C-F C-F (СН3)3С CH3CH2 H 168 C-Br CH C-F 5,6-diF 5,6-диF 6-Br (СН3)3С CH3CH2 H 169 C-Cl CH C-CF3 6-Cl (СН3)3С mp °С H * Hydrochloride salt Соль гидрохлорида Один куб.см мелкоизмельченного талька помещали в 30 мл широкогорлую стеклянную банку с завинчивающейся крышкой. Один мл соответствующего испытываемого раствора в ацетоне капали из пипетки на тальк, чтобы получить 1,25 мг активного ингредиента на банку. Банки подвергали действию слабого потока воздуха до тех пор, пока ацетон не испарялся. Высушенный тальк разрыхляли, добавляли 1 куб.см зерен проса в качестве корма для насекомых, и в каждую банку добавляли 25 мл влажной почвы. Банку закрывали, а содержимое тщательно перемешивали на вихревом смесителе. Вслед за этим в каждую банку добавляли десять личинок, повреждающих корни, в 3-ей возрастной стадии, и банки неплотно закрывали, чтобы имелся воздухообмен для личинок. Обработки проводили в течение 6 дней, делая подсчеты смертности. Найденные личинки считались мертвыми, поскольку они быстро разлагаются и их нельзя обнаружить. Концентрации, использовавшиеся в этом испытании, соответствовали приблизительного 50 кг/га. Испытания оценивались в соответствии со шкалой, приведенной ниже, а полученные данные приведены в таблицах 4, 5 и 6. Шкала оценки Пример 170 Инсектицидная и акарицидная оценка производных N-арилгидразина Испытываемые растворы получали путем растворения испытываемого соединения в 35% смеси ацетона в воде с получением концентрации 10.000 м.д. Последующие разбавления водой делали по мере необходимости. Spodoptera eridania, личинки в 3-ей стадии, южный червь (armyworm) Лист лимской фасоли Sieva, выросший до 7-8 см в длину, погружали в испытываемый раствор при перемешивании в течение 3 секунд и высушивали в вытяжном шкафу. Затем лист помещали в чашку Петри 100´10 мм, содержащую увлажненную фильтровальную бумагу на дне и десять гусениц в 3-ей возрастной стадии. На 3 и 5 дни делали наблюдения смертности, снижения в потреблении пищи, или других помех по сравнению с обычным развитием. Tetranychus urticae (штамм, устойчивый к ОР), 2-пятнистый красный клещик. Выбирали растения лимской фасоли Sieva с первичными листьями, выросшими до 7-8 см и вырезали, оставляя по одному растению на горшок. От зараженного листа, взятого из основной колонии, отрезали маленький кусочек и помещали на каждый лист испытываемых растений. Это делали примерно за 2 часа до обработки, чтобы позволить клещикам двигаться по испытываемому растению и отложить яйца. Размер отрезаемого зараженного листа меняли для получения примерно 100 клещиков на лист. Во время проверяемой обработки кусочек листа, используемый для переноса клещиков, удаляли и выбрасывали. Вновь зараженные клещиком растения погружали в испытываемый раствор на 3 секунды при перемешивании и ставили в вытяжной шкаф для сушки. Через 2 дня один лист снимали и подсчитывали смертность. Через 5 дней снимали другой лист и делали наблюдения смертности яиц и/или вновь появившихся личинок. Diabrotic undecimpunctata howardi, южная личинка, повреждающая корни зерновых, в 3-ей возврастной стадии . Оценка 0 нет еффекта 1 10-25 2 26-35 3 36-45 4 46-55 5 56-65 6 66-75 7 76-85 8 86-99 9 15 % смертности 100 35563 Таблица 4 Инсектицидная и акарицидная оценка N-ариламидразонов Insecticidal and Acaricidal Evaluation of N-Arylamidrazones Соединение (прим. №) Compound (Ex. №) 85 Червь Armyworm1 (300 ppm) м.д. 0 % Mortality % смертности 2-пятн. клещик 2-Spotted Mite2 (300 ppm) м.д. 0 Корневая личинка Corn Rootworm3 (50 kg/ha) 50 кг/га 100 86 100 0 80 87 40 90 100 88 89 0 о 100 90 0 о 20 91 0 80 100 92 0 0 100 93 0 0 100 94 80 100 95 80 0 100 96 100 40 80 97 '0 0 100 98 40 0 40 100 0 40 0 101 0 0 60 102 0 60 100 103 40 0 100 104 0 90 50 105 20 0 90 106 40 0 100 107 100 108 90 50 100 109 0 0 50 110 0 0 100 111 100 40 90 112 40 100 20 113 20 100 100 114 40 100 100 115 0 0 100 116 20 50 100 117 20 0 100 118 50 70 100 119 100 50 90 120 30 20 121 80 40 100 122 0 0 40 123 0 0 60 124 50 80 100 16 35563 Продолжение таблицы 4 Соединение (прим. №) Compound (Ex. №) 125 Червь Armyworm1 (300 ppm) м.д. 0 % Mortality % смертности 2-пятн. клещик 2-Spotted Mite2 (300 ppm) м.д. 30 Корневая личинка Corn Rootworm3 (50 kg/ha) 50 кг/га 100 126 0 80 90 128 0 0 30 129 100 40 0 130 80 80 100 131 70 0 100 132 40 100 133 0 0 134 0 30 0 135 0 0 0 136 0 70 100 137 0 0 100 138 0 0 100 139 0 70 100 140 0 0 50 141 100 0 0 142 0 0 100 143 0 0 100 144 0 0 100 145 0 0 100 146 0 0 100 147 0 0 100 148 50 0 100 149 100 80 80 150 0 60 100 152 80 0 100 153 100 0 100 156 0 100 157 0 0 100 158 40 0 100 159 0 0 100 160 0 0 100 161 0 0 162 0 100 100 163 0 0 100 164 0 0 100 167 0 0 100 168 0 80 90 169 0 0 100 1 Armyworm is 3rd instar larvae, southern armyworm 2-Spotted Mite is 2-spotted spider mite (OP-resistant) 3 Corn Rootworm is 3rd instar southern corn rootworm 2 17 35563 1 представляет личинку 3-ей стадии, южный червь (armyworm) 2-пятнистый клещик представляет собой 2-пятнистого красного клещика (устойчив к ОР) 3 Корневая личинка представляет собой южную личинку, повреждающую корни зерновых, в 3-ей стадии 2 Таблица 5 Инсектицидная и акарицидная оценка N-арилгицразидов Insecticidal and Acaricidal Evaluation of N-Arylhydrazides Соединение (прим. №) Compound (Ex. №) 1 Червь Armyworm1 (300 ppm) м.д. 8 % Mortality % смертности 2-пятн. клещик 2-Spotted Mite2 (300 ppm) м.д. 0 Корневая личинка Corn Rootworm3 (50 kg/ha) 50 кг/га 9 2 0 0 7 3 9 4 0 0 7 5 0 0 8 6 0 0 0 7 0 0 0 8 5 0 8 9 0 0 0 10 1 9 3 11 1 0 9 12 4 0 4 13 0 9 3 14 7 0 7 15 9 0 3 16 0 0 0 17 1 3 0 18 2 0 6 19 9 0 0 20 0 0 0 21 0 0 7 22 0 0 0 23 0 0 0 24 0 0 0 25 9 0 8 26 0 0 0 27 4 0 6 28 2 0 0 29 3 0 0 30 0 2 4 31 0 0 0 32 1 0 0 33 0 0 0 34 8 0 2 35 5 0 0 36 8 0 0 18 35563 Продолжение таблицы 5 Соединение (прим. №) Compound (Ex. №) 37 Червь Armyworm1 (300 ppm) м.д. 4 % Mortality % смертности 2-пятн. клещик 2-Spotted Mite2 (300 ppm) м.д. 0 Корневая личинка Corn Rootworm3 (50 kg/ha) 50 кг/га 0 39 0 0 0 40 9 0 9 41 3 0 9 42 0 2 4 1 Armyworm is 3rd instar larvae, southern armyworm 2-Spotted Mite is 2-spotted spider mite (OP-resistant) 3 Corn Rootworm is 3rd instar southern corn rootworm 1 представляет личинку 3-ей стадии, южный червь (armyworm) 2 2-пятнистый клещик представляет собой 2-пятнистого красного клещика (устойчив к ОР) 3 Корневая личинка представляет собой южную личинку, повреждающую корни зерновых, в 3-ей стадии 2 Таблица 6 Инсектицидная и акарицидная оценка замещенных N-арилгидразиноил галогенидов Insecticidal and Acaricidal Evaluation of Substituted N-Arylhydrazinoyl Halides Соединение (прим. №) Compound (Ex. №) 78 Червь Armyworm1 (300 ppm) м.д. 90 % Mortality % смертности 2-пятн. клещик 2-Spotted Mite2 (300 ppm) м.д. 90 Корневая личинка Corn Rootworm3 (50 kg/ha) 50 кг/га 0 54 80 100 0 58 0 0 0 59 0 100 0 64 90 100 66 80 100 20 71 90 90 30 73 50 100 0 77 100 90 80 79 100 100 100 1 Armyworm is 3rd instar larvae, southern armyworm 2-Spotted Mite is 2-spotted spider mite (OP-resistant) 3 Corn Rootworm is 3rd instar southern corn rootworm 1 представляет личинку 3-ей стадии, южный червь (armyworm) 2 2-пятнистый клещик представляет собой 2-пятнистого красного клещика (устойчив к ОР) 3 Корневая личинка представляет собой южную личинку, повреждающую корни зерновых, в 3-ей стадии 2 19 35563 __________________________________________________________ ДП "Український інститут промислової власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 __________________________________________________________ Підписано до друку ________ 2001 р. Формат 60х84 1/8. Обсяг ______ обл.-вид. арк. Тираж 50 прим. Зам._______ ____________________________________________________________ УкрІНТЕІ, 03680, Київ-39 МСП, вул. Горького, 180. (044) 268-25-22 ___________________________________________________________ 20
ДивитисяДодаткова інформація
Назва патенту англійськоюN-arylhydrazine derivatives, a process for the preparation thereof, a method to control insects and a composition to control insects
Автори англійськоюFurch Joseph Augustus, Kuhn David George, Hunt David Allen, Lew Albert Chien, Gronostajski Cynthia Emma
Назва патенту російськоюПроизводные n-арилгидразина, способ их получения, способ угнетения насекомых и композиция для угнетения насекомых
Автори російськоюФерч Джозеф Августус, Кун Дэвид Джордж, Хант Дэвид Аллен, Лью Альберт Чин, Гроностайски Синтиа Эмма
МПК / Мітки
МПК: C07C 251/78, A01N 37/28, A01N 37/52, A01N 43/40, C07C 251/74, C07C 251/22, A01N 43/58
Мітки: похідні, композиція, n-арилгідразину, спосіб, пригнічення, одержання, комах
Код посилання
<a href="https://ua.patents.su/20-35563-pokhidni-n-arilgidrazinu-sposib-kh-oderzhannya-sposib-prignichennya-komakh-ta-kompoziciya-dlya-prignichennya-komakh.html" target="_blank" rel="follow" title="База патентів України">Похідні n-арилгідразину, спосіб їх одержання, спосіб пригнічення комах та композиція для пригнічення комах</a>
Попередній патент: Похідні 7-ізоіндолінілхінолону і 7-ізоіндолінілнафтирідону
Наступний патент: Лікарський засіб для профілактики і лікування порушень ліпоїдного і холестеринового обміну речовин і спосіб профілактики і лікування цих порушень
Випадковий патент: Спосіб стимуляції овуляції фолікулів на яєчниках самок великої рогатої худоби